Изобретение относится к области получения кристаллических цеолитных материалов с заданными морфологическими и текстурными свойствами, которые могут быть использованы в качестве компонентов катализаторов.
Цеолит морденит (структурный тип MOR, далее MOR) широко используется в качестве компонента катализаторов таких процессов нефтехимии, как изомеризация н-парафиновых углеводородов, диспропорционирование и трансалкилирование алкилароматических углеводородов, изомеризация ксилолов и алкилирование бензола олефинами.
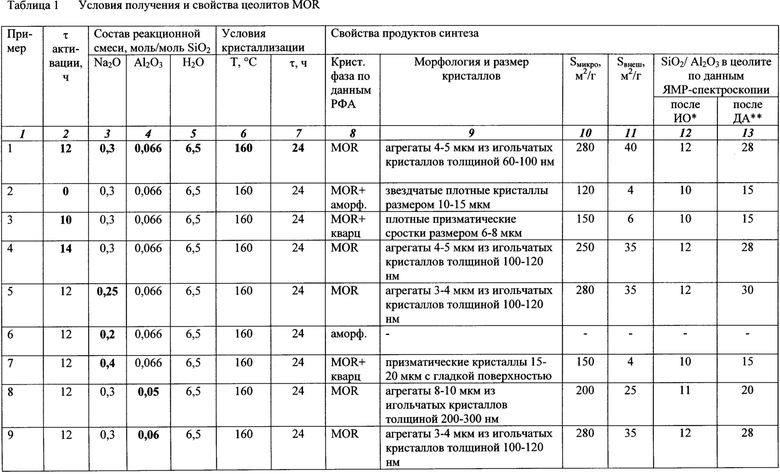
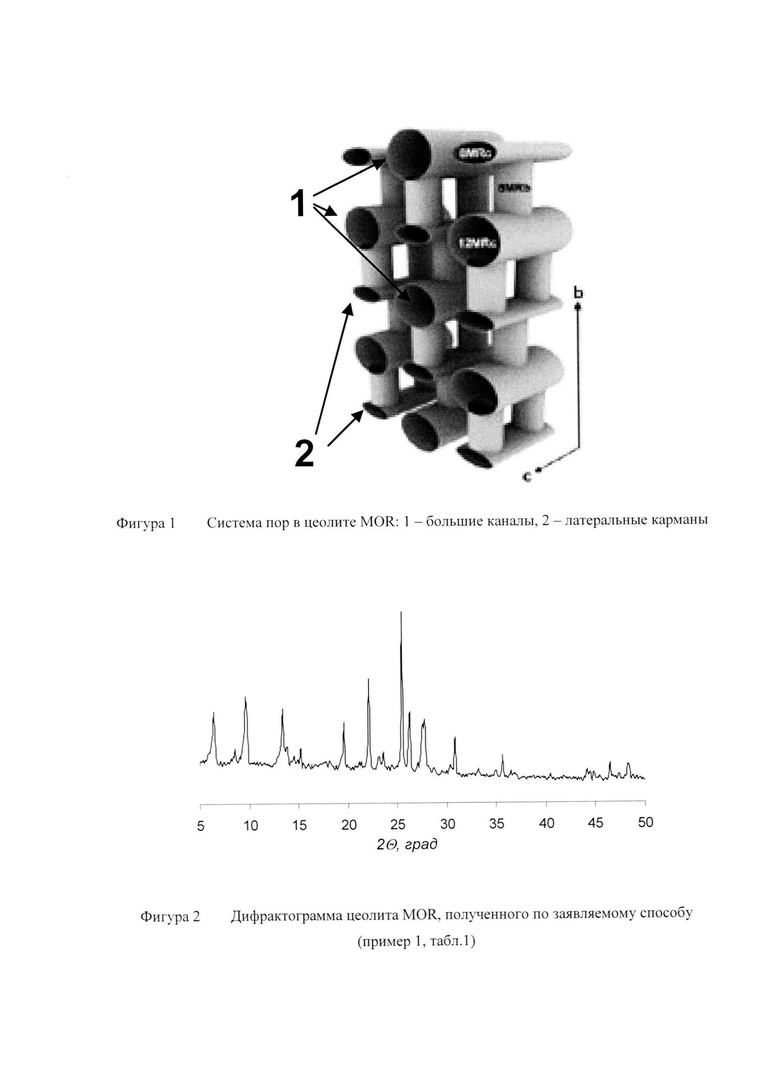
MOR относится к кристаллическим микропористым алюмосиликатам. Основой для построения кристаллического каркаса MOR является вторичная структурная единица 5-1, представляющая собой пятичленное кремнекислородное кольцо с присоединенным тетраэдром. В кристаллическом каркасе MOR присутствует два типа микропор. Первый тип пор ограничен 12-членными эллиптическими кольцами размером 0,65×0,7 нм, второй тип пор ограничен 8-членными кольцами размером 0,26×0,57 нм. Система организации пор в цеолите MOR показана на Фиг. 1. В связи с тем, что латеральные карманы в силу размерных ограничений практически недоступны для реагирующих молекул, пористую структуру MOR принято считать одномерной, т.е. образованной одним типом пор с параллельными «большими» каналами, ориентированными вдоль оси с.
Формирование кристаллов MOR происходит в результате гидротермальной кристаллизации в автоклавах при температурах 140-200°С и автогенном давлении из реакционных смесей на основе источников оксида кремния, оксида алюминия, неорганической щелочи и воды. Кристаллизация идет путем последовательно-параллельных процессов образования первичного игольчатого кристалла, растущего преимущественно вдоль оси с, и агрегации игольчатых кристаллов в массивный кристалл. Соотношение скорости роста первичных кристаллов и скорости их агрегации определяет морфологические и текстурные свойства MOR. Высокая скорость агрегации первичных игольчатых кристаллов приводит к образованию плотных крупных (до 20-30 мкм) микропористых кристаллов MOR с различной морфологией (шестигранной призматической, вытянутой, звездчатой) с малыми величинами внешней поверхности. При уменьшении скорости агрегации, MOR получают в виде иерархических цеолитных материалов, представляющих собой агрегаты первичных кристаллов, обладающие развитой внешней поверхностью.
Практическое использование плотных крупных кристаллов MOR ограничено несколькими факторами. Первый фактор связан с диффузионными ограничениями молекул в крупном кристалле. При использовании крупнокристаллического MOR в качестве катализатора в результате транспортных затруднений молекул-реагентов и продуктов реакции в порах цеолита протекание каталитического процесса ограничено приповерхностным слоем кристалла, составляющем не более 15% от его полного объема. В результате эффективность катализатора снижается.
Второй фактор связан с особенностями химического состава и локализации алюминия в кристаллическом каркасе. Цеолит MOR после синтеза имеет отношение SiO2/Al2O3, близкое 10. Отрицательный заряд алюмокислородных тетраэдров в каркасе цеолита компенсирован катионами натрия. Для придания MOR кислотных свойств и использования его в катализе, цеолит подвергают модифицированию, целью которого является замена катиона натрия на протон. Модифицирование проводится либо путем ионного обмена в растворе соли аммония с последующим прокаливанием, либо обработкой раствором кислоты. Однако в структуре морденита значительная часть алюмокислородных тетраэдров локализована в латеральных карманах. Кислотные центры, локализованные в латеральных карманах, из-за размера карманов (0,26×0,57 нм) оказываются недоступными для молекул реагентов, что снижает эффективность катализатора. Для увеличения доступности кислотных центров MOR используют метод деалюминирования. Этот метод представляет собой модифицирование цеолита сочетанием таких обработок, как ионный обмен и обработка кислотой, или ионный обмен, прокаливание и обработка кислотой. В ходе ионного обмена (декатионирования) достигается максимально возможная замена катионов натрия в 12-членных каналах MOR на катионы аммония. В ходе прокаливания аммонийной формы MOR при температурах 600-800°С происходит частичное разрушение кристаллического каркаса MOR в результате разрыва связи Si-О-Al и миграция алюминия из решеточных во внерешеточные позиции. Вымывание внерешеточных фрагментов из структуры цеолита происходит в результате кислотной обработки, для которой, как показано в [Giudici R., Kouwenhoven H.W., Prins R. Comparison of nitric and oxalic acid in the dealumination of mordenite // Applied Catalysis A: General, 2000, V. 203, P. 101-110; Nesterenko N.S., Kuznetsov A.S., Timoshin S.E., Fajula F., Ivanova I.I. Transalkylation of polynuclear aromatics with diisopropylbenzene over zeolite catalysts // Applied Catalysis A: General, 2006, V. 307, P. 70-77], могут быть использованы неорганические (азотная) и органические (щавелевая, метансульфоновая) кислоты.
В результате совокупного действия описанных методов модифицирования MOR достигаются:
- увеличение отношения SiO2/Al2O3, что в свою очередь приводит к росту силы кислотных центров MOR и росту стабильности цеолита,
- рост доступности кислотных центров MOR в результате образования дополнительной пористости.
Для крупных плотных кристаллов MOR в силу диффузионных ограничений описанное модифицирование может протекать только в приповерхностном слое, что ограничивает возможности процедуры деалюминирования и направленного регулирования свойств цеолита. Перечисленные факторы определяют перспективность разработок способов получения цеолита MOR в виде агрегатов с развитой внешней поверхностью.
Для ингибирования реакции агломерации первичных кристаллов MOR используют синтетические приемы и методы, позволяющие уменьшать скорость процесса агрегирования первичных кристаллов цеолита или предотвращать этот процесс.
Из уровня техники известны приемы синтеза цеолита MOR с использованием модифицированного источника оксида кремния.
Описан способ получения цеолита MOR в виде сноповидных агрегатов размером 6-8 мкм, образованных игольчатыми нанокристаллами толщиной 50-100 нм и длиной 2-5 мкм, ориентированными параллельно друг другу [Dai G., Нао W., Xiao Н., Маа J., Li R. Hierarchical mordenite zeolite nano-rods bundles favourable to bulky molecules // Chemical Physics Letters, 2017, v. 686, p.111-115], [Патент CN 106185976 (A), 2016], включающий приготовление реакционной смеси на основе дистиллированной воды, алюмината натрия, гидроксида натрия, кристаллической затравки в количестве 0,5% масс, от массы реакционной смеси, наноразмерного источника оксида кремния в виде пирогенного материала с поверхностью, модифицированной соединением диметилоктадецил[3-(триметоксисилил)пропил] аммоний хлорид (далее R), с итоговым составом SiO2:R:0,033Al2O3:0,23Na2O:26H2O; кристаллизацию реакционной смеси в две стадии при 100°С в течение 12 ч и при 140°С в течение 12 суток; выделение, отмывку, высушивание и прокаливание полученного материала при 600°; ионный обмен цеолита в 1 М растворе нитрата аммония.
В результате перечисленных процедур получают цеолит MOR в виде сноповидных агрегатов размером 6-8 мкм, образованных игольчатыми нанокристаллами толщиной 50-100 нм и длиной 2-5 мкм. В синтезе этого материала предотвращение агрегирования первичных игольчатых кристаллов достигается благодаря наличию на поверхности сырьевого источника оксида кремния (и, в итоге, на поверхности цеолитных наноигл) привитых углеводородных групп, препятствующих сближению и слипанию наноигл. Полученный материал используют в качестве катализатора бензилирования мезитилена бензил хлоридом.
Недостатками описанного способа являются использование дорогостоящего источника оксида кремния, высокий расход органического модификатора, высокая длительность синтеза, превышающая 12 суток, и низкая производительность кристаллизатора в результате высокого разбавления реакционной смеси с мольным отношением H2O/SiO2=26.
Из уровня техники известны приемы синтеза цеолита MOR с использованием органических соединений, содержащих катионы четвертичного алкиламмония и катионные ПАВ.
Описан способ получения цеолита MOR в виде сфероидных агломератов размеров 15-20 мкм, образованных нанокристаллами размером 50-100 нм [Yuan Y., Wang L., Liu H., Tian P., Yang M., Xu Sh., Liu Zh. Facile preparation of nanocrystal-assembled hierarchical mordenite zeolites with remarkable catalytic performance // Chinese Journal of Catalysis, 2015, V. 36, p. 1910-1919]. Синтез иерархического цеолитного материала проводят путем последовательных операций, включающих приготовление реакционной смеси последовательным смешиванием водного раствора NaOH, поверхностно-активного вещества C12H25-N+(CH3)2-C2H4-N+(CH3)2-C12H25Br2 (далее С12-2-12), гидроксида тетраэтиламмония (C2H5)4NOH, алюмината натрия, коллоидного кремнезема в виде кремнезоля; кристаллизацию реакционной смеси состава SiO2:0,033Al2O3:0,25Na2O:0,10(C2H5)4NOH:0,05C12-2-12:40H2O при 135°С в течение 5-7 суток; выделение, отмывку, высушивание и прокаливание полученного материала при 550°; ионный обмен цеолита в 1 М растворе нитрата аммония.
В результате перечисленных процедур получают цеолит MOR в виде сфероидных агломератов размером 15-20 мкм, образованных первичными сферическими нанокристаллами размером 50-100 нм. Изменение морфологии и размера первичных кристаллов достигается путем адсорбции на поверхности растущего кристалла двухзарядного катиона ПАВ С12-2-12. В результате адсорбции и ингибирования поверхности кристалла ограничивается приток реагентов из жидкой фазы кристаллизации и рост первичного кристалла прекращается. Полученный материал используют в качестве катализатора крекинга углеводородов.
Недостатками описанного способа являются использование дорогостоящих органических соединений, высокая длительность синтеза и низкая производительность кристаллизатора в результате высокого разбавления реакционной смеси с мольным отношением H2O/SiO2=40.
Наиболее близким к предложенному техническому решению является способ получения MOR в виде сноповидных агрегатов размером 4-5 мкм, образованных игольчатыми кристаллами толщиной 100-500 нм [CN 102659134(A), 2012]. Способ включает приготовление реакционной смеси на основе гидроксида натрия, дисперсного кремнезема, источника алюминия, воды и кристаллической затравки в виде цеолитного молекулярного сита, содержащего в кристаллической структуре пятичленные кольца (цеолиты ZSM-5, силикалит-1, ZSM-11, ZSM-35), кристаллизацию смеси с рН=11-13 при температуре 150-170° в течение 0,3-3 сут. Реакционная смесь имеет следующий состав в мольных отношениях компонентов: SiO2/Al2O3=10-100, Na2O/SiO2=0,18-0,33, H2O/SiO2=20-80, содержание кристаллической затравки составляет 0,1-10%.
Недостатками данного способа являются низкая производительность кристаллизатора, оцениваемая по величине мольного отношения H2O/SiO2=20-80, характеризующего высокое разбавление реакционной смеси, необходимость предварительных синтезов цеолитов, содержащих в своей структуре сдвоенные пятичленные кольца для использования такого цеолита в качестве кристаллической затравки, а также большая толщина игольчатого кристалла, достигающая 500 нм.
Технической проблемой настоящего изобретения является разработка способа получения цеолита MOR, обеспечивающего высокую производительность процесса кристаллизации и получение высококристалличного цеолита в виде агломератов игольчатых кристаллов с толщиной игольчатого кристалла, обеспечивающей достижение высокой степени деалюминирования.
Техническим результатом настоящего изобретения является получение цеолита MOR высокого качества с высоким выходом, в виде агрегатов с габаритными размерами (продольными и поперечными размерами) 3-5 мкм, образованных первичными игольчатыми кристаллами толщиной 60-120 нм, обеспечивающей высокую степень деалюминирования цеолита благодаря развитой внешней поверхности, составляющей 35-50 м2/г.
Заявленный технический результат достигается получением цеолита MOR в результате выполнения следующих этапов: приготовление реакционной смеси, характеризующейся составом, соответствующим области кристаллизации MOR, активация реакционной смеси при перемешивании, кристаллизация реакционной смеси в гидротермальных условиях при перемешивании, выделение, отмывка, высушивание, декатионирование и деалюминирование кристаллического продукта.
Согласно изобретению, реакционную смесь для синтеза MOR готовят на основе силикагеля, свежеприготовленного раствора алюмината натрия, гидроксида натрия и дистиллированной воды. Отличительной особенностью реакционной смеси по заявляемому способу является высокая концентрация сухого вещества, оцениваемая по мольному отношению H2O/SiO2 от 6 до 8. Также в реакционной смеси обеспечиваются мольные соотношения компонентов, соответствующие области кристаллизации MOR, а именно Al2O3/SiO2 от 0,06 до 0,08, Na2O/SiO2 от 0,25 до 0,3.
Активацию реакционной смеси проводят при комнатной температуре в течение 12-14 ч при перемешивании.
Предпочтительно, кристаллизацию реакционной смеси проводят в гидротермальных условиях при температуре 150-160°С в течение 24-48 ч при перемешивании.
Согласно изобретению, по окончании кристаллизации полученный цеолит выделяют из реакционной смеси фильтрованием и дополнительно подвергают отмывке, высушиванию, декатионированию и деалюминированию с использованием стандартных методик в соответствии с [Verified Synthesis of Zeolitic Materials. Second Edition. Edit. H. Robson. Elsevier.2001. 266 p. ISBN: 0-444-50703-5] и [Giudici R., Kouwenhoven H.W., Prins R. Comparison of nitric and oxalic acid in the dealumination of mordenite // Applied Catalysis A: General, 2000, V. 203, P. 101-110].
При приготовлении реакционной смеси в качестве источника оксида кремния были использованы частицы силикагеля размером менее 1 мм, полученные размолом промышленных марок силикагелей, в том числе отходов от производства силикагелей после технологической стадии рассева. Силикагель является материалом с высокой реакционной способностью и низкой стабильностью в щелочных растворах. В ходе приготовления реакционной смеси при обработке силикагеля в смеси раствора гидроксида натрия и свежеприготовленного раствора алюмината натрия происходят параллельно-последовательные процессы растворения силикагеля под действием щелочи и взаимодействия продуктов растворения силикагеля с алюминатными ионами. Это взаимодействие приводит к формированию аморфного алюмосиликатного гидрогеля, являющегося основой для образования кристаллического каркаса MOR. Необходимость использования свежеприготовленного раствора алюмината натрия связана с тем, что при хранении раствора алюмината натрия более 24 ч в объеме раствора в результате гидролиза происходят процессы полимеризации. Образование полиалюминатных анионов снижает реакционную способность алюмината натрия, что негативно влияет на его взаимодействие с продуктами растворения силикагеля и на свойства образующегося алюмосиликатного геля как прекурсора цеолита MOR и его способность кристаллизоваться MOR в условиях по заявляемому способу. Предпочтительно использование для приготовления реакционной смеси свежеприготовленного раствора алюмината натрия с концентрацией 32-35% масс.
По заявляемому способу, реакционная смесь характеризуется высокой степенью концентрирования, оцениваемого по величине мольного отношения Н2О/SiO2 от 6 до 8. Проведение кристаллизации при таком концентрировании реакционной смеси обеспечивает формирование MOR в виде агрегатов размером 3-5 мкм, образованных игольчатыми кристаллами толщиной 60-120 нм с площадью внешней поверхности кристаллов не менее 35 м2/г. Концентрирование реакционной смеси, связанное с увеличением содержания сухого вещества в реакционной смеси, приводит к образованию большого числа зародышей кристаллов. В результате за небольшое время синтеза удается достичь преимущества в скорости роста первичных игольчатых кристаллов по сравнению с их агрегацией в плотный кристалл. Кроме того, высокая концентрация сухого вещества в реакционной смеси способствует высокому выходу MOR, составляющему 82-85%, рассчитанному по формуле (mЦ(SiO2)+mЦ(Al2O3)) / (mPC(SiO2)+mPC(Al2O3)), где mЦ(SiO2)) и mЦ(Al2O3) - массы оксида кремния и оксида алюминия в цеолите по данным химического анализа, (mPC(SiO2) и mPC(Al2O3) - массы оксида кремния и оксида алюминия, взятые для приготовления реакционной смеси. Также высокое концентрирование обеспечивает высокую производительность автоклава-кристаллизатора, составляющую 250 кг цеолита с 1 м3 автоклава.
Уменьшение отношения Н2О/SiO2 в реакционной смеси ниже 6 приводит к загустеванию реакционной смеси, увеличению ее вязкости, трудностям при перемешивании в ходе приготовления и гидротермальной кристаллизации реакционной смеси и образованию кварца как единственной кристаллической фазы. Увеличение отношения Н2О/SiO2 в реакционной смеси выше 8 приводит к снижению производительности автоклава-кристаллизатора, росту размера агрегатов при увеличении толщины игольчатых кристаллов.
Уменьшение отношения Al2O3/SiO2 в реакционной смеси ниже 0,06 приводит к увеличению размеров агрегатов до 8-10 мкм, при этом толщина игольчатых кристаллов увеличивается до 200-300 нм, что негативно влияет на процесс деалюминирования цеолита. Увеличение отношения Al2O3/SiO2 в реакционной смеси выше 0,08 приводит к уменьшению кристалличности MOR, увеличению размеров кристаллов, формированию их в виде крупных плотных сноповидных сростков, при уменьшении площади внешней поверхности кристаллов до 4-6 м2/г. В результате процесс деалюминирования кристаллов затрудняется.
При уменьшении отношения Na2O/SiO2 в реакционной смеси ниже 0,25 цеолит не образуется. Увеличение отношения Na2O/SiO2 в реакционной смеси выше 0,3 приводит к изменению селективности кристаллизации, присутствию в продуктах кристаллизации кварца и формированию морденита в виде крупных плотных кристаллов.
Активацию реакционной смеси проводят при комнатной температуре и перемешивании. Использование этой стадии связано с максимальным обеспечением процессов деполимеризации силикагеля как источника оксида кремния и формирования алюмосиликатного гидрогеля как прекурсора MOR в результате взаимодействия алюминатных ионов и продуктов растворения силикагеля. Проведение активации менее 12 ч приводит к образованию примесной фазы кварца, увеличению размеров агрегатов и росту из плотности, что сказывается на уменьшении площади внешней поверхности кристаллов. Проведение активации более 14 ч не влияет на свойства продуктов кристаллизации, но приводит к увеличению энергозатрат, что технологически не целесообразно.
Уменьшение температуры кристаллизации ниже 150°С приводит к снижению скорости кристаллизации и присутствию в продукте кристаллизации значительных количеств аморфной фазы. Увеличение температуры кристаллизации выше 160°С увеличивает скорость кристаллизации, приводит к росту размеров агломератов и толщины первичных игольчатых кристаллов, а также к увеличению энергозатрат на стадию гидротермальной кристаллизации, что технологически не целесообразно. Длительность кристаллизации определяется температурой кристаллизации и составляет при температуре 150°С 48 ч, при температуре 160°С 24 ч.
Заявляемый способ получения цеолита MOR включает последовательное выполнение следующих операций:
- приготовления реакционной смеси на основе алюмината натрия, гидроксида натрия, силикагеля и дистиллированной воды,
- кристаллизации реакционной смеси в гидротермальных условиях при температуре 150-160°С в течение 24-48 ч при перемешивании,
- выделения цеолита из продуктов кристаллизации, отмывки, высушивания, декатионирования и деалюминирования с использованием известных стандартных методик.
Заявляемый способ, реализуемый в результате совокупности перечисленных операций, позволяет получать цеолит MOR с высокой кристалличностью, не содержащий кристаллических и аморфных примесей, в виде агрегатов размером 3-5 мкм, образованных игольчатыми кристаллами толщиной 60-120 нм, обладающих пористой структурой с развитой внешней поверхностью, составляющей 35-50 м2/г.
Размер агрегатов 3-5 мкм позволяет проводить выделение MOR на разных стадиях процесса получения цеолита (из продуктов кристаллизации, ионообменного раствора, раствора кислоты при деалюминировании) на простейших фильтрующих устройствах, без использования специального оборудования, в т.ч. центрифуг и декантеров. Получаемые цеолитные агрегаты размером 3-5 мкм образованы игольчатыми кристаллами толщиной 60-120 мкм. Длина первичного игольчатого кристалла составляет 2-4 мкм. Агрегация игольчатых кристаллов происходит параллельно кристаллографической оси с, определяющей направление роста кристаллов.
В табл. 1 приведены условия получения цеолитов и характеристики цеолитов MOR.
Приготовление реакционной смеси проводили с использованием механического верхнеприводного перемешивающего устройства Wise Stir НТ50АХ для вязких систем с пропеллерной мешалкой. Кристаллизацию реакционной смеси проводили в лабораторных реакторах высокого давления РВД-3-1000 объемом 1 л с тефлоновым вкладышем, внешним перемешивающим устройством, якорной мешалкой и внешним регулируемым нагревом. Выделение и отмывку кристаллического продукта проводили на вакуумной фильтровальной установке до рН промывных вод 9. MOR высушивали при температуре 100°С в течение 12 ч в сушильном шкафу UT-4683.
Декатионирование проводили путем пятикратного ионного обмена в 1 М растворе нитрата аммония при 80°С и перемешивании при длительности одной процедуры ионного обмена 3 ч. Деалюминирование проводили путем сочетания процедур прокаливания и кипячения в растворе кислоты. Прокаливание аммонийной формы MOR проводили при 700°С в лабораторной печи СНОЛ 12/12-В в течение 1 ч. Кислотную обработку MOR проводили кипячением прокаленного цеолита в 1 М растворе азотной кислоты при перемешивании в колбе с обратным холодильником в течение 1 ч.
Фазовый анализ образцов проводили с использованием дифрактограмм, полученных на рентгеновском дифрактометре D2PHASER (Bruker), излучение CuKa. Запись дифрактограмм осуществляли в интервале углов 5-40 град. 20 с шагом 0.05 град. Кристаллическую фазу MOR идентифицировали с использованием базы данных Международной цеолитной ассоциации [http://europe.iza-structure.org/IZA-SC/framework. php?STC=MWW].
Морфологию и размер кристаллов фиксировали по микрофотографиям СЭМ, полученным на сканирующем электронном микроскопе Hitachi ТМ3030. Перед съемкой на поверхность образцов наносили слой золота методом напыления в вакууме.
Площадь поверхности микропор и площадь внешней поверхности кристаллов определяли с использованием метода низкотемпературной адсорбции-десорбции азота на поромере ASAP 2010 (Micromeritics). Для расчетов величин поверхности использовали программное обеспечение прибора.
Спектры ЯМР ВМУ 29Si и 27Al регистрировали на приборе VARIAN Unity Inova AS-500. Состояние алюминия в образцах определяли на основании набора и положения максимумов на спектрах ЯМР 27Al. Деконволюцию ЯМР-спектров 29Si и расчет отношения Si/Al проводили аналогично [Barras J., Klinowski J., McComb D.W.27AI and 29Si Solid-state NMR Studies of Dealuminated Mordenite // J. Chem. Soc. Faraday Trans. 1994. V. 90. N. 24. Р. 3719].
Доступность кислотных центров оценивали по данным термопрограммированной десорбции аммиака (ТПД(NH3)) согласно [Verified Synthesis of Zeolitic Materials. Second Edition. Edit. H.Robson. Elsevier.2001. 266 p. ISBN: 0-444-50703-5] и по данным ИК-спектроскопии адсорбированного пиридина согласно [Nesterenko N.S., Kuznetsov A.S., Timoshin S.E., Fajula F., Ivanova I.I. Transalkylation of polynuclear aromatics with diisopropylbenzene over zeolite catalysts // Applied Catalysis A: General, 2006, V. 307, P. 70-77].]. ТПД-кривые NH3 получали с использованием анализатора хемосорбции УСГА-101 производства компании "УНИСИТ" (Россия). ИК-спектры регистрировали на приборе  с DTGS-детектором.
с DTGS-детектором.
Ниже приведены конкретные примеры реализации изобретения.
Пример 1
Реакционную смесь готовят непосредственно в автоклаве-кристаллизаторе. В автоклав заливают 375 г дистиллированной воды, затем при перемешивании добавляют 67,3 г NaOH. В полученный раствор добавляют 141,4 г свежеприготовленного раствора алюмината натрия с концентрацией 35% масс. В полученную смесь небольшими порциями всыпают 240 г силикагеля. Полученную реакционную смесь гомогенизируют в течение 1 ч, после чего автоклав герметизируют и начинают отсчет времени активации, которую проводят при перемешивании и комнатной температуре в течение 12 ч. По окончании активации включают нагрев автоклава-кристаллизатора и поднимают температуру в автоклаве до 160°С. Кристаллизацию проводят при этой температуре и перемешивании в течение 24 ч. По окончании кристаллизации и охлаждения автоклава MOR выделяют из жидких продуктов кристаллизации на фильтре и отмывают до рН промывных вод 9. Отмытый MOR высушивают при 100°С в течение 12 ч. Ионный обмен (декатионирование) проводят путем ионного обмена в 1 М растворе нитрата аммония при температуре 80°С, массовом отношении раствор:цеолит, равном 10:1 и перемешивании. Проводят пять циклов ионного обмена длительностью 3 ч каждый с промежуточным выделением цеолита из отработанного раствора нитрата аммония на фильтре без отмывки. По окончании декатионирования MOR выделяют и отмывают на фильтре для удаления избытка нитрата аммония с поверхности кристаллов и высушивают при 100°С в течение 12 ч. Высушенную аммонийную форму MOR помещают в разогретую до 700°С лабораторную печь на 1 ч. Прокаленный и остывший до комнатной температуры MOR всыпают в коническую колбу с кипящим и перемешивающимся 1 М раствором азотной кислоты. Массовое отношение раствор кислоты: цеолит составляет 5:1. Кипячение проводят в колбе с обратным холодильником при перемешивании в течение 1 ч. После кислотной обработки MOR выделяют на фильтре из отработанного раствора кислоты и отмывают от избытка кислоты. Отмытый деалюминированный MOR высушивают при 100°С в течение 12 ч. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл.1.
Примеры 1, 2-4 показывают влияние наличия и длительности активации на свойства MOR.
Пример 2
Синтез MOR проводят аналогично примеру 1, но активацию не проводят, а сразу после окончания гомогенизации реакционной смеси начинают подъем температуры в автоклаве до температуры кристаллизации. Получают цеолит MOR, содержащий примеси аморфной фазы, характеристики которого представлены в табл. 1.
Пример 3
Синтез MOR проводят аналогично примеру 1, но активацию проводят в течение 10 ч. Получают цеолит MOR, содержащий примеси кварца, характеристики которого представлены в табл. 1.
Пример 4
Синтез MOR проводят аналогично примеру 1, но активацию проводят в течение 14 ч. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Примеры 1, 5-7 показывают влияние мольного отношения Na2O/SiO2 в реакционной смеси на свойства MOR.
Пример 5
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 51,2 г NaOH. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл.1.
Пример 6
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 35,2 г NaOH. Получают аморфный материал (табл. 1).
Пример 7
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 99,2 г NaOH. Получают цеолит MOR, содержащий примесь кварца. Характеристики материала представлены в табл. 1.
Примеры 1, 8-11 показывают влияние мольного отношения Al2O3/SiO2 в реакционной смеси на свойства MOR.
Пример 8
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 399,6 г дистиллированной воды, 74,4 г гидроксида натрия и 106 г свежеприготовленного раствора алюмината натрия с концентрацией 35% масс. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Пример 9
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 369 г дистиллированной воды, 70,4 г гидроксида натрия и 127,3 г свежеприготовленного раствора алюмината натрия с концентрацией 35% масс. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл.1.
Пример 10
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 343,8 г дистиллированной воды, 61,6 г гидроксида натрия и 169,4 г свежеприготовленного раствора алюмината натрия с концентрацией 35% масс. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Пример 11
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 318,6 г дистиллированной воды, 52,8 г гидроксида натрия и 212 г свежеприготовленного раствора алюмината натрия с концентрацией 35% масс. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Примеры 1, 12-15 показывают влияние мольного отношения Al2O3/SiO2 в реакционной смеси на свойства MOR. Пример 12
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 253,8 г дистиллированной воды. В качестве единственной кристаллической фазы получают кварц (табл. 1).
Пример 13
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 325,8 г дистиллированной воды. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Пример 14
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 469,8 г дистиллированной воды. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл.1.
Пример 15
Синтез MOR проводят аналогично примеру 1, но для приготовления реакционной смеси берут 613,8 г дистиллированной воды. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл.1.
Примеры 1 и 16 показывают предпочтительность использования свежеприготовленного раствора алюмината натрия.
Пример 16
Синтез MOR проводят аналогично примеру 1, но для приготовления берут раствор алюмината натрия с концентрацией 35% масс, старенный в течение 48 ч при комнатной температуре. Получают материал, содержащий следовые количества MOR.
Примеры 1, 17-19 показывают влияние температуры кристаллизации на свойства MOR.
Пример 17
Синтез MOR проводят аналогично примеру 1, но кристаллизацию проводят при 140°С в течение 72 ч. Получают материал, содержащий следовые количества MOR.
Пример 18
Синтез MOR проводят аналогично примеру 1, но кристаллизацию проводят при 150°С в течение 48 ч. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Пример 19
Синтез MOR проводят аналогично примеру 1, но кристаллизацию проводят при 170°С в течение 24 ч. Получают фазово чистый цеолит MOR, характеристики которого представлены в табл. 1.
Высокое качество цеолита MOR, достигаемое выполнением совокупности заявляемых параметров синтеза, дополнительно иллюстрируется с помощью Фигур 2 и 3 и табл. 2.
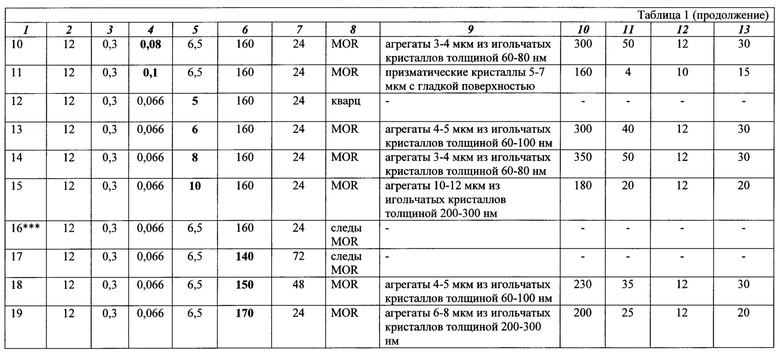
На Фиг. 2 показана порошковая дифрактограмма цеолита MOR, полученного по заявляемому способу (пример 1, табл. 1). Набор дифракционных максимумов на дифрактограмме полностью соответствует набору для цеолита MOR из базы цеолитных структур Международной цеолитной ассоциации (IZA). На дифрактограмме цеолита MOR, полученного по заявляемому способу, отсутствует гало в области углов 15-30 град. 2Θ, что подтверждает высокую кристалличность материала и отсутствие в нем аморфной фазы.
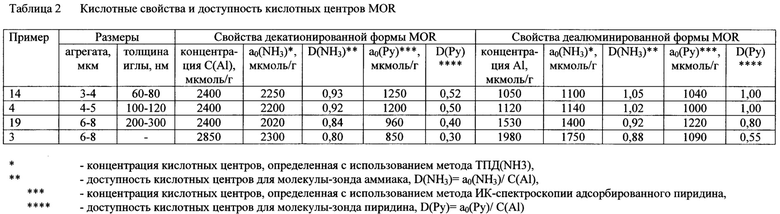
На Фиг. 3 представлена микрофотография сканирующей электронной микроскопии цеолита MOR, полученного по заявляемому способу (пример 1, табл. 1). Как следует из фиг. 3, цеолит MOR, полученный по заявляемому способу (пример 1, табл. 1), представляет собой агрегаты размером 4-5 мкм, образованные игольчатыми кристаллами толщиной 60-100 нм. Также для цеолитов MOR, получаемых по заявляемому способу, толщина игольчатого кристалла может составлять 60-80 нм (примеры 10, 14), 100-120 нм (примеры 4, 5, 9) при размере агрегатов 3-5 мкм. Общим для всех цеолитов, получаемых по заявляемому способу является способ агрегации игольчатых кристаллов вдоль кристаллографической оси с.
Толщина игольчатого кристалла 60-120 нм обуславливает развитую внешнюю поверхность MOR, получаемых по заявляемому способу, составляющую 35-50 м2/г при высоком значении площади поверхности микропор, составляющей 280-350 м2/г. Совокупность морфологических и текстурных свойств цеолитов обеспечивает высокую степень деалюминирования кристаллического каркаса цеолитов MOR, получаемых по заявляемому способу: мольное отношение SiO2/Al2O3 увеличивается от 12 в аммонийных формах до 28-30 в деалюминированных формах (примеры 1, 4, 5, 9, 10, 13, 14, 18, табл. 1), тогда как для крупных плотных кристаллов это отношение возрастает только до 15 (примеры 2, 3, 7, 11, табл. 1), а в агрегатах с толщиной игольчатого кристалла 200-300 нм -до 20 (примеры 8, 15, 19, табл. 1).
Кислотные свойства цеолитов традиционно оценивают с использованием молекул-зондов. В качестве зондов используют вещества, содержащие атом азота с неподеленной парой электронов, способной образовывать донорно-акцепторную связь с кислотным центром цеолита (протоном). Наиболее часто используют аммиак, пиридин и его производные. Аммиак взаимодействует с кислотным центром цеолита с образованием иона аммония. Его детектирование методом термопрограммированной десорбции позволяет оценить общую концентрацию кислотных центров в цеолите, т.к. размер молекулы аммиака позволяет проникать как в большие каналы, так и в латеральные карманы MOR. Результаты определения концентрации кислотных центров с использованием молекулы-зонда аммиака не отражают реальной доступности кислотных центров MOR, т.к. в силу размерных ограничений большинство органических реагентов не могут проникнуть в латеральные карманы и достичь кислотного центра. Для оценки реальной доступности кислотных центров в MOR используют молекулу-зонд пиридин (Ру) с размером 0,55 нм. При взаимодействии с протоном кислотного центра MOR пиридин образует ион пиридиния, регистрируемый в ИК-спектрах цеолита. В декатионированной форме MOR (водородной форме цеолита, образующейся после прокаливания аммонийной формы) с использованием Ру определяют кислотные центры, локализованные в больших каналах, а в деалюминированной форме - и кислотные центры в раскрывшихся латеральных карманах.
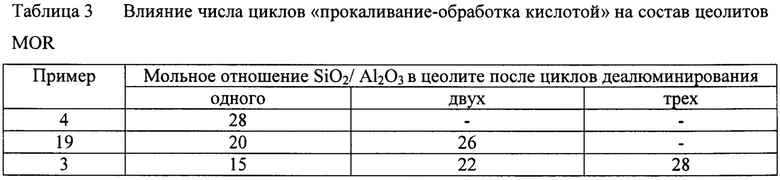
Преимущества цеолитов MOR, синтезированных по заявляемому способу, иллюстрируются табл. 2, в которой представлены данные о химическом составе и кислотных свойствах цеолитов MOR, полученных по заявляемому способу (примеры 14 и 4, табл. 1) и цеолитов MOR, отличающихся морфологией (примеры 19 и 3, табл. 1). Как показано на Фиг. 4 и в табл. 2, для примеров 14 (Фиг. 4а), 4 (Фиг. 4б) и 19 (Фиг. 4в) растет толщина первичного игольчатого кристалла, у примера 3 (Фиг. 4 г) грани цеолитного кристалла гладкие. Различия в толщине первичного игольчатого кристалла (примеры 14, 4, 19) и в морфологии цеолитного кристалла (пример 3) приводят к различиям в доступности кислотных центров как для аммиака, так и для пиридина уже в декатионированных формах цеолитов (табл. 2). В цеолитах MOR из примеров 14 и 4 с наименьшей толщиной цеолитной иглы (60-80 и 100-120 нм соответственно) обеспечивается наибольшая доступность зондов к кислотным центрам. С ростом толщины иглы и изменения морфологии цеолитного кристалла доступность зондов к кислотным центрам ухудшается.
В результате деалюминирования, сопровождающегося раскрытием латеральных карманов, доступность кислотных центров растет. При этом глубокое деалюминирование, достигаемое благодаря толщине игольчатого кристалла 60-120 нм и развитой внешней поверхности в цеолитах MOR 35-50 м2/г по примерам 14 и 4 обеспечивает 100%-ную доступность кислотных центров цеолита (табл. 2). В цеолитах MOR по примерам 19 и 3 с толщиной иглы 200-300 нм и гладкой поверхностью кристалла соответственно доступность кислотных центров для пиридина составляет 0,8 и 0,55.
Преимущества в доступности кислотных центров цеолитов MOR, получаемых по заявляемому способу, могут быть реализованы при использовании деалюминированных форм цеолитов в качестве катализаторов или компонентов катализаторов превращений углеводородов.
Преимущества в синтезе цеолитов MOR по заявляемому способу заключаются также в минимальном числе процедур модифицирования, необходимых для достижения высокой степени деалюминирования цеолита. В табл. 3 показано, что для цеолитов MOR по примерам 19 и 3 глубина деалюминирования, определяемая отношением SiO2/Al2O3 около 30, может быть достигнута проведением дополнительных циклов процедур «прокаливание-обработка кислотой». Если для MOR по примеру 4 необходим один цикл такого модифицирования, то для MOR по примеру 19 необходимо проведение двух циклов, а по примеру 3 - трех циклов. Проведение дополнительных процедур модифицирования для агрегатов MOR с толщиной игольчатого кристалла 200-300 нм или MOR с крупными кристаллами сопряжено со значительными энергорасходами и, кроме того, сопровождается аморфизацией цеолита.
Таким образом, реализация совокупности условий получения цеолита MOR, а именно качественного и количественного состава реакционной смеси на основе силикагеля, гидроксида натрия, свежеприготовленного раствора алюмината натрия и воды с соотношениями компонентов Al2O3/SiO2 от 0,06 до 0,08, Na2O/SiO2 от 0,25 до 0,3, Н2О/SiO2 от 6 до 8, активации реакционной смеси при комнатной температуре в течение 12-14 ч при перемешивании и кристаллизацию реакционной смеси в гидротермальных условиях при температуре 150-160°С в течение 24-48 ч при перемешивании обеспечивает получение высококачественных цеолитов MOR в виде агрегатов с продольными и поперечными размерами 3-5 мкм с развитой внешней поверхностью 35-50 м2/г, образованных игольчатыми кристаллами толщиной 60-120 нм. Совокупность достигаемых морфологических и текстурных свойств обеспечивает достижение высокой степени деалюминирования цеолита за однократное прохождение цикла процедур «ионный обмен - прокаливание - обработка кислотой».
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА ТИПА MWW | 2018 |
|
RU2712543C1 |
| ЦЕОЛИТ ТИПА MWW И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2740381C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА ТИПА MEL | 2018 |
|
RU2712549C1 |
| ГРАНУЛИРОВАННЫЙ БЕЗ СВЯЗУЮЩЕГО КРИСТАЛЛИЧЕСКИЙ ЦЕОЛИТ MFI И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2675018C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКРИСТАЛЛИЧЕСКОГО ЦЕОЛИТА ВЕА (варианты) И ПОЛУЧЕННЫЙ ЦЕОЛИТ ВЕА (варианты) | 2020 |
|
RU2737895C1 |
| Способ получения кристаллического цеолита семейства пентасил путем межцеолитных превращений. | 2021 |
|
RU2778923C1 |
| Способ получения кристаллического цеолита MEL и цеолит MEL | 2023 |
|
RU2805757C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА MFI | 2017 |
|
RU2640236C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОМОДУЛЬНОГО ЦЕОЛИТА ТИПА У | 1996 |
|
RU2090502C1 |
| Способ получения микро-мезопористого цеолита структурного типа морденит | 2023 |
|
RU2819615C1 |

Изобретение относится к области получения кристаллических цеолитных материалов с заданными текстурными и морфологическими свойствами кристаллов, которые могут быть использованы в качестве компонентов катализаторов, а именно к цеолиту типа MOR в виде агломератов с габаритными размерами 3-5 мкм, образованных первичными игольчатыми кристаллами с толщиной 60-120 мкм, ориентированными вдоль кристаллографической оси с внешней поверхностью 35-50 м2/г в качестве катализатора превращения углеводородов. Изобретение также относится к способу получения вышеуказанного цеолита, включающему приготовление реакционной смеси на основе источника оксида кремния, гидроксида натрия, алюмината натрия и воды, характеризующейся составом, соответствующим области кристаллизации MOR, активацию реакционной смеси и ее кристаллизацию при температуре 150-160°С в течение 24-48 ч, отмывку, сушку, ионный обмен и деалюминирование полученных кристаллов, отличающийся тем, что в качестве источника оксида кремния используют силикагель, при этом компоненты берут в следующем мольном соотношении Al2O3/SiO2 от 0,06 до 0,08, Na2O/SiO2 от 0,25 до 0,3, H2O/SiO2 от 6 до 8, активацию приготовленной реакционной смеси перед кристаллизацией осуществляют при комнатной температуре в течение 12-14 ч при перемешивании. Технический результат заключается в достижении высокой степени деалюминирования цеолита. 2 н. и 1 з.п. ф-лы, 3 табл., 19 пр., 4 ил.
1. Цеолит типа MOR в виде агломератов с габаритными размерами 3-5 мкм, образованных первичными игольчатыми кристаллами с толщиной 60-120 мкм, ориентированными вдоль кристаллографической оси с внешней поверхностью 35-50 м2/г в качестве катализатора превращения углеводородов.
2. Способ получения цеолита структурного типа MOR по п. 1, включающий приготовление реакционной смеси на основе источника оксида кремния, гидроксида натрия, алюмината натрия и воды, характеризующейся составом, соответствующим области кристаллизации MOR, активацию реакционной смеси и ее кристаллизацию при температуре 150-160°С в течение 24-48 ч, отмывку, сушку, ионный обмен и деалюминирование полученных кристаллов, отличающийся тем, что в качестве источника оксида кремния используют силикагель, при этом компоненты берут в следующем мольном соотношении Al2O3/SiO2 от 0,06 до 0,08, Na2O/SiO2 от 0,25 до 0,3, H2O/SiO2 от 6 до 8, активацию приготовленной реакционной смеси перед кристаллизацией осуществляют при комнатной температуре в течение 12-14 ч при перемешивании.
3. Способ по п. 1, отличающийся тем, что для приготовления реакционной смеси берут свежеприготовленный раствор алюмината натрия с концентрацией 32-35% масс.
| CN 102659134 A, 12.09.2012 | |||
| СЕЛЕКТИВНОЕ ДЕАЛЮМИНИРОВАНИЕ ЦЕОЛИТОВ СТРУКТУРНОГО ТИПА МОРДЕНИТА | 2009 |
|
RU2515729C2 |
| CN 106185976 A, 07.12.2016 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТОНКОСЛОЙНЫХ МОЛЕКУЛЯРНЫХ СИТ | 1997 |
|
RU2183499C2 |
| CN 105712371 B, 27.10.2017 | |||
| СУЮНДУКОВ Я.Т | |||
| и др., Использование природных цеолитов Зауралья Башкортостана для повышения плодородия почв и урожайности сельскохозяйственных культур (рекомендации производству), Сибай, СИЦ - филиал ГУП РБ | |||
Авторы
Даты
2021-03-03—Публикация
2019-12-09—Подача