Способ электролитического синтеза гексахлоррената цезия
Предлагаемый способ относится к области электролитического получения неорганических соединений щелочных металлов, а именно, гексахлоррената цезия, который может быть использован для приготовления электролитов, пригодных для электроосаждения рения.
Известен способ получения гексахлоррената цезия /1/ по химической реакции:
ReCl4 + 2CsCl (в конц. HCl) = Cs2ReCl6↓. (1)
Недостатком данного способа является использование исходного реактива хлорида рения (IV), который получают следующими способами. Первый способ заключается в последовательном хлорировании металлического рения газообразным хлором, с последующим частичным восстановлением водородом. Второй способ – обработка диоксида рения тионилхлоридом, который является токсичным. Таким образом, синтез исходного компонента для реакции (1) являются трудоемкими и неэкологичными.
По данным /2/ гексахлорренат цезия получают путем восстановления водных солянокислых растворов рениевой кислоты йодистым цезием по уравнению реакции (2):
2HReO4 + 6CsI + 14HCl = 2Cs2ReCl6↓ + 3I2↑ + 2CsCl + 8H2O. (2)
Недостатком данного способа является выделение газообразного йода в ходе реакции, который является токсичным.
Так же известен способ /3/ синтеза гексахлоррената цезия по уравнению реакции (3):
4CsReO4 + 16CCl4 = 2Cs2ReCl6↓ + 2ReCl5 + 5Cl2↑ + 16COCl2↑. (3)
Несмотря на высокий выход готового продукта по реакции, она обладает рядом значительных недостатков. К ним относятся высокие температура процесса (400°C) и давление (100атм.), а также выделение в ходе реакции газообразного хлора и дихлорангидрида угольной кислоты, которые являются чрезвычайно токсичными.
Согласно данным /4/, гексахлорренат цезия может быть синтезирован хлорированием металлического рения в расплав CsCl по уравнениям (4), (5):
2CsCl + 2Re + 5Cl2↑ = 2CsReCl6; (4)
2CsReCl6 + 2CsCl = 2Cs2ReCl6 + Cl2↑. (5)
К недостаткам данного способа можно отнести высокую температуру процесса (750°C), а также использование газообразного хлора.
Наиболее близким решением, с точки зрения используемых реактивов, является способ получения гексахлорената цезия по реакции (6), описанный в работе /5/:
ReO2 + 4HCl + 2CsCl = Cs2ReCl6↓ + 2H2O. (6)
Недостатком данного способа является использование в качестве исходного реактива оксида рения (IV), который получают следующими способами. Первый способ заключается в термическом разложении оксида рения (VII) под вакуумом. Второй способ – взаимодействие оксида рения (VII) с металлическим рением при температуре процесса 650°C. Таким образом, синтез исходного компонента для реакции (6) являются трудоемким и энергозатратным.
Задачей изобретения является разработка простого, экологичного, с низкими энергозатратами способа синтеза гексахлоррената цезия. Указанная задача решается за счет синтеза соли с использованием электрохимических методов, что позволяет упростить способ и снизить затраты на его реализацию.
Заявляемый способ синтеза гексахлоррената цезия осуществляется посредством электрохимической реакции ионизации металлического рения в растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия с концентрацией на пределе растворимости 1500г/л под действием переменного тока величиной 2А и частотой 1–50Гц с последующей химической реакцией.
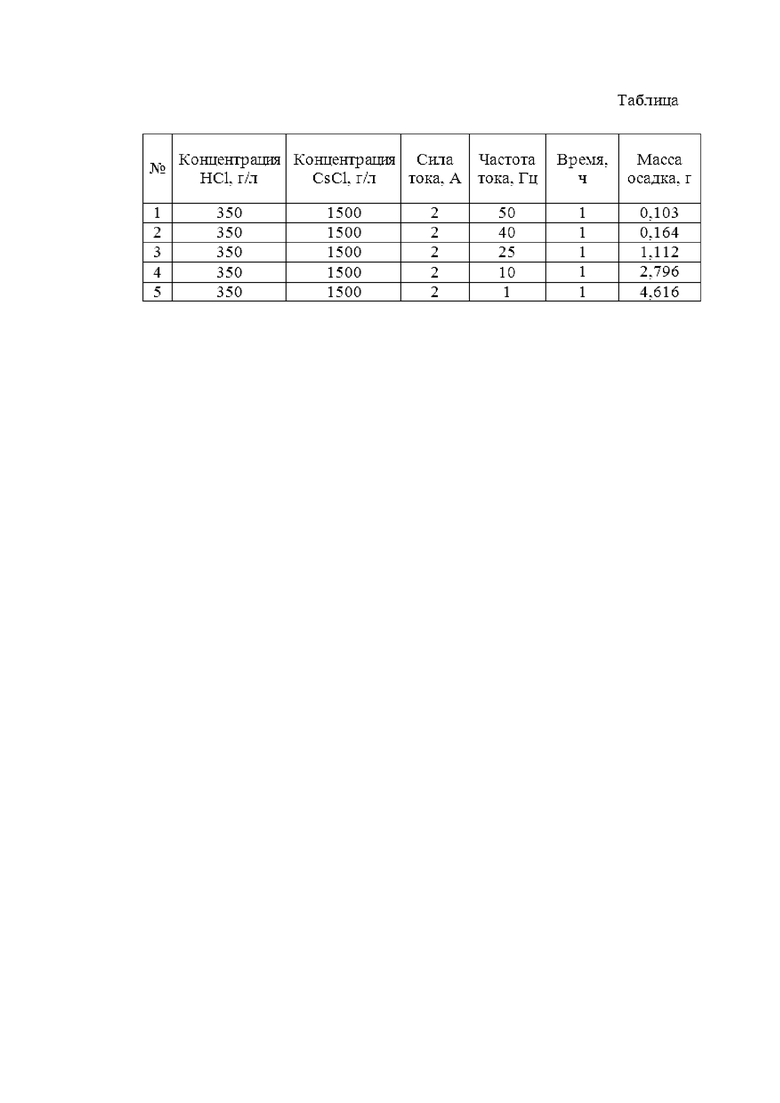
Сущность заявляемого способа поясняется Таблицей, где приведены режимы синтеза гексахлоррената цезия.
Технический результат достигается за счет проведения электролитического синтеза гексахлоррената цезия, который заключается в следующем. В водный раствор соляной кислоты концентрацией 350г/л добавляют хлорид цезия в количестве, соответствующем пределу растворимости соли – 1500г/л. Концентрация в 350г/л соответствует регламентируемым ГОСТ значениям. Синтез проводится в стеклянном термостатированном стакане. Ток электролиза 2А задается с помощью источника переменного тока с возможностью регулировки частоты в диапазоне от 1–50Гц. Материал катода и анода – металлический рений.
Под воздействием меньшего, чем 2А тока растворение рения идет слишком медленно, а при большем, чем 2А токе происходит активное газовыделение, что негативно сказывается на процессе синтеза. При частотах менее 1Гц проведение синтеза также возможно, но процесс требует использования сложного и дорогостоящего оборудования, что препятствует достижению заявленного результата. При частотах более 50 Гц растворения рения не происходит.
На катоде происходит реакция совместного выделения водорода (с выходом по току 95%) и металлического рения. За счет разных выходов по току на аноде и катоде в прианодном пространстве накапливаются ренийсодержащие ионы, которые взаимодействуют с насыщенным раствором хлорида цезия до образования ренийсодержащей соли – гексахлоррената цезия по уравнению (7).
Re4++2CsCl+4Cl-→Cs2ReCl6 (1)
Для подтверждения возможности реализации изобретения и достижения заявленного технического результата рассмотрим примеры осуществления изобретения.
Пример 1.
Электролитический синтез гексахлоррената цезия проводили в вводном растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия концентрацией 1500г/л. Электролиз вели в гальваностатических условиях при токе 2А. Частота тока составила 50Гц, время воздействия 1 час. В результате электролиза поверхность электродов покрывалась солевым осадком – гексахлоррената цезия, масса осадка составила 0,103г.
Пример 2.
Электролитический синтез гексахлоррената цезия проводили в вводном растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия концентрацией 1500г/л. Электролиз вели в гальваностатических условиях при токе 2А. Частота тока составила 40Гц, время воздействия 1 час. В результате электролиза поверхность электродов покрывалась солевым осадком – гексахлоррената цезия, масса осадка составила 0,164г.
Пример 3.
Электролитический синтез гексахлоррената цезия проводили в вводном растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия концентрацией 1500г/л. Электролиз вели в гальваностатических условиях при токе 2А. Частота тока составила 25Гц, время воздействия 1 час. В результате электролиза поверхность электродов покрывалась солевым осадком – гексахлоррената цезия, масса осадка составила 1,112г.
Пример 4.
Электролитический синтез гексахлоррената цезия проводили в вводном растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия концентрацией 1500г/л. Электролиз вели в гальваностатических условиях при токе 2А. Частота тока составила 10Гц, время воздействия 1 час. В результате электролиза поверхность электродов покрывалась солевым осадком – гексахлоррената цезия, масса осадка составила 2,796г.
Пример 5.
Электролитический синтез гексахлоррената цезия проводили в вводном растворе соляной кислоты концентрацией 350г/л с добавлением хлорида цезия концентрацией 1500г/л. Электролиз вели в гальваностатических условиях при токе 2А. Частота тока составила 1Гц, время воздействия 1 час. В результате электролиза поверхность электродов покрывалась солевым осадком – гексахлоррената цезия, масса осадка составила 4,616г.
Источники
1. Химические свойства неорганических веществ / Учеб. пособие для вузов. 3-е изд., испр. /Р. А. Лидин, В. А. Молочко, Л. Л. Андреева; под ред. Р. А. Лидина. – М.: Химия, 2000. 480 с.: ил.
2. Авторское свидетельство SU 291993, приор. от 12.05.1969, опубл. 14.09.1970, МПК С23С4/06.
3. Молчанов, А.М. Изучение влияния кислорода в расплавленном электролите CsCl –Cs2ReCl6 на текстуру и морфологию рениевых покрытий / А.М. Молчанов, К. К. Фазлутдинов, Л. М. Минченко, А. В. Исаков и др. // Вестник казанского технологического университета. –2012. –Т.15, №16. –78-81.
4. Борисова Л.В., Ермаков А.Н. Аналитическая химия рения – Наука , 1974. – 321 c.
5. Получение гексахлорренатов действием тетрахлорида углерода на перренаты (Hexachlororhenates(IV) by Action of Carbon Tetrachloride on Perrhenates) // Inorg. Chem. – 1964. – V.3, № 10. – P. 1388–1389.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ электрохимического получения компактных слоев металлического рения | 2017 |
|
RU2677452C1 |
| Электролитический способ получения покрытий и изделий из ниобия, легированного танталом | 2021 |
|
RU2775044C1 |
| Электролитический способ получения рениевых пленок | 2018 |
|
RU2710807C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ОСАЖДЕНИЯ РЕНИЯ | 1970 |
|
SU281993A1 |
| СПОСОБ ЭЛЕКТРОЛИТИЧЕСКОГО СИНТЕЗА ОСАДКОВ КРЕМНИЯ С РАЗВИТОЙ ПОВЕРХНОСТЬЮ ИЗ РАСПЛАВЛЕННЫХ СОЛЕЙ | 2024 |
|
RU2840651C1 |
| Способ извлечения циркония из облученных циркониевых материалов для снижения объема высокоактивных радиоактивных отходов | 2022 |
|
RU2804570C1 |
| СПОСОБ ПОЛУЧЕНИЯ 7-R-ПИРИДО[1,2-а]БЕНЗИМИДАЗОЛОВ | 2012 |
|
RU2522549C1 |
| БЕЗДИАФРАГМЕННЫЙ ЭЛЕКТРОСИНТЕЗ ЗАМЕЩЕННЫХ ПИРИДО[1,2-а]БЕНЗИМИДАЗОЛОВ | 2014 |
|
RU2556001C1 |
| Способ получения 1,2,3,4-тетрагидропиридо[1,2-a]бензимидазолов | 2020 |
|
RU2751058C1 |
| Способ электроосаждения сплошных осадков кремния из расплавленных солей | 2022 |
|
RU2795477C1 |
Изобретение относится к электролитическому получению гексахлоррената цезия, который может быть использован для приготовления электролитов, пригодных для электроосаждения рения. Синтез гексахлоррената цезия осуществляется путем электрохимической реакции ионизации металлического рения в растворе соляной кислоты концентрацией 350 г/л с добавлением хлорида цезия с концентрацией на пределе растворимости 1500 г/л под действием переменного тока 2 А и частотой 1–50 Гц с последующей химической реакцией. Способ обеспечивает упрощение синтеза гексахлоррената цезия и снижение затрат на его реализацию. 1 ил., 5 пр.
Cпособ синтеза гексахлоррената цезия, характеризующийся тем, что осуществляют электрохимическую реакцию ионизации металлического рения в растворе соляной кислоты концентрацией 350 г/л с добавлением хлорида цезия с концентрацией на пределе растворимости 1500 г/л под действием переменного тока 2 А и частотой 1–50 Гц с последующей химической реакцией.
| Horner W.W | |||
| et al | |||
| Hexachlororhenates (IV) by Action of Carbon Tetrachloride on Perrhenates., Inorg.Chem, 1964,V.3, pp.1388-1389 | |||
| Burgess J | |||
| et al | |||
| Solubilities of caesium hexachlororhenate(IV), hexabromorhenate(IV), and tetraoxorhenate(VII) in alcohol-water mixtures, and their relation to cosolvent characteristic volume., Journal of the Chemical |
Авторы
Даты
2021-10-28—Публикация
2019-12-24—Подача