ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительных заявок США №62/500578, поданной 3 мая 2017 года, №62/451271, поданной 27 января 2017 года и №62/397794, поданной 21 сентября 2017 года, каждая из которых включена посредством ссылки в полном объеме в допустимых случаях.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к области иммуномодулирования, и более конкретно к композициям и способам модулирования SIGLEC–15 (Siglec–15) и передачи сигнала, инициированного от него.
УРОВЕНЬ ТЕХНИКИ
Ig–подобные лектины, связывающие сиаловую кислоту («SIGLEC») представляют собой членов суперсемейства Ig. Эти трансмембранные белки 1–го типа включают в себя N–концевой V–домен, связывающий сиаловые кислоты, вариабельные количества C2–доменов Ig, трансмембранный участок и цитозольный хвост, и связываются специфично с сиаловыми кислотами, присоединенными к концевым участкам гликоконъюгатов клеточной поверхности. Были идентифицированы две первичные подгруппы SIGLEC: одна подгруппа включает в себя CD–33 и родственные CD33 SIGLEC, такие как SIGLEC–5, –6, –7, –8, –9, 10, –11, –14 и –16 у человека и CD33 и SIGLEC–E, –F, –G и –H у мыши (Crocker and Redelinghuys, Biochemical Society Transactions, 36 (6):1467–1471 (2008)). Вторая подгруппа состоит из Sn (сиалоадгезина) (SIGLEC–1), CD22 (SIGLEC–2), MAG (миелин–ассоциированного гликопротеина) (SIGLEC–4) и SIGLEC–15, все из которых являются высококонсервативными у млекопитающих. За исключением MAG, который экспрессируется в нервной системе, SIGLEC дифференциально экспрессируются в различных подгруппах лейкоцитов, где они играют роль в положительной и отрицательной регуляции иммунных и воспалительных ответов (McMillan and Crocker, Carbohydr. Res., 343:2050–2056 (2008) и Crocker, et al., Nat. Rev. Immunol., 7:255 266 (2007)).
Исследования свидетельствуют о том, что многие SIGLEC экспрессируются на иммунных клетках и имеют иммуносупрессорные свойства. В то же время подгруппа SIGLEC, в том числе SIGLEC–15, ассоциирована с активирующим белком сигнальной адаптерной молекулы DNAX, составляющим 12 кДа (DAP12), который имеет иммунорецепторный тирозиновый активационный мотив (ITAM) и включен в активацию иммунных клеток (Takamiya, et al., Glycobiology, 23(2):178–87 (2013)). SIGLEC–15 специфично экспрессируется на макрофагах и дендритных клетках селезенки и лимфатических узлов и предпочтительно распознает антиген sTn (Angata, et al., Glycobiology, 17(8):838–46 (2007) Epub 2007 May 4.). Клетки H157, сверхэкспрессирующие sTn (H157/ST6GalNAc–I), стимулировали секрецию TGF–β из экспрессирующих SIGLEC–15 макрофагов, индуцированных M–CSF (Takamiya, et al., Glycobiology, 23(2):178–87 (2013)). Кроме того, секреция TGF–β из клеток THP–1 усиливается в результате сверхэкспрессии SIGLEC–15 в клетках THP–1 и ST6GalNAc–I (фермента, ответственного за биосинтез структуры sTn) в клетках H157 соответственно, таким образом, что она может по меньшей мере частично зависеть от передачи сигнала с участием SIGLEC–15, индуцированного DAP12, а также одного или нескольких независимых от DAP12, зависимых от Sky или возможно независимых от Sky путей. TGF–β продуцируется как опухолевыми клетками, так и лейкоцитами, инфильтрующими в опухоль, в том числе макрофагами, и способствует прогрессированию и метастазированию опухолей, например, в результате усиления инвазии опухолевых клеток и в результате ингибирования функции иммунных клеток (Flavell, et al., Nat Rev Immunol, 10:554–567 (2010)). Эти данные могут свидетельствовать о том, что распознавание опухоль–ассоциированного sTn с помощью SIGLEC–15 активирует путь DAP12–Syk пути передачи сигнала, который усиливает продуцирование TGF–β из миелоидных клеток и в конечном итоге модифицирует микроокружение опухоли, что является предпочтительным для опухолевых клеток (Takamiya, et al., Glycobiology, 23(2):178–87 (2013)). SIGLEC–15 имеет типичный домен ITIM (SNYENL (SEQ ID NO:191)) в своем цитоплазматическом домене. Его функция еще подлежит характеризации.
В то же время имеется потребность в средствах и методиках модулирования SIGLEC–15 и передачи сигнала, инициированного от него.
Таким образом, целью данного изобретения является предложение композиций для детекции и модулирования SIGLEC–15.
Также целью данного изобретения является предложение способов модулирования SIGLEC–15 и передачи сигнала, инициированного от него, в целях повышения иммунного ответа или ослабления или обращения иммунной супрессии.
Также целью данного изобретения является предложение способа модулирования дифференцировки остеокластов в целях снижения резорбции костной ткани или повышения костеобразования.
Также целью данного изобретения является предложение способов лечения заболеваний и нарушений в результате модулирования SIGLEC–15 и передачи сигнала, инициированного от него.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Предложены молекулы, связывающие SIGLEC–15. Молекулы в типичном случае представляют собой антитело или его антиген–связывающий фрагмент, который иммуноспецифично связывается с SIGLEC–15. Например, в некоторых вариантах осуществления молекула, связывающая SIGLEC–15, содержит шесть областей, определяющих комплементарность (CDR), при этом CDR включают в себя три CDR легкой цепи полипептида, выбранного из группы, состоящей из SEQ ID NO:3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, или их варианта, последовательность которого по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична SEQ ID NO: 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, и три CDR тяжелой цепи полипептида, выбранного из группы, состоящей из SEQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119, или их варианта, последовательность которого по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична SEQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119, и при этом молекула, связывающая SIGLEC–15, связывается с SIGLEC–15. В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, содержит CDR легкой и тяжелой цепей мышиного анти–человеческого моноклонального антитела, называемого в данного документе как 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A.
В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, содержит вариабельный участок легкой цепи, содержащий аминокислотную последовательность полипептида, выбранного из группы, состоящей из SEQ ID NO:3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, или их варианта, последовательность которого по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична SEQ ID NO:3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, и/или вариабельный участок тяжелой цепи, содержащий аминокислотную последовательность полипептида, выбранного из группы, состоящей из SEQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119, или их варианта, последовательность которого по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична SEQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119. В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, содержит вариабельный(вариабельные) участок(участки) легкой и тяжелой цепей мышиных моноклональных анти–человеческих антител, называемых в данного документе как 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A.
В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, связывается с SIGLEC–15,
(I) расположенным на поверхности клетки (предпочтительно живой клетки);
(II) расположенным на поверхности клетки (предпочтительно живой клетки) в эндогенной концентрации;
(III) расположенным на поверхности живой клетки, и модулирует связывание между SIGLEC–15 (например, SEQ ID NO:1, SEQ ID NO:2 и т.д.) и Neu5Acα2–6GalNAcα, LRRC4C, контрецептором SIGLEC–15 (S15–CR) или их комбинацией;
(IV) расположенным на поверхности живой клетки, и снижает, предупреждает или ингибирует секрецию TGF–β;
(V) расположенным на поверхности живой клетки; или
(IV) их комбинацией.
Клетки, которые эндогенно экспрессируют SIGLEC–15, включают в себя макрофаги, дендритные клетки и раковые клетки.
Молекула, связывающая SIGLEC–15, может содержать один или несколько константных доменов из константной области иммуноглобулина (Fc). Константные домены могут представлять собой человеческие константные домены, например, домены IgA, IgD, IgE, IgG или IgM. В определенных вариантах осуществления константные домены IgG человека представляют собой домены IgG1, IgG2, IgG3 или IgG4. Молекула, связывающая SIGLEC–15, может быть детектируемым образом меченой или содержит конъюгированный токсин, лекарственное средство, рецептор, фермент лиганд рецептора. Молекула, связывающая SIGLEC–15, может представлять собой моноклональное антитело, человеческое антитело, химерное антитело, гуманизированное антитело или одноцепочечное антитело или их антигенсвязывающий фрагмент. Антитело может представлять собой моноспецифичное, биспецифичное, триспецифичное или мультиспецифичное антитело.
В одном варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее одну или несколько вариабельных легких цепей, имеющих аминокислотную последовательность SEQ ID NO: 195, 197, 199, 201 или 209.
В другом варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее одну или несколько вариабельных тяжелых цепей, имеющих аминокислотную последовательность SEQ ID NO:203, 206 или 207.
В другом варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее одну или несколько вариабельных легких цепей, имеющих аминокислотную последовательность SEQ ID NO: 195, 197, 199, 201 или 209, и одну или несколько вариабельных тяжелых цепей, имеющих аминокислотную последовательность SEQ ID NO:203, 206 и 207.
В одном варианте осуществления предложено антитело, имеющее CDR легких цепей SEQ ID NO:209, 195, 207, 199 или 201 и CDR тяжелых цепей SEQ ID NO:203, 206 или 207 и их комбинации.
В другом варианте осуществления предложено антитело, имеющее аминокислотную последовательность легкой цепи в соответствии с SEQ ID NO:209, 210 или 211.
В другом варианте осуществления предложено антитело, имеющее аминокислотную последовательность тяжелой цепи в соответствии с SEQ ID NO: 212, 213, 215 или 216.
В другом варианте осуществления предложено антитело, имеющее аминокислотную последовательность легкой цепи в соответствии с SEQ ID NO:209, 210 или 211 и аминокислотную последовательность тяжелой цепи в соответствии с SEQ ID NO: 212, 213, 215 или 216.
В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, является модифицированной таким образом, что молекула будет проявлять сниженную или отсутствующую активность связывания по отношению к Fc–рецептору (FcR). В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, является модифицированной таким образом, чтобы проявлять активности в направлении антителозависимой клеточноопосредованной цитотоксичности (ADCC) или комплементзависимой цитотоксичности (CDC).
В одном варианте осуществления предложен слитый белок, который по меньшей мере на 50, 60, 70, 80, 85, 90, 95, 96, 97, 98, 99 или 100% идентичен SEQ ID NO:193 или 194.
Также предложены фармацевтические композиции, содержащие молекулу, связывающую SIGLEC–15, и физиологически приемлемый носитель или наполнитель. В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, снижает или предупреждает связывание SIGLEC–15 с лигандом и/или его контрецептором, снижает или предупреждает передачу сигнала, опосредованную SIGLEC–15, или их комбинацию. Лиганд может представлять собой сиалированный гликопротеин. Лиганд может экспрессироваться на поверхности опухолевой клетки. В примерах ниже показано, что белок 4С, содержащий богатые лейцином повторы (LRRC4C), представляет собой лиганд к SIGLEC–15, и может экспрессироваться раковыми клетками. Контрецептор SIGLEC–15 также может экспрессироваться на поверхности иммунных клеток, таких как T–клетки, который при связывании SIGLEC–15, приводит к ингибированию T–клеток.
Также предложены способы лечения субъектов, нуждающихся в этом. В типичном случае способы включают введение субъекту эффективного количества молекулы, связывающей SIGLEC–15, например, в фармацевтической композиции. В некоторых вариантах осуществления молекула–антагонист, связывающая SIGLEC–15, повышает иммунный ответ, замедляет или предупреждает опухолевый рост, ингибирует опосредованную опухолью иммунную супрессию, уничтожает опухоли, снижает или блокирует активность опухоль–ассоциированных макрофагов (TAM) таким образом, чтобы изменить их активность, ослабляет опосредованную TAM иммунную супрессию, ослабляет или обращает T–клеточную супрессию, повышает T–клеточную пролиферацию или их комбинацию. В некоторых вариантах осуществления рак или опухоль содержит макрофаги, экспрессирующие SIGLEC–15. Молекулу, связывающую SIGLEC–15, можно вводить субъекту в эффективном количестве для снижения экспрессии и/или секреции TGF–β макрофагами. В некоторых вариантах осуществления субъект имеет рак или инфекционное заболевание. Рак может содержать клетки, экспрессирующие или сверхэкспрессирующие лиганд SIGLEC–15.
Также предложены способы снижения дифференцировки остеокластов, снижения резорбции костной ткани, повышения костеобразования и их комбинации в результате введения субъекту эффективного количества молекул–антагонистов, связывающих SIGLEC–15.
В некоторых вариантах осуществления молекула–агонист, связывающая SIGLEC–15, снижает иммунный ответ, повышает или усиливает T–клеточную супрессию, повышает T–клеточную пролиферацию или их комбинацию. Молекулу, связывающую SIGLEC–15, можно вводить субъекту в эффективном количестве для повышения экспрессии и/или секреции TGF–β макрофагами. В некоторых вариантах осуществления субъект имеет воспаление, аутоиммунное заболевание или представляет собой реципиента трансплантата.
Некоторые варианты осуществления включают введение субъекту второго терапевтического агента.
Также предложены способы детекции и диагностики. Любой из способов детекции и диагностики может сочетаться со способом лечения. Например, способ детекции или диагностики заболевания, нарушения или инфекции может включать (a) анализ экспрессии SIGLEC–15 в клетках или в образце ткани субъекта с помощью раскрываемых молекул, связывающих SIGLEC–15, и (b) сравнение уровня SIGLEC–15 с контрольным уровнем, при этом повышение анализируемого уровня SIGLEC–15 по сравнению с контрольным уровнем указывает на заболевание, нарушение или инфекцию.
Способ контроля прогрессирования заболевания, нарушения или инфекции может включать (a) анализ экспрессии SIGLEC–15 в клетках или в образце ткани субъекта, полученных в первой временной точке и более поздней временной точке с помощью раскрываемых молекул, связывающих SIGLEC–15; и (b) сравнение уровня экспрессии SIGLEC–15 в клетках или в образце ткани субъекта в первой и более поздних временных точках, при этом повышение анализируемого уровня SIGLEC–15 в более поздней временной точке по сравнению с первой временной точкой указывает на прогрессирование заболевания, нарушения или инфекции.
Предложен способ контроля ответа на лечение, который включает (a) анализ экспрессии SIGLEC–15 в клетках или в образце ткани субъекта до и после лечения с помощью раскрываемых молекул, связывающих SIGLEC–15; и (b) сравнение уровня SIGLEC–15 в динамике, при этом снижение анализируемого уровня SIGLEC–15 после лечения по сравнению с уровнем SIGLEC–15 до лечения указывает на благоприятный ответ на лечение.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 изображена кривая, которая показывает титр антител в плазме двух иммунизированных и двух неиммунзированных мышей с нокаутом по SIGLEC–15.
На Фиг. 2A–2C изображены выравнивания, которые показывают последовательности вариабельного участка легкой цепи 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B и 105A, и выделяют первую (2A), вторую (2B) и третью (2C) области, определяющие комплементарность (CDR).
На Фиг. 3A–3C изображены выравнивания, которые показывают последовательности вариабельного участка тяжелой цепи 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B и 105A, и выделяют первую (3A), вторую (3B) и третью (3C) области, определяющие комплементарность (CDR).
На Фиг. 4A изображена диаграмма измерения прямого связывания анти–SIGLEC–15 антител к человеческим или мышиным клеткам, экспрессирующим SIGLEC–15. На Фиг. 4B (1B2, 1C3, 1C12, 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9) и Фиг. 8C (6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104) и 105A (NC105)) изображены столбиковые диаграммы, которые показывают связывание анти–SIGLEC–15 антител (% позитивных клеток) с клетками, экспрессирующими SIGLEC–15, в анализе, проиллюстрированном на Фиг. 4A. На Фиг. 4C изображена столбиковая диаграмма, которая показывает связывание ант–SIGLEC–15 антител (1B2, 1C3, 1C12, 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104) и 105A (NC105)) (% позитивных клеток) с фиксированными в формалине клетками, экспрессирующими SIGLEC–15.
На Фиг. 5A–5B изображены линейные диаграммы, которые показывают связывание очищенного Ab 1C12, 8H8, 5G12, 3H10, 9A5, 6F8, 8C8, 1H3, 10G9, 1B2 и 1C3 Ab с клетками K562.hS15 (9A, за вычетом фонового связывания) и клетками 293T.mS15 (9B) (средняя интенсивность флуоресценции (MFI) в качестве функции концентрации первичных антител (мкг/мл)). На Фиг. 5C изображена точечная диаграмма связывания (MFI) очищенного Ab 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9 с клетками K562.hS15 по отношению к клеткам 293T.mS15.
На Фиг. 6A изображена столбиковая диаграмма, которая показывает процент клеток hS15+ U87, детектируемых с помощью каждого из Ab 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8 и 10G9 Ab. На Фиг. 6В изображена столбиковая диаграмма, которая показывает MFI клеток hS15+ U87, детектируемых с помощью каждого из Ab 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8 и 10G9 Ab. На Фиг. 6С изображена столбиковая диаграмма, которая показывает процент клеток S15+ U87, детектируемых с помощью каждого из Ab 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9А5 и 10G9 Ab.
На Фиг. 7A изображен эскиз, который иллюстрирует анализ блокирования антител. Клетки 293T, экспрессирующие лиганд LRRC4C, обрабатывают растворенным рецептором (hS15.hG1) и анти–S15 антителом, и затем связанный рецептор детектируют с помощью PE–анти–hFc антитела. На Фиг. 7B изображена столбиковая диаграмма, которая показывает % связывания hS15.G1 с антителами hS15.hG1–1 и 10G9, 5G12, 6F8, 8C8, 8H8, 9A5, 1C3, 1C12, 1H3, 3H10, 1B2, NC1, NC5, NC7 28A (NC28), NC38, NC41, NC53, 63A (NC63), NC73, NC74, NC76, 77A (NC77), 82B (NC82), NC84, NC87, NC90, 92A (NC92), CI3–33, CI1–33). На Фиг. 7C изображена столбиковая диаграмма, которая показывает блокирование S15/LRRC4C (%) контрольным mAb и антителами 1B2, 1C3, 1H3, 8H8, 6F8, 8C8, 9A5, 1C12, 3H10, 10G9 и 5G12. На Фиг. 7D изображена столбиковая диаграмма, которая показывает блокирование S15/LRRC4C (%) 1B2, 1C3, 1C12, 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9. На Фиг. 7E изображена столбиковая диаграмма, которая показывает блокирование S15/LRRC4C (%) 6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104) и 105A (NC105)).
На Фиг. 8A изображена диаграмма анализа T–клеточной супрессии. На Фиг. 8B и 8C изображены столбиковые диаграммы, показывающие обращение с помощью анти–S15 mAb опосредованной hS15.hG1 супрессии T–клеток человека в виде % поделившихся CD8+ T–клеток (12B) и CD4+ T–клеток (12C) и сравнивающие анализы, выполняемые с использованием (например, +hS15.hG1) (столбец слева в каждой паре) и без использования (например, –hS15.hG1) (столбец справа в каждой паре) hS15.hG1 в отношении антител 1B2, 1C3, 1C12 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9. На Фиг. 8D–8G изображены столбиковые диаграммы, которые показывают обращение с помощью анти–S15 mAb опосредованной hS15.hG1 супрессии Т–клеток человека в виде % поделившихся CD8+ T–клеток (Фиг. 8D и 8F) и CD4+ T–клеток (Фиг. 8E и 8G) в случае анализов, выполняемых с использованием hS15.hG1 в отношении антител 1B2, 1C3, 1C12 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9 (Фиг. 8D и 12E) и 6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104) и 105A (NC105) (Фиг. 8F и 8G). На Фиг. 8H и 8I изображены точечные диаграммы, которые показывают пролиферацию CD8 T–клеток в виде функции % блокирующей активности hS15_LRRC4C.
На Фиг. 9A изображена диаграмма анализа измерения изменения секреции INFγ. На Фиг. 9B изображена столбиковая диаграмма, которая показывает результаты анализа, представленного на диаграмме на Фиг. 13A, в отношении антител 1B2, 1C3, 1C12 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9.
На Фиг. 10 изображена столбиковая диаграмма, которая показывает TRAP (устойчивую к тартрату кислую фосфатазу) (поглощение, 540 нм) в присутствии антител 1C12, 8H8, 5G12, 3H10, 9A5, 6F8, 8C8, 1H3, 10G9, 1B2 и 1C3 в анализе образования остеокластов из свежевыделенных и обогащенных в отношении моноцитов PBMC 2 путями: сортировки с использованием колонки MACS (левая панель) или прикрепления к пластмассе в бессывороточной среде (правая панель).
На Фиг. 11 изображена диаграмма, которая иллюстрирует модель отрицательной регуляции иммунитета с помощью SIGLEC–15 в опухолевом микроокружении (TME), в том числе SIGLEC–15 (S15):SIGLEC–15–контррецептор (S15–CR) >>> T–клеточное направленное ингибирование пролиферации и цитокинеза, и/или SIGLEC–15:LRRC4C >>> продуцирование макрофагами TGF–β и иммунная супрессия в TME. Диаграмма показывает экспрессию SIGLEC–15 и его лигандов миелоидными клетками, Т–клетками и раковыми клетками, и передачу сигнала от них, а также взаимодействия между молекулами анти–SIGLEC–15 (блокирующими и нацеливающими) и анти–LRRC4C антителами и слитыми белками SIGLEC–15 (несшивающими/блокирующими).
На Фиг. 12A изображена таблица, которая показывает аминокислотную последовательность вариабельных легких цепей L1–L5 гуманизированного 5G12. На Фиг. 12В изображена таблица, которая показывает аминокислотную последовательность вариабельных тяжелых цепей H1–H3 гуманизированного 5G12.
На Фиг. 13A изображено выравнивание последовательности вариабельных легких цепей VL1–Vl5 гуманизированного 5G12 против мышиной VL. На Фиг. 13B изображено выравнивание последовательности вариабельных тяжелых цепей VH1–VH3 гуманизированного 5G12.
На Фиг. 14A изображена линейная диаграмма % пролиферации T–клеток против человеческого Fc S15 (мкг/мл), которая показывает, что % пролиферации T–клеток снижается по мере того, как повышается концентрация Fc S15. На Фиг. 14B изображена столбиковая диаграмма пг/мл IFN–γ в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15. На Фиг. 14С изображена столбиковая диаграмма пг/мл TNF–α в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15. На Фиг. 14D изображена столбиковая диаграмма пг/мл IL–6 в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15.
На Фиг. 15A и 15B изображены столбиковые диаграммы, которые показывают процент позитивных клеток в отношении связывания анти–S15 mAb, очищенного из гибридомы, с клетками, экспрессирующими человеческий S15 или мышиный S15.
На Фиг. 16A и 16B изображены столбиковые диаграммы процента поделившихся CD8+ T–клеток, обработанных указанными антителами. На Фиг. 16С и 16D изображены столбиковые диаграммы процента поделившихся CD4+ T–клеток, обработанных указанными антителами.
На Фиг. 17A и 17B изображены линейные диаграммы, которые показывают процент выживаемости в зависимости от дней после введения опухолевых клеток у животных, обработанных 5G12. На Фиг. 17C изображена линейная диаграмма процента прибавки веса в зависимости от дней после введения ID8.OVA.
На Фиг. 18 изображена линейная диаграмма процента прибавки веса в зависимости от дней после введения ID8.OVA.
На Фиг. 19A изображена схематическая диаграмма, которая показывает CD14+ моноциты человека, собранные из PBMC человека с помощью магнитных гранул для культивирования моноцитов Mitenyi после высевания в 96–луночных планшетах в присутствии M–CSF человека и RANKL человека совместно с указанными антителами. На Фиг. 19B изображена электронная микрофотография, которая показывает остеокласты, обработанные, как указано, 1H3. На Фиг. 19C изображена столбиковая диаграмма поглощения при 540 нм супернатанта, собранного через 7 дней, для анализа устойчивой к тартрату кислотой фосфатазы.
На Фиг. 20 изображена столбиковая диаграмма, которая показывает цитокины (пг/мл) INF–γ, IL–2, IL–4, IL–6, IL–10, IL–17A и TNF–α.
На Фиг. 21 изображена столбиковая диаграмма поглощения при 540 нм макрофагов RAW 264.7 мыши, культивированных в присутствии RANKL совместно с указанными антителами.
На Фиг. 22 изображено сравнение иллюстративных гуманизированных аминокислотных последовательностей вариабельных легких цепей 1H3.
На Фиг. 23 изображено сравнение иллюстративных гуманизированных аминокислотных последовательностей вариабельных тяжелых цепей 1H3.
На Фиг. 24 изображена иллюстрация предложенного механизма действия SIGLEC–15.
На Фиг. 25A изображена гистограмма FACS количества в зависимости от SIGLEC–15 PE, которая показывает, что макрофаги M2 экспрессируют SIGLEC–15. На Фиг. 25B изображена гистограмма FACS количества в зависимости от SIGLEC–15 PE в отношении макрофагов M1. На Фиг. 25C изображена гистограмма FACS количества в зависимости от SIGLEC –15 PE в отношении миелоидных клеток, происходящих из костного мозга мыши, обработанных макрофагальным колониестимулирующим фактором (M–CSF). На Фиг. 25D изображена гистограмма FACS количества в зависимости от SIGLEC –15 PE в отношении миелоидных клеток, происходящих из костного мозга мыши, обработанных M–CSF и интерлейкином–10 (IL–10). На Фиг. 25E изображена столбиковая диаграмма MFI–PE в отношении миелоидных клеток, происходящих из костного мозга мыши, обработанных M–CSF или M–CSF+IL10 и окрашенных изотипическим PE (прямоугольник серого цвета) или анти– SIGLEC–15 PE.
На Фиг. 26A изображена столбиковая диаграмма поглощения при 450 нм супернатантов из CD14+ моноцитов человека от донора №1603, высеянные в планшеты, покрытые Fc SIGLEC–15 (левый столбец точки концентрации) или растворенным SIGLEC–15 (правый столбец каждой точки концентрации). На Фиг. 26В изображена столбиковая диаграмма поглощения при 450 нм супернатантов из CD14+ моноцитов человека от донора №1704, высеянные в планшеты, покрытые Fc SIGLEC–15 (левый столбец точки концентрации) или растворенным SIGLEC–15 (правый столбец каждой точки концентрации). На Фиг. 26C изображена столбиковая диаграмма TNF–α (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1603. На Фиг. 26D изображена столбиковая диаграмма IL–6 (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1603. На Фиг. 26E изображена столбиковая диаграмма IL–1β (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1603. На Фиг. 26F изображена столбиковая диаграмма TNF–α (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1704. На Фиг. 26G изображена столбиковая диаграмма IL–6 (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1704. На Фиг. 26H изображена столбиковая диаграмма IL–1β (пг/мл) в зависимости от SIGLEC–15 Fc (мкг/мл) в отношении клеток от донора №1704.
На Фиг. 27A изображена диаграмма протокола эксперимента в случае Примера 19. На Фиг. 27B изображена столбиковая диаграмма % пролиферации CD8 миелоидных клеток человека, предварительно обработанных Fc S15; M2φ, M1φ, и незрелых DC, кокультивируемых с мечеными CFSE негативно селектируемыми аутологичными всеми T–клетками при соотношении клеток 1 миелоидная клетка: 2 T–клетки совместно с анти–CD3/CD28 гранулами (1 клетка из всех T–клеток: 2 гранулы). Столбцы слева направо обозначают: только T–клетки, T–клетки+гранулы, обработанные Fc S15, M2φ, M1φ, и imDC в случае Фиг. 27C–27G. На Фиг. 27C изображена столбиковая диаграмма IFN–γ (пг/мл) в отношении клеток, обработанных, как описано выше. На Фиг. 27D изображена столбиковая диаграмма TNF–α (пг/мл) в отношении клеток, обработанных, как описано выше. На Фиг. 27E изображен процент пролиферации CD4 в отношении клеток, обработанных, как описано выше. На Фиг. 27F изображена столбиковая диаграмма IL–6 (пг/мл) в отношении клеток, обработанных, как описано выше. На Фиг. 27G изображена столбиковая диаграмма IL–10 (пг/мл) в отношении клеток, обработанных, как описано выше.
На Фиг. 28A изображена линейная диаграмма поглощения при 450 нм в зависимости от mAb (мкг/мл) в отношении клеток от донора 1709. Верхняя линия представляет собой контрольное mAb, а нижняя линия представляет собой анти–S15 mAb. На Фиг. 28B изображено то же самое, что и на Фиг. 28A, но в отношении клеток от донора 1713.
На Фиг. 29 изображена диаграмма, которая иллюстрирует роль, которую SIGLEC–15 играет в образовании остеокластов.
На Фиг. 30A изображена гистограмма FACS CD14+ моноцитов человека, обработанных Fc S15 и окрашенных анти–αvβ3 интегрин mAb на 0–е сутки. На Фиг. 30В изображена гистограмма FACS CD14+ моноцитов человека, обработанных Fc S15 и окрашенных анти–αvβ3 интегрин mAb на 6–е сутки.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
I. Определения
Используемая в данном документе молекула считается способной «иммуноспецифично связываться» со второй молекулой, если такое связывание демонстрирует специфичность и аффинность антитела в отношении своего когнатного антигена. Считается, что антитела способны к «иммуноспецифичному связыванию» с целевым участком или конформацией («эпитопом») антигена, если такое связывание включает сайт распознавания антигена молекулы иммуноглобулина. Антитело, которое иммуноспецифично связывается с определенным антигеном, может связываться с другими антигенами с более низкой аффинностью, если другой антиген имеет некоторое сходство последовательности или конформационное сходство, которое распознается сайтом распознавания антигена, что определяется, например, с помощью иммунологических методов анализа, анализов BIACORE® или других анализов, известных в данной области техники, однако, не будет связываться с абсолютно неродственным антигеном. Предпочтительно, однако, чтобы антитела (и их антигенсвязывающие фрагменты) не давали перекрестную реакцию с другими антигенами. Антитела также могут связываться с другими молекулами с помощью способа, который не является иммуноспецифичным, например, с Fc–рецепторами, в результате связывания доменов в других участках/доменах молекулы, которые не включают сайт распознавания антигена, такой как Fc–участок.
Считается, что используемая в данном документе молекула «специфично связывается» со второй молекулой, если такое связывание демонстрирует специфичность и аффинность рецептора в отношении своего когнатного антигена. Молекула может быть способной физиологически связываться с более чем одной другой молекулой.
Предполагается, что используемый в данном документе термин «антитело» обозначает молекулу иммуноглобулина, которая имеет сайт распознавания антигена «вариабельного участка». Предполагается, что термин «вариабельный участок» разграничивает такой домен иммуноглобулина от доменов, которые повсеместно являются общими для антител (таких как Fc–домен антител). Вариабельный участок содержит «гипервариабельный участок», остатки которого отвечают за связывание с антигеном. Гипервариабельный участок содержит аминокислотные остатки из «области, определяющей комплементарность» или «CDR» (т.е. в типичном случае остатки в положениях примерно 24–34 (L1), 50–56 (L2) и 89–97 (L3) в вариабельном домене легкой цепи и остатки в положениях примерно 27–35 (H1), 50–65 (H2) и 95–102 (H3) в вариабельном домене тяжелой цепи; Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)), и/или такие остатки из «гипервариабельной петли» (т.е., остатки в положениях 26–32 (L1), 50–52 (L2) и 91–96 (L3) в вариабельном домене легкой цепи и 26–32 (H1), 53–55 (H2) и 96–101 (H3) в вариабельном домене тяжелой цепи; Chothia and Lesk, 1987, J. Mol. Biol. 196:901–917). Остатки «каркасной области» или «FR» представляют собой такие остатки вариабельного домена, которые отличаются от остатков гипервариабельного участка, определенного в данном документе. Термин антитело включает моноклональные антитела, мультиспецифичные антитела, человеческие антитела, гуманизированные антитела, синтетические антитела, химерные антитела, камелизованные антитела (см., например, Muyldermans et al., 2001, Trends Biochem. Sci. 26:230; Nuttall et al., 2000, Cur. Pharm. Biotech. 1:253; Reichmann and Muyldermans, 1999, J. Immunol. Meth. 231:25; международную публикацию №№ WO 94/04678 и WO 94/25591; патент США №6005079), одноцепочечные Fv (scFv) (см., например, Pluckthun в The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds. Springer–Verlag, New York, pp. 269–315 (1994)), одноцепочечные антитела, связанные дисульфидными связями Fv (sdFv), интраантитела и антиидиотипические (aнти–Id) антитела (в том числе, например, анти–Id и анти–анти–Id антитела, раскрываемые в данном документе). В частности, такие антитела включают молекулы иммуноглобулинов любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса.
Используемый в данном документе термин «антигенсвязывающий фрагмент» антитела относится к одной или нескольким частям антитела, которые содержат области, определяющие комплементарность («CDR»), и необязательно каркасные остатки, которые включают сайт распознавания антигена «вариабельного участка», и проявляют способность иммуноспецифично связываться с антигеном. Такие фрагменты включают Fab', F(ab')2, Fv, одноцепочечный фрагмент (ScFv) и их мутантные формы, встречающиеся в природе варианты и слитые белки, включающие сайт распознавания антигена «вариабельного участка» антитела и гетерологический белок (например, токсин, сайт распознавания антигена для другого антигена, фермент, рецептор или лиганд рецептора и т.д.).
Используемый в данном документе термин «фрагмент» относится к пептиду или полипептиду, содержащему аминокислотную последовательность из по меньшей мере 5 прилегающих друг к другу аминокислотных остатков, по меньшей мере 10 прилегающих друг к другу аминокислотных остатков, по меньшей мере 15 прилегающих друг к другу аминокислотных остатков, по меньшей мере 20 прилегающих друг к другу аминокислотных остатков, по меньшей мере 25 прилегающих друг к другу аминокислотных остатков, по меньшей мере 40 прилегающих друг к другу аминокислотных остатков, по меньшей мере 50 прилегающих друг к другу аминокислотных остатков, по меньшей мере 60 прилегающих друг к другу аминокислотных остатков, по меньшей мере 70 прилегающих друг к другу аминокислотных остатков, по меньшей мере 80 прилегающих друг к другу аминокислотных остатков, по меньшей мере 90 прилегающих друг к другу аминокислотных остатков, по меньшей мере 100 прилегающих друг к другу аминокислотных остатков, по меньшей мере 125 прилегающих друг к другу аминокислотных остатков, по меньшей мере 150 прилегающих друг к другу аминокислотных остатков, по меньшей мере 175 прилегающих друг к другу аминокислотных остатков, по меньшей мере 200 прилегающих друг к другу аминокислотных остатков или по меньшей мере 250 прилегающих друг к другу аминокислотных остатков.
Используемый в данном документе термин «модулировать» относится к способности изменять эффект, результат или активность (например, передачу сигнала). Такое модулирование может быть агонистическим или антагонистическим. Антагонистическое модулирование может быть частичным (т.е. облегчающим, но не устраняющим) или оно может полностью устранять такую активность (например, нейтрализация). Модулирование может включать интернализацию рецептора после связывания антитела или снижение экспрессии рецептора на целевой клетке. Агонистическое модулирование может усиливать или иным образом повышать или усиливать активность (например, передачу сигнала). В еще одном дополнительно варианте осуществления такое модулирование может изменять природу взаимодействия между лигандом и его когнатным рецептором таким образом, чтобы измерять природу вызванной передачи сигнала. Например, молекулы могут в результате связывания с лигандом или рецептором изменять способность таких молекул связываться с другими лигандами или рецепторами и, тем самым, изменять их общую активность. Предпочтительно такое модулирование будет обеспечивать по меньшей мере 10% изменение измеряемой активности иммунной системы, более предпочтительно по меньшей мере 50% изменение такой активности или по меньшей мере 2–кратное, 5–кратное, 10–кратное ил еще более предпочтительно по меньшей мере 100–кратное изменение такой активности.
Предполагается, что термин «по сути», используемый в контексте связывания или проявляемого эффекта, обозначает, что наблюдаемый эффект является физиологически или терапевтически значимым. Так, например, молекула способна значительно блокировать активность лиганда или рецептора, если степень блокады является физиологически или терапевтически значимой (например, если такая степень составляет более 60% полной величины, более 70% полной величины, более 75% полной величины, более 80% полной величины, более 85% полной величины, более 90% полной величины, более 95% полной величины или более 97% полной величины). Аналогично, считается, что молекула имеет по сути такую же иммуноспецифичность и/или характеристику, как другая молекула, если такие иммуноспецифичности и характеристики более чем на 60% идентичны, более чем на 70% идентичны, более чем 75% идентичны, более чем на 80% идентичны, более чем на 85% идентичны, более чем на 90% идентичны, более чем на 95% идентичны или более чем на 97% идентичны.
Используемые в данном документе «костимулирующие» сигналы включают в себя положительные костимулирующие сигналы (например, сигналы, которые приводят к повышению активности) и отрицательные костимулирующие сигналы (например, сигналы, которые приводят к ингибированию активности).
Используемый в данном документе термин «производное» относится к антителу или его антигенсвязывающему фрагменту, который иммуноспецифично связывается с той же самой мишенью исходного или эталонного антитела, но который отличается аминокислотной последовательностью от исходного или эталонного антитела или его антигенсвязывающего фрагмента в результате включения одной, двух, трех, четырех, пяти или более аминокислотных замен, добавлений, делеций или модификаций по отношению к исходному или эталонному антителу или его антигенсвязывающему фрагменту. Предпочтительно такие производные будут иметь по сути ту же самую иммуноспецифичность и/или характеристики или ту же самую иммуноспецифичность и характеристики, что и исходное или эталонное антитело или его антигенсвязывающий фрагмент. Аминокислотные замены или добавления таких производных могут включать встречающиеся в природе (т.е. кодируемые ДНК) или не встречающиеся в природе аминокислотные остатки. Термин «производное» включает в себя, например, химерные или гуманизированные варианты, а также варианты, имеющие измененные участки CH1, шарнирные участки, участки CH2, CH3 или CH4, для получения, например, антител и т.д., имеющих различные Fc–участки, которые проявляют усиленные или ослабленные эффекторные или связывающие характеристики.
Используемое в данном документе «химерное антитело» представляет собой молекулу, в которой различные части антитела происходят из различных молекул иммуноглобулинов, например, антитела, имеющие вариабельный участок, происходящий из отличного от человеческого антитела, и константный участок человеческого иммуноглобулина.
Используемый в данном документе термин «гуманизированное антитело» относится к иммуноглобулину, включающему каркасный участок иммуноглобулина человека и один или несколько CDR отличных от человеческого (как правило, мышиного или крысиного) иммуноглобулина. Отличный от человеческого иммуноглобулин, представляющий CDR, называется «донорским», а человеческий иммуноглобулин, представляющий каркас, называется «акцепторным». Константные участки могут не присутствовать, однако, если они имеются, они должны быть по сути идентичны константным участкам человеческих иммуноглобулинов, т.е., по меньшей мере приблизительно на 85–99%, предпочтительно приблизительно на 95% или более идентичны. Таким образом, все части гуманизированного иммуноглобулина, за исключением, возможно, CDR, по сути идентичны соответствующим частям встречающихся в природе последовательностей человеческих иммуноглобулинов. Гуманизированное антитело представляет собой антитело, содержащее легкую цепь гуманизированного иммуноглобулина и тяжелую цепь гуманизированного иммуноглобулина. Например, гуманизированное антитело не включало бы в себя типичное химерное антитело, поскольку, например, весь вариабельный участок химерного антитела является отличным от человеческого.
Используемый в данном документе термин «эндогенная концентрация» относится к уровню, при котором молекула экспрессируется в нативном состоянии (например, в отсутствие векторов экспрессии или рекомбинантных промоторов) клеткой (при этом клетка может представлять собой нормальную клетку, раковую клетку или инфицированную клетку).
Используемый в данном документе термин «лечить», «лечебный», «лечение» и «терапевтическое применение» относятся к устранению, ослаблению или нормализации одного или нескольких симптомов заболевания или нарушения, обостренных SIGLEC–15 или его лигандом.
Используемое в данном документе «терапетвически эффективное количество» относится к количеству терапевтического агента, которое является эффективным для опосредования клинически значимого устранения, ослабления или нормализации таких симптомов. Эффект является клинически значимым, если его величина является достаточной для оказания влияния на здоровье или прогноз заболевания субъекта–реципиента. Терапевтически эффективное количество может относиться к количеству терапевтического агента, достаточного для замедления или сведения к минимуму начала заболевания, например, задержки или сведения к минимуму распространения рака. Терапевтически эффективное количество может также относиться к количеству терапевтического агента, которое обеспечивает терапевтический эффект при лечении или контроле заболевания.
Используемый в данном документе термин «профилактичесий агент» относится к агенту, который может быть использован для предупреждения нарушения или заболевания до выявления каких–либо симптомов такого нарушения или заболевания. «Профилактически эффективное» количество представляет собой количество профилактического агента, достаточного для опосредования такой защиты. Профилактически эффективное количество может также относиться к количеству профилактического агента, которое обеспечивает профилактический эффект в предупреждении заболевания.
Используемый в данном документе термин «рак» относится к новообразованию или опухоли, образованной в результате патологического неконтролируемого роста клеток. Используемый в данном документе рак явным образом включает лейкозы и лимфомы. Термин «рак» относится к заболеванию, вовлекающему клетки, которые имеют потенциал к метастазированию в отдаленные участки и проявляют фенотипические признаки, которые отличаются от таковых клеток, не являющихся раковыми, например, образование колоний в трехмерном субстрате, таком как мягкий агар, или образование тубулярных сетей или паутинообразных матриц в трехмерной базальной мембране или препарате внеклеточного матрикса. Клетки, не являющиеся раковыми, не образуют колоний в мягком агаре и образуют отличающиеся структуры сферического типа в трехмерной базальной мембране или препаратах внеклеточного матрикса.
Используемая в данном документе «иммунная клетка» относится к любой клетке гемопоэтического происхождения, в том числе, но не ограничиваясь ими, Т–клеткам, B–клеткам, моноцитам, дендритным клеткам и макрофагам.
Используемая в данном документе «валентность» относится к числу сайтов связывания, доступных на молекулу.
Используемый в данном документе термин «иммунологический» или «иммунный» ответ представляет собой развитие полезного гуморального (антителоопосредованного) и/или клеточного (опосредованного антигенспецифичными Т–клетками или продуктами их секреции) ответа, направленного против пептида у пациента–реципиента. Такой ответ может представлять собой активный ответ, индуцированный введением иммуногена, или пассивный ответ, индуцированный введением антитела или примированных T–клеток. Клеточный иммунный ответ вызывается презентацией полипептидных эпитопов в ассоциации с молекулами MHC I или II класса в целях активации антигенспецифичных CD4+ T–хелперных клеток и/или CD8+ цитотоксических T–клеток. Ответ также может включать в себя активацию моноцитов, макрофагов, NK–клеток, базофилов, дендритных клеток, астроцитов, клеток микроглии, эозинофилов, активацию или рекрутинг нейтрофилов или других компонентов врожденного иммунитета. Наличие клеточно–опосредованного иммунологического ответа может быть определено с помощью анализов пролиферации (CD4+ T–клетки) или анализов с использованием CTL (цитотоксических Т–лимфоцитов). Относительный вклад гуморальных и клеточных ответов в защитный или терапевтический эффект иммуногена может быть охарактеризован с помощью раздельного выделения антител и Т–клеток из иммунизированного сингенного животного и измерения защитного или терапевтического эффекта у второго субъекта.
Используемый в данном документе «иммуногенный агент» или «иммуноген» способен индуцировать иммунологический ответ против самого себя при введении млекопитающему, необязательно в сочетании с адъювантом.
Используемые в данном документе термины «индивидуум», «хозяин», «субъект» и «пациент» используются в данном документе взаимозаменяемо и относятся к млекопитающему, в том числе, не ограничиваясь ими, человеку, грызунам, таким как мыши и крысы, и другим лабораторным животным.
Используемый в данном документе термин «полипептид» относится к цепи аминокислот любой длины, вне зависимости от модификации (например, фосфорилирования или гликозилирования). Термин полипептид включает в себя белки и их фрагменты. Полипептиды могут быть «экзогенными», означая, что они являются «гетерологичными», т.е. чужеродными по отношению к клетке–хозяину, подлежащей использованию, такими как человеческий полипептид, продуцируемый бактериальной клеткой. Полипептиды раскрыты в данном документе в виде последовательностей аминокислотных остатков. Эти последовательности пишутся слева направо в направлении от амино– к карбоксиконцу. В соответствии со стандартной номенклатурой последовательности аминокислотных остатков обозначаются как с помощью трехбуквенного, так и однобуквенного кода, указанного следующим образом: аланин (Ala, A), аргинин (Arg, R), аспарагин (Asn, N), аспарагиновая кислота (Asp, D), цистеин (Cys, C), глутамин (Gln, Q), глутаминовая кислота (Glu, E), глицин (Gly, G), гистидин (His, H), изолейцин (Ile, I), лейцин (Leu, L), лизин (Lys, K), метионин (Met, M), фенилаланин (Phe, F), пролин (Pro, P), серин (Ser, S), треонин (Thr, T), триптофан (Trp, W), тирозин (Tyr, Y) и валин (Val, V).
Используемый в данном документе термин «вариант» относится к полипептиду или полинуклеотиду, который отличается от эталонного полипептида или полинуклеотида, однако сохраняет основные свойства. Типичный вариант полипептида отличается аминокислотной последовательностью от другого, эталонного, полипептида. Как правило, отличия ограничены таким образом, что последовательности эталонного полипептида и варианта в целом очень похожи и во многих участках идентичны. Вариант и эталонный полипептид могут отличаться аминокислотной последовательностью вследствие одной или нескольких модификаций (например, замен, добавлений и/или делеций). Замещенный или вставленный аминокислотный остаток может представлять собой или может не представлять собой таковой, кодируемый с помощью генетического кода. Вариант полипептида может встречаться в природе, например, аллельный вариант или может представлять собой вариант, который, как известно, не встречается в природе.
Модификации и изменения могут быть выполнены в структуре полипептидов по данному раскрытию и по–прежнему можно получить молекулу, имеющую аналогичные характеристики, как и полипептид (например, консервативную аминокислотную замену). Например, определенные аминокислоты могут быть замещены на другие аминокислоты в последовательности без заметной потери активности. Поскольку это является интерактивной способностью и природой полипептида, которая определяет биологическую функциональную активность этого полипептида, то определенные аминокислотные замены могут быть выполнены в полипептидной последовательности и при этом по–прежнему можно получать полипептид с аналогичными свойствами.
При выполнении таких замен можно учитывать индекс гидропатичности аминокислот. Важность индекса гидропатичности аминокислот в обеспечении биологической функции полипептида в целом понятна в данной области техники. Известно, что определенные аминокислоты могут быть замещены другими аминокислотами, имеющими аналогичный индекс или балл гидропатичности, и по–прежнему приводить к образованию полипептида с аналогичной биологической активностью. Каждой аминокислоте был присвоен индекс гидропатичности на основании ее гидрофобности и зарядных характеристик. Эти индексы являются следующими: изолейцин (+4,5); валин (+4,2); лейцин (+3,8); фенилаланин (+2,8); цистеин/цистин (+2,5); метионин (+1,9); аланин (+1,8); глицин (–0,4); треонин (–0,7); серин (–0,8); триптофан (–0,9); тирозин (–1,3); пролин (–1,6); гистидин (–3,2); глутамат (–3,5); глутамин (–3,5); аспартат (–3,5); аспарагин (–3,5); лизин (–3,9); и аргинин (–4,5).
Считается, что относительный гидропатичный характер аминокислоты определяет вторичную структуру образующегося полипептида, которая, в свою очередь, определяет взаимодействие с другими молекулами, такими как ферменты, субстраты, рецепторы, антитела, антигены и кофакторы. В данной области техники известно, что аминокислота может быть замещена другой аминокислотой, имеющей аналогичный индекс гидропатичности, и по–прежнему можно получать функционально эквивалентный полипептид. При таких изменениях замена аминокислот, индексы гидропатичности которых находятся в пределах ± 2, является предпочтительной, таковые в пределах ± 1 являются особенно предпочтительными и таковые в пределах ± 0,5 являются еще более предпочтительными.
Замена подобных аминокислот также может быть выполнена на основании гидрофильности, в частности, если полипептид или пептид с эквивалентной биологической функцией, полученный подобным образом, предполагается использовать в иммунологических вариантах осуществления. Следующие значения гидрофильности были присвоены аминокислотным остаткам: аргинин (+3,0); лизин (+3,0); аспартат (+3,0 ± 1); глутамат (+3,0 ± 1); серин (+0,3); аспаригин (+0,2); глутамин (+0,2); глицин (0); пролин (–0,5 ± 1); треонин (–0,4); аланин (–0,5); гистидин (–0,5); цистеин (–1,0); метионин (–1,3); валин (–1,5); лейцин (–1,8); изолейцин (–1,8); тирозин (–2,3); фенилаланин (–2,5); триптофан (–3,4). Считается, что аминокислота может быть замещена другой, имеющей аналогичное значение гидрофильности, и по–прежнему можно получать биологически эквивалентный, и, в частности, иммунологически эквивалентный полипептид. При таких изменениях замена аминокислот, значения гидрофильности которых находятся в пределах ± 2, является предпочтительной, таковые в пределах ± 1 являются особенно предпочтительными и таковые в пределах ± 0,5 являются еще более предпочтительными.
Как указано выше, аминокислотные замены, как правило, основаны на относительном сходстве заместителей боковых цепей аминокислот, например, их гидрофобности, гидрофильности, заряде, размере и т.п. Иллюстративные замены, которые учитывают вышеизложенные характеристики, хорошо известны специалистам в данной области техники и включают (исходный остаток: иллюстративная замена): (Ala: Gly, Ser), (Arg: Lys), (Asn: Gln, His), (Asp: Glu, Cys, Ser), (Gln: Asn), (Glu: Asp), (Gly: Ala), (His: Asn, Gln), (Ile: Leu, Val), (Leu: Ile, Val), (Lys: Arg), (Met: Leu, Tyr), (Ser: Thr), (Thr: Ser), (Tip: Tyr), (Tyr: Trp, Phe) и (Val: Ile, Leu). Таким образом, варианты осуществления по данному раскрытию предусматривают функциональные или биологические эквиваленты полипептида, изложенные выше. В частности, варианты осуществления полипептидов могут включать варианты, которые на около 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или более идентичны последовательности полипептида, представляющего интерес.
Термин «процент (%) идентичности последовательности» определяют в виде процента нуклеотидов или аминокислот в кандидатной последовательности, которые идентичны нуклеотидам или аминокислотам в эталонной последовательности нуклеиновой кислоты, после выравнивания последовательностей и введения промежутков, при необходимости, для достижения максимального процента идентичности последовательностей. Выравнивание в целях определения процента идентичности последовательностей может быть достигнуто различными способами, которые находятся в пределах компетенции специалиста в данной области техники, например, с помощью общедоступного программного обеспечения, такого как программное обеспечение BLAST, BLAST–2, ALIGN, ALIGN–2 или Megalign (DNASTAR). Подходящие параметры для измерения выравнивания, в том числе любых выравниваний, необходимых для достижения максимального выравнивания по отношению к полному размеру последовательностей, подлежащих сравнению, могут быть определены с помощью известных способов.
В целях данного документа % идентичности последовательностей определенной нуклеотидной или аминокислотной последовательности C по отношению, с или против определенной нуклеотидной последовательности D (который альтернативно может быть перефразирован в виде определенной последовательности C, которая имеет или содержит определенный % идентичности последовательности по отношению, с или против определенной последовательности D) рассчитывается следующим образом:
100 умножить на дробь W/Z,
где W представляет собой число нуклеотидов или аминокислот, оцениваемых в качестве идентичных совпадений с помощью программы выравнивания последовательностей при выравнивании C и D в этой программе, и где Z представляет собой общее число нуклеотидов или аминокислот в D. Будет понятно, что в случае, если длина последовательности C не равна длине последовательности D, % идентичности последовательностей C по отношению к D не будет равной % идентичности последовательностей D по отношению к C.
Используемый в данном документе термин «фармацевтически приемлемый носитель» включает в себя любой из стандартных фармацевтических носителей, такой как фосфатно–солевой буферный раствор, вода и эмульсии, такие как эмульсия масло/вода или вода/масло, и различные типы увлажняющих агентов.
Используемые в данном документе термины «антигенная детерминанта» и «эпитоп» используются взаимозаменяемо и относятся к структуре, распознаваемой антителом.
Используемый в данном документе «конформационный эпитоп» представляет собой эпитоп, который содержит непрерывные участки аминокислотной последовательности антигена. Антитела связывают конформационный эпитоп на основании трехмерных свойств поверхности, формы или третичной структуры антигена.
Используемый в данном документе «линейный эпитоп» представляет собой эпитоп, который образован непрерывной последовательностью аминокислот из антигена. Линейные эпитопы в типичном случае содержат от около 5 до около 10 непрерывных аминокислотных остатков. Антитела связывают линейный эпитоп на основании первичной последовательности антигена.
Используемый в данном документе «паратоп», также называемый «антигенсвязывающим сайтом», представляет собой часть антитела, которое распознает и связывается с антигеном.
II. Композиции
A. Последовательности SIGLEC–15
Ig–подобный лектин 15, связывающий сиаловую кислоту («SIGLEC–15», также называемый антиген CD33–подобный 3 и CD33L3) представляет собой трансмембранный белок 1 типа, экспрессируемый на макрофагах и/или дендритных клетках селезенки и лимфатических узлов человека (Angata, et al., Glycobiology, 17(8):838–46 (2007), которая конкретным образом включена в данный документ посредством ссылки в полном объеме). Внеклеточный домен SIGLEC–15 связывается с сиалированными гликопротеинами и предпочтительно распознает структуру Neu5Acα2–6GalNAcα.
SIGLEC–15 ассоциируется с активирующим белком сигнальных адаптерных белков DNAX и (DAP)12 и DAP10 с помощью своего лизинового остатка (остаток K274) в трансмембранном домене, указывая на то, что он функционирует в качестве активирующей сигнальной молекулы. Ортологи SIGLEC–15 присутствуют не только у млекопитающих, но также и в других ответвлениях позвоночных, и считается, что они играют консервативную регуляторную роль в иммунной системе позвоночных.
SIGLEC–15 непосредственно регулирует T–клеточную функцию в результате ингибирования T–клеточной пролиферации и продуцирования провоспалительных цитокинов. SIGLEC–15 косвенно воздействует на T–клеточную функцию с помощью миелодиных клеток. SIGLEC–15, экспрессируемый на опухолевых клетках или макрофагах M2, взаимодействует со своим партнером по связыванию на миелодных клетках, обеспечивая сигнал для выживания и дифференцировки в уникальной популяции миелоидных клеток, которая продуцирует TNF–α, IL–6 и IL–1β. Секретируемые цитокины дополнительно активируют опухолевый рост. Эта подгруппа опухолевых клеток может влиять на T–клеточную функцию в результате снижения продуцирования IFN–γ в T–клетках.
Аминокислотные последовательности SIGLEC–15 человека известны в данной области техники и включают в себя, например,
MEKSIWLLACLAWVLPTGSFVRTKIDTTENLLNTEVHSSPAQRWSMQVPPEVSAEAGDA AVLPCTFTHPHRHYDGPLTAIWRAGEPYAGPQVFRCAAARGSELCQTALSLHGRFRLLGNPRRN DLSLRVERLALADDRRYFCRVEFAGDVHDRYESRHGVRLHVTAAPRIVNISVLPSPAHAFRALC TAEGEPPPALAWSGPALGNSLAAVRSPREGHGHLVTAELPALTHDGRYTCTAANSLGRSEASVY LFRFHGASGASTVALLLGALGFKALLLLGVLAARAARRRPEHLDTPDTPPRSQAQESNYENLSQ MNPRSPPATMCSP
(SEQ ID NO:1), UniProtKB – Q6ZMC9 (SIG15_HUMAN), и которая явно включена посредством ссылки в полном объеме.
SIGLEC–15 человека содержит сигнальную пептидную последовательность из аминокислот 1–19 SEQ ID NO:1, внеклеточный домен из аминокислот 20–263 SEQ ID NO:1 (изображен с помощью жирного и курсивного шрифта), трансмембранный домен из аминокислот 264–284 SEQ ID NO:1 и цитоплазматический домен из аминокислот 285–328 SEQ ID NO:1. Предполагается, что Ig–подобный V–домен происходит из аминокислот 40–158 SEQ ID NO:1 (изображен с помощью одиночного подчеркивания), и предполагается, что Ig–подобный C2–домен происходит из аминокислот 168–251 SEQ ID NO:1 (изображен с помощью двойного подчеркивания). Считается, что дисульфидные связи образуются между остатками 64 и 142; 95 и 104; и 187 и 237, и предполагается, что гликозилирование происходит в остатке 172. Аминокислоты 276–279 были обозначены как полилейциновый домен. Известным вариантом является вариант с заменой F273L.
Аминокислотные последовательности SIGLEC–15 мыши известны в данной области техники и включают в себя, например,
MEGSLQLLACLACVLQMGSLVKTRRDASGDLLNTEAHSAPAQRWSMQVPAEVNAEAGDA AVLPCTFTHPHRHYDGPLTAIWRSGEPYAGPQVFRCTAAPGSELCQTALSLHGRFRLLGNPRRN DLSLRVERLALADSGRYFCRVEFTGDAHDRYESRHGVRLRVTAAAPRIVNISVLPGPAHAFRAL CTAEGEPPPALAWSGPAPGNSSAALQGQGHGYQVTAELPALTRDGRYTCTAANSLGRAEASVYL FRFHGAPGTSTLALLLGALGLKALLLLGILGARATRRRLDHLVPQDTPPRSQAQESNYENLSQM SPPGHQLPRVCCEELLSHHHLVIHHEK
(SEQ ID NO:2), UniProtKB – A7E1W8 (A7E1W8_MOUSE), и которая явно включена посредством ссылки в полном объеме.
SIGLEC–15 мыши содержит сигнальную пептидную последовательность из аминокислот 1–23 SEQ ID NO:2, внеклеточный домен из аминокислот 24–262 SEQ ID NO:2 (изображен с помощью жирного и курсивного шрифта), трансмембранный домен из аминокислот 263–283 SEQ ID NO:2 и цитоплазматический домен из аминокислот 284–342 SEQ ID NO:2. Предполагается, что Ig–подобный V–домен происходит из аминокислот 40–145 SEQ ID NO:2 (изображен с помощью одиночного подчеркивания), и предполагается, что Ig–подобный C2–домен происходит из аминокислот 169–250 SEQ ID NO:2 (изображен с помощью двойного подчеркивания).
B. Молекулы, связывающие SIGLEC–15
Предложены молекулы, связывающие SIGLEC–15, такие как антитела и их антигенсвязывающие фрагменты и другие полипептиды, которые связываются с SIGLEC–15. Ниже предложены последовательности вариабельных участков тяжелой и легкой цепи и их CDR из мышиных анти–SIGLEC–15 антител. Предложены антитела, антигенсвязывающие фрагменты и другие полипептиды, содержащие одну или несколько из последовательностей, представленных ниже, и их вариантов. Например, предложены антитела, антигенсвязывающие фрагменты и полипептиды, содержащие одну, две или три CDR вариабельного участка легкой цепи анти–SIGLEC–15 антитела, и/или одну, две или три CDR вариабельного участка тяжелой цепи анти–SIGLEC–15 антитела, которые связываются с SIGLEC–15. В некоторых вариантах осуществления антитела, антигенсвязывающие фрагменты и полипептиды содержат вариабельный участок легкой цепи анти–SIGLEC–15 антитела, вариабельный участок тяжелой цепи анти–SIGLEC–15 антитела или их комбинацию и могут связываться с SIGLEC–15.
Например, раскрываемые молекулы могут иммуноспецифично связываться с SIGLEC–15 (например, SEQ ID NO:1, SEQ ID NO:2 и др.). Например, предложены молекулы, которые могут иммуноспецифично связываться с SIGLEC–15 человека:
(I) расположенным на поверхности клетки (предпочтительно живой клетки);
(II) расположенным на поверхности клетки (предпочтительно живой клетки) в эндогенной концентрации;
(III) расположенным на поверхности живой клетки, и модулирует связывание между SIGLEC–15 (например, SEQ ID NO:1, SEQ ID NO:2 и т.д.) и Neu5Acα2–6GalNAcα, LRRC4C, контрецептором SIGLEC–15 (S15–CR) или их комбинацией;
(IV) расположенным на поверхности живой клетки, и снижает, предупреждает или ингибирует секрецию TGF–β;
(V) расположенным на поверхности живой клетки, при этом клетка представляет собой миелоидную клетку, такую как макрофаг или дендритная клетка, или раковую клетку (например, клетку рака головного мозга, клетку почечно–клеточного рака (RCC), клетку саркомы Юинга, клетку рака молочной железы или клетку рака яичника);
(VI) их комбинацией.
1. Последовательности мышиного анти–человеческий SIGLEC–15 антитела
Как описано в Примерах ниже, мышей с нокаутом по SIGLEC–15 (n=2) иммунизировали hS15.mIg (внеклеточным доменом SIGLEC–15 человека [ECD], слитым с IgG2a мыши), эмульгированным с CFA (полным адъювантом Фрейнда), для генерации панели мышиных анти–человеческий SIGLEC–15 mAb.
Ниже предложены последовательности вариабельных участков легкой и тяжелой цепи моноклональных антител, продуцируемых двадцатью четырьмя гибридомами, называемых в данном документе 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A (также NC6 и №6), 28A (также NC28 и №28), 63A (также называемого NC63 и №63), 71A (также называемого NC71 и №71), 77A (также называемого NC77 и №77), 80A (также называемого NC80 и №80), 82B (также называемого NC82 и №82), 83B (также называемого NC83 и №83), 92A (также называемого NC92 и №92), 93B (также называемого NC93 и №93), 99B (также называемого NC99 и №99), 104B (также называемого NC104 и №104) и 105A (также называемого NC105 и №105). CDR подчеркнуты и выделены жирным шрифтом в контексте последовательностей легкой и тяжелой цепи. Последовательности и CDR также изображены в выравниваниях на Фиг. 2A–3C.
a. ПОСЛЕДОВАТЕЛЬНОСТИ 1B2:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 1B2 представляет собой:
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPWTFGGGTKLEIK
(SEQ ID NO:3), при этом
CDR1 легкой цепи 1B2: RSSQSIVHSNGNTYLE (SEQ ID NO:24)
CDR2 легкой цепи 1B2: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 1B2: FQGSHVPWT (SEQ ID NO:39).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 1B2, представляет собой:
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAGCATTGTACATAGTAATGGAAACACCTATTTAGAATGGTAC CTGCAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGA GGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGTGGACGTTCGGTGGA GGCACCAAGCTGGAAATCAAG
(SEQ ID NO:74).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 1B2 представляет собой:
EVQLVESGGGFVKPGGSLKLSCAASGFTFSDYGMHWVRQAPEKGLEWVAYISSGSSIIY YADTVKGRFTISRDNAKNTLFLQMTSLRSEDTAMYYCARDHYHGNGSDYWGQGTTLTVSS
(SEQ ID NO:13), при этом
CDR1 тяжелой цепи 1B2: GFTFSDYGMH (SEQ ID NO:46),
CDR2 тяжелой цепи 1B2: YISSGSSIIYYADTVKG (SEQ ID NO:56),
CDR3 тяжелой цепи 1B2: DHYHGNGSDY (SEQ ID NO:67).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 1B2, представляет собой:
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTCGTGAAGCCTGGAGGGTCCCTGAAACT CTCCTGTGCAGCCTCTGGATTCACTTTCAGTGACTATGGAATGCACTGGGTTCGTCAGGCTCCA GAGAAGGGGCTGGAGTGGGTTGCATACATTAGTAGTGGCAGTAGTATCATCTACTATGCAGACA CAGTGAAGGGCCGATTCACCATCTCCAGAGACAATGCCAAGAACACCCTGTTCCTGCAAATGAC CAGTCTGAGGTCTGAGGACACGGCCATGTATTACTGTGCAAGGGACCACTACCATGGTAACGGG TCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:85).
b. ПОСЛЕДОВАТЕЛЬНОСТИ 1C3:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 1C3 представляет собой:
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGFYYCMQHLEYPYTFGGGTRLEIK
(SEQ ID NO:4), при этом
CDR1 легкой цепи 1C3: RSSKSLLHSNGNTYLY (SEQ ID NO:25)
CDR2 легкой цепи 1C3: RMSNLAS (SEQ ID NO:33)
CDR3 легкой цепи 1C3: MQHLEYPYT (SEQ ID NO:40).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 1C3, представляет собой:
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATC CATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTATATTGGTTC CTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAG TCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGA GGCTGAGGATGTGGGTTTTTATTACTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGG GGGACCAGGCTGGAAATAAAA
(SEQ ID NO:75).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 1C3 представляет собой:
QVQLKQSGAELVKPGASVKISCKASGYIFTDYYVNWVKQRPGQGLEWIGKIGPGSVSIY YNEKFKGKATLTADKSSSTAYMQLSSLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA
(SEQ ID NO:14), при этом
CDR1 тяжелой цепи 1C3: GYIFTDYYVN (SEQ ID NO:47)
CDR2 тяжелой цепи 1C3: KIGPGSVSIYYNEKFKG (SEQ ID NO:57)
CDR3 тяжелой цепи 1C3: YYYGFAY (SEQ ID NO:68).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 1C3, представляет собой:
CAGGTCCAGCTGAAGCAGTCTGGAGCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGAT ATCCTGCAAGGCTTCTGGCTACATCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCT GGACAGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGGAAGTGTTAGTATTTACTACAATGAGA AGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAGCTCAG CAGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGGTTTGCTTAC TGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:86).
c. ПОСЛЕДОВАТЕЛЬНОСТИ 1H3:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 1H3 представляет собой:
DIQMTQASSSLSVSLGGRVTITCKASDHINNWLAWYQQKPGNAPRLLISGATSLETGVP SRFSGSGSGKDYTLSITSLQTEDVATYYCQQYWSSPLTFGAGTKLELK
(SEQ ID NO:5), при этом
CDR1 легкой цепи 1H3: KASDHINNWLA (SEQ ID NO:26)
CDR2 легкой цепи 1H3: GATSLET (SEQ ID NO:34)
CDR3 легкой цепи 1H3: QQYWSSPLT (SEQ ID NO:41).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 1H3, представляет собой:
GACATCCAGATGACACAGGCTTCATCCTCCTTGTCTGTATCTCTAGGAGGCAGAGTCAC CATTACTTGCAAGGCAAGTGACCACATTAATAATTGGTTGGCCTGGTATCAGCAGAAACCAGGA AATGCTCCTAGGCTCTTAATATCTGGTGCAACCAGTTTGGAAACTGGGGTTCCTTCAAGATTCA GTGGCAGTGGATCTGGAAAGGATTACACTCTCAGCATTACCAGTCTTCAGACTGAAGATGTTGC TACTTATTACTGTCAACAGTATTGGAGTTCTCCTCTCACGTTCGGTGCTGGGACCAAGCTGGAG CTGAAA
(SEQ ID NO:76).
ii. Гуманизированная легкая цепь
В одном варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной легкой цепи
DIQMTQSPSSLSASVGDRVTITCKASDHINNWLAWYQQKPGKAPKLLISGATSLETGVP SRFSGSGSGTDYTFTISSLQPEDIATYYCQQYWSSPLTFGGGTKVEIK (SEQ ID NO:209), при этом
CDR1 легкой цепи 1H3: KASDHINNWLA (SEQ ID NO:26)
CDR2 легкой цепи 1H3: GATSLET (SEQ ID NO:34)
CDR3 легкой цепи 1H3: QQYWSSPLT (SEQ ID NO:41).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
В другом варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной легкой цепи
DIQMTQSPSSLSASVGDRVTITCKASDHINNWLAWYQQKPGKVPKLLISGATSLETGVP SRFSGSGSGTDYTLTISSLQPEDVATYYCQQYWSSPLTFGGGTKVEIK (SEQ ID NO:210), при этом
CDR1 легкой цепи 1H3: KASDHINNWLA (SEQ ID NO:26)
CDR2 легкой цепи 1H3: GATSLET (SEQ ID NO:34)
CDR3 легкой цепи 1H3: QQYWSSPLT (SEQ ID NO:41).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
В еще одном варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной легкой цепи
DIQMTQSPSSLSASVGDRVTITCKASDHINNWLAWYQQKPGKAPKLLISGATSLETGVP SRFSGSGSGTDYTLTISSLQPEDVATYYCQQYWSSPLTFGGGTKVEIK (SEQ ID NO:211), при этом
CDR1 легкой цепи 1H3: KASDHINNWLA (SEQ ID NO:26)
CDR2 легкой цепи 1H3: GATSLET (SEQ ID NO:34)
CDR3 легкой цепи 1H3: QQYWSSPLT (SEQ ID NO:41).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
iii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 1H3 представляет собой:
QVQLKESGPGLVAPSQSLSITCTVSGFSLSNYGVHWVRQPPGKGLEWLVLIWSDGSTTY NSALKSRLSISKDNSKSQVFLKMNSLQTGDTAMYYCARHPYDDYSGYYYTMDYWGQGTSVTVSS
(SEQ ID NO:15), при этом
CDR1 тяжелой цепи 1H3: NYGVH (SEQ ID NO:48)
CDR2 тяжелой цепи 1H3: LIWSDGSTTYNSALKS (SEQ ID NO:58)
CDR3 тяжелой цепи 1H3: HPYDDYSGYYYTMDY (SEQ ID NO:69).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 1H3, представляет собой:
CAGGTGCAGCTGAAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCAT CACATGCACCGTCTCAGGGTTCTCATTAAGCAATTATGGTGTACACTGGGTTCGCCAGCCTCCA GGAAAGGGTCTGGAGTGGCTGGTACTGATATGGAGTGATGGAAGCACAACCTATAATTCAGCTC TCAAATCCAGACTGAGCATCAGCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAG TCTCCAAACTGGTGACACAGCCATGTACTACTGTGCCAGACATCCCTATGATGATTATTCCGGC TATTACTATACTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCA
(SEQ ID NO:87).
iv. Гуманизированные тяжелые цепи
В одном варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной тяжелой цепи
QVQLQESGPGLVKPSETLSLTCTVSGFSLSNYGVHWVRQPPGKGLEWIVLIWSDGSTTY NSALKSRVTISKDTSKNQVSLKLSSVTAADTAVYYCARHPYDDYSGYYYTMDYWGQGTLVTVSS (SEQ ID NO:212), при этом
CDR1 тяжелой цепи 1H3: NYGVH (SEQ ID NO:48)
CDR2 тяжелой цепи 1H3: LIWSDGSTTYNSALKS (SEQ ID NO:58)
CDR3 тяжелой цепи 1H3: HPYDDYSGYYYTMDY (SEQ ID NO:69).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
В другом варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной тяжелой цепи
QVQLQESGPGLVKPSETLSLTCTVSGFSLSNYGVHWVRQPPGKGLEWIGLIWSDGSTTY ASALKSRVTISKDTSKNQVSLKLSSVTAADTAVYYCARHPYDDYSGYYYTMDYWGQGTLVTVS (SEQ ID NO:213), при этом
CDR1 тяжелой цепи 1H3: NYGVH (SEQ ID NO:48)
CDR2 тяжелой цепи 1H3: LIWSDGSTTYASALKS (SEQ ID NO:214)
CDR3 тяжелой цепи 1H3: HPYDDYSGYYYTMDY (SEQ ID NO:69).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
В еще одном варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной тяжелой цепи
QVQLQESGPGLVKPSETLSLTCTVSGFSLSNYGVHWVRQPPGKGLEWIGLIWSDGSTTY NPSLKSRVTISKDTSKNQVSLKLSSVTAADTAVYYCARHPYDDYSGYYYTMDYWGQGTLVTVS (SEQ ID NO:215), при этом
CDR1 тяжелой цепи 1H3: NYGVH (SEQ ID NO:48)
CDR2 тяжелой цепи 1H3: LIWSDGSTTYNPSLKS (SEQ ID NO:218)
CDR3 тяжелой цепи 1H3: HPYDDYSGYYYTMDY (SEQ ID NO:69).
Подчеркнутые аминокислоты изменены по отношению к исходной последовательности.
В другом варианте осуществления предложено гуманизированное анти–SIGLEC–15 антитело, имеющее аминокислотную последовательность вариабельной тяжелой цепи
QVQLQESGPGLVKPSETLSLTCTVSGFSLSNYGVHWVRQPPGKGLEWIGLIWSEGSTTY ASALKSRVTISKDTSKNQVSLKLSSVTAADTAVYYCARHPYDDYSGYYYTMDYWGQGTLVTVS (SEQ ID NO:216), при этом
CDR1 тяжелой цепи 1H3: NYGVH (SEQ ID NO:48)
CDR2 тяжелой цепи 1H3: LIWSEGSTTYASALKS (SEQ ID NO:217)
CDR3 тяжелой цепи 1H3: HPYDDYSGYYYTMDY (SEQ ID NO:69).
d. ПОСЛЕДОВАТЕЛЬНОСТИ 1C12:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 1C12 представляет собой:
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPWTFGGGTKLEIK
(SEQ ID NO:3), при этом
CDR1 легкой цепи 1C12: RSSQSIVHSNGNTYLE (SEQ ID NO:24)
CDR2 легкой цепи 1C12: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 1C12: FQGSHVPWT (SEQ ID NO:39).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 1C12, представляет собой:
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAGCATTGTACATAGTAATGGAAACACCTATTTAGAATGGTAC CTGCAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGA GGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGTGGACGTTCGGTGGA GGCACCAAGCTGGAAATCAA
(SEQ ID NO:77).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 1C12 представляет собой:
EVQLVESGGGLVKPGGSLKLSCAASGFSFSDYGMHWVRQAPEKGLEWVAYISSGSSILY YADIVKGRFTISRDNAKNTLFLQMTSLRSEDTAMYYCARDHYHGNGSDYWGQGTTLTVSS
(SEQ ID NO:16), при этом
CDR1 тяжелой цепи 1C12: GFSFSDYGMH (SEQ ID NO:49)
CDR2 тяжелой цепи 1C12: YISSGSSILYYADIVK (SEQ ID NO:59)
CDR3 тяжелой цепи 1C12: DHYHGNGSDY (SEQ ID NO:67).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 1C12, представляет собой:
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTAGTGAAGCCTGGAGGGTCCCTGAAACT CTCCTGTGCAGCCTCTGGTTTCTCTTTCAGTGACTATGGAATGCACTGGGTTCGTCAGGCTCCA GAGAAGGGGCTGGAGTGGGTTGCATACATTAGTAGTGGCAGTAGTATCCTCTACTATGCAGACA TAGTGAAGGGCCGATTCACCATCTCCAGAGACAATGCCAAGAACACCCTGTTCCTGCAAATGAC CAGTCTGAGGTCTGAGGACACGGCCATGTATTACTGTGCAAGGGACCACTACCATGGTAACGGG TCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:88).
e. ПОСЛЕДОВАТЕЛЬНОСТИ 3H10:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 3H10 представляет собой:
QIILTQSPAIMSASPGEKVTMTCSASSSTSFMHWYQQKPGTSPKRWIFDTSKLASGVPG RFIGSGSGTSYSLTISTMEAEDAATYYCHQRSAYPWTFGGGTKLEIK
(SEQ ID NO:6), при этом
CDR1 легкой цепи 3H10: SASSSTSFMH (SEQ ID NO:27)
CDR2 легкой цепи 3H10: DTSKLA (SEQ ID NO:35)
CDR3 легкой цепи 3H10: HQRSAYPWT (SEQ ID NO:42).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 3H10, представляет собой:
CAAATTATTCTCACCCAGTCTCCAGCAATCATGTCTGCATCTCCAGGGGAGAAGGTCAC CATGACCTGCAGTGCCAGCTCAAGTACAAGTTTCATGCACTGGTACCAGCAGAAGCCAGGCACC TCCCCCAAAAGATGGATTTTTGACACATCCAAACTGGCTTCTGGAGTCCCTGGTCGCTTCATTG GTAGTGGGTCTGGGACCTCTTATTCTCTCACAATCAGCACCATGGAGGCTGAAGATGCTGCCAC TTATTACTGCCATCAGCGGAGTGCTTACCCATGGACGTTCGGTGGAGGCACCAAGCTGGAAATC AAA
(SEQ ID NO:78).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 3H10 представляет собой:
EVQLQQSGAELVRPGASVKLSCTASGFNIKDYYMHWVKERPEQGLEWIGRIDPEDGDIE YDPKFQGKATMTADTSSNTAYLQFSSLTSEDTAVYYCVTDYDYDGGWFAYWGQGTLVTVSA
(SEQ ID NO:17), при этом
CDR1 тяжелой цепи 3H10: GFNIKDYYMH (SEQ ID NO:50)
CDR2 тяжелой цепи 3H10: RIDPEDGDIEYDPKFQG (SEQ ID NO:60)
CDR3 тяжелой цепи 3H10: DYDYDGGWFAY (SEQ ID NO:70).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 3H10, представляет собой:
GAGGTTCAGCTGCAGCAGTCTGGGGCAGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTT GTCCTGCACAGCTTCTGGCTTCAACATTAAAGACTACTATATGCACTGGGTGAAAGAGAGGCCT GAACAGGGCCTGGAGTGGATTGGAAGGATTGATCCTGAGGATGGTGATATTGAATATGACCCGA AGTTCCAGGGCAAGGCCACTATGACTGCAGATACATCCTCCAACACAGCCTACCTGCAGTTCAG CAGCCTGACATCTGAGGACACTGCCGTCTATTATTGTGTCACGGACTATGATTACGACGGAGGC TGGTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:89).
f. ПОСЛЕДОВАТЕЛЬНОСТИ 5G12:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 5G12 представляет собой:
DIKMTQSPSSMYASLGERVTITCKASQDINSYLSWFQQKPGKSPKTLIYRANRLVDGVP SRFSGSGSGQDYSLTISSLEYEDMGIYYCLQYDEFPYTFGGGTKLEIKR
(SEQ ID NO:7), при этом
CDR1 легкой цепи 5G12: KASQDINSYLS (SEQ ID NO:28)
CDR2 легкой цепи 5G12: RANRLVD (SEQ ID NO:36)
CDR3 легкой цепи 5G12: LQYDEFPYT (SEQ ID NO:43).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 5G12, представляет собой:
GACATCAAGATGACCCAGTCTCCATCTTCCATGTATGCATCTCTAGGAGAGAGAGTCAC TATCACTTGCAAGGCGAGTCAGGACATTAATAGCTATTTAAGCTGGTTCCAGCAGAAACCAGGG AAATCTCCTAAGACCCTGATCTATCGTGCAAACAGATTGGTAGATGGGGTCCCATCAAGGTTCA GTGGCAGTGGATCTGGGCAAGATTATTCTCTCACCATCAGCAGCCTGGAGTATGAAGATATGGG AATTTATTATTGTCTACAGTATGATGAGTTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAA ATAAAA
(SEQ ID NO:79).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 5G12 представляет собой:
QVQLQQPGAELVKPGASVKMSCKASGYTFTSYWITWVIQRPGQGLEWIGDIYCGSDTMH YNEKFKNKATLTVDTSSSTAYMQLSSLTSEDSAVYYCARWWDYGSSYDYFDYWGQGTTLTVSS
(SEQ ID NO:18), при этом
CDR1 тяжелой цепи 5G12: GYTFTSYWIT (SEQ ID NO:51)
CDR2 тяжелой цепи 5G12: DIYCGSDTMHYNEKFKN (SEQ ID NO:61)
CDR3 тяжелой цепи 5G12: WWDYGSSYDYFDY (SEQ ID NO:71).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 5G12, представляет собой:
CAGGTCCAACTGCAGCAGCCTGGGGCTGAGCTTGTGAAGCCTGGGGCTTCAGTGAAGAT GTCCTGCAAGGCTTCTGGCTACACCTTCACCAGCTACTGGATAACCTGGGTGATACAGAGGCCG GGACAAGGCCTTGAGTGGATTGGAGATATTTATTGTGGTAGTGATACTATGCACTACAATGAGA AGTTCAAGAACAAGGCCACACTGACTGTAGACACATCCTCCAGCACAGCCTACATGCAGCTCAG CAGCCTGACATCTGAGGACTCTGCGGTCTATTACTGTGCAAGATGGTGGGACTACGGTAGTAGC TACGACTACTTTGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:90).
g. ПОСЛЕДОВАТЕЛЬНОСТИ 6F8:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 6F8 представляет собой:
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGVYYCMQHLEYPYTFGGGTKLEIKR
(SEQ ID NO:8), при этом
CDR1 легкой цепи 6F8: RSSKSLLHSNGNTYLY (SEQ ID NO:25)
CDR2 легкой цепи 6F8: RMSNLAS (SEQ ID NO:33)
CDR3 легкой цепи 6F8: MQHLEYPYT (SEQ ID NO:40).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 6F8, представляет собой:
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATC CATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTGTATTGGTTC CTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAG TCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGA GGCTGAGGATGTGGGTGTTTATTATTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGG GGGACCAAGCTGGAAATAAAA
(SEQ ID NO:80).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 6F8 представляет собой:
QVQLKQSGPELVRPGASVKISCEASGYTFTDYYVNWVKQRPGRGLEWIGKIGPGSVSIY YNEKFKDKATLTADKSSSTAYMQLSGLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA
(SEQ ID NO:19), при этом
CDR1 тяжелой цепи 6F8: GYTFTDYYVN (SEQ ID NO:52)
CDR2 тяжелой цепи 6F8: KIGPGSVSIYYNEKFKD (SEQ ID NO:62)
CDR3 тяжелой цепи 6F8: YYYGFAY (SEQ ID NO:68).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 6F8, представляет собой:
CAGGTCCAGCTGAAGCAGTCTGGACCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGAT ATCCTGCGAGGCTTCTGGCTACACCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCT GGACGGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGGAAGTGTTAGTATTTACTACAATGAGA AGTTCAAGGACAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAGCTCAG CGGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGTTTTGCTTAC TGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:91).
h. ПОСЛЕДОВАТЕЛЬНОСТИ 8C8:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 8C8 представляет собой:
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGVYYCMQHLEYPYTFGGGTKLEIK
(SEQ ID NO:9), при этом
CDR1 легкой цепи 8C8: RSSKSLLHSNGNTYLY (SEQ ID NO:25)
CDR2 легкой цепи 8C8: RMSNLAS (SEQ ID NO:33)
CDR3 легкой цепи 8C8: MQHLEYPYT (SEQ ID NO:40).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 8C8, представляет собой:
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATC CATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTGTATTGGTTC CTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAG TCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGA GGCTGAGGATGTGGGTGTTTATTACTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGG GGGACCAAGCTGGAAATAAAA
(SEQ ID NO:81).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 8C8 представляет собой:
QVQLKQSGAELVKPGASVKISCKASGYTFTDYYVNWVKQRPGQGLEWIGKIGPESVSIY YSEKFKAKATLTADKSSSTAYMQLSSLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA
(SEQ ID NO:20), при этом
CDR1 тяжелой цепи 8C8: GYTFTDYYVN (SEQ ID NO:52)
CDR2 тяжелой цепи 8C8: KIGPESVSIYYSEKFKA (SEQ ID NO:63)
CDR3 тяжелой цепи 8C8: YYYGFAY (SEQ ID NO:68).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 8C8, представляет собой:
CAGGTCCAGCTGAAGCAGTCTGGAGCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGAT ATCCTGCAAGGCTTCTGGCTACACCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCT GGACAGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGAAAGTGTTAGTATTTATTACAGTGAGA AGTTCAAGGCCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAACTCAG CAGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGGTTTGCTTAC TGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:92).
i. ПОСЛЕДОВАТЕЛЬНОСТИ 8H8:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 8H8 представляет собой:
QAVVTQESALTTSPGETVTLTCRSSSGAVTTGNFANWVQEKPDHLFTGLIGGTNNRAPG VPARFSGSLIGDKAALTITGAQTEDEAIYFCALWYSNHWVFGGGTKLTVL
(SEQ ID NO:10), при этом
CDR1 легкой цепи 8H8: RSSSGAVTTGNFAN (SEQ ID NO:29)
CDR2 легкой цепи 8H8: GTNNRAP (SEQ ID NO:37)
CDR3 легкой цепи 8H8: ALWYSNHWV (SEQ ID NO:44).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 8H8, представляет собой:
CAGGCTGTTGTGACTCAGGAATCTGCACTCACCACATCACCTGGTGAAACAGTCACACT CACTTGTCGCTCAAGTTCTGGGGCTGTTACAACTGGTAACTTTGCCAACTGGGTCCAAGAAAAA CCAGATCATTTATTCACTGGTCTAATAGGTGGTACCAACAACCGAGCTCCAGGTGTTCCTGCCA GATTCTCAGGCTCCCTGATTGGAGACAAGGCTGCCCTCACCATCACAGGGGCACAGACTGAGGA TGAGGCAATATATTTCTGTGCTCTATGGTACAGCAACCACTGGGTGTTCGGTGGAGGAACCAAA CTGACTGTCCTA
(SEQ ID NO:82).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 8H8 представляет собой:
EVQLLETGGGLVQPGGSRGLSCEGSGFTFSGFWMSWVRQTPGKTLEWIGDINSDGSAIN YAPSIKDRFTIFRDNDKNTLYLQMNNVRSEDTATYFCVRYDDYGYFDVWGTGTTVTVSS
(SEQ ID NO:21), при этом
CDR1 тяжелой цепи 8H8: GFTFSGFWMS (SEQ ID NO:53)
CDR2 тяжелой цепи 8H8: DINSDGSAINYAPSIKD (SEQ ID NO:64)
CDR3 тяжелой цепи 8H8: YDDYGYFDV (SEQ ID NO:72).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 8H8, представляет собой:
GAAGTGCAGCTGTTGGAGACTGGAGGAGGCTTGGTGCAACCGGGGGGGTCACGGGGACT CTCTTGTGAAGGCTCAGGGTTCACTTTTAGTGGCTTCTGGATGAGCTGGGTTCGACAGACACCT GGGAAGACCCTGGAGTGGATTGGAGACATTAATTCTGATGGCAGTGCAATAAACTACGCACCAT CCATAAAGGATCGATTCACTATCTTCAGAGACAATGACAAGAACACCCTGTACCTGCAGATGAA CAATGTGCGATCGGAGGACACAGCCACGTATTTCTGTGTGAGATATGATGATTACGGGTACTTC GATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA
(SEQ ID NO:93).
j. ПОСЛЕДОВАТЕЛЬНОСТИ 9A5:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 9A5 представляет собой:
DVVMTQTPLTLSVTIGQSASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK
(SEQ ID NO:11), при этом
CDR1 легкой цепи 9A5: KSSQSLLDSDGKTYLN (SEQ ID NO:30)
CDR2 легкой цепи 9A5: LVSKLDS (SEQ ID NO:38)
CDR3 легкой цепи 9A5: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 9A5, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAGTCAGCCTC CATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGA GGCTGAGGATTTGGGAGTTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAATAAAA
(SEQ ID NO:83).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 9A5 представляет собой:
HVQLQQSGAELARPGASVKLSCKASGYTFTSYGLIWVKQRTGQGLEWIGEIYPRSGNTY YNEKFKGKATLTADISSSTAYMELRSLTSEDSAVYFCASSSPHGDYWGQGTTLTVSS
(SEQ ID NO:22), при этом
CDR1 тяжелой цепи 9A5: GYTFTSYGLI (SEQ ID NO:54)
CDR2 тяжелой цепи 9A5: EIYPRSGNTYYNEKFKG (SEQ ID NO:65)
CDR3 тяжелой цепи 9A5: SSPHGDY (SEQ ID NO:73).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 9A5, представляет собой:
CACGTTCAGCTGCAGCAGTCTGGAGCTGAGTTGGCGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTTTAATCTGGGTGAAGCAGAGAACT GGACAGGGCCTTGAGTGGATTGGAGAGATTTATCCTAGAAGTGGTAATACTTACTACAATGAGA AGTTCAAGGGCAAGGCCACACTGACTGCAGACATATCCTCCAGCACAGCGTACATGGAGCTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGTTCCTCTCCTCACGGGGACTAC TGGGGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:94).
k. ПОСЛЕДОВАТЕЛЬНОСТИ 10G9:
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 10G9 представляет собой:
QAVVTQESALTTSPGETVTLTCRSSTGAVTTSNYANWVQEKPDHLFTGLIGGTNNRAPG VPARFSGSLIGDKAALTITGAQTEDEAIYFCALWYSNHWVFGGGTKLTVL
(SEQ ID NO:12), при этом
CDR1 легкой цепи 10G9: RSSTGAVTTSNYAN (SEQ ID NO:31)
CDR2 легкой цепи 10G9: GTNNRAP (SEQ ID NO:37)
CDR3 легкой цепи 10G9: ALWYSNHWV (SEQ ID NO:44).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 10G9, представляет собой:
CAGGCTGTTGTGACTCAGGAATCTGCACTCACCACATCACCTGGTGAAACAGTCACACT CACTTGTCGCTCAAGTACTGGGGCTGTTACAACTAGTAACTATGCCAACTGGGTCCAAGAAAAA CCAGATCATTTATTCACTGGTCTAATAGGTGGTACCAACAACCGAGCTCCAGGTGTTCCTGCCA GATTCTCAGGCTCCCTGATTGGAGACAAGGCTGCCCTCACCATCACAGGGGCACAGACTGAGGA TGAGGCAATATATTTCTGTGCTCTATGGTACAGCAACCACTGGGTGTTCGGTGGAGGAACCAAA CTGACTGTCCTA
(SEQ ID NO:84).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 10G9 представляет собой:
EVQLLETGGGLVQPGGSRGLSCEGSGFTFSDFWMSWVRQTPGKTLEWIGDINSDGSAVN YAPSIKDQFTIFRDNDKRTLHLQMINVRSEDTATYFCVRYDDYGYFDVWGTGTTVTVSS
(SEQ ID NO:23), при этом
CDR1 тяжелой цепи 10G9: GFTFSDFWMS (SEQ ID NO:55)
CDR2 тяжелой цепи 10G9: DINSDGSAVNYAPSIKD (SEQ ID NO:66)
CDR3 тяжелой цепи 10G9: YDDYGYFDV (SEQ ID NO:72).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 10G9, представляет собой:
GAAGTGCAGCTGTTGGAGACTGGAGGAGGCTTAGTGCAACCTGGGGGGTCACGGGGACT CTCTTGTGAAGGCTCAGGGTTCACTTTTAGTGACTTCTGGATGAGCTGGGTTCGACAGACACCT GGGAAGACCCTGGAGTGGATTGGAGACATTAATTCTGATGGCAGTGCAGTTAACTACGCACCAT CCATAAAGGATCAATTCACTATCTTCAGAGACAATGACAAGAGGACCCTGCACCTGCAGATGAT CAATGTTCGATCGGAGGACACAGCCACGTATTTCTGTGTGAGATATGATGATTACGGGTACTTC GATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA
(SEQ ID NO:95).
l. ПОСЛЕДОВАТЕЛЬНОСТИ 6A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 6A представляет собой:
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLRISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK
(SEQ ID NO:96), при этом
CDR1 легкой цепи 6A: RSSQSIVHSNGNTYLE (SEQ ID NO:24)
CDR2 легкой цепи 6A: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 6A: FQGSHVPLT (SEQ ID NO:157).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 6A, представляет собой:
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTAC CTGCAGAAGCCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAGGATCAGCAGAGTGGA GGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCT GGGACCAAGCTGGAGCTGAAA
(SEQ ID NO:120).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 6A представляет собой:
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDTE YASKFQDKATITTDTSSNTAYLQLSSLTSEDTAVYYCTTYVGFAYWGQGTLVTVST
(SEQ ID NO:108), при этом
CDR1 тяжелой цепи 6A: DDYMH (SEQ ID NO:162)
CDR2 тяжелой цепи 6A: CIDPENGDTEYASKFQD (SEQ ID NO:170)
CDR3 тяжелой цепи 6A: YVGFAY (SEQ ID NO:182).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 6A, представляет собой:
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAACTTGTGAGGCCAGGGGCCTCAGTCAAGTT GTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCT GAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATACTGAATATGCCTCGA AATTCCAGGACAAGGCCACTATAACAACAGACACATCCTCCAACACAGCCTACCTGCAGCTCAG CAGCCTGACATCTGAGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGCTTACTGG GGCCAAGGGACTCTGGTCACTGTCTCTACA
(SEQ ID NO:133).
m. ПОСЛЕДОВАТЕЛЬНОСТИ 28A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 28A представляет собой:
DVVMTQTPLTLSIPIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSEL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK
(SEQ ID NO:97), при этом
CDR1 легкой цепи 28A: KSSQSLLDSDGKTYLN (SEQ ID NO:30)
CDR2 легкой цепи 28A: LVSELDS (SEQ ID NO:153)
CDR3 легкой цепи 28A: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 28A, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGATTCCCATTGGACAACCAGCCTC CATCTCTTGTAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTCATCTATCTGGTGTCTGAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGA GGCTGAAGATTTGGGAGTTTATTATTGTTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAATAAAA
(SEQ ID NO:121).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 28A представляет собой:
QVQLQQSGAELARPGASVKLSCKASGYTFISYGITWVKQRTGQGLEWIGEIHPRSGNTY YNENFKDRASLTADKSSSTAYMEVRSLTSEDSAVYFCARGGPGDYWGQGTTLTVSS
(SEQ ID NO:109), при этом
CDR1 тяжелой цепи 28A: SYGIT (SEQ ID NO:163)
CDR2 тяжелой цепи 28A: EIHPRSGNTYYNENFKD (SEQ ID NO:171)
CDR3 тяжелой цепи 28A: GGPGDY (SEQ ID NO:183).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 28A, представляет собой:
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCTGGCTACACCTTCATAAGCTATGGTATAACCTGGGTGAAGCAGAGAACT GGACAGGGCCTTGAGTGGATTGGAGAGATTCATCCTAGAAGTGGTAATACTTACTACAATGAGA ATTTCAAGGACAGGGCCTCACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGAGGTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGGGGTGGGCCGGGGGACTACTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:134).
n. ПОСЛЕДОВАТЕЛЬНОСТИ 63A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 63A представляет собой:
DVVMTQTPLTLSVTIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK
(SEQ ID NO:98), при этом
CDR1 легкой цепи 63A: KSSQSLLDSDGKTYLN (SEQ ID NO:30)
CDR2 легкой цепи 63A: LVSKLDS (SEQ ID NO:38)
CDR3 легкой цепи 63A: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 63A, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTC CATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGA GGCTGAGGATTTGGGAGTTTATTATTGTTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAATAAAA
(SEQ ID NO:122).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 63A представляет собой:
QVQLQQSGAELARPGASVKLSCKASGYTFTSYGISWVKQRTGQGLEWIGQIYPRSDNTY YNERFKGKATLTADKSSSTAYMALRSLTSEDSAVYFCAREGGPDYWGQGTTLTVSS
(SEQ ID NO:110), при этом
CDR1 тяжелой цепи 63A: SYGIS (SEQ ID NO:164)
CDR2 тяжелой цепи 63A: QIYPRSDNTYYNERFKGK (SEQ ID NO:172)
CDR3 тяжелой цепи 63A: EGGPDY (SEQ ID NO:184).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 63A, представляет собой:
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTATAAGCTGGGTGAAGCAGAGAACT GGACAGGGCCTTGAGTGGATTGGACAGATTTATCCTAGAAGTGACAATACTTACTACAATGAGA GGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGCGCTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGAGAGGGGGGTCCCGACTACTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:135).
o. ПОСЛЕДОВАТЕЛЬНОСТИ 71A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 71A представляет собой:
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK
(SEQ ID NO:99), при этом
CDR1 легкой цепи 71A: RSSQSIVHSNGNTYLE (SEQ ID NO:24)
CDR2 легкой цепи 71A: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 71A: FQGSHVPLT (SEQ ID NO:157).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 71A, представляет собой:
GACGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTAC CTACAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGA GGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCT GGGACCAAGCTGGAGCTGAAA
(SEQ ID NO:123).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 71A представляет собой:
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDIE YASRFQGKATMTADTSSNTAYLQLTSLTSADTAVYYCTTYVGFGYWGQGTLVTVSA
(SEQ ID NO:111), при этом
CDR1 тяжелой цепи 71A: DDYMH (SEQ ID NO:162)
CDR2 тяжелой цепи 71A: CIDPENGDIEYASRFQG (SEQ ID NO:173)
CDR3 тяжелой цепи 71A: YVGFGY (SEQ ID NO:185).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 71A, представляет собой:
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTT GTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCT GAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATATTGAATATGCCTCGA GGTTCCAGGGCAAGGCCACTATGACAGCAGACACATCCTCCAACACAGCCTACCTGCAGCTCAC CAGCCTGACATCTGCGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGG GGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:136).
p. ПОСЛЕДОВАТЕЛЬНОСТИ 77A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 77A представляет собой:
DVLMTQSPLSLPVSLGDQASISCRSSQNIVHSNGNTYLEWYLKKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGMYYCFQGSHVPLTFGAGTKLELK
(SEQ ID NO:100), при этом
CDR1 легкой цепи 77A: RSSQNIVHSNGNTYLE (SEQ ID NO:146)
CDR2 легкой цепи 77A: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 77A: FQGSHVPLT (SEQ ID NO:157).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 77A, представляет собой:
GATGTTTTGATGACCCAAAGTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAACATAGTACATAGTAATGGTAACACCTATTTAGAATGGTAC CTGAAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTCTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGA GGCTGAGGATCTGGGAATGTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGAGCT GGGACCAAGCTGGAGCTGAAA
(SEQ ID NO:124).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 77A представляет собой:
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDTE YASKFQGKATITADTSSNTVYLQLSSLTSEDTAVYYCTTYVGFGYWGQGTLVTVSA
(SEQ ID NO:112), при этом
CDR1 тяжелой цепи 77A: DDYMH (SEQ ID NO:162)
CDR2 тяжелой цепи 77A: CIDPENGDTEYASKFQG (SEQ ID NO:174)
CDR3 тяжелой цепи 77A: YVGFGY (SEQ ID NO:185).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 77A, представляет собой:
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTT GTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCT GAACAGGGCCTGGAGTGGATTGGATGTATTGATCCTGAGAATGGTGATACTGAATATGCCTCGA AGTTCCAGGGCAAGGCCACTATAACAGCAGACACATCCTCCAACACAGTCTACCTGCAGCTCAG CAGCCTGACATCTGAGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGG GGCCAGGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:137).
q. ПОСЛЕДОВАТЕЛЬНОСТИ 80A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 80A представляет собой:
DIVMTQSPSSLTVTAGEKVTMSCKSNQSLLNSGDQKNYLTWYQQKPGQPPKLLIYWAST RESGVPDRFTGSGSGTDFTLTISSVQAEDLAIYYCQNDYSYPLTFGAGTKLELK
(SEQ ID NO:101), при этом
CDR1 легкой цепи 80A: KSNQSLLNSGDQKNYLT (SEQ ID NO:147)
CDR2 легкой цепи 80A: WASTRES (SEQ ID NO:154)
CDR3 легкой цепи 80A: QNDYSYPLT (SEQ ID NO:158).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 80A, представляет собой:
GACATTGTGATGACACAGTCTCCATCCTCCCTGACTGTGACAGCAGGAGAGAAGGTCAC TATGAGCTGCAAGTCCAATCAGAGTCTGTTAAACAGTGGAGATCAAAAGAACTACTTGACCTGG TACCAGCAGAAACCAGGGCAGCCTCCTAAACTATTGATCTACTGGGCATCCACTAGGGAATCTG GGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGAACAGATTTCACTCTCACCATCAGCAGTGT GCAGGCTGAAGACCTGGCAATTTATTACTGTCAGAATGATTATAGTTATCCACTCACGTTCGGT GCTGGGACCAAGCTGGAGCTGAAA
(SEQ ID NO:125).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 80A представляет собой:
QVQLKQSGAELVRPGASVKLSCRASGYTFTDFYINWVKQRPGQGLEWIARIYPGSDETY YNEKFKDKVTLTAEKSSSTAYMQLSSLTSEDSAVYFCALWFFDVWGTGTTVTVSS
(SEQ ID NO:113), при этом
CDR1 тяжелой цепи 80A: DFYIN (SEQ ID NO:165)
CDR2 тяжелой цепи 80A: RIYPGSDETYYNEKFKD (SEQ ID NO:175)
CDR3 тяжелой цепи 80A: WFFDV (SEQ ID NO:186).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 80A, представляет собой:
CAGGTCCAACTGAAGCAGTCTGGGGCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAGGGCTTCTGGCTACACTTTCACTGACTTCTACATAAACTGGGTGAAGCAGAGGCCT GGACAGGGACTTGAGTGGATTGCAAGGATTTATCCTGGAAGTGATGAGACTTACTACAATGAGA AGTTTAAGGACAAGGTCACACTGACTGCAGAAAAATCCTCCAGCACTGCCTACATGCAGCTCAG CAGCCTGACATCTGAGGACTCTGCTGTCTATTTCTGTGCCCTCTGGTTCTTCGATGTCTGGGGC ACAGGGACCACGGTCACCGTCTCCTCA
(SEQ ID NO:138).
r. ПОСЛЕДОВАТЕЛЬНОСТИ 82B
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 82В представляет собой:
DVVMTQTPLTLSVTIGQSASISCKSSQSLLDSDGNTYLNWLLQRPGQSPKRLIYLVSEL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK
(SEQ ID NO:102), при этом
CDR1 легкой цепи 82В: KSSQSLLDSDGNTYLN (SEQ ID NO:148)
CDR2 легкой цепи 82В: LVSELDS (SEQ ID NO:153)
CDR3 легкой цепи 82В: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 82В, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACTATTGGACAATCAGCCTC CATCTCTTGCAAGTCAAGTCAGAGCCTCCTAGATAGTGATGGAAACACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATTTGGTGTCTGAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGA GGCTGAGGATTTGGGAGTTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAATAAAA
(SEQ ID NO:126).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 82В представляет собой:
QVQLQQSGAELARPGASVKLSCKASGYTFTSDGITWVKQRTGQGLEWIGQIHPRSGNTY YNGKFKGKATLTADRSSSTTYMELRSLTSEDSAVYFCAKTGTGDYWGQGTTLTVSS
(SEQ ID NO:114), при этом
CDR1 тяжелой цепи 82В: SDGIT (SEQ ID NO:166)
CDR2 тяжелой цепи 82В: QIHPRSGNTYYNGKFKG (SEQ ID NO:176)
CDR3 тяжелой цепи 82В: TGTGDY (SEQ ID NO:187).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 82В, представляет собой:
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGTTGGCGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCGGGCTACACCTTCACAAGCGATGGTATTACCTGGGTGAAGCAGAGAACT GGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACCTACTACAATGGGA AGTTCAAGGGCAAGGCCACACTGACTGCAGACAGATCCTCCAGCACAACGTACATGGAACTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAAAACTGGGACGGGGGACTACTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:139).
s. ПОСЛЕДОВАТЕЛЬНОСТИ 83B
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 83В представляет собой:
EIQMTQSPSSMSASLGDRITITCQATQDIVKNLNWYQQKPGKPPSFLIYYATELAEGVP SRFSGSGSGSDYSLTISNLESEDFADYYCLQFYEFPYTFGGGTKLEIK
(SEQ ID NO:103), при этом
CDR1 легкой цепи 83В: QATQDIVKNLN (SEQ ID NO:149)
CDR2 легкой цепи 83В: YATELAE (SEQ ID NO:155)
CDR3 легкой цепи 83В: LQFYEFPYT (SEQ ID NO:159).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 83В, представляет собой:
GAAATCCAGATGACCCAGTCTCCATCCTCTATGTCTGCATCTCTGGGAGACAGAATAAC CATCACTTGCCAGGCAACTCAAGACATTGTTAAGAATTTAAACTGGTATCAGCAGAAACCAGGG AAACCCCCTTCATTCCTGATCTATTATGCAACTGAACTGGCAGAAGGGGTCCCATCAAGGTTCA GTGGCAGTGGGTCTGGGTCAGACTATTCTCTGACAATCAGCAACCTGGAGTCTGAAGATTTTGC AGACTATTACTGTCTACAGTTTTATGAATTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAA ATAAAA
(SEQ ID NO:127).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 83В представляет собой:
EVQLQQSGPELVKPGASVKMSCKASGYTFTDYNMHWVKQSHGKSLEWIGYINPNNGGTS YNQKFKDKATLTVNKSSSTAFMELRSLASEDSAVYYCARSDWEDCWGQGTTLTVSS
(SEQ ID NO:115), при этом
CDR1 тяжелой цепи 83В: DYNMH (SEQ ID NO:167)
CDR2 тяжелой цепи 83В: YINPNNGGTSYNQKFKD (SEQ ID NO:177)
CDR3 тяжелой цепи 83В: SDWEDC (SEQ ID NO:188).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 83В, представляет собой:
GAGGTCCAGCTGCAACAGTCTGGACCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGAT GTCCTGCAAGGCTTCTGGATACACATTCACTGACTACAACATGCACTGGGTGAAGCAGAGCCAT GGAAAGAGCCTTGAGTGGATTGGATATATTAACCCTAACAATGGTGGTACTAGCTACAACCAGA AGTTCAAGGACAAGGCCACATTGACTGTAAACAAGTCCTCCAGCACAGCCTTCATGGAGCTCCG CAGCCTGGCATCGGAGGATTCTGCAGTCTATTACTGTGCAAGGTCTGACTGGGAAGACTGCTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:140).
t. ПОСЛЕДОВАТЕЛЬНОСТИ 92A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 92A представляет собой:
QIVLTQSPAIMSASLGEEITLICSASSSVSYMHWYQQKSGTSPKLLIYRTSNLASGVPS RFSGSGSGTFYSLTISSVEAEDAADYYCHQWSSWTFGGGTQLEIK
(SEQ ID NO:104), при этом
CDR1 легкой цепи 92A: SASSSVSYMH (SEQ ID NO:150)
CDR2 легкой цепи 92A: RTSNLAS (SEQ ID NO:156)
CDR3 легкой цепи 92A: HQWSSWT (SEQ ID NO:160).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 92A, представляет собой:
CAAATTGTTCTCACCCAGTCTCCAGCAATCATGTCTGCATCTCTAGGGGAGGAGATCAC CCTAATTTGCAGTGCCAGCTCGAGTGTAAGTTACATGCACTGGTACCAGCAGAAGTCAGGCACT TCTCCCAAACTCTTGATTTATCGCACATCCAACCTGGCTTCTGGAGTCCCTTCTCGCTTCAGTG GCAGTGGGTCTGGGACCTTTTATTCTCTTACAATCAGCAGTGTGGAGGCTGAAGATGCTGCCGA TTATTACTGCCATCAGTGGAGTAGTTGGACGTTCGGTGGAGGCACCCAGCTGGAAATCAAA
(SEQ ID NO:128).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 92A представляет собой:
DVQLQESGPGLVKFSQSLSLTCSVTGYSITSGYYWNWIRQFPGNKLEWMGYIRHDGSNN YNPSLKNRISITRDTSKNQFFLKLNSVITEDTATYYCVREIYDGSSGYFDVWGTGTTVTVSS
(SEQ ID NO:116), при этом
CDR1 тяжелой цепи 92A: SGYYWN (SEQ ID NO:168)
CDR2 тяжелой цепи 92A: YIRHDGSNNYNPSLKN (SEQ ID NO:178)
CDR3 тяжелой цепи 92A: EIYDGSSGYFDVWGT (SEQ ID NO:189).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 92A, представляет собой:
GATGTACAGCTTCAGGAGTCAGGACCTGGCCTCGTGAAATTTTCTCAGTCTCTGTCTCT CACCTGCTCTGTCACTGGCTACTCCATCACCAGTGGTTATTACTGGAACTGGATCCGGCAGTTT CCAGGAAACAAACTGGAATGGATGGGCTACATAAGACACGATGGTAGCAATAACTACAACCCGT CTCTCAAAAATCGAATCTCCATCACTCGTGACACATCTAAGAACCAGTTTTTCCTGAAGTTGAA TTCTGTGATTACTGAGGACACAGCCACATATTACTGTGTAAGAGAGATCTATGATGGTTCCTCC GGGTACTTCGATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA
(SEQ ID NO:141).
u. ПОСЛЕДОВАТЕЛЬНОСТИ 93B
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 93В представляет собой:
DIVMTQSPSSLTVTAGEKVTMSCKSSQSLLNSGNQKNYLTWYQQKPGQPPKLLIYWAST RESGVPDRFTGSGSGTDFTLTISNVQPEDLAVYYCQNDYSFPFTFGSGTELEMK
(SEQ ID NO:105), при этом
CDR1 легкой цепи 93В: KSSQSLLNSGNQKNYLT (SEQ ID NO:151)
CDR2 легкой цепи 93В: WASTRES (SEQ ID NO:154)
CDR3 легкой цепи 93В: QNDYSFPFT (SEQ ID NO:161).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 93В, представляет собой:
GACATTGTGATGACACAGTCTCCATCCTCCCTGACTGTGACAGCAGGAGAGAAGGTCAC TATGAGCTGCAAGTCCAGTCAGAGTCTGTTAAACAGTGGAAATCAAAAGAATTACTTGACCTGG TACCAGCAGAAACCAGGACAGCCTCCTAAACTGTTGATCTACTGGGCATCCACTAGGGAATCTG GGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGAACAGATTTCACTCTCACCATTAGCAATGT GCAGCCTGAAGACCTGGCAGTTTATTACTGTCAGAATGATTATAGTTTTCCATTCACGTTCGGC TCGGGGACAGAGTTGGAAATGAAA
(SEQ ID NO:129).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 93В представляет собой:
QVQLKQSGAELVRPGASVKLSCKASGYTFTDYYINWVKQRPGQGLEWIARIYPGNGNTD YNEKFKDKATLTAEKSSTTAYIQLSSLTSEDSAVYFCCLWYFDVWGTGTTVTVSS
(SEQ ID NO:117), при этом
CDR1 тяжелой цепи 93В: DYYIN (SEQ ID NO:169)
CDR2 тяжелой цепи 93В: RIYPGNGNTDYNEKFKD (SEQ ID NO:179)
CDR3 тяжелой цепи 93В: WYFDV (SEQ ID NO:190).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 93В, представляет собой:
CAGGTCCAGCTGAAGCAGTCTGGGGCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCTGGCTACACTTTCACTGACTACTATATAAACTGGGTGAAGCAGAGGCCT GGACAGGGACTTGAGTGGATTGCAAGGATTTATCCTGGAAATGGTAATACTGACTACAATGAGA AGTTCAAGGACAAGGCCACACTGACTGCAGAAAAATCCTCCACCACTGCCTACATACAACTCAG CAGTCTGACATCTGAGGACTCTGCTGTCTATTTCTGTTGCCTCTGGTACTTCGATGTCTGGGGC ACAGGAACCACGGTCACCGTCTCCTCA
(SEQ ID NO:142).
v. ПОСЛЕДОВАТЕЛЬНОСТИ 99B
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 99В представляет собой:
DVVMTQTPLTLSVTIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGIYYCWQGTHFPFTFGSGTKLEIK
(SEQ ID NO:106), при этом
CDR1 легкой цепи 99В: KSSQSLLDSDGKTYLN (SEQ ID NO:30)
CDR2 легкой цепи 99В: LVSKLDS (SEQ ID NO:38)
CDR3 легкой цепи 99В: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 99В, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTC CATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGA GGCTGAGGATTTGGGAATTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAATAAAA
(SEQ ID NO:130).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 99В представляет собой:
QVQLQQSGAELARPGASVKLSCKASGYTFTSDGITWLKQRTGQGLEWIGQIHPRSGNTY YNEKFKGKATLTADKSSSTAYMELRSLTSEDSAVYFCAKTGTGDYWGQGTTLTVSS
(SEQ ID NO:118), при этом
CDR1 тяжелой цепи 99В: SDGIT (SEQ ID NO:166)
CDR2 тяжелой цепи 99В: QIHPRSGNTYYNEKFKG (SEQ ID NO:180)
CDR3 тяжелой цепи 99В: TGTGDY (SEQ ID NO:187).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 99В, представляет собой:
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCT GTCCTGCAAGGCTTCGGGCTACACCTTCACAAGCGACGGTATAACCTGGCTGAAACAGAGAACT GGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACCTACTACAATGAGA AGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGAACTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAAAACTGGGACGGGGGACTACTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:143).
w. ПОСЛЕДОВАТЕЛЬНОСТИ 104B
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 104В представляет собой:
DVVMTQTPLTLSVTIGQPASISCKSSLSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKIIRVEAEDLGIYYCWQGTHFPFTFGSGTKLEVK
(SEQ ID NO:107), при этом
CDR1 легкой цепи 104В: KSSLSLLDSDGKTYLN (SEQ ID NO:152)
CDR2 легкой цепи 104В: LVSKLDS (SEQ ID NO:38)
CDR3 легкой цепи 104В: WQGTHFPFT (SEQ ID NO:45).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 104В, представляет собой:
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTC CATCTCTTGCAAGTCAAGTCTGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTG TTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAG TCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCATCAGAGTGGA GGCTGAGGATTTGGGAATTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCG GGGACAAAGTTGGAAGTAAAA
(SEQ ID NO:131).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 104В представляет собой:
QVQLQQSGPELARPGASVKLSCKASGYTFTSYGISWVKQRTGQGLEWIGQIHPRSGNTY YNENFKGKATLTAAKSSSTAYLELRSLTSEDSAVYFCAREGGPDYWGQGTTLTVSS
(SEQ ID NO:119), при этом
CDR1 тяжелой цепи 104В: SYGIS (SEQ ID NO:164)
CDR2 тяжелой цепи 104В: QIHPRSGNTYYNENFKG (SEQ ID NO:181)
CDR3 тяжелой цепи 104В: EGGPDY (SEQ ID NO:184).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 104В, представляет собой:
CAGGTTCAGCTGCAGCAGTCTGGGCCTGAGCTGGCGAGGCCTGGGGCCTCAGTGAAGCT GTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTATAAGCTGGGTGAAGCAAAGAACT GGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACTTACTACAATGAGA ACTTCAAGGGCAAGGCCACACTGACTGCAGCCAAATCCTCCAGCACAGCGTACCTGGAGCTCCG CAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGAGAGGGGGGTCCCGACTACTGG GGCCAAGGCACCACTCTCACAGTCTCCTCA
(SEQ ID NO:144).
x. ПОСЛЕДОВАТЕЛЬНОСТИ 105A
i. Легкая цепь
Аминокислотная последовательность вариабельного участка легкой цепи 105A представляет собой:
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK
(SEQ ID NO:99), при этом
CDR1 легкой цепи 105A: RSSQSIVHSNGNTYLE (SEQ ID NO:24)
CDR2 легкой цепи 105A: KVSNRFS (SEQ ID NO:32)
CDR3 легкой цепи 105A: FQGSHVPLT (SEQ ID NO:157).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок легкой цепи 105A, представляет собой:
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTC CATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTAC CTACAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGG TCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGA GGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCT GGGACCAAGCTGGAGCTGAAA
(SEQ ID NO:132).
ii. Тяжелая цепь
Аминокислотная последовательность вариабельного участка тяжелой цепи 105A представляет собой:
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDIE YASRFQGKATMTADTSSNTAYLQLTSLTSADTAVYYCTTYVGFGYWGQGTLVTVSA
(SEQ ID NO:111), при этом
CDR1 тяжелой цепи 105A: DDYMH (SEQ ID NO:162)
CDR2 тяжелой цепи 105A: CIDPENGDIEYASRFQG (SEQ ID NO:173)
CDR3 тяжелой цепи 105A: YVGFGY (SEQ ID NO:185).
Последовательность нуклеиновой кислоты, кодирующая вариабельный участок тяжелой цепи 105A, представляет собой:
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTT GTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCT GAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATATTGAATATGCCTCGA GGTTCCAGGGCAAGGCCACTATGACAGCAGACACATCCTCCAACACAGCCTACCTGCAGCTCAC CAGCCTGACATCTGCGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGG GGCCAAGGGACTCTGGTCACTGTCTCTGCA
(SEQ ID NO:145).
2. Анти–SIGLEC–15 антитела и их
антигенсвязывающие фрагменты
Раскрыты молекулы, связывающие SIGLEC–15, в том числе антитела и их антигенсвязывающие фрагменты, которые связываются с одним или несколькими полипептидами или слитыми белками SIGLEC–15, или их фрагменты или варианты. Антитела, раскрываемые в данном документе, в типичном случае представляют собой моноклональные антитела или их антигенсвязывающие фрагменты, которые связываются с эпитопом, присутствующим на полипептиде SIGLEC–15 или его фрагменте или слиянии. В некоторых вариантах осуществления антитело связывается с конформационным эпитопом. В некоторых вариантах осуществления антитело связывается с линейным эпитопом. Линейный эпитоп может состоять из 4, 5, 6, 7, 8, 9, 10, 11 или более непрерывных аминокислот в длину. Эпитоп может содержать один или несколько неаминокислотных элементов, посттрансляционных модификаций или их комбинацию. Примеры посттрансляционных модификаций содержат, но не ограничиваясь ими, гликозилирование, фосфорилирование, ацетилирование, цитруллинирование и убиквитирование. Например, антитела могут связывать эпитоп, который образуется по меньшей мере частично с помощью одной или нескольких углеводных групп.
Антитело или его антигенсвязыающий фрагмент может связываться с эпитопом, который присутствует на эндогенном полипептиде SIGLEC–15 или рекомбинантном полипептиде SIGLEC–15 или его комбинации. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент связывается с внеклеточным доменом SIGLEC–15 или его фрагментом или эпитопом, образованным из него. В некоторых вариантах осуществления антитело или его антигенсвязывающий фрагмент представляет собой функциональное блокирующее антитело, которое ослабляет или предупреждает связывание SIGLEC–15 с одним или несколькими из его лигандов, ослабляет внутриклеточную передачу сигнала, модулированного с помощью SIGLEC–15 или его комбинацию.
Как описано выше, SIGLEC–15 связывается с сиалированными гликопротеинами и предпочтительно распознают структуру Neu5Acα2–6GalNAcα. Экспериментальные Примеры ниже иллюстрируют то, что SIGLEC–15 связывается с белком 4С, содержащим богатые лейцином повторы (LRRC4C) (также называемым лиганд нетрина–G1 и NGL–1), который может быть зависимым или независимым от структуры Neu5Acα2–6GalNAcα. Последовательности нуклеиновых кислот и полипептидные последовательности LRRC4C известны в данной области техники и включают в себя, например,
MLNKMTLHPQQIMIGPRFNRALFDPLLVVLLALQLLVVAGLVRAQTCPSVCSCSNQFSK VICVRKNLREVPDGISTNTRLLNLHENQIQIIKVNSFKHLRHLEILQLSRNHIRTIEIGAFNGL ANLNTLELFDNRLTTIPNGAFVYLSKLKELWLRNNPIESIPSYAFNRIPSLRRLDLGELKRLSY ISEGAFEGLSNLRYLNLAMCNLREIPNLTPLIKLDELDLSGNHLSAIRPGSFQGLMHLQKLWMI QSQIQVIERNAFDNLQSLVEINLAHNNLTLLPHDLFTPLHHLERIHLHHNPWNCNCDILWLSWW IKDMAPSNTACCARCNTPPNLKGRYIGELDQNYFTCYAPVIVEPPADLNVTEGMAAELKCRAST SLTSVSWITPNGTVMTHGAYKVRIAVLSDGTLNFTNVTVQDTGMYTCMVSNSVGNTTASATLNV TAATTTPFSYFSTVTVETMEPSQDEARTTDNNVGPTPVVDWETTNVTTSLTPQSTRSTEKTFTI PVTDINSGIPGIDEVMKTTKIIIGCFVAITLMAAVMLVIFYKMRKQHHRQNHHAPTRTVEIINV DDEITGDTPMESHLPMPAIEHEHLNHYNSYKSPFNHTTTVNTINSIHSSVHEPLLIRMNSKDNV QETQI (SEQ ID NO:192, UniProtKB – Q9HCJ2 LRC4C_HUMAN, и которая явно включена посредством ссылки в полном объеме).
SIGLEC–15 может также связываться с контррецептором (S15–CR) на иммунных клетках, таких как T–клетки.
Таким образом, в некоторых вариантах осуществления функциональная блокирующая молекула (молекула–антагонист), связывающая SIGLEC–15, ослабляет, ингибирует или предупреждает взаимодействие между SIGLEC–15 и его лигандом, таким как гликопротеин, имеющий структуру Neu5Acα2–6GalNAcα, LRRC4C или контрецептор SIGLEC–15.
В некоторых вариантах осуществления связывание антитела или его антигенсвязывающего фрагмента с SIGLEC–15 может повышать иммунную активацию, ослаблять иммунную супрессию или их комбинацию. Например, в конкретных вариантах осуществления антитело или его антигенсвязывающий фрагмент связывается с Ig–подобным V–доменом или Ig–подобным C2–доменом SIGLEC–15. В некоторых вариантах осуществления эпитоп содержит сайт связывания SIGLEC–15 с сиаловой кислотой (например, эпитоп содержит остаток 143 SEQ ID NO:1).
В некоторых вариантах осуществления антитело связывается с частью или всем тем же самым эпитопом, что и моноклональное антитело 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A. Эпитоп может представлять собой линейный эпитоп или конформационный эпитоп. В некоторых вариантах осуществления антитело имеет ту же самую специфичность эпитопа, что и моноклональное антитело 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A. Это может быть достигнуто в результате получения рекомбинантного антитела, которое содержит паратоп моноклонального антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A. В некоторых вариантах осуществления молекула, связывающая SIGLEC–15, содержит некоторые или все CDR легкой цепи, весь вариабельный участок легкой цепи, некоторые или все CDR тяжелой цепи, весь вариабельный участок тяжелой цепи или их комбинацию любого мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A.
Молекулы, связывающие SIGLEC–15, могут содержать CDR, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 99% идентична аминокислотной последовательности CDR упомянутых выше клонов, и которые проявляют иммуноспецифичное связывание с SIGLEC–15.
Например, раскрываемые молекулы могут содержать одну или несколько CDR легкой цепи, имеющих аминокислотные последовательности любой из SEQ ID NO:24–45 и 146–161. Молекула может содержать по меньшей мере одну CDR1 легкой цепи, одну CDR2 легкой цепи и одну CDR3 легкой цепи. Например, молекула может содержать CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:24–31 и 146–152. Молекула может содержать CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:32–38 и 153–156. Молекула может содержать CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:39–45 и 157–161.
В конкретных вариантах осуществления молекула содержит CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи, при этом CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи содержат аминокислотные последовательности:
Раскрываемые молекулы могут содержать одну или несколько CDR тяжелой цепи, имеющих аминокислотные последовательности любой из SEQ ID NO:46–73 и 162–190. Молекула может содержать по меньшей мере одну CDR1 тяжелой цепи, одну CDR2 тяжелой цепи и одну CDR3 тяжелой цепи. Молекула может содержать CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:46–55 и 162–169. Молекула может содержать CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:56–66 и 170–181. Молекула может содержать CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:67–73 и 182–190.
В конкретных вариантах осуществления молекула содержит CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи, при этом CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи содержат аминокислотные последовательности:
Молекулы, связывающие SIGLEC–15, могут содержать аминокислотную последовательность вариабельной тяжелой цепи и/или вариабельной легкой цепи, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или на 100% идентична аминокислотной последовательности вариабельной тяжелой цепи и/или легкой цепи антитела, продуцируемого любым из вышеупомянутых клонов, и которая проявляет иммуноспецифичное связывание с SIGLEC–15 человека.
Например, раскрываемые молекулы, связывающие SIGLEC–15, могут содержать вариабельный участок легкой цепи, имеющий аминокислотную последовательность SEQ ID NO:3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, или ее вариант, содержащий последовательность, по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична SEQ ID NO:3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107, и которая проявляет иммуноспецифичное связывание с SIGLEC–15.
Дополнительно или в альтернативном случае раскрываемые молекулы, связывающие SIGLEC–15, могут содержать вариабельный участок тяжелой цепи, имеющий аминокислотную последовательность SEQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119, или ее вариант, содержащий последовательность, по меньшей мере на 50%, 60%, 70%, 80%, 85%, 90%, 95%, 99% или более идентична EQ ID NO:13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118 или 119, и которая проявляет иммуноспецифичное связывание с SIGLEC–15.
Молекула, связывающая SIGLEC–15, может представлять собой молекулу иммуноглобулина (например, антитело, диатело, слитый белок и др.), которая содержит одну, две или три CDR легкой цепи или одну, две или три CDR тяжелой цепи (например, в некоторых вариантах осуществления три CDR легкой цепи и три CDR тяжелой цепи), при этом CDR легкой цепи содержат:
(1) CDR1 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(2) CDR2 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(3) CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(4) CDR1 легкой цепи и CDR2 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(5) CDR1 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(6) CDR2 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
или
(7) CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
Молекула может представлять собой молекулу иммуноглобулина, которая содержит одну, две или три CDR легкой цепи или одну, две или три CDR тяжелой цепи (например, в некоторых вариантах осуществления три CDR легкой цепи и три CDR тяжелой цепи), при этом CDR тяжелой цепи содержат:
(1) CDR1 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(2) CDR2 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(3) CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(4) CDR1 тяжелой цепи и CDR2 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(5) CDR1 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(6) CDR2 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
или
(7) CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
Молекула может представлять собой молекулу иммуноглобулина, которая содержит одну, две или три CDR легкой цепи или одну, две или три CDR тяжелой цепи (например, в некоторых вариантах осуществления три CDR легкой цепи и три CDR тяжелой цепи), при этом CDR легкой цепи содержат:
(1) CDR1 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(2) CDR2 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(3) CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(4) CDR1 легкой цепи и CDR2 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(5) CDR1 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(6) CDR2 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
или
(7) CDR1 легкой цепи, CDR2 легкой цепи и CDR3 легкой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
и при этом CDR тяжелой цепи содержат:
(1) CDR1 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(2) CDR2 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(3) CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(4) CDR1 тяжелой цепи и CDR2 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(5) CDR1 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
(6) CDR2 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента;
или
(7) CDR1 тяжелой цепи, CDR2 тяжелой цепи и CDR3 тяжелой цепи мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A или его гуманизированного фрагмента.
Например, антитело может иметь одну или несколько CDR мышиного 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A, или его химерного антитела, или гуманизированного варианта, имеющего CDR, соответствующую (соответствующие) CDR мышиного анти–человеческий SIGLEC–15 антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B или 105A.
В одном варианте осуществления предложено гуманизированное моноклональное антитело, имеющее аминокислотную последовательность вариабельной легкой цепи, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или на 100% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 227, 228 и 229, и/или аминокислотную последовательность вариабельной тяжелой цепи, которая по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 99% или на 100% идентична аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 230, 231, 233 и 235.
3. Композиции антител
Раскрываемые молекулы, связывающие SIGLEC–15, могут представлять собой антитела или их антигенсвязывающие фрагменты. Раскрываемые антитела и их антигенсвязывающие фрагменты включают в себя целый иммуноглобулин (т.е. интактное антитело) любого класса, его фрагменты и синтетические белки, содержащие по меньшей мере антигенсвязывающий вариабельный домен антитела. В некоторых вариантах осуществления раскрываемая молекула содержит как легкую, так и по меньшей мере вариабельный домен тяжелой цепи антитела. В других вариантах осуществления такие молекулы могут дополнительно содержать одно или несколько из участков CH1, шарнирных участков, участков CH2, CH3 и CH4 тяжелой цепи (в особенности участки CH1 и шарнирные участки, или участки CH1, шарнирные участки и участки CH2, иди участки CH1, шарнирные участки, участки CH2 и CH3). Антитело может быть выбрано из любого класса иммуноглобулинов, в том числе IgM, IgG, IgD, IgA и IgE и любого изотипа, в том числе IgG1, IgG2, IgG3 и IgG4. В некоторых вариантах осуществления константный домен представляет собой фиксирующий комплемент константный домен, при этом предпочтительно, чтобы антитело проявляло цитотоксическую активность, а класс в типичном случае представлял бы собой IgG1. В других вариантах осуществления, в которых такая цитотоксическая активность не является необходимой, константный домен может представлять сбой класс IgG2 или IgG4. Антитело может содержать последовательности из более одного класса или изотипа, и выбор определенных константных доменов для оптимизации необходимых эффекторных функций находится в пределах компетенции специалиста в данной области техники.
Вариабельные домены отличаются последовательностью между антителами и используются в связывании и специфичности каждого конкретного антитела в отношении своего определенного антигена. Однако вариабельность обычно не распределена равномерно в вариабельных доменах антител. В типичном случае она сосредоточена в трех сегментах, называемых областями, определяющими комплементарность (CDR) или гипервариабельными участками, как в вариабельных доменах легкой цепи, так и тяжелой цепи. Наиболее высококонсервативные участки вариабельных доменов называются каркасом (FR). Каждый из вариабельных доменов нативных тяжелых и легких цепей содержит четыре участка FR, по большей части принимающих конфигурацию бета–листа, соединенных тремя CDR, которые образуют петли, объединяющие структуру бета–листа и в некоторых случаях образующие ее часть. CDR в каждой цепи удерживаются в непосредственной близости друг с другом с помощью участков FR и совместно с CDR из другой цепи участвуют в образовании антигенсвязывающего сайта антител.
Также раскрыты фрагменты антител, которые имеют биологическую активность. Фрагменты, присоединенные или не присоединенные к другим последовательностям, содержат вставки, делеции, замены или другие определенные модификации определенных участков или определенных аминокислотных остатков, при условии, что активность фрагмента по сути не является измененной или нарушенной по сравнению с немодифицированным антителом или фрагментом антитела.
Методики могут быть приспособлены для получения одноцепочечных антител, специфичных к антигенному белку по данному раскрытию. Способы получения одноцепочечных антител хорошо известны специалистам в данной области техники. Одноцепочечное антитело может быть получено с помощью слияния друг с другом вариабельных доменов тяжелой и легкой цепей с использованием короткого пептидного линкера, тем самым восстанавливая антигенсвязывающий сайт на одной молекуле. Вариабельные фрагменты одноцепочечных антител (scFv), в которых C–конец одного вариабельного домена связан с N–концом другого вариабельного домена с помощью пептида или линкера из 15–25 аминокислот были разработаны без существенного нарушения связывания с антигеном или специфичности связывания. Линкер выбирают таким образом, чтобы он обеспечивал связывание тяжелой цепи и легкой цепи друг с другом в их соответствующей конформационной ориентации.
Двухвалентные одноцепочечные вариабельные фрагменты (di–scFv) могут быть разработаны с помощью связывания двух scFv. Это может быть выполнено в результате получения одной пептидной цепи с двумя участками VH и двумя участками VL, образующими тандемные scFv. ScFv также могут быть сконструированы с помощью линкерных пептидов, которые являются слишком короткими, чтобы два вариабельных участка складывались вместе (около пяти аминокислот), обеспечивая димеризацию scFv. Этот тип известен как диатела. Было показано, что диатела имеют константы диссоциации до 40 раз ниже, чем соответствующие scFv, означая, что они имеют намного более высокую аффиность по отношению к своей мишени. Еще более короткие линкеры (одна или две аминокислоты) приводят к образованию тримеров (триател или триотел). Также были получены тетратела. Они проявляют даже более высокую аффинность в отношении к мишеням, чем диатела.
Моноклональное антитело получают по сути из гомогенной популяции антител, т.е. отдельные антитела в популяции являются идентичными, за исключением возможных встречающихся в природе мутаций, которые могут присутствовать в небольшой подгруппе молекул антител. Моноклональные антитела включают в себя «химерные» антитела, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, происходящих из определенного вида или принадлежащих к определенному классу или подклассу антител, тогда как остальная часть цепи (цепей) идентична или гомологична соответствующим последовательностям в антителах, происходящих из другого вида или принадлежащих к другому классу или подклассу антител, а также фрагментам таких антител, до тех пор, пока они проявляют необходимую антагонистическую активность.
a. Химерные и гуманизированные антитела
Также предложены химерные антитела и их антигенсвязывающие фрагменты, включающие в себя одну или несколько из раскрываемых последовательностей и их функциональные варианты.
Способы получения химерных антител известны в данной области техники. См., например, Morrison, 1985, Science 229:1202; Oi et al., 1986, BioTechniques 4:214; Gillies et al., 1989, J. Immunol. Methods 125:191–202, и патенты США №№6311415, 5807715, 4816567 и 4816397. Химерные антитела, содержащие одну или несколько CDR от отличных от человека видов и каркасные участки из молекулы человеческого иммуноглобулина, могут быть получены с помощью ряда методик, известных в данной области техники, в том числе, например, встраивания CDR (EP 239400, международная публикация № WO 91/09967; и патенты США №№5225539, 5530101 и 5585089), венирования и перекладки (EP 592106; EP 519596; Padlan, 1991, Molecular Immunology 28(4/5):489–498; Studnicka et al., 1994, Protein Engineering 7:805; и Roguska et al., 1994, Proc. Natl. Acad. Sci. USA 91:969) и перестановки цепей (патент США №5565332).
Раскрываемые молекулы могут представлять собой человеческие или гуманизированные антитела или их антигенсвязывающие фрагменты. Многие отличные от человеческих антитела (например, таковые, происходящие от мышей, крыс или кроликов) являются естественным образом антигенными у человека и, тем самым, вызывают нежелательные иммунные ответы при введении человеку. Таким образом, использование человеческих или гуманизированных антител в способах способствует снижению вероятности того, что антитело, вводимое человеку, вызовет нежелательный иммунный ответ.
Могут быть использованы трансгенные животные (например, мыши), которые способны при иммунизации продуцировать полный репертуар человеческих антител в отсутствие продуцирования эндогенных иммуноглобулинов. Например, было описано, что гомозиготная делеция гена связывающего участка тяжелой цепи антитела (J(H)) у химерных и мутантных в отношении зародышевой линии мышей приводит к полному ингибированию продуцирования эндогенных антител. Перенос набора генов иммуноглобулинов зародышевой линии человека в таких мутантных в отношении зародышевой линии мышей приведет к продуцированию человеческих антител при антигенной стимуляции.
Необязательно антитела генерируют у других видов и «гуманизируют» для введения у человека. Гуманизированные формы отличных от человеческих (например, мышиных) антител представляют собой химерные иммуноглобулины, иммуноглобулиновые цепи или их фрагменты (такие как Fv, Fab, Fab’, F(ab’)2 или другие антигенсвязывающие последовательности антител), которые содержат минимальную последовательность, происходящую из отличного от человеческого иммуноглобулина. Гуманизированные антитела включают в себя человеческие иммуноглобулины (реципиентное антитело), в которых остатки из области, определяющей комплементарность, (CDR) реципиентного антитела замещены остатками из CDR отличного от человека вида (донорское антитело), такого как мышь, крыса или кролик, имеющего необходимую специфичность, аффинность и способность. В некоторых случаях остатки каркасного участка Fv человеческого иммуноглобулина замещены соответствующими отличными от человеческих остатками. Гуманизированные антитела также могут содержать остатки, которые не встречаются ни в реципиентном антителе, ни в импортированных последовательностях CDR или каркасных последовательностях. Как правило, гуманизированное антитело будет включать по сути все по меньшей мере из одного или в типичном случае из двух вариабельных доменов, в которых все или фактически все из участков CDR соответствуют таковым отличным от человеческого иммуноглобулина и все или фактически все из участков FR происходят из консенсусной последовательности человеческого иммуноглобулина. Гуманизированное антитело в оптимальном случае также будет содержать по меньшей мере часть константного участка иммуноглобулина (Fc), в типичном случае такового человеческого иммуноглобулина.
Способы гуманизации отличных от человеческих антител хорошо известны в данной области техники, см., например, европейские патенты №№EP 239400, EP 592106 и EP 519596; международные публикации WO 91/09967 и WO 93/17105; патенты США №№5225539, 5530101, 5565332, 5585089, 5766886 и 6407213; и Padlan, 1991, Molecular Immunology 28(4/5):489498; Studnicka et al., 1994, Protein Engineering 7(6):805–814; Roguska et al., 1994, PNAS 91:969973; Tan et al., 2002, J. Immunol. 169:1119–1125; Caldas et al., 2000, Protein Eng. 13:353–360; Morea et al., 2000, Methods 20:26779; Baca et al., 1997, J. Biol. Chem. 272:1067810684; Roguska et al., 1996, Protein Eng. 9:895904; Couto et al., 1995, Cancer Res. 55 (23 Supp):5973s5977s; Couto et al., 1995, Cancer Res. 55:171722; Sandhu, 1994, Gene 150:40910; Pedersen et al., 1994, J. Mol. Biol. 235:959–973; Jones et al., 1986, Nature 321:522–525; Reichmann et al., 1988, Nature 332:323–329; и Presta, 1992, Curr. Op. Struct. Biol. 2:593–596).
Как правило, гуманизированное антитело имеет один или несколько аминокислотных остатков, введенных в него из источника, который отличается от человеческого. Эти отличные от человеческих аминокислотные остатки часто называется «импортируемыми» остатками, которые в типичном случае получают из «импортируемого» вариабельного домена. Методики гуманизации антител, как правило, включают использование технологии рекомбинантных ДНК в целях манипуляции с последовательностью ДНК, кодирующей одну или несколько полипептидных цепей молекулы антитела. Гуманизация может быть по сути осуществлена с помощью замены CDR грызунов или последовательностей CDR на соответствующие последовательности человеческого антитела. Соответственно, гуманизированная форма отличного от человеческого антитела (или его фрагмента) представляет собой химерное антитело или фрагмент, в котором по сути менее чем интактный человеческий вариабельный домен был замещен соответствующей последовательностью от отличного от человека вида. При практическом применении гуманизированные антитела в типичном случае представляют собой человеческие антитела, в которых некоторых остатки CDR и возможно некоторые остатки FR замещены остатками из аналогичных сайтов в антителах грызунов.
Выбор человеческих вариабельных доменов, как легких, так и тяжелых цепей, подлежащих использованию при получении гуманизированных антител, может быть очень важным для снижения антигенности. В соответствии с методом «наилучшего приближения» последовательность вариабельного домена антитела грызуна подвергают скринингу против всей библиотеки известных последовательностей человеческих вариабельных доменов. Человеческую последовательность, которая является наиболее близкой к таковой грызуна, затем принимают в качестве человеческого каркасного участка (FR) иммунизированного антитела. В другом способе используется определенный каркасный участок, происходящий из консенсусной последовательности всех человеческих антител определенной подгруппы легких или тяжелых цепей. Одинаковый каркасный участок может быть использован для нескольких отличающихся гуманизированных антител.
Кроме того, важно, чтобы антитела были гуманизированными с сохранением высокой аффинности в отношении антигена и других благоприятных биологических свойств. Для достижения этой цели гуманизированные антитела могут быть получены в результате анализа исходных последовательностей и различных концептуальных гуманизированных продуктов с помощью пространственных моделей исходных и гуманизированных последовательностей. Пространственные модели иммуноглобулинов являются общедоступными и известными специалистам в данной области техники. Доступны компьютерные программы, которые иллюстрируют и демонстрируют возможные пространственные конформационные структуры некоторых кандидатных иммуноглобулиновых последовательностей. Исследование этих изображений способствует анализу вероятной роли остатков в функционировании кандидатной иммуноглобулиновой последовательности, т.е. анализу остатков, которые влияют на способность кандидатного иммуноглобулина связываться со своим антигеном. В этом отношении остатки FR можно выбирать и комбинировать из консенсусной и импортируемой последовательности таким образом, чтобы была достигнута необходимая характеристика антитела, такая как повышенная аффинность в отношении целевого(целевых) антигена(антигенов). Как правило, остатки CDR непосредственно и в наибольшей степени по сути оказывают влияние на связывание с антигеном.
Производное человеческого, гуманизированного или химерного антитела может содержать по сути все по меньшей мере из одного или в типичном случае из двух вариабельных доменов, в которых все или по сути все из участков CDR соответствуют таковым отличным от человеческого иммуноглобулина (т.е. донорского антитела) и все или по сути все из каркасных участков соответствуют таковым консенсусной последовательности человеческого иммуноглобулина. Такие антитела также могут включать по меньшей мере часть константного участка иммуноглобулина (Fc), в типичном случае такового человеческого иммуноглобулина. Константные домены таких антител могут быть выбраны исходя из предполагаемой функции антитела, в частности, эффекторной функции, которая может быть необходимой. В некоторых вариантах осуществления константные домены таких антител представляют собой или могут включать в себя домены IgA, IgD, IgE, IgG или IgM человека. В конкретном варианте осуществления используют константные домены IgG человека, особенно изотипов IgG1 и IgG3, если производное гуманизированного антитела предполагается использовать для терапевтического применения, и необходимы эффекторные функции антител, такие активность в направлении антителозависимой клеточноопосредованной цитотоксичности (ADCC) и комплементзависимой цитотоксичности (CDC). В альтернативных вариантах осуществления используют изотипы IgG2 и IgG4, если антитело предполагается использовать для терапевтических целей и не требуется эффекторная функция антител. Константные Fc–домены, содержащие одну или несколько аминокислотных модификаций, которые изменяют эффекторные функции антител, такие как таковые, раскрыты в опубликованных патентных заявках США №№2005/0037000 и 2005/0064514.
Каркасные участки и области CDR гуманизированного антитела не должны точно соответствовать исходным последовательностям, например, донорская CDR или консенсусный каркасный участок можно мутировать с помощью замены, вставки или делеции по меньшей мере одного остатка таким образом, CDR или каркасный остаток в этом сайте не соответствовал ни консенсусному участку, ни донорскому антителу. В некоторых вариантах осуществления такие мутация не являются значительными. Как правило, по меньшей мере 75% остатков гуманизированного антитела будут соответствовать таковым исходного каркасного участка (FR) и последовательностям CDR, более часто 90% и наиболее часто 95%. Гуманизированные антитела могут быть получены с помощью ряда методик, известных в данной области техники, в том числе, но не ограничиваясь ими, встраивания CDR (Европейский патент №239400; международная публикация №WO 91/09967; и патенты США №№5225539, 5530101 и 5585089), венирования и перекладки (Европейские патенты №№592106 и 519596; Padlan, 1991, Molecular Immunology 28(4/5):489–498; Studnicka et al., 1994, Protein Engineering 7(6):805–814, и Roguska et al., 1994, Proc. Natl. Acad. Sci. 91:969–973), перестановки цепей (патент США №5565332), а также методик, раскрываемых, например, в патентах США №№6407213, 5766886, 5585089, международной публикации №WO 9317105, Tan et al., 2002, J. Immunol. 169:1119–25, Caldas et al., 2000, Protein Eng. 13:353–60, Morea et al., 2000, Methods 20:267–79, Baca et al., 1997, J. Biol. Chem. 272:10678–84, Roguska et al., 1996, Protein Eng. 9:895–904, Couto et al., 1995, Cancer Res. 55 (23 Supp):5973s5977s, Couto et al., 1995, Cancer Res. 55:171722, Sandhu, 1994, Gene 150:40910, Pedersen et al., 1994, J. Mol. Biol. 235:95973, Jones et al., 1986, Nature 321:522–525, Riechmann et al., 1988, Nature 332:323, и Presta, 1992, Curr. Op. Struct. Biol. 2:593–596.
Часто каркасные остатки в каркасных участках будут замещаться соответствующим остатком из CDR донорского антитела для изменения, предпочтительно, повышения связывания с антигеном. Эти каркасные замены идентифицируют с помощью способов, хорошо известных в данной области техники, например, с помощью моделирования взаимодействий CDR и каркасных остатков в целях идентификации каркасных остатков, важных для связывания с антигеном, и сравнения последовательностей в целях идентификации необычных каркасных участков в определенных положениях. (См., например, Queen et al., патент США №5585089; публикации США №№2004/0049014 и 2003/0229208; патенты США №№6350861; 6180370; 5693762; 5693761; 5585089 и 5530101, и Riechmann et al., 1988, Nature 332:323).
Человеческие, химерные или гуманизированные производные раскрываемых мышиных анти–человеческий SIGLEC–15 антител могут быть использованы для способов in vivo у человека. Мышиные антитела или антитела других видов могут быть предпочтительно использованы для многих применений (например, анализов детекции in vitro или in situ, экстренного применения in vivo и т.д.). Такое человеческое или гуманизированное антитело может содержать аминокслотные замены, делеции или добавления в одном или нескольких отличных от человеческих CDR. Производное гуманизированного антитела может иметь по сути такое же связывание, более сильное связывание или более слабое связывание по сравнению с не являющимся производным гуманизированным антителом. В конкретных вариантах осуществления один, два, три, четыре или пять аминокислотных остатков CDR были замещены, удалены или добавлены (т.е. мутированы). Полностью человеческие антитела особенно предпочтительны для терапевтического лечения субъектов–людей.
Такие антитела человека могут быть получены с помощью ряда способов, известных в данной области техники, в том числе способов фагового дисплея с использованием библиотек антител, происходящих из человеческих иммуноглобулиновых последовательностей (см. патенты США №№4444887 и 4716111; и международные публикации №№WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735 и WO 91/10741). Такие антитела человека могут быть получены с помощью трансгенных мышей, которые неспособны экспрессировать функциональные эндогенные иммуноглобулины, однако которые могут экспрессировать гены человеческих иммуноглобулинов.
Например, генные комплексы тяжелой и легкой цепи человеческих иммуноглобулинов могут быть введены случайным образом или с помощью гомологичной рекомбинации в эмбриональные стволовые клетки мыши. Альтернативно человеческая вариабельная область, константная область и область разнообразия могут быть введены в мышиные эмбриональные стволовые клетки, помимо генов человеческой тяжелой и легкой цепи. Генам мышиных иммуноглобулинов тяжелой и легкой цепи можно придать нефункциональность в отдельности или одновременно с введением локусов человеческих иммуноглобулинов с помощью гомологичной рекомбинации. В частности, гомозиготная делеция участка JH предупреждает продуцирование эндогенных антител. Модифицированные эмбриональные стволовые клетки экспандируют и вводят с помощью микроинъекции в бластоцисты с получением химерных мышей. Затем химерных мышей скрещивают с получением гомозиготного потомства, которое экспрессирует человеческие антитела. Трансгенных мышей иммунизируют с помощью стандартных методик выбранным антигеном, например, всем или частью полипептида. Моноклональные антитела, направленные против антигена, могут быть получены от иммунизированных трансгенных мышей с помощью стандартной методики получения гибридом (см., например, патент США №5916771). Трансгены человеческих иммуноглобулинов, находящиеся в трансгенных мышах, реаранжировываются во время дифференцировки B–клеток и впоследствии подвергаются переключению класса и соматической мутации. Таким образом, с помощью такой методики можно получить терапевтически пригодные антитела IgG, IgA, IgM и IgE. Описание этой методики получения антител человека см. в Lonberg and Huszar (1995, Int. Rev. Immunol. 13:65–93, которая включена в данный документ посредством ссылки в полном объеме). Подробное описание этой методики получения человеческих антител и человеческих моноклональных антител и протоколы получения таких антител см., например, в международных публикациях №№WO 98/24893, WO 96/34096 и WO 96/33735; и патентах США №№5413923, 5625126, 5633425, 5569825, 5661016, 5545806, 5814318 и 5939598, которые включены в данный документ посредством ссылки в полном объеме. Помимо этого, производством человеческих антител, направленных против выбранного антигена, могут заниматься компании, такие как Abgenix, Inc. (Фримонт, Калифорния) и Medarex (Принстон, Нью–Джерси), используя методики, подобной той, которая описана выше.
Последовательности ДНК, кодирующие человеческие акцепторные каркасные последовательности включают в себя, но не ограничиваясь ими, сегменты FR из сегмента VH1–18 и JH6 зародышевой линии человека VH и сегмента VK–A26 и JK4 из зародышевой линии человека VL. В конкретном варианте осуществления одна или несколько из CDR вводят в каркасные области с помощью стандартных методик рекомбинантной ДНК. Каркасные участки могут встречаться в природе или представлять собой консенсусные каркасные участки, и, предпочтительно человеческие каркасные участки (см., например, Chothia et al., 1998, “Structural Determinants In The Sequences Of Immunoglobulin Variable Domain,” J. Mol. Biol. 278: 457–479 в отношении перечня человеческих каркасных участков).
i. Гуманизированное 5G12
В одном варианте осуществления предложено гуманизированное антитело 5G12 или его антигенсвязывающий фрагмент.
b. Одноцепочечные антитела
Молекулы, связывающие SIGLEC–15, могут представлять собой одноцепочечные антитела. Способы получения одноцепочечных антител хорошо известны специалистам в данной области техники. Одноцепочечное антитело получают с помощью слияния друг с другом вариабельных доменов тяжелой и легкой цепей с использованием короткого пептидного линкера, тем самым восстанавливая антигенсвязывающий сайт на одной молекуле. Вариабельные фрагменты одноцепочечных антител (scFv), в которых C–конец одного вариабельного домена связан с N–концом другого вариабельного домена с помощью пептида или линкера из 15–25 аминокислот были разработаны без существенного нарушения связывания с антигеном или специфичности связывания. Линкер выбирают таким образом, чтобы он обеспечивал связывание тяжелой цепи и легкой цепи друг с другом в их соответствующей конформационной ориентации. У этих Fv отсутствуют константные участки (Fc), присутствующие в тяжелых и легких цепях нативного антитела.
c. Моновалентные антитела
Способы in vitro также подходят для получения моновалентных антител. Расщепление антител с получением их фрагментов, в частности, фрагментов Fab, может быть осуществлено с помощью стандартных методик, известных в данной области техники. Например, расщепление может быть осуществлено с помощью папаина. Папаиновое расщепление антител в типичном случае приводит к образованию двух идентичных антигенсвязывающих фрагментов, называемых фрагментами Fab, при этом каждый имеет один антигенсвязывающий сайт и остаточный Fc–фрагмент. Пепсиновая обработка приводит к образованию фрагмента, называемого F(ab’)2–фрагментом, который имеет два антигенсвязывающих сайта и по–прежнему способен перекрестно сшивать антиген.
Фрагменты Fab, образуемые при расщеплении антитела, также содержат константные домены легкой цепи и первый константный домен тяжелой цепи. Фрагменты Fab’ отличаются от фрагментов Fab добавлением нескольких остатков на карбоксиконце домена тяжелой цепи, содержащих один или несколько цистеинов из шарнирного участка антитела. Фрагмент F(ab’)2 представляет собой бивалентный фрагмент, содержащий два фрагмента Fab’, связанных с помощью дисульфидного мостика в шарнирном участке. Fab’–SH в данном документе представляет собой обозначение Fab’, в котором цистеиновый (цистеиновые) остаток(остатки) константных доменов имеет(имеют) свободную тиольную группу. Фрагменты антител изначально были получены в виде пар фрагментов Fab’, которые имеют между собой шарнирые цистеины. Также известны другие химические связи фрагментов антител.
d. Конъюгаты или слияния фрагментов антител
Нацеливающая функция антитела может быть использована терапевтически в результате связывания антитела или его антигенсвязывающего фрагмента с терапевтическим агентом. Такое связывание антитела или фрагмента (например, по меньшей мере части константного участка (Fc) иммуноглобулина) с терапевтическим агентом может быть достигнуто посредством получения иммуноконъюгата или посредством получения слитого белка, содержащего антитело или его антигенсвязывающий фрагмент и терапевтический агент.
Такое связывание антитела или фрагмента с терапевтическим агентом может быть достигнуто посредством получения иммуноконъюгата или посредством получения слитого белка, или в результате связывания антитела или фрагмента с нуклеиновой кислотой, такой как миРНК, содержащего антитело или фрагмент антитела и терапевтический агент.
В некоторых вариантах осуществления антитело модифицируют в целях изменения его времени полужизни. В некоторых вариантах осуществления желательно увеличить время полужизни антитела таким образом, чтобы оно присутствовало в кровотоке или в области лечения в течение более длительных периодов времени. Например, может быть желательным поддерживать титры антитела в кровотоке или в области, подлежащей лечению, в течение более длительных периодов времени. Могут быть сконструированы антитела с вариантами Fc, которые увеличивают время полужизни, например, с помощью технологии увеличения времени полужизни антител Xtend™ (Xencor, Монровия, Калифорния). В других вариантах осуществления время полужизни анти–ДНК антитела снижают в целях уменьшения потенциальных побочных эффектов. Раскрываемые конъюгаты могут быть использованы для модификации определенного биологического ответа. Лекарственный фрагмент не следует понимать как ограниченный классическими химическими терапевтическими агентами. Например, лекарственный фрагмент может представлять собой белок или полипептид, имеющий необходимую биологическую активность. Такие белки могут включать в себя, например, токсин, такой как абрин, рицин A, экзотоксин синегнойной палочки или дифтерийный токсин.
e. Моно– и мультиспецифичные антитела
В некоторых вариантах осуществления раскрываемые антитела являются моноспецифичными, связываясь только с SIGLEC–15. Также предложены биспецифичные производные таких антител, триспецифичные производные таких антител или производные антител более высокой мультиспецифичности, которые проявляют специфичность в отношении различных мишеней иммунной системы помимо их специфичности в отношении SIGLEC–15 человека. Например, такие антитела могут связываться с SIGLEC–15 человека и с антигеном, который является важным нацеливания антитела на конкретный тип клеток или ткань (например, на антиген, ассоциированный с раковым антигеном опухоли, подлежащей лечению). В другом варианте осуществления такое мультиспецифичное антитело связывается с молекулами (рецепторами или лигандами), участвующими в альтернативных иммуномодуляторных путях, таких как B7–H1, PD–1, CTLA4, TIM3, TIM4, OX40, CD40, GITR, 4–1–BB, LIGHT или LAG3, в целях повышения иммуномодуляторных эффектов и комбинирования нескольких механизмов действия, таких как блокирование лигандов, активация иммунных клеток и прямое нацеливание на опухоль, в одной молекуле.
f. Производные
Также раскрыто получение и использование «производных» любой из молекул, связывающих SIGLEC–15. Производная молекула, например, антитело или фрагмент антитела, может быть модифицирована с помощью химических модификаций с использованием методик, известных специалистам в данной области техники, в том числе, но не ограничиваясь ими, определенного химического расщепления, ацетилирования, составления, метаболического синтеза туникамицина и др. Термин производное включает в себя неаминокислотные модификации, например, аминокислоты, которые могут быть гликозилированными (например, имеют измененное содержание маннозы, 2–N–ацетилглюкозамина, галактозы, фукозы, глюкозы, сиаловой кислоты, 5–N–ацетилнейраминовой кислоты, 5–гликольнейраминовой кислоты и др.), ацетилированными, пегилированными, фосфорилированными, амидированными, дериватизированными с помощью известных защитных/блокирующих групп, протеолитического расщепления, связанными с клеточным лигандом или другим белком и т.д. В некоторых вариантах осуществления измененные углеводные модификации модулируют одно или несколько из следующего: растворимость антитела, ослабление субклеточного транспорта и секреции антитела, активацию сборки антитела, конформационную целостность и антителоопосредованную эффекторную функцию.
В конкретном варианте осуществления измененные углеводные модификации усиливают антителоопосредованную эффекторную функцию по отношению к антителу, не имеющему углеводной модификации. Углеводные модификации, которые приводят к измененной антителоопосредованной эффекторной функции, хорошо известны в данной области техники (например, см., Shields, R.L. et al. (2002) “Lack Of Fucose On Human IgG N–Linked Oligosaccharide Improves Binding To Human Fcgamma RIII And Antibody–Dependent Cellular Toxicity,” J. Biol. Chem. 277(30): 26733–26740; Davies J. et al. (2001) “Expression Of GnTIII In A Recombinant Anti–CD20 CHO Production Cell Line: Expression Of Antibodies With Altered Glycoforms Leads To An Increase In ADCC Through Higher Affinity For FC Gamma RIII,” Biotechnology & Bioengineering 74(4): 288–294). Способы изменения содержания углеводов известны специалистам в данной области техники, см., например, Wallick, S.C. et al. (1988) “Glycosylation Of A VH Residue Of A Monoclonal Antibody Against Alpha (1–6) Dextran Increases Its Affinity For Antigen,” J. Exp. Med. 168(3): 1099–1109; Tao, M.H. et al. (1989) “Studies Of Aglycosylated Chimeric Mouse–Human IgG. Role Of Carbohydrate In The Structure And Effector Functions Mediated By The Human IgG Constant Region,” J. Immunol. 143(8): 2595–2601; Routledge, E.G. et al. (1995) “The Effect Of Aglycosylation On The Immunogenicity Of A Humanized Therapeutic CD3 Monoclonal Antibody,” Transplantation 60(8):847–53; Elliott, S. et al. (2003) “Enhancement Of Therapeutic Protein In Vivo Activities Through Glycoengineering,” Nature Biotechnol. 21:414–21; Shields, R.L. et al. (2002) “Lack Of Fucose On Human IgG N–Linked Oligosaccharide Improves Binding To Human Fcgamma RIII And Antibody–Dependent Cellular Toxicity,” J. Biol. Chem. 277(30): 26733–26740).
Раскрываемые антитела могут быть модифицированы с помощью рекомбинантных средств в целях повышения эффективности антитела в опосредовании необходимой функции. Таким образом, антитела можно модифицировать с помощью замен с использованием рекомбинантных средств. В типичном случае замены будут представлять собой консервативные замены. Например, по меньшей мере одну аминокислоту в константном участке антитела можно заменить другим остатком. См., например, патент США №5624821, патент США №6194551, заявку №WO 9958572; и Angal, et al., Mol. Immunol. 30:105–08 (1993). Модификация аминокислот включает в себя делеции, добавления, замены аминокислот. В некоторых случаях такие изменения выполняют в целях ослабления нежелательных активностей, например, комплементзависимой цитотоксичности. Часто антитела метят с помощью связывания, как ковалентно, так и нековалентно, вещества, которое обеспечивает детектируемый сигнал. Большое разнообразие меток и методик конъюгирования известны и широко описаны как в научной, так и в патентной литературе. Эти антитела можно подвергать скринингу в отношении связывания с полипептидами SIGLEC–15 или их фрагментами или слияниями. См., например, Antibody Engineering: A Practical Approach (Oxford University Press, 1996).
В некоторых вариантах осуществления производное антитела будет иметь аналогичную или идентичную функцию с исходным антителом. В другом варианте осуществления производное антитела будет проявлять измененную активность по отношению к исходному антителу. Например, производное антитела (или его фрагмента) может связываться с его эпитопом более прочно или быть более устойчивым к протеолизу по сравнению с исходным антителом.
Замены, добавления или делеции в дериватизированных антителах могут происходить в Fc–участке антитела и могут, таким образом, способствовать модификации аффинности связывания антитела с одним или несколькими FcγR. Способы модификации антител с помощью модифицированного связывания с одним или несколькими FcγR В известны данной области техники, см., например, публикации PCT №№WO 04/029207, WO 04/029092, WO 04/028564, WO 99/58572, WO 99/51642, WO 98/23289, WO 89/07142, WO 88/07089 и патенты США №№5843597 и 5642821.
В некоторых вариантах осуществления предложены антитела, Fc–участок которых был удален (например, Fab или F(ab)2 и др.) или модифицирован таким образом, чтобы молекула проявляла сниженную аффинность связывания с Fc–рецептором (FcR) или не связывалась с ним, или проявляла повышенные активности в направлении антителозависимой клеточноопосредованной цитотоксичности (ADCC) и комплементзависимой цитотоксичности (CDC). В некоторых вариантах осуществления антитела имеют измененную аффинность в отношении активации FcγR, например, FcγRIIIA. Такие модификации могут также иметь измененную Fc–опосредованную эффекторную функцию. Модификации, которые влияют на Fc–опосредованную эффекторную функцию, хорошо известны в данной области техники (см. патент США №6194551 и WO 00/42072). В одном конкретном варианте осуществления модификация Fc–участка приводит к образованию антитела с измененной антителоопосредованной эффекторной функцией, измененным связыванием с другими Fc–рецепторами (например, активирующими Fc–рецепторами), измененной активностью в направлении антителозависимой клеточноопосредованной цитотоксичности (ADCC), измененной активностью связывания с C1q, измененной активностью в направлении комплементзависимой цитотоксичности (CDC), фагоцитарной активности или их комбинацией.
Дериватизированные антитела могут быть использованы для изменения времени полужизни (например, времени полужизни в сыворотке) исходных антител у млекопитающего, такого как, человека. Например, такое изменение может приводить к времени полужизни более 15 дней, более 20 дней, более 25 дней, более 30 дней, более 35 дней, более 40 дней, более 45 дней, более 2 месяцев, более 3 месяцев, более 4 месяцев или более 5 месяцев. Увеличенное время полужизни гуманизированных антител или их фрагментов у млекопитающего, такого как, человека, приводит к более высокому титру указанных антител или фрагментов антител в сыворотке у млекопитающего, и, таким образом, снижает частоту введения указанных антител или фрагментов антител и/или снижает концентрацию указанных антител или фрагментов антител, которые подлежат введению. Антитела или их фрагменты, имеющие увеличенное время полужизни in vivo, можно генерировать с помощью методик, известных специалистам в данной области техники. Например, антитела или их фрагменты с увеличенным временем полужизни in vivo, можно генерировать с помощью модифицирования (например, замены, удаления или добавления) аминокислотных остатков, идентифицированных в качестве участвующих во взаимодействии между Fc–доменом и FcRn–рецептором. В целях увеличения биологического времени полужизни могут быть сконструированы гуманизированные антитела (см., например, патент США №6277375). Например, гуманизированные антитела могут быть сконструированы в домене Fc–шарнира в целях получения увеличенного времени полужизни in vivo или в сыворотке.
Антитела или их фрагменты с увеличенным временем полужизни in vivo можно генерировать с помощью присоединения к указанным антителам или фрагментам антител полимерных молекул, таких как полиэтиленгликоль (ПЭГ) с высоким молекулярным весом. ПЭГ может быть присоединен к указанным антителам или фрагментам антител с использованием или без использования мультифункционального линкера с помощью сайт–специфичной конъюгации ПЭГ с N– или C–концом указанных антител или фрагментов антител или с помощью эпсилон–аминогрупп, присутствующих в остатках лизина. Будет использована дериватизация линейных или разветвленных полимеров, которая приводит к минимальной потере биологической активности. В целях обеспечения соответствующей конъюгации молекул ПЭГ с антителами степень конъюгации будет тщательно контролироваться с помощью SDS–PAGE и масс–спектрометрии. Не вступивший в реакцию ПЭГ может быть отделен от конъюгатов антитело–ПЭГ с помощью, например, эксклюзионной или ион–обменной хроматографии.
В целях получения композиций, которые могут быть введены в кровеносную систему млекопитающих по сути без иммуногенного ответа антитела также могут быть модифицированы с помощью способов и связывающих агентов, описанных Davis et al. (см. патент США №4179337).
Каркасные остатки гуманизированных антител могут быть модифицированными. Остатки в каркасных участках будут замещены соответствующим остатком из CDR донорского антитела в целях изменения, предпочтительно, например, повышения связывания с антигеном. Эти каркасные замены могут быть идентифицированы с помощью способов, хорошо известных в данной области техники, например, с помощью моделирования взаимодействий CDR и каркасных остатков в целях идентификации каркасных остатков, важных для связывания с антигеном, и сравнения последовательностей в целях идентификации необычных каркасных участков в определенных положениях. (см., например, патент США №5585089; и Riechmann, L. et al. (1988) “Reshaping Human Antibodies For Therapy,” Nature 332:323–327).Раскрываемые молекулы, связывающие SIGLEC–15, могут быть рекомбинантно слиты или химически конъюгированы (в том числе как с помощью ковалентных, так и нековалентных конъюгаций) с гетерологичной молекулой (т.е., неродственной молекулой). Слияние необязательно должно быть прямым, а может происходить с использованием линкерных последовательностей.
В некоторых вариантах осуществления такие гетерологичные молекулы представляют собой полипептиды, имеющие по меньшей мере 10, по меньшей мере 20, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90 или по меньшей мере 100 аминокислот. Такие гетерологичные молекулы в альтернативном случае могут представлять собой ферменты, гормоны, рецепторы клеточной поверхности, лекарственные фрагменты, такие как: специфичные в отношении макрофагов нацеливающие агенты (такие как внутриклеточная карбоксилэстераза, hCE1 (Needham, L.A. et al. (2011) “Drug Targeting To Monocytes And Macrophages Using Esterase–Sensitive Chemical Motif,” J. Pharmacol. Exp. Ther. DOI:10.1124/jpet.111.183640), хитин и хитозан (Muzzarelli, R.A. (2010) “Chitins And Chitosans As Immunoadjuvants And Non–Allergenic Drug Carriers,” Mar Drugs 8(2):292–312), галактозилированный липопротеин низкой плотности (Wu, F. et al. (009) “Galactosylated LDL Nanoparticles: A Novel Targeting Delivery System To Deliver Antigen To Macrophages And Enhance Antigen Specific T Cell Responses,” Molec. Pharm. 6(5):1506–1517), N–formyl–Met–Leu–Phe (fMLF), специфичный в отношении макрофагов хемоаттрактант (Wan, L. et al. (2008) “Optimizing Size And Copy Number For PEG–Fmlf (N–Formyl–Methionyl–Leucyl–Phenylalanine) Nanocarrier Uptake By Macrophages,” Bioconjug. Chem. 19(1):28–38), малеилированный или маннозилированный белок, такой как малеилированный альбумин (Anatelli, F. et al. (2006) “Macrophage–Targeted Photosensitizer Conjugate Delivered By Intratumoral Injection,” Mol Pharm. 3(6):654–664; Bansal, P. et al. (1999) “MHC Class I–Restricted Presentation Of Maleylated Protein Binding To Scavenger Receptors,” J. Immunol. 162(8):4430–4437); см. также Mukhopadhyay, A. et al. (2003) “Intracellular Delivery Of Drugs To Macrophages,” Adv. Biochem. Eng. Biotechnol. 84:183–209), токсины (такие как абрин, рицин A, экзотоксин синегнойной палочки (т.е., PE–40), дифтерийный токсин, рицин, гелонин или противовирусный белок лаконоса), белки (такие как фактор некроза опухоли, интерферон (например, α–интерферон, β–интерферон), фактор роста нервов, тромбоцитарный фактор роста, тканевой активатор плазминогена или апоптический агент (например, фактор некроза опухоли α, фактор некроза опухоли β)), модификаторы биологического ответа (такие как, например, лимфокин (например, интерлейкин–1 («IL–1»), интерлейкин–2 («IL–2»), интерлейкин–6 («IL–6»)), гранулоцитарно–макрофагальный колониестимулирующий фактор («GM–CSF»), гранулоцитарный колониестимулирующий фактор («G–CSF») или макрофагальный колониестимулирующий фактор («M–CSF»)), или факторы роста (например, гормон роста («GH»))), цитотоксины (например, цитостатический или цитоцидальный агент, такой как паклитаксел, цитохалазин B, грамицидин D, этидия бромид, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1–дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин и их аналоги или гомологи), антиметаболиты (например, метотрексат, 6–меркаптопурин, 6–тиогуанин, цитарабин, 5–фторурацил, дакарбазин), алкилирующие агенты (например, мехлорэтамин, тиотепа, хлорамбуцил, мелфалан, BiCNU® (кармустин; BSNU) и ломустин (CCNU), циклотосфамид, бусульфан, дибромманнитол, стрепрозоцин, митомицин C и цис–диаминодихлорплатина (II) (DDP), цисплатин), антрациклины (например, даунорубицин (ранее называвшийся дауномицин) и доксорубицин), антибиотики (например, дактиномицин (ранее называвшийся актиномицин), блеомицин, митрамицин и антрамицин (AMC)) или антимитотические средства (например, винкристин и винбластин).
В другом варианте осуществления молекулы могут конъюгируют со вторым антителом с образованием гетероконъюгата антитела, описанного Segal в патенте США №4676980. Такие гетероконъюгатные антитела могут дополнительно связываться с гаптенами (такими как флуоресцеин и др.) или клеточными маркерами (например, 4–1–BB, B7–H1, PD–1, CD4, CD8, CD14, CD25, CD27, CD40, CD68, CD163, CTLA4, GITR, LAG–3, OX40, TIM3, TIM4, TLR2, LIGHT и др.) или цитокинами (например, IL–4, IL–7, IL–10, IL–12, IL–15, IL–17, TGF–бета, IFNg, Flt3, BLys) или хемокинами (например, CCL21) и т.д.
Fc–участок слитого белка может отличаться изотипом или подклассом, может быть химерным или гибридным, и/или может быть модифицированным, например, в целях усиления эффекторных функций, контроля времени полужизни, тканевой доступности, улучшения биофизических характеристик, таких как стабильность, и усовершенствования эффективности производства (и меньших затрат). В данной области техники известно много модификаций, пригодных при разработке раскрываемых слитых белков, и способов их получения, см., например, Mueller, J.P. et al. (1997) “Humanized Porcine VCAM–Specific Monoclonal Antibodies With Chimeric IgG2/G4 Constant Regions Block Human Leukocyte Binding To Porcine Endothelial Cells,” Mol. Immun. 34(6):441–452, Swann, P.G. (2008) “Considerations For The Development Of Therapeutic Monoclonal Antibodies,” Curr. Opin. Immun. 20:493–499 (2008), и Presta, L.G. (2008) “Molecular Engineering And Design Of Therapeutic Antibodies,” Curr. Opin. Immun. 20:460–470. В некоторых вариантах осуществления Fc–участок представляет собой нативный Fc–участок IgG1, IgG2 или IgG4. В некоторых вариантах осуществления Fc–участок является гибридным, например, химерным, состоящим из константных Fc–участков IgG2/IgG4. Модификации Fc–участка включают, но не ограничиваясь ими, IgG4, модифицированный в целях предупреждения связывания с Fc–гамма рецепторами и комплементом, IgG1, модифицированный в целях повышения связывания с одним или несколькими Fc–гамма рецепторами, IgG1, модифицированный в целях сведения к минимуму эффекторной функции (аминокислотные изменения), IgG1 с измененным гликаном/без гликана (обычно с помощью изменения хозяина экспрессии), и IgG1 с измененным зависимым от pH связыванием с FcRn. Fc–участок может содержать весь шарнирный участок или менее чем весь шарнирный участок.
Терапевтический эффект у пациентов, получавших ритуксимаб (химерное мышь/человек моноклональное антитело IgG1 против CD20) для лечения неходжкинской лимфомы или макроглобулинемии Вальденстрема коррелировал с экспрессией у индивидов аллельных вариантов Fcγ–рецепторов с отличающимися внутренними аффинностями в отношении Fc–домена IgG1 человека. В частности, пациенты с аллелями высокой аффинности активирующего Fc–рецептора CD16A с низкой аффинностью (FcγRIIIA) показали более высокие уровни ответа, а в случае неходжкинской лимфомы – повышенную выживаемость без прогрессирования. Таким образом, Fc–домен раскрываемых антител или их фрагментов может содержать одну или несколько аминокислотных вставок, делеций или замен, которые ослабляют связывание с ингибирующим Fc–рецептором CD32B с низкой аффинностью (FcγRIIB) и сохраняют уровни связывания дикого типа или усиливают связывание с активирующим Fc–рецептором CD16A с низкой аффинностью (FcγRIIIA).
Другой вариант осуществления включает гибриды IgG2–4 и мутанты IgG4, которые имеют ослабленное связывание с FcγR, что увеличивает их время полужизни. Иллюстративные гибриды IG2–4 и мутанты IgG4 описаны в Angal, S. et al. (1993) “A Single Amino Acid Substitution Abolishes The Heterogeneity Of Chimeric Mouse/Human (Igg4) Antibody,” Molec. Immunol. 30(1):105–108; Mueller, J.P. et al. (1997) “Humanized Porcine VCAM–Specific Monoclonal Antibodies With Chimeric IgG2/G4 Constant Regions Block Human Leukocyte Binding To Porcine Endothelial Cells,” Mol. Immun. 34(6):441–452; и патенте США №6982323. В некоторых вариантах осуществления домен IgG1 и/или IgG2 является модифицированным, например, Angal, S. et al. (1993) описывают варианты IgG1 и IgG2, в которых серин 241 замещен пролином.
В некоторых вариантах осуществления Fc–домен таких молекул содержит аминокислотные вставки, делеции и замены, которые усиливают связывание с CD16A. В данной области техники известно большое количество замен в Fc–домене IgG1 человека, которые повышают связывание с CD16A и ослабляют связывание с CD32B и которые описаны в Stavenhagen, J.B. et al. (2007) “Fc Optimization Of Therapeutic Antibodies Enhances Their Ability To Kill Tumor Cells In Vitro And Controls Tumor Expansion In Vivo Via Low–Affinity Activating Fcgamma Receptors,” Cancer Res. 57(18):8882–8890. Иллюстративные варианты Fc–доменов IgG1 человека со ослабленным связыванием с CD32B и/или повышенным связыванием с CD16A, содержат замены F243L, R929P, Y300L, V305I или P296L. Эти аминокислотные замены могут присутствовать в Fc–домене IgG1 человека в любой комбинации. В одном варианте осуществления вариант Fc–домена IgG1 человека содержит замену F243L, R929P и Y300L. В другом варианте осуществления вариант Fc–домена IgG1 человека содержит замену F243L, R929P, Y300L, V305I и P296L. В другом варианте осуществления вариант Fc–домена IgG1 человека содержит замену N297Q, поскольку эта мутация устраняет связывание FcR.
Методики конъюгирования таких терапевтических фрагментов с антителами хорошо известны, см., например, Arnon et al., “Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy”, in Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), 1985, pp. 243–56, Alan R. Liss, Inc.); Hellstrom et al., “Antibodies For Drug Delivery”, in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), 1987, pp. 623–53, Marcel Dekker, Inc. ); Thorpe, “Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review”, in Monoclonal Antibodies ‘84: Biological And Clinical Applications, Pinchera et al. (eds.), 1985, pp. 475–506); “Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy”, in Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), 1985, pp. 303–16, Academic Press; и Thorpe et al. (1982) “The Preparation And Cytotoxic Properties Of Antibody–Toxin Conjugates,” Immunol. Rev. 62:119–158.
Раскрываемые молекулы могут быть слиты с маркерными последовательностями, такими как пептид, в целях облегчения очистки. В некоторых вариантах осуществления маркерная аминокислотная последовательность представляет собой гексагистидиновый пептид, гемагглютинин с тэгом «HA», который соответствует эпитопу, происходящему из гемагглютининового белка вируса гриппа (Wilson, I.A. et al. (1984) “The Structure Of An Antigenic Determinant In A Protein,” Cell, 37:767–778), и тэгом «flag» (Knappik, A. et al. (1994) “An Improved Affinity Tag Based On The FLAG Peptide For The Detection And Purification Of Recombinant Antibody Fragments,” Biotechniques 17(4):754–761).
Раскрываемые молекулы, связывающие SIGLEC–15, могут быть конъюгированы с или терапевтическим агентом или другой молекулой, для которой предпочтительным является увеличение времени полужизни в сыворотке. Антитела могут быть использованы в диагностических целях (in vivo, in situ или in vitro), например, для контроля развития или прогрессирования заболевания, нарушения или инфекции в виде части процедуры клинического исследования, например, для определения эффективности определенного режима лечения или выбора пациентов, которые более вероятно ответят на определенную терапию (таких как таковые, экспрессирующие высокие уровни SIGLEC–15).
Детекция может быть облегчена в результате связывания молекулы, такой как антитело или его антигенсвязывающий фрагмент, с детектируемым веществом. Примеры детектируемых веществ включают в себя различные ферменты, простетические группы, флуоресцентные вещества, люминесцентные вещества, биолюминесцентные вещества, радиоактивные вещества, позитрон–эмиссионные металлы и нерадиоактивные ионы парамагнитных металлов. Детектируемое вещество может быть связано или как непосредственно с антителом прямо, так и опосредовано, через посредника (такого как, например, линкер, известный в данной области техники) с помощью методик, известных в данной области техники. См., например, патент США №4741900 в отношении ионов металлов, которые могут быть конъюгированы с антителами для применения в качестве диагностических средств. Такая диагностика и детекция могут осуществляться с помощью соединения антитела с детектируемыми веществами, в том числе, но не ограничиваясь ими, различные ферменты, в том числе, но не ограничиваясь ими, пероксидазу хрена, щелочную фосфатазу, бета–галактозидазу или ацетилхолинэстеразу; комплексы с простетической группой, такие как, но не ограничиваясь ими, стрептавидин/биотин и авидин/биотин; флуоресцентные вещества, такие как, но не ограничиваясь ими, умбеллиферон, флуоресцеин, флуоресцеина изотиоцинат, родамин, дихлортриазиниламина флуоресцеин, дансилхлорид или фикоэритрин; люминесцентные вещества, такие как, но не ограничиваясь им, люминол; биолюминесцентные вещества, такие как, но не ограничиваясь ими, люцифераза, люциферин и экворин; радиоактивные вещества, такие как, но не ограничиваясь ими, висмут (213Bi), углерод (14C), хром (51Cr), кобальт (57Co), фтор (18F), гадолиний (153Gd, 159Gd), галлий (68Ga, 67Ga), германий (68Ge), гольмий (166Ho), индий (115In, 113In, 112In, 111In), йод (131I, 125I, 123I, 121I), лантан (140La), лютеций (177Lu), марганец (54Mn), молибден (99Mo), палладий (103Pd), фосфор (32P), празеодим (142Pr), прометий (149Pm), рений (186Re, 188Re), родий (105Rh), рутений (97Ru), самарий (153Sm), скандий (47Sc), селен (75Se), стронций (85Sr), сера (35S), технеций (99Tc), таллий (201Ti), олово (113Sn, 117Sn), тритий (3H), ксенон (133Xe), иттербий (169Yb, 175Yb), иттрий (90Y), цинк (65Zn); позитрон–эмиссионные металлы с использованием различных видов позитрон–эмиссионной томографии, а также нерадиоактивные ионы парамагнитных металлов.
Раскрываемые молекулы могут быть прикреплены к твердым подложкам, которые особенно пригодны для иммунологических анализов или очистки целевого антигена или других молекул, которые способны связываться с целевым антигеном, который был иммобилизирован на подложке с помощью связывания с антителом или антиген–связывающим фрагментом. Такие твердые подложки включают в себя, но не ограничиваясь ими, стекло, целлюлозу, полиакриламид, нейлон, полистирен, поливинилхлорид или полипропилен.
Также раскрыты молекулы нуклеиновых кислот (ДНК или РНК), которые кодируют любые такие антитела, слитые белки или фрагменты, а также векторные молекулы (такие как плазмиды), которые способны переносить или реплицировать такие молекулы нуклеиновых кислот. Нуклеиновые кислоты могут быть одноцепочечными, двуцепочечными, могут содержать одноцепочечные и двуцепочечные участки.
3. Способы получения
Молекулы, связывающие SIGLEC–15, могут быть получены с помощью любого способа, известного в данной области техники, пригодного для получения полипептидов, например, синтеза in vitro, образования рекомбинантной ДНК и т.п. Гуманизированные антитела в типичном случае получают с помощью технологии рекомбинантной ДНК. Антитела могут быть получены с помощью технологии экспрессии рекомбинантных иммуноглобулинов. Рекомбинантное получение иммуноглобулиновых молекул, в том числе гуманизированных антител, описано в патенте США №4816397 (Boss et al.), патентах США №№6331415 и 4816567 (оба принадлежат Cabilly et al.), патента Великобритании GB 2188638 (Winter et al.) и патента Великобритании GB 2209757. Методики рекомбинантной экспрессии иммуноглобулинов, в том числе гуманизированных иммуноглобулинов, также можно найти в Goeddel et al., Gene Expression Technology Methods in Enzymology Vol. 185 Academic Press (1991), и Borreback, Antibody Engineering, W. H. Freeman (1992). Дополнительную информацию в отношении генерирования, разработки и экспрессии рекомбинантных антител можно найти в Mayforth, Designing Antibodies, Academic Press, San Diego (1993).
Иллюстративный способ получения рекомбинантных химерных антител может включать следующее: a) конструирование с помощью стандартных методов молекулярной биологии вектора экспрессии, который кодирует и экспрессирует тяжелую цепь антитела, в которой CDR и вариабельный участок анти–SIGLEC–15 антитела сливают с Fc–участком, происходящим из человеческого иммуноглобулина, приводя тем самым к получению вектора для экспрессии тяжелой цепи химерного антитела; b) конструирование с помощью стандартных методов молекулярной биологии вектора экспрессии, который кодирует и экспрессирует легкую цепь антитела мышиного анти–человеческий SIGLEC–15 моноклонального антитела, приводя тем самым к получению вектора для экспрессии легкой цепи химерного антитела; c) перенос векторов экспрессии в клетку–хозяина с помощью стандартных методов молекулярной биологии в целях получения трансфицированной клетки–хозяина для экспрессии химерных антител; и d) культивирование трансфицированной клетки с помощью стандартных методик культивирования клеток в целях получения химерных антител.
Иллюстративный способ получения рекомбинантных гуманизированных антител может включать следующее: a) конструирование с помощью стандартных методов молекулярной биологии вектора экспрессии, который кодирует и экспрессирует тяжелую цепь анти–человеческий SIGLEC–15 антитела, в котором CDR и минимальная часть каркаса вариабельного участка, которые требуются для сохранения специфичности связывания донорского антитела, происходят из гуманизированных вариантов анти–человеческий SIGLEC–15 антитела (антитела), а оставшаяся часть антитела происходит из человеческого иммуноглобулина, приводя тем самым к получению вектора для экспрессии тяжелой цепи гуманизированного антитела; b) конструирование с помощью стандартных методов молекулярной биологии вектора экспрессии, который кодирует и экспрессирует легкую цепь антитела, в котором CDR и минимальная часть каркаса вариабельного участка, которые требуются для сохранения специфичности связывания донорского антитела, происходят из отличного от человеческого иммуноглобулина, такого как раскрываемые мышиные анти–человеческий SIGLEC–15 антитела, а оставшаяся часть антитела происходит из человеческого иммуноглобулина, приводя тем самым к получению вектора для экспрессии легкой цепи гуманизированного антитела; c) перенос векторов экспрессии в клетку–хозяина с помощью стандартных методов молекулярной биологии в целях получения трансфицированной клетки–хозяина для экспрессии гуманизированных антител; и d) культивирование трансфицированной клетки с помощью стандартных методик культивирования клеток для получения гуманизированных антител.
В отношении каждого иллюстративного способа клетки–хозяева могут быть котрансфицированы такими векторами экспрессии, которые могут содержать различные селектируемые маркеры, однако, за исключением кодирующих последовательностей тяжелой и легкой цепи, могут быть предпочтительно идентичными. Эта процедура обеспечивает равную экспрессию полипептидов тяжелой и легкой цепи. В альтернативном случае может быть использован один вектор, который кодирует полипептиды тяжелой и легкой цепи. Кодирующие последовательности тяжелой и легкой цепи могут включать кДНК или геномную ДНК или и то и другое. Клетка–хозяин, используемая для экспрессии рекомбинантного антитела, может быть как бактериальной клеткой, такой как Escherichia coli, так и эукариотической клеткой (например, клеткой яичника китайского хомяка (CHO) или клеткой HEK–293). Выбор вектора экспрессии зависит от выбора клетки–хозяина, и может быть выбран таким образом, чтобы иметь необходимые характеристики экспрессии и регуляции в выбранной клетке–хозяине. Другие клеточные линии, которые могут быть использованы, включают, но не ограничиваясь ими, CHO–K1, NSO и PER.C6 (Crucell, Лейден, Нидерланды).
Любые из раскрываемых антител могут быть использованы для создания антиидиотипических антител с помощью методик, хорошо известных специалистам в данной области техники (см., например, Greenspan, N.S. et al. (1989) “Idiotypes: Structure And Immunogenicity,” FASEB J. 7:437–444; и Nisinoff, A. (1991) “Idiotypes: Concepts And Applications,” J. Immunol. 147(8):2429–2438).
C. Молекулы, связывающие лиганд SIGLEC–15
Также предложены молекулы, которые связываются с лигандами SIGLEC–15, такими как белки SIGLEC–15, слитые белки SIGLEC–15 и их фрагменты и варианты. Молекула, связывающая лиганд SIGLEC–15, может связываться с лигандом SIGLEC–15, такими как сиалированный гликопротеин, LRRC4C, контррецептор SIGLEC–15 и др. В некоторых вариантах осуществления молекула, связывающая лиганд SIGLEC–15, может индуцировать передачу сигнала с участием лиганда SIGLEC–15. В некоторых вариантах осуществления молекула, связывающая лиганд SIGLEC–15, блокирует или иным образом ослабляет взаимодействие между SIGLEC–15 и его лигандом, не индуцируя передачу сигнала с участием SIGLEC–15 или его лиганда. Молекулы, связывающие лиганд SIGLEC–15, могут быть использованы для модулирования активности SIGLEC–15, как описано более подробно ниже и проиллюстрировано в Примерах, и могут быть использованы в терапевтических целях для лечения субъекта, нуждающегося в этом.
1. Полипептиды SIGLEC–15
В некоторых вариантах осуществления молекула, связывающая лиганд SIGLEC–15, представляет собой SIGLEC–15 или его фрагмент или вариант. Например, в некоторых вариантах осуществления молекулы, связывающие лиганд SIGLEC–15, включают в себя полипептиды, по меньшей мере на 50, 60, 70, 80, 85, 90, 95, 96, 97, 98, 99 или 100% идентичны SEQ ID NO:1 или 2, или его фрагменту, такому как внеклеточный домен или его субдомен, такой как домен IgV, домен IgC или их комбинация. В некоторых вариантах осуществления полипептид SIGLEC–15 является растворенным или иным образом внеклеточным. Например, в некоторых вариантах осуществления SIGLEC–15 не имеет одного или нескольких из трансмембранного домена, цитоплазматического домена или лидерной последовательности.
2. Слитые белки SIGLEC–15
В некоторых вариантах осуществления молекула, связывающая лиганд SIGLEC–15, представляет собой слитый белок SIGLEC–15. Предложены слитые белки, содержащие полипептиды SIGLEC–15, связанные с другими полипептидами, в целях образования слитых белков. Слитые полипептиды SIGLEC–15 могут иметь первого партнера слияния, представляющего собой все или часть из белка SIGLEC–15, слитого (i) непосредственно со вторым полипептидом, или (ii) необязательно слитого с линкерной пептидной последовательностью, которая слита со вторым полипептидом. Слитые белки необязательно содержат домен, который функционирует таким образом, чтобы димеризовать два или более слитых белков. В некоторых вариантах осуществления слитый белок не подлежит димеризации или мультимеризации или не димеризируется или не мультимеризируется. Пептидный/полипептидный линкерный домен может представлять собой как отдельный домен, так в альтернативном случае содержаться в одном из других доменов (полипептида SIGLEC–15 или второго полипепида) слитого белка. Аналогичным образом, домен, который функционирует таким образом, что димеризовать или мультимеризовать слитые домены, может представлять собой как отдельный домен, так в альтернативном случае содержаться в одном из других доменов (полипептида SIGLEC–15, второго полипептида или пептидного/полипептидного линкерного домена) слитого белка. В некоторых вариантах осуществления домен димеризации/мультимеризации и пептидный/полипептидный линкерный домен представляют собой одно и то же.
Слитые белки, раскрываемые в данном документе, представлены формулой I:
N–R1–R2–R3–C,
где «N» представляет собой N–конец слитого белка, «C» представляет собой C–конец слитого белка, «R1» представляет собой полипептид SIGLEC–15, «R2» представляет собой необязательный пептидный/полипептидный линкерный домен и «R3» представляет собой второй полипептид. В альтернативном случае R3 может представлять собой полипептид SIGLEC–15 и R1 может представлять собой второй полипептид.
Слитые белки могут быть димеризованными или мультимеризованными. Димеризация или мультимеризация может происходить между или в пределах одного или нескольких слитых белков с участием доменов димеризации или мультимеризации. В альтернативном случае димертация или мультимеризация слистых белков может происходить с помощью химического сшивания. Димеры или мультимеры, которые образуются, могут быть гомодимерными/гомомультимерными или гетеродимерными/гетеромультимерными. Как описано ранее, в некоторых вариантах осуществления слитый белок не подлежит димеризации или мультимеризации или не димеризируется или не мультимеризируется.
В некоторых вариантах осуществления второй полипептид содержит один или несколько доменов константного участка тяжелой цепи иммуноглобулина, например, аминокислотную последовательность, соответствующую шарнирным участкам, участкам CH2 и/или CH3 цепи Cγ1 человеческого иммуноглобулина, шарнирным участкам, участкам CH2 и/или CH3 цепи Cγ2a мышиного иммуноглобулина, участкам CH2 и/или CH3 Cγ1 человеческого иммуноглобулина и т.д.
Fc–участок слитого белка может отличаться изотипом или подклассом, может быть химерным или гибридным, и/или может быть модифицированным, например, в целях усиления эффекторных функций, контроля времени полужизни, тканевой доступности, улучшения биофизических характеристик, таких как стабильность, и усовершенствования эффективности производства (и меньших затрат). В данной области техники известно много модификаций, пригодных при разработке раскрываемых слитых белков, и способов их получения, см., например, Mueller, et al., Mol. Immun., 34(6):441–452 (1997), Swann, et al., Cur. Opin. Immun., 20:493–499 (2008), и Presta, Cur. Opin. Immun. 20:460–470 (2008). В некоторых вариантах осуществления Fc–участок представляет собой нативный Fc–участок IgG1, IgG2 или IgG4. В некоторых вариантах осуществления Fc–участок является гибридным, например, химерным, состоящим из константных Fc–участков IgG2/IgG4. Модификации Fc–участка включают, но не ограничиваясь ими, IgG4, модифицированный в целях предупреждения связывания с Fc–гамма рецепторами и комплементом, IgG1, модифицированный в целях повышения связывания с одним или несколькими Fc–гамма рецепторами, IgG1, модифицированный в целях сведения к минимуму эффекторной функции (аминокислотные изменения), IgG1 с измененным гликаном/без гликана (обычно с помощью изменения хозяина экспрессии), и IgG1 с измененным зависимым от pH связыванием с FcRn. Fc–участок может содержать весь шарнирный участок или менее чем весь шарнирный участок.
Терапевтический эффект у пациентов, получавших ритуксимаб (химерное мышь/человек моноклональное антитело IgG1 против CD20) для лечения неходжкинской лимфомы или макроглобулинемии Вальденстрема коррелировал с экспрессией у индивидов аллельных вариантов Fcγ–рецепторов с отличающимися внутренними аффинностями в отношении Fc–домена IgG1 человека. В частности, пациенты с аллелями высокой аффинности активирующего Fc–рецептора CD16A с низкой аффинностью (FcγRIIIA) показали более высокие уровни ответа, а в случае неходжкинской лимфомы – повышенную выживаемость без прогрессирования. В другом варианте осуществления Fc–домен может содержать одну или несколько аминокислотных вставок, делеций или замен, которые ослабляют связывание с ингибирующим Fc–рецептором CD32B с низкой аффинностью (FcγRIIB) и сохраняют уровни связывания дикого типа или усиливают связывание с активирующим Fc–рецептором CD16A с низкой аффинностью (FcγRIIIA).
Другой вариант осуществления включает гибриды IgG2–4 и мутанты IgG4, которые имеют ослабленное связывание с FcR, что увеличивает их время полужизни. Иллюстративные гибриды IG2–4 и мутанты IgG4 описаны в Angal, S. et al., Molecular Immunology, 30(1):105–108 (1993); Mueller, J. et al., Molecular Immonology, 34(6): 441–452 (1997); и патент США №6982323 Wang et al. В некоторых вариантах осуществления домен IgG1 и/или IgG2 удаляют, например, Angal S, et al. описывают IgG1 и IgG2, имеющие серин 241, замещенный пролином.
В некоторых вариантах осуществления Fc–домен содержит аминокислотные вставки, делеции и замены, которые усиливают связывание с CD16A. В данной области техники известно большое количество замен в Fc–домене IgG1 человека, которые повышают связывание с CD16A и ослабляют связывание с CD32B и которые описаны в Stavenhagen, et al., Cancer Res., 57(18):8882–90 (2007). Иллюстративные варианты Fc–доменов IgG1 человека с ослабленным связыванием с CD32B и/или повышенным связыванием с CD16A, содержат замены F243L, R929P, Y300L, V305I или P296L. Эти аминокислотные замены могут присутствовать в Fc–домене IgG1 человека в любой комбинации. В одном варианте осуществления вариант Fc–домена IgG1 человека содержит замену F243L, R929P и Y300L. В другом варианте осуществления вариант Fc–домена IgG1 человека содержит замену F243L, R929P, Y300L, V305I и P296L. В другом варианте осуществления вариант Fc–домена IgG1 человека содержит замену N297Q, поскольку эта мутация устраняет связывание FcR.
Раскрываемые слитые белки необязательно содержат пептидный или полипептидный линкерный домен, который отделяет полипептид SIGLEC–15 от второго полипептида. В некоторых вариантах осуществления линкерный домен содержит шарнирный участок иммуноглобулина. В предпочтительном варианте осуществления шарнирный участок происходит из человеческого иммуноглобулина. Подходящие человеческие иммуноглобулины, из которых может происходить шарнир, включают в себя IgG, IgD и IgA. В предпочтительном варианте осуществления шарнирный участок происходит из IgG человека. Аминокислотные последовательности иммуноглобулиновых шарнирных участков и других доменов хорошо известны в данной области техники.
Иллюстративный слитый белок представляет собой слитый белок SIGLEC15 ECD– Fc IgG1 (L234F/L235E/P331S).
MEWSWVFLFFLSVTTGVHS FVRTKIDTTENLLNTEVHSSPAQRWSMQVPPEVSAEAGDA AVLPCTFTHPHRHYDGPLTAIWRAGEPYAGPQVFRCAAARGSELCQTALSLHGRFRLLGNPRRN DLSLRVERLALADDRRYFCRVEFAGDVHDRYESRHGVRLHVTAAPRIVNISVLPSPAHAFRALC TAEGEPPPALAWSGPALGNSLAAVRSPREGHGHLVTAELPALTHDGRYTCTAANSLGRSEASVY LFRFHGASG DKTHTCPPCPAPEFEGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKF NWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPASIEKTISKA KGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGS FFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG (SEQ ID NO:193).
Мышиная лидерная последовательность изображена с помощью подчеркивания. Внеклеточный домен SIGLEC–15 (ECD) изображен с помощью курсивного шрифта. Шарнирный участок изображен с помощью двойного подчеркивания. Оставшаяся последовательность происходит из Fc IgG1. Мутации L234F/L235E/P331S в Fc–домене IgG1 изображены с помощью жирного шрифта и пунктирного подчеркивания.
В некоторых вариантах осуществления лидерная последовательность отделена или иным образом устранена из слитого белка. Например, слитый белок может иметь последовательность:
FVRTKIDTTENLLNTEVHSSPAQRWSMQVPPEVSAEAGDAAVLPCTFTHPHRHYDGPLT AIWRAGEPYAGPQVFRCAAARGSELCQTALSLHGRFRLLGNPRRNDLSLRVERLALADDRRYFC RVEFAGDVHDRYESRHGVRLHVTAAPRIVNISVLPSPAHAFRALCTAEGEPPPALAWSGPALGN SLAAVRSPREGHGHLVTAELPALTHDGRYTCTAANSLGRSEASVYLFRFHGASG DKTHTCPPCP APEFEGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREE QYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPASIEKTISKAKGQPREPQVYTLPPSRDEL TKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNV FSCSVMHEALHNHYTQKSLSLSPG (SEQ ID NO:194).
В некоторых вариантах осуществления слитый белок по меньшей мере на 50, 60, 70, 80, 85, 90, 95, 96, 97, 98, 99 или 100% идентичен SEQ ID NO:193 или 194.
В некоторых вариантах осуществления лидерная последовательность, линкер (например, шарнирный участок), второй партнер слияния (например, Fc–домен IgG1) или их комбинация замещены другой (другими) последовательностью(последовательностями) (например, альтернативной лидерной последовательностью, шарниром, Fc–доменом и т.д.). Подходящие заместители хорошо известны в данной области техники. См., например, патент США №9005616, который явно включены посредством ссылки в полном объеме.
3. Нуклеиновые кислоты, кодирующие SIGLEC–15, и клетки, содержащие SIGLEC–15
Также предложены векторы, кодирующие полипептиды SIGLEC–15, их фрагменты и слитые белки. Нуклеиновые кислоты, такие как таковые, описанные выше, могут быть включены в векторы для экспрессии в клетках. Таким образом, также предложены клетки, содержащие и экспрессирующие полипептиды SIGLEC–15, их фрагменты и слияния. Используемый в данном документе «вектор» представляет собой репликон, такой как плазмиду, фаг, вирус или космиду, в который может быть включен другой сегмент ДНК, таким образом, чтобы приводить к репликации включенного фрагмента. Векторы могут представлять собой векторы экспрессии. «Вектор экспрессии» представляет собой вектор, который включает одну или несколько последовательностей контроля экспрессии, а «последовательность контроля экспрессии» представляет собой последовательность ДНК, которая контролирует и регулирует транскрипцию и/или трансляцию другой последовательности ДНК.
Нуклеиновые кислоты в векторах могут быть функционально связаны с одной или несколькими последовательностями контроля экспрессии. Используемый в данном документе «функционально связанный» означает включенный в генетическую конструкцию таким образом, что последовательности контроля экспрессии эффективно контролируют экспрессию кодирующей последовательности, представляющей интерес. Примеры последовательностей контроля экспрессии включают в себя промоторы, энхансеры и участки терминации транскрипции. Промотор представляет собой последовательность контроля экспрессии, состоящую из участка молекулы ДНК, в типичном случае в пределах 100 нуклеотидов выше точки, в которой начинается транскрипция (как правило, возле сайта инициации в случае РНК–полимерезы II). Для контроля кодирующей последовательности промотором необходимо расположить сайт инициации трансляции рамки считывания полипептида между первым и около пятидесятым нуклеотидами ниже промотора. Энхансеры обеспечивают специфичность экспрессии с точки зрения времени, положения и уровня. В отличие от промоторов, энхансеры могут функционировать при расположении на различных расстояниях от сайта транскрипции. Энхансер может быть расположен ниже сайта инициации транскрипции. Кодирующая последовательность является «функционально связанной» и находится «под контролем» последовательностей контроля экспрессии в клетке, если РНК–полимераза может транскрибировать кодирующую последовательность в мРНК, которая затем может быть транслирована в белок, кодируемый кодирующей последовательностью.
Подходящие векторы экспрессии включают в себя, но не ограничиваясь ими, плазмиды и вирусные векторы, происходящие, например, из бактериофага, бакуловируса, вируса табачной мозаики, вируса герпеса, цитомегаловируса, ретровирусов, вирусов осповакцины, аденовирусов и аденоассоциированных вирусов. Многочисленные векторы и системы экспрессии коммерчески доступны от таких корпораций, как Novagen (Мадисон, Висконсин), Clontech (Пало–Альто, Калифорния), Stratagene (Ла–Хойя, Калифорния) и Invitrogen Life Technologies (Карлсбад, Калифорния).
Вектор экспрессии может содержать тэговые последовательность. Тэговые последовательности в типичном случае экспрессируются в виде слияния с кодируемым полипептидом. Такие тэги могут быть включены в любом месте в пределах полипептида, в том числе как на карбоксильном, так и на аминоконце. Примеры пригодных тэгов включают в себя, но не ограничиваясь ими, зеленый флуоресцентный белок (GFP), глутатион–S–трансферазу (GST), полигистидин, c–myc, гемагглютинин, тэг Flag™ (Kodak, Нью–Гейвен, Коннектикут), белок, связывающий мальтозу E, и белок А. В некоторых вариантах осуществления молекула нуклеиновой кислоты, кодирующая слитый полипептид SIGLEC–15, присутствует в векторе, содержащем нуклеиновые кислоты, которые кодируют один или несколько доменов константного участка тяжелой цепи Ig, например, аминокислотную последовательность, соответствующую шарнирным участкам, участкам CH2 и CH3 цепи Cγ1 человеческого иммуноглобулина.
Векторы, содержащие нуклеиновые кислоты, подлежащие экспрессии, могут быть перенесены в клетки–хозяева. Термин «клетка–хозяин» предусматривает включение прокариотических и эукариотических клеток, в которые рекомбинантный вектор экспрессии может быть введен. Используемые в данном документе «трансформированный» и «трансфицированный» включают в себя введение молекулы нуклеиновой кислоты (например, вектора) в клетку с помощью одной из ряда методик. Несмотря на то, что отсутствует ограничение определенной методикой, ряд этих методик хорошо известен в данной области техники. Прокариотические клетки могут быть трансформированы нуклеиновыми кислотами, например, с помощью электропорации или трансформации, опосредованной хлоридом кальция. Нуклеиновые кислоты могут быть трансфицированы в клетки млекопитающих с помощью методик, в том числе, например, копреципитации фосфатом кальция, трансфекции, опосредованной DEAE–декстраном, липофекции, электропорации или микроинъекции. Клетки–хозяева (например, прокариотическая клетка или эукариотическая клетка, такая как клетка CHO) может быть использована, например, для продуцирования слитых полипептидов SIGLEC–15, описанных в данном документе.
Описанные векторы могут быть использованы для экспрессии SIGLEC–15 в клетках. Иллюстративный вектор включает, но не ограничиваясь им, аденовирусный вектор. Один подход включает в себя перенос нуклеиновых кислот в первичные клетки в культуре после аутологичной трансплантации ex vivo трансформированных клеток, как системно, так и в определенный орган или ткань. Способы ex vivo включают, например, этапы сбора клеток от субъекта, культивирования клеток, трансдукции их вектором экспрессии и поддержания клеток в условиях, подходящих для экспрессии кодируемых полипептидов. Эти способы хорошо известны в области молекулярной биологии. Этап трансдукции может быть осуществлен с помощью стандартных средств, используемых для генной терапии ex vivo, в том числе, например, копреципитации фосфатом кальция, липофекции, электропорации, вирусной инфекции и биолистического переноса генов. В альтернативном случае могут быть использованы липосомы или полимерные микрочастицы. Клетки, которые были успешно трансдуцированы, затем можно селектировать, например, в отношении экспрессии кодирующей последовательности или гена лекарственной устойчивости. Затем клетки могут быть летальным образом облучены (при необходимости) и инъецированы или иплантированы в субъекта. В одном варианте осуществления векторы экспрессии, содержащие нуклеиновые кислоты, кодирующие слитые белки, трансфицируют в клетки, которые вводят субъекту, нуждающемуся в этом.
Терапию нуклеиновыми кислотами in vivo можно осуществить с помощью прямого переноса функционально активной ДНК в соматическую ткань или орган млекопитающих in vivo. Например, нуклеиновые кислоты, кодирующие полипептиды, раскрываемые в данном документе, можно вводить непосредственно в лимфоидные ткани или опухоли. В альтернативном случае специфичное в отношении лимфоидной ткани нацеливание может быть достигнуто с помощью специфичных в отношении лимфоидной ткани регуляторных элементов транскрипции (TRE), таких как специфичный в отношении B–лимфоцитов, Т–лимфоцитов или дендритных клеток TRE. Специфичные в отношении лимфоидной ткани TRE известны в данной области техники.
Нуклеиновые кислоты также могут быть введены in vivo с помощью вирусных средств. Молекулы нуклеиновых кислот, кодирующие слитые белки, могут быть упакованы в ретровирусные векторы с помощью пакующих клеточных линий, которые продуцируют дефектные по репликации вирусы, как известно в данной области техники. Могут быть использованы другие вирусные векторы, в том числе рекомбинантные аденовирусы и вирус осповакцины, которые могут быть выполнены нереплицирующими. Помимо оголенной ДНК или РНК или вирусных векторов, в качестве векторов могут быть использованы сконструированные бактерии.
Нуклеиновые кислоты также могут быть доставлены с помощью других носителей, в том числе липосом, полимерных микро– и наночастиц и поликатионов, таких как асиалогликопротеин/полилизин.
Кроме опосредованного вирусами и носителями переноса генов in vivo, физические средства, хорошо известные в данной области техники, могут быть использованы для прямого переноса ДНК, в том числе введение плазидной ДНК и перенос генов, опосредованный бомбардировкой частицами.
D. Фармацевтические композиции
Предложены фармацевтические композиции, содержащие раскрываемые молекулы, связывающие SIGLEC–15. Фармацевтические композиции, содержащие молекулу, связывающую SIGLEC–15, могут быть предназначены для введения с помощью парентеральных (внутримышечной, интраперитонеальной, внутривенной (в/в) или подкожной инъекции), трансдермальных (как пассивно, так и с помощью ионофореза или электропорации) или трансмукозальных (назальных, вагинальных, ректальных или сублингвальных) путей введения или с помощью биоразлагаемых вкладов и могут быть разработаны в лекарственных формах, подходящих для каждого пути введения.
В некоторых подходах in vivo композиции, раскрываемые в данном документе, вводят субъекту в терапевтически эффективном количестве. Используемый в данном документе термин «эффективное количество» или «терапевтически эффективное количество» означает дозу, достаточную для лечения, ингибирования или нормализации одного или нескольких симптомов нарушения, подлежащего лечению, или для обеспечения иным образом необходимого фармакологического и/или физиологического эффекта. Точная доза будет варьировать в зависимости от ряда факторов, таких как зависящие от субъекта переменные (например, возраст, состояние иммунной системы и т.д.), заболевание и лечение, подлежащее проведению.
В случае раскрываемых молекул, связывающих SIGLEC–15, по мере проведения дополнительных исследований, будет появляться информация в отношении уровней доз для лечения различных состояний у различных пациентов, и специалист в данной области техники, учитывая терапевтический контекст, возраст и общее состояние здоровья реципиента, будет способен определить соответствующую дозу. Выбранная дозировка зависит от необходимого терапевтического эффекта, от пути введения и от длительности необходимого лечения. Как правило, в случае внутривенной инъекции или инфузии, доза может быть более низкой.
Доза, вводимая пациенту, в типичном случае составляет от 0,01 мг/кг до 100 мг/кг веса тела пациента. Доза, вводимая пациенту, может составлять, например, от 0,01 мг/кг до 20 мг/кг, от 0,01 мг/кг до 10 мг/кг, от 0,01 мг/кг до 5 мг/кг, от 0,01 до 2 мг/кг, от 0,01 до 1 мг/кг, от 0,01 мг/кг до 0,75 мг/кг, от 0,01 мг/кг до 0,5 мг/кг, от 0,01 мг/кг до 0,25 мг/кг, от 0,01 до 0,15 мг/кг, от 0,01 до 0,10 мг/кг, от 0,01 до 0,05 мг/кг или от 0,01 до 0,025 мг/кг веса тела пациента. Иллюстративные конкретные дозы включают, но не ограничиваясь ими, 0,2 мг/кг, 0,3 мг/кг, 1 мг/кг, 3 мг/кг, 6 мг/кг или 10 мг/кг. Доза, как минимум 0,01 мг/кг, считается, подходящей для того, чтобы оказать заметные фармакодинамические эффекты. Предполагается, что уровни доз 0,10–1 мг/кг являются наиболее подходящими. Также предполагается, что более высокие дозы (например, 1–30 мг/кг) были бы активными.
Как правило, человеческие антитела имеют более длительное время полужизни в организме человека, чем антитела от других видов, благодаря иммунному ответу на чужеродные полипептиды. Таким образом, более низкие дозы человеческих антител и менее частое введение часто является возможным. Кроме того, доза и частота введения антител по данному изобретению или их фрагментов могут быть снижены с помощью повышенного захвата и проникновения в ткани антител в результате модификаций, таких как, например, липидация.
В определенных вариантах осуществления молекулу, связывающую SIGLEC–15, вводят локально, например, с помощью инъекции непосредственно в участок, подлежащий лечению. В типичном случае инъекция вызывает повышенную локальную концентрацию композиции на основе молекулы, связывающий SIGLEC–15, которая является более высокой, чем таковая, которая может быть достигнута с помощью системного введения. Композиции на основе молекулы, связывающий SIGLEC–15, могут быть комбинированы с матрицей, как описано ниже, для содействия в создании повышенной локальной концентрации полипептидных композиций в результате снижения пассивной диффузии полипептидов вне участка, подлежащего лечению.
1. Составы для парентерального введения
В некоторых вариантах осуществления композиции, раскрываемые в данном документе, вводят в водном растворе с помощью парентеральной инъекции или инфузии. Состав также может находиться в форме суспензии или эмульсии. В целом предложены фармацевтические композиции, содержащие эффективные количества молекулы, связывающей SIGLEC–15, и необязательно содержащие фармацевтически приемлемые разбавители, консерванты, солюбилизаторы, эмульгаторы, адъюванты и/или носители. Такие композиции необязательно содержат одно или несколько из следующего: разбавители, стерильную воду, забуференный физиологический раствор с различным содержанием буфера (например, Трис–HCl, ацетатный, фосфатный), pH и ионной силой; и вспомогательные вещества, такие как детергенты и солюбилизирующие агенты (например, TWEEN 20 (полисорбат–20), TWEEN 80 (полисорбат–80)), антиоксиданты (например, аскорбиновую кислоту, метабисульфит натрия) и консерванты (например, тимерасол, бензиловый спирт) и объемообразующие вещества (например, лактозу, маннит). Примеры неводных растворителей и носителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и инъекционные органические сложные эфиры, такие как этилолеат. Составы могут быть лиофилизированнными или повторно растворенными/ресуспендированными непосредственно перед использованием. Состав может быть стерилизован, например, с помощью фильтрации через фильтр, удерживающий бактерий, с помощью включения стерилизующих агентов в композиции, с помощью облучения композиций или с помощью нагревания композиций.
2. Полимерные матрицы с контролируемой доставкой
Молекулы, связывающие SIGLEC–15, раскрываемые в данном документе, также могут быть введены в составах с контролируемым высвобождением. Полимерные изделия с контролируемым высвобождением могут быть изготовлены для длительного системного высвобождения после имплантации полимерного изделия (стержня, цилиндра, пленки, диска) или инъекции (микрочастицы). Матрица может быть представлена в форме микрочастиц, таких как микросферы, в которых агент диспергирован в твердой полимерной матрице, или микрокапсулы, в которых ядро состоит из материла, отличного от полимерной оболочки, и пептид диспергирован или суспендирован в ядре, которое может быть жидким или твердым по своей природе. Если в данном документе специально не определено, то микрочастицы, микросферы и микрокапсулы используются взаимозаменяемо. В альтернативном случае полимер может быть отлит в виде тонкой пластины или пленки, варьирующих от нанометров до четырех сантиметров, порошка, полученного с помощью измельчения или с помощью других стандартных методик, или даже геля, такого как гидрогель.
Как бионеразлагаемые, так и биоразлагаемые матрицы могут быть использованы для доставки слитых полипептидов или нуклеиновых кислот, кодирующих слитые полипептиды. Они могут представлять собой природные или синтетические полимеры. Синтетические полимеры в типичном случае имеют более хорошую характеристику разложения и профили высвобождения. Полимер выбирают на основе периода времени, в течение которого требуется высвобождение. В некоторых случаях самым подходящим может быть линейное высвобождение, хотя, в других случаях импульсное высвобождение или «масштабное высвобождение» могут обеспечить более эффективные результаты. Полимер может находиться в форме гидрогеля (в типичном случае при поглощении до около 90% от веса воды) и может необязательно быть сшитым с многовалентными ионами или полимерами.
Матрицы могут быть получены с помощью испарения растворителя, высушивания распылением, экстракции растворителя и другими способами, известными специалистам в данной области техники. Биоразрушаемые микросферы могут быть приготовлены с помощью любых способов, разработанных для получения микросфер в целях лекарственной доставки, например, как описано Mathiowitz and Langer, J. Controlled Release, 5:13–22 (1987); Mathiowitz, et al., Reactive Polymers, 6:275–283 (1987); и Mathiowitz, et al., J. Appl. Polymer Sci., 35:755–774 (1988).
Можно разработать изделия для локального высвобождения в целях воздействия на область имплантации или инъекции, которые в типичном случае будут доставлять дозу, которая представляет собой намного меньшую дозу, чем доза для лечения всего организма или системной доставки. Их можно имплантировать или вводить подкожно, в мышцу, жировую ткань или проглатывать.
III. Способы применения
Также предложены способы применения раскрываемых молекул, связывающих SIGLEC–15, и молекул, связывающих лиганд SIGLEC–15. Раскрыты применения таких молекул в целях повышения иммунных ответов, замедления или предупреждения опухолевого роста, ингибирования опосредованной опухолью иммунной супрессии, уничтожения опухолей и/или истощения или блокирования активности опухоль–ассоциированных макрофагов (TAM) таким образом, чтобы изменить их активность, снизить опосредованную TAM иммунную супрессию, ослабить или обратить T–клеточную супрессию. Также предложены применения таких молекул в диагностике и лечении рака и других заболеваний.
TAM обеспечивают связь между воспалением и раком. Макрофаги представляют собой клетки иммунной системы, происходящие из активированных моноцитов крови. Они главным образом распознаются в качестве участвующих в воспалительных ответах, индуцированных патогенами или повреждением тканей, в результате деятельности, направленной на удаление (т.е. фагоцитоз) патогенов, мертвых клеток, клеточного дебриса и различных компонентов внеклеточного матрикса (ECM). Было обнаружено, что макрофаги являются важным компонентом в опухолевом микроокружении и составляют до 50% опухолевой массы.
Помимо опосредованного фагоцитоза, макрофаги секретируют проангиогенные факторы роста и протеазы, ремоделирующие матрикс, и, тем самым, играют роль в развитии сосудистой инфраструктуры (т.е., ангиогенеза), необходимой для развития и роста опухоли (Pollard, J.W. (2009), Nat. Rev. Immunol. 9:259–270). Наличие макрофагов в опухоли, по–видимому, способствует росту опухоли. Ряд исследований свидетельствует о том, что наличие опухоль–ассоциированных макрофагов в опухоли представляет собой негативный прогностический фактор выживаемости (Farinha, P. et al. (2005), Blood 106:2169–2174; Dave, S.S. et al. (2004), N. Engl. J. Med. 351:2159–2169; Solinas, G. et al. (2009), J. Leukoc. Biol. 86(5):1065–1073). TAM, а также нейтрофилы, фибробласты и другие клетки взаимодействуют с опухолевыми клетками для облегчения ангиогенеза в опухолях (Nucera, S. et al. (2011), Int. J. Dev. Biol. doi: 10.1387/ijdb.103227sn; Zamarron, B.F. et al. (2011), Int. J. Biol. Sci. 7(5):651–658; Liu, J. et al. (2011), PLoS One. 6(4):e19495; Rigo, A. et al. (2010), Molec. Cancer 9(273):1–13; Lin, J.Y. et al. (2011), Chin. J. Cancer 30(4):280–286; Vergati, M. (2011), J. Biomed. Biotechnol. 2011:182413).
Исследования показывают, что SIGLEC–15 индуцибельно экспрессируется на TAM и усиливает секрецию TGF–β в результате сочетания распознавания опухолевых клеток с
путем передачи сигнала DAP12–Syk (Takamiya, et al., Glycobiology, 23(2):178–87 (2013). В конкретной модели, предложенной Takamiya, M–CSF, секретируемый опухолевыми клетками, индуцирует дифференцировку моноцитов в макрофаги, сопровождаемую экспрессией SIGLEC–15. Взаимодействие между сиалилированным антигеном Tn и SIGLEC–15 усиливает продуцирование TGF–β из макрофагов посредством пути DAP12–Syk, способствуя развитию опухолевого микроокружения в направлении иммунной супрессии и, тем самым, прогрессирования опухоли и даже метастазирования.
Связывание функциональных блокирующих или ослабляющих анти–SIGLEC–15 антител с SIGLEC–15 может приводить к ослаблению, блокированию, антагонизации, нормализации или полному устранению способности SIGLEC–15 связываться с одним или несколькими его лигандами и, тем самым, снижению или предупреждению передачи ингибирующего иммунного сигнала, в том числе, но не ограничиваясь ей, секреции TGF–β, опосредованной SIGLEC–15. Повышенная экспрессия TGF–β часто коррелирует со злокачественностью многих видов рака и нарушением ингибирующего ответа в отношении клеточного роста в ответ на TGF–β и приводит к онкогенезу, обусловленному иммуносупрессией. Ослабление опосредованной SIGLEC–15 секреции TGF–β приводит к общему повышению иммунных ответов и прямому или косвенному снижению прогрессирования опухоли у субъекта.
Примеры, представленные ниже, показывают, что функциональные ослабляющие и блокирующие анти–SIGLEC–15 антитела, в том числе таковые, раскрываемые в данном документе, могут обращать опосредованную SIGLEC–15 супрессию CD4+ и CD8+ T–клеточной пролиферации в анализе пролиферации мононуклеарных клеток периферической крови (PBMC).
Таким образом, предложены способы ослабления иммунной супрессии и/или повышения иммунного ответа, в наиболее типичном случае в результате введения субъекту, нуждающемуся в этом, эффективного количества анти–SIGLEC–15 функционального блокирующего антитела.
Подходящие антитела, полипептиды и слитые белки раскрыты в данном документе и могут быть дополнительно селектированы с помощью анализов in vitro, в том числе, но не ограничиваясь ими: пролиферации, миграции, адгезии, роста на мягком агаре, ангиогенеза, межклеточной связи, апоптоза, транспорта, передачи сигналов и анализов in vivo, таких как ингибирование опухолевого роста. Иллюстративные анализы исследования функции раскрываемых антител предложены в Примерах, представленных ниже.
Антитела, предложенные в данном документе, могут также быть пригодными в диагностических и исследовательских применениях. Например, ненейтрализующие антитела могут связываться с конкретным антигеном, не ингибируя связывания с рецептором или биологическую активность антигена, и могут быть использованы в анализах захвата и других анализах с осаждением (например, ИФА). Нейтрализующие (например, функциональные блокирующие) антитела могут быть пригодны в анализах конкурентного связывания.
Антитела могут быть пригодными для количественной оценки полипептидов SIGLEC–15 и их лиганда.
A. Молекулы, повышающие иммунный ответ
1. Терапевтические и профилактические применения
Предложено терапевтическое и/или профилактическое применение молекул (особенно антител и их антигенсвязывающих фрагментов), которые иммуноспецифично связывают молекулы, связывающие SIGLEC–15 и лиганд SIGLEC–15 человека, и которые способны ослаблять связывание между SIGLEC–15 и одним или несколькими из его лигандов и/или контррецепторов (например, молекул–антагонистов).
В некоторых вариантах осуществления молекулы ослабляют или предупреждают связывание между SIGLEC–15 и сиалированным гликопротеиновым лигандом, например, сиалированными гликопротеинами, эндогенно экспрессируемыми клетками субъекта, и ослабляют или предупреждают передачу сигнала, опосредованного SIGLEC–15. Дополнительно или в альтернативном случае молекулы могут ослаблять или предупреждать связывание между SIGLEC–15 и его контррецептором и ослаблять или предупреждать передачу сигнала, опосредованного SIGLEC–15 и/или передачу сигнала через контррецептор. Например, раскрываемые молекулы могут связываться с антигенами в одном или нескольких сайтах SIGLEC–15, нарушающих функционирование сайта связывания с сиаловой кислотой (например, эпитопе, содержащем остаток 143 SEQ ID NO:1) и/или сайта связывания, важного в отношении контррецептора SIGLEC–15. Иллюстративные композиции проиллюстрированы в Примерах, представленных ниже. Например, в некоторых вариантах осуществления 5G12, 6F8, 8C8, 1C3, 1C12, 3H10 и 1B2 представляют собой «сильные блокаторы», а 10G9, 8H8 и 9A5 – «частичные блокаторы». Таким образом, в некоторых вариантах осуществления молекулы, используемые для положительного модулирования иммунного ответа, содержат одну, две, три, четыре, пять или все шесть CDR 5G12, 6F8, 8C8, 1C3, 1C12, 3H10, 1B2, 10G9, 8H8 или 9A5. В некоторых вариантах осуществления молекулы содержат вариабельный участок легкой цепи и/или вариабельный участок тяжелой цепи 5G12, 6F8, 8C8, 1C3, 1C12, 3H10, 1B2, 10G9, 8H8 или 9A5. В некоторых вариантах осуществления предложено мышиное анти–человеческое антитело 5G12, 6F8, 8C8, 1C3, 1C12, 3H10, 1B2, 10G9, 8H8 или 9A5 или его химерный или гуманизированный вариант.
Как описано выше, взаимодействия между SIGLEC–15 и сиалированными гликопротеиновыми лигандами и/или контррецепторами SIGLEC–15 может ингибировать пролиферацию T–клеток и повышать продуцирование цитокинов, таких как TGF–β. Таким образом, в некоторых вариантах осуществления введение раскрываемых молекул, связывающих SIGLEC–15, субъекту, положительно модулирует иммунную систему субъекта в результате блокирования или иным образом антагонизации связывания/взаимодействия лиганда SIGLEC–15 и/или контрецептора. В другом варианте осуществления авидность и/или аффинность анти–SIGLEC–15 антитела могут быть такими, что оно связывается только с клетками, которые экспрессируют очень высокие уровни SIGLEC–15, которые, например, представляют собой опухоль–ассоциированные макрофаги (TAM) или раковые клетки, и, тем самым, обеспечивают специфичное нацеливание на такую клеточную популяцию. Таким образом, в некоторых вариантах осуществления молекулы ослабляют продуцирование TGF–β, например, в опухолевом микроокружении. В некоторых вариантах осуществления клетки, экспрессирующие SIGLEC–15, представляют собой моноциты. В более конкретных вариантах осуществления клетки, экспрессирующие SIGLEC–15, представляют собой макрофаги, например, TAM.
Как указано выше, раскрываемые антитела и антигенсвязывающие фрагменты могут связываться с TAM и по сути блокировать их с тем, чтобы модулировать их иммунную супрессорную активность. Кроме того, такие антитела могут быть использованы для истощения TAM с SIGLEC–15 в опухолевом микроокружении или снижения концентрации TAM в периферической крови. В одном варианте осуществления такую модуляцию или истощение осуществляют с помощью анти–SIGLEC–15 антител, которые связываются с сайтом с тем, чтобы ослабить или нарушить нормальную функцию SIGLEC–15. Как следствие такого нарушения, активность TAM снижается (модулируется) и/или фактическая или эффективная (функциональная) концентрация макрофагов в опухоли снижается. В альтернативном случае такая модуляция или истощение осуществляется с помощью анти–SIGLEC–15 антител, которые конъюгируют с токсином таким образом, что их связывание с TAM приводит к гибели макрофага.
Кроме того, раскрываемые молекулы–антагонисты молекулы могут быть использованы для индукции, повышения или усиления T–клеточной пролиферации. В некоторых вариантах осуществления T–клеточный ответ индуцируется в результате ослабления или предупреждения связывания SIGLEC–15 с контррецептором на T–клетке. Положительная модуляция иммунной системы является особенно предпочтительной при лечении видов рака и хронических инфекций, и, таким образом, раскрываемые композиции могут быть использованы при лечении таких нарушений.
2. Субъекты, подлежащие лечению
a. Лечение рака
Раскрываемые функциональные ослабляющие композиции и способы могут быть использованы для лечения рака. Как правило, способы включают стимуляцию или усиление иммунного ответа в отношении рака, ослабление или предупреждение роста или прогрессирования опухоли или их комбинацию у субъекта с помощью введения субъекту количества молекулы, связывающей SIGLEC–15. Способ может ослаблять один или несколько симптомов рака.
Раковые клетки приобретают характерный набор функциональных возможностей во время своего развития, хотя и посредством разных механизмов. Такие возможности включают в себя уклонение от апоптоза, самодостаточность ростовых сигналов, нечувствительность к антиростовым сигналам, тканевую инвазию/метастазирование, неограниченный экспликативный потенциал и длительный ангиогенез. Термин «раковая клетка» предусматривает включение в себя предзлокачественных и злокачественных раковых клеток. В некоторых вариантах осуществления рак относится к доброкачественной опухоли, которая сохранилась локализованной. В других вариантах осуществления рак относится к злокачественной опухоли, которая инвазировала и разрушила соседние структуры организма и распространилась в отдаленные участки. В еще одних вариантах осуществления рак ассоциирован со специфическим раковым антигеном (например, антигеном, свойственным для всех видов карциномы (KS 1/4), антигеном карциномы яичника (CA125), простатспецифическим антигеном (PSA), раково–эмбриональным антигеном (CEA), CD19, CD20, HER2/neu и др.).
Способы и композиции, раскрываемые в данном документ, пригодны в лечении или предупреждении ряда видов рака и других патологических пролиферативных заболеваний, в том числе (но не ограничиваясь ими) следующих: карциномы, в том числе таковой мочевого пузыря, молочной железы, кишечника, почки, печени, легкого, яичника, поджелудочной железы, желудка, шейки матки, щитовидной железы и кожи; в том числе плоскоклеточной карциномы; гематопоэтических опухолей лимфоидной клеточной линии, в том числе лейкоза, острого лимфоцитарного лейкоза, острого лимфобластного лейкоза, B–клеточной лимфомы, T–клеточной лимфомы, лимфомы Беркитта; гематопоэтических опухолей миелоидной клеточной линии, в том числе острых и хронических миелогенных лейкозов и промиелоцитарного лейкоза; опухолей мезенхимального происхождения, в том числе фибросаркомы и рабдомиосаркомы; другие опухоли, в том числе меланомы, семиномы, тератокарциномы, нейробластомы и глиомы; опухолей центральной и периферической нервной системы, в том числе астроцитомы, нейробластомы, глиомы и шванномы; опухолей мезенхимального происхождения, в том числе фибросаркомы, рабдомиосаркомы и остеосаркомы; и других опухолей, в том числе меланомы, пигментной ксеродермы, кератоакантому, семиномы, фолликулярного рака щитовидной железы и тератокарциномы.
Виды рака, вызванные нарушениями апоптоза, также могут подлежать лечению с помощью раскрываемых способов и композиций. Такие виды рака могут включать в себя, но не ограничиваясь ими, фолликулярные лимфомы, карциномы с мутациями p53, гормонзависимые опухоли молочной железы, предстательной железы и яичника, и предраковые поражения, такие как семейный аденоматозный полипоз и миелодиспластические синдромы. В конкретных вариантах осуществления злокачественную опухоль или диспролиферативные изменения (такие как метаплазии и дисплазии) или гиперпролиферативные нарушения лечат или предупреждают с помощью этих способов и композиций в яичнике, мочевом пузыре, молочной железе, кишечнике, легком, коже, поджелудочной железе или матке. В других конкретных вариантах осуществления саркому, меланому или лейкоз лечат или предупреждают с помощью раскрываемых способов и композиций.
Раскрываемые композиции и способы особенно пригодны для лечения видов рака, которые ассоциированы с клетками, которые экспрессируют аномально высокие уровни самого SIGLEC–15 или гликопротеиновых лигандов SIGLEC–15, видов рака с большим количеством опухоль–ассоциированных макрофагов, особенно, если макрофаги экспрессируют SIGLEC–15, и/или рака, при котором другой(другие) тип(типы) клеток экспрессирует(экспрессируют) высокие уровни SIGLEC–15 или лигандов SIGLEC–15.
Конкретные виды рака и соответствующие нарушения, которые можно лечить или предупреждать с помощью способов и композиций, раскрываемых в данном документе, включают в себя, но не ограничиваясь ими, лейкозы, в том числе, но не ограничиваясь ими, острый лейкоз, острый лимфоцитарный лейкоз, острые миелоцитарные лейкозы, такие как миелобластические, промиелоцитарные, миеломоноцитарные, моноцитарные лейкозы, эритролейкозы и миелодиспластический синдром, хронические лейкозы, такие как, но не ограничиваясь ими, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический лимфоцитарный лейкоз, лейкоз волосковых клеток; истинная полицитемия; лимфомы, такие как, но не ограничиваясь ими, ходжкинская лимфома или неходжкинская лимфома; лимфомы (например, диффузную B–крупноклеточную лимфому (DLBCL), негативную в отношении киназы анапластической лимфомы (ALK); диффузную B–крупноклеточную лимфому (DLBCL), позитивную в отношении киназы анапластической лимфомы (ALK); ALK+ анапластическую крупноклеточную лимфому(ALCL), позитивную в отношении киназы анапластической лимфомы (ALK), острую миелоидную лимфому (AML)); множественные миеломы, такие как, но не ограничиваясь ими, тлеющая множественная миелома, несекреторная миелома, остеосклеротическая миелома, лейкоз плазматических клеток, солитарная плазмоцитома и экстрамедуллярная плазмоцитома; макроглобулинемия Вальденстрема; моноклональная гаммапатия неустановленной этиологии; доброкачественная моноклональная гаммапатия; болезнь тяжелых цепей; саркомы костей и соединительной ткани, такие как, но не ограничиваясь ими, саркома кости, остеосаркома, хондросаркома, саркома Юинга, гигантоклеточная саркома, фибросаркома кости, хордома, периостальная саркома, саркомы мягких тканей, ангиосаркома (гемангиосаркома), фибросаркома, саркома Капоши, лейомиосаркома, липосаркома, лимфангиосаркома, неврилеммома, рабдомиосаркома, синовиальная саркома; опухоли мозга, в том числе, но не ограничиваясь ими, глиому, астроцитому, глиому ствола мозга, эпендимому, олигодендроглиому, неглиальную опухоль, неврилеммому слухового нерва, краниофарингиому, медуллобластому, менингиому, пинеоцитому, пинеобластому, первичную лимфому мозга; рак молочной железы, в том числе, но не ограничиваясь ими, аденокарциному, лобулярную (мелкоклеточная) карциному, внутрипротоковую карциному, медуллярный рак молочной железы, слизеобразующий рак молочной железы, тубулярный рак молочной железы, папиллярный рак молочной железы, болезнь Пэджета и отечно–инфильтративный рак молочной железы; рак надпочечников, в том числе, но не ограничиваясь ими, феохромоцитомную и адренокортикальную карциному; рак щитовидной железы, такой как, но не ограничиваясь ими, папиллярный или фолликулярный рак щитовидной железы, медуллярный рак щитовидной железы и анапластический рак щитовидной железы; рак поджелудочной железы, в том числе, но не ограничиваясь ими, инсулиному, гастриному, глюкагоному, випому, соматостатиному и карциноидную опухоль и опухоль островковых клеток; злокачественные опухоли гипофиза, в том числе, но не ограничиваясь ими, болезнь Кушинга, пролактиному, акромегалию и несахарный диабет; злокачественные опухоли глаз, в том числе, но не ограничиваясь ими, меланому глаза, такую как меланома радужной оболочки, хороидальная меланома и меланома цилиарного тела и ретинобластома; злокачественные опухоли влагалища, в том числе, но не ограничиваясь ими, плоскоклеточную карциному, аденокарциному и меланому; рак вульвы, в том числе, но не ограничиваясь ими, плоскоклеточную карциному, меланому, аденокарциному, карциному базальных клеток, саркому и болезнь Пэджета; злокачественные опухоли шейки матки, в том числе, но не ограничиваясь ими, плоскоклеточную карциному и аденокарциному; злокачественные опухоли матки, в том числе, но не ограничиваясь ими, карциному эндометрия и саркому матки; злокачественные опухоли яичника, в том числе, но не ограничиваясь ими, эпителиальную карциному яичника, пограничную опухоль, эмбрионально–клеточную опухоль и стромальную опухоль; злокачественные опухоли пищевода, в том числе, но не ограничиваясь ими, плоскоклеточный рак, аденокарциному, аденоидно–кистозную карциному, мукоэпидермоидную карциному, аденосквамозную карциному, саркому, меланому, плазмоцитому, бородавчатую карциному и овсяно–клеточную (мелкоклеточную) карциному; злокачественные опухоли желудка, в том числе, но не ограничиваясь ими, аденокарциному, грибовидно разрастающуюся (полипоид), изъязвленную, поверхностно распространяющуюся, диффузно распространяющуюся, злокачественную лимфому, липосаркому, фибросаркому и карциносаркому; злокачественные опухоли кишечника; злокачественные опухоли прямой кишки; злокачественные опухоли печени, в том числе, но не ограничиваясь ими, гепатоцеллюлярную карциному и гепатобластому, злокачественные опухоли желчного пузыря, в том числе, но не ограничиваясь ей, аденокарциному; холангиокарциномы, в том числе, но не ограничиваясь ими, папиллярные, узловые и диффузные; злокачественные опухоли легких, в том числе, но не ограничиваясь ими, немелкоклеточный рак легких, плоскоклеточную карциному (эпидермоидную карциному), аденокарциному, крупноклеточную карциному и мелкоклеточный рак легких; злокачественные опухоли яичек, в том числе, но не ограничиваясь ими, герминому, семиному, анапластическую, классическую (типичную), сперматоцитарную, несеминому, эмбриональную карциному, тератому, карциному, хориокарциному (опухоль желточного мешка), злокачественные опухоли предстательной железы, в том числе, но не ограничиваясь ими, аденокарциному, лейомиосаркому и рабдомиосаркому; злокачественные опухоли пениса; злокачественные опухли ротовой полости, в том числе, но не ограничиваясь ими, плоскоклеточную карциному; базальноклеточные злокачественные опухоли; злокачественные опухоли слюнных желез, в том числе, но не ограничиваясь ими, аденокарциному, мукоэпидермоидную карциному и аденоидо–кистозную карциному; злокачественные опухоли глотки, в том числе, но не ограничиваясь ими, плоскоклеточный рак и бородавчатый рак; злокачественные опухоли кожи, в том числе, но не ограничиваясь ими, базальноклеточную карциному, плоскоклеточную карциному и меланому, поверхностно распространяющуюся меланому, узелковую меланому, злокачественную меланому лентиго, акральную лентигинозную меланому; злокачественные опухоли почек, в том числе, но не ограничиваясь ими, почечно–клеточный рак, аденокарциному, гипернефрому, фибросаркому, рак переходных клеток (почечной лоханки и/или мочеточника); опухоль Вильмса; злокачественные опухоли мочевого пузыря, в том числе, но не ограничиваясь ими, карциному переходных клеток, плоскоклеточный рак, аденокарциному, карциносаркому. Кроме того, виды рака включают в себя миксосаркому, остеогенную саркому, эндотелиосаркому, лимфангиотелиосаркому, мезотелиому, синовиому, гемангиобластому, эпителиальную карциному, цистаденосаркому, бронхогенную карциному, карциному потовых желез, карциному сальных желез, папиллярную карциному и папиллярные аденокарциномы (обзор таких нарушений см. в Fishman et al., 1985, Medicine, 2nd Ed., J.B. Lippincott Co., Philadelphia and Murphy et al., 1997, Informed Decisions: The Complete Book of Cancer Diagnosis, Treatment, and Recovery, Viking Penguin, Penguin Books U.S.A., Inc., United States of America).
b. Лечение инфекций
Раскрываемые функциональные ослабляющие композиции и способы могут быть использованы для лечения инфекций и инфекционный заболеваний. Как правило, способы включают стимуляцию или усиление иммунного ответа в отношении агента, вызывающего инфекцию, ослабление или предупреждение прогрессирования инфекционных заболеваний или их комбинацию у субъекта с помощью введения субъекту количества молекулы, связывающей SIGLEC–15. Способ может ослаблять один или несколько симптомов инфекции.
Инфекция или заболевание может быть вызвано бактерией, вирусом, простейшим, гельминтом или другим микробным патогеном, который проникает внутриклеточно и подвергается атаке, например, со стороны цитотоксических T–лимфоцитов.
Инфекция или заболевание может быть острым или хроническим. Острая инфекция в типичном случае представляет собой инфекцию малой длительности. Во время острой микробной инфекции иммунные клетки начинают экспрессировать иммуномодулирующие рецепторы. Соответственно, в некоторых вариантах осуществления способ включает повышение иммунного стимулирующего ответа против острой инфекции.
Инфекция может быть вызвана, например, но не ограничиваясь ими, Candida albicans, Listeria monocytogenes, Streptococcus pyogenes, Streptococcus pneumoniae, Neisseria meningitidis, Staphylococcus aureus, Escherichia coli, Acinetobacter baumannii, Pseudomonas aeruginosa или Mycobacterium.
В некоторых вариантах осуществления раскрываемые композиции используют для лечения хронических инфекций, например, инфекций, в которых происходило T–клеточное истощение или T–клеточная анергия, приводя к тому, что инфекция сохраняется у хозяина в течение длительного периода времени.
Иллюстративные инфекции, подлежащие лечению, представляют собой хронические инфекции, вызванные вирусом гепатита, вирусом иммунодефицита человека (ВИЧ), T–лимфотропным вирусом человека (HTLV), вирусом герпеса, вирусом Эпштейна–Барр или вирусом папилломы человека.
Поскольку вирусные инфекции удаляются преимущественно T–клетками, то повышение T–клеточной активности было бы терапевтически полезным в ситуациях, когда более быстрое или тщательное удаление инфекционного вирусного агента было бы предпочтительным для субъекта–животного или субъекта–человека. Таким образом, раскрываемые композиции можно вводить для лечения местных или системных вирусных инфекций, в том числе, но не ограничиваясь ими, иммунодефицита (например, ВИЧ), папилломы (например, ВПЧ), герпеса (например, ВПГ), энцефалита, гриппа (например, вируса гриппа A человека) и простуды (например, риновируса человека) и других вирусных инфекций, вызванных, например, HTLV, вирусом гепатита, респираторным синцитальным вирусом, вирусом осповакцины и вирусом бешенства. Молекулы могут быть введены местно для лечения вирусных кожных заболеваний, таких как герпетические поражения или опоясывающий герпес или генитальные бородавки. Молекулы также могут быть введены системно для лечения системных вирусных заболеваний, в том числе, но не ограничиваясь ими, СПИДа, гриппа, простуды или энцефалита.
Иллюстративные инфекции, которые могут подлежать лечению, включают, но не ограничиваясь ими, инфекции, вызванные микроорганизмами, в том числе, но не ограничиваясь ими, Actinomyces, Anabaena, Bacillus, Bacteroides, Bdellovibrio, Bordetella, Borrelia, Campylobacter, Caulobacter, Chlamydia, Chlorobium, Chromatium, Clostridium, Corynebacterium, Cytophaga, Deinococcus, Escherichia, Francisella, Halobacterium, Heliobacter, Haemophilus, Hemophilus influenza тип B (HIB), Hyphomicrobium, Legionella, Leptspirosis, Listeria, Meningococcus A, B и C, Methanobacterium, Micrococcus, Myobacterium, Mycoplasma, Myxococcus, Neisseria, Nitrobacter, Oscillatoria, Prochloron, Proteus, Pseudomonas, Phodospirillum, Rickettsia, Salmonella, Shigella, Spirillum, Spirochaeta, Staphylococcus, Streptococcus, Streptomyces, Sulfolobus, Thermoplasma, Thiobacillus, and Treponema, Vibrio, Yersinia, Cryptococcus neoformans, Histoplasma capsulatum, Candida albicans, Candida tropicalis, Nocardia asteroides, Rickettsia ricketsii, Rickettsia typhi, Mycoplasma pneumoniae, Chlamydial psittaci, Chlamydial trachomatis, Plasmodium falciparum, Trypanosoma brucei, Entamoeba histolytica, Toxoplasma gondii, Trichomonas vaginalis и Schistosoma mansoni.
Другие микроорганизмы, которые могут подлежать лечению с помощью раскрываемых композиций и способов, включают в себя бактерии, такие как таковые Klebsiella, Serratia, Pasteurella; патогены, ассоциированные с холерой, столбняком, ботулизмом, сибирской язвой, чумой и болезнью Лайма; или грибковые или паразитические патогены, такие как Candida (albicans, krusei, glabrata, tropicalis и др.), Cryptococcus, Aspergillus (fumigatus, niger и др.), Genus Mucorales (mucor, absidia, rhizophus), Sporothrix (schenkii), Blastomyces (dermatitidis), Paracoccidioides (brasiliensis), Coccidioides (immitis) и Histoplasma (capsulatuma), Entamoeba, histolytica, Balantidium coli, Naegleria fowleri, Acanthamoeba sp., Giardia lambia, Cryptosporidium sp., Pneumocystis carinii, Plasmodium vivax, Babesia microti, Trypanosoma brucei, Trypanosoma cruzi, Toxoplasma gondi и др.), Sporothrix, Blastomyces, Paracoccidioides, Coccidioides, Histoplasma, Entamoeba, Histolytica, Balantidium, Naegleria, Acanthamoeba, Giardia, Cryptosporidium, Pneumocystis, Plasmodium, Babesia или Trypanosoma и др.
B. Молекулы, ослабляющие иммунный ответ
1. Терапевтические и профилактические применения
Предложено терапевтическое и/или профилактическое применение молекул (особенно антител или их антигенсвязывающих фрагментов), которые связывают SIGLEC–15 человека или его лиганд, и которые способны повышать или усиливать связывание между SIGLEC–15 и одним или несколькими из его лигандов и/или контрецепторов (например, молекул–агонистов), а также предложено непосредственное повышение или усиление сигнала, опосредованного SIGLEC–15 или контррецептором.
Как описано выше, взаимодействия между SIGLEC–15 и сиалированными гликопротеиновыми лигандами и/или контррецепторами SIGLEC–15 может ингибировать пролиферацию T–клеток и повышать продуцирование цитокинов, таких как TGF–β. Таким образом, в некоторых вариантах осуществления введение функциональных активирующих молекул, связывающих SIGLEC–15, или функциональных активирующих молекул, связывающих лиганд SIGLEC–15, субъекту, отрицательно модулирует иммунную систему субъекта в результате индукции или иного агонизирования связывания/взаимодействия лиганда SIGLEC–15 и/или контрецептора или непосредственной стимуляции передачи сигнала с участием SIGLEC–15 или контррецептора SIGLEC–15. В некоторых вариантах осуществления молекулы повышают продуцирование TGF–β и/или его секрецию, например, из моноцитов, таких как макрофаги.
Кроме того, раскрытые молекулы–агонисты, связывающие SIGLEC–15 и связывающие лиганд SIGLEC–15, могут быть использованы для ослабления или снижения T–клеточной пролиферации. В некоторых вариантах осуществления T–клеточный ответ индуцируется в результате повышения или усиления связывания SIGLEC–15 с контррецептором на T–клетке. Отрицательная модуляция иммунной системы является особенно необходимой при лечении воспалительных и аутоиммунных заболеваний и нарушений и для лечения или предупреждения отторжения трансплантата и/или заболевания «трансплантат против хозяина», и, тем самым, раскрываемые композиции могут быть использованы в лечении таких нарушений.
a. Воспалительные ответы
В некоторых вариантах осуществления молекулы–агонисты SIGLEC–15 используются для лечения или облегчения одного или нескольких симптомов воспаления, например, острого, хронического или персистирующего воспаления.
Иммунный ответ, включающий в себя воспаление, может быть ингибирован или ослаблен у субъекта, предпочтительно человека, с помощью введения эффективного количества молекулы, связывающей SIGLEC–15, для ингибирования или ослабления биологической активности иммунной клетки (например, T–клеток или B–клеток) или для снижения количества провоспалительных молекул в области воспаления. Иллюстративные провоспалительные молекулы включают в себя, но не ограничиваясь ими, IL–1β, TNF–α, IFN–γ, IL–18, IL–17, IL–6, IL–23, IL–22, IL–21 и MMP.
b. Гипервоспалительный ответ
В некоторых вариантах осуществления молекулы, связывающие SIGLEC–15, оказывают тормозящее действие на иммунную систему. Например, молекула, связывающая SIGLEC–15, может быть использована для контроля иммунного стимулирующего ответа в отношении инфекции, которая вызывает повреждение здоровых тканей в результате гипервоспалительного ответа. Соответственно, в некоторых вариантах осуществления агенты вводят субъекту с инфекций, который также претерпевает гипервоспалительный ответ. В таких случаях контроль избыточных иммунных ответов может быть полезным для субъекта.
c. Воспалительные и аутоиммунные заболевания/нарушения
Раскрываемые композиции также могут быть использованы для лечения воспалительных или аутоиммунных заболеваний и нарушений. Иллюстративные воспалительные или аутоиммунные заболевания/нарушения, которые можно лечить, включают в себя, но не ограничиваясь ими, ревматоидный артрит, системную красную волчанку, гнездную алопецию, анкилозирующий спондилит, антифосфолипидный синдром, аутоиммунную болезнь Аддисона, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунное заболевание внутреннего уха, аутоиммунный лимфопролиферативный синдром (ALPS), аутоиммунную тромбоцитопеническую пурпуру (ATP), болезнь Бехчета, буллезный пемфигоид, кардиомиопатию, спру–целиакию, дерматит, синдром хронической усталости и иммунодефицита (CFIDS), хроническую воспалительную димиелинизирующую полинейропатию, рубцующийся пемфигоид, болезнь холодовых агглютининов, Crest–синдром, болезнь Крона, болезнь Дего, дерматомиозит, ювенильный дерматомиозит, дискоидную волчанку, первичную криоглобулинемию смешанного типа, фибромиалгию, фибромиозит, болезнь Грейвса, синдром Гийена–Барре, тиреоидит Хашимото, идиопатический легочный фиброз, идиопатическую тромбоцитопеническую пурпуру (ITP), Ig А–нефропатию, инсулинзависимый сахарный диабет (I типа), ювенильный артрит, болезнь Меньера, смешанное заболевание соединительной ткани, рассеянный склероз, миастению gravis, вульгарный пемфигус, пернициозную анемию, узелковые периартерит, полихондрию, полигландулярный синдром, ревматическую полимиалгию, полимиозит и дерматомиозит, первичную агаммаглобулинемию, первичный биллиарный цирроз печени, псориаз, феномен Рейно, синдром Рейтера, ревматическую лихорадку, саркоидоз, склеродермию, синдром Шегрена, синдром скованного человека, артериит Такаясу, височный артериит/гигантоклеточный артериит, язвенный колит, увеит, васкулит, витилиго и грануломатоз Вегенера.
В некоторых вариантах осуществления воспалительное или аутоиммунное заболевание вызвано патогеном или представляет собой результат инфекции.
d. Трансплантаты
Молекулы, связывающие SIGLEC–15, могут быть использованы для ослабления или ингибирования отторжения трансплантата у субъекта, предпочтительно субъекта–человека. Отторжение трансплантата может быть ингибировано или ослаблено у субъекта с помощью введения эффективного количества молекулы–агониста, связывающей SIGLEC–15, для ингибирования или ослабления биологической активности иммунной клетки или для снижения количеств провоспалительных цитокинов или других молекул, ассоциированных с воспалением или способствующих воспалению в области трансплантата.
Трансплантируемый материал может представлять собой клетки, ткани, органы, конечности, пальцы или части тела, предпочтительно человеческого тела. Трансплантаты в типичном случае являются аллогенными или ксеногенными. Молекулу–агонист SIGLEC–15 в типичном случае вводят субъекту в эффективном количества для ослабления или ингибирования отторжения трансплантата. Молекулу можно вводить системно или локально с помощью любого пути введения. В некоторых вариантах осуществления молекулы вводят в область трансплантации до, во время или после трансплантации.
Молекулы можно вводить непосредственно в клетки, ткань или орган, подлежащие трансплантации ex vivo. В одном варианте осуществления трансплантируемый материал приводят в контакт с молекулой, связывающей SIGLEC–15, до трансплантации, после трансплантации или и то и другое.
В других вариантах осуществления молекулу, связывающую SIGLEC–15, вводят в иммунные ткани или органы, такие как лимфатические узлы или селезенка.
i. Клетки
Популяции любых типов клеток могут быть трансплантированы в субъекта. Клетки могут быть гомогенными или гетерогенными. Гетерогенный означает, что клеточная популяция содержит более одного типа клеток. Иллюстративные клетки включают в себя клетки–предшественницы, такие как стволовые клетки и плюрипотентные клетки, которые могут быть собраны от донора и трасплантированы субъекту. Перед трансплантацией клетки необязательно обрабатывают ex vivo. Клетки могут представлять собой аутологичные или гетерологичные клетки.
ii. Ткани
Любая ткань может быть использована в качестве трансплантата. Иллюстративные ткани включают в себя кожу, жировую ткань, сердечно–сосудистую ткань, такую как вены, артерии, капилляры, клапаны; нервную ткань, костный мозг, легочную ткань, глазную ткань, такую как роговица и хрусталик, хрящевую, костную и мышечную ткань. Ткань может быть модифицирована, как описано выше.
iii. Органы
Иллюстративные органы, которые могут быть использованы для трансплантата, включают в себя, но не ограничиваясь ими, почку, печень, сердце, селезенку, мочевой пузырь, легкое, желудок, глаз, язык, поджелудочную железу, кишечник и др. Орган, подлежащий трансплантации, также может быть модифицирован перед трансплантацией, как описано выше.
В одном варианте осуществления предложен способ ингибирования или ослабления хронического отторжения трансплантата у субъекта с помощью введения эффективного количества молекулы, связывающей SIGLEC–15, для ингибирования или ослабления хронического отторжения трансплантата по сравнению с контролем.
e. Заболевание «трансплантат против хозяина» (GVHD)
Молекулы также могут быть использованы для лечения заболевания «трансплантат против хозяина» (GVHD) с помощью введения эффективного количества молекулы, связывающей SIGLEC–15, для облегчения одного или нескольких симптомов, ассоциированных с GVHD. GVHD представляет собой основное осложнение, ассоциированное с аллогенной трансплантацией гематопоэтических стволовых клеток, при котором функциональные стволовые клетки в трансплантированном костном мозге распознают реципиента как «чужеродного» и организовывают иммунологическую атаку. При определенных обстоятельствах это также может иметь место при переливании крови. Симптомы GVD включают в себя кожную сыпь или изменение цвета или текстуры кожи, диарею, тошноту, нарушение печеночной функции, пожелтение кожи, повышенную восприимчивость к инфекции, сухость и раздражительность глаз и чувствительность или сухость во рту.
f. Сахарный диабет
Молекулы–агонисты, связывающие SIGLEC–15, могут быть использованы для лечения сахарного диабета. Способ включает трансплантацию инсулин–продуцирующих клеток субъекту и введение субъекту эффективного количества молекулы для ослабления или ингибирования отторжения трансплантата. Предпочтительно инсулин–продуцирующие клетки представляют собой бета–клетки или островковые клетки. В определенных вариантах осуществления инсулин–продуцирующие клетки представляют собой рекомбинантные клетки, разработанные в целях продуцирования инсулина.
Инсулин–продуцирующие клетки могут быть покрыты капсулой с матрицей, такой как полимерная матрица, с помощью подходящих полимеров, в том числе, но не ограничиваясь ими, альгината, агарозы, гиалуроновой кислоты, коллагена, синтетических мономеров, альбумина, фибриногена, фибронектина, витронектина, ламинина, декстрана, сульфата декстрана, хондроитинсульфата, дерматансульфата, кератансульфата, хитина, хитозана, гепарана, гепарансульфата или их комбинации.
C. Терапевтическое ингибирование резорбции костной ткани остеокластами
Исследования показывают, что экспрессия и функция SIGLEC–15 важны при остеокластогенезе (Stuible, et al., J. Biol Chem., 289(10): 6498–6512 (2014), Ishida–Kitagawa, J. Biol. Chem., 287, 17493–17502 (2012), каждая из которых явно включена посредством ссылки в полном объеме). Несмотря на то, что белок SIGLEC–15 является значительно активируется во время дифференцировки остеокластов, этот белок не подлежит выявлению в недифференцированных клетках. Результаты указывают на то, что SIGLEC–15 и DAP12 образуют комплекс при эндогенных уровнях экспрессии в остеокластах. Мыши с нокаутом по SIGLEC–15(–/–) проявляют умеренный остеопороз.
Исследования in vivo также показывают, что анти–SIGLEC–15 антитело может ингибировать активность остеокластов в физиологическом контексте и обеспечивать терапевтическую стратегию в целях ослабления потери костной ткани. Несмотря на то, что активация рецепторов на клеточной поверхности и их эндоцитозная отрицательная регуляция часто являются сочетанными в качестве средства ограничения интенсивности и длительности передачи сигнала, передача сигнала и эндоцитоз с участием SIGLEC–15, по–видимому, происходят исключительно друг с другом, в зависимости от того, индуцирует ли лигирование антител кластеризацию или просто димеризацию рецепторов.
SIGLEC–15 представляет собой рецептор, характерный для остеокластов, с высокоограниченным паттерном экспрессии, и, тем самым, виды терапии, нацеленные на SIGLEC–15, являются избирательными. Анти–SIGLEC–15 антитела ингибируют дифференцировку остеокластов на сравнительно поздней стадии, тем самым, сохраняя сочетанную связь между остеокластами и остеобластами и предупреждая осложнения существующих видов терапии, нацеленных на остеокласты, которые могут индуцировать гибель остеокластов (бисфосфонаты) или предупреждать их дифференцировку на ранней стадии (деносумаб), приводя к нежелательным побочным эффектам, в том числе остеонекроз челюсти и атипичные переломы бедра.
Таким образом, в некоторых вариантах осуществления раскрываемые молекулы (особенно антитела или их антигенсвязывающие фрагменты), которые иммуноспецифично связывают SIGLEC–15 человека и которые способны ослаблять или блокировать связывание между SIGLEC–15 и одним или несколькими из его лигандов и/или контррецепторов (например, молекулами–агонистами), также можно вводить субъекту, нуждающемуся в этом, в эффективном количестве для ослабления или ингибирования дифференцировки остеокластов, их функционирования или комбинации. В некоторых вариантах осуществления молекулы вводят в эффективном количестве для ослабления потери костной ткани, повышения костеобразования, повышения минеральной плотности костной ткани или их комбинации.
D. Нацеливание и детекция
Раскрываемые молекулы, связывающие SIGLEC–15 и связывающие лиганд SIGLEC–15, вне зависимости от их воздействия на функцию SIGLEC–15, могут быть использованы для доставки терапевтического груза и/или детекции наличия SIGLEC–15 или его лиганда соответственно на клетках или тканях. Например, молекулы, связывающие SIGLEC–15 и связывающие рецептор SIGLEC–15, могут быть конъюгированы с биологической молекулой, представляющей интерес, с образованием конъюгата. Груз, содержащий фармакологически активные молекулы, такие как неорганические и органические молекулы, фармацевтические агенты, лекарственные препараты, пептиды, белки, генетический материал и др., может быть конъюгирован с молекулой, связывающей SIGLEC–15 или связывающей лиганд SIGLEC–15, которая затем может нацеливать груз в клетки или ткани, экспрессирующие SIGLEC–15 или его лиганд соответственно. Молекулы SIGLEC–15 могут быть химически связаны с полипептидом с помощью пептидной связи или с помощью химической или пептидной линкерной молекулы. Способы присоединения лекарственного препарата или другого низкомолекулярного фармацевтического препарата к фрагменту антитела хорошо известны и включают в себя химические линкеры, такие как N–сукцинимидил(4–йодацетил)–аминобензоат; сульфосукцинимидил(4–йодацетил)–аминобензоат; 4–сукцинимидил–оксикарбонил–.A–инвертированный.–(2–пиридилтио)толуол; сульфосукцинимидил–6–[.альфа.–метил–.A–инвертированный.–(пиридилдитиол)–толуами–до]гексаноат; N–сукцинимидил–3–(–2–пиридилтио)–проприонат; сукцинимидил–6–[3(–(–2–пиридилтио)–проприонамидо]гексаноат; сульфосукцинимидил–6–[3(–(–2–пиридилдитио)–пропионамидо]гексаноат; 3–(2–пиридилдитио)–пропионилгидразин, реактив Эдмана, дихлортриазиновую кислоту, S–(2–тиопиридил)–L–цистеин и т.п.
Слитые белки могут быть сконструированы таким образом, чтобы расположить белок, представляющий интерес, на амино– или карбоксиконце как тяжелой, так и легкой цепи антитела, хотя вся тяжелая цепь может не потребоваться. Потенциальные конфигурации включают в себя применение усеченных участков тяжелой и легкой цепи со спейсерными последовательностями или без них, при необходимости, в целях поддержания функциональной целостности присоединяемого белка.
В альтернативном случае может быть разработана универсальная система носителей. Например, различные белки или ДНК могут быть конъюгированы с распространенным носителем, таким как белок A, поли–L–лизин, гексагистидин и т.п. Конъюгированный носитель впоследствии может образовывать комплекс с молекулами, связывающими SIGLEC–15 или связывающими лиганд SIGLEC–15. Небольшая часть молекулы–носителя, которая отвечает за связывание иммуноглобулина, могла быть использована в качестве носителя. Другие аналогичные конфигурации включают в себя конструирование носителей, которые взаимодействуют с белками, разработанными в тяжелой или легкой цепи антитела.
В некоторых вариантах осуществления молекулы, связывающие SIGLEC–15 или связывающие лиганд SIGLEC–15, конъюгируют или иным образом включают в или на наноноситель для нацеливания на клетки, позитивные в отношении SIGLEC–15 или лиганда SIGLEC–15. Наноноситель, например, микро– или нанополимерные частицы, липосомы, нанотрубки и т.д. могут содержать активный агент для доставки в клетки, позитивные в отношении SIGLEC–15 или лиганда SIGLECt–15, или их микроокружение.
Аналогичным образом, молекулы, связывающие SIGLEC–15 или лиганд SIGLEC–15, могут быть конъюгированы с детектируемым маркером или могут быть неконъюгированными и детектируемыми с помощью вторичного реагента в целях детекции экспрессии SIGLEC–15 или лиганда SIGLEC–15 соответственно, in vitro или in vivo. Таким образом, молекулы могут быть использованы для визуализации, иммуногистохимического анализа и других анализов.
IV. Комбинированные виды терапии
Раскрываемые молекулы, связывающие SIGLEC–15 и лиганд SIGLEC–15, можно вводить субъекту, нуждающемуся в этом, в отдельности или в комбинации с одним или несколькими дополнительными терапевтическими агентами. В некоторых вариантах осуществления молекулу, связывающую SIGLEC–15 или связывающую лиганд SIGLEC–15, и дополнительный терапевтический агент вводят раздельно, но одновременно. Молекулу, связывающую SIGLEC–15 или связывающую лиганд SIGLEC–15, и дополнительный терапевтический агент можно также вводить в виде части одной и той же композиции. В некоторых вариантах осуществления молекулу, связывающую SIGLEC–15 и связывающую лиганд SIGLEC–15, и второй терапевтический агент вводят раздельно и в различное время, однако в виде части одной и той же схемы лечения.
Субъекту можно вводить первый терапевтический агент за 1, 2, 3, 4, 5, 6 или более часов или за 1, 2, 3, 4, 5, 6, 7 или более дней до введения второго терапевтического агента. В некоторых вариантах осуществления субъекту можно вводить одну или несколько доз первого агента каждые 1, 2, 3, 4, 5, 6 7, 14, 21, 28, 35 или 48 дней до первого введения второго агента. Молекула, связывающая SIGLEC–15 или связывающая лиганд SIGLEC–15, может представлять собой первый или второй терапевтический агент. В некоторых вариантах осуществления одну или несколько молекул, связывающих SIGLEC–15, и одну или несколько молекул, связывающих лиганд SIGLEC–15, вводят в комбинации.
Молекулу, связывающую SIGLEC–15 и/или связывающую лиганд SIGLEC–15, и дополнительный терапевтический агент можно вводить в виде части схемы лечения. Например, если первый терапевтический агент можно вводить субъекту на каждый четвертый день, то второй терапевтический агент можно вводить на первый, второй, третий или четвертый день или их комбинации. Первый терапевтический агент или второй терапевтический агент можно вводить повторно в течение всей схемы лечения.
Иллюстративные молекулы включают, но не ограничиваясь ими, цитокины, химиотерапевтические агенты, радионуклиды, другие иммунотерапевтические препараты, ферменты, антибиотики, противовирусные препараты (особенно ингибиторы протеаз в отдельности или в комбинации с нуклеозидами для лечения ВИЧ или гепатита B или C), противопаразитарные препараты (для лечения гельминтов, простейших), факторы роста, ингибиторы роста, гормоны, антагонисты гормонов, антитела и их биоактивные фрагменты (в том числе гуманизированные, одноцепочечные и химерные антитела), препараты на основе антигенов и вакцин (в том числе адъюванты), пептидные лекарственные препараты, противовоспалительные препараты, лиганды, которые связываются с Toll–подобными рецепторами (в том числе, но не ограничиваясь ими, полиинозиновая:полицитидиловая кислота (polyI:C) и олигонуклеотиды CpG) в целях активации врожденной иммунной системы, молекулы, которые мобилизуют и адаптируют иммунную систему, другие молекулы, которые активируют или усиливают действие цитотоксических T–лимфоцитов, естественных клеток–киллеров и T–хелперов, а также других молекул, которые дезактивируют или оказывают отрицательную регуляцию на супрессорные или регуляторные T–клетки.
Дополнительные терапевтические агенты выбирают на основе патологического состояния, нарушения или заболевания, подлежащих лечению. Например, молекулу, связывающую SIGLEC–15, можно вводить совместно с одним или несколькими дополнительными агентами, которые функционируют таким образом, чтобы усиливать или активировать иммунный ответ или ослаблять или ингибировать иммунный ответ.
A. Химиотерапевтические агенты
Молекулы, связывающие SIGLEC–15 и связывающие лиганд SIGLEC–15, можно комбинировать с одним или несколькими химиотерапевтическими агентами и проапоптическими агентами. Иллюстративные химиотерапевтические агенты включают в себя, но не ограничиваясь ими, амсакрин, блеомицин, бусульфан, капецитабин, карбоплатин, кармустин, хлорамбуцил, цисплатин, кладрибин, клофарабин, кризантаспазу, циклофосфамид, цитарабин, дакарбазин, дактиномицин, даунорубицин, доцетаксел, доксорубицин, эпирубицин, этопозид, флударабин, фторурацил, гемцитабин, гидроксикарбамид, идарубицин, ифосфамид, иринотекан, лейковорин, липосомальный доксорубицин, липосомальный даунорубицин, ломустин, мелфалан, меркаптопурин, месну, метотрексат, митомицин, митоксантрон, оксалиплатин, паклитаксел, пеметрексед, пентостатин, прокарбазин, ралтитрексид, сатраплатин, стрептозоцин, тегафур–урацил, темозоломид, тенипозид, тиотепу, тиогуанин, топотекан, треосульфан, винбластин, винкристин, виндезин, винорелбин или их комбинацию. Иллюстративные проапоптические агенты включают в себя, но не ограничиваясь ими, флударабин, стауроспорин, циклогексимид, актиномицин D, лактозилкерамид, 15d–PGJ(2) и их комбинации.
B. Другие иммуномодуляторы
1. Антагонисты PD–1
В некоторых вариантах осуществления молекулы, связывающие SIGLEC–15 и связывающие лиганд SIGLEC–15, вводят совместно с антагонистом PD–1. Белок программируемой смерти–1 (PD–1) представляет собой члена семейства рецепторов CD28, который доставляет отрицательный иммунный ответ при индуцировании на T–клетках. Контакт между PD–1 и одним из его лигандом (B7–H1 или B7–DC) индуцирует ингибирующий ответ, который снижает T–клеточную мультипликацию и/или силу и/или длительность T–клеточного ответа. Подходящие антагонисты PD–1 описаны в патентах США №№8114845, 8609089 и 8709416, которые явно включены в данный документ посредством ссылки в полном объеме, и включают в себя соединения или агенты, которые как связываются с лигандом PD–1, так и блокируют его в целях нарушения или ингибирования связывания лиганда с рецептором PD–1, или связываются непосредственно с рецептором PD–1 и блокируют его, не индуцируя передачу ингибирующего сигнала через рецептор PD–1.
В некоторых вариантах осуществления антагонист рецептора PD–1 связывается непосредственно с рецептором PD–1, не вызывая передачу ингибирующего сигнала, и также связывается с лигандом рецептора PD–1 в целях ослабления или ингибирования передачи сигнала с помощью лиганда через рецептор PD–1. Благодаря снижению числа и/или содержания лигандов, которые связываются с рецептором PD–1 и вызывают передачу ингибирующего сигнала, меньше клеток ослабляется в результате отрицательного сигнала, доставляемого с помощью передачи сигнала с участием PD–1, и может быть достигнут более устойчивый иммунный ответ.
Считается, что передача сигнала с участием PD–1 регулируется с помощью связывания с лигандом PD–1 (таким как B7–H1 или B7–DC) в непосредственной близости к пептидному антигену, презентируемому главным комплексом гистосовместимости (MHC) (см., например, Freeman, Proc. Natl. Acad. Sci. U.S.A, 105:10275–10276 (2008)). Таким образом, белки, антитела или малые молекулы, которые предупреждают колигирование PD–1 и TCR на T–клеточной мембране также являются пригодными антагонистами PD–1.
В некоторых вариантах осуществления антагонисты рецептора PD–1 представляют собой низкомолекулярные антагонисты или антитела, которые ослабляют или нарушают передачу сигнала с участием рецептора PD–1 в результате связывания с лигандами PD–1 или с самим PD–1, особенно в случаях, если колигирование PD–1 с TCR не следует за таким связыванием, тем самым, не вызывая передачу ингибирующего сигнала через рецептор PD–1.
Другие антагонисты PD–1, предусмотренные способами данного изобретения, включают в себя антитела, которые связываются с PD–1 или лигандами PD–1 и другими антителами.
Подходящие анти–PD–1 антитела включают в себя, но не ограничиваясь ими, таковые, описанные в следующих патентах США: 7332582, 7488802, 7521051, 7524498, 7563869, 7981416, 8088905, 8287856, 8580247, 8728474, 8779105, 9067999, 9073994, 9084776, 9205148, 9358289, 9387247, 9492539, 9492540, все из которых включены посредством ссылки в полном объеме.
См. также Berger et al., Clin. Cancer Res., 14:30443051 (2008).
Иллюстративные анти–B7–H1 (также называемые анти–PD–L1) антитела включают в себя, но не ограничиваясь ими, таковые, описанные в следующих патентах США: 8383796, 9102725, 9273135, 9393301 и 9580507, все из которых явно включены в данный документ посредством ссылки в полном объеме.
В отношении анти–B7–DC (также называемых анти–PD–L2) антитела см. патенты США №№: 7411051, 7052694, 7390888, 8188238 и 9255147, все из которых явно включены в данный документ посредством ссылки в полном объеме.
Другие иллюстративные антагонисты рецептора PD–1 включают в себя, но не ограничиваясь ими, полипептиды B7–DC, в том числе гомологи и варианты таковых, а также активные фрагменты любого из вышеуказанных и слитые белки, которые включают любой из них. В некоторых вариантах осуществления слитые белки включают в себя растворенный участок B7–DC, связанный с Fc–участком антитела, такого как IgG человека, и не включает все или часть из трансмембранного участка B7–DC человека.
Антагонист PD–1 также может представлять собой фрагмент B7–H1 млекопитающего, например, от мыши или примата, такого как человека, при этом фрагмент связывается с PD–1 и блокирует его, но не приводит к передаче ингибирующего сигнала через PD–1. Фрагменты также могут представлять собой часть слитого белка, например, слитого белка Ig.
Другие пригодные полипептиды–антагонисты PD–1 включают в себя таковые, которые связываются с лигандами рецептора PD–1. Они включают в себя рецепторный белок PD–1 или их растворенные фрагменты, которые связываются с лигандами PD–1, такими как B7–H1 или B7–DC, и предупреждают связывание с эндогенным рецептором PD–1, тем самым предупреждая передачу ингибирующего сигнала. Также было показано, что B7–H1 связывается с белком B7.1 (Butte et al., Immunity, Vol. 27, pp. 111–122, (2007)). Такие фрагменты также включают в себя растворенную часть ECD белка PD–1, который содержит мутации, такие как мутация A99L, которая повышает связывание с природными лигандами (Molnar et al., PNAS, 105:10483–10488 (2008)). B7–1 или его растворенные фрагменты, которые связываются с лигандом B7–H1 и предупреждают связывание с эндогенным рецептором PD–1, тем самым предупреждая передачу ингибирующего сигнала, также являются пригодными.
Антисмысловые нуклеиновые кислоты PD–1 и B7–H1, как ДНК, так и РНК, а также молекулы миРНК, также могут представлять собой антагонисты PD–1. Такие антисмысловые молекулы предупреждают экспрессию PD–1 на T–клетках, а также продуцирование T–клеточных лигандов, таких как B7–H1, PD–L1 и/или PD–L2. Например, миРНК (например, около 21 нуклеотида в длину, которая является специфичной в отношении гена, кодирующего PD–1 или кодирующего лиганд PD–1, и олигонуклеотиды которой можно легко приобрести коммерчески), образующие комплексы с носителями, такими как полиэтиленимин (см. Cubillos–Ruiz et al., J. Clin. Invest. 119(8): 2231–2244 (2009), легко захватывается клетками, которые экспрессируют PD–1, а также лиганды PD–1, и ослабляют экспрессию этих рецепторов и лигандов в целях достижения снижения передачи ингибирующего сигнала в T–клетках, тем самым, активируя T–клетки.
2. Антагонисты CTLA4
Другие молекулы, пригодные в опосредовании эффектов T–клеток в иммунном ответе, также предусмотрены в качестве дополнительных терапевтических агентов. В некоторых вариантах осуществления молекула представляет собой антагонист CTLA4, например, антагонистическое анти–CTLA4 антитело. Пример анти–CTLA4 антитела для применения в способах данного изобретения включает в себя антитело, описанное в PCT/US2006/043690 (Fischkoff et al., WO/2007/056539).
Дозы анти–PD–1, анти–B7–H1 и анти–CTLA4 антитела известны в данной области техники и могут находиться в диапазоне, например, от 0,1 до 100 мг/кг или в более коротких диапазонах от 1 до 50 мг/кг или от 10 до 20 мг/кг. Подходящая доза для субъекта–человека может составлять от 5 до 15 мг/кг, при этом 10 мг/кг антитела (например, человеческого анти–PD–1 антитела) представляет собой конкретный вариант осуществления.
Конкретные примеры анти–CTLA4 антитела, пригодного в способах данного изобретения, представляют собой ипилимумаб, человеческое анти–CTLA4 антитело, вводимое в дозе, например, около 10 мг/кг, и тремелимумуб, человеческое анти–CTLA4 антитело, вводимое в дозе, например, около 15 мг/кг. См. также Sammartino, et al., Clinical Kidney Journal, 3(2):135–137 (2010), опубликованную он–лайн в декабре 2009 г.
В других вариантах осуществления антагонист представляет собой малую молекулу. Было показано, что ряд малых органических молекул связывается с лигандом B7–1 с предупреждением связывания с CTLA4 (см. Erbe et al., J. Biol. Chem., 277:7363–7368 (2002). Такие малые органические молекулы можно вводить в отдельности или совместно с анти–CTLA4 антителом в целях ослабления передачи ингибирующего сигнала T–клеток.
3. Потенциирующие агенты
В некоторых вариантах осуществления дополнительные терапевтические агенты включают в себя потенциирующий агент. Потенциирующий агент действует в целях повышения эффективности положительного регулятора иммунного ответа, возможно, в результате более одного механизма, несмотря на то, что точный механизм действия не является обязательным для широкого практического применения данного изобретения.
В некоторых вариантах осуществления потенциирующий агент представляет собой циклофосфамид. Циклофосфамид (CTX, Cytoxan® или Neosar®) представляет собой оксазофосфориновый лекарственный препарат, а аналоги включают в себя ифосфамид (IFO, ифекс), перфосфамид, трофосфамид (трофосфамид; иксотен) и фармацевтически приемлемые соли, сольваты, пролекарственные препараты и их метаболиты (заявка на патент США 20070202077, которая включена в полном объеме). Ифосфамид (MITOXANA®) представляет собой структурный аналог циклофосфамида и считается, что его механизм действия является идентичным или по сути аналогичным таковому циклофосфамида. Перфосфамид (4–гидропероксициклофосфамид) и трофосфамид также представляют собой алкилирующие агенты, которые являются структурно связанными с циклофосфамидом. Например, перфосфамид алкилирует ДНК, тем самым ингибируя репликацию ДНК и синтез РНК и белков. Новые оксазофосфориновые производные были разработаны и оценены в целях повышения избирательности и ответа при пониженной токсичности для хозяина (Liang J, Huang M, Duan W, Yu XQ, Zhou S. Design of new oxazaphosphorine anticancer drugs. Curr Pharm Des. 2007;13(9):963–78. Review). Они включают в себя мафосфамид (NSC 345842), глуфосфамад (D19575, бета–D–глюкозилфосфорамидиприт), S–(–)–бромфосфамид (CBM–11), NSC 612567 (алдофосфамид пергидротиазин) и NSC 613060 (алдофосфамид тиазолидин). Мафосфамид представляет собой оксазофосфориновый аналог, который представляет собой химически стабильную соль 4–тиоэтансульфоновой кислоты 4–гидрокси–CPA. Глюфосфамид представляет собой производное IFO, в котором изофосфорамидиприт, алкилирующий метаболит IFO, гликозидически связан с молекулой бета–D–глюкозы. Дополнительные циклофосфамидные аналоги описаны в патенте США 5190929 под названием «Циклофосфамидные аналоги, пригодные в качестве противоопухолевых агентов», который включен в данный документ посредством ссылки в полном объеме.
Несмотря на то, что сам по себе CTX является нетоксичным, некоторые из его метаболитов представляют собой цитотоксические алкилирующие агенты, которые вызывают сшивание ДНК, а в более высоких дозах разрывы нитей. Многие клетки являются устойчивыми к CTX, поскольку они экспрессируют высокие уровни детоксифицирующего фермента альдегиддегидрогеназы (ALDH). CTX нацеливается на пролиферирующие лимфоциты, поскольку лимфоциты (но не гепатопоэтический стволовые клетки) экспрессируют лишь незначительные уровни ALDH, а делящиеся клетки являются наиболее чувствительными к агентам алкилирования ДНК.
Низкие дозы CTX (<200 мг/кг) могут оказывать иммуностимулирующие эффекты, в том числе стимуляцию противоопухолевых иммунных ответов у человека и в мышиных моделях рака (Brode & Cooke Crit Rev. Immunol. 28:109–126 (2008)). Такие низкие дозы явяются субтерапевтическими и не имеют прямой противоопухолевой активности. В отличие от этого, высокие дозы CTX ингибируют противоопухолевый ответ. Несколько механизмов могут объяснять роль CTX в потенциации противоопухолевого иммунного ответа: (a) истощение CD4+CD25+FoxP3+ Treg (и, в частности, пролиферирующих Treg, которые могут быть особенно супрессивными), (b) истощение B–лимфоцитов; (c) индукция оксида нитрита (NO), приводящая к супрессии роста опухолевых клеток; (d) мобилизация и экспансия CD11b+Gr–1+ MDSC. Эти первичные эффекты оказывают многочисленные вторичные эффекты; например, после истощения Treg макрофаги продуцируют больше IFN–γ и меньше IL–10. Также было показано, что CTX индуцирует экспрессию IFN I типа и активирует гомеостатическую пролиферацию лимфоцитов.
Истощение Treg наиболее часто указывается в качестве механизма, с помощью которого CTX потенциирует противоопухолевый ответ. Это заключение основано отчасти на результатах экспериментов по адаптивному переносу. В опухолевой модели AB1–HA обработка CTX на сутки 9 приводит к 75% уровню излечения. Перенос очищенных Treg на сутки 12 почти полностью ингибировал ответ со стороны CTX (van der Most et al. Cancer Immunol. Immunother. 58:1219–1228 (2009). Аналогичный результат наблюдали в опухолевой модели HHD2: адаптивный перенос CD4+CD25+ Treg после предварительной обработки CTX устранял терапевтический ответ на вакцину (Taieb, J. J. Immunol. 176:2722–2729 (2006)).
Многочисленные клинические исследования у человека продемонстрировали, что низкодозный CTX является безопасный, хорошо переносимым и эффективным агентом для активации противоопухолевых ответов (Bas, & Mastrangelo Cancer Immunol. Immunother. 47:1–12 (1998)).
Оптимальная доза CTX для потенциирования противоопухолевого иммунного ответа представляет собой таковую, которая снижает общее количество T–клеток в результате снижения уровней Treg ниже нормального диапазона, но который остается субтерапевтическим (см. Machiels et al. Cancer Res. 61:3689–3697 (2001)).
В клинических исследованиях у человека, в которых был использован CTX в качестве иммунопотенциирующего агента, обычно использовали дозу 300 мг/м2. В случае среднего мужчины (6 футов (182 см), 170 фунтов (78 кг) с площадью поверхности тела 1,98 м2), 300 мг/м2 составляет 8 мг/кг или 624 мг от общего белка. В мышиных моделях рака эффективность была показана при дозах, находящихся в диапазоне 15–150 мг/кг, что соответствует 0,45–4,5 мг от общего белка у мыши весом 30 г (Machiels et al. Cancer Res. 61:3689–3697 (2001), Hengst et al Cancer Res. 41:2163–2167 (1981), Hengst Cancer Res. 40:2135–2141 (1980)).
В случае более крупных млекопитающих, таких как примат, таких как пациент–человек, могут быть использованы такие дозы в мг/м2, однако также могут быть использованы однократные дозы в течение конечного периода времени. Такие однократные дозы можно вводить на ежедневной основе в течение конечного периода времени, такого как до 3 дней, или до 5 дней, или до 7 дней, или до 10 дней, или до 15 дней или до 20 дней или до 25 дней, все они явно предусмотрены данным изобретением. Та же самая схема может быть использована в отношении других потенциирующих агентов, упомянутых в данном документе.
В других вариантах осуществления потенциирующий агент представляет собой агент, который снижает активность и/или число регуляторных T–лимфоцитов (T–reg), таких как синитиниб (SUTENT®), анти–TGFβ антитело или иматиниб (GLEEVAC®). Упомянутая схема лечения может также включать в себя введение адъюванта.
Пригодные потенциирующие агенты также включают ингибиторы митоза, такие как паклитаксол, ингибиторы ароматазы (например, летрозол) и ингибиторы ангиогенеза (ингибиторы VEGF, например, авастин, VEGF–Trap) (см., например, Li et al., Clin Cancer Res. 2006 Nov 15; 12(22):6808–16.), антрациклины, оксалиплатин, доксорубицин, антагонисты TLR4 и антагонисты IL–18.
C. Противомикробные препараты
В одном варианте осуществления молекулы, связывающие SIGLEC–15 и связывающие лиганд SIGLEC–15, могут быть использованы в превентивной или профилактической роли в лечении и предупреждении заболевания, как описано в данном документе, а также в контексте тяжелых травматических повреждений, таких как большой ожог, открытый перелом, случайная ампутация или другие раны. Таким образом, молекулы, связывающие SIGLEC–15 или связывающие лиганд SIGLEC–15, можно вводить субъекту в комбинации с противомикробным препаратом, таким как антибиотик, противогрибковый препарат, противовирусный препарат, противопаразитарный препарат или эфирное масло.
В некоторых вариантах осуществления субъекту вводят молекулы, связывающие SIGLEC–15, и/или противомикробный препарат во время приема в больницу в целях предупреждения последующих бактериальных, грибковых или вирусных осложнений. Антибиотик может нацеливаться на патогены, а молекулы, связывающие SIGLEC–15 или связывающие лиганд SIGLEC–15, могут стимулировать иммунную систему обеспечивать усиленный ответ на лечение или предупреждать последующую инфекцию или заболевание.
D. Иммуносупрессивные агенты
В некоторых вариантах осуществления иммунный ответ или воспалительное/аутоиммунное заболевание/нарушение лечат с помощью введения субъекту молекулы, связывающей SIGLEC–15 или связывающей лиганд SIGLEC–15, и второго агента, которые представляет собой иммуносупрессор. Иммуносупрессивные агенты включают в себя, но не ограничиваясь ими, антитела против других лимфоцитарных поверхностных маркеров (например, CD40, альфа–4 интегрина) или против цитокинов, слитые белки (например, CTLA–4–Ig (Orencia®), TNFR–Ig (Enbrel®)), блокаторы TNF–α, такие как энбрел, ремикейд, цимзия и хумира, циклофосфамид (CTX) (например, Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune™), метотрексат (MTX) (например, Rheumatrex®, Trexall®), белимумаб (например, Benlysta®) или другие иммуносупрессивные препараты (например, циклоспорин A, FK506–подобные соединения, рапамициновые соединения или стероиды), антипролиферативные препараты, цитотоксические агенты или другие соединения, которые могут содействовать иммуносупрессии.
Терапевтический агент может представлять собой слитый белок CTLA–4, такой как CTLA–4–Ig (абатацепт). Слитые белки CTLA–4–Ig конкурируют с костимулирующим рецептором, CD28, на T–клетках за связывание с CD80/CD86 (B7–1/B7–2) на антигенпрезентирующих клетках, и, тем самым, функционируют таким образом, чтобы ингибировать T–клеточную активность. В другом варианте осуществления терапевтический агент представляет собой слитый белок CTLA–4–Ig, известный как белатацепт. Белатацепт содержит две аминокислотные замены (L104E и A29Y), которые значительным образом повышают его авидность в отношении CD86 in vivo. В другом варианте осуществления терапевтический агент представляет собой Maxy–4.
В другом варианте осуществления терапевтический агент представляет собой циклофосфамид (CTX). Циклофосфамид (генерическое название Endoxan®, Cytoxan®, Neosar®, Procytox®, Revimmune™), также известный как цитофосфан, представляет собой алкилирующий агент на основе азотистого иприта из группы оксазофоринов. Он используется для лечения различных типов рака и некоторых аутоиммунных нарушений. Циклофосфамид (CTX) представляет собой основной лекарственный препарат, используемый для лечения диффузного пролиферативного гломерулонефрита у пациентов с почечной волчанкой.
Терапевтический агент можно вводить в эффективном количестве для снижения уровней анти–двунитевая ДНК антител (анти–ds DNA) в крови и сыворотке крови и/или снижения протеинурии у пациента, нуждающегося в этом.
В другом варианте осуществления терапевтический агент повышает количество аденозина в сыворотке крови, см., например, WO 08/147482. Например, второй терапевтический агент может представлять собой CD73–Ig, рекомбинантный CD73 или другой агент (например, цитокин или моноклональное антитело или малую молекулу), который повышает экспрессию CD73, см., например, WO 04/084933. В другом варианте осуществления терапевтический агент представляет собой интерферон–бета.
Терапевтический агент может представлять собой тизабри или другой лекарственный препарат для лечения MS. В другом варианте осуществления второй терапевтический агент предпочтительно лечит хроническое воспаление, при этом схема лечения нацелена как на острое, так и хроническое воспаление. В предпочтительном варианте осуществления второй терапевтический препарат представляет собой блокатор TNF–α.
Терапевтический агент может представлять собой молекулу, которая ингибирует или ослабляет дифференцировку, пролиферацию, активность и/или продуцирование и/или секрецию цитокинов Th1, Th17, Th22, и/или другими клетками, которые секретируют или заставляют другие клетки секретировать воспалительные молекулы, в том числе, но не ограничиваясь ими, IL–1β, TNF–α, IFN–γ, IL–18 IL–17, IL–6, IL–23, IL–22, IL–21 и MMP. В другом варианте осуществления терапевтический агент представляет собой малую молекулу, которая взаимодействует с Treg, усиливает активность Treg, активируют или усиливает секрецию IL–10 Treg, повышает число Treg, повышает супрессивную способность Treg или их комбинации.
В некоторых вариантах осуществления композиция повышает активность или продуцирование Treg. Иллюстративные агенты, усиливающие Treg, включают, но не ограничиваясь ими, глюкокортикоид флутиказон, сальметерол, антитела против IL–12, IFN–γ и IL–4; витамин D3 и дексаметазон и их комбинации.
В некоторых вариантах осуществления терапевтический агент представляет собой антитело, например, функциональное блокирующее антитело против провоспалительной молекулы, такой как IL–6, IL–23, IL–22 или IL–21.
Используемый в данном документе термин «рапамициновое соединение» включает в себя нейтральное трициклическое соединение рапамицин, производные рапамицина, аналоги рапамицина и другие макролидные соединения, которые, как предполагается, имеют тот же самый механизм действия, что и рапамицин (например, ингибирование функции цитокинов). Выражение «рапамициновые соединения» включает в себя соединения, со структурным сходством в отношении рапамицина, например, соединения с аналогичной макроциклической структурой, которые были модифицированы в целях усиления терапевтической эффективности. Иллюстративные рапамициновые соединения известны в данной области техники (см., например, WO95122972, WO 95116691, WO 95104738, патент США №6015809; 5989591; патент США №5567709; 5559112; 5530006; 5484790; 5385908; 5202332; 5162333; 5780462; 5120727).
Выражение «FK506–подобные соединения» включает в себя FK506 и производные и аналоги FK506, например, соединения со структурным сходством в отношении FK506, например, соединения с аналогичной макроциклической структурой, которые были модифицированы в целях усиления терапевтической эффективности. Примеры FK506–подобных соединений включают в себя, например, таковые, описанные в WO 00101385. Предпочтительно, выражение «рапамициновое соединение», используемое в данном документе, не включает в себя FK506–подобные соединения.
E. Противовоспалительные препараты
Другие подходящие терапевтические агенты включают в себя, но не ограничиваясь ими, противовоспалительные агенты. Противовоспалительный агент может быть стероидным, нестероидным или их комбинацией. В одном варианте осуществления предложены композиции для перорального применения, содержащие от около 1% (вес/вес) до около 5% (вес/вес), в типичном случае около 2,5% (вес/вес) противовоспалительного агента. Иллюстративные примеры нестероидных противовоспалительных агентов включают в себя, но не ограничиваясь ими, оксикамы, такие как пироксикам, изоксикам, теноксикам, судоксикам; салицилаты, такие как аспирин, дисалцид, бенорилат, трилизат, сафаприн, солприн, дифлунизал и фендозал; производные уксусной кислоты, такие как диклофенак, фенклофенак, индометацин, сулиндак, толметин, изоксепак, фурофенак, тиопинак, зидометацин, ацематацин, фентиазак, зомепирак, клинданак, оксепинак, фелбинак и кеторолак; фенаматы, такие как мефенамовая, меклофенамовая, флуфенамовая, нифлуминовая и толфенамовая кислоты; производные пропионовой кислоты, такие как ибупрофен, напроксен, беноксапрофен, флурбипрофен, кетопрофен, фенопрофен, фенбуфен, индопрофен, пирпрофен, карпрофен, оксапрозин, пранопрофен, миропрофен, тиоксапрофен, супрофен, алминопрофен и тиапрофен; пиразолы, такие как фенилбутазон, оксифенбутазон, фепразон, азапропазон и триметазон. Также могут быть использованы смеси этих нестероидных противовоспалительных агентов.
Иллюстративные примеры стероидных противовоспалительных препаратов включают, но не ограничиваясь ими, кортикостероиды, такие как гидрокортизон, гидроксилтриамцинолон, альфа–метилдексаметазон, дексаметазона фосфат, беклометазона дипропионаты, клобетазола валерат, дезодин, дезоксиметазон, дезоксикортикостерона ацетат, дексаметазон, дихлоризон, дифлоразона диацетат, дифлукортолона валерат, флуадренолон, флуклоролона ацетонид, флудрокортизон, флуметазона пивалат, флуозинолона ацетонид, флуоцинонид, флукортина бутилэстеразы, флуокортолон, флупреднидена (флупреднилидена) ацетат, флурандренолон, галцинонид, гидрокортизона ацетат, гидрокортизона бутират, метилпреднизолон, триамцинолона ацетонид, кортизон, кортодоксон, флуцетонид, флудрокортизон, дифлуорозона диацетат, флурадренолон, флудрокортизон, дифлурозона диацетат, флурадренолона ацетонид, медризон, амцинафел, амцинамид, бетаметазон и сумма его сложных эфиров, хлорпреднизон, хлорпреднизона ацетат, клокортелон, клесинолон, дихлоризон, дифлурпреднат, флуклоронид, флунизолид, флуорометалон, флуперолон, флупреднизолон, гидрокортизона валерат, гидрокортизона циклопентилпропионат, мепреднизон, параметазон, преднизолон, преднизон, беклометазона дипропионат, триамцинолон и их смеси.
V. Способы диагностики
Молекулы, связывающие SIGLEC–15, в частности, антитела и их антигенсвязывающие фрагменты, могут быть использованы для диагностических целей, например, для выявления, диагностики или контроля заболеваний, нарушений или инфекций, ассоциированных с экспрессией SIGLEC–15, или для определения или содействия в определении или идентификации подходящих популяций или профилей пациентов. Любой из способов может сочетаться со способом лечения субъекта, например, с помощью введения субъекту эффективного количества одного или нескольких терапевтических молекул, связывающих SIGLEC–15.
Выявление или диагностика заболевания, нарушения или инфекции, в том числе, но не ограничиваясь этим, рака, может включать в себя: (a) анализ экспрессии SIGLEC–15 или его производных в клетках, сыворотке крови, плазме крови, крови или в образце ткани (например, опухолевом образце) субъекта с помощью одного или нескольких антител (или их фрагментов), которые иммуноспецифично связываются с такими антигенами; и (b) сравнение уровня антигена с контрольным уровнем, например, уровнями в образцах нормальных тканей, при этом повышение анализируемого уровня антигена по сравнению с контрольным уровнем антигена свидетельствует о заболевании, нарушении или инфекции. Такие антитела и фрагменты предпочтительно могут быть использованы в иммунологических анализах, таких как иммуноферментный анализ (ИФА), радиоиммунологический анализ (RIA) и проточная цитометрия (FACS).
В некоторых вариантах осуществления антитела или их фрагменты используются для анализа IHC в клетках образца ткани in vitro или in situ или in vivo. Таким образом, антитела и фрагменты можно использовать при выявлении и диагностике заболевания, нарушения или инфекции у человека. В одном варианте осуществления такая диагностика включает в себя: a) введение субъекту (например, парентерально, подкожно или интраперитонеально) эффективного количества такого меченого антитела или антигенсвязывающего фрагмента; b) ожидание в течение периода времени после введения, необходимого для обеспечения предпочтительного концентрирования меченой молекулы в участках у субъекта, где экспрессируется SIGLEC–15 (и в случае несвязанной меченой молекулы восстановления к исходному уровню); c) определение исходного уровня; и d) детекция меченого антитела у субъекта таким образом, что локализованная детекция меченого антитела выше или ниже исходного уровня свидетельствует о том, что субъект имеет заболевание, нарушение или инфекцию, и показывает положение и относительную уровень экспрессии SIGLEC–15+ ткани. В соответствии с этим вариантом осуществления антитело может быть помечено визуализирующим фрагментом, который является детектируемым in vivo с помощью системы визуализации, известной специалисту в данной области техники. Исходный уровень может быть определен с помощью различных способов, в том числе сравнения количества детектируемой меченой молекулы со стандартным значением, ранее определенным для конкретной системы.
Другие способы включают, например, контроль прогрессирования заболевания, нарушения или инфекции в результате (a) анализа экспрессии SIGLEC–15 в клетках или в образце ткани субъекта, полученных в первой временной точке и более поздней временной точке с помощью молекулы, связывающей SIGLEC–15; и (b) сравнения уровня экспрессии SIGLEC–15 в клетках или в образце ткани субъекта в первой и более поздних временных точках, при этом повышение анализируемого уровня SIGLEC–15 в более поздней временной точке по сравнению с первой временной точкой указывает на прогрессирование заболевания, нарушения или инфекции.
Способ контроля ответа на лечение может включать (a) анализ экспрессии SIGLEC–15 в клетках или в образце ткани субъекта до и после лечения с помощью молекулы, связывающей SIGLEC–15; и (b) сравнение уровня SIGLEC–15 в динамике, при этом снижение анализируемого уровня SIGLEC–15 после лечения по сравнению с уровнем SIGLEC–15 до лечения указывает на благоприятный ответ на лечение.
Специалисту в данной области техники будет понятно, что размер субъекта и используемая система визуализации будут определять количество визуализационного фрагмента, необходимого для получения диагностических изображений.
В зависимости от нескольких переменных, в том числе типа используемой метки и способа введения, период времени после введения, необходимый для обеспечения предпочтительного концентрирования меченой молекулы в участках у субъекта, и для восстановления несвязанной меченой молекулы к исходному уровню, составляет от 6 до 48 часов или от 6 до 24 часов или от 6 до 12 часов. В другом варианте осуществления период времени после введения составляет от 5 до 20 дней или от 5 до 10 дней.
В одном варианте осуществления контроль заболевания, нарушения или инфекции проводят путем повторения способа диагностики заболевания, нарушения или инфекции, например, через один месяц после первоначального диагноза, через шесть месяцев после первоначального диагноза, через один год после первоначального диагноза и т.д.
Наличие меченой молекулы у субъекта можно выявить с помощью способов, известных в данной области техники для визуализации in vivo. Эти способы зависят от типа используемой метки. Специалисты в данной области техники смогут определить соответствующий способ детекции конкретной метки. Способы и изделия, которые могут быть использованы в способах диагностики, включают, но не ограничиваясь ими, компьютерную томографию (КТ), полноразмерную визуализацию, такую как позитрон–эмиссионную томографию (ПЭТ), магнитно–резонансную томографию (МРТ) и сонографию.
В конкретном варианте осуществления молекулу метят радиоизотопом и выявляют у пациента с помощью чувствительного к излучению хирургического инструмента (Thurston et al., патент США №5441050). В другом варианте осуществления молекулу метят флуоресцентным соединением и выявляют у пациента с помощью чувствительного к флуоресценции сканирующего инструмента. В другом варианте осуществления молекулу метят позитрон–эмиссионным металлом и выявляют у пациента с помощью позитрон–эмиссионной томографии. В еще одном варианте осуществления молекулу метят парамагнитной меткой и выявляют у пациента с помощью магнитно–резонансной томографии (МРТ).
VI. Наборы
Раскрываемые молекулы, связывающие SIGLEC–15, или связывающие лиганд SIGLEC–15, могут быть упакованы в герметичный контейнер, такой как ампула или саше, с указанием количества. Молекулы могут поставляться в виде сухого стерилизованного лиофилизированного порошка или безводного концентрата в герметичном контейнере и могут быть разведены, например, водой или физиологическим раствором до соответствующей концентрации для введения субъекту. Например, молекулы могут поставляться в виде сухого стерильного лиофилизированного порошка в герметическом контейнере в лекарственной форме по меньшей мере 5 мг, или по меньшей мере 10 мг, по меньшей мере 15 мг, по меньшей мере 25 мг, по меньшей мере 35 мг, по меньшей мере 45 мг, по меньшей мере 50 мг или по меньшей мере 75 мг. Лиофилизированные молекулы могут храниться при температуре от 2 до 8°C в своем исходном контейнере и в типичном случае вводятся в течение 12 часов или в течение 6 часов или в течение 5 часов или в течение 3 часов или в течение 1 часа после разведения.
В альтернативном варианте осуществления молекулы поставляются в жидкой форме в герметичном контейнере с указанием количества и концентрации. В некоторых вариантах осуществления жидкая форма молекул поставляется в герметичном контейнере, содержащем по меньшей мере 1 мг/мл или по меньшей мере 2,5 мг/мл, по меньшей мере 5 мг/мл, по меньшей мере 8 мг/мл, по меньшей мере 10 мг/мл, по меньшей мере 15 мг/мл, по меньшей мере 25 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 150 мг/мл, по меньшей мере 200 мг/мл молекул.
Также предложены фармацевтические упаковки и наборы, содержащие один или несколько контейнеров, наполненных молекулами, связывающими SIGLEC–15, или связывающими лиганд SIGLEC–15. Кроме того, один или несколько других профилактических или терапевтических агентов, пригодных для лечения заболевания, также могут быть включены в фармацевтическую упаковку или или набор. Фармацевтическая упаковка или набор также может содержать один или несколько контейнеров, наполненных одним или несколькими из компонентов раскрываемых фармацевтических композиций. Необязательно вместе с таким контейнером(контейнерами) может находиться уведомление в форме, предписанной государственным органом, регулирующим производство, применение или продажу фармацевтических препаратов или биологических продуктов, при этом уведомление указывает на разрешение органом производства, применения или продажи для введения человеком.
Также предложены наборы, разработанные для вышеописанных способов. Варианты осуществления в типичном случае включают в себя одну или несколько молекул, связывающих SIGLEC–15, или связывающих лиганд SIGLEC–15. В конкретных вариантах осуществления набор также содержит один или несколько других профилактических или терапевтических агентов, пригодных для лечения рака, в одном или нескольких контейнерах.
Примеры
Пример 1: Анти–SIGLEC–15 антитела и последовательности их тяжелых и легких цепей
Материалы и методы
Мышиные анти–человеческий SIGLEC–15 моноклональные антитела
Мышей с нокаутом по SIGLEC–15 (n=2) иммунизировали hS15.mIg (внеклеточным доменом SIGLEC–15 человека [ECD], слитым с IgG2a мыши), эмульгированным с CFA (полным адъювантом Фрейнда). Мыши также получали инъекцию GM–CSF и анти–CD40 антитела. Через 2 недели мышей также стимулировали тем же самым иммуногеном. Титр антисыворотки анализировали с помощью исследования сыворотки, собранной при кровотечении при надрезе хвоста в планшет для ИФА, покрытый hS15.hIg (ECD SIGLEC 15 человека, слитым с IgG1 человека) при различном разведении, от 1:1000 до 1:100000000. На Фиг. 1 изображено, что анти–hS15 антитела детектировали при разведении >1:100000. Через две недели мыши получали 3–ю дозу антигена. Через три дня после окончательной стимуляции спленоциты мышей собирали и ресуспендировали в RPMI с добавлением 10% FBS и глутамина, а позже сливали с образованием гибридом.
Электрослияние спленоцитов с нокаутом по SIGLEC–15 (S15 KO)
Слитые клетки высевали в метилцеллюлозный гель/среду; в слитом состоянии клетки криоконсерваровали и их можно было размораживать для другой партии клонирования.
Единичные клоны отбирали и помещали в 10×96–луночных планшетов (960 клонов).
Через 2 недели собирали супернатант.
RACE
Идентификацию RACE (быстую амплификацию концов кДНК) тяжелой и легкой цепей осуществляли в соответствии со следующим протоколом: (1) денатурация мРНК, (2) синтез кДНК, (3) реакция 5’RACE, (4) анализ результатов ПЦР (на агарозном геле для визуализации амплифицированного фрагмента ДНК – соответствующие фрагменты ДНК вариабельного участка антитела должны иметь размер 500–700 пар оснований, (5) клонированис с помощью TOPO ПЦР–позитивных полос; (6) ПЦР–амплификация клонов TOPO с последующим гель–электрофорезом и извлечением из агарозного геля, (7) сиквенирование в целом 218 клонов, (8) проведение анализа CDR с помощью данных о сиквенировании (участки CDR определяли с помощью VBASE2, доступной через vbase2.org).
Результаты
Антитела противлонировали с помощью методов RACE. После сиквенирования 218 клонированных фрагментов ДНК с помощью анализа последовательности антител идентифицировали одну тяжелую цепь и одну легкую цепь для 24 образцов антител, называемых в данном документе 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9, 6A, 28A, 63A, 71A, 77A, 80A, 82B, 83B, 92A, 93B, 99B, 104B и 105A. Последовательности представлены ниже и выше. Последовательности тяжелых и легких цепей и CDR представлены выше, ниже и изображены на Фиг. 2A–3C.
ПОСЛЕДОВАТЕЛЬНОСТИ 1B2:
Аминокислотная последовательность VL 1B2 в формате FASTA
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPWTFGGGTKLEIK (SEQ ID NO:3)
Нуклеотидная последовательность VL 1B2 в формате FASTA
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGCATTGTACATAGTAATGGAAACACCTATTTAGAATGGTACCTGCAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGTGGACGTTCGGTGGAGGCACCAAGCTGGAAATCAAG (SEQ ID NO:74)
Аминокислотная последовательность VH 1B2 в формате FASTA
EVQLVESGGGFVKPGGSLKLSCAASGFTFSDYGMHWVRQAPEKGLEWVAYISSGSSIIY YADTVKGRFTISRDNAKNTLFLQMTSLRSEDTAMYYCARDHYHGNGSDYWGQGTTLTVSS (SEQ ID NO:13)
Нуклеотидная последовательность VH 1B2 в формате FASTA
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTCGTGAAGCCTGGAGGGTCCCTGAAACTCTCCTGTGCAGCCTCTGGATTCACTTTCAGTGACTATGGAATGCACTGGGTTCGTCAGGCTCCAGAGAAGGGGCTGGAGTGGGTTGCATACATTAGTAGTGGCAGTAGTATCATCTACTATGCAGACACAGTGAAGGGCCGATTCACCATCTCCAGAGACAATGCCAAGAACACCCTGTTCCTGCAAATGACCAGTCTGAGGTCTGAGGACACGGCCATGTATTACTGTGCAAGGGACCACTACCATGGTAACGGGTCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:85)
ПОСЛЕДОВАТЕЛЬНОСТИ 1C3:
Аминокислотная последовательность VL 1C3 в формате FASTA
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGFYYCMQHLEYPYTFGGGTRLEIK (SEQ ID NO:4)
Нуклеотидная последовательность VL 1C3 в формате FASTA
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATCCATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTATATTGGTTCCTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAGTCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGAGGCTGAGGATGTGGGTTTTTATTACTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGGGGGACCAGGCTGGAAATAAAA (SEQ ID NO:75)
Аминокислотная последовательность VH 1C3 в формате FASTA
QVQLKQSGAELVKPGASVKISCKASGYIFTDYYVNWVKQRPGQGLEWIGKIGPGSVSIY YNEKFKGKATLTADKSSSTAYMQLSSLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA (SEQ ID NO:14)
Нуклеотидная последовательность VH 1C3 в формате FASTA
CAGGTCCAGCTGAAGCAGTCTGGAGCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGATATCCTGCAAGGCTTCTGGCTACATCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCTGGACAGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGGAAGTGTTAGTATTTACTACAATGAGAAGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAGCTCAGCAGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGGTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:86)
ПОСЛЕДОВАТЕЛЬНОСТИ 1H3:
Аминокислотная последовательность VL 1H3 в формате FASTA
DIQMTQASSSLSVSLGGRVTITCKASDHINNWLAWYQQKPGNAPRLLISGATSLETGVP SRFSGSGSGKDYTLSITSLQTEDVATYYCQQYWSSPLTFGAGTKLELK (SEQ ID NO:5)
Нуклеотидная последовательность VL 1H3 в формате FASTA
GACATCCAGATGACACAGGCTTCATCCTCCTTGTCTGTATCTCTAGGAGGCAGAGTCACCATTACTTGCAAGGCAAGTGACCACATTAATAATTGGTTGGCCTGGTATCAGCAGAAACCAGGAAATGCTCCTAGGCTCTTAATATCTGGTGCAACCAGTTTGGAAACTGGGGTTCCTTCAAGATTCAGTGGCAGTGGATCTGGAAAGGATTACACTCTCAGCATTACCAGTCTTCAGACTGAAGATGTTGCTACTTATTACTGTCAACAGTATTGGAGTTCTCCTCTCACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:76)
Аминокислотная последовательность VH 1H3 в формате FASTA
QVQLKESGPGLVAPSQSLSITCTVSGFSLSNYGVHWVRQPPGKGLEWLVLIWSDGSTTY NSALKSRLSISKDNSKSQVFLKMNSLQTGDTAMYYCARHPYDDYSGYYYTMDYWGQGTSVTVSS (SEQ ID NO:15)
Нуклеотидная последовательность VH 1H3 в формате FASTA
CAGGTGCAGCTGAAGGAGTCAGGACCTGGCCTGGTGGCGCCCTCACAGAGCCTGTCCATCACATGCACCGTCTCAGGGTTCTCATTAAGCAATTATGGTGTACACTGGGTTCGCCAGCCTCCAGGAAAGGGTCTGGAGTGGCTGGTACTGATATGGAGTGATGGAAGCACAACCTATAATTCAGCTCTCAAATCCAGACTGAGCATCAGCAAGGACAACTCCAAGAGCCAAGTTTTCTTAAAAATGAACAGTCTCCAAACTGGTGACACAGCCATGTACTACTGTGCCAGACATCCCTATGATGATTATTCCGGCTATTACTATACTATGGACTACTGGGGTCAAGGAACCTCAGTCACCGTCTCCTCA (SEQ ID NO:87)
ПОСЛЕДОВАТЕЛЬНОСТИ 1C12:
Аминокислотная последовательность VL 1C12 в формате FASTA
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPWTFGGGTKLEIK (SEQ ID NO:3)
Нуклеотидная последовательность VL 1C12 в формате FASTA
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGCATTGTACATAGTAATGGAAACACCTATTTAGAATGGTACCTGCAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGTGGACGTTCGGTGGAGGCACCAAGCTGGAAATCAA (SEQ ID NO:77)
Аминокислотная последовательность VH 1C12 в формате FASTA
EVQLVESGGGLVKPGGSLKLSCAASGFSFSDYGMHWVRQAPEKGLEWVAYISSGSSILY YADIVKGRFTISRDNAKNTLFLQMTSLRSEDTAMYYCARDHYHGNGSDYWGQGTTLTVSS (SEQ ID NO:16)
Нуклеотидная последовательность VH 1C12 в формате FASTA
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCTTAGTGAAGCCTGGAGGGTCCCTGAAACTCTCCTGTGCAGCCTCTGGTTTCTCTTTCAGTGACTATGGAATGCACTGGGTTCGTCAGGCTCCAGAGAAGGGGCTGGAGTGGGTTGCATACATTAGTAGTGGCAGTAGTATCCTCTACTATGCAGACATAGTGAAGGGCCGATTCACCATCTCCAGAGACAATGCCAAGAACACCCTGTTCCTGCAAATGACCAGTCTGAGGTCTGAGGACACGGCCATGTATTACTGTGCAAGGGACCACTACCATGGTAACGGGTCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:88)
ПОСЛЕДОВАТЕЛЬНОСТИ 3H10:
Аминокислотная последовательность VL 3H10 в формате FASTA
QIILTQSPAIMSASPGEKVTMTCSASSSTSFMHWYQQKPGTSPKRWIFDTSKLASGVPG RFIGSGSGTSYSLTISTMEAEDAATYYCHQRSAYPWTFGGGTKLEIK (SEQ ID NO:6)
Нуклеотидная последовательность VL 3H10 в формате FASTA
CAAATTATTCTCACCCAGTCTCCAGCAATCATGTCTGCATCTCCAGGGGAGAAGGTCACCATGACCTGCAGTGCCAGCTCAAGTACAAGTTTCATGCACTGGTACCAGCAGAAGCCAGGCACCTCCCCCAAAAGATGGATTTTTGACACATCCAAACTGGCTTCTGGAGTCCCTGGTCGCTTCATTGGTAGTGGGTCTGGGACCTCTTATTCTCTCACAATCAGCACCATGGAGGCTGAAGATGCTGCCACTTATTACTGCCATCAGCGGAGTGCTTACCCATGGACGTTCGGTGGAGGCACCAAGCTGGAAATCAAA (SEQ ID NO:78)
Аминокислотная последовательность VH 3H10 в формате FASTA
EVQLQQSGAELVRPGASVKLSCTASGFNIKDYYMHWVKERPEQGLEWIGRIDPEDGDIE YDPKFQGKATMTADTSSNTAYLQFSSLTSEDTAVYYCVTDYDYDGGWFAYWGQGTLVTVSA (SEQ ID NO:17)
Нуклеотидная последовательность VH 3H10 в формате FASTA
GAGGTTCAGCTGCAGCAGTCTGGGGCAGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTTGTCCTGCACAGCTTCTGGCTTCAACATTAAAGACTACTATATGCACTGGGTGAAAGAGAGGCCTGAACAGGGCCTGGAGTGGATTGGAAGGATTGATCCTGAGGATGGTGATATTGAATATGACCCGAAGTTCCAGGGCAAGGCCACTATGACTGCAGATACATCCTCCAACACAGCCTACCTGCAGTTCAGCAGCCTGACATCTGAGGACACTGCCGTCTATTATTGTGTCACGGACTATGATTACGACGGAGGCTGGTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:89)
ПОСЛЕДОВАТЕЛЬНОСТИ 5G12:
Аминокислотная последовательность VL 5G12 в формате FASTA
DIKMTQSPSSMYASLGERVTITCKASQDINSYLSWFQQKPGKSPKTLIYRANRLVDGVP SRFSGSGSGQDYSLTISSLEYEDMGIYYCLQYDEFPYTFGGGTKLEIKR (SEQ ID NO:7)
Нуклеотидная последовательность VL 5G12 в формате FASTA
GACATCAAGATGACCCAGTCTCCATCTTCCATGTATGCATCTCTAGGAGAGAGAGTCACTATCACTTGCAAGGCGAGTCAGGACATTAATAGCTATTTAAGCTGGTTCCAGCAGAAACCAGGGAAATCTCCTAAGACCCTGATCTATCGTGCAAACAGATTGGTAGATGGGGTCCCATCAAGGTTCAGTGGCAGTGGATCTGGGCAAGATTATTCTCTCACCATCAGCAGCCTGGAGTATGAAGATATGGGAATTTATTATTGTCTACAGTATGATGAGTTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAAATAAAA (SEQ ID NO:79)
Аминокислотная последовательность VH 5G12 в формате FASTA
QVQLQQPGAELVKPGASVKMSCKASGYTFTSYWITWVIQRPGQGLEWIGDIYCGSDTMH YNEKFKNKATLTVDTSSSTAYMQLSSLTSEDSAVYYCARWWDYGSSYDYFDYWGQGTTLTVSS (SEQ ID NO:18)
Нуклеотидная последовательность VH 5G12 в формате FASTA
CAGGTCCAACTGCAGCAGCCTGGGGCTGAGCTTGTGAAGCCTGGGGCTTCAGTGAAGATGTCCTGCAAGGCTTCTGGCTACACCTTCACCAGCTACTGGATAACCTGGGTGATACAGAGGCCGGGACAAGGCCTTGAGTGGATTGGAGATATTTATTGTGGTAGTGATACTATGCACTACAATGAGAAGTTCAAGAACAAGGCCACACTGACTGTAGACACATCCTCCAGCACAGCCTACATGCAGCTCAGCAGCCTGACATCTGAGGACTCTGCGGTCTATTACTGTGCAAGATGGTGGGACTACGGTAGTAGCTACGACTACTTTGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:90)
ПОСЛЕДОВАТЕЛЬНОСТИ 6F8:
Аминокислотная последовательность VL 6F8 в формате FASTA
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGVYYCMQHLEYPYTFGGGTKLEIKR (SEQ ID NO:8)
Нуклеотидная последовательность VL 6F8 в формате FASTA
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATCCATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTGTATTGGTTCCTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAGTCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGAGGCTGAGGATGTGGGTGTTTATTATTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGGGGGACCAAGCTGGAAATAAAA (SEQ ID NO:80)
Аминокислотная последовательность VH 6F8 в формате FASTA
QVQLKQSGPELVRPGASVKISCEASGYTFTDYYVNWVKQRPGRGLEWIGKIGPGSVSIY YNEKFKDKATLTADKSSSTAYMQLSGLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA (SEQ ID NO:19)
Нуклеотидная последовательность VH 6F8 в формате FASTA
CAGGTCCAGCTGAAGCAGTCTGGACCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGATATCCTGCGAGGCTTCTGGCTACACCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCTGGACGGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGGAAGTGTTAGTATTTACTACAATGAGAAGTTCAAGGACAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAGCTCAGCGGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGTTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:91)
ПОСЛЕДОВАТЕЛЬНОСТИ 8C8:
Аминокислотная последовательность VL 8C8 в формате FASTA
DIVMTQAAPSVPVTPGESVSISCRSSKSLLHSNGNTYLYWFLQRPGQSPQLLIYRMSNL ASGVPDRFGGSGSGTAFTLRISRVEAEDVGVYYCMQHLEYPYTFGGGTKLEIK (SEQ ID NO:9)
Нуклеотидная последовательность VL 8C8 в формате FASTA
GATATTGTGATGACTCAGGCTGCACCCTCTGTACCTGTCACTCCTGGAGAGTCAGTATCCATCTCCTGCAGGTCTAGTAAGAGTCTCCTGCATAGTAATGGCAACACTTACTTGTATTGGTTCCTGCAGAGGCCAGGCCAGTCTCCTCAGCTCCTGATATATCGGATGTCCAACCTTGCCTCAGGAGTCCCAGACAGGTTCGGTGGCAGTGGGTCAGGAACTGCTTTCACACTGAGAATCAGTAGAGTGGAGGCTGAGGATGTGGGTGTTTATTACTGTATGCAACATCTAGAATATCCGTACACGTTCGGAGGGGGGACCAAGCTGGAAATAAAA (SEQ ID NO:81)
Аминокислотная последовательность VH 8C8 в формате FASTA
QVQLKQSGAELVKPGASVKISCKASGYTFTDYYVNWVKQRPGQGLEWIGKIGPESVSIY YSEKFKAKATLTADKSSSTAYMQLSSLTSEDSAVYFCASYYYGFAYWGQGTLVTVSA (SEQ ID NO:20)
Нуклеотидная последовательность VH 8C8 в формате FASTA
CAGGTCCAGCTGAAGCAGTCTGGAGCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGATATCCTGCAAGGCTTCTGGCTACACCTTCACTGACTATTATGTAAACTGGGTGAAGCAGAGGCCTGGACAGGGCCTTGAGTGGATTGGAAAGATTGGTCCTGAAAGTGTTAGTATTTATTACAGTGAGAAGTTCAAGGCCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCCTACATGCAACTCAGCAGCCTGACATCTGAGGACTCTGCAGTCTATTTCTGTGCAAGTTATTACTACGGGTTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:92)
ПОСЛЕДОВАТЕЛЬНОСТИ 8H8:
Аминокислотная последовательность VL 8H8 в формате FASTA
QAVVTQESALTTSPGETVTLTCRSSSGAVTTGNFANWVQEKPDHLFTGLIGGTNNRAPG VPARFSGSLIGDKAALTITGAQTEDEAIYFCALWYSNHWVFGGGTKLTVL (SEQ ID NO:10)
Нуклеотидная последовательность VL 8H8 в формате FASTA
CAGGCTGTTGTGACTCAGGAATCTGCACTCACCACATCACCTGGTGAAACAGTCACACTCACTTGTCGCTCAAGTTCTGGGGCTGTTACAACTGGTAACTTTGCCAACTGGGTCCAAGAAAAACCAGATCATTTATTCACTGGTCTAATAGGTGGTACCAACAACCGAGCTCCAGGTGTTCCTGCCAGATTCTCAGGCTCCCTGATTGGAGACAAGGCTGCCCTCACCATCACAGGGGCACAGACTGAGGATGAGGCAATATATTTCTGTGCTCTATGGTACAGCAACCACTGGGTGTTCGGTGGAGGAACCAAACTGACTGTCCTA (SEQ ID NO:82)
Аминокислотная последовательность VH 8H8 в формате FASTA
EVQLLETGGGLVQPGGSRGLSCEGSGFTFSGFWMSWVRQTPGKTLEWIGDINSDGSAIN YAPSIKDRFTIFRDNDKNTLYLQMNNVRSEDTATYFCVRYDDYGYFDVWGTGTTVTVSS (SEQ ID NO:21)
Нуклеотидная последовательность VH 8H8 в формате FASTA
GAAGTGCAGCTGTTGGAGACTGGAGGAGGCTTGGTGCAACCGGGGGGGTCACGGGGACTCTCTTGTGAAGGCTCAGGGTTCACTTTTAGTGGCTTCTGGATGAGCTGGGTTCGACAGACACCTGGGAAGACCCTGGAGTGGATTGGAGACATTAATTCTGATGGCAGTGCAATAAACTACGCACCATCCATAAAGGATCGATTCACTATCTTCAGAGACAATGACAAGAACACCCTGTACCTGCAGATGAACAATGTGCGATCGGAGGACACAGCCACGTATTTCTGTGTGAGATATGATGATTACGGGTACTTCGATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA (SEQ ID NO:93)
ПОСЛЕДОВАТЕЛЬНОСТИ 9A5:
Аминокислотная последовательность VL 9A5 в формате FASTA
DVVMTQTPLTLSVTIGQSASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK (SEQ ID NO:11)
Нуклеотидная последовательность VL 9A5 в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAGTCAGCCTCCATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGAGGCTGAGGATTTGGGAGTTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAA (SEQ ID NO:83)
Аминокислотная последовательность VH 9A5 в формате FASTA
HVQLQQSGAELARPGASVKLSCKASGYTFTSYGLIWVKQRTGQGLEWIGEIYPRSGNTY YNEKFKGKATLTADISSSTAYMELRSLTSEDSAVYFCASSSPHGDYWGQGTTLTVSS (SEQ ID NO:22)
Нуклеотидная последовательность VH 9A5 в формате FASTA
CACGTTCAGCTGCAGCAGTCTGGAGCTGAGTTGGCGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTTTAATCTGGGTGAAGCAGAGAACTGGACAGGGCCTTGAGTGGATTGGAGAGATTTATCCTAGAAGTGGTAATACTTACTACAATGAGAAGTTCAAGGGCAAGGCCACACTGACTGCAGACATATCCTCCAGCACAGCGTACATGGAGCTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGTTCCTCTCCTCACGGGGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:94)
ПОСЛЕДОВАТЕЛЬНОСТИ 10G9:
Аминокислотная последовательность VL 10G9 в формате FASTA
QAVVTQESALTTSPGETVTLTCRSSTGAVTTSNYANWVQEKPDHLFTGLIGGTNNRAPG VPARFSGSLIGDKAALTITGAQTEDEAIYFCALWYSNHWVFGGGTKLTVL (SEQ ID NO:12)
Нуклеотидная последовательность VL 10G9 в формате FASTA
CAGGCTGTTGTGACTCAGGAATCTGCACTCACCACATCACCTGGTGAAACAGTCACACTCACTTGTCGCTCAAGTACTGGGGCTGTTACAACTAGTAACTATGCCAACTGGGTCCAAGAAAAACCAGATCATTTATTCACTGGTCTAATAGGTGGTACCAACAACCGAGCTCCAGGTGTTCCTGCCAGATTCTCAGGCTCCCTGATTGGAGACAAGGCTGCCCTCACCATCACAGGGGCACAGACTGAGGATGAGGCAATATATTTCTGTGCTCTATGGTACAGCAACCACTGGGTGTTCGGTGGAGGAACCAAACTGACTGTCCTA (SEQ ID NO:84)
Аминокислотная последовательность VH 10G9 в формате FASTA
EVQLLETGGGLVQPGGSRGLSCEGSGFTFSDFWMSWVRQTPGKTLEWIGDINSDGSAVN YAPSIKDQFTIFRDNDKRTLHLQMINVRSEDTATYFCVRYDDYGYFDVWGTGTTVTVSS (SEQ ID NO:23)
Нуклеотидная последовательность VH 10G9 в формате FASTA
GAAGTGCAGCTGTTGGAGACTGGAGGAGGCTTAGTGCAACCTGGGGGGTCACGGGGACTCTCTTGTGAAGGCTCAGGGTTCACTTTTAGTGACTTCTGGATGAGCTGGGTTCGACAGACACCTGGGAAGACCCTGGAGTGGATTGGAGACATTAATTCTGATGGCAGTGCAGTTAACTACGCACCATCCATAAAGGATCAATTCACTATCTTCAGAGACAATGACAAGAGGACCCTGCACCTGCAGATGATCAATGTTCGATCGGAGGACACAGCCACGTATTTCTGTGTGAGATATGATGATTACGGGTACTTCGATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA (SEQ ID NO:95)
ПОСЛЕДОВАТЕЛЬНОСТИ 6A:
Аминокислотная последовательность VL 6A в формате FASTA
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLRISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK (SEQ ID NO:96)
Нуклеотидная последовательность VL 6A в формате FASTA
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTACCTGCAGAAGCCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAGGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:120)
Аминокислотная последовательность VH 6A в формате FASTA
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDTE YASKFQDKATITTDTSSNTAYLQLSSLTSEDTAVYYCTTYVGFAYWGQGTLVTVST (SEQ ID NO:108)
Нуклеотидная последовательность VH 6A в формате FASTA
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAACTTGTGAGGCCAGGGGCCTCAGTCAAGTTGTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCTGAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATACTGAATATGCCTCGAAATTCCAGGACAAGGCCACTATAACAACAGACACATCCTCCAACACAGCCTACCTGCAGCTCAGCAGCCTGACATCTGAGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGCTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTACA (SEQ ID NO:133)
ПОСЛЕДОВАТЕЛЬНОСТИ 28A:
Аминокислотная последовательность VL 28A в формате FASTA
DVVMTQTPLTLSIPIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSEL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK (SEQ ID NO:97)
Нуклеотидная последовательность VL 28A в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGATTCCCATTGGACAACCAGCCTCCATCTCTTGTAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTCATCTATCTGGTGTCTGAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGAGGCTGAAGATTTGGGAGTTTATTATTGTTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAA (SEQ ID NO:121)
Аминокислотная последовательность VH 28A в формате FASTA
QVQLQQSGAELARPGASVKLSCKASGYTFISYGITWVKQRTGQGLEWIGEIHPRSGNTY YNENFKDRASLTADKSSSTAYMEVRSLTSEDSAVYFCARGGPGDYWGQGTTLTVSS (SEQ ID NO:109)
Нуклеотидная последовательность VH 28A в формате FASTA
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCATAAGCTATGGTATAACCTGGGTGAAGCAGAGAACTGGACAGGGCCTTGAGTGGATTGGAGAGATTCATCCTAGAAGTGGTAATACTTACTACAATGAGAATTTCAAGGACAGGGCCTCACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGAGGTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGGGGTGGGCCGGGGGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:134)
ПОСЛЕДОВАТЕЛЬНОСТИ 63A:
Аминокислотная последовательность VL 63A в формате FASTA
DVVMTQTPLTLSVTIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK (SEQ ID NO:98)
Нуклеотидная последовательность VL 63A в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTCCATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGAGGCTGAGGATTTGGGAGTTTATTATTGTTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAA (SEQ ID NO:122)
Аминокислотная последовательность VH 63A в формате FASTA
QVQLQQSGAELARPGASVKLSCKASGYTFTSYGISWVKQRTGQGLEWIGQIYPRSDNTY YNERFKGKATLTADKSSSTAYMALRSLTSEDSAVYFCAREGGPDYWGQGTTLTVSS (SEQ ID NO:110)
Нуклеотидная последовательность VH 63A в формате FASTA
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTATAAGCTGGGTGAAGCAGAGAACTGGACAGGGCCTTGAGTGGATTGGACAGATTTATCCTAGAAGTGACAATACTTACTACAATGAGAGGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGCGCTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGAGAGGGGGGTCCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:135)
ПОСЛЕДОВАТЕЛЬНОСТИ 71A:
Аминокислотная последовательность VL 71A в формате FASTA
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK (SEQ ID NO:99)
Нуклеотидная последовательность VL 71A в формате FASTA
GACGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTACCTACAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:123)
Аминокислотная последовательность VH 71A в формате FASTA
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDIE YASRFQGKATMTADTSSNTAYLQLTSLTSADTAVYYCTTYVGFGYWGQGTLVTVSA (SEQ ID NO:111)
Нуклеотидная последовательность VH 71A в формате FASTA
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTTGTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCTGAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATATTGAATATGCCTCGAGGTTCCAGGGCAAGGCCACTATGACAGCAGACACATCCTCCAACACAGCCTACCTGCAGCTCACCAGCCTGACATCTGCGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:136)
ПОСЛЕДОВАТЕЛЬНОСТИ 77A:
Аминокислотная последовательность VL 77A в формате FASTA
DVLMTQSPLSLPVSLGDQASISCRSSQNIVHSNGNTYLEWYLKKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGMYYCFQGSHVPLTFGAGTKLELK (SEQ ID NO:100)
Нуклеотидная последовательность VL 77A в формате FASTA
GATGTTTTGATGACCCAAAGTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAACATAGTACATAGTAATGGTAACACCTATTTAGAATGGTACCTGAAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTCTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAATGTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGAGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:124)
Аминокислотная последовательность VH 77A в формате FASTA
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDTE YASKFQGKATITADTSSNTVYLQLSSLTSEDTAVYYCTTYVGFGYWGQGTLVTVSA (SEQ ID NO:112)
Нуклеотидная последовательность VH 77A в формате FASTA
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTTGTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCTGAACAGGGCCTGGAGTGGATTGGATGTATTGATCCTGAGAATGGTGATACTGAATATGCCTCGAAGTTCCAGGGCAAGGCCACTATAACAGCAGACACATCCTCCAACACAGTCTACCTGCAGCTCAGCAGCCTGACATCTGAGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGGGGCCAGGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:137)
ПОСЛЕДОВАТЕЛЬНОСТИ 80A:
Аминокислотная последовательность VL 80A в формате FASTA
DIVMTQSPSSLTVTAGEKVTMSCKSNQSLLNSGDQKNYLTWYQQKPGQPPKLLIYWAST RESGVPDRFTGSGSGTDFTLTISSVQAEDLAIYYCQNDYSYPLTFGAGTKLELK (SEQ ID NO:101)
Нуклеотидная последовательность VL 80A в формате FASTA
GACATTGTGATGACACAGTCTCCATCCTCCCTGACTGTGACAGCAGGAGAGAAGGTCACTATGAGCTGCAAGTCCAATCAGAGTCTGTTAAACAGTGGAGATCAAAAGAACTACTTGACCTGGTACCAGCAGAAACCAGGGCAGCCTCCTAAACTATTGATCTACTGGGCATCCACTAGGGAATCTGGGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGAACAGATTTCACTCTCACCATCAGCAGTGTGCAGGCTGAAGACCTGGCAATTTATTACTGTCAGAATGATTATAGTTATCCACTCACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:125)
Аминокислотная последовательность VH 80A в формате FASTA
QVQLKQSGAELVRPGASVKLSCRASGYTFTDFYINWVKQRPGQGLEWIARIYPGSDETY YNEKFKDKVTLTAEKSSSTAYMQLSSLTSEDSAVYFCALWFFDVWGTGTTVTVSS (SEQ ID NO:113)
Нуклеотидная последовательность VH 80A в формате FASTA
CAGGTCCAACTGAAGCAGTCTGGGGCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAGGGCTTCTGGCTACACTTTCACTGACTTCTACATAAACTGGGTGAAGCAGAGGCCTGGACAGGGACTTGAGTGGATTGCAAGGATTTATCCTGGAAGTGATGAGACTTACTACAATGAGAAGTTTAAGGACAAGGTCACACTGACTGCAGAAAAATCCTCCAGCACTGCCTACATGCAGCTCAGCAGCCTGACATCTGAGGACTCTGCTGTCTATTTCTGTGCCCTCTGGTTCTTCGATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA (SEQ ID NO:138)
ПОСЛЕДОВАТЕЛЬНОСТИ 82B:
Аминокислотная последовательность VL 82B в формате FASTA
DVVMTQTPLTLSVTIGQSASISCKSSQSLLDSDGNTYLNWLLQRPGQSPKRLIYLVSEL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGVYYCWQGTHFPFTFGSGTKLEIK (SEQ ID NO:102)
Нуклеотидная последовательность VL 82B в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACTATTGGACAATCAGCCTCCATCTCTTGCAAGTCAAGTCAGAGCCTCCTAGATAGTGATGGAAACACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATTTGGTGTCTGAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGAGGCTGAGGATTTGGGAGTTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAA (SEQ ID NO:126)
Аминокислотная последовательность VH 82B в формате FASTA
QVQLQQSGAELARPGASVKLSCKASGYTFTSDGITWVKQRTGQGLEWIGQIHPRSGNTY YNGKFKGKATLTADRSSSTTYMELRSLTSEDSAVYFCAKTGTGDYWGQGTTLTVSS (SEQ ID NO:114)
Нуклеотидная последовательность VH 82B в формате FASTA
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGTTGGCGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCGGGCTACACCTTCACAAGCGATGGTATTACCTGGGTGAAGCAGAGAACTGGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACCTACTACAATGGGAAGTTCAAGGGCAAGGCCACACTGACTGCAGACAGATCCTCCAGCACAACGTACATGGAACTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAAAACTGGGACGGGGGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:139)
ПОСЛЕДОВАТЕЛЬНОСТИ 83B:
Аминокислотная последовательность VL 83B в формате FASTA
EIQMTQSPSSMSASLGDRITITCQATQDIVKNLNWYQQKPGKPPSFLIYYATELAEGVP SRFSGSGSGSDYSLTISNLESEDFADYYCLQFYEFPYTFGGGTKLEIK (SEQ ID NO:103)
Нуклеотидная последовательность VL 83B в формате FASTA
GAAATCCAGATGACCCAGTCTCCATCCTCTATGTCTGCATCTCTGGGAGACAGAATAACCATCACTTGCCAGGCAACTCAAGACATTGTTAAGAATTTAAACTGGTATCAGCAGAAACCAGGGAAACCCCCTTCATTCCTGATCTATTATGCAACTGAACTGGCAGAAGGGGTCCCATCAAGGTTCAGTGGCAGTGGGTCTGGGTCAGACTATTCTCTGACAATCAGCAACCTGGAGTCTGAAGATTTTGCAGACTATTACTGTCTACAGTTTTATGAATTTCCGTACACGTTCGGAGGGGGGACCAAGCTGGAAATAAAA (SEQ ID NO:127)
Аминокислотная последовательность VH 83B в формате FASTA
EVQLQQSGPELVKPGASVKMSCKASGYTFTDYNMHWVKQSHGKSLEWIGYINPNNGGTS YNQKFKDKATLTVNKSSSTAFMELRSLASEDSAVYYCARSDWEDCWGQGTTLTVSS (SEQ ID NO:115)
Нуклеотидная последовательность VH 82B в формате FASTA
GAGGTCCAGCTGCAACAGTCTGGACCTGAGCTGGTGAAGCCTGGGGCTTCAGTGAAGATGTCCTGCAAGGCTTCTGGATACACATTCACTGACTACAACATGCACTGGGTGAAGCAGAGCCATGGAAAGAGCCTTGAGTGGATTGGATATATTAACCCTAACAATGGTGGTACTAGCTACAACCAGAAGTTCAAGGACAAGGCCACATTGACTGTAAACAAGTCCTCCAGCACAGCCTTCATGGAGCTCCGCAGCCTGGCATCGGAGGATTCTGCAGTCTATTACTGTGCAAGGTCTGACTGGGAAGACTGCTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:140)
ПОСЛЕДОВАТЕЛЬНОСТИ 92A:
Аминокислотная последовательность VL 92A в формате FASTA
QIVLTQSPAIMSASLGEEITLICSASSSVSYMHWYQQKSGTSPKLLIYRTSNLASGVPS RFSGSGSGTFYSLTISSVEAEDAADYYCHQWSSWTFGGGTQLEIK (SEQ ID NO:104)
Нуклеотидная последовательность VL 92A в формате FASTA
CAAATTGTTCTCACCCAGTCTCCAGCAATCATGTCTGCATCTCTAGGGGAGGAGATCACCCTAATTTGCAGTGCCAGCTCGAGTGTAAGTTACATGCACTGGTACCAGCAGAAGTCAGGCACTTCTCCCAAACTCTTGATTTATCGCACATCCAACCTGGCTTCTGGAGTCCCTTCTCGCTTCAGTGGCAGTGGGTCTGGGACCTTTTATTCTCTTACAATCAGCAGTGTGGAGGCTGAAGATGCTGCCGATTATTACTGCCATCAGTGGAGTAGTTGGACGTTCGGTGGAGGCACCCAGCTGGAAATCAAA (SEQ ID NO:128)
Аминокислотная последовательность VH 92A в формате FASTA
DVQLQESGPGLVKFSQSLSLTCSVTGYSITSGYYWNWIRQFPGNKLEWMGYIRHDGSNN YNPSLKNRISITRDTSKNQFFLKLNSVITEDTATYYCVREIYDGSSGYFDVWGTGTTVTVSS (SEQ ID NO:116)
Нуклеотидная последовательность VH 92A в формате FASTA
GATGTACAGCTTCAGGAGTCAGGACCTGGCCTCGTGAAATTTTCTCAGTCTCTGTCTCTCACCTGCTCTGTCACTGGCTACTCCATCACCAGTGGTTATTACTGGAACTGGATCCGGCAGTTTCCAGGAAACAAACTGGAATGGATGGGCTACATAAGACACGATGGTAGCAATAACTACAACCCGTCTCTCAAAAATCGAATCTCCATCACTCGTGACACATCTAAGAACCAGTTTTTCCTGAAGTTGAATTCTGTGATTACTGAGGACACAGCCACATATTACTGTGTAAGAGAGATCTATGATGGTTCCTCCGGGTACTTCGATGTCTGGGGCACAGGGACCACGGTCACCGTCTCCTCA (SEQ ID NO:141)
ПОСЛЕДОВАТЕЛЬНОСТИ 93B:
Аминокислотная последовательность VL 93B в формате FASTA
DIVMTQSPSSLTVTAGEKVTMSCKSSQSLLNSGNQKNYLTWYQQKPGQPPKLLIYWAST RESGVPDRFTGSGSGTDFTLTISNVQPEDLAVYYCQNDYSFPFTFGSGTELEMK (SEQ ID NO:105)
Нуклеотидная последовательность VL 93B в формате FASTA
GACATTGTGATGACACAGTCTCCATCCTCCCTGACTGTGACAGCAGGAGAGAAGGTCACTATGAGCTGCAAGTCCAGTCAGAGTCTGTTAAACAGTGGAAATCAAAAGAATTACTTGACCTGGTACCAGCAGAAACCAGGACAGCCTCCTAAACTGTTGATCTACTGGGCATCCACTAGGGAATCTGGGGTCCCTGATCGCTTCACAGGCAGTGGATCTGGAACAGATTTCACTCTCACCATTAGCAATGTGCAGCCTGAAGACCTGGCAGTTTATTACTGTCAGAATGATTATAGTTTTCCATTCACGTTCGGCTCGGGGACAGAGTTGGAAATGAAA (SEQ ID NO:129)
Аминокислотная последовательность VH 93B в формате FASTA
QVQLKQSGAELVRPGASVKLSCKASGYTFTDYYINWVKQRPGQGLEWIARIYPGNGNTD YNEKFKDKATLTAEKSSTTAYIQLSSLTSEDSAVYFCCLWYFDVWGTGTTVTVSS (SEQ ID NO:117)
Нуклеотидная последовательность VH 93B в формате FASTA
CAGGTCCAGCTGAAGCAGTCTGGGGCTGAACTGGTGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACTTTCACTGACTACTATATAAACTGGGTGAAGCAGAGGCCTGGACAGGGACTTGAGTGGATTGCAAGGATTTATCCTGGAAATGGTAATACTGACTACAATGAGAAGTTCAAGGACAAGGCCACACTGACTGCAGAAAAATCCTCCACCACTGCCTACATACAACTCAGCAGTCTGACATCTGAGGACTCTGCTGTCTATTTCTGTTGCCTCTGGTACTTCGATGTCTGGGGCACAGGAACCACGGTCACCGTCTCCTCA (SEQ ID NO:142)
ПОСЛЕДОВАТЕЛЬНОСТИ 99B:
Аминокислотная последовательность VL 99B в формате FASTA
DVVMTQTPLTLSVTIGQPASISCKSSQSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKISRVEAEDLGIYYCWQGTHFPFTFGSGTKLEIK (SEQ ID NO:106)
Нуклеотидная последовательность VL 99B в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTCCATCTCTTGCAAGTCAAGTCAGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCAGCAGAGTGGAGGCTGAGGATTTGGGAATTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAATAAAA (SEQ ID NO:130)
Аминокислотная последовательность VH 99B в формате FASTA
QVQLQQSGAELARPGASVKLSCKASGYTFTSDGITWLKQRTGQGLEWIGQIHPRSGNTY YNEKFKGKATLTADKSSSTAYMELRSLTSEDSAVYFCAKTGTGDYWGQGTTLTVSS (SEQ ID NO:118)
Нуклеотидная последовательность VH 99B в формате FASTA
CAGGTTCAGCTGCAGCAGTCTGGAGCTGAGCTGGCGAGGCCTGGGGCTTCAGTGAAGCTGTCCTGCAAGGCTTCGGGCTACACCTTCACAAGCGACGGTATAACCTGGCTGAAACAGAGAACTGGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACCTACTACAATGAGAAGTTCAAGGGCAAGGCCACACTGACTGCAGACAAATCCTCCAGCACAGCGTACATGGAACTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAAAACTGGGACGGGGGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:143)
ПОСЛЕДОВАТЕЛЬНОСТИ 104B:
Аминокислотная последовательность VL 104B в формате FASTA
DVVMTQTPLTLSVTIGQPASISCKSSLSLLDSDGKTYLNWLLQRPGQSPKRLIYLVSKL DSGVPDRFTGSGSGTDFTLKIIRVEAEDLGIYYCWQGTHFPFTFGSGTKLEVK (SEQ ID NO:107)
Нуклеотидная последовательность VL 104B в формате FASTA
GATGTTGTGATGACCCAGACTCCACTCACTTTGTCGGTTACCATTGGACAACCAGCCTCCATCTCTTGCAAGTCAAGTCTGAGCCTCTTAGATAGTGATGGAAAGACATATTTGAATTGGTTGTTACAGAGGCCAGGCCAGTCTCCAAAGCGCCTAATCTATCTGGTGTCTAAACTGGACTCTGGAGTCCCTGACAGGTTCACTGGCAGTGGATCAGGGACAGATTTCACACTGAAAATCATCAGAGTGGAGGCTGAGGATTTGGGAATTTATTATTGCTGGCAAGGTACACATTTTCCATTCACGTTCGGCTCGGGGACAAAGTTGGAAGTAAAA (SEQ ID NO:131)
Аминокислотная последовательность VH 104B в формате FASTA
QVQLQQSGPELARPGASVKLSCKASGYTFTSYGISWVKQRTGQGLEWIGQIHPRSGNTY YNENFKGKATLTAAKSSSTAYLELRSLTSEDSAVYFCAREGGPDYWGQGTTLTVSS (SEQ ID NO:119)
Нуклеотидная последовательность VH 104B в формате FASTA
CAGGTTCAGCTGCAGCAGTCTGGGCCTGAGCTGGCGAGGCCTGGGGCCTCAGTGAAGCTGTCCTGCAAGGCTTCTGGCTACACCTTCACAAGCTATGGTATAAGCTGGGTGAAGCAAAGAACTGGACAGGGCCTTGAGTGGATTGGACAGATTCATCCTAGAAGTGGTAATACTTACTACAATGAGAACTTCAAGGGCAAGGCCACACTGACTGCAGCCAAATCCTCCAGCACAGCGTACCTGGAGCTCCGCAGCCTGACATCTGAGGACTCTGCGGTCTATTTCTGTGCAAGAGAGGGGGGTCCCGACTACTGGGGCCAAGGCACCACTCTCACAGTCTCCTCA (SEQ ID NO:144)
ПОСЛЕДОВАТЕЛЬНОСТИ 105A:
Аминокислотная последовательность VL 105A в формате FASTA
DVLMTQTPLSLPVSLGDQASISCRSSQSIVHSNGNTYLEWYLQKPGQSPKLLIYKVSNR FSGVPDRFSGSGSGTDFTLKISRVEAEDLGVYYCFQGSHVPLTFGAGTKLELK (SEQ ID NO:99)
Нуклеотидная последовательность VL 105A в формате FASTA
GATGTTTTGATGACCCAAACTCCACTCTCCCTGCCTGTCAGTCTTGGAGATCAAGCCTCCATCTCTTGCAGATCTAGTCAGAGTATTGTACATAGTAATGGAAACACCTATTTAGAATGGTACCTACAGAAACCAGGCCAGTCTCCAAAGCTCCTGATCTACAAAGTTTCCAACCGATTTTCTGGGGTCCCAGACAGGTTCAGTGGCAGTGGATCAGGGACAGATTTCACACTCAAGATCAGCAGAGTGGAGGCTGAGGATCTGGGAGTTTATTACTGCTTTCAAGGTTCACATGTTCCGCTCACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAA (SEQ ID NO:132)
Аминокислотная последовательность VH 105A в формате FASTA
EVQLQQSGAELVRPGASVKLSCTASGFNIKDDYMHWVKQRPEQGLEWIGCIDPENGDIE YASRFQGKATMTADTSSNTAYLQLTSLTSADTAVYYCTTYVGFGYWGQGTLVTVSA (SEQ ID NO:111)
Нуклеотидная последовательность VH 105A в формате FASTA
GAGGTTCAGCTGCAGCAGTCTGGGGCTGAGCTTGTGAGGCCAGGGGCCTCAGTCAAGTTGTCCTGCACAGCTTCTGGCTTTAACATTAAAGACGACTATATGCACTGGGTGAAACAGAGGCCTGAACAGGGCCTGGAGTGGATTGGATGCATTGATCCTGAGAATGGTGATATTGAATATGCCTCGAGGTTCCAGGGCAAGGCCACTATGACAGCAGACACATCCTCCAACACAGCCTACCTGCAGCTCACCAGCCTGACATCTGCGGACACTGCCGTCTATTACTGTACTACATACGTTGGATTTGGTTACTGGGGCCAAGGGACTCTGGTCACTGTCTCTGCA (SEQ ID NO:145)
Пример 2: Анти–huS15 антитела связываются с клетками, экспрессирующими S15 человека или S15 мыши
Материалы и методы
Линии опухолевых клеток 293T человека и CRC MC38 мыши трансдуцировали лентивектором, несущим SIGLEC 15 человека или SIGLEC 15 мыши. Клетки сортировали для определения стабильных клеточных линий S15 человека и S15 мыши. Стабильные клетки 293T.hS15 и MC38.mS15 ресуспендировали в буфере для FACS и Fc–рецепторы перед инкубацией блокировали с очищенными анти–SIGLEC–15 mAb. 1E05 клеток в 100 мкл буфера для FACS разделяли на аликвоты в целях разделения пробирок и добавляли 1 мкг очищенного mAb. Клетки инкубировали при 4 C в течение 30 минут, затем промывали дважды буфером для FACS. Клетки ресуспендировали в 100 мкл буфера для FACS и 0,005 мкг анти–мышиный IgG–PE вторичное антитело добавляли к образцам, инкубировали в течение 30 минут и промывали дважды с избытком буфера для FACS. Клетки фиксировали в буфере для фиксации и затем анализировали с помощью проточной цитометрии.
Анализ представлен на Фиг. 4A.
Результаты
Анти–huS15 антитела, в том числе 1B2, 1C3, 1C12, 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9 (Фиг. 4B) и 6A (NC6), 28A (NC28), 63A (NC63), 71A (NC71), NC74, 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), NC87, 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104), 105A (NC105) (Фиг. 4C) исследовали в отношении связывания с клетками, экспрессирующими S15 человека или S15 мыши. Результаты представлены на Фиг. 4B–4C.
Анти–huS15 антитела, в том числе 1B2, 1C3, 1C12, 1H3, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9 и 6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104) или 105A (NC105), также исследовани в отношении связывания с клетками, фиксированными в формалине. Результаты показаны на Фиг. 4D.
Пример 3: Очищенные антитела связываются с SIGLEC–15 мыши и человека
Материалы и методы
Клетки 293T, транзиентно трансфицированные S15–TM (Operetta)
Клетки K562, транзиентно трансфицированные S15–TM (FACS)
Клетки 293T транзиентно трансфицировали плаздидной ДНК с SIGLEC–15 мыши с помощью липофектаминовой системы, а клетки K562 трансфицировали плазмидной ДНК с SIGLEC–15 человека с помощью электропорации. 1e5 трансфицированных клеток в 100 мкл буфера для FACS (PBS, содержащий 0,5% сыворотки крови) разделяли на аликвоты в целях разделения пробирок и добавляли 1 мкг очищенного mAb. Клетки инкубировали при 4 C в течение 30 минут, затем промывали дважды буфером для FACS. Клетки ресуспендировали в 100 мкл буфера для FACS и 0,005 мкг анти–мышиный IgG–PE вторичное антитело добавляли к образцам, инкубировали в течение 30 минут и промывали дважды с избытком буфера для FACS. Клетки фиксировали в буфере для фиксации (2% формальдегид в PBS) и затем анализировали с помощью проточной цитометрии.
Клетки U87 ресуспендировали в буфере для FACS и Fc–рецепторы блокировали до инкубации с очищенными анти–SIGLEC–15 mAb. 1e5 клеток в 100 мкл буфера для FACS разделяли на аликвоты в целях разделения пробирок и добавляли 1 мкг очищенного mAb. Клетки инкубировали при 4 C в течение 30 минут, затем промывали дважды буфером для FACS. Клетки ресуспендировали в 100 мкл буфера для FACS и 0,005 мкг анти–мышиный IgG–PE вторичное антитело добавляли к образцам, инкубировали в течение 30 минут и промывали дважды с избытком буфера для FACS. Клетки фиксировали в буфере для фиксации и затем анализировали с помощью проточной цитометрии.
Результаты
Очищенные антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9 исследовали в отношении связывания с SIGLEC–15 мыши (mS15), экспрессируемым клетками 293T (производная с высокой способностью к трансфекции человеческих эмбриональных клеток почки 293) и SIGLEC–15 человека (hS15), экспрессируемым клетками K–562 (плевральный выпот женщины в возрасте 53 лет с хроническим миелогенным лейкозом в терминальном бластном кризе). Результаты представлены на Фиг. 5A–5C.
Очищенные антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5, 10G9 и 5F10 также исследовали в отношении связывания с клетками глиомы U87 человека, которые эндогенно экспрессируют SIGLEC–15 человека (hS15). Результаты изображены на Фиг. 6A–6C, которые показывают, процент hS15+ клеток (Фиг. 6A и 6C) и среднюю интенсивность флуоресценции (MFI) (Фиг. 6B) соответственно для каждого антитела.
Пример 4: Анти–SIGLEC–15 антитела могут блокировать функцию SIGLEC–15
Материалы и методы
Получение hS15.hG1
Мономер слитого белка S15, содержащий весь внеклеточный домен S15, слитый с остовом IgG, получали для анализов аффинности и конкурентных анализов. Расщепляемую тромбином кДНК hS15.hFc субклонировали в pEE17.4 Фрагментированные слитые белки наблюдаются в транзиентно трансфицированных клетках CHO, но не в клетках 293 при 37°C. Интактный слитый белок экспрессируется более эффективно при 31°C.
Слитый белок имеет последовательность:
MEWSWVFLFFLSVTTGVHS FVRTKIDTTENLLNTEVHSSPAQRWSMQVPPEVSAEAGDA AVLPCTFTHPHRHYDGPLTAIWRAGEPYAGPQVFRCAAARGSELCQTALSLHGRFRLLGNPRRN DLSLRVERLALADDRRYFCRVEFAGDVHDRYESRHGVRLHVTAAPRIVNISVLPSPAHAFRALC TAEGEPPPALAWSGPALGNSLAAVRSPREGHGHLVTAELPALTHDGRYTCTAANSLGRSEASVY LFRFHGASG DKTHTCPPCPAPEFEGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKF NWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPASIEKTISKA KGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGS FFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPG (SEQ ID NO:193).
Слитый сигнальный белок с отщепляемой сигнальной последовательностью представляет собой:
FVRTKIDTTENLLNTEVHSSPAQRWSMQVPPEVSAEAGDAAVLPCTFTHPHRHYDGPLT AIWRAGEPYAGPQVFRCAAARGSELCQTALSLHGRFRLLGNPRRNDLSLRVERLALADDRRYFC RVEFAGDVHDRYESRHGVRLHVTAAPRIVNISVLPSPAHAFRALCTAEGEPPPALAWSGPALGN SLAAVRSPREGHGHLVTAELPALTHDGRYTCTAANSLGRSEASVYLFRFHGASG DKTHTCPPCP APEFEGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREE QYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPASIEKTISKAKGQPREPQVYTLPPSRDEL TKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNV FSCSVMHEALHNHYTQKSLSLSPG (SEQ ID NO:194).
Мышиная лидерная последовательность изображена с помощью подчеркивания. Внеклеточный домен SIGLEC–15 (ECD) изображен с помощью курсивного шрифта. Шарнирный участок изображен с помощью двойного подчеркивания. Оставшаяся последовательность происходит из Fc IgG1. Мутации L234F/L235E/P331S в Fc–домене IgG1 изображены с помощью жирного шрифта и пунктирного подчеркивания.
Блокирующий анализ
Клетки 293T.LRRC4C создавали с помощью 2 циклов трансдукции Lenti–LRRC4C.
Стабильные клетки 293T.LRRC4C ресуспендировали в буфере для FACS и Fc–рецепторы перед инкубацией блокировали. 1E05 клеток в 100 мкл буфера для FACS разделяли на аликвоты в целях разделения пробирок и сначала добавляли 2 мкг очищенного mAb, с последующим добавлением 0,2 мкг hSIGLEC–15hFc. Клетки инкубировали при 4 C в течение 30 минут, затем промывали дважды буфером для FACS. Клетки ресуспендировали в 100 мкл буфера для FACS и 0,005 мкг анти–человеческий IgG–PE вторичное антитело добавляли к образцам, инкубировали в течение 30 минут и промывали дважды с избытком буфера для FACS. Клетки фиксировали в буфере для фиксации и затем анализировали с помощью проточной цитометрии в целях определения связывания SIGLEC–15 с LRRC4C.
1 мкг/мл hS15.hG1+100 мкг супа или 33 мкг/мл Cl №3, №1
Анализ представлен на Фиг. 7A.
Результаты
Результаты представлены на Фиг. 7B–7E.
Полные блокаторы взаимодействия S15/LRRC4C включают, но не ограничиваясь ими:
5G12, 6F8, 8C8, 1C3, 1C12, 3H10, 1B2
Частичные блокаторы включают, но не ограничиваясь ими:
10G9, 8H8, 9A5
Пример 5: анти–S15 mAb обращает опосредованную hS15.hG1 супрессию T–клеток человека
Материалы и методы
Анализ пролиферации PBMC
Покрытое анти–CD3 антитело @ 0,05 мкг/мл
Все PBMC человека +/– 5 мкг/мл hS15.hFc и 12 мкг/мл анти–SIGLEC–15 mAb или контролей, как указано
Анти–человеческий CD3 (клон OKT3) антитело наносили при 0,03 мкг/мл в 100 мкл PBS на лукне 96–луночного плоскодонного планшета для культивирования тканей в течение ночи при 4 C. PBS и несвязанный CD3 аспирировали непосредственно перед добавлением компонентов для анализа. Все PBMC от здорового донора–человека метили 5 мкM CFSE в течение 10 минут в полной среде RPMI (содержащей 10% FBS) при 37 C и промывали 2 раза перед суспендированием в целях добавления в лунки при концентрации 2,5E05 клеток/лунка. Растворенное hSiglec–15hFc или контроли добавляли в лунки в конечной концентрации 5 мкг/мл, в то время как очищенные анти–SIGLEC–15 mAb или контроли добавляли к лункам в конечной концентрации 12 мкг/мл. Планшеты инкубировали при 37 C в CO2 инкубаторе в течение 72 часов. После удаления небольшого количестве супернатанта для анализа цитокинов клетки переносили в круглодонный планшет, Fc–рецепторы блокировали и клетки окрашивали CD4 и CD8 флуоресцентными mAb в течение 30 минут при 4 C. Клетки промывали в буфере для FACS, с последующей фиксацией для анализа с помощью проточной цитометрии. Уровни IFN–гамма в кондиционированном супернатанте анализировали с помощью набора для ИФА MSD.
Анализы изображены на Фиг. 8A и 9A.
Результаты
Очищенные антитела 1B2, 1C3, 1H3, 1C12, 3H10, 5G12, 6F8, 8C8, 8H8, 9A5 и 10G9 исследовали в анализе пролиферации PBMC (Фиг. 8B, 8C, 8D и 8E) и 6A (NC6), 28A (NC28), 63A (NC63), 77A (NC77), 80A (NC80), 82B (NC82), 83B (NC83), 92A (NC92), 93B (NC93), 99B (NC99), 104B (NC104), 105A (NC105) (Фиг. 8F и 8G). CD4+ и CD8+ T–клетки гейтировали и анализировали в отношении разведения CFSE в качестве показателя клеточного деления (пролиферации). Повышенное разведение указывало на более высокую клеточную пролиферацию. Эти результаты показывают, что определенные анти–S15 mAb могут обращать опосредованную hS15.hG1 супрессию T–клеток человека.
Однако блокирование взаимодействия hS15 и LRRC4C не коррелирует с усилением T–клеточной функции. Результаты показаны на Фиг. 8H и 8I.
Также идентифицировали анти–S15 mAb, которые обращают опосредованное hS15.hG1 ослабление продуцирования IFNγ в T–клетках человека. Результаты представлены на Фиг. 9B.
Пример 6: Анти–S15 mAb могут блокировать образование остеокластов
Материалы и методы
Свежеприготовленные PBMC выделяли и обогащали в отношении моноцитов 2 путями:
с помощью сортировки с использованием колонки MACS (Фиг.10, левая панель); или
с помощью прикрепления к пластмассе в бессывороточной среде (Фиг. 10, правая панель).
Клетки культивировали с M–CSF и RANKL в течение 8 дней с анти–25E9 или анти–S15 mAb и анализировали в отношении TRAP (устойчивой к тартрату кислой фосфатазе).
Результаты
Результаты, изображенные на Фиг. 15, показывют, что анти–S15 mAb могут блокировать образование остеокластов.
Пример 7: Гуманизированные антитела 5G12
Клон 5G12 гуманизировали, получая три гуманизированные тяжелые цепи и пять гуманизированных легких цепей (Фиг. 12A и 12B).
hVL1 5G12
DIQMTQSPSSLSASVGDRVTITCKASQDINSYLSWFQQKPGKAPKTLIYRANRLVDGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCLQYDEFPYTFGGGTKVEIK (SEQ ID NO:219)
CDR1 hVL1 5G12
KASQDINSYLS (SEQ ID NO:28)
CDR2 hVL1 5G12
RANRLVD (SEQ ID NO:36)
CDR3 hVL1 5G12
LQYDEFPYT (SEQ ID NO:43)
hVL2 5G12
DIQMTQSPSSLSASVGDRVTITCKASQDINTYLSWFQQKPGKAPKTLIYRANRLVDGVP SRFSGSGSGTDYTLTISSLQPEDFATYYCLQYDEFPYTFGGGTKVEIK (SEQ ID NO:195)
CDR1 hVL2 5G12
KASQDINTYLS (SEQ ID NO:196)
CDR2 hVL2 5G12
RANRLVD (SEQ ID NO:36)
CDR3 hVL2 5G12
LQYDEFPYT (SEQ ID NO:43)
hVL3 5G12
DIQMTQSPSSLSASVGDRVTITCKASQDINVYLSWFQQKPGKAPKTLIYRANRLVDGVP SRFSGSGSGTDYTLTISSLQPEDFATYYCLQYDEFPYTFGGGTKVEIK (SEQ ID NO:197)
CDR1 hVL3 5G12
KASQDINVYLS (SEQ ID NO:198)
CDR2 hVL3 5G12
RANRLVD (SEQ ID NO:36)
CDR3 hVL3 5G12
LQYDEFPYT (SEQ ID NO:43)
hVL4 5G12
DIQMTQSPSSLSASVGDRVTITCKASQDIQSYLSWFQQKPGKAPKTLIYRANRLVDGVP SRFSGSGSGTDYTLTISSLQPEDFATYYCLQYDEFPYTFGGGTKVEIK (SEQ ID NO:199)
CDR1 hVL4 5G12
KASQDIQSYLS (SEQ ID NO:200)
CDR2 hVL4 5G12
RANRLVD (SEQ ID NO:36)
CDR3 hVL4 5G12
LQYDEFPYT (SEQ ID NO:43)
hVL5 5G12
DIQMTQSPSSLSASVGDRVTITCKASQDINVYLSWFQQKPGKAPKTLIYRANRLTSGVP SRFSGSGSGTDYTLTISSLQPEDFATYYCLQYDEFPYTFGGGTKVEIK (SEQ ID NO:201)
CDR1 hVL5 5G12
KASQDINVYLS (SEQ ID NO:198)
CDR2 hVL5 5G12
RANRLTS (SEQ ID NO:202)
CDR3 hVL5 5G12
LQYDEFPYT (SEQ ID NO:43)
hVH1 5G12
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWITWVRQAPGQGLEWMGDIYSGSDTMH YAEKFQGRVTLTVDTSTSTAYMELSSLRSEDTAVYYCARWWDYGSSYDYFDYWGQGTLVTVSS (SEQ ID NO:203)
CDR1 hVH1 5G12
SYWIT (SEQ ID NO:204)
CDR2 hVH1 5G12
DIYSGSDTMHYAEKFQG (SEQ ID NO:205)
CDR3 hVH1 5G12
WWDYGSSYDYFDY (SEQ ID NO:71)
hVH2 5G12
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWITWVRQAPGQGLEWMGDIYSGSDTTH YAEKFQGRVTLTVDTSTSTAYMELSSLRSEDTAVYYCARWWDYGSSYDYFDYWGQGTLVTVSS (SEQ ID NO:206)
hVH2 CDR1
SYWIT (SEQ ID NO:204)
hVH2 CDR2
DIYSGSDTTHYAEKFQG (SEQ ID NO:374)
hVH2 CDR3
WWDYGSSYDYFDY (SEQ ID NO:71)
hVH3 5G12
QVQLVQSGAEVKKPGASVKVSCKASGYTFTSYWISWVRQAPGQGLEWMGDIYSGSDTTH YAEKFQGRVTLTVDTSTSTAYMELSSLRSEDTAVYYCARWWDYGSSYDYFDYWGQGTLVTVSS (SEQ ID NO:207)
CDR1 hVH3 5G12 SYWIS (SEQ ID NO:208)
CDR2 hVH3 5G12
DIYSGSDTTHYAEKFQG (SEQ ID NO:374)
CDR3 hVH3 5G12
WWDYGSSYDYFDY (SEQ ID NO:71)
Пример 8: Мембраносвязанный S15 является иммуносупрессорным.
Материалы и методы
Способ для анализа Т–клеточной супрессии в PMBC in vitro:
периферические мононуклеарные клетки крови (PBMC), полученные в результате афереза богатых лейкоцитами продуктов здорового донора (KeyBiologics, Мемфис, Теннеси), собирали с помощью стандартной процедуры с использованием градиента фиколла с последующей криоконсервацией. В день анализа замороженные PBMC размораживали, промывали полной средой RPMI (RPMI–C, RPMI [ThermoFisher] + 10% сывороткой FetalClone III [HyClone]) и подсчитывали. Клетки метили 5 мкM CFSE (ThermoFisher) в RPMI–C в течение 10 минут при 37oC, с последующими двумя промываниями RPMI–C. Все PMBC (3E05 клеток/лунка) высевали в 96–луночные плоскодонные планшеты Corning Costar, которые предварительно покрывали анти–человеческий CD3 антителом (OKT3, 50 нг/мл; eBioScience) в течение ночи при 4oC. Слитый белок SIGLEC–15–Fc hG1 добавляли в лунки в указанных конечных концентрациях. Клетки культивировали в течение 72 часов при 37oC. Через 72 часа 50 мкл супернатанта собирали из лунок и незамедлительно замораживали для анализа уровней цитокинов. Затем клетки собирали из каждой лунки с помощью пипетирования и переносили в круглодонный планшет для проточно–цитометрического окрашивания и анализа. Fc–рецепторы блокировали FcX TruStain (2 мкл/лунка; Biolegend), с последующим окрашиванием антителами против CD4 APC–eFluor 780 (2 мкл/лунка; ThermoFisher) и CD8 eFluor 450 (2 мкл/лунка; ThermoFisher) в течение одного часа при 4oC. После инкубации планшеты промывали дважды буфером для FACS (PBS, содержащий 1% сыворотку FetalClone III). Клетки ресуспендировали в 150 мкл буфера для фиксации (3% формальдегид в PBS) и анализировали с помощью проточного цитометра YETI (Propel Labs). Данные анализировали с помощью FlowJo. Данные представляли в виде процента клеток, которые делятся, на основании разведения CFSE по сравнению с нестимулированными CD4+ и CD8+ T–клетками. Супернатанты анализировали с помощью набора U–PLEX (Meso Scale Diagnostics [MSD)]) в отношении IFN–γ, TNF–α и IL–6 в соответствии с инструкциями. U–PLEX считывали с помощью инструмента Meso QuickPlex SQ 120.
Результаты
Мембраносвязанный S15 является иммуносупрессорным. На Фиг. 14A изображена линейная диаграмма % пролиферации T–клеток против человеческого Fc S15 (мкг/мл), которая показывает, что % пролиферации T–клеток снижается по мере того, как повышается концентрация Fc S15. PBMA человека метили CFSE и добавляли к анти–0CD3 (OKT3) антителам, покрывающих 96–луночные планшеты, и культивировали в течение 3 дней со слитым белком Fc S15 человека при указанных концентрациях. На Фиг. 14B изображена столбиковая диаграмма пг/мл IFN–γ в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15. На Фиг. 14С изображена столбиковая диаграмма пг/мл TNF–α в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15. На Фиг. 14D изображена столбиковая диаграмма пг/мл IL–6 в кондиционированных супернатантах из клеток, обработанных 0 или 5 мкг/мл Fc S15.
Пример 9: Связывания анти–s15 mAb, очищенного из гибридомы, с клетками, экспрессирующими S15 человека или s15 мыши.
Материалы и методы
Клетки 293T, стабильно экспрессирующие S15 человека (293T.hS15), и клетки MC38, стабильно экспрессирующие S15 мыши (MC38.mS15), собирали из культуры тканей. После одной промывки PBS клетки засевали в 96–луночный планшет с U–образным дном (5E04 клеток/лунка) в целях окрашивания. Сначала клетки смешивали с 1 мкг указанных антител, очищенных из гибридом мыши в буфере для окрашивания для FACS (PBS, содержащий 1% сыворотки FetalClone III) и инкубировали в течение 30 минут на льду. Затем клетки промывали один раз буфером для FACS с последующей инкубацией с конъгированным PE анти–мышиный Ig антителом (eBioscience) в течение 30 минут на льду. Клетки промывали один раз буфером для FACS и ресуспендировали в 100 мкл буфера для FACS перед анализом с помощью проточного цитометра YETI (Propel Labs). Данные анализировали с помощью FlowJo. Данные предсталяли в виде процента клеток, которые являются PE позитивными в общей клеточной популяции, гейтированной с помощью прямого светорассеяния (FSC) и бокового светорассеяния (SSC).
Результаты
На Фиг. 15A и 15B изображен процент позитивных клеток в отношении связывания анти–S15 mAb, очищенного из гибридомы, с клетками, экспрессирующими человеческий S15 или мышиный S15. Связывание оценивали с помощью анализа FACS клеток, инкубированных с указанными антителами с последующим инкубированием с PE конъюгированным анти–мышиный Ig антителом. Клетки анализировали в отношении PE+ популяций с помощью FACS.
Пример 10: Очищенные анти–S15 mAb из гибридом обращают опосредованную мембраносвязанным S15 супрессию.
Материалы и методы
Способ исследования обращения опосредованной Fc SIGLEC–15 супрессии с помощью анти–SIGLEC–15 mAb в анализе Т–клеточной пролиферации во всех PBMC:
так же, как и на Фиг. 14, выше, с незначительными изменениями:
периферические мононуклеарные клетки крови (PBMC), полученные в результате афереза богатых лейкоцитами продуктов здорового донора (KeyBiologics, Мемфис, Теннеси), собирали с помощью стандартной процедуры с использованием градиента фиколла с последующей криоконсервацией. В день анализа замороженные PBMC размораживали, промывали полной средой RPMI (RPMI–C, RPMI [ThermoFisher] + 10% сывороткой FetalClone III [HyClone]) и подсчитывали. Клетки метили 5 мкM CFSE (ThermoFisher) в RPMI–C в течение 10 минут при 37°C, с последующими двумя промываниями RPMI–C. Все PMBC (3E05 клеток/лунка) высевали в 96–луночные плоскодонные планшеты Corning Costar, которые предварительно покрывали анти–человеческий CD3 антителом (OKT3, 50 нг/мл; eBioScience) в течение ночи при 4°C. Слитый белок SIGLEC–15–hG1 добавляли в лунки при 5 мкг/мл (конечная концентрация). Указанные анти–SIGLEC–15 mAb затем добавляли к указаным лункам при 12 мкг/мл (конечная концентрация). Клетки культивировали в течение 72 часов при 37°C. Через 72 часа 50 мкл супернатанта собирали из лунок и незамедлительно замораживали для анализа уровней цитокинов. Затем клетки собирали из каждой лунки с помощью пипетирования и переносили в круглодонный планшет для проточно–цитометрического окрашивания и анализа. Fc–рецепторы блокировали FcX TruStain (2 мкл/лунка; Biolegend), с последующим окрашиванием антителами против CD4 APC–eFluor 780 (2 мкл/лунка; ThermoFisher) и CD8 eFluor 450 (2 мкл/лунка; ThermoFisher) в течение одного часа при 4°C. После инкубации планшеты промывали дважды буфером для FACS (PBS, содержащий 1% сыворотку FetalClone III). Клетки ресуспендировали в 150 мкл буфера для фиксации (3% формальдегид в PBS) и анализировали с помощью проточного цитометра YETI (Propel Labs). Данные анализировали с помощью FlowJo. Данные представляли в виде процента клеток, которые делятся, на основании разведения CFSE по сравнению с нестимулированными CD4+ и CD8+ T–клетками. Супернатанты анализировали с помощью набора U–PLEX (Meso Scale Diagnostics [MSD)]) в отношении IFN–γ, TNF–α и IL–6 в соответствии с инструкциями. U–PLEX считывали с помощью инструмента Meso QuickPlex SQ 120.
Результаты
На Фиг. 16A и 16B изображены столбиковые диаграммы процента поделившихся CD8+ T–клеток, обработанных указанными антителами. На Фиг. 16С и 16D изображены столбиковые диаграммы процента поделившихся CD4+ T–клеток, обработанных указанными антителами.
Пример 11: биологическая активность in vivo очищенных 5G12 в трех опухолевых моделях.
Материалы и методы
Способы для опухолевых моделей in vivo:
Модель колоректальной опухоли
Фиг. 17A: Опухолевые клетки MC38 (ATCC), трансдуцированные и отсортированные в отношении сверхэкспресси SIGLEC–15, инъецировали подкожно по 2E05 клеток в 100 мкл в выбритый правый бок мышей C57BL/6N (Charles River). Пяти мышам/группа обработки вводили 200 мкг контрольного IgG (Innovative Research) или очищенного не содержащего эндотоксина анти–SIGLEC–15 антитела противлона 5G12 через шесть дней после инъекции. Обработки продолжали каждые четыре дня в общей сложности четырьмя дозами. Опухоль измеряли 3 раза на каждой неделе. Объем опухоли рассчитывали в виде (длина × ширина^2)*0,5. Мышей выводили из эксперимента, когда опухоль достигала 2000 мм3.
Опухолевая модель лимфомы
Фиг. 17B: Опухолевые клетки EG7 (ATCC) представляют собой опухолевые клетки EL4, трансфицированные в целях экспрессии овальбумина куриного яйца (OVA). Клетки культивировали в течение 10 дней перед подкожной инъекцией 2E05 опухолевых клеток в выбритый правый бок мышей C57BL/6N (Charles River). Десять мышей/группа обработки обрабатывали 200 мкг контрольного IgG или очищенного не содержащего эндотоксина анти–SIGLEC–15 антитела противлона 5G12. Обработки начинали через восемь дней после инъекции EG7 и мышей обрабатывали каждые четыре дня в общей сложности четырьмя дозами. Объем опухоли рассчитывали в виде (длина × ширина^2)*0,5. Мышей выводили из эксперимента, когда опухоль достигала 2000 мм3 или когда опухоли достигала среднего диаметра 15 см.
Модель рака яичника
Фиг. 17C: Опухолевые клетки ID8–OVA представляют собой клеточную линию ID8 рака яичников мышей, стабильно трансфицированную в целях экспрессии овальбумина куриного яйца (OVA). Клетки культивировали в течение 10 дней перед интраперитонеальной инъекцией 5E06 клеток. Через три недели мышам адаптивно переносили с помощью интраперитонеальной инъекции 5E05 OT–I Tg/Rag2–/– T–клеток, которые выделяли с помощью CD8+ T–клеточной негативной селекции (Miltenyi Biotec). Обработку начинали через один день (день 22; n=10/группа). Мыши получали 200 мкг каждые четыре дня в общей сложности 5 доз контрольного IgG или очищенного не содержащего эндотоксина анти–SIGLEC–15 антитела противлона 5G12. Мышей взвешивали через 30 дней после инъекции опухоли и опухолевую нагрузку анализировали с помощью прибавки веса. Данные представляли в виде процента прибавки веса на мышь от исходного веса в течение 30 дней. Мышей выводили из эксперимента при достижении 150% прибавки веса или более 30 грамм.
Результаты
5G12 показало повышение процента выживаемости в колоректальной модели (Фиг. 17A) и модели лимфомы (Фиг. 17B). 5G12 также показало снижение опухолевой нагрузки (Фиг. 17C). На Фиг. 18 изображен процент выживаемости после инокуляции ID8/OVA.
Пример 12: Оценка аффинности рекомбинантных mAb в отношении мономерного белка S15
Эксперименты с оптимизированной KD осуществляли с использованием инструмента ForteBio Octet RED96 с помощью сенсоров захвата анти–человеческий Fc антитела (AHC, 18–5060; ForteBio). Буфер для анализа предсталял собой PBS, содержащий 0,05% Твин–20, а буфер для регенерации представлял собой 10 мМ глицин (pH 1,5). Сначала антитела загружали при 1 мкг/мл в течение 600 секунд. Затем следовал второй исходный этап длительностью 60 секунд, этап ассоциации длительностью 300 секунд в мономере внеклеточного домена (ECD) S15 и в конечном итоге этап диссоциации длительностью 1200 секунд. Концентрации мономера варьировали от 100 нМ до 1,56 нМ в сериях с двухкратным разведением, также включали холостую лунку. Данные обрабатывали с помощью компьютерной программы для анализа данных ForteBio версии 7.0; использовали глобальное сходство в сочетании с вычитанием эталонных лунок. Описанные значения представляют собой среднее по меньшей мере из трех независимых октетных циклов.
Результаты представлены в Табл. 1.
Таблица 1: Оценка аффинности рекомбинантных mAb в отношении мономерного белка S15 (n=3–6 циклов)
Пример 13: Эпитоп–специфическая сортировка анти–S15 mAb
Эксперименты с эпитоп–специфической сортировкой осуществляли с использованием инструмента ForteBio Octet RED96 с помощью стрептавидиновых (SA, 18–5019; ForteBio) сенсоров. После второго исходного этапа длительностью 30 секунд меченый биотином слитый белок S15–mG1 загружали на сенсоры при 10 мкг/мл в течение 600 секунд. За этим следовал второй этап ассоциации длительностью 600 секунд в 1–м антителе (30 мкг/мл), второй исходный этап длительностью 30 секунд и второй этап ассоциации длительностью 400 секунд во 2–м антителе (15 мкг/мл). Буфер для анализа представлял собой PBS, а буфер для регенерации представлял собой 10 мМ глицин (pH 3,0). Данные обрабатывали с помощью компьютерной программы для анализа данных ForteBio версии 7.0, а кривые в отношении 2–го антитела отдельно анализировали в отношении конкурентного связывания. Кривая во время второго этапа ассоциации, которая отличается от таковой первого этапа ассоциации, указывает на связывание с незанятым эпитопом. Отсутствие дополнительного связывания указывает на блокирование эпитопа.
Результаты представлены в Табл. 2.
Таблица 2: Эпитоп–специфическая сортировка S15
Пример 14: Aнти–человеческий S15 антитело клона 1H3 ингибирует образование остеокластов у человека in vitro
Материалы и методы
PBMC выделяли в результате афереза богатых лейкоцитами продукта, приобретенного в Key Biologics, LLC. Богатый лейкоцитами продукт наслаивали на прокладку из фиколла и центрифугировали в течение 30 минут при 400 RCF. Клетки в интерфазе фиколла удаляли, промывали 3 раз в PBS и затем замораживали в FBS с 10% DMSO. В день эксперимента флакон замороженных PBMC удаляли из хранения в жидком азоте и размораживали. Моноциты выделяли с помощью набора для выделения моноцитов MACS (130–096–537; Miltenyi Biotec) согласно инструкциям производителя. Выделенные клетки на 99% были жизнеспособными. Клетки высевали в 96–луночные плоскодонные планшеты для культивирования тканей при плотности 3E05 клеток/см2, 1E05 клеток в 100 мкл среды для анализа на лунку. Среда для анализа состояла из среды α–MEM (Gibco 32571–036) с добавлением 10% FBS, 1 мМ пирувата натрия, 25 нг/мл макрофагального колониестимулирующего фактора человека (Miltenyi, 103–096–491) и 30 нг/мл RANKL человека (Miltenyi, 130–093–988). Клетки прикреплялись к планшету за 3,5 часа до добавления 10 мкл 50 мкг/мл анти–S15 антитела, конечная концентрация составляла 4,55 мкг/мл. Для каждого антитела оценивали три лунки. Через три дня после инкубации среду заменяли и добавляли свежие антитела. На седьмые сутки супернатанты переносили из исходных планшетов в круглодонные 96–луночные планшеты и центрифугировали с удалением клеточного дебриса. Моноциты/остеокласты окрашивали с помощью набора для окрашивания TRAP от B–Bridge International, Inc. (PMC–AK04F–COS) согласно инструкциям производителя и получали изображение с помощью Invitrogen EVOS FL Color. Для оценки уровней TRAP (устойчивой к тартрату кислой фосфатазы) в супернатанте 50 мкл буфера из набора для окрашивания TRAP комбинировали с 9 мкл супернатанта и инкубировали при 37°C в течение трех часов. Фиксировали поглощение в каждой лунке при 540 нМ. Оставшийся супернатант замораживали при –80°C для более позднего анализа цитокинов.
Результаты
На Фиг. 19A изображена схематическая диаграмма, которая показывает CD14+ моноциты человека, собранные из PBMC человека с помощью магнитных гранул для культивирования моноцитов Mitenyi после высевания в 96–луночных планшетах в присутствии M–CSF человека и RANKL человека совместно с указанными антителами. На Фиг. 19B изображена микрофотография, показывающая остеокласты. На Фиг. 19C изображена столбиковая диаграмма поглощения при 540 нм супернатанта, собранного через 7 дней, для анализа устойчивой к тартрату кислотой фосфатазы.
Пример 15: 1H3 ослабляет продуцирование IL–6 и TNF–α, опосредованной M–CSF и RANKL в моноцитах человека
Материалы и методы
Супернатанты из лунок с No–RANKL (только M–CSF), контрольным mAB (M–SCF+RANKL+контрольное mAb) и 1H3 (M–CSF+RANKL+1H3) из эксперимента, описанного выше, собирали и исследовали для анализа цитокинов.
Результаты
На Фиг. 20 изображена столбиковая диаграмма, которая показывает цитокины (пг/мл) INF–γ, IL–2, IL–4, IL–6, IL–10, IL–17A и TNF–α.
Пример 16: Aнти–человеческий S15 mAb 1H3 предупреждает образование остеокластов у мыши in vitro
Материалы и методы
Макрофаги мышей RAW 264.7 высевали в плоскодонный 96–луночный планшет при плотности 1,5E04 клеток/см2, 4800 клеток в 90 мкл среды на лунку. Среда состояла из DMEM с 10% FBS, 1 мM пирувата натрия и 50 нг/мл RANKL мыши (eBioscience, 14–8612–80). Клетки оставляли для прикрепления в течение двух часов перед добавлением 10 мкл указанного антитела (50 мкг/мл) в лунки, приводя к конечной концентрации 5 мкг/мл; антитела оценивали в трех лунках. Клетки дифференцировались в течение пяти дней, в течение этого времени клетки окрашивали и супернатант анализировали в отношении содержания TRAP, как описано выше.
Результаты
На Фиг. 21 изображена столбиковая диаграмма поглощения при 540 нм макрофагов RAW 264.7 мыши, культивированных в присутствии RANKL совместно с указанными антителами.
Пример 17: Экспрессия SIGLEC–15 повышена в макрофагах M2 человека
Материалы и методы
Экспрессия SIGLEC–15
CD14+ моноциты человека выделяли из PBMC человека с помощью набора магнитных гранул для негативной селекции (Miltenyi Biotec) и обрабатывали M–CSF в течение 3 дней, затем клетки культивировали в присутствии IL–10 (поляризация макрофагов M2) или IFN–γ/LipiA (поляризация макрофагов M1) еще в течение 3 дней. Экспрессию SIGLEC–15 на клеточной поверхности выявляли с помощью окрашивания анти–SIGLEC–15 антителом с последующим анализом FACS.
Индукция экспрессии SIGLEC–15
Клетки костного мозга мыши собирали от мышей Balb/C. Прикрепившиеся клетки удаляли с помощью присоединения к пластмассовой чашке для культивирования. Плавающие гематопоэтические клетки мыши собирали и обрабатывали M–CSF в течение 3 дней с последующей прямой обработкой M–CSF или обработкой M–CSF+IL–10 еще в течение 4 дней. Обработанные клетки собирали и окрашивали маркерами миелоидных клеток (CD11b и F4/80) и мечеными PE анти–S15 антителами с помощью анализа FACS. Средняя интенсивность флуоресценции PE изображена на графике в нижней панели. M–CSF слегка повышал экспрессию S15.
Результаты
Экспрессию SIGLEC–15 наблюдали в макрофагах M2 человека (Фиг. 25A), но не в макрофагах M1 человека (Фиг. 25B).
M–CSF и IL–10 повышают экспрессию S15 в миелоидных клетках, происходящих из костного мозга мыши (Фиг. 25C–25E).
Пример 18: SIGLEC–15 способствует выживанию миелоидных клеток человека и повышает продуцирование провоспалительных цитокинов
Материалы и методы
CD14+ моноциты человека сначала выделяли из PBMC человека (от 2 здоровых доноров) с помощью набора магнитных гранул для негативной селекции (Miltenyi Biotec) и высевали в 96–луночном планшете, покрытым слитым белком SIGLEC–15 (иммобилизированный SIGLEC–15) или без покрытия. но с добавлением слитого белка SIGLEC–15 в культуральную среду (растворенный SIGLEC–15) в концентрации, показанной на фигуре. Через шесть дней кондиционированный супернатант собирали для анализа цитокинов с помощью набора MSD. Жизнеспособность клеток оценивали с помощью добавления в планшет XTT (ThermoFisher). Через 2 часа после культивирования клеточный метаболизм/жизнеспособность измеряли с помощью считывания поглощения при 450 нм.
Результаты
Более высокое поглощение выявляли в лунках, как с иммобилизированным Fc SIGLEC–15, так и с растворенным Fc SIGLEC–15. Анализ цитокинов показал, что S15 дозозависимо повышал продуцирование TNF–α, IL–6 и IL–1β в обработанных лунках (данные из лунок с растворенным S15 представлены в данном документе).
Пример 19: Обработанные Fc SIGLEC–15 миелоидные клетки человека влияют на функцию T–клеток человека
Материалы и методы
На Фиг. 27A изображена схематическая диаграмма для следующего эксперимента. CD14+ моноциты человека выделяли из PBMC человека (от 2 здоровых доноров) с помощью набора магнитных гранул для негативной селекции (Miltenyi Biotec) и обрабатывали Fc SIGLEC–15 в течение 6 дней, как описано выше, или поляризовали в отношении макрофагов M2 или M1, или обрабатывали GM–CSF и IL–4 для дифференцировки клеток до незрелых дендритных клеток (imDC). Клетки собирали с помощью осторожного соскребывания из чашки для культивирования. После центрифугирование клетки ресуспендировали и кокультивировали с мечеными CFSE негативно селектированными аутологичными всеми T клетками при соотношении 1 миелоидная клетка: 2 T–клетки совместно с анти–CD3/CD28 гранулами (1 клетка из всех T–клеток: 2 гранулы). Через пять дней кондиционированный супернатант собирали для анализа цитокинов с помощью мультиплексного набора MSD от MSD. Клетки собирали и окрашивали анти–CD4 и анти–CD8 антителами. T–клеточную пролиферацию анализировали с помощью анализа FACS в целях измерения разведенной CFSE клеточной популяции.
Результаты
Данные показали, что обработанные Fc SIGLEC–15 миелоидные клетки ослабляли опосредованную анти–CD3/CD28 гранулами CD4 и CD8 T–клеточную пролиферацию с использованием клеток от этого конкретного донора (донор №1707), а супрессия не была такой же выраженной, как в случае макрофагов M2 (Фиг. 27B–27G). Анализ цитокинов показал, что обработанные S15 миелоидные клетки значимо нарушали опосредованное анти–CD3/CD28 гранулами продуцирование IFN–γ, TNF–α, IL–6 и IL–10. Данные от других исследуемых доноров показали, что обработанные S15 клетки ограничивали супрессию T–клеточной пролиферации, однако в большинстве случаев заметную супрессию продукции цитокинов.
Пример 20: Анти–SIGLEC–15 mAb дозозависимо блокировало опосредованный S15 эффект выживания миелоидных клеток человека
Материалы и методы
CD14+ моноциты человека выделяли из PBMC человека (от 2 здоровых доноров) с помощью набора магнитных гранул для негативной селекции (Miltenyi Biotec) и высевали в 96–луночный планшет с 5 мкг/мл слитого белка Fc S15 совместно с mAb в случае SIGLEC–15, серийно разведенного в соотношении 1:2 исходя из 20 мкг/мл. Клетки культивировали в течение 7 дней. Жизнеспособность/метаболизм клеток оценивали с помощью добавления в планшет XTT (ThermoFisher). Через 2 часа после культивирования клеточный метаболизм/жизнеспособность измеряли с помощью считывания поглощения при 450 нм. Высокое поглощение выявляли в лунках со слитым белком Fc S15 без каких–либо антител (mAb отсутствует). Низкое поглощение получали в лунках без слитого белка Fc S15 (Fc S15 отсутствует).
Результаты
Анти–SIGLEC–15 mAb дозозависимо снижало поглощение (нижняя линия). Контрольное антитело (верхняя линия) не оказывало влияния на выживание и метаболизм клеток. На Фиг. 28A (донор 1709) и 28B (донор 1713) изображено, что анти–S15 mAb дозозависимо блокировало опосредованный S15 эффект выживания в миелоидных клетках человека.
Пример 21: SIGLEC–15 играет основную роль в образовании остеокластов
M–CSF, экспрессируемый на остеобластах и стромальных клетках, индуцирует экспрессию SIGLEC–15 на миелоидных клетках, который взаимодействуют с партнером по связыванию SIGLEC–15 как в цис–, так и транс–положении и стимулирует миелоидные клетки продуцировать провоспалительные цитокины, такие как TNF–α, IL–6 и IL–1β и повышать экспрессию αvβ3 интегрина. Совместно с передачей сигнала с участием RANKL, клетки–предшественники остеокластов сливаются и образуют многоядерные остеокласты (Фиг. 29).
Пример 22: SIGLEC–15 индуцирует экспрессию интегрина αvβ3 в CD14+ моноцитах человека
Материалы и методы
CD14+ моноциты человека выделяли из PBMC человека с помощью набора магнитных гранул для негативной селекции (Miltenyi Biotec) и обрабатывали 5 мкг/мл слитого белка Fc S15 в течение 6 дней. Через шесть дней обработанные Fc S15 миелоидные клетки собирали и окрашивали анти–αvβ3 интегрин антителом (клон 23C6).
Результаты
По сравнению с окрашиванием изотипическим контрольным антителом, а также окрашиванием клеток до обработки Fc S15 на сутки 0, экспрессия αvβ3 интегрина была повышенной в миелоидных клетках с обработкой Fc S15 (Фиг. 30A и 30B).
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же самые значения, как обычно понимается специалистом в области техники, к которой принадлежит раскрываемое изобретение. Публикации, цитируемые в данном документе, и материалы, в отношении которых они цитируются, включены явно посредством ссылки.
Специалистам в данной области техники будут понятны многие эквиваленты конкретных вариантов осуществления изобретения, описанного в данном документе, или с помощью проведения обычных экспериментов они будут способны установить такие эквиваленты. Предполагается, что такие эквиваленты охвачены следующей формулой изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> НЕКСТКЬЮР, ИНК.
ЛЬЮ, Линда
ФЛИС, Даллас, Бенджамин
ЛАНГЕРМАНН, Соломон
<120> АНТИТЕЛА ПРОТИВ SIGLEC–15 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 064467.003US
<140> 16/334,409
<141> 2019-03-19
<150> 62/397,794
<151> 2016-09-21
<150> 62/451,271
<151> 2017-01-27
<150> 62/500,578
<151> 2017-05-03
<150> PCT/US17/52714
<151> 2017-09-21
<160> 374
<170> PatentIn version 3.5
<210> 1
<211> 328
<212> Белок
<213> Homo sapiens
<400> 1
Met Glu Lys Ser Ile Trp Leu Leu Ala Cys Leu Ala Trp Val Leu Pro
1 5 10 15
Thr Gly Ser Phe Val Arg Thr Lys Ile Asp Thr Thr Glu Asn Leu Leu
20 25 30
Asn Thr Glu Val His Ser Ser Pro Ala Gln Arg Trp Ser Met Gln Val
35 40 45
Pro Pro Glu Val Ser Ala Glu Ala Gly Asp Ala Ala Val Leu Pro Cys
50 55 60
Thr Phe Thr His Pro His Arg His Tyr Asp Gly Pro Leu Thr Ala Ile
65 70 75 80
Trp Arg Ala Gly Glu Pro Tyr Ala Gly Pro Gln Val Phe Arg Cys Ala
85 90 95
Ala Ala Arg Gly Ser Glu Leu Cys Gln Thr Ala Leu Ser Leu His Gly
100 105 110
Arg Phe Arg Leu Leu Gly Asn Pro Arg Arg Asn Asp Leu Ser Leu Arg
115 120 125
Val Glu Arg Leu Ala Leu Ala Asp Asp Arg Arg Tyr Phe Cys Arg Val
130 135 140
Glu Phe Ala Gly Asp Val His Asp Arg Tyr Glu Ser Arg His Gly Val
145 150 155 160
Arg Leu His Val Thr Ala Ala Pro Arg Ile Val Asn Ile Ser Val Leu
165 170 175
Pro Ser Pro Ala His Ala Phe Arg Ala Leu Cys Thr Ala Glu Gly Glu
180 185 190
Pro Pro Pro Ala Leu Ala Trp Ser Gly Pro Ala Leu Gly Asn Ser Leu
195 200 205
Ala Ala Val Arg Ser Pro Arg Glu Gly His Gly His Leu Val Thr Ala
210 215 220
Glu Leu Pro Ala Leu Thr His Asp Gly Arg Tyr Thr Cys Thr Ala Ala
225 230 235 240
Asn Ser Leu Gly Arg Ser Glu Ala Ser Val Tyr Leu Phe Arg Phe His
245 250 255
Gly Ala Ser Gly Ala Ser Thr Val Ala Leu Leu Leu Gly Ala Leu Gly
260 265 270
Phe Lys Ala Leu Leu Leu Leu Gly Val Leu Ala Ala Arg Ala Ala Arg
275 280 285
Arg Arg Pro Glu His Leu Asp Thr Pro Asp Thr Pro Pro Arg Ser Gln
290 295 300
Ala Gln Glu Ser Asn Tyr Glu Asn Leu Ser Gln Met Asn Pro Arg Ser
305 310 315 320
Pro Pro Ala Thr Met Cys Ser Pro
325
<210> 2
<211> 342
<212> Белок
<213> Mus musculus
<400> 2
Met Glu Gly Ser Leu Gln Leu Leu Ala Cys Leu Ala Cys Val Leu Gln
1 5 10 15
Met Gly Ser Leu Val Lys Thr Arg Arg Asp Ala Ser Gly Asp Leu Leu
20 25 30
Asn Thr Glu Ala His Ser Ala Pro Ala Gln Arg Trp Ser Met Gln Val
35 40 45
Pro Ala Glu Val Asn Ala Glu Ala Gly Asp Ala Ala Val Leu Pro Cys
50 55 60
Thr Phe Thr His Pro His Arg His Tyr Asp Gly Pro Leu Thr Ala Ile
65 70 75 80
Trp Arg Ser Gly Glu Pro Tyr Ala Gly Pro Gln Val Phe Arg Cys Thr
85 90 95
Ala Ala Pro Gly Ser Glu Leu Cys Gln Thr Ala Leu Ser Leu His Gly
100 105 110
Arg Phe Arg Leu Leu Gly Asn Pro Arg Arg Asn Asp Leu Ser Leu Arg
115 120 125
Val Glu Arg Leu Ala Leu Ala Asp Ser Gly Arg Tyr Phe Cys Arg Val
130 135 140
Glu Phe Thr Gly Asp Ala His Asp Arg Tyr Glu Ser Arg His Gly Val
145 150 155 160
Arg Leu Arg Val Thr Ala Ala Ala Pro Arg Ile Val Asn Ile Ser Val
165 170 175
Leu Pro Gly Pro Ala His Ala Phe Arg Ala Leu Cys Thr Ala Glu Gly
180 185 190
Glu Pro Pro Pro Ala Leu Ala Trp Ser Gly Pro Ala Pro Gly Asn Ser
195 200 205
Ser Ala Ala Leu Gln Gly Gln Gly His Gly Tyr Gln Val Thr Ala Glu
210 215 220
Leu Pro Ala Leu Thr Arg Asp Gly Arg Tyr Thr Cys Thr Ala Ala Asn
225 230 235 240
Ser Leu Gly Arg Ala Glu Ala Ser Val Tyr Leu Phe Arg Phe His Gly
245 250 255
Ala Pro Gly Thr Ser Thr Leu Ala Leu Leu Leu Gly Ala Leu Gly Leu
260 265 270
Lys Ala Leu Leu Leu Leu Gly Ile Leu Gly Ala Arg Ala Thr Arg Arg
275 280 285
Arg Leu Asp His Leu Val Pro Gln Asp Thr Pro Pro Arg Ser Gln Ala
290 295 300
Gln Glu Ser Asn Tyr Glu Asn Leu Ser Gln Met Ser Pro Pro Gly His
305 310 315 320
Gln Leu Pro Arg Val Cys Cys Glu Glu Leu Leu Ser His His His Leu
325 330 335
Val Ile His His Glu Lys
340
<210> 3
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 3
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 4
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 4
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Phe Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 5
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 5
Asp Ile Gln Met Thr Gln Ala Ser Ser Ser Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Lys Asp Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 6
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 6
Gln Ile Ile Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Thr Ser Phe Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Thr Ser Pro Lys Arg Trp Ile Phe
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ile Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Thr Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys His Gln Arg Ser Ala Tyr Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 7
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 7
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105
<210> 8
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 8
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg
<210> 9
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 9
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp Phe Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Arg Met Ser Asn Leu Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Gly Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln His
85 90 95
Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 10
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 10
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Ser Gly Ala Val Thr Thr Gly
20 25 30
Asn Phe Ala Asn Trp Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly
35 40 45
Leu Ile Gly Gly Thr Asn Asn Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Ile Gly Asp Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Thr Glu Asp Glu Ala Ile Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 11
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 11
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 12
<211> 109
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 12
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly
35 40 45
Leu Ile Gly Gly Thr Asn Asn Arg Ala Pro Gly Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Ile Gly Asp Lys Ala Ala Leu Thr Ile Thr Gly Ala
65 70 75 80
Gln Thr Glu Asp Glu Ala Ile Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
His Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 13
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 13
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Ser Gly Ser Ser Ile Ile Tyr Tyr Ala Asp Thr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Thr Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Gly Asn Gly Ser Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 14
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 14
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Lys Ile Gly Pro Gly Ser Val Ser Ile Tyr Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Ser Tyr Tyr Tyr Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ala
115
<210> 15
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 15
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Val Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 16
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 16
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Ser Gly Ser Ser Ile Leu Tyr Tyr Ala Asp Ile Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Thr Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Gly Asn Gly Ser Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 17
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 17
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Lys Glu Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Glu Asp Gly Asp Ile Glu Tyr Asp Pro Lys Phe
50 55 60
Gln Gly Lys Ala Thr Met Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Phe Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Thr Asp Tyr Asp Tyr Asp Gly Gly Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 18
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 18
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Ile Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile Tyr Cys Gly Ser Asp Thr Met His Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 19
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 19
Gln Val Gln Leu Lys Gln Ser Gly Pro Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Glu Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg Pro Gly Arg Gly Leu Glu Trp Ile
35 40 45
Gly Lys Ile Gly Pro Gly Ser Val Ser Ile Tyr Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Ser Tyr Tyr Tyr Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ala
115
<210> 20
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 20
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Lys Ile Gly Pro Glu Ser Val Ser Ile Tyr Tyr Ser Glu Lys Phe
50 55 60
Lys Ala Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Ser Tyr Tyr Tyr Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ala
115
<210> 21
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 21
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Gly Leu Ser Cys Glu Gly Ser Gly Phe Thr Phe Ser Gly Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Thr Pro Gly Lys Thr Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Ser Asp Gly Ser Ala Ile Asn Tyr Ala Pro Ser Ile
50 55 60
Lys Asp Arg Phe Thr Ile Phe Arg Asp Asn Asp Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Asn Val Arg Ser Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Tyr Asp Asp Tyr Gly Tyr Phe Asp Val Trp Gly Thr Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 22
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 22
His Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Leu Ile Trp Val Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Tyr Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Ile Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Ser Ser Ser Pro His Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu
100 105 110
Thr Val Ser Ser
115
<210> 23
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 23
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Gly Leu Ser Cys Glu Gly Ser Gly Phe Thr Phe Ser Asp Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Thr Pro Gly Lys Thr Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Ser Asp Gly Ser Ala Val Asn Tyr Ala Pro Ser Ile
50 55 60
Lys Asp Gln Phe Thr Ile Phe Arg Asp Asn Asp Lys Arg Thr Leu His
65 70 75 80
Leu Gln Met Ile Asn Val Arg Ser Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Tyr Asp Asp Tyr Gly Tyr Phe Asp Val Trp Gly Thr Gly Thr
100 105 110
Thr Val Thr Val Ser Ser
115
<210> 24
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 24
Arg Ser Ser Gln Ser Ile Val His Ser Asn Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 25
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Stnthetic construct
<400> 25
Arg Ser Ser Lys Ser Leu Leu His Ser Asn Gly Asn Thr Tyr Leu Tyr
1 5 10 15
<210> 26
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 26
Lys Ala Ser Asp His Ile Asn Asn Trp Leu Ala
1 5 10
<210> 27
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 27
Ser Ala Ser Ser Ser Thr Ser Phe Met His
1 5 10
<210> 28
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 28
Lys Ala Ser Gln Asp Ile Asn Ser Tyr Leu Ser
1 5 10
<210> 29
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 29
Arg Ser Ser Ser Gly Ala Val Thr Thr Gly Asn Phe Ala Asn
1 5 10
<210> 30
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 30
Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn
1 5 10 15
<210> 31
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 31
Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 32
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 32
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 33
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 33
Arg Met Ser Asn Leu Ala Ser
1 5
<210> 34
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 34
Gly Ala Thr Ser Leu Glu Thr
1 5
<210> 35
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 35
Asp Thr Ser Lys Leu Ala
1 5
<210> 36
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 36
Arg Ala Asn Arg Leu Val Asp
1 5
<210> 37
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 37
Gly Thr Asn Asn Arg Ala Pro
1 5
<210> 38
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 38
Leu Val Ser Lys Leu Asp Ser
1 5
<210> 39
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 39
Phe Gln Gly Ser His Val Pro Trp Thr
1 5
<210> 40
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 40
Met Gln His Leu Glu Tyr Pro Tyr Thr
1 5
<210> 41
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 41
Gln Gln Tyr Trp Ser Ser Pro Leu Thr
1 5
<210> 42
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 42
His Gln Arg Ser Ala Tyr Pro Trp Thr
1 5
<210> 43
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 43
Leu Gln Tyr Asp Glu Phe Pro Tyr Thr
1 5
<210> 44
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 44
Ala Leu Trp Tyr Ser Asn His Trp Val
1 5
<210> 45
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 45
Trp Gln Gly Thr His Phe Pro Phe Thr
1 5
<210> 46
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 46
Gly Phe Thr Phe Ser Asp Tyr Gly Met His
1 5 10
<210> 47
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 47
Gly Tyr Ile Phe Thr Asp Tyr Tyr Val Asn
1 5 10
<210> 48
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 48
Asn Tyr Gly Val His
1 5
<210> 49
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 49
Gly Phe Ser Phe Ser Asp Tyr Gly Met His
1 5 10
<210> 50
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 50
Gly Phe Asn Ile Lys Asp Tyr Tyr Met His
1 5 10
<210> 51
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 51
Gly Tyr Thr Phe Thr Ser Tyr Trp Ile Thr
1 5 10
<210> 52
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 52
Gly Tyr Thr Phe Thr Asp Tyr Tyr Val Asn
1 5 10
<210> 53
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 53
Gly Phe Thr Phe Ser Gly Phe Trp Met Ser
1 5 10
<210> 54
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 54
Gly Tyr Thr Phe Thr Ser Tyr Gly Leu Ile
1 5 10
<210> 55
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 55
Gly Phe Thr Phe Ser Asp Phe Trp Met Ser
1 5 10
<210> 56
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 56
Tyr Ile Ser Ser Gly Ser Ser Ile Ile Tyr Tyr Ala Asp Thr Val Lys
1 5 10 15
Gly
<210> 57
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 57
Lys Ile Gly Pro Gly Ser Val Ser Ile Tyr Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 58
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 58
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
<210> 59
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 59
Tyr Ile Ser Ser Gly Ser Ser Ile Leu Tyr Tyr Ala Asp Ile Val Lys
1 5 10 15
<210> 60
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 60
Arg Ile Asp Pro Glu Asp Gly Asp Ile Glu Tyr Asp Pro Lys Phe Gln
1 5 10 15
Gly
<210> 61
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 61
Asp Ile Tyr Cys Gly Ser Asp Thr Met His Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asn
<210> 62
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 62
Lys Ile Gly Pro Gly Ser Val Ser Ile Tyr Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asp
<210> 63
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 63
Lys Ile Gly Pro Glu Ser Val Ser Ile Tyr Tyr Ser Glu Lys Phe Lys
1 5 10 15
Ala
<210> 64
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 64
Asp Ile Asn Ser Asp Gly Ser Ala Ile Asn Tyr Ala Pro Ser Ile Lys
1 5 10 15
Asp
<210> 65
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 65
Glu Ile Tyr Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 66
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 66
Asp Ile Asn Ser Asp Gly Ser Ala Val Asn Tyr Ala Pro Ser Ile Lys
1 5 10 15
Asp
<210> 67
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 67
Asp His Tyr His Gly Asn Gly Ser Asp Tyr
1 5 10
<210> 68
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 68
Tyr Tyr Tyr Gly Phe Ala Tyr
1 5
<210> 69
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 69
His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
1 5 10 15
<210> 70
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 70
Asp Tyr Asp Tyr Asp Gly Gly Trp Phe Ala Tyr
1 5 10
<210> 71
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 71
Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr
1 5 10
<210> 72
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 72
Tyr Asp Asp Tyr Gly Tyr Phe Asp Val
1 5
<210> 73
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 73
Ser Ser Pro His Gly Asp Tyr
1 5
<210> 74
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 74
gatgttttga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagcattgta catagtaatg gaaacaccta tttagaatgg 120
tacctgcaga aaccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
tggacgttcg gtggaggcac caagctggaa atcaag 336
<210> 75
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 75
gatattgtga tgactcaggc tgcaccctct gtacctgtca ctcctggaga gtcagtatcc 60
atctcctgca ggtctagtaa gagtctcctg catagtaatg gcaacactta cttatattgg 120
ttcctgcaga ggccaggcca gtctcctcag ctcctgatat atcggatgtc caaccttgcc 180
tcaggagtcc cagacaggtt cggtggcagt gggtcaggaa ctgctttcac actgagaatc 240
agtagagtgg aggctgagga tgtgggtttt tattactgta tgcaacatct agaatatccg 300
tacacgttcg gaggggggac caggctggaa ataaaa 336
<210> 76
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 76
gacatccaga tgacacaggc ttcatcctcc ttgtctgtat ctctaggagg cagagtcacc 60
attacttgca aggcaagtga ccacattaat aattggttgg cctggtatca gcagaaacca 120
ggaaatgctc ctaggctctt aatatctggt gcaaccagtt tggaaactgg ggttccttca 180
agattcagtg gcagtggatc tggaaaggat tacactctca gcattaccag tcttcagact 240
gaagatgttg ctacttatta ctgtcaacag tattggagtt ctcctctcac gttcggtgct 300
gggaccaagc tggagctgaa a 321
<210> 77
<211> 335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 77
gatgttttga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagcattgta catagtaatg gaaacaccta tttagaatgg 120
tacctgcaga aaccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
tggacgttcg gtggaggcac caagctggaa atcaa 335
<210> 78
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 78
caaattattc tcacccagtc tccagcaatc atgtctgcat ctccagggga gaaggtcacc 60
atgacctgca gtgccagctc aagtacaagt ttcatgcact ggtaccagca gaagccaggc 120
acctccccca aaagatggat ttttgacaca tccaaactgg cttctggagt ccctggtcgc 180
ttcattggta gtgggtctgg gacctcttat tctctcacaa tcagcaccat ggaggctgaa 240
gatgctgcca cttattactg ccatcagcgg agtgcttacc catggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 79
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 79
gacatcaaga tgacccagtc tccatcttcc atgtatgcat ctctaggaga gagagtcact 60
atcacttgca aggcgagtca ggacattaat agctatttaa gctggttcca gcagaaacca 120
gggaaatctc ctaagaccct gatctatcgt gcaaacagat tggtagatgg ggtcccatca 180
aggttcagtg gcagtggatc tgggcaagat tattctctca ccatcagcag cctggagtat 240
gaagatatgg gaatttatta ttgtctacag tatgatgagt ttccgtacac gttcggaggg 300
gggaccaagc tggaaataaa a 321
<210> 80
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 80
gatattgtga tgactcaggc tgcaccctct gtacctgtca ctcctggaga gtcagtatcc 60
atctcctgca ggtctagtaa gagtctcctg catagtaatg gcaacactta cttgtattgg 120
ttcctgcaga ggccaggcca gtctcctcag ctcctgatat atcggatgtc caaccttgcc 180
tcaggagtcc cagacaggtt cggtggcagt gggtcaggaa ctgctttcac actgagaatc 240
agtagagtgg aggctgagga tgtgggtgtt tattattgta tgcaacatct agaatatccg 300
tacacgttcg gaggggggac caagctggaa ataaaa 336
<210> 81
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 81
gatattgtga tgactcaggc tgcaccctct gtacctgtca ctcctggaga gtcagtatcc 60
atctcctgca ggtctagtaa gagtctcctg catagtaatg gcaacactta cttgtattgg 120
ttcctgcaga ggccaggcca gtctcctcag ctcctgatat atcggatgtc caaccttgcc 180
tcaggagtcc cagacaggtt cggtggcagt gggtcaggaa ctgctttcac actgagaatc 240
agtagagtgg aggctgagga tgtgggtgtt tattactgta tgcaacatct agaatatccg 300
tacacgttcg gaggggggac caagctggaa ataaaa 336
<210> 82
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 82
caggctgttg tgactcagga atctgcactc accacatcac ctggtgaaac agtcacactc 60
acttgtcgct caagttctgg ggctgttaca actggtaact ttgccaactg ggtccaagaa 120
aaaccagatc atttattcac tggtctaata ggtggtacca acaaccgagc tccaggtgtt 180
cctgccagat tctcaggctc cctgattgga gacaaggctg ccctcaccat cacaggggca 240
cagactgagg atgaggcaat atatttctgt gctctatggt acagcaacca ctgggtgttc 300
ggtggaggaa ccaaactgac tgtccta 327
<210> 83
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 83
gatgttgtga tgacccagac tccactcact ttgtcggtta ccattggaca gtcagcctcc 60
atctcttgca agtcaagtca gagcctctta gatagtgatg gaaagacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctaatct atctggtgtc taaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tttgggagtt tattattgct ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa ataaaa 336
<210> 84
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 84
caggctgttg tgactcagga atctgcactc accacatcac ctggtgaaac agtcacactc 60
acttgtcgct caagtactgg ggctgttaca actagtaact atgccaactg ggtccaagaa 120
aaaccagatc atttattcac tggtctaata ggtggtacca acaaccgagc tccaggtgtt 180
cctgccagat tctcaggctc cctgattgga gacaaggctg ccctcaccat cacaggggca 240
cagactgagg atgaggcaat atatttctgt gctctatggt acagcaacca ctgggtgttc 300
ggtggaggaa ccaaactgac tgtccta 327
<210> 85
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 85
gaggtgcagc tggtggagtc tgggggaggc ttcgtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cactttcagt gactatggaa tgcactgggt tcgtcaggct 120
ccagagaagg ggctggagtg ggttgcatac attagtagtg gcagtagtat catctactat 180
gcagacacag tgaagggccg attcaccatc tccagagaca atgccaagaa caccctgttc 240
ctgcaaatga ccagtctgag gtctgaggac acggccatgt attactgtgc aagggaccac 300
taccatggta acgggtccga ctactggggc caaggcacca ctctcacagt ctcctca 357
<210> 86
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 86
caggtccagc tgaagcagtc tggagctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta catcttcact gactattatg taaactgggt gaagcagagg 120
cctggacagg gccttgagtg gattggaaag attggtcctg gaagtgttag tatttactac 180
aatgagaagt tcaagggcaa ggccacactg actgcagaca aatcctccag cacagcctac 240
atgcagctca gcagcctgac atctgaggac tctgcagtct atttctgtgc aagttattac 300
tacgggtttg cttactgggg ccaagggact ctggtcactg tctctgca 348
<210> 87
<211> 369
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 87
caggtgcagc tgaaggagtc aggacctggc ctggtggcgc cctcacagag cctgtccatc 60
acatgcaccg tctcagggtt ctcattaagc aattatggtg tacactgggt tcgccagcct 120
ccaggaaagg gtctggagtg gctggtactg atatggagtg atggaagcac aacctataat 180
tcagctctca aatccagact gagcatcagc aaggacaact ccaagagcca agttttctta 240
aaaatgaaca gtctccaaac tggtgacaca gccatgtact actgtgccag acatccctat 300
gatgattatt ccggctatta ctatactatg gactactggg gtcaaggaac ctcagtcacc 360
gtctcctca 369
<210> 88
<211> 357
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 88
gaggtgcagc tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggttt ctctttcagt gactatggaa tgcactgggt tcgtcaggct 120
ccagagaagg ggctggagtg ggttgcatac attagtagtg gcagtagtat cctctactat 180
gcagacatag tgaagggccg attcaccatc tccagagaca atgccaagaa caccctgttc 240
ctgcaaatga ccagtctgag gtctgaggac acggccatgt attactgtgc aagggaccac 300
taccatggta acgggtccga ctactggggc caaggcacca ctctcacagt ctcctca 357
<210> 89
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 89
gaggttcagc tgcagcagtc tggggcagag cttgtgaggc caggggcctc agtcaagttg 60
tcctgcacag cttctggctt caacattaaa gactactata tgcactgggt gaaagagagg 120
cctgaacagg gcctggagtg gattggaagg attgatcctg aggatggtga tattgaatat 180
gacccgaagt tccagggcaa ggccactatg actgcagata catcctccaa cacagcctac 240
ctgcagttca gcagcctgac atctgaggac actgccgtct attattgtgt cacggactat 300
gattacgacg gaggctggtt tgcttactgg ggccaaggga ctctggtcac tgtctctgca 360
<210> 90
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 90
caggtccaac tgcagcagcc tggggctgag cttgtgaagc ctggggcttc agtgaagatg 60
tcctgcaagg cttctggcta caccttcacc agctactgga taacctgggt gatacagagg 120
ccgggacaag gccttgagtg gattggagat atttattgtg gtagtgatac tatgcactac 180
aatgagaagt tcaagaacaa ggccacactg actgtagaca catcctccag cacagcctac 240
atgcagctca gcagcctgac atctgaggac tctgcggtct attactgtgc aagatggtgg 300
gactacggta gtagctacga ctactttgac tactggggcc aaggcaccac tctcacagtc 360
tcctca 366
<210> 91
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 91
caggtccagc tgaagcagtc tggacctgaa ctggtgaggc ctggggcttc agtgaagata 60
tcctgcgagg cttctggcta caccttcact gactattatg taaactgggt gaagcagagg 120
cctggacggg gccttgagtg gattggaaag attggtcctg gaagtgttag tatttactac 180
aatgagaagt tcaaggacaa ggccacactg actgcagaca aatcctccag cacagcctac 240
atgcagctca gcggcctgac atctgaggac tctgcagtct atttctgtgc aagttattac 300
tacggttttg cttactgggg ccaagggact ctggtcactg tctctgca 348
<210> 92
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 92
caggtccagc tgaagcagtc tggagctgag ctggtgaagc ctggggcttc agtgaagata 60
tcctgcaagg cttctggcta caccttcact gactattatg taaactgggt gaagcagagg 120
cctggacagg gccttgagtg gattggaaag attggtcctg aaagtgttag tatttattac 180
agtgagaagt tcaaggccaa ggccacactg actgcagaca aatcctccag cacagcctac 240
atgcaactca gcagcctgac atctgaggac tctgcagtct atttctgtgc aagttattac 300
tacgggtttg cttactgggg ccaagggact ctggtcactg tctctgca 348
<210> 93
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 93
gaagtgcagc tgttggagac tggaggaggc ttggtgcaac cgggggggtc acggggactc 60
tcttgtgaag gctcagggtt cacttttagt ggcttctgga tgagctgggt tcgacagaca 120
cctgggaaga ccctggagtg gattggagac attaattctg atggcagtgc aataaactac 180
gcaccatcca taaaggatcg attcactatc ttcagagaca atgacaagaa caccctgtac 240
ctgcagatga acaatgtgcg atcggaggac acagccacgt atttctgtgt gagatatgat 300
gattacgggt acttcgatgt ctggggcaca gggaccacgg tcaccgtctc ctca 354
<210> 94
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 94
cacgttcagc tgcagcagtc tggagctgag ttggcgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttctggcta caccttcaca agctatggtt taatctgggt gaagcagaga 120
actggacagg gccttgagtg gattggagag atttatccta gaagtggtaa tacttactac 180
aatgagaagt tcaagggcaa ggccacactg actgcagaca tatcctccag cacagcgtac 240
atggagctcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aagttcctct 300
cctcacgggg actactgggg ccaaggcacc actctcacag tctcctca 348
<210> 95
<211> 354
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 95
gaagtgcagc tgttggagac tggaggaggc ttagtgcaac ctggggggtc acggggactc 60
tcttgtgaag gctcagggtt cacttttagt gacttctgga tgagctgggt tcgacagaca 120
cctgggaaga ccctggagtg gattggagac attaattctg atggcagtgc agttaactac 180
gcaccatcca taaaggatca attcactatc ttcagagaca atgacaagag gaccctgcac 240
ctgcagatga tcaatgttcg atcggaggac acagccacgt atttctgtgt gagatatgat 300
gattacgggt acttcgatgt ctggggcaca gggaccacgg tcaccgtctc ctca 354
<210> 96
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 96
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Arg Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 97
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 97
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Ile Pro Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Glu Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 98
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 98
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 99
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 99
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 100
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 100
Asp Val Leu Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Asn Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Lys Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Met Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105 110
<210> 101
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 101
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Asn Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asp Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Ile Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys
<210> 102
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 102
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Glu Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 103
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 103
Glu Ile Gln Met Thr Gln Ser Pro Ser Ser Met Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Ile Thr Ile Thr Cys Gln Ala Thr Gln Asp Ile Val Lys Asn
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Pro Pro Ser Phe Leu Ile
35 40 45
Tyr Tyr Ala Thr Glu Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ser Asp Tyr Ser Leu Thr Ile Ser Asn Leu Glu Ser
65 70 75 80
Glu Asp Phe Ala Asp Tyr Tyr Cys Leu Gln Phe Tyr Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 104
<211> 104
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 104
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Ile Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr
35 40 45
Arg Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Phe Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Asp Tyr Tyr Cys His Gln Trp Ser Ser Trp Thr Phe Gly
85 90 95
Gly Gly Thr Gln Leu Glu Ile Lys
100
<210> 105
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 105
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Asn Val Gln Pro Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Phe Pro Phe Thr Phe Gly Ser Gly Thr Glu Leu Glu Met
100 105 110
Lys
<210> 106
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 106
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 107
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 107
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Leu Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp Leu Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Lys Arg Leu Ile Tyr Leu Val Ser Lys Leu Asp Ser Gly Val Pro
50 55 60
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ile Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys Trp Gln Gly
85 90 95
Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr Lys Leu Glu Val Lys
100 105 110
<210> 108
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Synethetic construct
<400> 108
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Asp
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Cys Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Ser Lys Phe
50 55 60
Gln Asp Lys Ala Thr Ile Thr Thr Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Tyr Val Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Thr
115
<210> 109
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 109
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ile Ser Tyr
20 25 30
Gly Ile Thr Trp Val Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Asn Phe
50 55 60
Lys Asp Arg Ala Ser Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Val Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Gly Gly Pro Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 110
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 110
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Tyr Pro Arg Ser Asp Asn Thr Tyr Tyr Asn Glu Arg Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Ala Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Glu Gly Gly Pro Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 111
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 111
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Asp
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Cys Ile Asp Pro Glu Asn Gly Asp Ile Glu Tyr Ala Ser Arg Phe
50 55 60
Gln Gly Lys Ala Thr Met Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Thr Ser Leu Thr Ser Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Tyr Val Gly Phe Gly Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 112
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 112
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Asp
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Cys Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Ser Lys Phe
50 55 60
Gln Gly Lys Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Val Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Tyr Val Gly Phe Gly Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 113
<211> 114
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 113
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe Thr Asp Phe
20 25 30
Tyr Ile Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Ala Arg Ile Tyr Pro Gly Ser Asp Glu Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Val Thr Leu Thr Ala Glu Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Leu Trp Phe Phe Asp Val Trp Gly Thr Gly Thr Thr Val Thr Val
100 105 110
Ser Ser
<210> 114
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 114
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Gly Ile Thr Trp Val Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Gly Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Arg Ser Ser Ser Thr Thr Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Lys Thr Gly Thr Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 115
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 115
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asn Pro Asn Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asn Lys Ser Ser Ser Thr Ala Phe
65 70 75 80
Met Glu Leu Arg Ser Leu Ala Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Asp Trp Glu Asp Cys Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 116
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 116
Asp Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Phe Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Arg His Asp Gly Ser Asn Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Leu Asn Ser Val Ile Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Val Arg Glu Ile Tyr Asp Gly Ser Ser Gly Tyr Phe Asp Val Trp Gly
100 105 110
Thr Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 117
<211> 114
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 117
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Ala Arg Ile Tyr Pro Gly Asn Gly Asn Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Ala Glu Lys Ser Ser Thr Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Cys Leu Trp Tyr Phe Asp Val Trp Gly Thr Gly Thr Thr Val Thr Val
100 105 110
Ser Ser
<210> 118
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 118
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Gly Ile Thr Trp Leu Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Lys Thr Gly Thr Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 119
<211> 115
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 119
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Lys Gln Arg Thr Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Asn Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ala Ala Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys
85 90 95
Ala Arg Glu Gly Gly Pro Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 120
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 120
gatgttttga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagtattgta catagtaatg gaaacaccta tttagaatgg 120
tacctgcaga agccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaggatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
ctcacgttcg gtgctgggac caagctggag ctgaaa 336
<210> 121
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 121
gatgttgtga tgacccagac tccactcact ttgtcgattc ccattggaca accagcctcc 60
atctcttgta agtcaagtca gagcctctta gatagtgatg gaaagacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctcatct atctggtgtc tgaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
agcagagtgg aggctgaaga tttgggagtt tattattgtt ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa ataaaa 336
<210> 122
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 122
gatgttgtga tgacccagac tccactcact ttgtcggtta ccattggaca accagcctcc 60
atctcttgca agtcaagtca gagcctctta gatagtgatg gaaagacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctaatct atctggtgtc taaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tttgggagtt tattattgtt ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa ataaaa 336
<210> 123
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 123
gacgttttga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagtattgta catagtaatg gaaacaccta tttagaatgg 120
tacctacaga aaccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
ctcacgttcg gtgctgggac caagctggag ctgaaa 336
<210> 124
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 124
gatgttttga tgacccaaag tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gaacatagta catagtaatg gtaacaccta tttagaatgg 120
tacctgaaga aaccaggcca gtctccaaag ctcctgatct acaaagtctc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggaatg tattactgct ttcaaggttc acatgttccg 300
ctcacgttcg gagctgggac caagctggag ctgaaa 336
<210> 125
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 125
gacattgtga tgacacagtc tccatcctcc ctgactgtga cagcaggaga gaaggtcact 60
atgagctgca agtccaatca gagtctgtta aacagtggag atcaaaagaa ctacttgacc 120
tggtaccagc agaaaccagg gcagcctcct aaactattga tctactgggc atccactagg 180
gaatctgggg tccctgatcg cttcacaggc agtggatctg gaacagattt cactctcacc 240
atcagcagtg tgcaggctga agacctggca atttattact gtcagaatga ttatagttat 300
ccactcacgt tcggtgctgg gaccaagctg gagctgaaa 339
<210> 126
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 126
gatgttgtga tgacccagac tccactcact ttgtcggtta ctattggaca atcagcctcc 60
atctcttgca agtcaagtca gagcctccta gatagtgatg gaaacacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctaatct atttggtgtc tgaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tttgggagtt tattattgct ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa ataaaa 336
<210> 127
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 127
gaaatccaga tgacccagtc tccatcctct atgtctgcat ctctgggaga cagaataacc 60
atcacttgcc aggcaactca agacattgtt aagaatttaa actggtatca gcagaaacca 120
gggaaacccc cttcattcct gatctattat gcaactgaac tggcagaagg ggtcccatca 180
aggttcagtg gcagtgggtc tgggtcagac tattctctga caatcagcaa cctggagtct 240
gaagattttg cagactatta ctgtctacag ttttatgaat ttccgtacac gttcggaggg 300
gggaccaagc tggaaataaa a 321
<210> 128
<211> 312
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 128
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctctagggga ggagatcacc 60
ctaatttgca gtgccagctc gagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttctccca aactcttgat ttatcgcaca tccaacctgg cttctggagt cccttctcgc 180
ttcagtggca gtgggtctgg gaccttttat tctcttacaa tcagcagtgt ggaggctgaa 240
gatgctgccg attattactg ccatcagtgg agtagttgga cgttcggtgg aggcacccag 300
ctggaaatca aa 312
<210> 129
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 129
gacattgtga tgacacagtc tccatcctcc ctgactgtga cagcaggaga gaaggtcact 60
atgagctgca agtccagtca gagtctgtta aacagtggaa atcaaaagaa ttacttgacc 120
tggtaccagc agaaaccagg acagcctcct aaactgttga tctactgggc atccactagg 180
gaatctgggg tccctgatcg cttcacaggc agtggatctg gaacagattt cactctcacc 240
attagcaatg tgcagcctga agacctggca gtttattact gtcagaatga ttatagtttt 300
ccattcacgt tcggctcggg gacagagttg gaaatgaaa 339
<210> 130
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 130
gatgttgtga tgacccagac tccactcact ttgtcggtta ccattggaca accagcctcc 60
atctcttgca agtcaagtca gagcctctta gatagtgatg gaaagacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctaatct atctggtgtc taaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
agcagagtgg aggctgagga tttgggaatt tattattgct ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa ataaaa 336
<210> 131
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 131
gatgttgtga tgacccagac tccactcact ttgtcggtta ccattggaca accagcctcc 60
atctcttgca agtcaagtct gagcctctta gatagtgatg gaaagacata tttgaattgg 120
ttgttacaga ggccaggcca gtctccaaag cgcctaatct atctggtgtc taaactggac 180
tctggagtcc ctgacaggtt cactggcagt ggatcaggga cagatttcac actgaaaatc 240
atcagagtgg aggctgagga tttgggaatt tattattgct ggcaaggtac acattttcca 300
ttcacgttcg gctcggggac aaagttggaa gtaaaa 336
<210> 132
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 132
gatgttttga tgacccaaac tccactctcc ctgcctgtca gtcttggaga tcaagcctcc 60
atctcttgca gatctagtca gagtattgta catagtaatg gaaacaccta tttagaatgg 120
tacctacaga aaccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
ctcacgttcg gtgctgggac caagctggag ctgaaa 336
<210> 133
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 133
gaggttcagc tgcagcagtc tggggctgaa cttgtgaggc caggggcctc agtcaagttg 60
tcctgcacag cttctggctt taacattaaa gacgactata tgcactgggt gaaacagagg 120
cctgaacagg gcctggagtg gattggatgc attgatcctg agaatggtga tactgaatat 180
gcctcgaaat tccaggacaa ggccactata acaacagaca catcctccaa cacagcctac 240
ctgcagctca gcagcctgac atctgaggac actgccgtct attactgtac tacatacgtt 300
ggatttgctt actggggcca agggactctg gtcactgtct ctaca 345
<210> 134
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 134
caggttcagc tgcagcagtc tggagctgag ctggcgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttctggcta caccttcata agctatggta taacctgggt gaagcagaga 120
actggacagg gccttgagtg gattggagag attcatccta gaagtggtaa tacttactac 180
aatgagaatt tcaaggacag ggcctcactg actgcagaca aatcctccag cacagcgtac 240
atggaggtcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aaggggtggg 300
ccgggggact actggggcca aggcaccact ctcacagtct cctca 345
<210> 135
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 135
caggttcagc tgcagcagtc tggagctgag ctggcgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttctggcta caccttcaca agctatggta taagctgggt gaagcagaga 120
actggacagg gccttgagtg gattggacag atttatccta gaagtgacaa tacttactac 180
aatgagaggt tcaagggcaa ggccacactg actgcagaca aatcctccag cacagcgtac 240
atggcgctcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aagagagggg 300
ggtcccgact actggggcca aggcaccact ctcacagtct cctca 345
<210> 136
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 136
gaggttcagc tgcagcagtc tggggctgag cttgtgaggc caggggcctc agtcaagttg 60
tcctgcacag cttctggctt taacattaaa gacgactata tgcactgggt gaaacagagg 120
cctgaacagg gcctggagtg gattggatgc attgatcctg agaatggtga tattgaatat 180
gcctcgaggt tccagggcaa ggccactatg acagcagaca catcctccaa cacagcctac 240
ctgcagctca ccagcctgac atctgcggac actgccgtct attactgtac tacatacgtt 300
ggatttggtt actggggcca agggactctg gtcactgtct ctgca 345
<210> 137
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 137
gaggttcagc tgcagcagtc tggggctgag cttgtgaggc caggggcctc agtcaagttg 60
tcctgcacag cttctggctt taacattaaa gacgactata tgcactgggt gaaacagagg 120
cctgaacagg gcctggagtg gattggatgt attgatcctg agaatggtga tactgaatat 180
gcctcgaagt tccagggcaa ggccactata acagcagaca catcctccaa cacagtctac 240
ctgcagctca gcagcctgac atctgaggac actgccgtct attactgtac tacatacgtt 300
ggatttggtt actggggcca ggggactctg gtcactgtct ctgca 345
<210> 138
<211> 342
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 138
caggtccaac tgaagcagtc tggggctgaa ctggtgaggc ctggggcttc agtgaagctg 60
tcctgcaggg cttctggcta cactttcact gacttctaca taaactgggt gaagcagagg 120
cctggacagg gacttgagtg gattgcaagg atttatcctg gaagtgatga gacttactac 180
aatgagaagt ttaaggacaa ggtcacactg actgcagaaa aatcctccag cactgcctac 240
atgcagctca gcagcctgac atctgaggac tctgctgtct atttctgtgc cctctggttc 300
ttcgatgtct ggggcacagg gaccacggtc accgtctcct ca 342
<210> 139
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 139
caggttcagc tgcagcagtc tggagctgag ttggcgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttcgggcta caccttcaca agcgatggta ttacctgggt gaagcagaga 120
actggacagg gccttgagtg gattggacag attcatccta gaagtggtaa tacctactac 180
aatgggaagt tcaagggcaa ggccacactg actgcagaca gatcctccag cacaacgtac 240
atggaactcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aaaaactggg 300
acgggggact actggggcca aggcaccact ctcacagtct cctca 345
<210> 140
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 140
gaggtccagc tgcaacagtc tggacctgag ctggtgaagc ctggggcttc agtgaagatg 60
tcctgcaagg cttctggata cacattcact gactacaaca tgcactgggt gaagcagagc 120
catggaaaga gccttgagtg gattggatat attaacccta acaatggtgg tactagctac 180
aaccagaagt tcaaggacaa ggccacattg actgtaaaca agtcctccag cacagccttc 240
atggagctcc gcagcctggc atcggaggat tctgcagtct attactgtgc aaggtctgac 300
tgggaagact gctggggcca aggcaccact ctcacagtct cctca 345
<210> 141
<211> 363
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 141
gatgtacagc ttcaggagtc aggacctggc ctcgtgaaat tttctcagtc tctgtctctc 60
acctgctctg tcactggcta ctccatcacc agtggttatt actggaactg gatccggcag 120
tttccaggaa acaaactgga atggatgggc tacataagac acgatggtag caataactac 180
aacccgtctc tcaaaaatcg aatctccatc actcgtgaca catctaagaa ccagtttttc 240
ctgaagttga attctgtgat tactgaggac acagccacat attactgtgt aagagagatc 300
tatgatggtt cctccgggta cttcgatgtc tggggcacag ggaccacggt caccgtctcc 360
tca 363
<210> 142
<211> 342
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 142
caggtccagc tgaagcagtc tggggctgaa ctggtgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttctggcta cactttcact gactactata taaactgggt gaagcagagg 120
cctggacagg gacttgagtg gattgcaagg atttatcctg gaaatggtaa tactgactac 180
aatgagaagt tcaaggacaa ggccacactg actgcagaaa aatcctccac cactgcctac 240
atacaactca gcagtctgac atctgaggac tctgctgtct atttctgttg cctctggtac 300
ttcgatgtct ggggcacagg aaccacggtc accgtctcct ca 342
<210> 143
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 143
caggttcagc tgcagcagtc tggagctgag ctggcgaggc ctggggcttc agtgaagctg 60
tcctgcaagg cttcgggcta caccttcaca agcgacggta taacctggct gaaacagaga 120
actggacagg gccttgagtg gattggacag attcatccta gaagtggtaa tacctactac 180
aatgagaagt tcaagggcaa ggccacactg actgcagaca aatcctccag cacagcgtac 240
atggaactcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aaaaactggg 300
acgggggact actggggcca aggcaccact ctcacagtct cctca 345
<210> 144
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 144
caggttcagc tgcagcagtc tgggcctgag ctggcgaggc ctggggcctc agtgaagctg 60
tcctgcaagg cttctggcta caccttcaca agctatggta taagctgggt gaagcaaaga 120
actggacagg gccttgagtg gattggacag attcatccta gaagtggtaa tacttactac 180
aatgagaact tcaagggcaa ggccacactg actgcagcca aatcctccag cacagcgtac 240
ctggagctcc gcagcctgac atctgaggac tctgcggtct atttctgtgc aagagagggg 300
ggtcccgact actggggcca aggcaccact ctcacagtct cctca 345
<210> 145
<211> 345
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 145
gaggttcagc tgcagcagtc tggggctgag cttgtgaggc caggggcctc agtcaagttg 60
tcctgcacag cttctggctt taacattaaa gacgactata tgcactgggt gaaacagagg 120
cctgaacagg gcctggagtg gattggatgc attgatcctg agaatggtga tattgaatat 180
gcctcgaggt tccagggcaa ggccactatg acagcagaca catcctccaa cacagcctac 240
ctgcagctca ccagcctgac atctgcggac actgccgtct attactgtac tacatacgtt 300
ggatttggtt actggggcca agggactctg gtcactgtct ctgca 345
<210> 146
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 146
Arg Ser Ser Gln Asn Ile Val His Ser Asn Gly Asn Thr Tyr Leu Glu
1 5 10 15
<210> 147
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 147
Lys Ser Asn Gln Ser Leu Leu Asn Ser Gly Asp Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 148
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 148
Lys Ser Ser Gln Ser Leu Leu Asp Ser Asp Gly Asn Thr Tyr Leu Asn
1 5 10 15
<210> 149
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 149
Gln Ala Thr Gln Asp Ile Val Lys Asn Leu Asn
1 5 10
<210> 150
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 150
Ser Ala Ser Ser Ser Val Ser Tyr Met His
1 5 10
<210> 151
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 151
Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 152
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 152
Lys Ser Ser Leu Ser Leu Leu Asp Ser Asp Gly Lys Thr Tyr Leu Asn
1 5 10 15
<210> 153
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 153
Leu Val Ser Glu Leu Asp Ser
1 5
<210> 154
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 154
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 155
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 155
Tyr Ala Thr Glu Leu Ala Glu
1 5
<210> 156
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 156
Arg Thr Ser Asn Leu Ala Ser
1 5
<210> 157
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 157
Phe Gln Gly Ser His Val Pro Leu Thr
1 5
<210> 158
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 158
Gln Asn Asp Tyr Ser Tyr Pro Leu Thr
1 5
<210> 159
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 159
Leu Gln Phe Tyr Glu Phe Pro Tyr Thr
1 5
<210> 160
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 160
His Gln Trp Ser Ser Trp Thr
1 5
<210> 161
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 161
Gln Asn Asp Tyr Ser Phe Pro Phe Thr
1 5
<210> 162
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 162
Asp Asp Tyr Met His
1 5
<210> 163
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 163
Ser Tyr Gly Ile Thr
1 5
<210> 164
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 164
Ser Tyr Gly Ile Ser
1 5
<210> 165
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 165
Asp Phe Tyr Ile Asn
1 5
<210> 166
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 166
Ser Asp Gly Ile Thr
1 5
<210> 167
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 167
Asp Tyr Asn Met His
1 5
<210> 168
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 168
Ser Gly Tyr Tyr Trp Asn
1 5
<210> 169
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 169
Asp Tyr Tyr Ile Asn
1 5
<210> 170
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 170
Cys Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Ser Lys Phe Gln
1 5 10 15
Asp
<210> 171
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 171
Glu Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Asn Phe Lys
1 5 10 15
Asp
<210> 172
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 172
Gln Ile Tyr Pro Arg Ser Asp Asn Thr Tyr Tyr Asn Glu Arg Phe Lys
1 5 10 15
Gly Lys
<210> 173
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 173
Cys Ile Asp Pro Glu Asn Gly Asp Ile Glu Tyr Ala Ser Arg Phe Gln
1 5 10 15
Gly
<210> 174
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 174
Cys Ile Asp Pro Glu Asn Gly Asp Thr Glu Tyr Ala Ser Lys Phe Gln
1 5 10 15
Gly
<210> 175
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 175
Arg Ile Tyr Pro Gly Ser Asp Glu Thr Tyr Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asp
<210> 176
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 176
Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Gly Lys Phe Lys
1 5 10 15
Gly
<210> 177
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 177
Tyr Ile Asn Pro Asn Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 178
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 178
Tyr Ile Arg His Asp Gly Ser Asn Asn Tyr Asn Pro Ser Leu Lys Asn
1 5 10 15
<210> 179
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 179
Arg Ile Tyr Pro Gly Asn Gly Asn Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Asp
<210> 180
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 180
Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 181
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 181
Gln Ile His Pro Arg Ser Gly Asn Thr Tyr Tyr Asn Glu Asn Phe Lys
1 5 10 15
Gly
<210> 182
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 182
Tyr Val Gly Phe Ala Tyr
1 5
<210> 183
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 183
Gly Gly Pro Gly Asp Tyr
1 5
<210> 184
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 184
Glu Gly Gly Pro Asp Tyr
1 5
<210> 185
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 185
Tyr Val Gly Phe Gly Tyr
1 5
<210> 186
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 186
Trp Phe Phe Asp Val
1 5
<210> 187
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 187
Thr Gly Thr Gly Asp Tyr
1 5
<210> 188
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 188
Ser Asp Trp Glu Asp Cys
1 5
<210> 189
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 189
Glu Ile Tyr Asp Gly Ser Ser Gly Tyr Phe Asp Val Trp Gly Thr
1 5 10 15
<210> 190
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 190
Trp Tyr Phe Asp Val
1 5
<210> 191
<211> 6
<212> Белок
<213> Homo sapiens
<400> 191
Ser Asn Tyr Glu Asn Leu
1 5
<210> 192
<211> 640
<212> Белок
<213> Homo sapiens
<400> 192
Met Leu Asn Lys Met Thr Leu His Pro Gln Gln Ile Met Ile Gly Pro
1 5 10 15
Arg Phe Asn Arg Ala Leu Phe Asp Pro Leu Leu Val Val Leu Leu Ala
20 25 30
Leu Gln Leu Leu Val Val Ala Gly Leu Val Arg Ala Gln Thr Cys Pro
35 40 45
Ser Val Cys Ser Cys Ser Asn Gln Phe Ser Lys Val Ile Cys Val Arg
50 55 60
Lys Asn Leu Arg Glu Val Pro Asp Gly Ile Ser Thr Asn Thr Arg Leu
65 70 75 80
Leu Asn Leu His Glu Asn Gln Ile Gln Ile Ile Lys Val Asn Ser Phe
85 90 95
Lys His Leu Arg His Leu Glu Ile Leu Gln Leu Ser Arg Asn His Ile
100 105 110
Arg Thr Ile Glu Ile Gly Ala Phe Asn Gly Leu Ala Asn Leu Asn Thr
115 120 125
Leu Glu Leu Phe Asp Asn Arg Leu Thr Thr Ile Pro Asn Gly Ala Phe
130 135 140
Val Tyr Leu Ser Lys Leu Lys Glu Leu Trp Leu Arg Asn Asn Pro Ile
145 150 155 160
Glu Ser Ile Pro Ser Tyr Ala Phe Asn Arg Ile Pro Ser Leu Arg Arg
165 170 175
Leu Asp Leu Gly Glu Leu Lys Arg Leu Ser Tyr Ile Ser Glu Gly Ala
180 185 190
Phe Glu Gly Leu Ser Asn Leu Arg Tyr Leu Asn Leu Ala Met Cys Asn
195 200 205
Leu Arg Glu Ile Pro Asn Leu Thr Pro Leu Ile Lys Leu Asp Glu Leu
210 215 220
Asp Leu Ser Gly Asn His Leu Ser Ala Ile Arg Pro Gly Ser Phe Gln
225 230 235 240
Gly Leu Met His Leu Gln Lys Leu Trp Met Ile Gln Ser Gln Ile Gln
245 250 255
Val Ile Glu Arg Asn Ala Phe Asp Asn Leu Gln Ser Leu Val Glu Ile
260 265 270
Asn Leu Ala His Asn Asn Leu Thr Leu Leu Pro His Asp Leu Phe Thr
275 280 285
Pro Leu His His Leu Glu Arg Ile His Leu His His Asn Pro Trp Asn
290 295 300
Cys Asn Cys Asp Ile Leu Trp Leu Ser Trp Trp Ile Lys Asp Met Ala
305 310 315 320
Pro Ser Asn Thr Ala Cys Cys Ala Arg Cys Asn Thr Pro Pro Asn Leu
325 330 335
Lys Gly Arg Tyr Ile Gly Glu Leu Asp Gln Asn Tyr Phe Thr Cys Tyr
340 345 350
Ala Pro Val Ile Val Glu Pro Pro Ala Asp Leu Asn Val Thr Glu Gly
355 360 365
Met Ala Ala Glu Leu Lys Cys Arg Ala Ser Thr Ser Leu Thr Ser Val
370 375 380
Ser Trp Ile Thr Pro Asn Gly Thr Val Met Thr His Gly Ala Tyr Lys
385 390 395 400
Val Arg Ile Ala Val Leu Ser Asp Gly Thr Leu Asn Phe Thr Asn Val
405 410 415
Thr Val Gln Asp Thr Gly Met Tyr Thr Cys Met Val Ser Asn Ser Val
420 425 430
Gly Asn Thr Thr Ala Ser Ala Thr Leu Asn Val Thr Ala Ala Thr Thr
435 440 445
Thr Pro Phe Ser Tyr Phe Ser Thr Val Thr Val Glu Thr Met Glu Pro
450 455 460
Ser Gln Asp Glu Ala Arg Thr Thr Asp Asn Asn Val Gly Pro Thr Pro
465 470 475 480
Val Val Asp Trp Glu Thr Thr Asn Val Thr Thr Ser Leu Thr Pro Gln
485 490 495
Ser Thr Arg Ser Thr Glu Lys Thr Phe Thr Ile Pro Val Thr Asp Ile
500 505 510
Asn Ser Gly Ile Pro Gly Ile Asp Glu Val Met Lys Thr Thr Lys Ile
515 520 525
Ile Ile Gly Cys Phe Val Ala Ile Thr Leu Met Ala Ala Val Met Leu
530 535 540
Val Ile Phe Tyr Lys Met Arg Lys Gln His His Arg Gln Asn His His
545 550 555 560
Ala Pro Thr Arg Thr Val Glu Ile Ile Asn Val Asp Asp Glu Ile Thr
565 570 575
Gly Asp Thr Pro Met Glu Ser His Leu Pro Met Pro Ala Ile Glu His
580 585 590
Glu His Leu Asn His Tyr Asn Ser Tyr Lys Ser Pro Phe Asn His Thr
595 600 605
Thr Thr Val Asn Thr Ile Asn Ser Ile His Ser Ser Val His Glu Pro
610 615 620
Leu Leu Ile Arg Met Asn Ser Lys Asp Asn Val Gln Glu Thr Gln Ile
625 630 635 640
<210> 193
<211> 486
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 193
Met Glu Trp Ser Trp Val Phe Leu Phe Phe Leu Ser Val Thr Thr Gly
1 5 10 15
Val His Ser Phe Val Arg Thr Lys Ile Asp Thr Thr Glu Asn Leu Leu
20 25 30
Asn Thr Glu Val His Ser Ser Pro Ala Gln Arg Trp Ser Met Gln Val
35 40 45
Pro Pro Glu Val Ser Ala Glu Ala Gly Asp Ala Ala Val Leu Pro Cys
50 55 60
Thr Phe Thr His Pro His Arg His Tyr Asp Gly Pro Leu Thr Ala Ile
65 70 75 80
Trp Arg Ala Gly Glu Pro Tyr Ala Gly Pro Gln Val Phe Arg Cys Ala
85 90 95
Ala Ala Arg Gly Ser Glu Leu Cys Gln Thr Ala Leu Ser Leu His Gly
100 105 110
Arg Phe Arg Leu Leu Gly Asn Pro Arg Arg Asn Asp Leu Ser Leu Arg
115 120 125
Val Glu Arg Leu Ala Leu Ala Asp Asp Arg Arg Tyr Phe Cys Arg Val
130 135 140
Glu Phe Ala Gly Asp Val His Asp Arg Tyr Glu Ser Arg His Gly Val
145 150 155 160
Arg Leu His Val Thr Ala Ala Pro Arg Ile Val Asn Ile Ser Val Leu
165 170 175
Pro Ser Pro Ala His Ala Phe Arg Ala Leu Cys Thr Ala Glu Gly Glu
180 185 190
Pro Pro Pro Ala Leu Ala Trp Ser Gly Pro Ala Leu Gly Asn Ser Leu
195 200 205
Ala Ala Val Arg Ser Pro Arg Glu Gly His Gly His Leu Val Thr Ala
210 215 220
Glu Leu Pro Ala Leu Thr His Asp Gly Arg Tyr Thr Cys Thr Ala Ala
225 230 235 240
Asn Ser Leu Gly Arg Ser Glu Ala Ser Val Tyr Leu Phe Arg Phe His
245 250 255
Gly Ala Ser Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
260 265 270
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
275 280 285
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
290 295 300
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
305 310 315 320
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
325 330 335
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
340 345 350
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
355 360 365
Pro Ala Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
370 375 380
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
385 390 395 400
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
405 410 415
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
420 425 430
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
435 440 445
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
450 455 460
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
465 470 475 480
Leu Ser Leu Ser Pro Gly
485
<210> 194
<211> 467
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 194
Phe Val Arg Thr Lys Ile Asp Thr Thr Glu Asn Leu Leu Asn Thr Glu
1 5 10 15
Val His Ser Ser Pro Ala Gln Arg Trp Ser Met Gln Val Pro Pro Glu
20 25 30
Val Ser Ala Glu Ala Gly Asp Ala Ala Val Leu Pro Cys Thr Phe Thr
35 40 45
His Pro His Arg His Tyr Asp Gly Pro Leu Thr Ala Ile Trp Arg Ala
50 55 60
Gly Glu Pro Tyr Ala Gly Pro Gln Val Phe Arg Cys Ala Ala Ala Arg
65 70 75 80
Gly Ser Glu Leu Cys Gln Thr Ala Leu Ser Leu His Gly Arg Phe Arg
85 90 95
Leu Leu Gly Asn Pro Arg Arg Asn Asp Leu Ser Leu Arg Val Glu Arg
100 105 110
Leu Ala Leu Ala Asp Asp Arg Arg Tyr Phe Cys Arg Val Glu Phe Ala
115 120 125
Gly Asp Val His Asp Arg Tyr Glu Ser Arg His Gly Val Arg Leu His
130 135 140
Val Thr Ala Ala Pro Arg Ile Val Asn Ile Ser Val Leu Pro Ser Pro
145 150 155 160
Ala His Ala Phe Arg Ala Leu Cys Thr Ala Glu Gly Glu Pro Pro Pro
165 170 175
Ala Leu Ala Trp Ser Gly Pro Ala Leu Gly Asn Ser Leu Ala Ala Val
180 185 190
Arg Ser Pro Arg Glu Gly His Gly His Leu Val Thr Ala Glu Leu Pro
195 200 205
Ala Leu Thr His Asp Gly Arg Tyr Thr Cys Thr Ala Ala Asn Ser Leu
210 215 220
Gly Arg Ser Glu Ala Ser Val Tyr Leu Phe Arg Phe His Gly Ala Ser
225 230 235 240
Gly Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu
245 250 255
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
260 265 270
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
275 280 285
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
290 295 300
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
305 310 315 320
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
325 330 335
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Ser
340 345 350
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
355 360 365
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
370 375 380
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
385 390 395 400
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
405 410 415
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
420 425 430
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
435 440 445
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
450 455 460
Ser Pro Gly
465
<210> 195
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 195
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 196
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 196
Lys Ala Ser Gln Asp Ile Asn Thr Tyr Leu Ser
1 5 10
<210> 197
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 197
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 198
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 198
Lys Ala Ser Gln Asp Ile Asn Val Tyr Leu Ser
1 5 10
<210> 199
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 199
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Gln Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 200
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 200
Lys Ala Ser Gln Asp Ile Gln Ser Tyr Leu Ser
1 5 10
<210> 201
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 201
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Thr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 202
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 202
Arg Ala Asn Arg Leu Thr Ser
1 5
<210> 203
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 203
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Met His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 204
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 204
Ser Tyr Trp Ile Thr
1 5
<210> 205
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 205
Asp Ile Tyr Ser Gly Ser Asp Thr Met His Tyr Ala Glu Lys Phe Gln
1 5 10 15
Gly
<210> 206
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 207
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 207
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 208
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 208
Ser Tyr Trp Ile Ser
1 5
<210> 209
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 209
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 210
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 210
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 211
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 211
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 212
<211> 123
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 212
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Val Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 213
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 213
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser
115 120
<210> 214
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 214
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys Ser
1 5 10 15
<210> 215
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 215
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser
115 120
<210> 216
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 216
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Leu Ile Trp Ser Glu Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser
115 120
<210> 217
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 217
Leu Ile Trp Ser Glu Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys Ser
1 5 10 15
<210> 218
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 218
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 219
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 219
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 220
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 220
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp
35 40
<210> 221
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 221
Asp Ile Val Met Thr Gln Ala Ala Pro Ser Val Pro Val Thr Pro Gly
1 5 10 15
Glu Ser Val Ser Ile Ser Cys Arg Ser Ser Lys Ser Leu Leu His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Tyr Trp
35 40
<210> 222
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 222
Asp Ile Gln Met Thr Gln Ala Ser Ser Ser Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp
35
<210> 223
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 223
Gln Ile Ile Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Thr Ser Phe Met
20 25 30
His Trp
<210> 224
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 224
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp
35
<210> 225
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 225
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Ser Gly Ala Val Thr Thr Gly
20 25 30
Asn Phe Ala Asn Trp
35
<210> 226
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 226
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp
35 40
<210> 227
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 227
Gln Ala Val Val Thr Gln Glu Ser Ala Leu Thr Thr Ser Pro Gly Glu
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp
35
<210> 228
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 228
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Ile Pro Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp
35 40
<210> 229
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 229
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp
35 40
<210> 230
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 230
Asp Val Leu Met Thr Gln Ser Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Asn Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp
35 40
<210> 231
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 231
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Asn Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asp Gln Lys Asn Tyr Leu Thr Trp
35 40
<210> 232
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 232
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Ser Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Asp Gly Asn Thr Tyr Leu Asn Trp
35 40
<210> 233
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 233
Glu Ile Gln Met Thr Gln Ser Pro Ser Ser Met Ser Ala Ser Leu Gly
1 5 10 15
Asp Arg Ile Thr Ile Thr Cys Gln Ala Thr Gln Asp Ile Val Lys Asn
20 25 30
Leu Asn Trp
35
<210> 234
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 234
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Glu Ile Thr Leu Ile Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp
<210> 235
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 235
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp
35 40
<210> 236
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 236
Asp Val Val Met Thr Gln Thr Pro Leu Thr Leu Ser Val Thr Ile Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Leu Ser Leu Leu Asp Ser
20 25 30
Asp Gly Lys Thr Tyr Leu Asn Trp
35 40
<210> 237
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 237
Tyr Leu Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Lys Val
1 5 10 15
Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Thr Asp
35
<210> 238
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 238
Phe Leu Gln Arg Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Arg Met
1 5 10 15
Ser Asn Leu Ala Ser Gly Val Pro Asp Arg Phe Gly Gly Ser Gly Ser
20 25 30
Gly Thr Ala
35
<210> 239
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 239
Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile Ser Gly Ala
1 5 10 15
Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Lys Asp
35
<210> 240
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 240
Tyr Gln Gln Lys Pro Gly Thr Ser Pro Lys Arg Trp Ile Phe Asp Thr
1 5 10 15
Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ile Gly Ser Gly Ser
20 25 30
Gly Thr Ser
35
<210> 241
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 241
Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr Arg Ala
1 5 10 15
Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Gln Asp
35
<210> 242
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 242
Val Gln Glu Lys Pro Asp His Leu Phe Thr Gly Leu Ile Gly Gly Thr
1 5 10 15
Asn Asn Arg Ala Pro Gly Val Pro Ala Arg Phe Ser Gly Ser Leu Ile
20 25 30
Gly Asp Lys
35
<210> 243
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 243
Leu Leu Gln Arg Pro Gly Gln Ser Pro Lys Arg Leu Ile Tyr Leu Val
1 5 10 15
Ser Lys Leu Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
20 25 30
Gly Thr Asp
35
<210> 244
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 244
Leu Leu Gln Arg Pro Gly Gln Ser Pro Lys Arg Leu Ile Tyr Leu Val
1 5 10 15
Ser Glu Leu Asp Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
20 25 30
Gly Thr Asp
35
<210> 245
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 245
Tyr Leu Lys Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Lys Val
1 5 10 15
Ser Asn Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Thr Asp
35
<210> 246
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 246
Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Trp Ala
1 5 10 15
Ser Thr Arg Glu Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser
20 25 30
Gly Thr Asp
35
<210> 247
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 247
Tyr Gln Gln Lys Pro Gly Lys Pro Pro Ser Phe Leu Ile Tyr Tyr Ala
1 5 10 15
Thr Glu Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Ser Asp
35
<210> 248
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 248
Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Leu Leu Ile Tyr Arg Thr
1 5 10 15
Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
20 25 30
Gly Thr Phe
35
<210> 249
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 249
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr
1 5 10 15
Tyr Cys Phe Gln Gly Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 250
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 250
Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val Gly Phe Tyr
1 5 10 15
Tyr Cys Met Gln His Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
20 25 30
Arg Leu Glu Ile Lys
35
<210> 251
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 251
Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr Glu Asp Val Ala Thr Tyr
1 5 10 15
Tyr Cys Gln Gln Tyr Trp Ser Ser Pro Leu Thr Phe Gly Ala Gly Thr
20 25 30
Lys Leu Glu Leu Lys
35
<210> 252
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 252
Tyr Ser Leu Thr Ile Ser Thr Met Glu Ala Glu Asp Ala Ala Thr Tyr
1 5 10 15
Tyr Cys His Gln Arg Ser Ala Tyr Pro Trp Thr Phe Gly Gly Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 253
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 253
Tyr Ser Leu Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr
1 5 10 15
Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 254
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 254
Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
1 5 10 15
Tyr Cys Met Gln His Leu Glu Tyr Pro Tyr Thr Phe Gly Gly Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 255
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 255
Ala Ala Leu Thr Ile Thr Gly Ala Gln Thr Glu Asp Glu Ala Ile Tyr
1 5 10 15
Phe Cys Ala Leu Trp Tyr Ser Asn His Trp Val Phe Gly Gly Gly Thr
20 25 30
Lys Leu Thr Val Leu
35
<210> 256
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 256
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr
1 5 10 15
Tyr Cys Trp Gln Gly Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 257
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 257
Phe Thr Leu Arg Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr
1 5 10 15
Tyr Cys Phe Gln Gly Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr
20 25 30
Lys Leu Glu Leu Lys
35
<210> 258
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 258
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Met Tyr
1 5 10 15
Tyr Cys Phe Gln Gly Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr
20 25 30
Lys Leu Glu Leu Lys
35
<210> 259
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 259
Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Ile Tyr
1 5 10 15
Tyr Cys Gln Asn Asp Tyr Ser Tyr Pro Leu Thr Phe Gly Ala Gly Thr
20 25 30
Lys Leu Glu Leu Lys
35
<210> 260
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 260
Tyr Ser Leu Thr Ile Ser Asn Leu Glu Ser Glu Asp Phe Ala Asp Tyr
1 5 10 15
Tyr Cys Leu Gln Phe Tyr Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 261
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 261
Tyr Ser Leu Thr Ile Ser Ser Val Glu Ala Glu Asp Ala Ala Asp Tyr
1 5 10 15
Tyr Cys His Gln Trp Ser Ser Trp Thr Phe Gly Gly Gly Thr Gln Leu
20 25 30
Glu Ile Lys
35
<210> 262
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 262
Phe Thr Leu Thr Ile Ser Asn Val Gln Pro Glu Asp Leu Ala Val Tyr
1 5 10 15
Tyr Cys Gln Asn Asp Tyr Ser Phe Pro Phe Thr Phe Gly Ser Gly Thr
20 25 30
Glu Leu Glu Met Lys
35
<210> 263
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 263
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr
1 5 10 15
Tyr Cys Trp Gln Gly Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr
20 25 30
Lys Leu Glu Ile Lys
35
<210> 264
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 264
Phe Thr Leu Lys Ile Ile Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr
1 5 10 15
Tyr Cys Trp Gln Gly Thr His Phe Pro Phe Thr Phe Gly Ser Gly Thr
20 25 30
Lys Leu Glu Val Lys
35
<210> 265
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 265
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr
1 5 10 15
Tyr Cys Phe Gln Gly Ser His Val Pro Leu Thr Phe Gly Ala Gly Thr
20 25 30
Lys Leu Glu Leu Lys
35
<210> 266
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 266
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala
35 40
<210> 267
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 267
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ile Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg
35 40
<210> 268
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 268
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro
35 40
<210> 269
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 269
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Asp Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala
35 40
<210> 270
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 270
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Lys Glu Arg
35 40
<210> 271
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 271
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Ile Gln Arg
35 40
<210> 272
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 272
Gln Val Gln Leu Lys Gln Ser Gly Pro Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Glu Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg
35 40
<210> 273
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 273
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Val Asn Trp Val Lys Gln Arg
35 40
<210> 274
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 274
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Gly Leu Ser Cys Glu Gly Ser Gly Phe Thr Phe Ser Gly Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Thr
35 40
<210> 275
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 275
His Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Leu Ile Trp Val Lys Gln Arg
35 40
<210> 276
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 276
Glu Val Gln Leu Leu Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Arg Gly Leu Ser Cys Glu Gly Ser Gly Phe Thr Phe Ser Asp Phe
20 25 30
Trp Met Ser Trp Val Arg Gln Thr
35 40
<210> 277
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 277
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Asp
20 25 30
Tyr Met His Trp Val Lys Gln Arg
35 40
<210> 278
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 278
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ile Ser Tyr
20 25 30
Gly Ile Thr Trp Val Lys Gln Arg
35 40
<210> 279
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 279
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Lys Gln Arg
35 40
<210> 280
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 280
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe Thr Asp Phe
20 25 30
Tyr Ile Asn Trp Val Lys Gln Arg
35 40
<210> 281
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 281
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Gly Ile Thr Trp Val Lys Gln Arg
35 40
<210> 282
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 282
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met His Trp Val Lys Gln Ser
35 40
<210> 283
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 283
Asp Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Phe Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe
35 40
<210> 284
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 284
Gln Val Gln Leu Lys Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Val Lys Gln Arg
35 40
<210> 285
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 285
Gln Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Gly Ile Thr Trp Leu Lys Gln Arg
35 40
<210> 286
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 286
Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Ala Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Lys Gln Arg
35 40
<210> 287
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 287
Pro Glu Lys Gly Leu Glu Trp Val Ala Tyr Ile Ser Ser Gly Ser Ser
1 5 10 15
Ile Ile Tyr Tyr Ala Asp Thr Val Lys Gly Arg Phe Thr Ile Ser Arg
20 25 30
Asp Asn Ala Lys Asn Thr Leu Phe Leu
35 40
<210> 288
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 288
Pro Gly Gln Gly Leu Glu Trp Ile Gly Lys Ile Gly Pro Gly Ser Val
1 5 10 15
Ser Ile Tyr Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 289
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 289
Pro Gly Lys Gly Leu Glu Trp Leu Val Leu Ile Trp Ser Asp Gly Ser
1 5 10 15
Thr Thr Tyr Asn Ser Ala Leu Lys Ser Arg Leu Ser Ile Ser Lys Asp
20 25 30
Asn Ser Lys Ser Gln Val Phe Leu
35 40
<210> 290
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 290
Pro Glu Lys Gly Leu Glu Trp Val Ala Tyr Ile Ser Ser Gly Ser Ser
1 5 10 15
Ile Leu Tyr Tyr Ala Asp Ile Val Lys Gly Arg Phe Thr Ile Ser Arg
20 25 30
Asp Asn Ala Lys Asn Thr Leu Phe Leu
35 40
<210> 291
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 291
Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Glu Asp Gly
1 5 10 15
Asp Ile Glu Tyr Asp Pro Lys Phe Gln Gly Lys Ala Thr Met Thr Ala
20 25 30
Asp Thr Ser Ser Asn Thr Ala Tyr Leu
35 40
<210> 292
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 292
Pro Gly Gln Gly Leu Glu Trp Ile Gly Asp Ile Tyr Cys Gly Ser Asp
1 5 10 15
Thr Met His Tyr Asn Glu Lys Phe Lys Asn Lys Ala Thr Leu Thr Val
20 25 30
Asp Thr Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 293
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 293
Pro Gly Arg Gly Leu Glu Trp Ile Gly Lys Ile Gly Pro Gly Ser Val
1 5 10 15
Ser Ile Tyr Tyr Asn Glu Lys Phe Lys Asp Lys Ala Thr Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 294
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 294
Pro Gly Gln Gly Leu Glu Trp Ile Gly Lys Ile Gly Pro Glu Ser Val
1 5 10 15
Ser Ile Tyr Tyr Ser Glu Lys Phe Lys Ala Lys Ala Thr Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 295
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 295
Pro Gly Lys Thr Leu Glu Trp Ile Gly Asp Ile Asn Ser Asp Gly Ser
1 5 10 15
Ala Ile Asn Tyr Ala Pro Ser Ile Lys Asp Arg Phe Thr Ile Phe Arg
20 25 30
Asp Asn Asp Lys Asn Thr Leu Tyr Leu
35 40
<210> 296
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 296
Thr Gly Gln Gly Leu Glu Trp Ile Gly Glu Ile Tyr Pro Arg Ser Gly
1 5 10 15
Asn Thr Tyr Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Asp Ile Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 297
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 297
Pro Gly Lys Thr Leu Glu Trp Ile Gly Asp Ile Asn Ser Asp Gly Ser
1 5 10 15
Ala Val Asn Tyr Ala Pro Ser Ile Lys Asp Gln Phe Thr Ile Phe Arg
20 25 30
Asp Asn Asp Lys Arg Thr Leu His Leu
35 40
<210> 298
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 298
Pro Glu Gln Gly Leu Glu Trp Ile Gly Cys Ile Asp Pro Glu Asn Gly
1 5 10 15
Asp Thr Glu Tyr Ala Ser Lys Phe Gln Asp Lys Ala Thr Ile Thr Thr
20 25 30
Asp Thr Ser Ser Asn Thr Ala Tyr Leu
35 40
<210> 299
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 299
Thr Gly Gln Gly Leu Glu Trp Ile Gly Glu Ile His Pro Arg Ser Gly
1 5 10 15
Asn Thr Tyr Tyr Asn Glu Asn Phe Lys Asp Arg Ala Ser Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 300
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 300
Thr Gly Gln Gly Leu Glu Trp Ile Gly Gln Ile Tyr Pro Arg Ser Asp
1 5 10 15
Asn Thr Tyr Tyr Asn Glu Arg Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 301
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 301
Pro Glu Gln Gly Leu Glu Trp Ile Gly Cys Ile Asp Pro Glu Asn Gly
1 5 10 15
Asp Thr Glu Tyr Ala Ser Lys Phe Gln Gly Lys Ala Thr Ile Thr Ala
20 25 30
Asp Thr Ser Ser Asn Thr Val Tyr Leu
35 40
<210> 302
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 302
Pro Gly Gln Gly Leu Glu Trp Ile Ala Arg Ile Tyr Pro Gly Ser Asp
1 5 10 15
Glu Thr Tyr Tyr Asn Glu Lys Phe Lys Asp Lys Val Thr Leu Thr Ala
20 25 30
Glu Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 303
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 303
Thr Gly Gln Gly Leu Glu Trp Ile Gly Gln Ile His Pro Arg Ser Gly
1 5 10 15
Asn Thr Tyr Tyr Asn Gly Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Asp Arg Ser Ser Ser Thr Thr Tyr Met
35 40
<210> 304
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 304
His Gly Lys Ser Leu Glu Trp Ile Gly Tyr Ile Asn Pro Asn Asn Gly
1 5 10 15
Gly Thr Ser Tyr Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Val
20 25 30
Asn Lys Ser Ser Ser Thr Ala Phe Met
35 40
<210> 305
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 305
Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Arg His Asp Gly Ser
1 5 10 15
Asn Asn Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Thr Arg Asp
20 25 30
Thr Ser Lys Asn Gln Phe Phe Leu
35 40
<210> 306
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 306
Pro Gly Gln Gly Leu Glu Trp Ile Ala Arg Ile Tyr Pro Gly Asn Gly
1 5 10 15
Asn Thr Asp Tyr Asn Glu Lys Phe Lys Asp Lys Ala Thr Leu Thr Ala
20 25 30
Glu Lys Ser Ser Thr Thr Ala Tyr Ile
35 40
<210> 307
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 307
Thr Gly Gln Gly Leu Glu Trp Ile Gly Gln Ile His Pro Arg Ser Gly
1 5 10 15
Asn Thr Tyr Tyr Asn Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Asp Lys Ser Ser Ser Thr Ala Tyr Met
35 40
<210> 308
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 308
Thr Gly Gln Gly Leu Glu Trp Ile Gly Gln Ile His Pro Arg Ser Gly
1 5 10 15
Asn Thr Tyr Tyr Asn Glu Asn Phe Lys Gly Lys Ala Thr Leu Thr Ala
20 25 30
Ala Lys Ser Ser Ser Thr Ala Tyr Leu
35 40
<210> 309
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 309
Pro Glu Gln Gly Leu Glu Trp Ile Gly Cys Ile Asp Pro Glu Asn Gly
1 5 10 15
Asp Ile Glu Tyr Ala Ser Arg Phe Gln Gly Lys Ala Thr Met Thr Ala
20 25 30
Asp Thr Ser Ser Asn Thr Ala Tyr Leu
35 40
<210> 310
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 310
Gln Met Thr Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
1 5 10 15
Arg Asp His Tyr His Gly Asn Gly Ser Asp Tyr Trp Gly Gln Gly Thr
20 25 30
Thr Leu Thr Val Ser Ser
35
<210> 311
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 311
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Ser Tyr Tyr Tyr Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
20 25 30
Val Ser Ala
35
<210> 312
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 312
Lys Met Asn Ser Leu Gln Thr Gly Asp Thr Ala Met Tyr Tyr Cys Ala
1 5 10 15
Arg His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr
20 25 30
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser
35 40
<210> 313
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 313
Gln Phe Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Val
1 5 10 15
Thr Asp Tyr Asp Tyr Asp Gly Gly Trp Phe Ala Tyr Trp Gly Gln Gly
20 25 30
Thr Leu Val Thr Val Ser Ala
35
<210> 314
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 314
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala
1 5 10 15
Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr Phe Asp Tyr Trp Gly
20 25 30
Gln Gly Thr Thr Leu Thr Val Ser Ser
35 40
<210> 315
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 315
Gln Leu Ser Gly Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Ser Tyr Tyr Tyr Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
20 25 30
Val Ser Ala
35
<210> 316
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 316
Gln Met Asn Asn Val Arg Ser Glu Asp Thr Ala Thr Tyr Phe Cys Val
1 5 10 15
Arg Tyr Asp Asp Tyr Gly Tyr Phe Asp Val Trp Gly Thr Gly Thr Thr
20 25 30
Val Thr Val Ser Ser
35
<210> 317
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 317
Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Ser Ser Ser Pro His Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
20 25 30
Val Ser Ser
35
<210> 318
<211> 37
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 318
Gln Met Ile Asn Val Arg Ser Glu Asp Thr Ala Thr Tyr Phe Cys Val
1 5 10 15
Arg Tyr Asp Asp Tyr Gly Tyr Phe Asp Val Trp Gly Thr Gly Thr Thr
20 25 30
Val Thr Val Ser Ser
35
<210> 319
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 319
Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr
1 5 10 15
Thr Tyr Val Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
20 25 30
Ser Thr
<210> 320
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 320
Glu Val Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Arg Gly Gly Pro Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val
20 25 30
Ser Ser
<210> 321
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 321
Ala Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Arg Glu Gly Gly Pro Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val
20 25 30
Ser Ser
<210> 322
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 322
Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr
1 5 10 15
Thr Tyr Val Gly Phe Gly Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
20 25 30
Ser Ala
<210> 323
<211> 33
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 323
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Leu Trp Phe Phe Asp Val Trp Gly Thr Gly Thr Thr Val Thr Val Ser
20 25 30
Ser
<210> 324
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 324
Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Lys Thr Gly Thr Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val
20 25 30
Ser Ser
<210> 325
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 325
Glu Leu Arg Ser Leu Ala Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala
1 5 10 15
Arg Ser Asp Trp Glu Asp Cys Trp Gly Gln Gly Thr Thr Leu Thr Val
20 25 30
Ser Ser
<210> 326
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 326
Lys Leu Asn Ser Val Ile Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Val
1 5 10 15
Arg Glu Ile Tyr Asp Gly Ser Ser Gly Tyr Phe Asp Val Trp Gly Thr
20 25 30
Gly Thr Thr Val Thr Val Val Thr Val Ser Ser
35 40
<210> 327
<211> 33
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 327
Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Cys
1 5 10 15
Leu Trp Tyr Phe Asp Val Trp Gly Thr Gly Thr Thr Leu Thr Val Ser
20 25 30
Ser
<210> 328
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 328
Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Phe Cys Ala
1 5 10 15
Arg Glu Gly Gly Pro Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
20 25 30
Ser Ala
<210> 329
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 329
Gln Leu Thr Ser Leu Thr Ser Ala Asp Thr Ala Val Tyr Tyr Cys Thr
1 5 10 15
Thr Tyr Val Gly Phe Gly Tyr Trp Gly Gln Gly Thr Leu Val Thr Val
20 25 30
Ser Ala
<210> 330
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 330
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser
65 70
<210> 331
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 331
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr
65 70
<210> 332
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 332
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr
65 70
<210> 333
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 333
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr
65 70
<210> 334
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 334
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Gln Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr
65 70
<210> 335
<211> 72
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 335
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Thr Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Thr
65 70
<210> 336
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 336
Leu Thr Ile Ser Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys
1 5 10 15
Leu Gln Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu
20 25 30
Glu Ile Lys
35
<210> 337
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 337
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys
1 5 10 15
Leu Gln Tyr Asp Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val
20 25 30
Glu Ile Lys
35
<210> 338
<211> 74
<212> Белок
<213> Искусственная последовательность
<220>
<223> Synthetic contruct
<400> 338
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Ile Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile Tyr Cys Gly Ser Asp Thr Met His Tyr Asn Glu Lys Phe
50 55 60
Lys Asn Lys Ala Thr Leu Thr Val Asp Thr
65 70
<210> 339
<211> 74
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 339
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Met His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr
65 70
<210> 340
<211> 74
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 340
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr
65 70
<210> 341
<211> 74
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 341
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr Ala Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Val Asp Thr
65 70
<210> 342
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 342
Ser Ser Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp
1 5 10 15
Ser Ala Val Tyr Tyr Cys Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr
20 25 30
Asp Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
35 40 45
<210> 343
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 343
Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
1 5 10 15
Thr Ala Val Tyr Tyr Cys Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr
20 25 30
Asp Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
35 40 45
<210> 344
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 344
Asp Ile Lys Met Thr Gln Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
50 55 60
<210> 345
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 345
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
50 55 60
<210> 346
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 346
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Thr Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
50 55 60
<210> 347
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 347
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
50 55 60
<210> 348
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 348
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Gln Ser Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser
50 55 60
<210> 349
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 349
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asn Val Tyr
20 25 30
Leu Ser Trp Phe Gln Gln Lys Pro Gly Lys Ala Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Thr Ser Gly Val Pro Ser
50 55 60
<210> 350
<211> 47
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 350
Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Leu Thr Ile Ser
1 5 10 15
Ser Leu Glu Tyr Glu Asp Met Gly Ile Tyr Tyr Cys Leu Gln Tyr Asp
20 25 30
Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
35 40 45
<210> 351
<211> 47
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 351
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser
1 5 10 15
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Asp
20 25 30
Glu Phe Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
35 40 45
<210> 352
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 352
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Ile Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asp Ile Tyr Cys Gly Ser Asp Thr Met His Tyr
50 55 60
<210> 353
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 353
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Met His Tyr
50 55 60
<210> 354
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 354
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Thr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr
50 55 60
<210> 355
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 355
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr
50 55 60
<210> 356
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 356
Asn Glu Lys Phe Lys Asn Lys Ala Thr Leu Thr Val Asp Thr Ser Ser
1 5 10 15
Ser Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala
20 25 30
Val Tyr Tyr Cys Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr
35 40 45
Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val
50 55 60
<210> 357
<211> 61
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 357
Ala Glu Lys Phe Gln Gly Arg Val Thr Leu Thr Val Asp Thr Ser Thr
1 5 10 15
Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala
20 25 30
Val Tyr Tyr Cys Ala Arg Trp Trp Asp Tyr Gly Ser Ser Tyr Asp Tyr
35 40 45
Phe Asp Tyr Trp Gly Gln Gly Thr Thr Val Thr Val Val
50 55 60
<210> 358
<211> 56
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 358
Asp Ile Gln Met Thr Gln Ala Ser Ser Ser Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr
50 55
<210> 359
<211> 56
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 359
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr
50 55
<210> 360
<211> 56
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 360
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr
50 55
<210> 361
<211> 51
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 361
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Lys Asp Tyr Thr
1 5 10 15
Leu Ser Ile Thr Ser Leu Gln Thr Glu Asp Val Ala Thr Tyr Tyr Cys
20 25 30
Gln Gln Tyr Trp Ser Ser Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu
35 40 45
Glu Leu Lys
50
<210> 362
<211> 51
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 362
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
1 5 10 15
Phe Thr Ile Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys
20 25 30
Gln Gln Tyr Trp Ser Ser Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
35 40 45
Glu Ile Lys
50
<210> 363
<211> 51
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 363
Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Thr
1 5 10 15
Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Val Ala Thr Tyr Tyr Cys
20 25 30
Gln Gln Tyr Trp Ser Ser Pro Leu Thr Phe Gly Gly Gly Thr Lys Val
35 40 45
Glu Ile Lys
50
<210> 364
<211> 49
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 364
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Val
<210> 365
<211> 49
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 365
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Val
<210> 366
<211> 49
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 366
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly
<210> 367
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 367
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
20 25 30
Met Asn Ser Leu Gln Thr Gly Asp Thr Ala Met Tyr Tyr Cys Ala Arg
35 40 45
<210> 368
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 368
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Ser Ala Leu Lys Ser
1 5 10 15
Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu Lys
20 25 30
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
35 40 45
<210> 369
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 369
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys Ser
1 5 10 15
Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu Lys
20 25 30
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
35 40 45
<210> 370
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 370
Leu Ile Trp Ser Asp Gly Ser Thr Thr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu Lys
20 25 30
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
35 40 45
<210> 371
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 371
Leu Ile Trp Ser Glu Gly Ser Thr Thr Tyr Ala Ser Ala Leu Lys Ser
1 5 10 15
Arg Val Thr Ile Ser Lys Asp Thr Ser Lys Asn Gln Val Ser Leu Lys
20 25 30
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
35 40 45
<210> 372
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 372
His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr Trp
1 5 10 15
Gly Gln Gly Thr Ser Val Thr Val Ser
20 25
<210> 373
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 373
His Pro Tyr Asp Asp Tyr Ser Gly Tyr Tyr Tyr Thr Met Asp Tyr Trp
1 5 10 15
Gly Gln Gly Thr Leu Val Thr Val Ser
20 25
<210> 374
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 374
Asp Ile Tyr Ser Gly Ser Asp Thr Thr His Tyr Ala Glu Lys Phe Gln
1 5 10 15
Gly
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОЛЕКУЛЫ АНТИ-SIGLEC-9 АНТИТЕЛА | 2020 |
|
RU2833330C1 |
| АНТИТЕЛА ПРОТИВ SARS-COV-2 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2021 |
|
RU2832025C1 |
| ПОЛИПЕПТИДЫ, МОДУЛИРУЮЩИЕ SIGLEC-ЗАВИСИМЫЕ ИММУННЫЕ ОТВЕТЫ | 2017 |
|
RU2776807C2 |
| Антитела против CXCR2 и их применение | 2019 |
|
RU2807067C2 |
| CD47-АНТИГЕНСВЯЗЫВАЮЩАЯ ЕДИНИЦА И ЕЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2780859C2 |
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИТЕЛО ПРОТИВ LILRB1 И ЕГО ПРИМЕНЕНИЯ | 2021 |
|
RU2813373C1 |
| АНТИТЕЛА, КОТОРЫЕ СВЯЗЫВАЮТ ОПУХОЛЕВУЮ ТКАНЬ, ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ | 2020 |
|
RU2806915C2 |
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |

























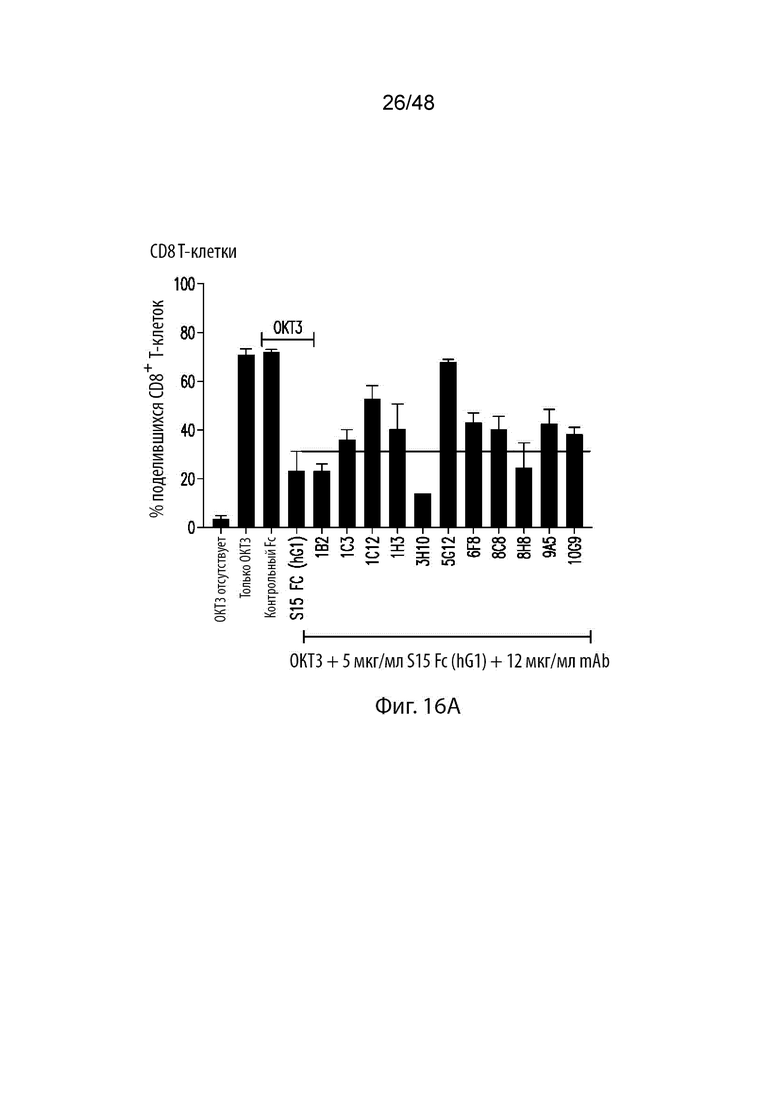





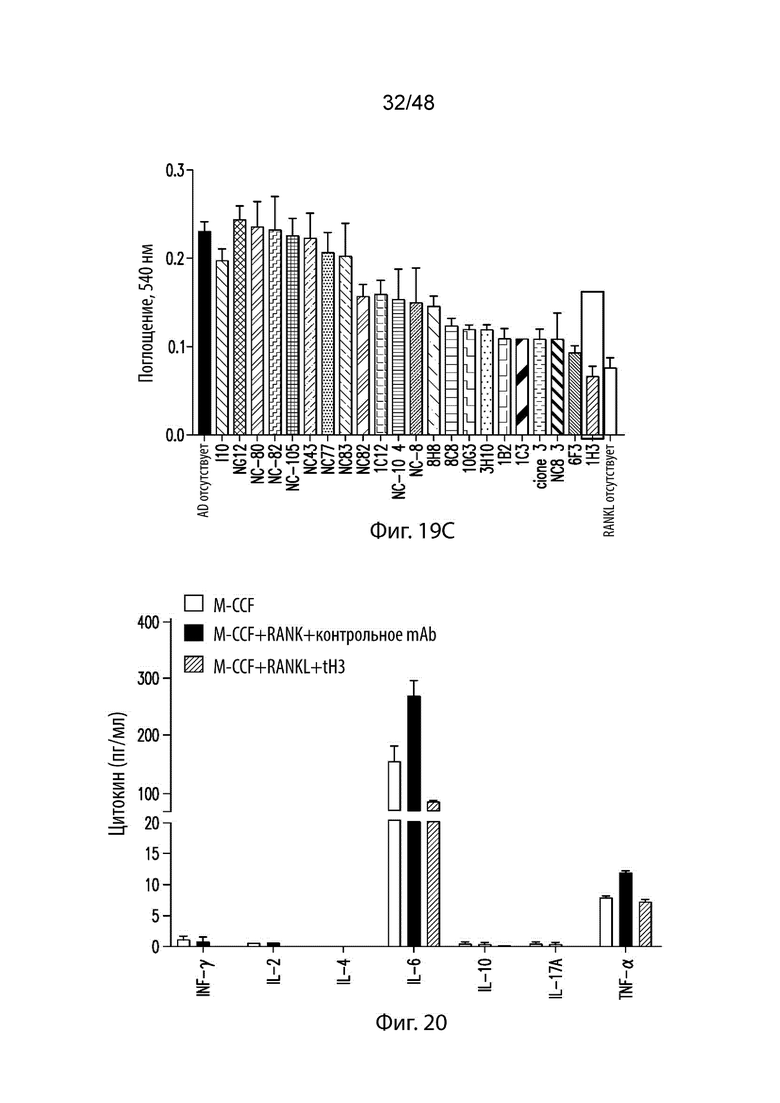










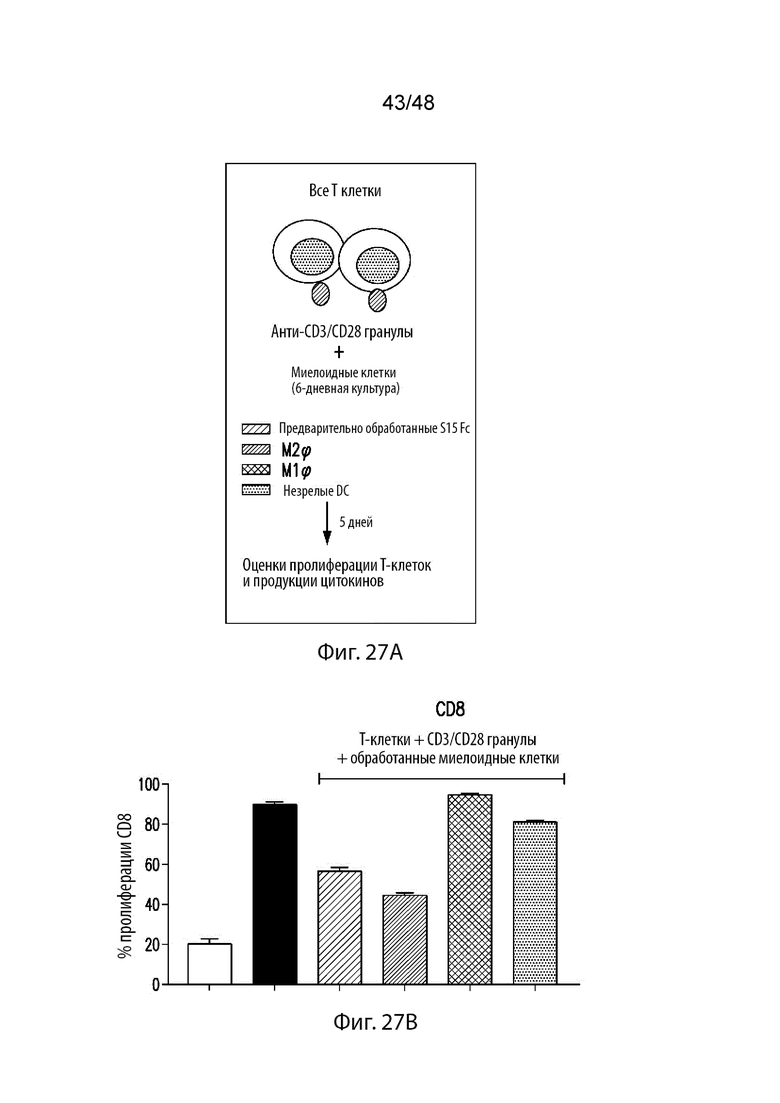





Изобретение относится к области биотехнологии, в частности к моноклональному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с SIGLEC-15, а также к содержащей его фармацевтической композиции. Изобретение эффективно для лечения опухоли у пациента, а также для усиления иммунного ответа у пациента. 16 н. и 12 з.п. ф-лы, 86 ил., 2 табл., 22 пр.
1. Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с SIGLEC-15,
где антитело содержит три CDR тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах любой последовательности вариабельной области тяжелой цепи (HCVR), выбранной из группы, состоящей SEQ ID NO:203, 206, 207; и три CDR легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах любой последовательности вариабельной области легкой цепи (LCVR), выбранной из группы, состоящей из SEQ ID NO:195, 197, 199, 201 и 219.
2. Моноклональное антитело или антигенсвязывающий фрагмент по п.1, содержащее:
(а) домен HCDR1 с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:204 и 208;
(b) домен HCDR2 с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:205 и 374;
(c) домен HCDR3 с аминокислотной последовательностью SEQ ID NO:71;
(d) домен LCDR1 с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO:28, 196, 198 и 200;
(е) домен LCDR2 c аминокислотной последовательностью, выбранную из группы, состоящей из SEQ ID NO:36 и 202; и
(f) домен LCDR3 с аминокислотной последовательностью SEQ ID NO:43.
3. Фармацевтическая композиция, содержащая эффективное количество моноклонального антитела или его антигенсвязывающего фрагмента по п.1 или 2 в комбинации со вспомогательным веществом для уменьшения SIGLEC-15-опосредованной иммуносупрессии у индивида.
4. Способ лечения опухоли у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.1 или 2 для снижения опухолевой нагрузки у пациента.
5. Способ по п.4, в котором опухоль представляет собой колоректальную опухоль, лимфому или опухоль яичника.
6. Способ усиления иммунного ответа у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.1 или 2 в количестве, эффективном для усиления иммунного ответа у пациента.
7. Способ по п.6, в котором усиленный иммунный ответ замедляет или предотвращает рост опухоли, ингибирует опосредованную опухолью иммуносупрессию, уничтожает опухоли, истощает или блокирует активность опухоль-ассоциированных макрофагов (TAM), снижает опосредованную опухолью иммуносупрессию, снижает или вызывает регресс Т-клеточной супрессии, увеличивает пролиферацию Т-клеток или приводит к их комбинации.
8. Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с SIGLEC-15,
где антитело содержит вариабельную область тяжелой цепи (HCVR) с последовательностью SEQ ID NO:18; и вариабельную область легкой цепи (LCVR) с последовательностью SEQ ID NO:7.
9. Моноклинальное антитело по п.8, в котором HCVR содержит
HCDR1 с SEQ ID NO:51,
HCDR2 c SEQ ID NO:61,
HCDR3 c SEQ ID NO:71,
LCDR1 c SEQ ID NO:28,
LCDR2 c SEQ ID NO:36 и
LCDR3 с SEQ ID NO:43.
10. Фармацевтическая композиция, содержащая эффективное количество моноклонального антитела или его антигенсвязывающего фрагмента по п.8 или 9 в комбинации со вспомогательным веществом для уменьшения SIGLEC-15-опосредованной иммуносупрессии у индивида.
11. Способ лечения опухоли у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.8 или 9 для снижения опухолевой нагрузки у пациента.
12. Способ по п.11, в котором опухоль представляет собой колоректальную опухоль, лимфому или опухоль яичника.
13. Способ усиления иммунного ответа у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.8 или 9 в количестве, эффективном для усиления иммунного ответа у пациента.
14. Способ по п.13, в котором усиленный иммунный ответ замедляет или предотвращает рост опухоли, ингибирует опосредованную опухолью иммуносупрессию, уничтожает опухоли, истощает или блокирует активность опухоль-ассоциированных макрофагов (ТAM), снижает опосредованную опухолью иммуносупрессию, снижает или вызывает регресс Т-клеточной супрессии, увеличивает пролиферацию Т-клеток или приводит к их комбинации.
15. Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с SIGLEC-15,
где антитело содержит вариабельную область тяжелой цепи (HCVR) с последовательностью SEQ ID NO:15; и вариабельную область легкой цепи (LCVR) с последовательностью SEQ ID NO:5.
16. Моноклональные антитела по п.15, в котором HCVR содержит
HCDR1 с SEQ ID NO:48
HCDR2 c SEQ ID NO:58,
HCDR3 c SEQ ID NO:69,
LCDR1 c SEQ ID NO:26,
LCDR2 c SEQ ID NO:34 и
LCDR3 с SEQ ID NO:41.
17. Фармацевтическая композиция, содержащая эффективное количество моноклонального антитела или его антигенсвязывающего фрагмента по п.15 или 16 в комбинации со вспомогательным веществом для уменьшения SIGLEC-15-опосредованной иммуносупрессии у индивида.
18. Способ лечения опухоли у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.15 или 16 для снижения опухолевой нагрузки у пациента.
19. Способ по п.18, в котором опухоль представляет собой колоректальную опухоль, лимфому или опухоль яичника.
20. Способ усиления иммунного ответа у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.15 или 16 в количестве, эффективном для усиления иммунного ответа у пациента.
21. Способ по п.20, в котором усиленный иммунный ответ замедляет или предотвращает рост опухоли, ингибирует опосредованную опухолью иммуносупрессию, уничтожает опухоли, истощает или блокирует активность опухоль-ассоциированных макрофагов (TAM), снижает опосредованную опухолью иммуносупрессию, снижает или вызывает регресс Т-клеточной супрессии, увеличивает пролиферацию Т-клеток или приводит к их комбинации.
22. Моноклональное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с SIGLEC-15,
где антитело содержит три CDR тяжелой цепи (HCDR1, HCDR2 и HCDR3) в пределах любой последовательности вариабельной области тяжелой цепи (HCVR), выбранной из группы, состоящей SEQ ID NO:212, 213, 215 и 216; и три CDR легкой цепи (LCDR1, LCDR2 и LCDR3) в пределах любой последовательности вариабельной области легкой цепи (LCVR), выбранной из группы, состоящей из SEQ ID NO:209, 210 и 211.
23. Моноклональное антитело или антиген-связывающий фрагмент по п.22, содержащее:
(а) домен HCDR1 с аминокислотной последовательностью SEQ ID NO:48;
(b) домен HCDR2 c аминокислотной последовательностью, выбранную из группы, состоящей из SEQ ID NO:58, 214, 217 и 218;
(c) домен HCDR3 с аминокислотной последовательностью SEQ ID NO:69;
(d) домен LCDR1 с аминокислотной последовательностью SEQ ID NO:26;
(e) домен LCDR2 с аминокислотной последовательностью SEQ ID NO:34; и
(f) домен LCDR3 с аминокислотной последовательностью SEQ ID NO:41.
24. Фармацевтическая композиция, содержащая эффективное количество моноклонального антитела или его антигенсвязывающего фрагмента по п.22 или 23 в комбинации со вспомогательным веществом для уменьшения SIGLEC-15-опосредованной иммуносупрессии у индивида.
25. Способ лечения опухоли у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.22 или 23 для снижения опухолевой нагрузки у пациента.
26. Способ по п.25, в котором опухоль представляет собой колоректальную опухоль, лимфому или опухоль яичника.
27. Способ усиления иммунного ответа у пациента, включающий введение пациенту терапевтически эффективного количества моноклонального антитела по п.22 или 23 в количестве, эффективном для усиления иммунного ответа у пациента.
28. Способ по п.27, в котором усиленный иммунный ответ замедляет или предотвращает рост опухоли, ингибирует опосредованную опухолью иммуносупрессию, уничтожает опухоли, истощает или блокирует активность опухоль-ассоциированных макрофагов (ТAM), снижает опосредованную опухолью иммуносупрессию, снижает или вызывает регресс Т-клеточной супрессии, увеличивает пролиферацию Т-клеток или приводит к их комбинации.
| WO2013034660 A1, 14.03.2013 | |||
| WO2011041894 A1, 06.10.2010 | |||
| TAKASHI ANGATA et al., Siglec-15: an immune system Siglec conserved throughout vertebrate evolution, Glycobiology, 2007, vol | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Углеподъемник для паровозов | 1924 |
|
SU838A1 |
| MATTHEW STUIBLE et al., Mechanism and Function of Monoclonal Antibodies Targeting Siglec-15 for Therapeutic Inhibition of Osteoclastic Bone | |||
Авторы
Даты
2021-11-12—Публикация
2017-09-21—Подача