Изобретение относится к химической промышленности, в частности к технологии получения нанодисперсного катализатора методом горения раствора применительно к технологии получения углеродных наноматериалов и водорода. Разработанный катализатор, в состав которого входят металлы из подгруппы VIII (например, Ni, Fe, Co и др.) и оксиды металлов подгруппы II-IV (например, Al, Mg и др.), выполняющие роль носителей катализатора. Нанодисперсный катализатор может быть использован в химической промышленности, порошковой металлургии, нанотехнологии, в частности, в процессе получения углеродных наноматериалов и водорода методом каталитического разложения метана и/или других углеводородных газов и их смесей. Углеродные наноматериалы могут быть использованы в области катализа, технологии композитных и теплоизоляционных материалов, электронике и в других областях науки и техники.
Известно несколько способов получения нанодисперсных частиц катализатора методом синтеза горением раствора:
1. Метод синтеза наноразмерных частиц катализатора из кристаллогидратов данных металлов путем восстановления органическим восстановителем (гексаметилтетрамином) при температуре синтеза 450°С (Synthesis of Ni-based catalysts by hexamethylenetetramine-nitrates solution combustion method for co-production of hydrogen and nanofibrous carbon from methane / D.G. Kuvshinov, P.B. Kurmashov, A.G. Bannov, M.V. Popov, G.G. Kuvshinov // International Journal of Hydrogen Energy. – 2019. – Vol. 44, iss. 31. – P. 16271-16286).
Недостатком данного способа является присутствие дополнительной стадии на этапе приготовления катализатора, в частности процесса смешения кристаллогидратов данных металлов с органическим восстановителем (гексаметилтетрамином), сопровождающееся дополнительной стадией прогрева при температуре 127°С, охлаждения до комнатной температуры с последующей стадией прокалки (восстановления) в муфельной печи исходных кристаллогидратов до их оксидного состояния.
2. Метод, основанный на реакции получения оксидов металлов из кристаллогидратов в результате восстановления гексаметилтетрамина при температуре 400°С (Prakash A.S., Khadar A.M.A., Patil K.C., and Hegde M.S. Hexamethylenetetramine: A new fuel for solution combustion synthesis of complex metal oxides // Journal of Materials Synthesis and Processing, 2002; 10:135-141).
Недостатком данного способа является то, что исходный образец катализатора вводят в предварительно нагретую до 400°С реакционную камеру печи. Возникающий при этом термоудар и градиент температур в исследуемом образце катализатора активирует реакцию горения гексаметилтетрамина, сопровождающейся резким выделением теплоты в результате протекания экзотермической реакции сопровождающегося самовоспламенения, с последующим образованием пенообразной массы в объеме сосуда. В предлагаемом способе отсутствует контролировать начальную температуру синтеза катализатора возможность с высокой точностью, которая, в свою очередь, может снизить активность катализатора.
3. Синтез наноразмерных порошков из солей металлов, образованных в результате горения воспламеняемых реагентов, в частности аминокислоты (глицина) (Патент США 5114702, МПК С01В 13/18, 1992 год). Процесс реализуется в три стадии: упаривание водного раствора до образования гелеобразной пасты, нагрев полученного промежуточного продукта до температуры воспламенения глицина (200°С) с последующей стадией прокалки при температуре 600-700°С.
Недостатком предложенного способа является трехстадийность метода синтеза катализатора, а также введение дополнительной стадии окисления продуктов реакции синтеза.
4. Синтез оксидных порошков редкоземельных металлов, получаемых в результате горения (воспламенения) тетраформил триазина (C4H16N6O2), сопровождаемого процессом восстановления кристаллогидратов данных металлов до оксидной фазы при температуре 500°С и температуре горения смеси более 1000°С (Manoharan S.S, Patil K.C. Combustion route to fine particle perovskite oxides // Journal of Solid State Chemistry, 1993, v.102, p.267-276).
Недостатком данного способа является синтез катализаторов из солей редкоземельных металлов, а также необходимость в организации дополнительной стадии окисления катализатора в воздушной среде при температуре 800°С в течение 1 ч.
Общим недостатком этих способов является то, что процесс сопровождается дополнительной стадией смешения исходных компонентов при температурах соответствующих температуре разложения солей кристаллогидратов данных металлов; синтез нанодисперсных частиц катализатора реализуется при высоких температурах синтеза, кроме того процесс сопровождается дополнительной стадией прокалки (окисления) предшественника катализатора в воздушной среде.
Наиболее близким по технической сущности и достигаемому результату является способ получения нанодисперсных частиц катализатора (Патент РФ №2318723 С2, С01В 13/18, опубликован 14.04.2006). Сущность этого способа заключается в том, что получаемые нанодисперсные порошки оксидов металлов получают путем приготовления смеси растворов или расплавов кристаллогидратов соответствующих металлов и органического восстановителя (мочевина, лимонная и щавельная кислоты или соли этих кислот, глицина, гидразина или их солей, карбогидразида, оксалдигридразида, гидроксиламина или их солей, полиакриловую кислоту).
Процесс проводят в реакторе непрерывного действия при температуре 400-700°С, сопровождающегося стадией упаривания водных растворов и/или расплавов до инициирования реакции горения активного компонента с последующим образованием продуктов реакции в результате протекания самоподдерживающейся реакции горения. Синтез реализуется на нагреваемой поверхности, в качестве которой используют различные вращающиеся поверхности, такие как диск, чаши, трубы, валки, а также их модификации. Следовательно, в процессе приготовления катализатора с нагреваемой поверхности непрерывно удаляются газообразные вещества, а продукт реакции собирается в сборник. Недостатком данного способа является аппаратурно-технологическая схема производства нанодисперсных частиц катализатора, которая не позволяет обеспечить равномерное температурное поле во всем объеме реактора, нуждается в непрерывном удалении из зоны реакции образующихся твердых и газообразных продуктов, имеет высокие энергозатраты, связанные с нагревом рабочей зоны реактора.
Задачей (техническим результатом) настоящего изобретения является уменьшение энергозатрат на производство катализатора, перспективного для синтеза углеродных наноматериалов и водорода.
Поставленная техническая задача получения нанодисперсного катализатора достигается путем приготовления совместного комплексного раствора из кристаллогидратов по меньшей мере одного металла, проявляющие окислительные свойства, и органического соединения (глицина) растворенного в дистиллированной воде и проявляющего восстановительные свойства, при этом нагрев полученного комплексного раствора осуществляется до температур 350-450°С при скорости нагрева 1-15°С/мин, сопровождающегося упариванием комплексного раствора до гелеобразного состояния с последующим воспламенением самоподдерживающейся реакции горения органического соединения с образованием нанодисперсного катализатора.
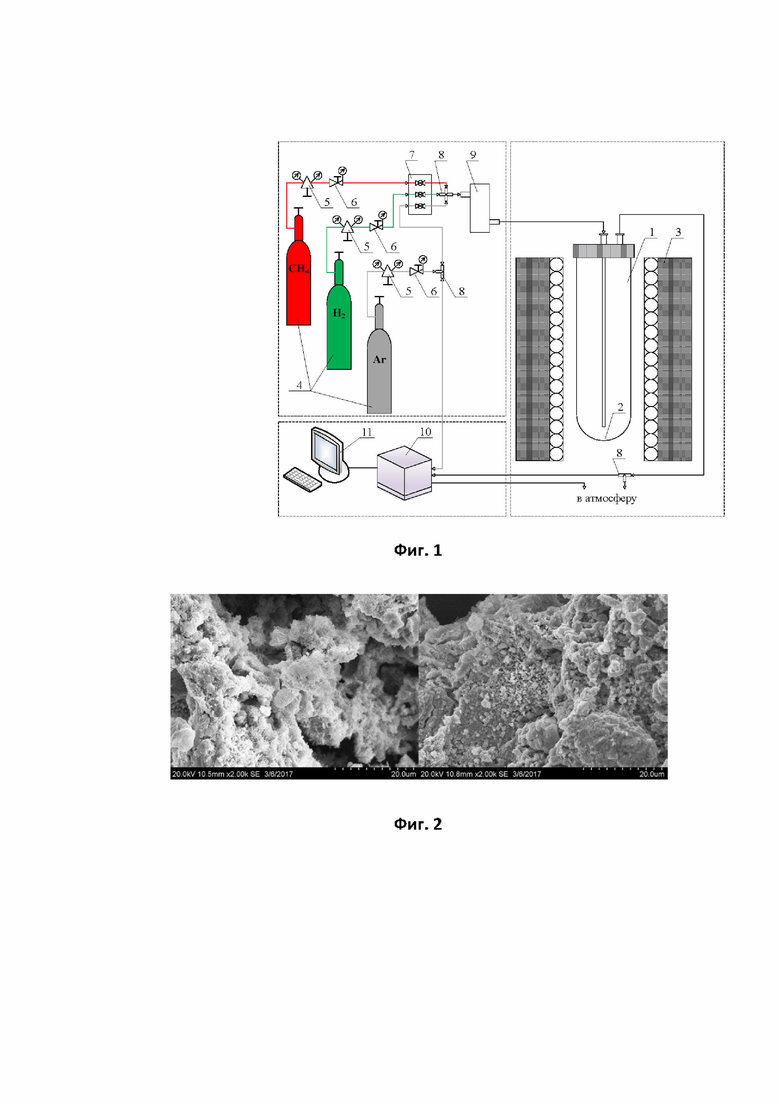
На фиг. 1 представлена принципиальная схема лабораторной установки для осуществления каталитической реакции разложения метана на углеродные наноматериалы и водород.
На фиг. 2 показаны микрофотографии синтезируемых частиц нанодисперсного катализатора, полученные с помощью сканирующей электронной микроскопии (СЭМ).
На фиг. 3 показаны микрофотографии синтезируемых частиц нанодисперсного катализатора, полученные с помощью просвечивающей электронной микроскопа (ПЭМ).
На фиг. 4 показаны микрофотографии углеродных наноматериалов, синтезированных на катализаторе, полученном методом горения раствора.
Оценка эффективности работы синтезируемых образцов катализаторов осуществлялась в реакции разложения метана на водород и углеродный наноматериал, осаждаемый на нанодисперсном катализаторе.
Процесс тестирования синтезируемых образцов катализатора осуществлялся в лабораторной каталитической установке следующим образом (см. фиг. 1). В рабочий объем реактора (1) загружался исследуемый образец катализатора (2) массой 12 мг, реактор в дальнейшем размещался в трубчатой электропечи сопротивления (3). Система подготовки газа предназначена для обеспечения точного дозирования и подачи газа в реактор. Данная система состоит: из газовых баллонов (метан, водород, аргон) (4), редукторов высокого (5) и низкого (6) давления, шарового вентиля (7), газового смесителя (8), а также автоматического регулятора расхода газа (9). Тестирование катализатора производили в среде метана, при температуре 550°С и давлении 1 атм. Удельный расход метана на протяжении всего эксперимента составлял 100 л/(ч⋅гкат). Анализ газообразных продуктов реакции осуществлялся газовым хроматографом (10) в автоматическом режиме с применением программного обеспечения «Хромос», установленного на персональном компьютере (11).
Заявленный способ содержит следующие стадии: приготовление совместного комплексного раствора из кристаллогидратов данных металлов (окислителя) и органического соединения (восстановителя) растворенного в дистиллированной воде, перемешивание полученной комплексного раствора, нагрев до температур 350-450°С, сопровождающееся упариванием комплексного раствора до гелеобразного состояния с последующим воспламенением самоподдерживающейся реакции горения органического соединения с образованием нанодисперсного катализатора.
В качестве критерия оценки эффективности катализатора использовали удельный выход углеродного наноматериала, который осаждался на нанодисперсном катализаторе в процессе каталитической реакции, а также удельный выход водорода на единицу массы катализатора.
Получаемый катализатор характеризуется высокой удельной поверхностью не менее чем 150 м2/г, за счет смешения на молекулярном уровне основных компонентов реакции (окислителя и восстановителя), быстроты протекания реакции горения и охлаждения образца, интенсивности выделения газообразных продуктов реакции.
Катализаторы, приготовленные предлагаемым способом, имеют ряд преимуществ по сравнению с другими способами синтеза (соосаждения, механоактивации, золь-гель синтез и др.), в частности: одностадийный метод получения нанодисперсных порошков катализатора, отсутствие в необходимости осуществления процесса восстановления катализатора, малые трудо- и энергозатраты. Сущность изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Пример 1. В фарфоровой чаше в объеме 100 мл дистиллированной воды были растворены навески кристаллогидратов Ni(NO3)2·6H2O массой 13,375 г, Al(NO3)3·9H2O – 2,2075 г и глицина – 1,5 г. Далее приготовленный раствор исходных компонентов помещался в муфельную печь. Восстановление катализатора осуществлялось при температуре 450°С и скорости нагрева 1°С/мин.
Пример 2. Аналогичен примеру 1, отличается тем, что навеска глицина составляет 0,5 г. Восстановление катализатора осуществлялось при температуре 350°С и скорости нагрева 1°С/мин.
Пример 3. Аналогичен примеру 1, отличается тем, что восстановление катализатора осуществлялось при температуре 350°С при скорости роста температуры печи 1°С/мин, а также изотермической выдержки катализатора в течение 20 минут при температуре 350°С.
Пример 4. Аналогичен примеру 2, отличается тем, что навеска глицина составляет 0,5 г. Восстановление катализатора осуществлялось при температуре 450°С при скорости роста температуры печи 1°С/мин, а также изотермической выдержки катализатора в течение 20 минут при температуре 450°С.
Пример 5. Аналогичен примеру 1, отличается тем, что восстановление катализатора осуществлялось при скорости роста температуры печи 10°С/мин, а также изотермической выдержке катализатора в течение 20 минут при температуре 450°С.
Пример 6. Аналогичен примеру 2, отличается тем, что восстановление катализатора осуществлялось при скорости роста температуры печи 10°С/мин, а также изотермической выдержки катализатора в течение 20 минут при температуре 350°С.
Пример 7. Аналогичен примеру 1, отличается тем, что восстановление катализатора осуществлялось при температуре 350°С и скорости нагрева 10°С/мин.
Пример 8. Аналогичен примеру 2, отличается тем, что восстановление катализатора осуществлялось при температуре 450°С и скорости нагрева 10°С/мин.
Пример 9. Аналогичен примеру 1, отличается тем, что восстановление катализатора осуществлялось при скорости роста температуры печи 15°С/мин.
Из представленных примеров следует, что изобретение позволяет синтезировать нанодисперсный катализатора (Фиг. 2 и 3), характеризующийся высокой каталитической активностью в реакции разложения метана на углеродные наноматериалы и водород.
Данные об основных показателях процесса синтеза нанодисперсного катализатора применительно к технологии синтеза углеродных наноматериалов и водорода по предлагаемому способу представлены в таблице 1.
Таким образом, катализаторы, приготовленные предлагаемым способом, по сравнению с другими способами синтеза (соосаждения, механоактивации, золь-гель синтез и др.), имеют ряд преимуществ, в частности: одностадийный метод получения нанодисперсных порошков катализатора, отсутствие в необходимости осуществления процесса восстановления катализатора, малые трудо- и энергозатраты.
Таблица 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ НАНОРАЗМЕРНОГО КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ УГЛЕРОДНЫХ НАНОМАТЕРИАЛОВ И ВОДОРОДА | 2023 |
|
RU2835078C1 |
| Способ получения водорода и углеродного наноматериала, катализатор для его осуществления и способ приготовления катализатора | 2023 |
|
RU2808321C1 |
| Способ получения водорода и углеродных нановолокон и установка для осуществления такого способа | 2023 |
|
RU2836235C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОДИСПЕРСНЫХ НАНЕСЕННЫХ КАТАЛИЗАТОРОВ И СИНТЕЗ УГЛЕРОДНЫХ НАНОТРУБОК | 2008 |
|
RU2373995C1 |
| Способ получения углеродного наноматериала и водорода (варианты) и устройство для получения углеродного наноматериала и водорода в непрерывном режиме | 2022 |
|
RU2790169C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ ФУРФУРОЛА | 2018 |
|
RU2689417C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ Pd-CeO НАНЕСЕННЫХ КАТАЛИЗАТОРОВ | 2005 |
|
RU2297279C1 |
| СПОСОБ АКТИВАЦИИ МЕТАЛЛОКСИДНЫХ КАТАЛИЗАТОРОВ СИНТЕЗА УГЛЕРОДНЫХ НАНОМАТЕРИАЛОВ | 2010 |
|
RU2443470C2 |
| Катализатор гидроизомеризации н-алканов и способ его приготовления | 2016 |
|
RU2632890C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И ПРОЦЕСС ГИДРОДЕОКСИГЕНАЦИИ КИСЛОРОДОРГАНИЧЕСКИХ ПРОДУКТОВ БЫСТРОГО ПИРОЛИЗА БИОМАССЫ | 2007 |
|
RU2335340C1 |

Изобретение относится к химической промышленности, в частности к технологии получения нанодисперсного катализатора, и может быть использовано в химической промышленности, порошковой металлургии, нанотехнологии. Способ получения нанодисперсного катализатора для синтеза углеродных наноматериалов и водорода путем приготовления совместного комплексного раствора из кристаллогидратов по меньшей мере одного металла, проявляющего окислительные свойства, и органического соединения, растворенного в дистиллированной воде, проявляющего восстановительные свойства, при этом нагрев полученного комплексного раствора осуществляется до температуры 350-450°С при скорости нагрева 1-15°С/мин, сопровождающегося процессом упаривания комплексного раствора до гелеобразного состояния с последующим воспламенением самоподдерживающейся реакции горения органического соединения с формированием нанодисперсного катализатора. Техническим результатом является уменьшение энергозатрат на производство катализатора, перспективного для синтеза углеродных наноматериалов и водорода. 3 з.п. ф-лы, 4 ил., 1 табл.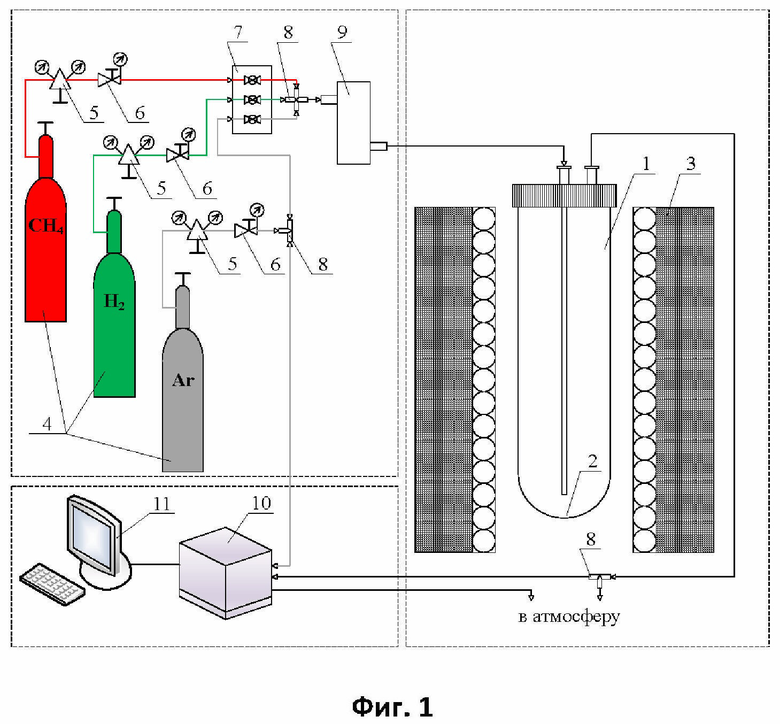
1. Способ получения нанодисперсного катализатора для синтеза углеродных наноматериалов и водорода путем приготовления совместного комплексного раствора из кристаллогидратов по меньшей мере одного металла, проявляющего окислительные свойства, и органического соединения, растворенного в дистиллированной воде, проявляющего восстановительные свойства, отличающийся тем, что нагрев полученного комплексного раствора осуществляется до температуры 350-450°С при скорости нагрева 1-15°С/мин, сопровождающегося процессом упаривания комплексного раствора до гелеобразного состояния с последующим воспламенением самоподдерживающейся реакции горения органического соединения с формированием нанодисперсного катализатора.
2. Способ по п.1, отличающийся тем, что в качестве активных компонентов катализатора используют кристаллогидраты подгруппы VIII.
3. Способ по п.1, отличающийся тем, что в качестве носителей катализатора используют кристаллогидраты подгруппы II-IV.
4. Способ по п.1, отличающийся тем, что получаемый нанодисперсный катализатор используют в реакции синтеза углеродного наноматериала и водорода без его восстановления в потоке водорода.
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ ОКСИДОВ МЕТАЛЛОВ | 2006 |
|
RU2318723C2 |
| US 5114702 A1, 19.05.1992 | |||
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДОВ МЕТАЛЛОВ, ИХ СМЕСЕЙ И ТВЕРДЫХ РАСТВОРОВ | 2002 |
|
RU2226498C2 |
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНЫХ ОКСИДОВ ЭЛЕМЕНТОВ | 1994 |
|
RU2073638C1 |
Авторы
Даты
2022-06-21—Публикация
2021-09-24—Подача