Область техники
Изобретение относится к органической химии и направлено на создание препаратов для лечения энтеровирусных инфекций (ЭВИ) на основе органических соединений.
Уровень техники.
Вирус Коксаки - группа высоко контагиозных энтеровирусов, попадающих в организм человека через слизистую ротовой полости и далее, достигая кишечника, активно размножающихся в кишечнике. В тяжелой форме болезнь может поражать нервную систему, включая головной мозг, а также нарушать работу сердца, влиять на изменения в мышечной ткани этого органа, и негативно сказываться на печени.
Ввиду отсутствия зарегистрированных этиотопных препаратов для терапии ЭВИ, поиск противовирусных препаратов нового поколения с улучшенными характеристиками актуален.
Большая часть вирусных инфекций сопровождаются генерацией активных форм кислорода. Поэтому использование антиоксидантов для профилактики и лечения вирусных заболеваний активно изучается [В.В. Зарубаев, А.В. Слита, Н.А. Калинина, А.В. Гаршинина, А.А. Штро, Л.А. Карпинская. Протективная активность интерферона в комбинации с различными антиоксидантами в отношении экспериментальной летальной гриппозной инфекции //РМЖ, 2012, №28, 1416-1420], [R. Sgarbanti, D. Amatore, I. Celestino, M.E. Marcocci, A. Fraternale, M.R. Ciriolo, M. Magnani, R. Saladino, E. Garaci, A.T. Palamara L. Nencioni. Intracellular Redox State as Target for Anti-Influenza Therapy: Are Antioxidants Always Effective? // Curr. Top. Med. Chem. 2014, Vol.14, №22, p. 2529-2541].
Комбинацией противовирусных (противогриппозных) и антиоксидантных свойств обладают, например, производные аминофенолов 1 [О. Shadyro, G. Ksendzova, G. Polozov, V. Sorokin, E. Boreko, O. Savinova, B. Dubovik, N. Bizunok. Synthesis and study of antiviral and anti-radical properties of aminophenol derivatives // Bioorganic & Medicinal Chemistry Letters, 2008, Vol.18, p. 2420-2423], 6-нитро-1,2,4-триазолоазины с полифенольными фрагментами 2 [E.N. Ulomskiy, A.V. Ivanova, E.B. Gorbunov, I.L. Esaulkova, A.V. Slita, E.O. Sinegubova, E.K. Voinkov, R.A. Drokin, I.I. Butorin, E.R. Gazizullina, E.L. Gerasimova, V.V. Zarubaev, V.L. Rusinov. Synthesis and biological evaluation of 6-nitro-1,2,4-triazoloazines containing polyphenol fragments possessing antioxidant and antiviral activity // Bioorganic & Medicinal Chemistry Letters, 2020, Vol.30, p. 127216] и аминометансульфоновые кислоты 3 [R.E. Khoma, V.O. Gelmboldt, A.A. Ennan, T.L. Gridina, A.S. Fedchuk, V.P. Lozitsky, I.M. Rakipov, A.S. Vladyka. Synthesis and antioxidant and anti-influenza activity of aminomethanesulfonic acids // Pharm. Chem. J., 2019, Vol.53, №5, p. 436]
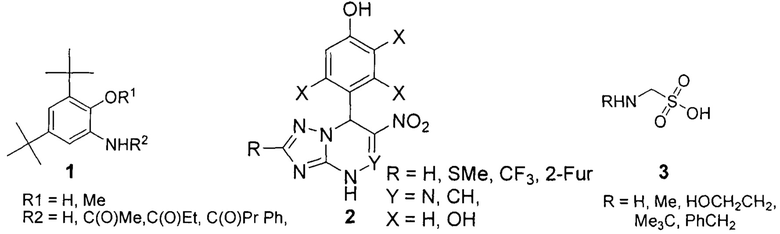
Однако зарегистрированных препаратов, реализующих противовирусный потенциал в отношении вирусов рода Enterovirus посредством антиоксидантных свойств, в настоящий момент нет. Известно несколько групп малых молекул, активных в отношении энтеровирусов разных групп in vitro и in vivo: вещества, связывающиеся с вирусным капсидом (плеконарил и его производные, пиродавир, вапендавир, покапавир), ингибиторы вирусных протеаз (рупинтривир и его производные), ингибиторы полимеразного комплекса вирусов (рибавирин, 5-нитро-цитидин,флуоксетин, дибукаин). Однако среди тех групп соединений, которые успешно прошли доклинические исследования, ни для одного из препаратов не был показан хороший профиль эффективности и безопасности в выполненных клинических исследованиях. Кроме того, к соединениям, сходным по структуре и механизму действия, вирусы быстро вырабатывают перекрестную резистентность, что существенно ограничивает их применение.
Было установлено, что ряд производных 2-[5-(арил)-6-R-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолов 4-7 обладают антиоксидантной активностью [Т.Г. Федорченко, Г.Н. Липунова, А.В. Щепочкин, М.С. Валова, А.Н. Цмокалюк, П.А. Слепухин, О.Н. Чупахин. Синтез, спектральные, электрохимические и антиоксидантные свойства 2-[5-(арил)-6-R-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолов // ЖОрХ, 2020, Т. 56, №1, 52-64]
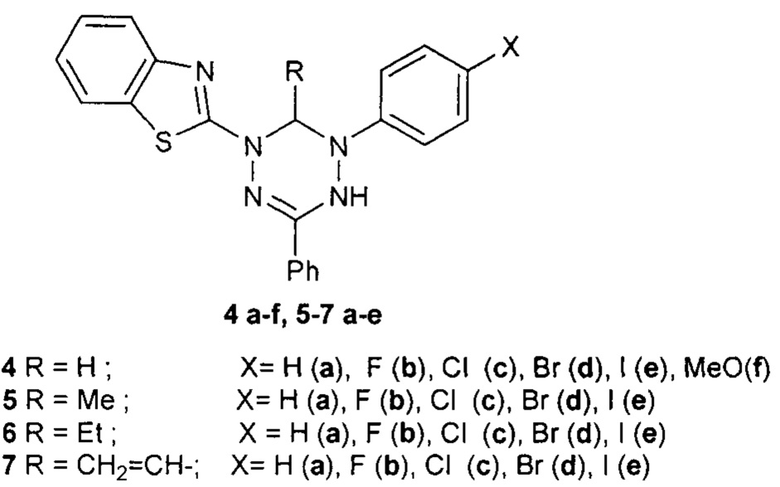
Раскрытие изобретения
Цель настоящего изобретения заключается в создании новых производных 5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил-бензотиазолов, способных ингибировать репродукцию энтеровирусов.
Заявленные соединения синтезировали алкилированием 5-(бензотиазол-2-ил)-1-(4-метоксифенил)-3-фенилформазана 8, с последующей циклизацией продуктов алкилирования по описанной ранее методике [Т.Г. Федорченко, Г.Н. Липунова, А.В. Щепочкин, М.С. Валова, А.Н. Цмокалюк, П.А. Слепухин, О.Н. Чупахин. Синтез, спектральные, электрохимические и антиоксидантные свойства 2-[5-(арил)-6-R-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолов // ЖОрХ, 2020, Т. 56, №1, 52-64]:
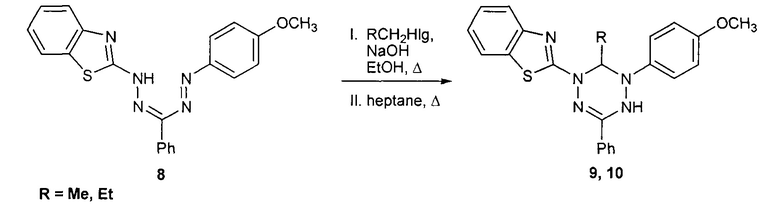
К суспензии 5-(бензотиазол-2-ил)-1-(4-метоксифенил)-3-фенилформазана 8 (0.309 г, 0.8 ммоль) в 20 мл этанола добавляют 30% водный раствор гидроксида натрия (0.12 мл, 0.9 ммоль). К полученному темно-фиолетовому раствору добавляют соответствующий алкил-галогенид (8.0 ммоль), смесь кипятят 15 минут. Растворитель отгоняют под вакуумом. К реакционной массе добавляют 30 мл гептана, кипятят в течение часа. Гептан отгоняют под вакуумом. Продукт выделяют из реакционной массы колоночной хроматографией на силикагеле (элюент : гексан/хлороформ 2:1).
Температуры плавления определены с помощью аппарата Stuart SMP3. Контроль за ходом реакций и чистотой полученных продуктов осуществлен методом ТСХ на пластинах Sorbfil ПТСХ-АФ-А-УФ. Колоночная хроматография проведена с использованием силикагеля Kieselgel 60 (размер частиц 0.040-0.063 мм, 230-00 меш). Спектры ЯМР получали на спектрометре Bruker Avance III-500 МГц. ИК-спектры поглощения записывали с помощью приставки DRA на спектрофотометре Spectrum One (Perkin Elmer). УФ спектры зарегистрированы в метаноле на спектрофотометре UV2600 фирмы Shimadzu (Япония). Масс-спектры записаны на приборе Bruker Daltonics maXis impact HD, метод ионизации ESI. Элементный анализ проведен с помощью автоматического элементного анализатора CHNS РЕ 2400, серия II (Perkin Elmer Instruments).
Примеры реализации изобретения
Структурная идентификация продуктов.
Пример 1. 2-(5-(4-Метоксифенил)-3-фенил-6-метил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил)-бензтиазол 9
Синтезировали по общей методике, в качестве алкилирующего агента использовали йодэтан. Выход 205 мг (62%). Т.пл. 191°С (МеОН). Спектр ЯМР 1Н, δ, м.д.: 1.49 д (3Н, J 6.9 Гц, СН3), 3.65 с (3Н, ОСН3), 6.20 кв (1Н, J 6.9 Гц, СН), 6.86 д (2Наром., J 9.2 Гц), 7.07 т (1Наром., J 8.1 Гц), 7.16 д(2Наром., J 9.2 Гц), 7.27 т (1Наром., J 8.1 ГЦ), 7.50 д (1Наром., J 8.1 Гц), 7.52-7.58 м (3Наром), 7.74 д (1Наром., J 8.1 Гц) 7.89-7.96 м (2Наром.), 9.56 уш.с (1H, NH). Спектр ЯМР, 13С, δ, м.д.: 16.19, 55.12, 67.60, 114.37, 118.87, 119.49, 121.26, 125.70, 125.86, 128.63, 130.51, 130.68, 131.19, 143.71, 144.26, 152.31, 155.17, 166.03. ИК спектр, v, см-1: 3332, 1595, 1533, 1504, 1444, 1277, 1178, 753, 693. Масс-спектр: найдено, m/z: 416.1535 [М+Н]+. Вычислено для C23H21N5OS, m/z. 415.1567. Рассчитано для C23H21N5OS, %: С, 66.48; Н, 5.09; N, 16.85. Найдено, %: С, 66.46; Н, 5.07; N, 16.83.
Пример 2. 2-(5-(4-Метоксифенил)-3-фенил-6-этил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил)-бензтиазол 10
Синтезировали по общей методике, в качестве алкилирующего агента использовали бромпропан. Выход 161 мг (47%). Т.пл. 187°С (МеОН). Спектр ЯМР 1Н, δ, м.д.: 1.12 т (3Н, СН3, J 7.8 Гц), 1.67-1.95 м (2Н, СН2), 3.65 с (3Н, ОСН3), 5.92-6.0 м (2Н, СН), 6.86 д (2Наром., J 8.8 Гц), 7.05 т (1Наром., J 7.2 Гц), 7.14 д (2Наром., J 8.8 Гц), 7.25 т (1Наром., J 7.2 Гц), 7.47 д (1Наром., J 8.0 Гц), 7.51-7.59 м (3Наром.), 7.72 д (1Наром., J 8.0 Гц) 7.86-7.95 м (2Наром.), 9.51 уш.с (1H, NH). Спектр ЯМР 13С, δ, м.д.: 9.72, 22.95, 55.11, 72.67, 114.39, 118.79, 119.55, 121.09, 125.89, 128.63, 130.53, 130.67, 131.18, 143.77, 144.66, 152.35, 155.13, 166.17. ИК спектр, v, см-1: 3177, 1596, 1536, 1505, 1446, 1276, 1178, 753, 693. Масс-спектр: найдено, m/z: 430.1700 [М+Н]+. Вычислено для C24H23N5OS, m/z: 429.1623. Рассчитано для C24H23N5OS, %: С, 67.11; Н, 5.40; N, 16.30. Найдено, %: С, 67.08; Н, 5.37; N, 16.29.
Пример 3. Оценка цитотоксичности соединений
Токсичность соединений была изучена в отношении клеток Vero. Клетки сеяли в 96-луночные планшеты и культивировали при 37°С в среде MEM с добавлением 10% сыворотки крупного рогатого скота в атмосфере 5% СО2 (в газопроточном инкубаторе Panasonic 170-AIC) до состояния монослоя. Из исследуемых соединений готовили маточный раствор концентрации 10 мг/мл в диметилсульфоксиде, после чего готовили серию трехкратных разведений препаратов в среде MEM от 1000 до 1 μg/ml. Растворенный препарат вносили в лунки планшетов и инкубировали 1 сутки при 37°С. По истечении этого срока клетки промывали 2 раза по 5 минут фосфатно-солевым буфером, и количество живых клеток оценивали при помощи микротетразолиевого теста (МТТ). С этой целью в лунки планшетов добавляли по 100 мкл раствора (5 мг/мл) 3-(4,5-диметилтиазолил-2) 2,5-дифенилтетразолия бромида (ICN Biochemicals Inc., Aurora, Ohio) на физиологическом растворе. Клетки инкубировали при 37°С в атмосфере 5% СО2 в течение 2 часов и промывали 5 минут фосфатно-солевым буфером. Осадок растворяли в 100 мкл на лунку ДМСО, после чего оптическую плотность в лунках планшетов измеряли на планшетном ридере Thermo Multiskan FC при длине волны 535 нм. По результатам теста для каждого продукта определяли 50% цитотоксическую дозу (СС50), т.е. концентрацию препарата, вызывающую гибель 50% клеток в культуре с использованием программного обеспечения GraphPadPrism6.
Значения СС50 для соединения 9 и 10 составили 850 мкг/мл и >1000 мкг/мл, соответственно. Полученные данные свидетельствуют о низкой токсичности полученных соединений, поскольку их следует отнести к 4-му из пяти существующих классу опасности (50% токсическая доза от 300 до 2000 мг/кг, или мкг/мл) [Классификация Европейской экономической комиссии ЕЭК ООН), https://unece.org/DAM/trans/danger/publi/ghs/ghs_rev07/Russian/03r_Part3.pdfl.
Пример 4. Оценка противовирусного действия
Противовирусную активность соединений изучали в культуре клеток Vero в отношении вируса Коксаки В3. Клетки Vero рассевали на 96-луночные планшеты, как описано в Примере 1. После формирования монослоя в лунки добавляли изучаемые соединения в соответствующих концентрациях (от 100 мкг/мл до 1 мкг/мл), инкубировали 1 час и заражали клетки вирусом Коксаки В3 при множественности заражения 0,01 TCID50 на клетку. Планшеты инкубировали 1 час, несвязавшийся вирус отмывали физиологическим раствором, добавляли свежие растворы соединений в тех же концентрациях и инкубировали планшеты при 37°С в атмосфере 5% СО2 в течение 24 часов. После этого инфекционную активность вирусного потомства в каждой лунке планшета определяли при помощи титрования на клетках Vero методом предельных разведений (титрование по конечной точке). Для этого из вируссодержащей жидкости готовили серию десятикратных разведений, заражали ими клетки Vero, предварительно посеянные в 96-луночные планшеты и инкубировали 72 часа при 37°С в атмосфере 5% СО2. По прошествии этого срока визуально отмечали наличие вирусспецифического цитопатогенного действия (ЦПД) в лунках планшетов. За титр вируса принимали максимальное разведение вируса, приводящее к появлению ЦПД в половине инфицированных лунок. Титр выражали в 50% цитотоксических дозах (TCID50/0,2 мл). На основании полученных данных с использованием программного обеспечения GraphPadPrism6 для каждого соединения рассчитывали значение 50% ингибирующей концентрации (IC50) - концентрации, снижающей титр вируса вдвое по сравнению с контролем, а также индекс селективности - отношение СС50 к IC50, показывающий, насколько избирательно соединение подавляет репродукцию вируса по сравнению с клеточным метаболизмом.
Полученные в результате экспериментов значения IC50 для соединений 9 и 10 составили 10 и 25,8 мкг/мл, соответственно. Таким образом, величины индексов селективности составили 85 и > 38, соответственно. Эти показатели намного превосходят пороговое значение SI=10, на основании которого делается заключение о перспективности того или иного соединения как потенциального противовирусного средства [Smee D., J Virol Methods; 2017:51-56], что убедительно доказывает высокие вирусингибирующие характеристики изученных соединений.
Результаты исследований представлены в таблице 1.
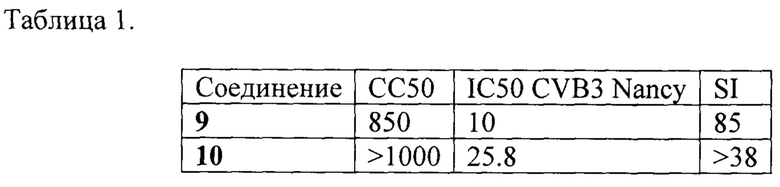
Заявляемые соединения (9, 10) проявляют высокую активность в отношении коллекционного штамма вируса Коксаки В3 (Nancy).
Таким образом, заявляемые 2-[5-(4-метоксифенил)-3-фенил-3-метил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазол (9) 2-[5-(4-метоксифенил)-3-фенил-6-этил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазол (10) обладают выраженной противовирусной активностью в отношении вируса Коксаки В3, а также низкой цитотоксичностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-[6-МЕТИЛ-3-(ТИЕН-2-ИЛ)-5-ФЕНИЛ-5,6-ДИГИДРО-4Н-[1,2,4,5]ТЕТРАЗИН-1-ИЛ]-БЕНЗОТИАЗОЛ С ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСОВ КОКСАКИ В3 | 2023 |
|
RU2836398C1 |
| 3-Нитро-4-гидрокси-7-пропаргилтио-[1,2,4]триазоло[5,1c][1,2,4]триазин и 3-нитро-4-гидрокси-7-этилтио-[1,2,4]триазоло[5,1c][1,2,4]триазин, обладающие противовирусной активностью | 2019 |
|
RU2775551C2 |
| 5-(Бензо[d]тиазол-2-ил)-6-метил-1-(4-метоксифенил)-3-(2-пиридил)-вердазил и способ его получения | 2023 |
|
RU2818595C1 |
| Диметил 7-метил-2-(пирролидин-1-ил)-4-фенилпирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилат и диметил 7-метил-2-(4-R-фенил)-4-(4-R-фенил)пирроло[2,1-ƒ][1,2,4]триазин-5,6-дикарбоксилаты, обладающие противовирусной активностью | 2021 |
|
RU2790376C1 |
| Средство, обладающее противовирусным действием в отношении герпесвируса человека I типа и энтеровируса В | 2022 |
|
RU2798659C1 |
| ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ 3,7-ДИЗАМЕЩЕННЫЕ [1,2,4]ТРИАЗОЛО[1,5-b][1,2,4,5]ТЕТРАЗИНЫ | 2022 |
|
RU2802300C1 |
| 2-(1,2,3-ТРИАЗОЛИЛ)ЗАМЕЩЕННЫЕ ЛИНЕЙНЫЕ ФУРОКУМАРИНЫ, ОБЛАДАЮЩИЕ АНТИВИРУСНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА A/Н1N1 | 2024 |
|
RU2841063C1 |
| 6,8-Дифтор-2-(4-(трифторметил)фенил)хроман-4-он в качестве ингибитора репродукции вирусов гриппа А и В и способ его получения | 2023 |
|
RU2826250C1 |
| 3-Бутилтио-1-(бета-D-2-дезоксирибофуранозил)-5-фенил-(4Н)-1,2,4-триазол, синтез, противогерпесвирусное действие | 2023 |
|
RU2815137C1 |
| СЕЛЕКТИВНЫЙ ПРОТИВОТУБЕРКУЛЕЗНЫЙ АГЕНТ, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ 3-ГИДРАЗОНО-6-(3,5-ДИМЕТИЛПИРАЗОЛ-1-ИЛ)- 1,2,4,5-ТЕТРАЗИН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2479311C2 |
Изобретение относится органической химии и включает 2-[5-(4-Метокси)-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолы формулы I. Технический результат - 2-[5-(4-Метокси)-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолы формулы I, обладающие противовирусной активностью в отношении вируса Коксаки. 1 табл., 4 пр.
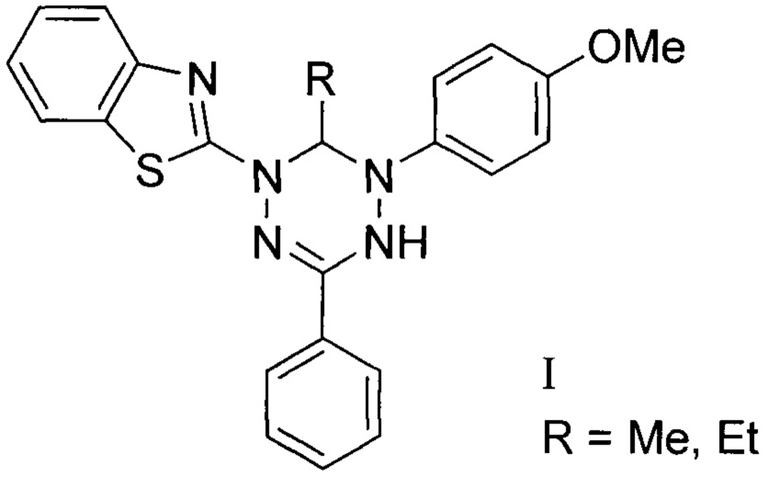
2-[5-(4-Метокси)-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолы, имеющие структурную формулу I, обладающие противовирусной активностью в отношении вируса Коксаки В3:
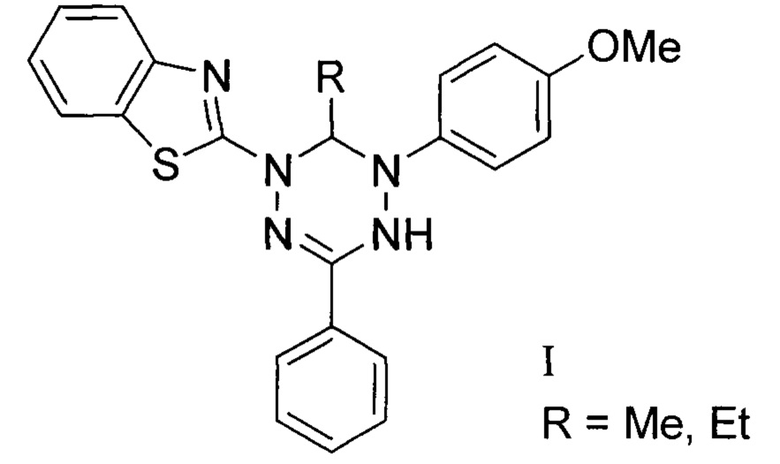 .
.
| Приспособление для смазывания рельсов на криволинейных участках пути | 1929 |
|
SU15094A1 |
| Федорченко Т.Г | |||
| и др., Синтез, спектральные, электрохимические и антиоксидантные свойства 2-[5-(арил)-6-R-3-фенил-5,6-дигидро-4Н-[1,2,4,5]тетразин-1-ил]-бензотиазолов | |||
| Журнал органической химии, 2020, том 56, 1, с.52-64 | |||
| Липунова Г.Н | |||
| и др., Новые аспекты химии формазанов | |||
| Российский химический журнал, 2016, том LX, 3, | |||
Авторы
Даты
2022-11-15—Публикация
2022-01-24—Подача