ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По настоящей заявке испрашивается приоритет временной заявки на патент США No. 62/488509, поданной 21 апреля 2018 г., полное содержание которой приведено в настоящем описании в качестве ссылки для всех целей.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к непрерывным полипептидам, содержащим фрагменты рецептора интерлейкина 4 и рецептора интерлейкина 13, происходящие из видов домашних животных, которые связываются с IL4 и/или IL13 из видов домашних животных, например, IL4 собачьих и IL13 собачьих. Это изобретение также относится к способам использования непрерывных полипептидов, например, для лечения индуцированных IL4 и/или IL13 состояний или уменьшения активности передачи сигналов IL4 и/или IL13 в клетках, например, у домашних животных, таких как собачьи, кошачьи и лошадиные.
УРОВЕНЬ ТЕХНИКИ
[0003] Интерлейкин 4 (IL4) представляет собой цитокин, стимулирующий дифференцировку наивных T-клеток-помощников до Th2-клеток. Интерлейкин 13 (IL13) оказывает сходные эффекты на иммуноциты. Как IL4, так и IL13 играют важные роли в опосредованных T-клетками иммунных ответах, напрямую ассоциированных с аллергией, например, атопическим дерматитом, и астмой. Общеизвестно, что IL4 может формировать передающий сигналы комплекс с гетеродимерными рецепторами либо из субъединицы альфа рецептора IL4 (IL4R) и γc, либо из IL4R и субъединицы альфа-1 рецептора IL13 (IL13R). IL13 может формировать передающий сигналы комплекс с гетеродимерными рецепторами IL4Ra и IL13Ra1. Внеклеточные домены IL4Ra или IL13Ra1 могут связываться с IL4 и/или IL13 и уменьшать концентрации свободных цитокинов, таким образом, уменьшая клинические признаки и симптомы, ассоциированные с дерматитом, астмой и другими нарушениями.
[0004] Виды домашних животных, таких как кошки, собаки и лошади, страдают от множества аллергических заболеваний, сходных с аллергическими заболеваниями человека, включая атопический дерматит и астму. Таким образом, остается необходимость в способах и соединениях, которые можно использовать специфическим образом для связывания IL4 и/или IL13 домашнего животного, для лечения индуцированных IL4/IL13 состояний и для уменьшения активности передачи сигналов IL4/IL13.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0005] В некоторых вариантах осуществления настоящее изобретение относится к непрерывному полипептиду IL13R/IL4R, содержащему внеклеточный домен полипептида IL13R и внеклеточный домен полипептида IL4R, где полипептиды IL13R и IL4R происходят из вида домашнего животного.
[0006] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R имеет формулу (I) IL13R-L1-IL4R-L2-FP или формулу (II) IL4R-L1-IL13R-L2-FP, где:
a. IL13R представляет собой внеклеточный домен полипептида IL13R, происходящий из вида домашнего животного,
b. IL4R представляет собой внеклеточный домен полипептида IL4R, происходящий из вида домашнего животного,
c. L1 представляет собой первый необязательный линкер,
d. L2 представляет собой второй необязательный линкер, и
e. FP представляет собой партнера по слиянию.
[0007] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R связывается с IL13 из вида домашнего животного с константой диссоциации (Kd) менее, чем 5×10-6 M, менее, чем 1×10-6 M, менее, чем 5×10-7 M, менее, чем 1×10-7 M, менее, чем 5×10-8 M, менее, чем 1×10-8 M, менее, чем 5×10-9 M, менее, чем 1×10-9 M, менее, чем 5×10-10 M, менее, чем 1×10-10 M, менее, чем 5×10 11 M, менее, чем 1×10 11 M, менее, чем 5×10-12 M, или менее, чем 1×10-12 M, при измерении посредством интерферометрии биослоя.
[0008] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R связывается с IL4 из вида домашнего животного с константой диссоциации (Kd) менее, чем 5×10-6 M, менее, чем 1×10-6 M, менее, чем 5×10-7 M, менее, чем 1×10-7 M, менее, чем 5×10-8 M, менее, чем 1×10-8 M, менее, чем 5×10-9 M, менее, чем 1×10-9 M, менее, чем 5×10-10 M, менее, чем 1×10-10 M, менее, чем 5×10 11 M, менее, чем 1×10 11 M, менее, чем 5×10-12 M, или менее, чем 1×10-12 M, при измерении посредством интерферометрии биослоя.
[0009] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R уменьшает передачу сигналов IL13 и/или IL4 у вида домашнего животного.
[0010] В некоторых вариантах осуществления вид домашнего животного представляет собой собачьих, кошачьих или лошадиных.
[0011] В некоторых вариантах осуществления внеклеточный домен полипептида IL13R является по меньшей мере на 85% идентичным аминокислотной последовательности из SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R является по меньшей мере на 90% идентичным аминокислотной последовательности из SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R является по меньшей мере на 95% идентичным аминокислотной последовательности из SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R является по меньшей мере на 98% идентичным аминокислотной последовательности из SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36.
[0012] В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит цистеин в положении, соответствующем положению 18 из SEQ ID NO: 22, соответствующем положению 18 из SEQ ID NO: 24 или соответствующем положению 18 из SEQ ID NO: 26. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит цистеин в положении 18 из SEQ ID NO: 22, в положении 18 из SEQ ID NO: 24, в положении 18 из SEQ ID NO: 26, в положении 15 из SEQ ID NO: 32, в положении 15 из SEQ ID NO: 34 или в положении 15 из SEQ ID NO: 36. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит аминокислотную последовательность, выбранную из SEQ ID NO: 32, SEQ ID NO: 34 и SEQ ID NO: 36. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит аминокислотную последовательность, выбранную из SEQ ID NO: 22, SEQ ID NO: 24 и SEQ ID NO: 26.
[0013] В некоторых вариантах осуществления внеклеточный домен полипептида IL4R является по меньшей мере на 85% идентичным аминокислотной последовательности из SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35 или SEQ ID NO: 37. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R является по меньшей мере на 90% идентичным аминокислотной последовательности из SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35 или SEQ ID NO: 37. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R является по меньшей мере на 95% идентичным аминокислотной последовательности из SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35, или SEQ ID NO: 37. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R является по меньшей мере на 98% идентичным аминокислотной последовательности из SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35, или SEQ ID NO: 37. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R содержит аминокислотную последовательность, выбранную из SEQ ID NO: 33, SEQ ID NO: 35 и SEQ ID NO: 37. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R содержит аминокислотную последовательность, выбранную из SEQ ID NO: 23, SEQ ID NO: 25, и SEQ ID NO: 27.
[0014] В некоторых вариантах осуществления каждый из L1 и L2, если он присутствует, независимо содержит аминокислотную последовательность, выбранную из G, GG, GGG, S, SS, SSS, GS, GSGS (SEQ ID NO: 38), GSGSGS (SEQ ID NO: 39), GGS, GGSGGS (SEQ ID NO: 40), GGSGGSGGS (SEQ ID NO: 41), GGGS (SEQ ID NO: 42), GGGSGGGS (SEQ ID NO: 43), GGGSGGGSGGGS (SEQ ID NO: 44), GSS, GSSGSS (SEQ ID NO: 45), GSSGSSGSS (SEQ ID NO: 46), GGSS (SEQ ID NO: 47), GGSSGGSS (SEQ ID NO: 48) и GGSSGGSSGGSS (SEQ ID NO: 49).
[0015] В некоторых вариантах осуществления партнер по слиянию выбран из Fc, альбумина и связывающего альбумин фрагмента. В некоторых вариантах осуществления Fc представляет собой (a) константную область тяжелой цепи собачьих, выбранную из константной области IgG-A, IgG-B, IgG-C и IgG-D; (b) константную область тяжелой цепи кошачьих, выбранную из константной области IgG1, IgG2a и IgG2b; или (c) константную область тяжелой цепи лошадиных, выбранную из константной области IgG1, IgG2, IgG3, IgG4, IgG5, IgG6 и IgG7.
[0016] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит последовательность, выбранную из SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30 и SEQ ID NO: 31.
[0017] В некоторых вариантах осуществления настоящее изобретение относится к нуклеиновой кислоте, кодирующей непрерывный полипептид IL13R/IL4R, описанный в настоящем описании выше. В некоторых вариантах осуществления настоящее изобретение относится к клетке-хозяину, содержащей нуклеиновую кислоту, кодирующую непрерывный полипептид IL13R/IL4R, описанный в настоящем описании выше. В некоторых вариантах осуществления настоящее изобретение относится к способу получения непрерывного полипептида IL13R/IL4R, включающему культивирование такой клетки-хозяина, содержащей нуклеиновую кислоту, кодирующую непрерывный полипептид IL13R/IL4R, описанный в настоящем описании выше, и выделение непрерывного полипептида. В некоторых вариантах осуществления настоящее изобретение относится к фармацевтической композиции, содержащей непрерывный полипептид IL13R/IL4R, описанный в настоящем описании, и фармацевтически приемлемый носитель.
[0018] В некоторых вариантах осуществления настоящее изобретение относится к способам лечения вида домашнего животного, имеющего индуцированное IL13 и/или IL4 состояние, включающим введение виду домашнего животного терапевтически эффективного количества непрерывного полипептида IL13R/IL4R, описанного в настоящем описании, или фармацевтической композиции, содержащей непрерывный полипептид IL13R/IL4R, описанный в настоящем описании. В некоторых вариантах осуществления вид домашнего животного представляет собой собачьих, кошачьих или лошадиных. В некоторых вариантах осуществления индуцированное IL13 и/или IL4 состояние представляет собой сопровождающееся зудом или аллергическое состояние, такое как атопический дерматит, зуд, астма, псориаз, склеродермия или экзема.
[0019] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтическую композицию вводят парентерально. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтическую композицию вводят внутримышечным способом, внутрибрюшинным способом, внутриспинномозговым способом, подкожным способом, внутриартериальным способом, внутрисуставным способом, интратекальным способом или ингаляционным способом.
[0020] В некоторых вариантах осуществления способ дополнительно включает введение ингибитора Jak, ингибитора PI3K, ингибитора AKT или ингибитора MAPK. В некоторых вариантах осуществления способ дополнительно включает введение одного или нескольких антител, выбранных из антитела против IL17, антитела против IL31, антитела против TNFα, антитела против CD20, антитела против CD19, антитела против CD25, антитела против IL4, антитела против IL13, антитела против IL23, антитела против IgE, антитела против CD11α, антитела против IL6R, антитела против α4-интегрина, антитела против IL12, антитела против IL1β и антитела против BlyS.
[0021] В некоторых вариантах осуществления настоящее изобретение относится к способам уменьшения активности передачи сигналов IL13 и/или IL4 в клетке, включающим подвергание клетки воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции, описанных в настоящем описании, в условиях, позволяющих связывание непрерывного полипептида с IL13 и/или IL4, таким образом, (a) уменьшение связывания IL/4 и/или IL-13 с нативным рецептором IL13 и/или нативным рецептором IL-4, и уменьшение опосредованной IL13 и/или IL4 передачи сигналов. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции ex vivo. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида или фармацевтической композиции in vivo. В некоторых вариантах осуществления клетка представляет собой клетку собачьих, клетку кошачьих или клетку лошадиных.
[0022] В некоторых вариантах осуществления настоящее изобретение относится к способам детекции IL13 или IL4 в образце из вида домашнего животного, включающим приведение образца в контакт с непрерывным полипептидом IL13R/IL4R или фармацевтической композицией, описанной в настоящем описании, в условиях, позволяющих связывание непрерывного полипептида с IL13 и/или IL4, и детекцию того, формируется ли комплекс между непрерывным полипептидом и IL13 и/или IL4 в образце. В некоторых вариантах осуществления образец представляет собой биологический образец, полученный из собачьих, кошачьих или лошадиных.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0023] ФИГ. 1 представляет собой график последовательного связывания IL4R-IL13R-Fc собачьих с IL4 собачьих и IL13 собачьих или с IL13 собачьих и IL4 собачьих, с использованием концентраций 30 мкг/мл IL4 и IL13 в PBS.
[0024] ФИГ. 2 представляет собой график последовательного связывания IL13R-IL4R-Fc собачьих с IL4 собачьих и IL13 собачьих или с IL13 собачьих и IL4 собачьих с использованием концентраций 30 мкг/мл IL4 и IL13 в PBS.
[0025] ФИГ. 3 представляет собой график нейтрализации активности IL4 собачьих посредством IL4R-IL13R-Fc собачьих в анализе пролиферации клеток TF1. IL4 собачьих (50 нг/мл или 3,85 нМ) использовали в анализе.
ОПИСАНИЕ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0026] В таблице 1 представлен список конкретных последовательностей, на которые ссылаются в настоящем описании.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0027] Настоящее изобретение относится к непрерывным полипептидам, связывающим IL13 и/или IL4 собачьих, IL13 и/или IL4 кошачьих, и/или IL13 и/или IL4 лошадиных. В некоторых вариантах осуществления непрерывные полипептиды содержат внеклеточный домен полипептида IL13R и внеклеточный домен полипептида IL4R. Настоящее изобретение относится также к способам получения или очистки непрерывных полипептидов. Настоящее изобретение относится к способам лечения с использованием непрерывных полипептидов для связывания IL13 и/или IL4 и ингибирования опосредованной IL13 и/или IL4 передачи сигналов. Такие способы включают, но без ограничения, способы лечения индуцированных IL13 и/или IL4 состояний у вида домашнего животного. Настоящее изобретение относится также к способам детекции IL13 и/или IL4 в образце из вида домашнего животного.
[0028] Для удобства читателя, представлены следующие определения терминов в рамках изобретения.
[0029] В рамках изобретения числовые термины, такие как Kd, рассчитывают на основании научных измерений и, таким образом, они подвержены соответствующей ошибке измерения. В некоторых случаях, числовой термин может включать числовые значения, округленные до ближайшей значащей цифры.
[0030] В рамках изобретения формы единственного числа означают «по меньшей мере один» или «один или несколько», если не указано иное. В рамках изобретения термин «или» означает «и/или», если не указано иное. В контексте множества зависимых пунктов формулы изобретения, использование «или» при ссылке, возвращающей к другим пункты формулы изобретения, относится к этим пунктам формулы изобретения только в качестве альтернативы.
Непрерывные полипептиды IL13R/IL4R
[0031] Настоящее изобретение относится к новым непрерывным полипептидам IL13R/IL4R, например, непрерывным полипептидам, связывающим IL13 и/или IL4 собачьих, IL13 и/или IL4 кошачьих, и/или IL13 и/или IL4 лошадиных.
[0032] «Аминокислотная последовательность» обозначает последовательность остатков аминокислот в пептиде или белке. Термины «полипептид» и «белок» используют взаимозаменяемо для обозначения полимера из остатков аминокислот, и они не ограничены минимумом длины. Такие полимеры из остатков аминокислот могут содержать природные или неприродные остатки аминокислот, и включают, но без ограничения, пептиды, олигопептиды, димеры, тримеры и мультимеры из остатков аминокислот. Как полноразмерные белки, так и их фрагменты, включены в это определение. Термины включают также постэкспрессионные модификации полипептида, например, гликозилирование, сиалирование, ацетилирование, фосфорилирование и т.п. Кроме того, для целей по настоящему описанию, «полипептид» относится к белку, включающему модификации, такие как делеции, добавления и замены (как правило, консервативного характера), в природной последовательности, при условии, что белок сохраняет желательную активность. Эти модификации могут являться преднамеренными, например, в результате сайт-направленного мутагенеза, или могут являться случайными, например, в результате мутаций у хозяев, продуцирующих белки, или ошибок, обусловленных амплификацией ПЦР.
[0033] Термин «непрерывный полипептид» в настоящем описании используют для обозначения не прерывающейся последовательности аминокислот. Непрерывный полипептид, как правило, транслирован с одной непрерывной последовательности ДНК. Ее можно получать посредством генной инженерии, например, посредством удаления стоп-кодона из последовательности ДНК для первого белка, затем добавления последовательности ДНК второго белка в рамке считывания, таким образом, что последовательность ДНК экспрессируется в форме одиночного белка. Как правило, это осуществляют посредством клонирования кДНК в экспрессирующий вектор в рамке считывания с существующим геном
[0034] «IL4R», в рамках изобретения, представляет собой полипептид, содержащий всю или фрагмент субъединицы альфа рецептора IL4, который связывается с IL-4.
[0035] Например, «IL4R» относится к полипептиду IL4R из любого источника из числа позвоночных, включая млекопитающих, таких как приматы (например, люди и яванские макаки), грызуны (например, мыши и крысы) и домашние животные (например, собаки, кошки и лошади), если не указано иное. В некоторых вариантах осуществления IL4R представляет собой фрагмент внеклеточного домена, который связывается с IL4. В некоторых таких вариантах осуществления, IL4R можно обозначать как внеклеточный домен IL4R (ECD). В некоторых вариантах осуществления IL4R содержит аминокислотную последовательность из SEQ ID NO: 7, SEQ ID NO:8, SEQ ID NO: 9, SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35 или SEQ ID NO: 37.
[0036] «IL13R», в рамках изобретения, представляет собой полипептид, содержащий всю или фрагмент субъединицы альфа-1 рецептора IL13, который связывается с IL-13.
[0037] Например, «IL13R» относится к полипептиду IL13R из любого источника из числа позвоночных, включая млекопитающих, таких как приматы (например, люди и яванские макаки), грызуны (например, мыши и крысы) и домашние животные (например, собаки, кошки и лошади), если не указано иное. В некоторых вариантах осуществления IL13R представляет собой фрагмент внеклеточного домена, который связывается с IL13. В некоторых таких вариантах осуществления, IL13R можно обозначать как внеклеточный домен IL13R (ECD). В некоторых вариантах осуществления полипептид IL13R содержит аминокислотную последовательность из SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36.
[0038] Термин «вид домашнего животного» относится к животному, пригодному в качестве компаньона для человека. В некоторых вариантах осуществления вид домашнего животного представляет собой небольшое животное, такое как животное из числа собачьих, кошачьих, собака, кошка, лошадь, кролик, хорек, морская свинка, грызун и т.д. В некоторых вариантах осуществления вид домашнего животного представляет собой сельскохозяйственное животное, такое как лошадь, корова, свинья и т.д.
[0039] «Внеклеточный домен» («ECD») представляет собой фрагмент полипептида, продолжающийся за пределы трансмембранного домена во внеклеточное пространство. Термин «внеклеточный домен», в рамках изобретения, может содержать полный внеклеточный домен или может содержать укороченный внеклеточный домен, лишенный одной или нескольких аминокислот, который связывается со своим лигандом. Состав внеклеточного домена может зависеть от алгоритма, используемого для определения того, какие аминокислоты находятся в мембране. Различные алгоритмы могут прогнозировать, и различные системы могут экспрессировать различные внеклеточные домены для данного белка.
[0040] Внеклеточный домен полипептида IL4R может содержать полный внеклеточный домен или укороченный внеклеточный домен IL4R, который связывается с IL4. В рамках изобретения, термины «внеклеточный домен полипептида IL4R», «ECD IL4R» и сходные термины относятся к полипептиду IL4R, который не содержит трансмембранного домена или цитоплазматического домена, даже если за термином следует открытое переходное слово, такое как «содержащий», «содержит» и т.п. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R представляет собой внеклеточный домен полипептида IL4R, происходящего из вида домашнего животного. Например, в некоторых вариантах осуществления внеклеточный домен полипептида IL4R происходит из IL4R собачьих, IL4R кошачьих или IL4R лошадиных. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R содержит аминокислотную последовательность из SEQ ID NO: 23, SEQ ID NO: 25 или SEQ ID NO: 27, или любой ее фрагмент. В некоторых вариантах осуществления внеклеточный домен полипептида IL4R содержит аминокислотную последовательность из SEQ ID NO: 33, SEQ ID NO: 35 или SEQ ID NO: 37, или любой ее фрагмент.
[0041] Внеклеточный домен полипептида IL13R может содержать полный внеклеточный домен или укороченный внеклеточный домен IL13R, который связывается с IL13. В рамках изобретения, термины «внеклеточный домен полипептида IL13R», «ECD IL13R», и сходные термины относятся к полипептиду IL13R, который не содержит трансмембранного домена или цитоплазматического домена, даже если за термином следует открытое переходное слово, такое как «содержащий», «содержит» и т.п.. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R представляет собой внеклеточный домен полипептида IL13R, происходящего из вида домашнего животного. Например, в некоторых вариантах осуществления внеклеточный домен полипептида IL13R происходит из IL13R собачьих, IL13R кошачьих или IL13R лошадиных. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит аминокислотную последовательность из SEQ ID NO: 22, SEQ ID NO: 24 или SEQ ID NO: 26, или любой ее фрагмент. В некоторых вариантах осуществления внеклеточный домен полипептида IL13R содержит аминокислотную последовательность из SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36, или любой ее фрагмент.
[0042] Термины «непрерывный полипептид IL13R/IL4R» и «непрерывный полипептид IL4R/IL13R» используют взаимозаменяемо для обозначения непрерывного полипептида, содержащего полипептид IL13R и полипептид IL4R, где термины не являются показательными для порядка, в котором полипептиды IL13R и IL4R встречаются в непрерывном полипептиде, если порядок не указан иным образом. Например, непрерывный полипептид IL13R/IL4R или непрерывный полипептид IL4R/IL13R могут относиться к полипептиду IL4R, которому предшествует в последовательности или за которым следует в последовательности полипептид IL13R. Кроме того, непрерывный полипептид IL13R/IL4R или непрерывный полипептид IL4R/IL13R могут относиться к полипептиду IL13R, которому предшествует в последовательности или за которым следует в последовательности полипептид IL4R.
[0043] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит полипептид IL13R, связанный с полипептидом IL4R на C-конце полипептида IL13R или на N-конце полипептида IL13R. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит полипептид IL4R, связанный с полипептидом IL13R на C-конце полипептида IL4R или на N-конце полипептида IL4R.
[0044] Непрерывный полипептид IL13R/IL4R по изобретению может содержать внеклеточный домен полипептида IL13R и/или внеклеточный домен полипептида IL4R, где полипептиды происходят из вида домашнего животного. Например, непрерывный полипептид может содержать внеклеточный домен полипептида IL4R из собаки, кошки или лошади, и/или может содержать внеклеточный домен полипептида IL13R из собаки, кошки или лошади.
[0045] «Дикий тип» относится к не подвергнутому мутагенезу варианту полипептида, который встречается в природе, или к его фрагменту. Полипептид дикого типа можно получать рекомбинантным способом. «ECD IL13R дикого типа» или «ECD IL4R дикого типа» относится к белку, имеющему аминокислотную последовательность, идентичную такому же фрагменту внеклеточного домена IL13R или IL4R, встречающемуся в природе.
[0046] «Вариант» представляет собой молекулу нуклеиновой кислоты или полипептида, которая отличается от эталонной молекулы нуклеиновой кислоты или полипептида в результате замен, делеций и/или добавлений одной или множества аминокислот и в основном сохраняет по меньшей мере одну биологическую активность эталонной молекулы нуклеиновой кислоты или полипептида.
[0047] «Биологически активная» молекула, или молекула, имеющая «биологическую активность», представляет собой молекулу, имеющую любую функцию, связанную или ассоциированную с метаболическим или физиологическим процессом, и/или имеющую структурные, регуляторные или биохимические функции природной молекулы. Биологически активные фрагменты полинуклеотида представляют собой фрагменты, имеющие активность, сходную, но не обязательно идентичную, с активностью полинуклеотида по настоящему изобретению. Биологически активный полипептид или его фрагмент включает полипептид, который может участвовать в биологической реакции, включая, но без ограничения, взаимодействие лиганд-рецептор или связывание антиген-антитело. Биологическая активность может включать улучшенную желательную активность, или уменьшенную нежелательную активность. Молекула может демонстрировать биологическую активность, когда она участвует в молекулярном взаимодействии с другой молекулой, таком как гибридизация, когда она имеет терапевтическую ценность для облегчения состояния заболевания, когда она имеет профилактическую ценность для индукции иммунного ответа, когда она имеет диагностическую и/или прогностическую ценность для определения присутствия молекулы, например, биологически активный фрагмент полинуклеотида, который можно детектировать как уникальный для молекулы полинуклеотида, и когда ее можно использовать в качестве праймера в полимеразной цепной реакции (ПЦР).
[0048] В рамках изобретения, «процент (%) идентичности аминокислотной последовательности» и «гомологию», применительно к последовательности молекулы нуклеиновой кислоты или полипептида, определяют как процент нуклеотидов или остатков аминокислот в эталонной последовательности, которые являются идентичными нуклеотидам или остаткам аминокислот в специфической последовательности молекулы нуклеиновой кислоты или полипептида, после выравнивания последовательностей и внесения пропусков, при необходимости, для достижения максимальной процентной идентичности последовательностей, и не рассматривая никакие консервативные замены в качестве части идентичности последовательностей. Выравнивание для целей определения процентной идентичности последовательностей можно осуществлять различными способами, находящимися в компетенции специалиста в данной области, например, с использованием публично доступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN или MEGALINE™ (DNASTAR). Специалисты в данной области могут определять подходящие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания на протяжении полной длины сравниваемых последовательностей.
[0049] В некоторых вариантах осуществления вариант имеет по меньшей мере приблизительно 50% идентичность последовательности с эталонной молекулой нуклеиновой кислоты или полипептида после выравнивания последовательностей и внесения пропусков, при необходимости, для достижения максимальной процентной идентичности последовательностей, и не рассматривая никакие консервативные замены в качестве части идентичности последовательностей. Такие варианты включают, например, полипептиды, где один или несколько остатков аминокислот добавлены, делетированы на N- или C-конце полипептида. В некоторых вариантах осуществления вариант имеет по меньшей мере приблизительно 50% идентичность последовательности, по меньшей мере приблизительно 60% идентичность последовательности, по меньшей мере приблизительно 65% идентичность последовательности, по меньшей мере приблизительно 70% идентичность последовательности, по меньшей мере приблизительно 75% идентичность последовательности, по меньшей мере приблизительно 80% идентичность последовательности, по меньшей мере приблизительно 85% идентичность последовательности, по меньшей мере приблизительно 90% идентичность последовательности, по меньшей мере приблизительно 95% идентичность последовательности, по меньшей мере приблизительно 98% идентичность последовательности с последовательностью эталонной нуклеиновой кислоты или полипептида.
[0050] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит внеклеточный домен полипептида IL13R, имеющий по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% идентичность последовательности с аминокислотной последовательностью из SEQ ID NO: 22, SEQ ID NO: 24, SEQ ID NO: 26, SEQ ID NO: 32, SEQ ID NO: 34 или SEQ ID NO: 36. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит внеклеточный домен полипептида IL4R, имеющий по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98% идентичность последовательности с аминокислотной последовательностью из SEQ ID NO: 23, SEQ ID NO: 25, SEQ ID NO: 27, SEQ ID NO: 33, SEQ ID NO: 35, или SEQ ID NO: 37.
[0051] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит внеклеточный домен полипептида IL13R, содержащий цистеин в положении, соответствующем положению 18 из SEQ ID NO: 22, в положении, соответствующем положению 18 из SEQ ID NO: 24, или в положении, соответствующем положению 18 из SEQ ID NO: 26. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит внеклеточный домен полипептида IL13R, содержащий цистеин в положении 18 из SEQ ID NO: 22, в положении 18 из SEQ ID NO: 24, в положении 18 из SEQ ID NO: 26, в положении 15 из SEQ ID NO: 32, в положении 15 из SEQ ID NO: 34, или в положении 15 из SEQ ID NO: 36.
[0052] «Точечная мутация» представляет собой мутацию, затрагивающую одиночный нуклеотид или остаток аминокислоты. Мутация может представлять собой потерю нуклеотида или аминокислоты, замену одного нуклеотида или остатка аминокислоты на другой, или вставку дополнительного нуклеотида или остатка аминокислоты.
[0053] Аминокислотная замена может включать, но без ограничения, замену одной аминокислоты в полипептиде на другую аминокислоту. Иллюстративные замены показаны в таблице 2. Аминокислотные замены можно вводить в представляющую интерес молекулу, и проводить скрининг продуктов по желательной активности, например, сохранению/улучшению связывания антигена, уменьшению иммуногенности, или улучшению ADCC или CDC, или улучшению фармакокинетики.
[0054] Таблица 2
[0055] Аминокислоты можно группировать в соответствии с общими свойствами боковой цепи:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, влияющие на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
[0056] Неконсервативные замены включают замену члена одного из этих классов на другой класс.
[0057] «Партнер по слиянию», в рамках изобретения, относится к дополнительному компоненту непрерывного полипептида IL13R/IL4R, такому как дополнительный полипептид, такой как альбумин, связывающий альбумин фрагмент или фрагмент молекулы иммуноглобулина. Партнер по слиянию может содержать домен для олигомеризации, такой как домен Fc тяжелой цепи иммуноглобулина.
[0058] «Полипептид поддающегося кристаллизации фрагмента (Fc)» представляет собой часть молекулы антитела, которая взаимодействует с эффекторными молекулами и клетками. Он содержит C-концевые части тяжелых цепей иммуноглобулинов. В рамках изобретения, полипептид Fc содержит фрагмент домена Fc с одним или несколькими видами биологической активности целого полипептида Fc. «Эффекторная функция» полипептида Fc представляет собой действие или активность, осуществляемые, полностью или частично, посредством антитела в ответ на стимул, и может включать связывание комплемента или индукцию ADCC (антителозависимой клеточной цитотоксичности).
[0059] Термин «IgX» или «Fc IgX» обозначает область Fc, происходящую из конкретного изотипа антитела (например, IgG, IgA, IgD, IgE, IgM и т.д.), где «X» обозначает изотип антитела. Таким образом, «IgG» или «Fc IgG» обозначает область Fc из цепи γ, «IgA» или «Fc IgA» обозначает область Fc из цепи α, «IgD» или «Fc IgD» обозначает область Fc из цепи δ, «IgE» или «Fc IgE» обозначает область Fc из цепи ε, «IgM» или «Fc IgM» обозначает область Fc из цепи μ и т.д. В некоторых вариантах осуществления область Fc IgG содержит CH1, шарнир, CH2, CH3 и CL1. «IgXN» или «Fc IgXN» означает, что область Fc происходит из конкретного подкласса изотипа антитела (такого как подкласс A, B, C или D IgG собачьих; подкласс 1, 2a или 2b IgG кошачьих; или подкласс IgG1, IgG2, IgG3, IgG4, IgG5, IgG6 или IgG7 IgG лошадиных и т.д.), где «N» обозначает подкласс.
[0060] В некоторых вариантах осуществления области IgX или IgXN происходят из домашнего животного, такого как собака, кошка или лошадь. В некоторых вариантах осуществления области IgG выделены из тяжелых цепей γ собачьих, таких как IgGA, IgGB, IgGC, или IgGD. В некоторых случаях, области Fc IgG выделены из тяжелых цепей γ кошачьих, таких как IgG1, IgG2a или IgG2b. В других случаях, области IgG выделены из тяжелых цепей γ лошадиных, таких как IgG1, IgG2, IgG3, IgG4, IgG5, IgG6 или IgG7. Полипептиды, содержащие область Fc из IgGA, IgGB, IgGC или IgGD, могут обеспечивать более высокие уровни экспрессии в рекомбинационных системах продукции.
[0061] «Сигнальная последовательность» относится к последовательности остатков аминокислот или кодирующих их полинуклеотидов, которая способствует секреции представляющего интерес полипептида и, как правило, отщепляется при экспорте полипептида в пространство снаружи мембраны поверхности клетки.
[0062] «Линкер» относится к одному или нескольким остаткам аминокислот, соединяющим первый полипептид с вторым полипептидом.
[0063] В некоторых вариантах осуществления линкер представляет собой богатый глицином, богатый серином или богатый GS гибкий, не структурный линкер. В некоторых вариантах осуществления линкер содержит две аминокислоты G (Gly) и/или S (Ser). Например, линкер может содержать G или повтор G (например, GG, GGG и т.д.); GS или повтор GS (например, GSGS (SEQ ID NO: 38), GSGSGS (SEQ ID NO: 39) и т.д.); GGS или повтор GGS (например, GGSGGS (SEQ ID NO: 40), GGSGGSGGS (SEQ ID NO: 41) и т.д.); GGGS (SEQ ID NO: 42) или повтор GGGS (SEQ ID NO: 42) (например, GGGSGGGS (SEQ ID NO: 43), GGGSGGGSGGGS (SEQ ID NO: 44) и т.д.); GSS или повтор GSS (например, GSSGSS (SEQ ID NO: 45), GSSGSSGSS (SEQ ID NO: 46) и т.д.); или GGSS (SEQ ID NO: 47) или повтор GGSS (SEQ ID NO: 47) (например, GGSSGGSS (SEQ ID NO: 48), GGSSGGSSGGSS (SEQ ID NO: 49) и т.д.).
[0064] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит по меньшей мере одного партнера по слиянию и/или по меньшей мере один линкер. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит необязательную сигнальную последовательность, необязательного партнера по слиянию и по меньшей мере один необязательный линкер. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R не содержит сигнальную последовательность, партнера по слиянию или линкер. В некоторых вариантах осуществления непрерывный полипептид IL13/IL4 транслируется с сигнальной последовательностью, но сигнальная последовательность отщепляется от непрерывного полипептида IL13R/IL4R.
[0065] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит:
Формула (I): IL13R-L1-IL4R-L2-FP или
Формула (II): IL4R-L1-IL13R-L2-FP,
где IL13R представляет собой полипептид внеклеточного (ECD) домена IL13R, происходящий из вида домашнего животного, IL4R представляет собой полипептид ECD IL4R, происходящий из вида домашнего животного, L1 представляет собой первый необязательный линкер, L2 представляет собой второй необязательный линкер, и FP представляет собой необязательного партнера по слиянию.
[0066] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R содержит аминокислотную последовательность, выбранную из SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19, SEQ ID NO: 20, SEQ ID NO: 21, SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 30, SEQ ID NO: 31.
Экспрессия и продукция непрерывного полипептида IL13R/IL4R
[0067] Настоящее изобретение относится к полинуклеотидным последовательностям, кодирующим весь или часть (например, внеклеточный домен) непрерывного полипептида IL13R/IL4R в присутствии или в отсутствие сигнальной последовательности. Если гомологичную сигнальную последовательность (т.е., сигнальную последовательность нативного IL-4R или IL13R) не используют в конструкции молекулы нуклеиновой кислоты, тогда можно использовать другую сигнальную последовательность, например, любую из сигнальных последовательностей, описанных в PCT US06/02951.
[0068] Как правило, нуклеотидную последовательность, кодирующую представляющий интерес полипептид, такой как непрерывный полипептид IL13R/IL4R, вставляют в экспрессирующий вектор, подходящий для экспрессии в выбранной клетке-хозяине.
[0069] «Вектор» представляет собой плазмиду, которую можно использовать для переноса последовательности ДНК от одного организма к другому или для экспрессии представляющего интерес гена. Вектор, как правило, включает точку начала репликации и регуляторные последовательности, регулирующие экспрессию представляющего интерес гена, и может нести или может не нести ген селективного маркера, такой как ген устойчивости к антибиотику. Вектор является пригодным для клетки-хозяина, в котором его необходимо экспрессировать. Вектор можно называть «рекомбинантным вектором», когда представляющий интерес ген присутствует в векторе.
[0070] «Клетка-хозяин» относится к клетке, которая может являться или является реципиентом вектора или выделенного полинуклеотида. Клетки-хозяева могут представлять собой прокариотические клетки или эукариотические клетки. Иллюстративные эукариотические клетки включают клетки млекопитающих, такие как клетки примата или не относящегося к примату животного; клетки грибов, таких как дрожжи; клетки растений; и клетки насекомых. Неограничивающие примеры клеток млекопитающих включают, но без ограничения, клетки NS0, клетки PER.C6® (Crucell), клетки 293 и клетки CHO, и их производные, такие как клетки 293-6E, DG44, CHO-S и CHO-K. Клетки-хозяева включают потомство одной клетки-хозяина, и потомство может не обязательно являться полностью идентичным (по морфологии или по комплементарности геномной ДНК) исходной родительской клетке из-за природной, случайной или преднамеренной мутации. Клетка-хозяин включает клетки, трансфицированные in vivo с использованием полинуклеотида(полинуклеотидов), кодирующих аминокислотную последовательность(последовательности), представленные в настоящем описании.
[0071] Термин «выделенная», в рамках изобретения, относится к молекуле, отделенной по меньшей мере от части компонентов, с которыми ее, как правило, обнаруживают в природе или продуцируют. Например, полипептид обозначают как «выделенный», когда он отделен по меньшей мере от некоторых из компонентов клетки, в которой он продуцирован. Когда полипептид секретирован клеткой после экспрессии, физическое отделение супернатанта, содержащего полипептид, от продуцировавшей его клетки, рассматривают как «выделение» полипептида. Подобным образом, полинуклеотид обозначают как «выделенный», когда он не является частью большего полинуклеотида (например, такого как геномная ДНК или митохондриальная ДНК, в случае полинуклеотида ДНК), в котором его, как правило, обнаруживают в природе, или отделен по меньшей мере от некоторых из компонентов клетки, в которой он продуцирован, например, в случае полинуклеотида РНК. Таким образом, полинуклеотид ДНК, содержащийся в векторе внутри клетки-хозяина, можно обозначать как «выделенная».
[0072] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R выделяют с использованием хроматографии, такой как эксклюзионная хроматография, ионообменная хроматография, хроматография на колонке с белком A, хроматография с гидрофобным взаимодействием и хроматография CHT.
[0073] Термины «метка» и «поддающаяся детекции метка» обозначают группу, присоединенную к непрерывному полипептиду IL13R/IL4R, чтобы сделать его поддающимся детекции. В некоторых вариантах осуществления метка представляет собой поддающийся детекции маркер, который может подавать сигнал, поддающийся детекции визуальными или инструментальными способами, например, включение меченной радиоактивной меткой аминокислоты или присоединение к полипептиду биотинильных групп, которые можно детектировать посредством меченного авидина (например, стрептавидина, имеющего флуоресцентный маркер или ферментативную активность, которые можно детектировать оптическими или колориметрическими способы). Примеры меток для полипептидов включают, но без ограничения, следующие: радиоактивные изотопы или радионуклиды (например, 3H, 14C, 35S, 90Y, 99Tc, 111In, 125I, 131I, 177Lu, 166Ho или 153Sm); хромогены, флуоресцентные метки (например, FITC, родамин, лантаниды фосфора), ферментные метки (например, пероксидаза хрена, люцифераза, щелочная фосфатаза); хемилюминесцентные маркеры; биотинильные группы; предопределенные полипептидные эпитопы, узнаваемые вторичным репортером (например, парные последовательности лейциновой молнии, участки связывания для вторичных антител, связывающие металл домены, эпитопные метки); и магнитные агенты, такие как хелаты гадолиния. Репрезентативные примеры меток, общепринятых для иммуноанализов, включают группы, образующие свет, например, соединения акридиния, и группы, образующие флуоресценцию, например, флуоресцеин. Для этой цели, собственно группа может не являться меченной поддающейся детекции меткой, но может становиться поддающейся детекции после реакции с другой группой.
Непрерывные полипептиды IL13R/IL4R в качестве захватов рецепторов-ловушек
[0074] Непрерывные полипептиды IL13R/IL4R по изобретению могут функционировать в качестве рецепторов-ловушек для захвата IL13 или IL4 и ингибирования их взаимодействия с IL13R и IL4R на клеточной поверхности. Рецепторы-ловушки, такие как рецепторы-ловушки по изобретению, узнают свои лиганды с высокой аффинностью и специфичностью, но являются структурно неспособными к передаче сигналов. Они конкурируют с рецепторами дикого типа за связывание лиганда и участие во взаимодействиях лиганд/рецептор, таким образом, модулируя активность или количество функционирующих рецепторов и/или клеточную активность, нижестоящую по отношению к рецепторам. Рецепторы-ловушки могут действовать как молекулярные ловушки для агонистических лигандов и таким образом, ингибировать индуцированную лигандом активацию рецептора.
[0075] «IL13», в рамках изобретения, относится к любому природному IL13, возникающему в результате экспрессии и процессинга IL13 в клетке. Термин включает IL13 из любого источника из числа позвоночных, включая млекопитающих, таких как приматы (например, люди и яванские макаки), грызуны (например, мыши и крысы) и домашние животные (например, собаки, кошки и лошади), если не указано иное. Термин включает также встречающиеся в природе варианты IL13, например, варианты сплайсинга или аллельные варианты.
[0076] В некоторых вариантах осуществления IL13 собачьих содержит аминокислотную последовательность из SEQ ID NO: 4. В некоторых вариантах осуществления IL13 кошачьих содержит аминокислотную последовательность из SEQ ID NO: 5. В некоторых вариантах осуществления IL13 лошадиных содержит аминокислотную последовательность из SEQ ID NO: 6.
[0077] «IL4», в рамках изобретения, относится к любому природному IL4, возникающему в результате экспрессии и процессинга IL4 в клетке. Термин включает IL4 из любого источника из числа позвоночных, включая млекопитающих, таких как приматы (например, люди и яванские макаки), грызуны (например, мыши и крысы) и домашние животные (например, собаки, кошки и лошади), если не указано иное. Термин включает также встречающиеся в природе варианты IL4, например, варианты сплайсинга или аллельные варианты.
[0078] В некоторых вариантах осуществления IL4 собачьих содержит аминокислотную последовательность из SEQ ID NO: 1. В некоторых вариантах осуществления IL4 кошачьих содержит аминокислотную последовательность из SEQ ID NO: 2. В некоторых вариантах осуществления IL4 лошадиных содержит аминокислотную последовательность из SEQ ID NO: 3.
[0079] Настоящее изобретение относится к непрерывным полипептидам IL13R/IL4R в качестве лекарственных средств. Непрерывные полипептиды IL13R/IL4R по изобретению связываются с IL13 и/или IL4, более подробно описанными в настоящем описании, для которых показана ассоциация с аллергическими заболеваниями. В различных вариантах осуществления, непрерывные полипептиды IL13R/IL4R могут связывать IL13 и IL4 с очень высокой аффинностью. В различных вариантах осуществления, непрерывные полипептиды IL13R/IL4R могут создавать помехи для передачи сигналов IL13 и IL4.
[0080] Термин «аффинность» обозначает силу общей суммы нековалентных взаимодействий между одним участком связывания молекулы (например, рецептора) и ее партнером по связыванию (например, лигандом). Аффинность молекулы X для ее партнера Y можно, в общем, представлять посредством константы диссоциации (KD). Аффинность можно измерять посредством общепринятых способов, известных в данной области, например, таких как иммуноблоттинг, ELISA KD, KinEx A, интерферометрия биослоя (BLI), или посредством устройств для поверхностного плазмонного резонанса.
[0081] Термины «KD», «Kd», «Kd» или «значение Kd» используют взаимозаменяемо для обозначения равновесной константы диссоциации для взаимодействия слитый рецептор - лиганд. В некоторых вариантах осуществления Kd слитой молекулы для ее лиганда измеряют с использованием анализов интерферометрии биослоя с использованием биосенсора, например, системы Octet® (Pall ForteBio LLC, Fremont, CA), в соответствии с инструкциями поставщика. Кратко, биотинилированный антиген связывают с сенсорным наконечником и связывание слитой молекулы мониторируют в течение девяноста секунд, и диссоциацию мониторируют в течение 600 секунд. Буфер для стадий разведения и связывания представляет собой 20 мМ фосфат, 150 мМ NaCl, pH 7,2. Нулевую кривую только с буфером вычитают для коррекции какого-либо смещения. Данные приводят в соответствие с моделью связывания 2:1 с использованием программного обеспечения для анализа данных ForteBio для определения константы скорости связывания (kon), константы скорости диссоциации (koff) и Kd. Равновесную константу диссоциации (Kd) рассчитывают как соотношение koff/kon. Термин «kon» относится к константе скорости для связывания молекулы X с ее партнером Y, и термин «koff» относится к константе скорости для диссоциации молекулы X или партнера Y из комплекса молекула X/партнер Y.
[0082] Термин «связывается» с веществом представляет собой термин, хорошо известный в данной области, и способы определения такого связывания также хорошо известны в данной области. Говорят, что молекула проявляет «связывание», если она вступает в реакцию с, вступает в ассоциацию с или имеет аффинность для конкретной клетки или вещества, и реакция, ассоциация или аффинность поддается детекции посредством одного или нескольких способов, известных в данной области, например, таких как иммуноблоттинг, ELISA KD, KinEx A, интерферометрия биослоя (BLI), посредством устройств для поверхностного плазмонного резонанса или т.д.
[0083] «Поверхностный плазмонный резонанс» обозначает оптический феномен, позволяющий анализ биоспецифических взаимодействий в реальном времени посредством детекции изменений в концентрациях белка в пределах матрицы биосенсора, например, с использованием системы BIAcore™ (BIAcore International AB, GE Healthcare company, Uppsala, Sweden и Piscataway, N.J.). Дополнительные описания, см. в Jonsson et al. (1993) Ann. Biol. Clin. 51: 19-26.
[0084] «Интерферометрия биослоя» относится к оптическому аналитическому способу, которым анализируют паттерн интерференции света, отражающегося от слоя иммобилизованного белка на наконечнике биосенсора и внутреннего эталонного слоя. Изменения количества молекул, связанных с наконечником биосенсора, вызывает сдвиги в паттерне интерференции, которые можно измерять в реальном времени. Неограничивающим примером устройства для интерферометрии биослоя является система Octet® (Pall ForteBio LLC). См., например, Abdiche et al., 2008, Anal. Biochem. 377: 209-277.
[0085] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R связывается с IL13 и/или IL4 собачьих, IL13 и/или IL4 кошачьих, или IL13 и/или IL4 лошадиных с константой диссоциации (Kd) менее, чем 5×10-6 M, менее, чем 1×10-6 M, менее, чем 5×10-7 M, менее, чем 1×10-7 M, менее, чем 5×10-8 M, менее, чем 1×10-8 M, менее, чем 5×10-9 M, менее, чем 1×10-9 M, менее, чем 5×10-10 M, менее, чем 1×10-10 M, менее, чем 5×10 11 M, менее, чем 1×10 11 M, менее, чем 5×10-12 M, или менее, чем 1×10-12 M, при измерении посредством интерферометрии биослоя. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R связывается с IL13 и/или IL4 собачьих, IL13 и/или IL4 кошачьих, или IL13 и/или IL4 лошадиных с Kd между 5×10-6 M и 1×10-6 M, между 5×10-6 M и 5×10-7 M, между 5×10-6 M и 1×10-7 M, между 5×10-6 M и 5×10-8 M, 5×10-6 M и 1×10-8 M, между 5×10-6 M и 5×10-9 M, между 5×10-6 M и 1×10-9 M, между 5×10-6 M и 5×10-10 M, между 5×10-6 M и 1×10-10 M, между 5×10-6 M и 5×10-11 M, между 5×10-6 M и 1×10-11 M, между 5×10-6 M и 5×10-12 M, между 5×10-6 M и 1×10-12 M, между 1×10-6 M и 5×10-7 M, между 1×10-6 M и 1×10-7 M, между 1×10-6 M и 5×10-8 M, 1×10-6 M и 1×10-8 M, между 1×10-6 M и 5×10-9 M, между 1×10-6 M и 1×10-9 M, между 1×10-6 M и 5×10-10 M, между 1×10-6 M и 1×10-10 M, между 1×10-6 M и 5×10-11 M, между 1×10-6 M и 1×10-11 M, между 1×10-6 M и 5×10-12 M, между 1×10-6 M и 1×10-12 M, между 5×10-7 M и 1×10-7 M, между 5×10-7 M и 5×10-8 M, 5×10-7 M и 1×10-8 M, между 5×10-7 M и 5×10-9 M, между 5×10-7 M и 1×10-9 M, между 5×10-7 M и 5×10-10 M, между 5×10-7 M и 1×10-10 M, между 5×10-7 M и 5×10-11 M, между 5×10-7 M и 1×10-11 M, между 5×10-7 M и 5×10-12 M, между 5×10-7 M и 1×10-12 M, между 1×10-7 M и 5×10-8 M, 1×10-7 M и 1×10-8 M, между 1×10-7 M и 5×10-9 M, между 1×10-7 M и 1×10-9 M, между 1×10-7 M и 5×10-10 M, между 1×10-7 M и 1×10-10 M, между 1×10-7 M и 5×10-11 M, между 1×10-7 M и 1×10-11 M, между 1×10-7 M и 5×10-12 M, между 1×10-7 M и 1×10-12 M, между 5×10-8 M и 1×10-8 M, между 5×10-8 M и 5×10-9 M, между 5×10-8 M и 1×10-9 M, между 5×10 8 M и 5×10-10 M, между 5×10-8 M и 1×10-10 M, между 5×10-8 M и 5×10-11 M, между 5×10 8 M и 1×10-11 M, между 5×10-8 M и 5×10-12 M, между 5×10-8 M и 1×10-12 M, 1×10-8 M и 5×10-9 M, между 1×10-8 M и 1×10-9 M, между 1×10-8 M и 5×10-10 M, между 1×10-8 M и 1×10-10 M, между 1×10-8 M и 5×10-11 M, между 1×10 8 M и 1×10-11 M, между 1×10-8 M и 5×10-12 M, между 1×10-8 M и 1×10-12 M, между 5×10-9 M и 1×10-9 M, между 5×10-9 M и 5×10-10 M, между 5×10-9 M и 1×10-10 M, между 5×10 9 M и 5×10-11 M, между 5×10 9 M и 1×10-11 M, между 5×10-9 M и 5×10-12 M, между 5×10-9 M и 1×10-12 M, между 1×10-9 M и 5×10-10 M, между 1×10-9 M и 1×10-10 M, между 1×10-9 M и 5×10-11 M, между 1×10-9 M и 1×10-11 M, между 1×10-9 M и 5×10-12 M, между 1×10-9 M и 1×10-12 M, между 5×10 10 M и 1×10-10 M, между 5×10-10 M и 5×10-11 M, между, 1×10-10 M и 5×10-11 M, 1×10-10 M и 1×10-11 M, между 1×10-10 M и 5×10-12 M, между 1×10-10 M и 1×10 12 M, между 5×10-11 M и 1×10-12 M, между 5×10-11 M и 5×10-12 M, между 5×10 11 M и 1×10-12 M, между 1×10-11 M и 5×10 12 M, или между 1×10-11 M и 1×10-12 M, при измерении посредством интерферометрии биослоя. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R связывается с IL13 и/или IL4 собачьих, IL13 и/или IL4 кошачьих, и/или IL13 и/или IL4 лошадиных.
[0086] «Уменьшать» или «ингибировать» означает снижать, уменьшать или осуществлять арест активности, функции или количества по сравнению с эталоном. В некоторых вариантах осуществления под «уменьшать» или «ингибировать» понимают способность вызывать общее уменьшение на 20% или более. В некоторых вариантах осуществления под «уменьшать» или «ингибировать» понимают способность вызывать общее уменьшение на 50% или более. В некоторых вариантах осуществления под «уменьшать» или «ингибировать» понимают способность вызывать общее уменьшение на 75%, 85%, 90%, 95% или более. В некоторых вариантах осуществления количество, указанное выше, ингибируют или уменьшают на протяжении периода времени, по сравнению с контрольной дозой (такой как плацебо), на протяжении такого же периода времени. «Эталон», в рамках изобретения, относится к любому образцу, стандарту или уровню, который используют для целей сравнения. Эталон можно получать из здорового или не пораженного заболеванием образца. В некоторых примерах, эталон получают из не пораженного заболеванием или не обработанного образца от домашнего животного. В некоторых примерах, эталон получают из одного или нескольких здоровых животных конкретного вида, не являющихся животными, которых подвергали тестированию или лечению.
[0087] Термин «существенно уменьшенное», в рамках изобретения, обозначает значительно высокую степень уменьшения между числовым значением и эталонным числовым значением, такую, что специалист в данной области может рассматривать различие между двумя значениями как статистически значимое в контексте биологической характеристики, измеряемой указанными значениями. В некоторых вариантах осуществления существенно уменьшенные числовые значения уменьшены более чем приблизительно на любое из 10%, 15% 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100%, по сравнению с эталонным значением.
[0088] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R может уменьшать передачу сигналов IL13 и/или IL4 у вида домашнего животного по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или на 100%, по сравнению с передачей сигналов IL13 и/или IL4 в отсутствие слитой молекулы. В некоторых вариантах осуществления передачу сигналов измеряют по уменьшению зависимой от IL4 пролиферации клеток TF-1. В некоторых вариантах осуществления уменьшение передачи сигналов IL13 и/или IL4, или уменьшение пролиферации составляет между 10% и 15%, между 10% и 20%, между 10% и 25%, между 10% и 30%, между 10% и 35%, между 10% и 40%, между 10% и 45%, между 10% и 50%, между 10% и 60%, между 10% и 70%, между 10% и 80%, между 10% и 90%, между 10% и 100%, между 15% и 20%, между 15% и 25%, между 15% и 30%, между 15% и 35%, между 15% и 40%, между 15% и 45%, между 15% и 50%, между 15% и 60%, между 15% и 70%, между 15% и 80%, между 15% и 90%, между 15% и 100%, между 20% и 25%, между 20% и 30%, между 20% и 35%, между 20% и 40%, между 20% и 45%, между 20% и 50%, между 20% и 60%, между 20% и 70%, между 20% и 80%, между 20% и 90%, между 20% и 100%, между 25% и 30%, между 25% и 35%, между 25% и 40%, между 25% и 45%, между 25% и 50%, между 25% и 60%, между 25% и 70%, между 25% и 80%, между 25% и 90%, между 25% и 100%, между 30% и 35%, между 30% и 40%, между 30% и 45%, между 30% и 50%, между 30% и 60%, между 30% и 70%, между 30% и 80%, между 30% и 90%, между 30% и 100%, между 35% и 40%, между 35% и 45%, между 35% и 50%, между 35% и 60%, между 35% и 70%, между 35% и 80%, между 35% и 90%, между 35% и 100%, между 40% и 45%, между 40% и 50%, между 40% и 60%, между 40% и 70%, между 40% и 80%, между 40% и 90%, между 40% и 100%, между 45% и 50%, между 45% и 60%, между 45% и 70%, между 45% и 80%, между 45% и 90%, между 45% и 100%, между 50% и 60%, между 50% и 70%, между 50% и 80%, между 50% и 90%, между 50% и 100%, между 60% и 70%, между 60% и 80%, между 60% и 90%, между 60% и 100%, между 70% и 80%, между 70% и 90%, между 70% и 100%, между 80% и 90%, между 80% и 100%, или между 90% и 100%.
Фармацевтические композиции
[0089] термины «фармацевтический состав» и «фармацевтическая композиция» относятся к препарату, который находится в такой форме, чтобы позволять биологической активности активного ингредиента(ингредиентов) являться эффективной, и который не содержит дополнительных компонентов, являющихся неприемлемо токсичными для субъекта, которому следует вводить состав.
[0090] «Фармацевтически приемлемый носитель» относится к нетоксичному твердому, полутвердому или жидкому наполнителю, разбавителю, инкапсулирующему материалу, вспомогательному средству для получения составов или носителю, общепринятому в данной области для использования с лекарственным средством, которые совместно составляют «фармацевтическую композицию» для введения субъекту. Фармацевтически приемлемый носитель не является токсичным для реципиентов во всех используемых дозах и концентрациях и является совместимым с другими ингредиентами состава. Фармацевтически приемлемый носитель является пригодным для используемого состава. Примеры фармацевтически приемлемых носителей включают оксид алюминия; стеарат алюминия; лецитин; сывороточные белки, такие как человеческий сывороточный альбумин, альбумин собачьих или других животных; буферы, такие как буферы фосфат, цитрат, трометамин или HEPES; глицин; сорбиновая кислота; сорбат калия; смеси частичных глицеридов насыщенных растительных жирных кислот; воду; соли или электролиты, такие как сульфат протамина, гидрофосфат динатрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния или трисиликат магния; поливинилпирролидон, вещества на основе целлюлозы; полиэтиленгликоль; сахарозу; маннит; или аминокислоты, включая, но без ограничения, аргинин.
[0091] Фармацевтическую композицию можно хранить в лиофилизированной форме. Таким образом, в некоторых вариантах осуществления способ получения включает стадию лиофилизации. Затем можно повторно получать состав лиофилизированной композиции, как правило, в форме водной композиции, пригодной для парентерального введения, перед введением собаке, кошке или лошади. В других вариантах осуществления, в частности, где слитая молекула является высоко устойчивой к термической и окислительной денатурации, фармацевтическую композицию можно хранить в форме жидкости, т.е., в форме водной композиции, которую можно вводить непосредственно или в соответствующем разведении, собаке, кошке или лошади. Лиофилизированную композицию можно разводить стерильной водой для инъекций (WFI). Можно включать бактериостатические реагенты, такие как бензиловый спирт. Таким образом, изобретение относится к фармацевтическим композициям в твердой или жидкой форме.
[0092] pH фармацевтических композиций может лежать в диапазоне от приблизительно pH 5 до приблизительно pH 8, при введении. Композиции по изобретению являются стерильными, если они предназначены для использования для терапевтических целей. Стерильности можно достигать любым из нескольких способов, известных в данной области, включая фильтрацию через стерильные мембраны для фильтрации (например, мембраны 0,2 микрона). Стерильность можно поддерживать с использованием или без использования антибактериальных средств.
Применения непрерывных полипептидов IL13R/IL4R и фармацевтических композиций
[0093] Непрерывные полипептиды IL13R/IL4R или фармацевтические композиции, содержащие непрерывные полипептиды IL13R/IL4R по изобретению, можно использовать для лечения индуцированного IL13 и/или IL4 состояния. В рамках изобретения, «индуцированное IL13 или IL4 состояние» обозначает заболевание, ассоциированное с, вызванное или отличающееся увеличенными уровнями или измененным распределением IL13 или IL4. Такие индуцированные IL13 и/или IL4 состояния включают, но без ограничения, сопровождающееся зудом или аллергическое заболевание. В некоторых вариантах осуществления индуцированное IL13 и/или IL4 состояние представляет собой атопический дерматит, зуд, астму, псориаз, склеродермию или экзему. Индуцированное IL13 или IL4 состояние может проявляться у домашнего животного, включая, но без ограничения, собачьих, кошачьих или лошадиных.
[0094] В рамках изобретения, «лечение» представляет собой способ получения преимущественных или желательных клинических результатов. «Лечение», в рамках изобретения, включает любое введение или применение лекарственного средства против заболевания у млекопитающего, включая домашнее животное. Для целей по этому описанию, преимущественные или желательные клинические результаты включают, но без ограничения, любое одно или несколько из: облегчения одного или нескольких симптомов, уменьшения степени заболевания, предотвращения или задержки распространения заболевания, предотвращения или задержки рецидива заболевания, задержки или замедления прогрессирования заболевания, облегчения состояния заболевания, ингибирования заболевания или прогрессирования заболевания, ингибирования или замедления заболевания или его прогрессирования, ареста его развития и ремиссии (либо частичной, либо полной). «Лечение» охватывает также уменьшение патологических последствий пролиферативных заболеваний. Способы, представленные в настоящем описании, предусматривают любой один или несколько из этих аспектов лечения. В соответствии с вышеуказанным, термин лечение не требует стопроцентного удаления всех аспектов нарушения.
[0095] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или содержащие его фармацевтические композиции можно использовать в соответствии со способами в настоящем описании для лечения индуцированных IL13 или IL4 состояний. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтические композиции вводят домашнему животному, например, из числа собачьих, кошачьих или лошадиных, для лечения индуцированного IL13 и IL4 состояния.
[0096] «Терапевтически эффективное количество» вещества/молекулы, агониста или антагониста можно менять в зависимости от таких факторов, как тип заболевания, подлежащего лечению, состояние заболевания, тяжесть и течение заболевания, тип терапевтической цели, любая предшествующая терапия, клинический анамнез, ответ на предшествующее лечение, решение лечащего ветеринара, возраст, пол и масса животного, и способность вещества/молекулы, агониста или антагониста вызывать желательный ответ у животного. Терапевтически эффективное количество также включает количество, при котором любые токсичные или неблагоприятные эффекты вещества/молекулы, агониста или антагониста перевешиваются терапевтически благоприятными эффектами. Терапевтически эффективное количество можно доставлять за одно или несколько введений. Терапевтически эффективное количество относится к количеству, эффективному, при необходимых дозах и в течение необходимых периодов времени, для достижения желательного терапевтического или профилактического результата.
[0097] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтическую композицию, содержащую непрерывный полипептид IL13R/IL4R, вводят парентерально, посредством подкожного введения, внутривенной инфузии или внутримышечной инъекции. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтическую композицию, содержащую непрерывный полипептид IL13R/IL4R, вводят в форме болюсной инъекции или посредством непрерывной инфузии в течение некоторого периода времени. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R или фармацевтическую композицию, содержащую непрерывный полипептид IL13R/IL4R, вводят внутримышечным, внутрибрюшинным, внутриспинномозговым, подкожным, внутриартериальным, внутрисуставным, интратекальным или ингаляционным способом.
[0098] Непрерывный полипептид IL13R/IL4R, описанный в настоящем описании, можно вводить в количестве в диапазоне от 0,1 мг/кг массы тела до 100 мг/кг массы тела на дозу. В некоторых вариантах осуществления слитый белок против IL13/IL4 можно вводить в количестве в диапазоне от 0,5 мг/кг массы тела до 50 мг/кг массы тела на дозу. В некоторых вариантах осуществления слитый белок против IL13/IL4 можно вводить в количестве в диапазоне от 1 мг/кг массы тела до 10 мг/кг массы тела на дозу. В некоторых вариантах осуществления слитую молекулу можно вводить в количестве в диапазоне от 0,5 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 1 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 5 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 10 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 20 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 50 мг/кг массы тела до 100 мг/кг массы тела, в диапазоне от 1 мг/кг массы тела до 10 мг/кг массы тела, в диапазоне от 5 мг/кг массы тела до 10 мг/кг массы тела, в диапазоне от 0,5 мг/кг массы тела до 10 мг/кг массы тела или в диапазоне от 5 мг/кг массы тела до 50 мг/кг массы тела.
[0099] Непрерывный полипептид IL13R/IL4R или фармацевтическую композицию, содержащую непрерывный полипептид IL13R/IL4R, можно вводить домашнему животному за один раз или на протяжении серий циклов лечения. Например, непрерывный полипептид IL13R/IL4R или фармацевтическую композицию, содержащую IL13R и IL4R, можно вводить по меньшей мере один раз, более одного раза, по меньшей мере два раза, по меньшей мере три раза, по меньшей мере четыре раза или по меньшей мере пять раз.
[00100] В некоторых вариантах осуществления дозу вводят один раз в неделю в течение по меньшей мере двух или трех последовательных недель, и в некоторых вариантах осуществления этот цикл лечения повторяют два или более раз, необязательно, с чередованием с одной или несколькими неделями без лечения. В других вариантах осуществления, терапевтически эффективную дозу вводят один раз в сутки в течение пяти последовательных суток, и в некоторых вариантах осуществления этот цикл лечения повторяют два или более раз, необязательно, с чередованием с одними или несколькими сутками или неделями без лечения.
[00101] Введение «в комбинации с» одним или несколькими дополнительными лекарственными средствами включает одновременное (параллельное) введение и следующее один за другим или последовательное введение в любом порядке. Термин «одновременно», в рамках изобретения, предназначен для обозначения введения двух или более лекарственных средств, где по меньшей мере часть введения перекрывается по времени или где введение одного лекарственного средства попадает в пределы короткого периода времени относительно введения другого лекарственного средства. Например, два или более лекарственных средств вводят с разделением по времени не более, чем указанное количество минут. Термин «последовательно», в рамках изобретения, предназначен для обозначения введения двух или более лекарственных средств, где введение одного или нескольких средств(а) продолжается после прекращения введения одного или нескольких других средств(а), или где введение одного или нескольких средств(а) начинается до введения одного или нескольких других средств(а). Например, введение двух или более лекарственных средств проводят с разделением по времени более, чем указанное количество минут. В рамках изобретения, «в сочетании с» относится к осуществлению одного варианта лечения в дополнение к другому варианту лечения. Таким образом, «в сочетании с» относится к осуществлению одного варианта лечения до, во время или после осуществления другого варианта лечения животного.
[00102] В некоторых вариантах осуществления способ включает введение в комбинации с непрерывным полипептидом IL13R/IL4R или фармацевтической композицией, содержащей непрерывный полипептид IL13R/IL4R, ингибитора Jak, ингибитора PI3K, ингибитора AKT или ингибитора MAPK. В некоторых вариантах осуществления способ включает введение в комбинации с непрерывным полипептидом IL13R/IL4R или фармацевтической композицией, содержащей непрерывный полипептид IL13R/IL4R, антитела против IL17, антитела против TNFα, антитела против CD20, антитела против CD19, антитела против CD25, антитела против IL31, антитела против IL23, антитела против IgE, антитела против CD11α, антитела против IL6R, антитела против α4-интегрина, антитела против IL12, антитела против IL1β или антитела против BlyS.
[00103] Настоящее изобретение относится к способам подвергания клетки воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции, содержащей непрерывный полипептид IL13R/IL4R, в условиях, позволяющих связывание с IL13 или IL4. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции ex vivo. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции in vivo. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида IL13R/IL4R. В некоторых вариантах осуществления клетку подвергают воздействию непрерывного полипептида IL13R/IL4R или фармацевтической композиции в условиях, позволяющих связывание слитой молекулы с внеклеточным IL13 или IL4. В некоторых вариантах осуществления клетку можно подвергать воздействию in vivo непрерывного полипептида IL13R/IL4R или фармацевтической композиции посредством одного или нескольких из способов введения, описанных в настоящем описании, включая, но без ограничения, внутрибрюшинную, внутримышечную, внутривенную инъекцию субъекту. В некоторых вариантах осуществления клетку можно подвергать воздействию ex vivo непрерывного полипептида IL13R/IL4R или фармацевтической композиции посредством воздействия на клетку культуральной среды, содержащей слитую молекулу или фармацевтическую композицию. В некоторых вариантах осуществления на проницаемость клеточной мембраны можно влиять с использованием любого количества способов, известных специалисту в данной области (таких как электропорация клеток или подвергание клеток воздействию раствора, содержащего хлорид кальция), перед подверганием клетки воздействию культуральной среды, содержащей слитую молекулу или фармацевтическую композицию.
[00104] В некоторых вариантах осуществления воздействие приводит к уменьшению функции передачи клеткой сигналов IL13 или IL4. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R может уменьшать передачу сигналов IL13 или IL4 в клетке по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или 100%, по сравнению с функцией передачи сигналов IL13 или IL4 в отсутствие непрерывного полипептида IL13R/IL4R. В некоторых вариантах осуществления уменьшение передачи сигналов IL13 или IL4 или уменьшение пролиферации TF-1 составляет между 10% и 15%, между 10% и 20%, между 10% и 25%, между 10% и 30%, между 10% и 35%, между 10% и 40%, между 10% и 45%, между 10% и 50%, между 10% и 60%, между 10% и 70%, между 10% и 80%, между 10% и 90%, между 10% и 100%, между 15% и 20%, между 15% и 25%, между 15% и 30%, между 15% и 35%, между 15% и 40%, между 15% и 45%, между 15% и 50%, между 15% и 60%, между 15% и 70%, между 15% и 80%, между 15% и 90%, между 15% и 100%, между 20% и 25%, между 20% и 30%, между 20% и 35%, между 20% и 40%, между 20% и 45%, между 20% и 50%, между 20% и 60%, между 20% и 70%, между 20% и 80%, между 20% и 90%, между 20% и 100%, между 25% и 30%, между 25% и 35%, между 25% и 40%, между 25% и 45%, между 25% и 50%, между 25% и 60%, между 25% и 70%, между 25% и 80%, между 25% и 90%, между 25% и 100%, между 30% и 35%, между 30% и 40%, между 30% и 45%, между 30% и 50%, между 30% и 60%, между 30% и 70%, между 30% и 80%, между 30% и 90%, между 30% и 100%, между 35% и 40%, между 35% и 45%, между 35% и 50%, между 35% и 60%, между 35% и 70%, между 35% и 80%, между 35% и 90%, между 35% и 100%, между 40% и 45%, между 40% и 50%, между 40% и 60%, между 40% и 70%, между 40% и 80%, между 40% и 90%, между 40% и 100%, между 45% и 50%, между 45% и 60%, между 45% и 70%, между 45% и 80%, между 45% и 90%, между 45% и 100%, между 50% и 60%, между 50% и 70%, между 50% и 80%, между 50% и 90%, между 50% и 100%, между 60% и 70%, между 60% и 80%, между 60% и 90%, между 60% и 100%, между 70% и 80%, между 70% и 90%, между 70% и 100%, между 80% и 90%, между 80% и 100% или между 90% и 100%.
[00105] Настоящее изобретение относится к способам использования непрерывного полипептида, полипептидов и полинуклеотидов IL13R/IL4R для детекции, диагностики и мониторирования индуцированного IL13 или IL4 состояния. Настоящее изобретение относится к способам определения того, может ли домашнее животное отвечать на терапию непрерывным полипептидом IL13R/IL4R. В некоторых вариантах осуществления способ включает детекцию того, имеет ли животное клетки, экспрессирующие IL13 или IL4, с использованием непрерывного полипептида IL13R/IL4R. В некоторых вариантах осуществления способ детекции включает приведение образца в контакт с антителом, полипептидом или полинуклеотидом и определение того, отличается ли уровень связывания от уровня связывания для эталонного или сравнительного образца (такого как контроль). В некоторых вариантах осуществления способ можно использовать для определения того, являются ли непрерывные полипептиды IL13R/IL4R, описанные в настоящем описании, подходящим лекарственным средством для рассматриваемого животного.
[00106] В некоторых вариантах осуществления образец представляет собой биологический образец. Термин «биологический образец» обозначает некоторое количество вещества из живого организма или ранее живого организма. В некоторых вариантах осуществления биологический образец представляет собой клетку или лизат клетки/ткани. В некоторых вариантах осуществления биологический образец включает, но без ограничения, кровь, (например, цельную кровь), плазму, сыворотку, мочу, синовиальную жидкость и эпителиальные клетки.
[00107] В некоторых вариантах осуществления клетки или лизат клетки/ткани приводят в контакт с непрерывным полипептидом IL13R/IL4R и определяют связывание между непрерывным полипептидом IL13R/IL4R и клеткой. Когда для тестируемой клетки показана активность связывания, по сравнению с эталонной клеткой из того же типа клеток, это может указывать на то, что субъект может получать преимущества от лечения с использованием непрерывного полипептида IL13R/IL4R. В некоторых вариантах осуществления тестируемые клетки происходят из ткани домашнего животного.
[00108] Можно использовать различные способы, известные в данной области, для детекции специфического связывания антитело-антиген. Иллюстративные иммуноанализы, которые можно проводить, включают поляризационный флуоресцентный иммуноанализ (FPIA), флуоресцентный иммуноанализ (FIA), ферментный иммуноанализ (EIA), нефелометрический иммуноанализ ингибирования (NIA), твердофазный иммуноферментный анализ (ELISA) и радиоиммунный анализ (RIA). Индикаторную группу или группу метки можно присоединять к рассматриваемым антителам, и их выбирают таким образом, чтобы они удовлетворяли требованиям, предъявляемым к различным применениям способа, которые часто продиктованы наличием оборудования для анализа и совместимыми способами иммуноанализа. Подходящие метки включают, без ограничения, радиоактивные изотопы (например, 125I, 131I, 35S, 3H или 32P), ферменты (например, щелочную фосфатазу, пероксидазу хрена, люциферазу или β-галактозидазу), флуоресцентные группы или белки (например, флуоресцеин, родамин, фикоэритрин, GFP, или BFP), или люминесцентные группы (например, наночастицы Qdot™, поставляемые Quantum Dot Corporation, Palo Alto, Calif.). Общие способы, используемые при осуществлении различных иммуноанализов, указанных выше, известны специалисту в данной области.
[00109] Для целей диагностики, непрерывный полипептид IL13R/IL4R можно метить поддающейся детекции группой, включая, но без ограничения, радиоактивные изотопы, флуоресцентные метки и различные ферментно-субстратные метки, известные в данной области. Способы конъюгации меток с полипептидами известны в данной области. В некоторых вариантах осуществления мечение непрерывного полипептида IL13R/IL4R не является необходимым, и его присутствие можно детектировать, например, с использованием антитела, которое связывается с непрерывным полипептидом IL13R/IL4R. В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R можно использовать в любом известном способе анализа, таком как анализы конкурентного связывания, прямые и опосредованные сэндвич-анализы и анализы иммунопреципитации. Zola, Monoclonal Antibodies: A Manual of Techniques, pp. 147-158 (CRC Press, Inc. 1987). Антитела и полипептиды против IL13 и IL4 можно также использовать для диагностических анализов in vivo, таких как визуализация in vivo. В общем, антитело или полипептид метят радиоактивным изотопом (таким как 111In, 99Tc, 14C, 131I, 125I, 3H или любая другая метка на основе радиоактивного изотопа, включая метки, описанные в настоящем описании), таким образом, что представляющие интерес клетки или ткань могут быть локализованы с использованием иммуносцинтиграфии. Непрерывный полипептид IL13R/IL4R можно также использовать в качестве окрашивающего реагента в патологии, с использованием способов, хорошо известных в данной области.
[00110] В некоторых вариантах осуществления непрерывный полипептид IL13R/IL4R используют для диагностики, и непрерывный полипептид IL13R/IL4R используют в качестве лекарственного средства. В некоторых вариантах осуществления первый и второй непрерывные полипептиды IL13R/IL4R являются различными.
[00111] Следующие примеры иллюстрируют конкретные аспекты описания и не предназначены для ограничения описания каким-либо образом.
ПРИМЕРЫ
Пример 1
Экспрессия и очистка IL4 и IL13 собачьих
[00112] Нуклеотидную последовательность, кодирующую белок IL13 собачьих (SEQ ID NO: 4), синтезировали с меткой поли-His на C-конце и клонировали в экспрессирующий вектор для млекопитающих, и переносили в клетки 293 или CHOS. Такой же способ использовали для клонирования и экспрессии нуклеотидной последовательности, кодирующей белок IL4 собачьих (SEQ ID NO: 1) с меткой поли-His на C-конце.
[00113] Супернатант, содержащий белок IL13 собачьих, собирали и фильтровали. IL13 собачьих подвергали аффинной очистке с использованием колонки Ni-NTA (аффинная смола CaptivA® с белком A, Repligen). Такой же способ использовали для очистки IL4 собачьих.
Пример 2
Внеклеточные домены IL13R и IL4R
[00114] Внеклеточные домены IL4R собачьих, кошачьих, и лошадиных, ответственные за связывание IL4 и/или IL13 собачьих, кошачьих и лошадиных, идентифицировали и определили их границы. Полноразмерные внеклеточные домены IL4R собачьих, IL4R кошачьих, и IL4 лошадиных идентифицировали как SEQ ID NO: 23, SEQ ID NO: 25, и SEQ ID NO: 27, соответственно. Фрагменты внеклеточных доменов IL4R собачьих, IL4R кошачьих и IL4R лошадиных, принятые как сохраняющие биологическую активность, идентифицировали как SEQ ID NO: 33, SEQ ID NO: 35 и SEQ ID NO: 37, соответственно.
[00115] Внеклеточные домены IL13R собачьих, кошачьих и лошадиных, ответственные за связывание IL4 и/или IL13 собачьих, кошачьих и лошадиных, идентифицировали и определили их границы. Полноразмерные внеклеточные домены IL13R собачьих, IL13R кошачьих и IL13R лошадиных идентифицировали как SEQ ID NO: 22, SEQ ID NO: 24, и SEQ ID NO: 26, соответственно. Фрагменты внеклеточных доменов IL13R собачьих, IL13R кошачьих и IL13R лошадиных, принятые как сохраняющие биологическую активность, идентифицировали как SEQ ID NO: 32, SEQ ID NO: 34 и SEQ ID NO: 36, соответственно.
[00116] Неспаренный цистеин (Cys) в IL13R собачьих (в положении 18 из SEQ ID NO: 22), IL13R кошачьих (в положении 18 SEQ ID NO: 24) и IL13R лошадиных (в положении 18 SEQ ID NO: 26) идентифицировали информатическим способом и определили как погруженный (неэкспонированный) на основании 3-D моделирования. Является маловероятным, что неспаренный цистеин будет формировать дисульфидные связи, и вероятность агрегации является низкой. Таким образом, сайт-направленный мутагенез этого остатка Cys не проводили.
Пример 3
Экспрессия и очистка непрерывных полипептидов IL13R/IL4R собачьих из клеток CHO
[00117] Нуклеотидные последовательности, кодирующие непрерывные полипептиды IL13R/IL4R собачьих, связанные с Fc IgGB, конструировали с сигнальной последовательностью. В случае непрерывного полипептида «IL13R-IL4R-IgGB» (SEQ ID NO: 20), внеклеточный домен IL13R (SEQ ID NO: 22) предшествует внеклеточному домену IL4R (SEQ ID NO: 23). В случае непрерывного полипептида IL4R-IL13R-IgGB (SEQ ID NO: 21), внеклеточный домен IL4R предшествует внеклеточному домену IL13R.
[00118] Нуклеотидные последовательности синтезировали химически и вставляли в экспрессирующий вектор, подходящий для трансфекции клетки-хозяина CHO. После трансфекции клеток CHO, слитые белки секретировались из клеток. Например, слитый белок очищали посредством одностадийной хроматографии на колонке с белком A.
[00119] Каждый из IL13R-IL4R-IgGB и IL4R-IL13R-IgGB можно экспрессировать и очищать за одну стадию с использованием колонки с белком A или других хроматографических способов, таких как ионообменная хроматография на колонке, хроматография на колонке с гидрофобным взаимодействием, хроматография на колонке в смешанном режиме, такая как CHT, или хроматография на мультимодальной колонке, такая как CaptoMMC. Можно использовать низкий pH или другие способы инактивации вируса и удаления вируса. Очищенный белок можно смешивать с наполнителями и стерилизовать посредством фильтрации для получения фармацевтической композиции по изобретению. Фармацевтическую композицию можно вводить собаке с атопическим дерматитом или астмой в количестве, достаточном для связывания и/или ингибирования IL13 и/или IL4.
[00120] Затем векторы использовали для проведения трансфекции в пилотном масштабе в клетках CHO S с использованием реагента для трансфекции FreestyleMax™ (Life Technologies). Супернатант собирали посредством осветления кондиционированных сред. Белок очищали за один проход стадии хроматографии с белком A и использовали для дальнейшего исследования.
Пример 4
Демонстрация активности связывания IL13 и IL4
[00121] В этом примере показано, что как IL13R-IL4R-IgGB (SEQ ID NO:20), так и IL4R-IL13R-IgGB (SEQ ID NO:21), связывают IL4 и IL13 собачьих с кинетикой, необходимой для терапевтической активности.
[00122] Анализ связывания проводили с использованием биосенсора Octet следующим образом. Кратко, IL4 собачьих (полученный с использованием клеток 293) биотинилировали. Свободный не вступивший в реакцию биотин удаляли от биотинилированного IL4 посредством интенсивного диализа. Биотинилированный IL4 собачьих связывали на сенсорных наконечниках со стрептавидином. Связывание IL4 с различными концентрациями (12, 16 и 44 нМ) IL13R-IL4R-IgGB (SEQ ID NO:20) мониторировали в течение девяноста секунд. Диссоциацию мониторировали в течение 600 секунд. Нулевую кривую только с буфером вычитали для коррекции какого-либо смещения. Данные приводили в соответствие с моделью связывания 1:1 с использованием программного обеспечения для анализа данных ForteBio™ для определения kon, koff и Kd. Буфер для разведения и всех стадий связывания представлял собой: 20 мМ фосфат, 150 мМ NaCl, pH 7,2. Kd для IL13R-IL4R-IgGB и лиганда IL4 составляла 8 x10-11.
[00123] Связывание IL4 собачьих с различными концентрациями (40,7, и 140 нМ) IL4R-IL13R-IgGB (SEQ ID NO:21) мониторировали в течение девяноста секунд. Диссоциацию мониторировали в течение 600 секунд. Нулевую кривую только с буфером вычитали для коррекции какого-либо смещения. Данные приводили в соответствие с моделью связывания 1:1 с использованием программного обеспечения для анализа данных ForteBio™ для определения kon, koff и Kd. Буфер для разведения и всех стадий связывания представлял собой: 20 мМ фосфат, 150 мМ NaCl, pH 7,2. Kd для IL4R-IL13R-IgGB и лиганд IL4 составляла 1,1 x10-11.
[00124] IL4 собачьих и IL13 собачьих с C-концевой меткой поли-His экспрессировали и очищали из клеток 293. EZ-Link NHS-LC-биотин получали из Thermo Scientific (кат. #21336), и биосенсоры со стрептавидином получали из ForteBio (кат. #18-509).
[00125] Проводили эксперименты последовательного связывания IL4 и IL13 с IL13R-IL4R-IgGB (SEQ ID NO:20). Биотинилированный IL13R-IL4R-IgGB собачьих связывали с сенсорными наконечниками со стрептавидином. IL13R-IL4R-IgGB собачьих подвергали воздействию либо (1) IL4 собачьих, за которым следовал IL13 собачьих, либо (2) IL13 собачьих, за которым следовал IL4 собачьих, с использованием концентраций 30 мкг/мл IL4 и IL13 в PBS (Фигура 1). Эти эксперименты показали, что как только IL13R-IL4R-IgGB связывался с IL13, он не мог связываться с IL4, и как только он связывался с IL4, его способность связываться с IL13 уменьшалась.
[00126] Проводили эксперименты последовательного связывания IL4 и IL13 с IL4R-IL13R-IgGB (SEQ ID NO:21). Биотинилированный IL4R-IL13R-IgGB собачьих связывали с сенсорными наконечниками со стрептавидином. IL4R-IL13R-IgGB собачьих подвергали воздействию либо (1) IL4 собачьих, за которым следовал IL13 собачьих, либо (2) IL13 собачьих, за которым следовал IL4 собачьих, с использованием концентраций 30 мкг/мл IL4 и IL13 в PBS (Фигура 2). Эти эксперименты показали, что как только IL4R-IL13R-IgGB связывался с IL13, он не мог связываться с IL4, и как только он связывался с IL4, его способность связываться с IL13 уменьшалась.
[00127] Считается, что тесное связывание IL13R-IL4R-IgGB и IL4R-IL13R-IgGB с IL4 или IL13 обусловлено вкладами одновременного связывания как с IL4R, так и с IL13R.
Пример 5
Клеточная функциональная активность IL4R-IL13R-Fc собачьих (SINK)
[00128] Клетки TF1 (ATCC, кат.# CRL-2003), линию клеток эритролейкоза человека, экспрессирующих эндогенные рецепторы интерлейкина 4 на клеточной поверхности, использовали в анализе пролиферации. Клетки, выращенные в RPMI1640 (Gibco, кат.#11875), дополненной 10% эмбриональной бычьей сывороткой, инактивированной нагреванием (Sigma, кат.#2868) и 2 нМ/мл GM-CSF человека (R&D System, кат.# 215-GM-010), в экспоненциальной фазе роста, использовали для этого анализа. Клетки промывали PBS дважды и ресуспендировали в вышеуказанной среде без GM-CSF. 20000 клеток на лунку рассевали в 96-луночный планшет (Corning, кат.# 3610). IL4R-IL13R-Fc собачьих (SINK) добавляли в сериях разведений, с последующим добавлением IL4 собачьих (Sino Biological Inc, кат.# 70021-DNAE-5) при 50 нг/мл. Клетки инкубировали при 37°C, 5% CO2 в течение 48 часов в общем объеме 100 мкл. По окончании инкубации, клетки охлаждали при комнатной температуре и анализировали по пролиферации/жизнеспособности посредством измерения клеточного содержания АТФ с использованием люминесцентного анализа жизнеспособности клеток CellTiter-Glo® (Promega, кат.# G7570).
[00129] В этом анализе 100 мкл предварительно смешанных реагентов A и B добавляли в каждую лунку. После встряхивания на орбитальном встряхивателе в течение 2 мин, клетки лизировали. Моно-оксигенация люциферина подвергалась катализу посредством люциферазы в присутствии Mg2+ и АТФ, присутствующих в клетках, что приводило к образованию люминесцентного сигнала, пропорционального количеству АТФ в клетках. Количество АТФ является прямо пропорциональным количеству клеток, присутствующих в культуре. Планшет инкубировали при комнатной температуре в течение 10 минут для стабилизации люминесцентного сигнала, и люминесценцию детектировали с использованием считывателя для микропланшетов Synergy HT (Biotek, Winooski, VT).
[00130] Данные анализировали с использованием 4-параметрического логистического подбора, и IC50 составляла 2,0 нМ. См. фигуру 3.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
--->
<110> Kindred Biosciences, Inc.
<120> МОЛЕКУЛА РЕЦЕПТОРА IL4/IL13 ДЛЯ ВЕТЕРИНАРНОГО ПРИМЕНЕНИЯ
<130> 01157-0008-00PCT
<150> US 62/488509
<151> 2017-04-21
<160> 49
<170> PatentIn версии 3.5
<210> 1
<211> 131
<212> белок
<213> Canis lupus
<400> 1
Met Gly Leu Thr Ser Gln Leu Ile Pro Thr Leu Val Cys Leu Leu Ala
1 5 10 15
Leu Thr Ser Thr Phe Val His Gly His Asn Phe Asn Ile Thr Ile Lys
20 25 30
Glu Ile Ile Lys Met Leu Asn Ile Leu Thr Ala Arg Asn Asp Ser Cys
35 40 45
Met Glu Leu Thr Val Asp Val Phe Thr Ala Pro Lys Asn Thr Ser Asp
50 55 60
Lys Glu Ile Phe Cys Arg Ala Ala Thr Val Leu Arg Gln Ile Tyr Thr
65 70 75 80
His Asn Cys Ser Asn Arg Tyr Leu Arg Gly Leu Tyr Arg Asn Leu Ser
85 90 95
Ser Met Ala Asn Lys Thr Cys Ser Met Asn Glu Ile Lys Lys Ser Thr
100 105 110
Leu Lys Asp Phe Leu Glu Arg Leu Lys Val Ile Met Gln Lys Lys Tyr
115 120 125
Tyr Arg His
130
<210> 2
<211> 132
<212> белок
<213> Felis catus
<400> 2
Met Asp Leu Thr Ser Gln Leu Ile Pro Ala Leu Val Cys Leu Leu Ala
1 5 10 15
Phe Thr Ser Thr Phe Val His Gly Gln Asn Phe Asn Asn Thr Leu Lys
20 25 30
Glu Ile Ile Lys Thr Leu Asn Ile Leu Thr Ala Arg Asn Asp Ser Cys
35 40 45
Met Glu Leu Thr Met Asp Val Leu Ala Ala Pro Lys Asn Thr Ser Asp
50 55 60
Lys Glu Ile Phe Cys Arg Ala Thr Thr Val Leu Arg Gln Ile Tyr Thr
65 70 75 80
His His Asn Cys Ser Thr Lys Phe Leu Lys Gly Leu Asp Arg Asn Leu
85 90 95
Ser Ser Met Ala Asn Arg Thr Cys Ser Val Asn Glu Val Lys Lys Cys
100 105 110
Thr Leu Lys Asp Phe Leu Glu Arg Leu Lys Ala Ile Met Gln Lys Lys
115 120 125
Tyr Ser Lys His
130
<210> 3
<211> 137
<212> белок
<213> Equus caballus
<400> 3
Met Gly Leu Thr Tyr Gln Leu Ile Pro Ala Leu Val Cys Leu Leu Ala
1 5 10 15
Cys Thr Ser Asn Phe Ile Gln Gly Cys Lys Tyr Asp Ile Thr Leu Gln
20 25 30
Glu Ile Ile Lys Thr Leu Asn Asn Leu Thr Asp Gly Lys Gly Lys Asn
35 40 45
Ser Cys Met Glu Leu Thr Val Ala Asp Ala Phe Ala Gly Pro Lys Asn
50 55 60
Thr Asp Gly Lys Glu Ile Cys Arg Ala Ala Lys Val Leu Gln Gln Leu
65 70 75 80
Tyr Lys Arg His Asp Arg Ser Leu Ile Lys Glu Cys Leu Ser Gly Leu
85 90 95
Asp Arg Asn Leu Lys Gly Met Ala Asn Gly Thr Cys Cys Thr Val Asn
100 105 110
Glu Ala Lys Lys Ser Thr Leu Lys Asp Phe Leu Glu Arg Leu Lys Thr
115 120 125
Ile Met Lys Glu Lys Tyr Ser Lys Cys
130 135
<210> 4
<211> 131
<212> белок
<213> Canis lupus
<400> 4
Met Ala Leu Trp Leu Thr Val Val Ile Ala Leu Thr Cys Leu Gly Gly
1 5 10 15
Leu Ala Ser Pro Ser Pro Val Thr Pro Ser Pro Thr Leu Lys Glu Leu
20 25 30
Ile Glu Glu Leu Val Asn Ile Thr Gln Asn Gln Ala Ser Leu Cys Asn
35 40 45
Gly Ser Met Val Trp Ser Val Asn Leu Thr Ala Gly Met Tyr Cys Ala
50 55 60
Ala Leu Glu Ser Leu Ile Asn Val Ser Asp Cys Ser Ala Ile Gln Arg
65 70 75 80
Thr Gln Arg Met Leu Lys Ala Leu Cys Ser Gln Lys Pro Ala Ala Gly
85 90 95
Gln Ile Ser Ser Glu Arg Ser Arg Asp Thr Lys Ile Glu Val Ile Gln
100 105 110
Leu Val Lys Asn Leu Leu Thr Tyr Val Arg Gly Val Tyr Arg His Gly
115 120 125
Asn Phe Arg
130
<210> 5
<211> 183
<212> белок
<213> Felis catus
<400> 5
Met Trp Phe Leu Asp Ser Thr Arg Gln Ser Gly Asp Gln Gly Gly Arg
1 5 10 15
Arg His Thr Trp Pro Ile Lys Ala Thr Ala Arg Gly Gln Gly His Lys
20 25 30
Pro Leu Ser Leu Gly Gln Pro Thr Cys Pro Leu Leu Ala Pro Pro Val
35 40 45
Leu Ala Leu Gly Ser Met Ala Leu Trp Leu Thr Val Val Ile Ala Leu
50 55 60
Thr Cys Leu Gly Gly Leu Ala Ser Pro Gly Pro His Ser Arg Arg Glu
65 70 75 80
Leu Lys Glu Leu Ile Glu Glu Leu Val Asn Ile Thr Gln Asn Gln Val
85 90 95
Ser Leu Cys Asn Gly Ser Met Val Trp Ser Val Asn Leu Thr Thr Gly
100 105 110
Met Tyr Cys Ala Ala Leu Glu Ser Leu Ile Asn Val Ser Asp Cys Thr
115 120 125
Ala Ile Gln Arg Thr Gln Arg Met Leu Lys Ala Leu Cys Thr Gln Lys
130 135 140
Pro Ser Ala Gly Gln Thr Ala Ser Glu Arg Ser Arg Asp Thr Lys Ile
145 150 155 160
Glu Val Ile Gln Leu Val Lys Asn Leu Leu Asn His Leu Arg Arg Asn
165 170 175
Phe Arg His Gly Asn Phe Lys
180
<210> 6
<211> 133
<212> белок
<213> Equus caballus
<400> 6
Met Ala Leu Trp Leu Thr Ala Val Ile Ala Leu Ala Cys Leu Gly Gly
1 5 10 15
Leu Ala Ser Pro Ala Pro Leu Pro Ser Ser Met Ala Leu Lys Glu Leu
20 25 30
Ile Lys Glu Leu Val Asn Ile Thr Gln Asn Gln Ala Pro Leu Cys Asn
35 40 45
Gly Ser Met Val Trp Ser Val Asn Leu Thr Ala Asp Thr Tyr Cys Arg
50 55 60
Ala Leu Glu Ser Leu Ser Asn Val Ser Thr Cys Ser Ala Ile Gln Asn
65 70 75 80
Thr Arg Lys Met Leu Thr Lys Leu Cys Pro His Gln Leu Ser Ala Gly
85 90 95
Gln Val Ser Ser Glu Arg Ala Arg Asp Thr Lys Ile Glu Val Ile Val
100 105 110
Leu Val Lys Asp Leu Leu Lys Asn Leu Arg Lys Ile Phe His Gly Gly
115 120 125
Lys His Val Asp Ala
130
<210> 7
<211> 823
<212> белок
<213> Canis lupus
<400> 7
Met Gly Arg Leu Cys Ser Gly Leu Thr Phe Pro Val Ser Cys Leu Val
1 5 10 15
Leu Val Trp Val Ala Ser Ser Gly Ser Val Lys Val Leu His Glu Pro
20 25 30
Ser Cys Phe Ser Asp Tyr Ile Ser Thr Ser Val Cys Gln Trp Lys Met
35 40 45
Asp His Pro Thr Asn Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu
50 55 60
Asp Phe Met Gly Ser Glu Asn His Thr Cys Val Pro Glu Asn Arg Glu
65 70 75 80
Asp Ser Val Cys Val Cys Ser Met Pro Ile Asp Asp Ala Val Glu Ala
85 90 95
Asp Val Tyr Gln Leu Asp Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser
100 105 110
Gly Ser Phe Gln Pro Ser Lys His Val Lys Pro Arg Thr Pro Gly Asn
115 120 125
Leu Thr Val His Pro Asn Ile Ser His Thr Trp Leu Leu Met Trp Thr
130 135 140
Asn Pro Tyr Pro Thr Glu Asn His Leu His Ser Glu Leu Thr Tyr Met
145 150 155 160
Val Asn Val Ser Asn Asp Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn
165 170 175
Val Thr Tyr Met Gly Pro Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys
180 185 190
Ser Gly Ala Ser Tyr Ser Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr
195 200 205
Asn Ser Thr Trp Ser Asp Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr
210 215 220
Tyr Glu Pro Trp Glu Gln His Leu Pro Leu Gly Val Ser Ile Ser Cys
225 230 235 240
Leu Val Ile Leu Ala Ile Cys Leu Ser Cys Tyr Phe Ser Ile Ile Lys
245 250 255
Ile Lys Lys Gly Trp Trp Asp Gln Ile Pro Asn Pro Ala His Ser Pro
260 265 270
Leu Val Ala Ile Val Ile Gln Asp Ser Gln Val Ser Leu Trp Gly Lys
275 280 285
Arg Ser Arg Gly Gln Glu Pro Ala Lys Cys Pro His Trp Lys Thr Cys
290 295 300
Leu Thr Lys Leu Leu Pro Cys Leu Leu Glu His Gly Leu Gly Arg Glu
305 310 315 320
Glu Glu Ser Pro Lys Thr Ala Lys Asn Gly Pro Leu Gln Gly Pro Gly
325 330 335
Lys Pro Ala Trp Cys Pro Val Glu Val Ser Lys Thr Ile Leu Trp Pro
340 345 350
Glu Ser Ile Ser Val Val Gln Cys Val Glu Leu Ser Glu Ala Pro Val
355 360 365
Asp Asn Glu Glu Glu Glu Glu Val Glu Glu Asp Lys Arg Ser Leu Cys
370 375 380
Pro Ser Leu Glu Gly Ser Gly Gly Ser Phe Gln Glu Gly Arg Glu Gly
385 390 395 400
Ile Val Ala Arg Leu Thr Glu Ser Leu Phe Leu Asp Leu Leu Gly Gly
405 410 415
Glu Asn Gly Gly Phe Cys Pro Gln Gly Leu Glu Glu Ser Cys Leu Pro
420 425 430
Pro Pro Ser Gly Ser Val Gly Ala Gln Met Pro Trp Ala Gln Phe Pro
435 440 445
Arg Ala Gly Pro Arg Ala Ala Pro Glu Gly Pro Glu Gln Pro Arg Arg
450 455 460
Pro Glu Ser Ala Leu Gln Ala Ser Pro Thr Gln Ser Ala Gly Ser Ser
465 470 475 480
Ala Phe Pro Glu Pro Pro Pro Val Val Thr Asp Asn Pro Ala Tyr Arg
485 490 495
Ser Phe Gly Ser Phe Leu Gly Gln Ser Ser Asp Pro Gly Asp Gly Asp
500 505 510
Ser Asp Pro Glu Leu Ala Asp Arg Pro Gly Glu Ala Asp Pro Gly Ile
515 520 525
Pro Ser Ala Pro Gln Pro Pro Glu Pro Pro Ala Ala Leu Gln Pro Glu
530 535 540
Pro Glu Ser Trp Glu Gln Ile Leu Arg Gln Ser Val Leu Gln His Arg
545 550 555 560
Ala Ala Pro Ala Pro Gly Pro Gly Pro Gly Ser Gly Tyr Arg Glu Phe
565 570 575
Thr Cys Ala Val Lys Gln Gly Ser Ala Pro Asp Ala Gly Gly Pro Gly
580 585 590
Phe Gly Pro Ser Gly Glu Ala Gly Tyr Lys Ala Phe Cys Ser Leu Leu
595 600 605
Pro Gly Gly Ala Thr Cys Pro Gly Thr Ser Gly Gly Glu Ala Gly Ser
610 615 620
Gly Glu Gly Gly Tyr Lys Pro Phe Gln Ser Leu Thr Pro Gly Cys Pro
625 630 635 640
Gly Ala Pro Thr Pro Val Pro Val Pro Leu Phe Thr Phe Gly Leu Asp
645 650 655
Thr Glu Pro Pro Gly Ser Pro Gln Asp Ser Leu Gly Ala Gly Ser Ser
660 665 670
Pro Glu His Leu Gly Val Glu Pro Ala Gly Lys Glu Glu Asp Ser Arg
675 680 685
Lys Thr Leu Leu Ala Pro Glu Gln Ala Thr Asp Pro Leu Arg Asp Asp
690 695 700
Leu Ala Ser Ser Ile Val Tyr Ser Ala Leu Thr Cys His Leu Cys Gly
705 710 715 720
His Leu Lys Gln Trp His Asp Gln Glu Glu Arg Gly Lys Ala His Ile
725 730 735
Val Pro Ser Pro Cys Cys Gly Cys Cys Cys Gly Asp Arg Ser Ser Leu
740 745 750
Leu Leu Ser Pro Leu Arg Ala Pro Asn Val Leu Pro Gly Gly Val Leu
755 760 765
Leu Glu Ala Ser Leu Ser Pro Ala Ser Leu Val Pro Ser Gly Val Ser
770 775 780
Lys Glu Gly Lys Ser Ser Pro Phe Ser Gln Pro Ala Ser Ser Ser Ala
785 790 795 800
Gln Ser Ser Ser Gln Thr Pro Lys Lys Leu Ala Val Leu Ser Thr Glu
805 810 815
Pro Thr Cys Met Ser Ala Ser
820
<210> 8
<211> 881
<212> белок
<213> Felis catus
<400> 8
Met Gly Arg Leu Cys Ser Gly Leu Thr Phe Pro Val Ser Cys Leu Ile
1 5 10 15
Leu Met Trp Ala Ala Gly Ser Gly Ser Val Lys Val Leu Arg Ala Pro
20 25 30
Thr Cys Phe Ser Asp Tyr Phe Ser Thr Ser Val Cys Gln Trp Asn Met
35 40 45
Asp Ala Pro Thr Asn Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu
50 55 60
Asn Phe Met Gly Ser Glu Asn Arg Thr Cys Val Pro Glu Asn Gly Glu
65 70 75 80
Gly Ala Ala Cys Ala Cys Ser Met Leu Met Asp Asp Phe Val Glu Ala
85 90 95
Asp Val Tyr Gln Leu His Leu Trp Ala Gly Thr Gln Leu Leu Trp Ser
100 105 110
Gly Ser Phe Lys Pro Ser Ser His Val Lys Pro Arg Ala Pro Gly Asn
115 120 125
Leu Thr Val His Pro Asn Val Ser His Thr Trp Leu Leu Arg Trp Ser
130 135 140
Asn Pro Tyr Pro Pro Glu Asn His Leu His Ala Glu Leu Thr Tyr Met
145 150 155 160
Val Asn Ile Ser Ser Glu Asp Asp Pro Thr Asp Val Ser Val Cys Ala
165 170 175
Ser Gly Phe Leu Cys His Leu Leu Gly Leu Arg Arg Val Glu Thr Gly
180 185 190
Ala Pro Gly Ala Arg Leu Pro Pro Trp Leu Cys Ala Pro Arg Pro Arg
195 200 205
Arg Val Pro Gly Ser Gln Cys Ala Val Ile Ser Cys Cys Arg Trp Val
210 215 220
Leu Ile Ala Leu Thr Ser Arg Gly Gly Arg Trp Arg Leu Thr Pro Gly
225 230 235 240
Leu Arg Ser Gln Thr Arg Tyr Val Ser Val Ala Glu Gly Leu Phe Gly
245 250 255
Ala Thr Pro Arg Val Leu Cys Pro Gly Thr Gln Ala Gly Leu Ala Ser
260 265 270
Ala Ala Arg Glu Gln Met Ser Pro Asp Pro Ser Ala Phe His Ser Ile
275 280 285
Asp Tyr Glu Pro Trp Glu Gln His Leu Pro Leu Gly Val Ser Ile Ser
290 295 300
Cys Leu Val Ile Leu Ala Val Cys Leu Ser Cys Tyr Leu Ser Val Ile
305 310 315 320
Lys Ile Lys Lys Glu Trp Trp Asp Gln Ile Pro Asn Pro Ala His Ser
325 330 335
His Leu Val Ala Ile Val Ile Gln Asp Pro Gln Val Ser Leu Trp Gly
340 345 350
Lys Arg Ser Arg Gly Gln Glu Pro Ala Lys Cys Pro His Trp Lys Thr
355 360 365
Cys Leu Arg Lys Leu Leu Pro Cys Leu Leu Glu His Gly Met Glu Arg
370 375 380
Lys Glu Asp Pro Ser Lys Ile Ala Arg Asn Gly Pro Ser Gln Cys Ser
385 390 395 400
Gly Lys Ser Ala Trp Cys Pro Val Glu Val Ser Lys Thr Ile Leu Trp
405 410 415
Pro Glu Ser Ile Ser Val Val Arg Cys Val Glu Leu Leu Glu Ala Pro
420 425 430
Val Glu Ser Glu Glu Glu Glu Glu Glu Glu Glu Asp Lys Gly Ser Phe
435 440 445
Cys Pro Ser Pro Val Asn Leu Glu Asp Ser Phe Gln Glu Gly Arg Glu
450 455 460
Gly Ile Ala Ala Arg Leu Thr Glu Ser Leu Phe Met Asp Leu Leu Gly
465 470 475 480
Val Glu Lys Gly Gly Phe Gly Pro Gln Gly Ser Leu Glu Ser Trp Phe
485 490 495
Pro Pro Pro Ser Gly Ser Ala Gly Ala Gln Met Pro Trp Ala Glu Phe
500 505 510
Pro Gly Pro Gly Pro Gln Glu Ala Ser Pro Gln Gly Lys Glu Gln Pro
515 520 525
Phe Asp Pro Arg Ser Asp Pro Leu Ala Thr Leu Pro Gln Ser Pro Ala
530 535 540
Ser Pro Thr Phe Pro Glu Thr Pro Pro Val Val Thr Asp Asn Pro Ala
545 550 555 560
Tyr Arg Ser Phe Gly Thr Phe Gln Gly Arg Ser Ser Gly Pro Gly Glu
565 570 575
Cys Asp Ser Gly Pro Glu Leu Ala Gly Arg Leu Gly Glu Ala Asp Pro
580 585 590
Gly Ile Pro Ala Ala Pro Gln Pro Ser Glu Pro Pro Ser Ala Leu Gln
595 600 605
Pro Glu Ala Glu Thr Trp Glu Gln Ile Leu Arg Gln Arg Val Leu Gln
610 615 620
His Arg Gly Ala Pro Ala Pro Ala Pro Gly Ser Gly Tyr Arg Glu Phe
625 630 635 640
Val Cys Ala Val Arg Gln Gly Ser Thr Gln Asp Ser Gly Val Gly Asp
645 650 655
Phe Gly Pro Ser Glu Glu Ala Gly Tyr Lys Ala Phe Ser Ser Leu Leu
660 665 670
Thr Ser Gly Ala Val Cys Pro Glu Ser Gly Gly Glu Ala Gly Ser Gly
675 680 685
Asp Gly Gly Tyr Lys Pro Phe Gln Ser Leu Thr Pro Gly Cys Pro Gly
690 695 700
Ala Pro Ala Pro Val Pro Val Pro Leu Phe Thr Phe Gly Leu Asp Ala
705 710 715 720
Glu Pro Pro His Cys Pro Gln Asp Ser Pro Leu Pro Gly Ser Ser Pro
725 730 735
Glu Pro Ala Gly Lys Ala Gln Asp Ser His Lys Thr Pro Pro Ala Pro
740 745 750
Glu Gln Ala Ala Asp Pro Leu Arg Asp Asp Leu Ala Ser Gly Ile Val
755 760 765
Tyr Ser Ala Leu Thr Cys His Leu Cys Gly His Leu Lys Gln Cys His
770 775 780
Gly Gln Glu Glu Gly Gly Glu Ala His Pro Val Ala Ser Pro Cys Cys
785 790 795 800
Gly Cys Cys Cys Gly Asp Arg Ser Ser Pro Leu Val Ser Pro Leu Arg
805 810 815
Ala Pro Asp Pro Leu Pro Gly Gly Val Pro Leu Glu Ala Ser Leu Ser
820 825 830
Pro Ala Ser Pro Ala Pro Leu Ala Val Ser Glu Glu Gly Pro Pro Ser
835 840 845
Leu Cys Phe Gln Pro Ala Leu Ser His Ala His Ser Ser Ser Gln Thr
850 855 860
Pro Lys Lys Val Ala Met Leu Ser Pro Glu Pro Thr Cys Thr Met Ala
865 870 875 880
Ser
<210> 9
<211> 809
<212> белок
<213> Equus caballus
<400> 9
Met Gly Cys Leu Cys Pro Gly Leu Thr Leu Pro Val Ser Cys Leu Ile
1 5 10 15
Leu Val Trp Ala Ala Gly Ser Gly Ser Val Lys Val Leu His Leu Thr
20 25 30
Ala Cys Phe Ser Asp Tyr Ile Ser Ala Ser Thr Cys Glu Trp Lys Met
35 40 45
Asp Arg Pro Thr Asn Cys Ser Ala Gln Leu Arg Leu Ser Tyr Gln Leu
50 55 60
Asn Asp Glu Phe Ser Asp Asn Leu Thr Cys Ile Pro Glu Asn Arg Glu
65 70 75 80
Asp Glu Val Cys Val Cys Arg Met Leu Met Asp Asn Ile Val Ser Glu
85 90 95
Asp Val Tyr Glu Leu Asp Leu Trp Ala Gly Asn Gln Leu Leu Trp Asn
100 105 110
Ser Ser Phe Lys Pro Ser Arg His Val Lys Pro Arg Ala Pro Gln Asn
115 120 125
Leu Thr Val His Ala Ile Ser His Thr Trp Leu Leu Thr Trp Ser Asn
130 135 140
Pro Tyr Pro Leu Lys Asn His Leu Trp Ser Glu Leu Thr Tyr Leu Val
145 150 155 160
Asn Ile Ser Lys Glu Asp Asp Pro Thr Asp Phe Lys Ile Tyr Asn Val
165 170 175
Thr Tyr Met Asp Pro Thr Leu Arg Val Thr Ala Ser Thr Leu Lys Ser
180 185 190
Arg Ala Thr Tyr Ser Ala Arg Val Lys Ala Arg Ala Gln Asn Tyr Asn
195 200 205
Ser Thr Trp Ser Glu Trp Ser Pro Ser Thr Thr Trp His Asn Tyr Tyr
210 215 220
Glu Gln Pro Leu Glu Gln Arg Leu Pro Leu Gly Val Ser Ile Ser Cys
225 230 235 240
Val Val Ile Leu Ala Ile Cys Leu Ser Cys Tyr Phe Ser Ile Ile Lys
245 250 255
Ile Lys Lys Glu Trp Trp Asp Gln Ile Pro Asn Pro Ala His Ser Pro
260 265 270
Leu Val Ala Ile Val Leu Gln Asp Ser Gln Val Ser Leu Trp Gly Lys
275 280 285
Gln Ser Arg Gly Gln Glu Pro Ala Lys Cys Pro Arg Trp Lys Thr Cys
290 295 300
Leu Thr Lys Leu Leu Pro Cys Leu Leu Glu His Gly Leu Gln Lys Glu
305 310 315 320
Glu Asp Ser Ser Lys Thr Val Arg Asn Gly Pro Phe Gln Ser Pro Gly
325 330 335
Lys Ser Ala Trp His Thr Val Glu Val Asn His Thr Ile Leu Arg Pro
340 345 350
Glu Ile Ile Ser Val Val Pro Cys Val Glu Leu Cys Glu Ala Gln Val
355 360 365
Glu Ser Glu Glu Glu Glu Val Glu Glu Asp Arg Gly Ser Phe Cys Pro
370 375 380
Ser Pro Glu Ser Ser Gly Ser Gly Phe Gln Glu Gly Arg Glu Gly Val
385 390 395 400
Ala Ala Arg Leu Thr Glu Ser Leu Phe Leu Gly Leu Leu Gly Ala Glu
405 410 415
Asn Gly Ala Leu Gly Glu Ser Cys Leu Leu Pro Pro Leu Gly Ser Ala
420 425 430
His Met Pro Trp Ala Arg Ile Ser Ser Ala Gly Pro Gln Glu Ala Ala
435 440 445
Ser Gln Gly Glu Glu Gln Pro Leu Asn Pro Glu Ser Asn Pro Leu Ala
450 455 460
Thr Leu Thr Gln Ser Pro Gly Ser Leu Ala Phe Thr Glu Ala Pro Ala
465 470 475 480
Val Val Ala Asp Asn Pro Ala Tyr Arg Ser Phe Ser Asn Ser Leu Ser
485 490 495
Gln Pro Arg Gly Pro Gly Glu Leu Asp Ser Asp Pro Gln Leu Ala Glu
500 505 510
His Leu Gly Gln Val Asp Pro Ser Ile Pro Ser Ala Pro Gln Pro Ser
515 520 525
Glu Pro Pro Thr Ala Leu Gln Pro Glu Pro Glu Thr Trp Glu Gln Met
530 535 540
Leu Arg Gln Ser Val Leu Gln Gln Gly Ala Ala Pro Ala Pro Ala Ser
545 550 555 560
Ala Pro Thr Gly Gly Tyr Arg Glu Phe Ala Gln Ala Val Lys Gln Gly
565 570 575
Gly Gly Ala Ala Gly Ser Gly Pro Ser Gly Glu Ala Gly Tyr Lys Ala
580 585 590
Phe Ser Ser Leu Leu Ala Gly Ser Ala Val Cys Pro Gly Gln Ser Gly
595 600 605
Val Glu Ala Ser Ser Gly Glu Gly Gly Tyr Arg Pro Tyr Glu Ser Pro
610 615 620
Asp Pro Gly Ala Pro Ala Pro Val Pro Val Pro Leu Phe Thr Phe Gly
625 630 635 640
Leu Asp Val Glu Pro Pro His Ser Pro Gln Asn Ser Leu Leu Pro Gly
645 650 655
Gly Ser Pro Glu Leu Pro Gly Pro Glu Pro Thr Val Lys Gly Glu Asp
660 665 670
Pro Arg Lys Pro Leu Leu Ser Ala Gln Gln Ala Thr Asp Ser Leu Arg
675 680 685
Asp Asp Leu Gly Ser Gly Ile Val Tyr Ser Ala Leu Thr Cys His Leu
690 695 700
Cys Gly His Leu Lys Gln Cys His Gly Gln Glu Glu His Gly Glu Ala
705 710 715 720
His Thr Val Ala Ser Pro Cys Cys Gly Cys Cys Cys Gly Asp Arg Ser
725 730 735
Ser Pro Pro Val Ser Pro Val Arg Ala Leu Asp Pro Pro Pro Gly Gly
740 745 750
Val Pro Leu Glu Ala Gly Leu Ser Leu Ala Ser Leu Gly Ser Leu Gly
755 760 765
Leu Ser Glu Glu Arg Lys Pro Ser Leu Phe Phe Gln Pro Ala Pro Gly
770 775 780
Asn Ala Gln Ser Ser Ser Gln Thr Pro Leu Thr Val Ala Met Leu Ser
785 790 795 800
Thr Gly Pro Thr Cys Thr Ser Ala Ser
805
<210> 10
<211> 427
<212> белок
<213> Canis lupus
<400> 10
Met Glu Arg Pro Ala Arg Leu Cys Gly Leu Trp Ala Leu Leu Leu Cys
1 5 10 15
Ala Ala Gly Gly Arg Gly Gly Gly Val Ala Ala Pro Thr Glu Thr Gln
20 25 30
Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn Leu Cys Thr Val
35 40 45
Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro Asn Cys Thr Leu
50 55 60
Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys Lys Ile Ala Pro
65 70 75 80
Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu Arg Ile Cys Leu
85 90 95
Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp Asn Pro Ser Ile
100 105 110
Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp Pro Glu Ser Ala
115 120 125
Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser Tyr Met Lys Cys
130 135 140
Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr Asn Tyr Thr Leu
145 150 155 160
Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln Cys Glu Asp Ile
165 170 175
Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala Leu Thr Asn Leu
180 185 190
Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile Val Val Lys Asp
195 200 205
Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val Pro Leu Thr Ser
210 215 220
His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu Phe Phe Gln Asn
225 230 235 240
Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn Phe Tyr Ser Arg
245 250 255
Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln Thr Glu Thr Asn
260 265 270
Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn Ser Glu Phe Glu
275 280 285
Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro Gly Val Leu Pro
290 295 300
Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr Asn Lys Leu Cys
305 310 315 320
Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln Ala Met Ser Ile
325 330 335
Gly Glu Asn Thr Asp Pro Thr Phe Tyr Ile Thr Met Leu Leu Ala Thr
340 345 350
Pro Val Ile Val Ala Gly Ala Ile Ile Val Leu Leu Leu Tyr Leu Lys
355 360 365
Arg Leu Lys Ile Ile Ile Phe Pro Pro Ile Pro Asp Pro Gly Lys Ile
370 375 380
Phe Lys Glu Met Phe Gly Asp Gln Asn Asp Asp Thr Leu His Trp Arg
385 390 395 400
Lys Tyr Asp Ile Tyr Glu Lys Gln Thr Lys Glu Glu Thr Asp Ser Val
405 410 415
Val Leu Ile Glu Asn Leu Lys Lys Ala Ser Gln
420 425
<210> 11
<211> 479
<212> белок
<213> Felis catus
<400> 11
Met Met Thr Lys Cys Ser Ser Asp Arg Asn Val Phe Lys Arg Lys Trp
1 5 10 15
Phe Leu Phe Pro Ala Ser Gln Tyr Thr Phe Arg Pro Ile His Gln Ala
20 25 30
Arg Pro Cys Glu Val Pro Ala Val His Leu Glu Pro Ser Pro Pro Trp
35 40 45
Glu Val Gly Leu Gly Leu Leu Asn Leu Glu Ser Glu Phe Arg Lys Leu
50 55 60
Gly Leu Arg Gly Arg Arg Leu Ala Ala Ala Pro Pro Asp Ser Arg Ala
65 70 75 80
Glu Ala Ala Ser Gln Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser
85 90 95
Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly
100 105 110
Ala Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys
115 120 125
Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro
130 135 140
Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn
145 150 155 160
Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro
165 170 175
Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His
180 185 190
Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser
195 200 205
Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys
210 215 220
Ile Leu Gln Cys Glu Asn Ile Tyr Arg Glu Gly Gln His Ile Gly Cys
225 230 235 240
Ser Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser
245 250 255
Val Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe
260 265 270
Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile
275 280 285
Lys Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn
290 295 300
Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn
305 310 315 320
Asn Ser Gln Thr Glu Thr His Asp Ile Phe Tyr Val Glu Glu Ala Lys
325 330 335
Cys Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe
340 345 350
Met Val Pro Gly Ile Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg
355 360 365
Val Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Arg Leu Trp Ser Asn
370 375 380
Trp Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Phe Tyr
385 390 395 400
Ile Thr Met Leu Leu Ala Thr Pro Val Ile Val Ala Gly Ala Ile Ile
405 410 415
Val Leu Leu Leu Tyr Leu Lys Arg Leu Lys Ile Ile Ile Phe Pro Pro
420 425 430
Ile Pro Asp Pro Gly Lys Ile Phe Lys Glu Met Phe Gly Asp Gln Asn
435 440 445
Asp Asp Ser Leu His Trp Lys Lys Tyr Asp Ile Tyr Glu Lys Gln Thr
450 455 460
Lys Glu Glu Thr Asp Ser Val Val Leu Ile Glu Asn Ala Ser Gln
465 470 475
<210> 12
<211> 407
<212> белок
<213> Equus caballus
<400> 12
Met Tyr Phe Leu Cys Leu Ile Trp Thr Glu Ser Gln Pro Pro Val Thr
1 5 10 15
Asn Leu Ser Val Ser Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp
20 25 30
Asn Pro Pro Glu Gly Val Ser Pro Asn Cys Ser Leu Trp Tyr Phe Ser
35 40 45
His Phe Gly Asn Lys Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg
50 55 60
Ser Lys Glu Val Pro Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser
65 70 75 80
Gln Cys Ser Thr Asn Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys
85 90 95
Cys Ile Ser Pro Pro Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu
100 105 110
Gln Cys Val Trp His Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro
115 120 125
Gly Lys Asn Ala Ser Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His
130 135 140
Ser Ser Leu Gly Lys Ile Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly
145 150 155 160
Gln His Ile Gly Cys Ser Phe Ala Leu Thr Glu Val Lys Asp Ser Ile
165 170 175
Phe Glu Gln His Ser Val Gln Ile Met Val Lys Asp Asn Ala Gly Lys
180 185 190
Ile Arg Pro Phe Phe Asn Ile Val Pro Leu Thr Ser His Val Lys Pro
195 200 205
Asp Pro Pro His Ile Lys Lys Leu Phe Phe Gln Asn Gly Asp Leu Tyr
210 215 220
Val Gln Trp Lys Asn Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr
225 230 235 240
Gln Val Glu Val Asn Asn Ser Gln Thr Glu Thr Arg Asp Ile Phe Ser
245 250 255
Val Glu Glu Ala Lys Cys Gln Asn Pro Glu Phe Glu Gly Asp Leu Glu
260 265 270
Gly Thr Ile Cys Phe Met Val Pro Gly Val Leu Pro Asp Thr Val Asn
275 280 285
Thr Val Arg Ile Arg Val Lys Thr Asn Lys Leu Cys Tyr Glu Asp Asp
290 295 300
Lys Leu Trp Ser Asn Trp Ser Gln Ala Met Ser Ile Gly Lys Lys Ala
305 310 315 320
Asp Pro Thr Phe Tyr Ile Ala Met Leu Leu Ile Ile Pro Val Ile Val
325 330 335
Ala Gly Ala Ile Ile Val Leu Leu Leu Tyr Leu Lys Arg Leu Lys Ile
340 345 350
Ile Met Phe Pro Pro Ile Pro Asp Pro Gly Lys Ile Phe Lys Glu Met
355 360 365
Phe Gly Asp Gln Asn Asp Asp Thr Leu His Trp Lys Lys Tyr Asp Ile
370 375 380
Tyr Glu Lys Gln Thr Lys Glu Glu Thr Asp Ser Val Val Leu Ile Glu
385 390 395 400
Asn Leu Lys Arg Ala Ser Gln
405
<210> 13
<211> 761
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL13R-IL4R-Fc (без сигнальной последовательности)
<400> 13
Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro
20 25 30
Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile
165 170 175
Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu
195 200 205
Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Gly Gly Gly Ser Gly
305 310 315 320
Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr
325 330 335
Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys
340 345 350
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu
355 360 365
Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys
370 375 380
Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp
385 390 395 400
Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser
405 410 415
Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn
420 425 430
Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu
435 440 445
Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp
450 455 460
Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro
465 470 475 480
Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser
485 490 495
Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp Ser Asp
500 505 510
Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro Lys Arg Glu
515 520 525
Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala Pro
530 535 540
Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys
545 550 555 560
Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val Val
565 570 575
Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp
580 585 590
Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln Phe
595 600 605
Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp
610 615 620
Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala Leu
625 630 635 640
Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His
645 650 655
Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser Lys
660 665 670
Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Asp
675 680 685
Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys
690 695 700
Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu
705 710 715 720
Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr
725 730 735
Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
740 745 750
Glu Ser Leu Ser His Ser Pro Gly Lys
755 760
<210> 14
<211> 758
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL4R-IL13R-IgGA (без сигнальной последовательности)
<400> 14
Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu
35 40 45
Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys
50 55 60
Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp
65 70 75 80
Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser
85 90 95
Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu
115 120 125
Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp
130 135 140
Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro
145 150 155 160
Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser
165 170 175
Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp Ser Asp
180 185 190
Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro Gly Gly Gly
195 200 205
Ser Gly Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val
210 215 220
Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala
225 230 235 240
Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln
245 250 255
Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu
260 265 270
Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu
275 280 285
Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu
290 295 300
Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn
305 310 315 320
Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro
325 330 335
Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile
340 345 350
Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser
355 360 365
Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val
370 375 380
Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn
385 390 395 400
Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys
405 410 415
Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro
420 425 430
Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn
435 440 445
Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys
450 455 460
Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met
465 470 475 480
Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val
485 490 495
Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp
500 505 510
Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Phe Asn Glu
515 520 525
Cys Arg Cys Thr Asp Thr Pro Pro Cys Pro Val Pro Glu Pro Leu Gly
530 535 540
Gly Pro Ser Val Leu Ile Phe Pro Pro Lys Pro Lys Asp Ile Leu Arg
545 550 555 560
Ile Thr Arg Thr Pro Glu Val Thr Cys Val Val Leu Asp Leu Gly Arg
565 570 575
Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Glu Val
580 585 590
His Thr Ala Lys Thr Gln Ser Arg Glu Gln Gln Phe Asn Gly Thr Tyr
595 600 605
Arg Val Val Ser Val Leu Pro Ile Glu His Gln Asp Trp Leu Thr Gly
610 615 620
Lys Glu Phe Lys Cys Arg Val Asn His Ile Asp Leu Pro Ser Pro Ile
625 630 635 640
Glu Arg Thr Ile Ser Lys Ala Arg Gly Arg Ala His Lys Pro Ser Val
645 650 655
Tyr Val Leu Pro Pro Ser Pro Lys Glu Leu Ser Ser Ser Asp Thr Val
660 665 670
Ser Ile Thr Cys Leu Ile Lys Asp Phe Tyr Pro Pro Asp Ile Asp Val
675 680 685
Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Arg Lys His Arg Met
690 695 700
Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys
705 710 715 720
Leu Ser Val Asp Lys Ser Arg Trp Gln Gln Gly Asp Pro Phe Thr Cys
725 730 735
Ala Val Met His Glu Thr Leu Gln Asn His Tyr Thr Asp Leu Ser Leu
740 745 750
Ser His Ser Pro Gly Lys
755
<210> 15
<211> 762
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL4R-IL13R-IgGB (без сигнальной последовательности)
<400> 15
Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu
35 40 45
Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys
50 55 60
Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp
65 70 75 80
Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser
85 90 95
Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu
115 120 125
Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp
130 135 140
Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro
145 150 155 160
Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser
165 170 175
Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp Ser Asp
180 185 190
Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro Gly Gly Gly
195 200 205
Ser Gly Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val
210 215 220
Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala
225 230 235 240
Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln
245 250 255
Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu
260 265 270
Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu
275 280 285
Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu
290 295 300
Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn
305 310 315 320
Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro
325 330 335
Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile
340 345 350
Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser
355 360 365
Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val
370 375 380
Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn
385 390 395 400
Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys
405 410 415
Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro
420 425 430
Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn
435 440 445
Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys
450 455 460
Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met
465 470 475 480
Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val
485 490 495
Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp
500 505 510
Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Pro Lys Arg
515 520 525
Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys Pro Ala
530 535 540
Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro
545 550 555 560
Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys Val Val
565 570 575
Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val
580 585 590
Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu Glu Gln
595 600 605
Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln
610 615 620
Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn Lys Ala
625 630 635 640
Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala
645 650 655
His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu Leu Ser
660 665 670
Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro
675 680 685
Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser
690 695 700
Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe
705 710 715 720
Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp
725 730 735
Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr
740 745 750
Gln Glu Ser Leu Ser His Ser Pro Gly Lys
755 760
<210> 16
<211> 760
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL4R-IL13R-IgGC (без сигнальной последовательности)
<400> 16
Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu
35 40 45
Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys
50 55 60
Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp
65 70 75 80
Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser
85 90 95
Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu
115 120 125
Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp
130 135 140
Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro
145 150 155 160
Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser
165 170 175
Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp Ser Asp
180 185 190
Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro Gly Gly Gly
195 200 205
Ser Gly Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val
210 215 220
Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala
225 230 235 240
Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln
245 250 255
Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu
260 265 270
Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu
275 280 285
Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu
290 295 300
Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn
305 310 315 320
Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro
325 330 335
Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile
340 345 350
Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser
355 360 365
Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val
370 375 380
Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn
385 390 395 400
Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys
405 410 415
Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro
420 425 430
Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn
435 440 445
Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys
450 455 460
Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met
465 470 475 480
Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val
485 490 495
Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp
500 505 510
Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Ala Lys Glu
515 520 525
Cys Glu Cys Lys Cys Asn Cys Asn Asn Cys Pro Cys Pro Gly Cys Gly
530 535 540
Leu Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp
545 550 555 560
Ile Leu Val Thr Ala Arg Thr Pro Thr Val Thr Cys Val Val Val Asp
565 570 575
Leu Asp Pro Glu Asn Pro Glu Val Gln Ile Ser Trp Phe Val Asp Ser
580 585 590
Lys Gln Val Gln Thr Ala Asn Thr Gln Pro Arg Glu Glu Gln Ser Asn
595 600 605
Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly His Gln Asp Trp
610 615 620
Leu Ser Gly Lys Gln Phe Lys Cys Lys Val Asn Asn Lys Ala Leu Pro
625 630 635 640
Ser Pro Ile Glu Glu Ile Ile Ser Lys Thr Pro Gly Gln Ala His Gln
645 650 655
Pro Asn Val Tyr Val Leu Pro Pro Ser Arg Asp Glu Met Ser Lys Asn
660 665 670
Thr Val Thr Leu Thr Cys Leu Val Lys Asp Phe Phe Pro Pro Glu Ile
675 680 685
Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro Glu Ser Lys Tyr
690 695 700
Arg Met Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr
705 710 715 720
Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg Gly Asp Thr Phe
725 730 735
Ile Cys Ala Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Ile
740 745 750
Ser Leu Ser His Ser Pro Gly Lys
755 760
<210> 17
<211> 758
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL4R-IL13R-IgGD (без сигнальной последовательности)
<400> 17
Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu
35 40 45
Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys
50 55 60
Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp
65 70 75 80
Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser
85 90 95
Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu
115 120 125
Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp
130 135 140
Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro
145 150 155 160
Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser
165 170 175
Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp Ser Asp
180 185 190
Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro Gly Gly Gly
195 200 205
Ser Gly Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val
210 215 220
Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala
225 230 235 240
Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln
245 250 255
Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu
260 265 270
Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu
275 280 285
Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu
290 295 300
Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn
305 310 315 320
Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro
325 330 335
Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile
340 345 350
Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser
355 360 365
Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val
370 375 380
Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn
385 390 395 400
Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys
405 410 415
Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro
420 425 430
Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn
435 440 445
Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys
450 455 460
Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met
465 470 475 480
Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val
485 490 495
Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp
500 505 510
Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Pro Lys Glu
515 520 525
Ser Thr Cys Lys Cys Ile Ser Pro Cys Pro Val Pro Glu Ser Leu Gly
530 535 540
Gly Pro Ser Val Phe Ile Phe Pro Pro Lys Pro Lys Asp Ile Leu Arg
545 550 555 560
Ile Thr Arg Thr Pro Glu Ile Thr Cys Val Val Leu Asp Leu Gly Arg
565 570 575
Glu Asp Pro Glu Val Gln Ile Ser Trp Phe Val Asp Gly Lys Glu Val
580 585 590
His Thr Ala Lys Thr Gln Pro Arg Glu Gln Gln Phe Asn Ser Thr Tyr
595 600 605
Arg Val Val Ser Val Leu Pro Ile Glu His Gln Asp Trp Leu Thr Gly
610 615 620
Lys Glu Phe Lys Cys Arg Val Asn His Ile Gly Leu Pro Ser Pro Ile
625 630 635 640
Glu Arg Thr Ile Ser Lys Ala Arg Gly Gln Ala His Gln Pro Ser Val
645 650 655
Tyr Val Leu Pro Pro Ser Pro Lys Glu Leu Ser Ser Ser Asp Thr Val
660 665 670
Thr Leu Thr Cys Leu Ile Lys Asp Phe Phe Pro Pro Glu Ile Asp Val
675 680 685
Glu Trp Gln Ser Asn Gly Gln Pro Glu Pro Glu Ser Lys Tyr His Thr
690 695 700
Thr Ala Pro Gln Leu Asp Glu Asp Gly Ser Tyr Phe Leu Tyr Ser Lys
705 710 715 720
Leu Ser Val Asp Lys Ser Arg Trp Gln Gln Gly Asp Thr Phe Thr Cys
725 730 735
Ala Val Met His Glu Ala Leu Gln Asn His Tyr Thr Asp Leu Ser Leu
740 745 750
Ser His Ser Pro Gly Lys
755
<210> 18
<211> 590
<212> белок
<213> Искусственная последовательность
<220>
<223> Felis catus, IL4R-IL13R (без сигнальной последовательности)
<400> 18
Ser Gly Ser Val Lys Val Leu Arg Ala Pro Thr Cys Phe Ser Asp Tyr
1 5 10 15
Phe Ser Thr Ser Val Cys Gln Trp Asn Met Asp Ala Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asn Phe Met Gly Ser Glu
35 40 45
Asn Arg Thr Cys Val Pro Glu Asn Gly Glu Gly Ala Ala Cys Ala Cys
50 55 60
Ser Met Leu Met Asp Asp Phe Val Glu Ala Asp Val Tyr Gln Leu His
65 70 75 80
Leu Trp Ala Gly Thr Gln Leu Leu Trp Ser Gly Ser Phe Lys Pro Ser
85 90 95
Ser His Val Lys Pro Arg Ala Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Val Ser His Thr Trp Leu Leu Arg Trp Ser Asn Pro Tyr Pro Pro Glu
115 120 125
Asn His Leu His Ala Glu Leu Thr Tyr Met Val Asn Ile Ser Ser Glu
130 135 140
Asp Asp Pro Thr Asp Val Ser Val Cys Ala Ser Gly Phe Leu Cys His
145 150 155 160
Leu Leu Gly Leu Arg Arg Val Glu Thr Gly Ala Pro Gly Ala Arg Leu
165 170 175
Pro Pro Trp Leu Cys Ala Pro Arg Pro Arg Arg Val Pro Gly Ser Gln
180 185 190
Cys Ala Val Ile Ser Cys Cys Arg Trp Val Leu Ile Ala Leu Thr Ser
195 200 205
Arg Gly Gly Arg Trp Arg Leu Thr Pro Gly Leu Arg Ser Gln Thr Arg
210 215 220
Tyr Val Ser Val Ala Glu Gly Leu Phe Gly Ala Thr Pro Arg Val Leu
225 230 235 240
Cys Pro Gly Thr Gln Ala Gly Leu Ala Ser Ala Ala Arg Glu Gln Met
245 250 255
Ser Pro Asp Pro Ser Ala Phe His Ser Ile Asp Tyr Glu Pro Gly Gly
260 265 270
Gly Ser Gly Ser Gln Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser
275 280 285
Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly
290 295 300
Ala Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys
305 310 315 320
Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro
325 330 335
Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn
340 345 350
Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro
355 360 365
Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His
370 375 380
Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser
385 390 395 400
Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys
405 410 415
Ile Leu Gln Cys Glu Asn Ile Tyr Arg Glu Gly Gln His Ile Gly Cys
420 425 430
Ser Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser
435 440 445
Val Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe
450 455 460
Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile
465 470 475 480
Lys Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn
485 490 495
Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn
500 505 510
Asn Ser Gln Thr Glu Thr His Asp Ile Phe Tyr Val Glu Glu Ala Lys
515 520 525
Cys Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe
530 535 540
Met Val Pro Gly Ile Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg
545 550 555 560
Val Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Arg Leu Trp Ser Asn
565 570 575
Trp Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr
580 585 590
<210> 19
<211> 525
<212> белок
<213> Искусственная последовательность
<220>
<223> Equus caballus, IL4R-IL13R (без сигнальной последовательности)
<400> 19
Ser Gly Ser Val Lys Val Leu His Leu Thr Ala Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Ala Ser Thr Cys Glu Trp Lys Met Asp Arg Pro Thr Asn Cys
20 25 30
Ser Ala Gln Leu Arg Leu Ser Tyr Gln Leu Asn Asp Glu Phe Ser Asp
35 40 45
Asn Leu Thr Cys Ile Pro Glu Asn Arg Glu Asp Glu Val Cys Val Cys
50 55 60
Arg Met Leu Met Asp Asn Ile Val Ser Glu Asp Val Tyr Glu Leu Asp
65 70 75 80
Leu Trp Ala Gly Asn Gln Leu Leu Trp Asn Ser Ser Phe Lys Pro Ser
85 90 95
Arg His Val Lys Pro Arg Ala Pro Gln Asn Leu Thr Val His Ala Ile
100 105 110
Ser His Thr Trp Leu Leu Thr Trp Ser Asn Pro Tyr Pro Leu Lys Asn
115 120 125
His Leu Trp Ser Glu Leu Thr Tyr Leu Val Asn Ile Ser Lys Glu Asp
130 135 140
Asp Pro Thr Asp Phe Lys Ile Tyr Asn Val Thr Tyr Met Asp Pro Thr
145 150 155 160
Leu Arg Val Thr Ala Ser Thr Leu Lys Ser Arg Ala Thr Tyr Ser Ala
165 170 175
Arg Val Lys Ala Arg Ala Gln Asn Tyr Asn Ser Thr Trp Ser Glu Trp
180 185 190
Ser Pro Ser Thr Thr Trp His Asn Tyr Tyr Glu Gln Pro Gly Gly Gly
195 200 205
Ser Gly Thr Glu Ser Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val
210 215 220
Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asn Pro Pro Glu Gly Val
225 230 235 240
Ser Pro Asn Cys Ser Leu Trp Tyr Phe Ser His Phe Gly Asn Lys Gln
245 250 255
Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu
260 265 270
Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu
275 280 285
Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Ile Ser Pro Pro Glu
290 295 300
Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn
305 310 315 320
Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Lys Asn Ala Ser Pro
325 330 335
Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile
340 345 350
Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser
355 360 365
Phe Ala Leu Thr Glu Val Lys Asp Ser Ile Phe Glu Gln His Ser Val
370 375 380
Gln Ile Met Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Phe Phe Asn
385 390 395 400
Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys
405 410 415
Lys Leu Phe Phe Gln Asn Gly Asp Leu Tyr Val Gln Trp Lys Asn Pro
420 425 430
Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn
435 440 445
Ser Gln Thr Glu Thr Arg Asp Ile Phe Ser Val Glu Glu Ala Lys Cys
450 455 460
Gln Asn Pro Glu Phe Glu Gly Asp Leu Glu Gly Thr Ile Cys Phe Met
465 470 475 480
Val Pro Gly Val Leu Pro Asp Thr Val Asn Thr Val Arg Ile Arg Val
485 490 495
Lys Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp
500 505 510
Ser Gln Ala Met Ser Ile Gly Lys Lys Ala Asp Pro Thr
515 520 525
<210> 20
<211> 780
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL13R-IL4R-IgGB (с сигнальной последовательностью)
<400> 20
Met Ala Val Leu Gly Leu Leu Phe Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser
20 25 30
Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly
35 40 45
Ala Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys
50 55 60
Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro
65 70 75 80
Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn
85 90 95
Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro
100 105 110
Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His
115 120 125
Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser
130 135 140
Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys
145 150 155 160
Ile Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys
165 170 175
Ser Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser
180 185 190
Val Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe
195 200 205
Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile
210 215 220
Lys Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn
225 230 235 240
Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn
245 250 255
Asn Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys
260 265 270
Cys Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe
275 280 285
Met Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg
290 295 300
Val Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn
305 310 315 320
Trp Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Gly Gly
325 330 335
Gly Ser Gly Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe
340 345 350
Ser Asp Tyr Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro
355 360 365
Thr Asn Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met
370 375 380
Gly Ser Glu Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val
385 390 395 400
Cys Val Cys Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr
405 410 415
Gln Leu Asp Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe
420 425 430
Gln Pro Ser Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val
435 440 445
His Pro Asn Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr
450 455 460
Pro Thr Glu Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val
465 470 475 480
Ser Asn Asp Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr
485 490 495
Met Gly Pro Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala
500 505 510
Ser Tyr Ser Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr
515 520 525
Trp Ser Asp Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro
530 535 540
Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys Cys
545 550 555 560
Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro Pro
565 570 575
Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr Cys
580 585 590
Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser Trp
595 600 605
Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg Glu
610 615 620
Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile Gly
625 630 635 640
His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn Asn
645 650 655
Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg Gly
660 665 670
Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu Glu
675 680 685
Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe Phe
690 695 700
Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu Pro
705 710 715 720
Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly Ser
725 730 735
Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln Arg
740 745 750
Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn His
755 760 765
Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
770 775 780
<210> 21
<211> 781
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, IL4R-IL13R-IgGB (с сигнальной последовательностью)
<400> 21
Met Ala Val Leu Gly Leu Leu Phe Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe
20 25 30
Ser Asp Tyr Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro
35 40 45
Thr Asn Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met
50 55 60
Gly Ser Glu Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val
65 70 75 80
Cys Val Cys Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr
85 90 95
Gln Leu Asp Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe
100 105 110
Gln Pro Ser Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val
115 120 125
His Pro Asn Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr
130 135 140
Pro Thr Glu Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val
145 150 155 160
Ser Asn Asp Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr
165 170 175
Met Gly Pro Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala
180 185 190
Ser Tyr Ser Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr
195 200 205
Trp Ser Asp Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro
210 215 220
Gly Gly Gly Ser Gly Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser
225 230 235 240
Val Ser Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro
245 250 255
Glu Gly Ala Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp
260 265 270
Asn Lys Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu
275 280 285
Val Pro Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser
290 295 300
Thr Asn Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro
305 310 315 320
Pro Pro Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val
325 330 335
Trp His Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn
340 345 350
Thr Ser Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu
355 360 365
Gly Lys Ile Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile
370 375 380
Gly Cys Ser Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln
385 390 395 400
His Ser Val Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro
405 410 415
Ser Phe Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro
420 425 430
His Ile Lys Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp
435 440 445
Lys Asn Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu
450 455 460
Val Asn Asn Ser Gln Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu
465 470 475 480
Ala Lys Cys Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile
485 490 495
Cys Phe Met Val Pro Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg
500 505 510
Ile Arg Val Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp
515 520 525
Ser Asn Trp Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr
530 535 540
Pro Lys Arg Glu Asn Gly Arg Val Pro Arg Pro Pro Asp Cys Pro Lys
545 550 555 560
Cys Pro Ala Pro Glu Met Leu Gly Gly Pro Ser Val Phe Ile Phe Pro
565 570 575
Pro Lys Pro Lys Asp Thr Leu Leu Ile Ala Arg Thr Pro Glu Val Thr
580 585 590
Cys Val Val Val Asp Leu Asp Pro Glu Asp Pro Glu Val Gln Ile Ser
595 600 605
Trp Phe Val Asp Gly Lys Gln Met Gln Thr Ala Lys Thr Gln Pro Arg
610 615 620
Glu Glu Gln Phe Asn Gly Thr Tyr Arg Val Val Ser Val Leu Pro Ile
625 630 635 640
Gly His Gln Asp Trp Leu Lys Gly Lys Gln Phe Thr Cys Lys Val Asn
645 650 655
Asn Lys Ala Leu Pro Ser Pro Ile Glu Arg Thr Ile Ser Lys Ala Arg
660 665 670
Gly Gln Ala His Gln Pro Ser Val Tyr Val Leu Pro Pro Ser Arg Glu
675 680 685
Glu Leu Ser Lys Asn Thr Val Ser Leu Thr Cys Leu Ile Lys Asp Phe
690 695 700
Phe Pro Pro Asp Ile Asp Val Glu Trp Gln Ser Asn Gly Gln Gln Glu
705 710 715 720
Pro Glu Ser Lys Tyr Arg Thr Thr Pro Pro Gln Leu Asp Glu Asp Gly
725 730 735
Ser Tyr Phe Leu Tyr Ser Lys Leu Ser Val Asp Lys Ser Arg Trp Gln
740 745 750
Arg Gly Asp Thr Phe Ile Cys Ala Val Met His Glu Ala Leu His Asn
755 760 765
His Tyr Thr Gln Glu Ser Leu Ser His Ser Pro Gly Lys
770 775 780
<210> 22
<211> 315
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, внеклеточный домен IL13R (без сигнальной последовательности)
<400> 22
Thr Glu Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro
20 25 30
Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile
165 170 175
Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu
195 200 205
Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Val Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr
305 310 315
<210> 23
<211> 207
<212> белок
<213> Искусственная последовательность
<220>
<223> Canis lupus, внеклеточный домен IL4R (без сигнальной последовательности)
<400> 23
Ser Gly Ser Gly Ser Val Lys Val Leu His Glu Pro Ser Cys Phe Ser
1 5 10 15
Asp Tyr Ile Ser Thr Ser Val Cys Gln Trp Lys Met Asp His Pro Thr
20 25 30
Asn Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly
35 40 45
Ser Glu Asn His Thr Cys Val Pro Glu Asn Arg Glu Asp Ser Val Cys
50 55 60
Val Cys Ser Met Pro Ile Asp Asp Ala Val Glu Ala Asp Val Tyr Gln
65 70 75 80
Leu Asp Leu Trp Ala Gly Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln
85 90 95
Pro Ser Lys His Val Lys Pro Arg Thr Pro Gly Asn Leu Thr Val His
100 105 110
Pro Asn Ile Ser His Thr Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro
115 120 125
Thr Glu Asn His Leu His Ser Glu Leu Thr Tyr Met Val Asn Val Ser
130 135 140
Asn Asp Asn Asp Pro Glu Asp Phe Lys Val Tyr Asn Val Thr Tyr Met
145 150 155 160
Gly Pro Thr Leu Arg Leu Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser
165 170 175
Tyr Ser Ala Arg Val Arg Ala Trp Ala Gln Thr Tyr Asn Ser Thr Trp
180 185 190
Ser Asp Trp Ser Pro Ser Thr Thr Trp Leu Asn Tyr Tyr Glu Pro
195 200 205
<210> 24
<211> 315
<212> белок
<213> Искусственная последовательность
<220>
<223> Felis catus, внеклеточный домен IL13R (без сигнальной последовательности)
<400> 24
Ser Gln Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro
20 25 30
Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asn Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile
165 170 175
Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu
195 200 205
Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr His Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Ile Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Arg Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr
305 310 315
<210> 25
<211> 270
<212> белок
<213> Искусственная последовательность
<220>
<223> Felis catus, внеклеточный домен IL4R (без сигнальной последовательности)
<400> 25
Ser Gly Ser Val Lys Val Leu Arg Ala Pro Thr Cys Phe Ser Asp Tyr
1 5 10 15
Phe Ser Thr Ser Val Cys Gln Trp Asn Met Asp Ala Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asn Phe Met Gly Ser Glu
35 40 45
Asn Arg Thr Cys Val Pro Glu Asn Gly Glu Gly Ala Ala Cys Ala Cys
50 55 60
Ser Met Leu Met Asp Asp Phe Val Glu Ala Asp Val Tyr Gln Leu His
65 70 75 80
Leu Trp Ala Gly Thr Gln Leu Leu Trp Ser Gly Ser Phe Lys Pro Ser
85 90 95
Ser His Val Lys Pro Arg Ala Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Val Ser His Thr Trp Leu Leu Arg Trp Ser Asn Pro Tyr Pro Pro Glu
115 120 125
Asn His Leu His Ala Glu Leu Thr Tyr Met Val Asn Ile Ser Ser Glu
130 135 140
Asp Asp Pro Thr Asp Val Ser Val Cys Ala Ser Gly Phe Leu Cys His
145 150 155 160
Leu Leu Gly Leu Arg Arg Val Glu Thr Gly Ala Pro Gly Ala Arg Leu
165 170 175
Pro Pro Trp Leu Cys Ala Pro Arg Pro Arg Arg Val Pro Gly Ser Gln
180 185 190
Cys Ala Val Ile Ser Cys Cys Arg Trp Val Leu Ile Ala Leu Thr Ser
195 200 205
Arg Gly Gly Arg Trp Arg Leu Thr Pro Gly Leu Arg Ser Gln Thr Arg
210 215 220
Tyr Val Ser Val Ala Glu Gly Leu Phe Gly Ala Thr Pro Arg Val Leu
225 230 235 240
Cys Pro Gly Thr Gln Ala Gly Leu Ala Ser Ala Ala Arg Glu Gln Met
245 250 255
Ser Pro Asp Pro Ser Ala Phe His Ser Ile Asp Tyr Glu Pro
260 265 270
<210> 26
<211> 315
<212> белок
<213> Искусственная последовательность
<220>
<223> Equus caballus, внеклеточный домен IL13R (без сигнальной последовательности)
<400> 26
Thr Glu Ser Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asn Pro Pro Glu Gly Val Ser Pro
20 25 30
Asn Cys Ser Leu Trp Tyr Phe Ser His Phe Gly Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Ile Ser Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Lys Asn Ala Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Glu Val Lys Asp Ser Ile Phe Glu Gln His Ser Val Gln Ile
165 170 175
Met Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Phe Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Lys Leu
195 200 205
Phe Phe Gln Asn Gly Asp Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr Arg Asp Ile Phe Ser Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Pro Glu Phe Glu Gly Asp Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Val Leu Pro Asp Thr Val Asn Thr Val Arg Ile Arg Val Lys Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Lys Lys Ala Asp Pro Thr
305 310 315
<210> 27
<211> 205
<212> белок
<213> Искусственная последовательность
<220>
<223> Equus caballus, внеклеточный домен IL4R (без сигнальной последовательности)
<400> 27
Ser Gly Ser Val Lys Val Leu His Leu Thr Ala Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Ala Ser Thr Cys Glu Trp Lys Met Asp Arg Pro Thr Asn Cys
20 25 30
Ser Ala Gln Leu Arg Leu Ser Tyr Gln Leu Asn Asp Glu Phe Ser Asp
35 40 45
Asn Leu Thr Cys Ile Pro Glu Asn Arg Glu Asp Glu Val Cys Val Cys
50 55 60
Arg Met Leu Met Asp Asn Ile Val Ser Glu Asp Val Tyr Glu Leu Asp
65 70 75 80
Leu Trp Ala Gly Asn Gln Leu Leu Trp Asn Ser Ser Phe Lys Pro Ser
85 90 95
Arg His Val Lys Pro Arg Ala Pro Gln Asn Leu Thr Val His Ala Ile
100 105 110
Ser His Thr Trp Leu Leu Thr Trp Ser Asn Pro Tyr Pro Leu Lys Asn
115 120 125
His Leu Trp Ser Glu Leu Thr Tyr Leu Val Asn Ile Ser Lys Glu Asp
130 135 140
Asp Pro Thr Asp Phe Lys Ile Tyr Asn Val Thr Tyr Met Asp Pro Thr
145 150 155 160
Leu Arg Val Thr Ala Ser Thr Leu Lys Ser Arg Ala Thr Tyr Ser Ala
165 170 175
Arg Val Lys Ala Arg Ala Gln Asn Tyr Asn Ser Thr Trp Ser Glu Trp
180 185 190
Ser Pro Ser Thr Thr Trp His Asn Tyr Tyr Glu Gln Pro
195 200 205
<210> 28
<211> 829
<212> белок
<213> Искусственная последовательность
<220>
<223> IL13R-IL4R-IgG2 кошачьих (без сигнальной последовательности)
<400> 28
Ser Gln Thr Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro
20 25 30
Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asn Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile
165 170 175
Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu
195 200 205
Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr His Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Ile Leu Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Arg Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Gly Gly Gly Ser Gly
305 310 315 320
Ser Ser Gly Ser Val Lys Val Leu Arg Ala Pro Thr Cys Phe Ser Asp
325 330 335
Tyr Phe Ser Thr Ser Val Cys Gln Trp Asn Met Asp Ala Pro Thr Asn
340 345 350
Cys Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asn Phe Met Gly Ser
355 360 365
Glu Asn Arg Thr Cys Val Pro Glu Asn Gly Glu Gly Ala Ala Cys Ala
370 375 380
Cys Ser Met Leu Met Asp Asp Phe Val Glu Ala Asp Val Tyr Gln Leu
385 390 395 400
His Leu Trp Ala Gly Thr Gln Leu Leu Trp Ser Gly Ser Phe Lys Pro
405 410 415
Ser Ser His Val Lys Pro Arg Ala Pro Gly Asn Leu Thr Val His Pro
420 425 430
Asn Val Ser His Thr Trp Leu Leu Arg Trp Ser Asn Pro Tyr Pro Pro
435 440 445
Glu Asn His Leu His Ala Glu Leu Thr Tyr Met Val Asn Ile Ser Ser
450 455 460
Glu Asp Asp Pro Thr Asp Val Ser Val Cys Ala Ser Gly Phe Leu Cys
465 470 475 480
His Leu Leu Gly Leu Arg Arg Val Glu Thr Gly Ala Pro Gly Ala Arg
485 490 495
Leu Pro Pro Trp Leu Cys Ala Pro Arg Pro Arg Arg Val Pro Gly Ser
500 505 510
Gln Cys Ala Val Ile Ser Cys Cys Arg Trp Val Leu Ile Ala Leu Thr
515 520 525
Ser Arg Gly Gly Arg Trp Arg Leu Thr Pro Gly Leu Arg Ser Gln Thr
530 535 540
Arg Tyr Val Ser Val Ala Glu Gly Leu Phe Gly Ala Thr Pro Arg Val
545 550 555 560
Leu Cys Pro Gly Thr Gln Ala Gly Leu Ala Ser Ala Ala Arg Glu Gln
565 570 575
Met Ser Pro Asp Pro Ser Ala Phe His Ser Ile Asp Tyr Glu Pro Ser
580 585 590
Pro Lys Thr Ala Ser Thr Ile Glu Ser Lys Thr Gly Glu Cys Pro Lys
595 600 605
Cys Pro Val Pro Glu Ile Pro Gly Ala Pro Ser Val Phe Ile Phe Pro
610 615 620
Pro Lys Pro Lys Asp Thr Leu Ser Ile Ser Arg Thr Pro Glu Val Thr
625 630 635 640
Cys Leu Val Val Asp Leu Gly Pro Asp Asp Ser Asn Val Gln Ile Thr
645 650 655
Trp Phe Val Asp Asn Thr Glu Met His Thr Ala Lys Thr Arg Pro Arg
660 665 670
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Pro Ile
675 680 685
Leu His Gln Asp Trp Leu Lys Gly Lys Glu Phe Lys Cys Lys Val Asn
690 695 700
Ser Lys Ser Leu Pro Ser Ala Met Glu Arg Thr Ile Ser Lys Ala Lys
705 710 715 720
Gly Gln Pro His Glu Pro Gln Val Tyr Val Leu Pro Pro Thr Gln Glu
725 730 735
Glu Leu Ser Glu Asn Lys Val Ser Val Thr Cys Leu Ile Lys Gly Phe
740 745 750
His Pro Pro Asp Ile Ala Val Glu Trp Glu Ile Thr Gly Gln Pro Glu
755 760 765
Pro Glu Asn Asn Tyr Gln Thr Thr Pro Pro Gln Leu Asp Ser Asp Gly
770 775 780
Thr Tyr Phe Leu Tyr Ser Arg Leu Ser Val Asp Arg Ser His Trp Gln
785 790 795 800
Arg Gly Asn Thr Tyr Thr Cys Ser Val Ser His Glu Ala Leu His Ser
805 810 815
His His Thr Gln Lys Ser Leu Thr Gln Ser Pro Gly Lys
820 825
<210> 29
<211> 829
<212> белок
<213> Искусственная последовательность
<220>
<223> IL4R-IL13R-IgG2 кошачьих (без сигнальной последовательности)
<400> 29
Ser Gly Ser Val Lys Val Leu Arg Ala Pro Thr Cys Phe Ser Asp Tyr
1 5 10 15
Phe Ser Thr Ser Val Cys Gln Trp Asn Met Asp Ala Pro Thr Asn Cys
20 25 30
Ser Ala Glu Leu Arg Leu Ser Tyr Gln Leu Asn Phe Met Gly Ser Glu
35 40 45
Asn Arg Thr Cys Val Pro Glu Asn Gly Glu Gly Ala Ala Cys Ala Cys
50 55 60
Ser Met Leu Met Asp Asp Phe Val Glu Ala Asp Val Tyr Gln Leu His
65 70 75 80
Leu Trp Ala Gly Thr Gln Leu Leu Trp Ser Gly Ser Phe Lys Pro Ser
85 90 95
Ser His Val Lys Pro Arg Ala Pro Gly Asn Leu Thr Val His Pro Asn
100 105 110
Val Ser His Thr Trp Leu Leu Arg Trp Ser Asn Pro Tyr Pro Pro Glu
115 120 125
Asn His Leu His Ala Glu Leu Thr Tyr Met Val Asn Ile Ser Ser Glu
130 135 140
Asp Asp Pro Thr Asp Val Ser Val Cys Ala Ser Gly Phe Leu Cys His
145 150 155 160
Leu Leu Gly Leu Arg Arg Val Glu Thr Gly Ala Pro Gly Ala Arg Leu
165 170 175
Pro Pro Trp Leu Cys Ala Pro Arg Pro Arg Arg Val Pro Gly Ser Gln
180 185 190
Cys Ala Val Ile Ser Cys Cys Arg Trp Val Leu Ile Ala Leu Thr Ser
195 200 205
Arg Gly Gly Arg Trp Arg Leu Thr Pro Gly Leu Arg Ser Gln Thr Arg
210 215 220
Tyr Val Ser Val Ala Glu Gly Leu Phe Gly Ala Thr Pro Arg Val Leu
225 230 235 240
Cys Pro Gly Thr Gln Ala Gly Leu Ala Ser Ala Ala Arg Glu Gln Met
245 250 255
Ser Pro Asp Pro Ser Ala Phe His Ser Ile Asp Tyr Glu Pro Gly Gly
260 265 270
Gly Ser Gly Ser Ser Gln Thr Gln Pro Pro Val Thr Asn Leu Ser Val
275 280 285
Ser Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asp Pro Pro Glu
290 295 300
Gly Ala Ser Pro Asn Cys Thr Leu Arg Tyr Phe Ser His Phe Asp Asn
305 310 315 320
Lys Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val
325 330 335
Pro Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr
340 345 350
Asn Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Thr Pro Pro
355 360 365
Pro Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp
370 375 380
His Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Arg Asn Thr
385 390 395 400
Ser Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly
405 410 415
Lys Ile Leu Gln Cys Glu Asn Ile Tyr Arg Glu Gly Gln His Ile Gly
420 425 430
Cys Ser Phe Ala Leu Thr Asn Leu Lys Asp Ser Ser Phe Glu Gln His
435 440 445
Ser Val Gln Ile Val Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Ser
450 455 460
Phe Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His
465 470 475 480
Ile Lys Arg Leu Phe Phe Gln Asn Gly Asn Leu Tyr Val Gln Trp Lys
485 490 495
Asn Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val
500 505 510
Asn Asn Ser Gln Thr Glu Thr His Asp Ile Phe Tyr Val Glu Glu Ala
515 520 525
Lys Cys Gln Asn Ser Glu Phe Glu Gly Asn Leu Glu Gly Thr Ile Cys
530 535 540
Phe Met Val Pro Gly Ile Leu Pro Asp Thr Leu Asn Thr Val Arg Ile
545 550 555 560
Arg Val Arg Thr Asn Lys Leu Cys Tyr Glu Asp Asp Arg Leu Trp Ser
565 570 575
Asn Trp Ser Gln Ala Met Ser Ile Gly Glu Asn Thr Asp Pro Thr Ser
580 585 590
Pro Lys Thr Ala Ser Thr Ile Glu Ser Lys Thr Gly Glu Cys Pro Lys
595 600 605
Cys Pro Val Pro Glu Ile Pro Gly Ala Pro Ser Val Phe Ile Phe Pro
610 615 620
Pro Lys Pro Lys Asp Thr Leu Ser Ile Ser Arg Thr Pro Glu Val Thr
625 630 635 640
Cys Leu Val Val Asp Leu Gly Pro Asp Asp Ser Asn Val Gln Ile Thr
645 650 655
Trp Phe Val Asp Asn Thr Glu Met His Thr Ala Lys Thr Arg Pro Arg
660 665 670
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Pro Ile
675 680 685
Leu His Gln Asp Trp Leu Lys Gly Lys Glu Phe Lys Cys Lys Val Asn
690 695 700
Ser Lys Ser Leu Pro Ser Ala Met Glu Arg Thr Ile Ser Lys Ala Lys
705 710 715 720
Gly Gln Pro His Glu Pro Gln Val Tyr Val Leu Pro Pro Thr Gln Glu
725 730 735
Glu Leu Ser Glu Asn Lys Val Ser Val Thr Cys Leu Ile Lys Gly Phe
740 745 750
His Pro Pro Asp Ile Ala Val Glu Trp Glu Ile Thr Gly Gln Pro Glu
755 760 765
Pro Glu Asn Asn Tyr Gln Thr Thr Pro Pro Gln Leu Asp Ser Asp Gly
770 775 780
Thr Tyr Phe Leu Tyr Ser Arg Leu Ser Val Asp Arg Ser His Trp Gln
785 790 795 800
Arg Gly Asn Thr Tyr Thr Cys Ser Val Ser His Glu Ala Leu His Ser
805 810 815
His His Thr Gln Lys Ser Leu Thr Gln Ser Pro Gly Lys
820 825
<210> 30
<211> 754
<212> белок
<213> Искусственная последовательность
<220>
<223> IL13R-IL4R-IgG2 лошадиных (без сигнальной последовательности)
<400> 30
Thr Glu Ser Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn
1 5 10 15
Leu Cys Thr Val Ile Trp Thr Trp Asn Pro Pro Glu Gly Val Ser Pro
20 25 30
Asn Cys Ser Leu Trp Tyr Phe Ser His Phe Gly Asn Lys Gln Asp Lys
35 40 45
Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu
50 55 60
Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp
65 70 75 80
Asn Pro Ser Ile Leu Val Glu Lys Cys Ile Ser Pro Pro Glu Gly Asp
85 90 95
Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser
100 105 110
Tyr Met Lys Cys Thr Trp Leu Pro Gly Lys Asn Ala Ser Pro Asp Thr
115 120 125
Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln
130 135 140
Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala
145 150 155 160
Leu Thr Glu Val Lys Asp Ser Ile Phe Glu Gln His Ser Val Gln Ile
165 170 175
Met Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Phe Phe Asn Ile Val
180 185 190
Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile Lys Lys Leu
195 200 205
Phe Phe Gln Asn Gly Asp Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn
210 215 220
Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln
225 230 235 240
Thr Glu Thr Arg Asp Ile Phe Ser Val Glu Glu Ala Lys Cys Gln Asn
245 250 255
Pro Glu Phe Glu Gly Asp Leu Glu Gly Thr Ile Cys Phe Met Val Pro
260 265 270
Gly Val Leu Pro Asp Thr Val Asn Thr Val Arg Ile Arg Val Lys Thr
275 280 285
Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln
290 295 300
Ala Met Ser Ile Gly Lys Lys Ala Asp Pro Thr Gly Gly Gly Ser Gly
305 310 315 320
Ser Ser Gly Ser Val Lys Val Leu His Leu Thr Ala Cys Phe Ser Asp
325 330 335
Tyr Ile Ser Ala Ser Thr Cys Glu Trp Lys Met Asp Arg Pro Thr Asn
340 345 350
Cys Ser Ala Gln Leu Arg Leu Ser Tyr Gln Leu Asn Asp Glu Phe Ser
355 360 365
Asp Asn Leu Thr Cys Ile Pro Glu Asn Arg Glu Asp Glu Val Cys Val
370 375 380
Cys Arg Met Leu Met Asp Asn Ile Val Ser Glu Asp Val Tyr Glu Leu
385 390 395 400
Asp Leu Trp Ala Gly Asn Gln Leu Leu Trp Asn Ser Ser Phe Lys Pro
405 410 415
Ser Arg His Val Lys Pro Arg Ala Pro Gln Asn Leu Thr Val His Ala
420 425 430
Ile Ser His Thr Trp Leu Leu Thr Trp Ser Asn Pro Tyr Pro Leu Lys
435 440 445
Asn His Leu Trp Ser Glu Leu Thr Tyr Leu Val Asn Ile Ser Lys Glu
450 455 460
Asp Asp Pro Thr Asp Phe Lys Ile Tyr Asn Val Thr Tyr Met Asp Pro
465 470 475 480
Thr Leu Arg Val Thr Ala Ser Thr Leu Lys Ser Arg Ala Thr Tyr Ser
485 490 495
Ala Arg Val Lys Ala Arg Ala Gln Asn Tyr Asn Ser Thr Trp Ser Glu
500 505 510
Trp Ser Pro Ser Thr Thr Trp His Asn Tyr Tyr Glu Gln Pro Asp Met
515 520 525
Ser Lys Cys Pro Lys Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
530 535 540
Val Phe Ile Phe Pro Pro Asn Pro Lys Asp Thr Leu Met Ile Ser Arg
545 550 555 560
Thr Pro Val Val Thr Cys Val Val Val Asn Leu Ser Asp Gln Tyr Pro
565 570 575
Asp Val Gln Phe Ser Trp Tyr Val Asp Asn Thr Glu Val His Ser Ala
580 585 590
Ile Thr Lys Gln Arg Glu Ala Gln Phe Asn Ser Thr Tyr Arg Val Val
595 600 605
Ser Val Leu Pro Ile Gln His Gln Asp Trp Leu Ser Gly Lys Glu Phe
610 615 620
Lys Cys Ser Val Thr Asn Val Gly Val Pro Gln Pro Ile Ser Arg Ala
625 630 635 640
Ile Ser Arg Gly Lys Gly Pro Ser Arg Val Pro Gln Val Tyr Val Leu
645 650 655
Pro Pro His Pro Asp Glu Leu Ala Lys Ser Lys Val Ser Val Thr Cys
660 665 670
Leu Val Lys Asp Phe Tyr Pro Pro Asp Ile Ser Val Glu Trp Gln Ser
675 680 685
Asn Arg Trp Pro Glu Leu Glu Gly Lys Tyr Ser Thr Thr Pro Ala Gln
690 695 700
Leu Asp Gly Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu Ser Leu Glu
705 710 715 720
Thr Ser Arg Trp Gln Gln Val Glu Ser Phe Thr Cys Ala Val Met His
725 730 735
Glu Ala Leu His Asn His Tyr Thr Lys Thr Asp Ile Ser Glu Ser Leu
740 745 750
Gly Lys
<210> 31
<211> 754
<212> белок
<213> Искусственная последовательность
<220>
<223> IL4R-IL13R-IgG2 лошадиных (без сигнальной последовательности)
<400> 31
Ser Gly Ser Val Lys Val Leu His Leu Thr Ala Cys Phe Ser Asp Tyr
1 5 10 15
Ile Ser Ala Ser Thr Cys Glu Trp Lys Met Asp Arg Pro Thr Asn Cys
20 25 30
Ser Ala Gln Leu Arg Leu Ser Tyr Gln Leu Asn Asp Glu Phe Ser Asp
35 40 45
Asn Leu Thr Cys Ile Pro Glu Asn Arg Glu Asp Glu Val Cys Val Cys
50 55 60
Arg Met Leu Met Asp Asn Ile Val Ser Glu Asp Val Tyr Glu Leu Asp
65 70 75 80
Leu Trp Ala Gly Asn Gln Leu Leu Trp Asn Ser Ser Phe Lys Pro Ser
85 90 95
Arg His Val Lys Pro Arg Ala Pro Gln Asn Leu Thr Val His Ala Ile
100 105 110
Ser His Thr Trp Leu Leu Thr Trp Ser Asn Pro Tyr Pro Leu Lys Asn
115 120 125
His Leu Trp Ser Glu Leu Thr Tyr Leu Val Asn Ile Ser Lys Glu Asp
130 135 140
Asp Pro Thr Asp Phe Lys Ile Tyr Asn Val Thr Tyr Met Asp Pro Thr
145 150 155 160
Leu Arg Val Thr Ala Ser Thr Leu Lys Ser Arg Ala Thr Tyr Ser Ala
165 170 175
Arg Val Lys Ala Arg Ala Gln Asn Tyr Asn Ser Thr Trp Ser Glu Trp
180 185 190
Ser Pro Ser Thr Thr Trp His Asn Tyr Tyr Glu Gln Pro Gly Gly Gly
195 200 205
Ser Gly Ser Thr Glu Ser Gln Pro Pro Val Thr Asn Leu Ser Val Ser
210 215 220
Val Glu Asn Leu Cys Thr Val Ile Trp Thr Trp Asn Pro Pro Glu Gly
225 230 235 240
Val Ser Pro Asn Cys Ser Leu Trp Tyr Phe Ser His Phe Gly Asn Lys
245 250 255
Gln Asp Lys Lys Ile Ala Pro Glu Thr His Arg Ser Lys Glu Val Pro
260 265 270
Leu Asn Glu Arg Ile Cys Leu Gln Val Gly Ser Gln Cys Ser Thr Asn
275 280 285
Glu Ser Asp Asn Pro Ser Ile Leu Val Glu Lys Cys Ile Ser Pro Pro
290 295 300
Glu Gly Asp Pro Glu Ser Ala Val Thr Glu Leu Gln Cys Val Trp His
305 310 315 320
Asn Leu Ser Tyr Met Lys Cys Thr Trp Leu Pro Gly Lys Asn Ala Ser
325 330 335
Pro Asp Thr Asn Tyr Thr Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys
340 345 350
Ile Leu Gln Cys Glu Asp Ile Tyr Arg Glu Gly Gln His Ile Gly Cys
355 360 365
Ser Phe Ala Leu Thr Glu Val Lys Asp Ser Ile Phe Glu Gln His Ser
370 375 380
Val Gln Ile Met Val Lys Asp Asn Ala Gly Lys Ile Arg Pro Phe Phe
385 390 395 400
Asn Ile Val Pro Leu Thr Ser His Val Lys Pro Asp Pro Pro His Ile
405 410 415
Lys Lys Leu Phe Phe Gln Asn Gly Asp Leu Tyr Val Gln Trp Lys Asn
420 425 430
Pro Gln Asn Phe Tyr Ser Arg Cys Leu Ser Tyr Gln Val Glu Val Asn
435 440 445
Asn Ser Gln Thr Glu Thr Arg Asp Ile Phe Ser Val Glu Glu Ala Lys
450 455 460
Cys Gln Asn Pro Glu Phe Glu Gly Asp Leu Glu Gly Thr Ile Cys Phe
465 470 475 480
Met Val Pro Gly Val Leu Pro Asp Thr Val Asn Thr Val Arg Ile Arg
485 490 495
Val Lys Thr Asn Lys Leu Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn
500 505 510
Trp Ser Gln Ala Met Ser Ile Gly Lys Lys Ala Asp Pro Thr Asp Met
515 520 525
Ser Lys Cys Pro Lys Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
530 535 540
Val Phe Ile Phe Pro Pro Asn Pro Lys Asp Thr Leu Met Ile Ser Arg
545 550 555 560
Thr Pro Val Val Thr Cys Val Val Val Asn Leu Ser Asp Gln Tyr Pro
565 570 575
Asp Val Gln Phe Ser Trp Tyr Val Asp Asn Thr Glu Val His Ser Ala
580 585 590
Ile Thr Lys Gln Arg Glu Ala Gln Phe Asn Ser Thr Tyr Arg Val Val
595 600 605
Ser Val Leu Pro Ile Gln His Gln Asp Trp Leu Ser Gly Lys Glu Phe
610 615 620
Lys Cys Ser Val Thr Asn Val Gly Val Pro Gln Pro Ile Ser Arg Ala
625 630 635 640
Ile Ser Arg Gly Lys Gly Pro Ser Arg Val Pro Gln Val Tyr Val Leu
645 650 655
Pro Pro His Pro Asp Glu Leu Ala Lys Ser Lys Val Ser Val Thr Cys
660 665 670
Leu Val Lys Asp Phe Tyr Pro Pro Asp Ile Ser Val Glu Trp Gln Ser
675 680 685
Asn Arg Trp Pro Glu Leu Glu Gly Lys Tyr Ser Thr Thr Pro Ala Gln
690 695 700
Leu Asp Gly Asp Gly Ser Tyr Phe Leu Tyr Ser Lys Leu Ser Leu Glu
705 710 715 720
Thr Ser Arg Trp Gln Gln Val Glu Ser Phe Thr Cys Ala Val Met His
725 730 735
Glu Ala Leu His Asn His Tyr Thr Lys Thr Asp Ile Ser Glu Ser Leu
740 745 750
Gly Lys
<210> 32
<211> 305
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL13R собачьих
<400> 32
Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn Leu Cys Thr
1 5 10 15
Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro Asn Cys Thr
20 25 30
Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys Lys Ile Ala
35 40 45
Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu Arg Ile Cys
50 55 60
Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp Asn Pro Ser
65 70 75 80
Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp Pro Glu Ser
85 90 95
Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser Tyr Met Lys
100 105 110
Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr Asn Tyr Thr
115 120 125
Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln Cys Glu Asp
130 135 140
Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala Leu Thr Asn
145 150 155 160
Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile Val Val Lys
165 170 175
Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val Pro Leu Thr
180 185 190
Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu Phe Phe Gln
195 200 205
Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn Phe Tyr Ser
210 215 220
Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln Thr Glu Thr
225 230 235 240
Asn Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn Ser Glu Phe
245 250 255
Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro Gly Val Leu
260 265 270
Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr Asn Lys Leu
275 280 285
Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln Ala Met Ser
290 295 300
Ile
305
<210> 33
<211> 184
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL4R собачьих
<400> 33
Lys Val Leu His Glu Pro Ser Cys Phe Ser Asp Tyr Ile Ser Thr Ser
1 5 10 15
Val Cys Gln Trp Lys Met Asp His Pro Thr Asn Cys Ser Ala Glu Leu
20 25 30
Arg Leu Ser Tyr Gln Leu Asp Phe Met Gly Ser Glu Asn His Thr Cys
35 40 45
Val Pro Glu Asn Arg Glu Asp Ser Val Cys Val Cys Ser Met Pro Ile
50 55 60
Asp Asp Ala Val Glu Ala Asp Val Tyr Gln Leu Asp Leu Trp Ala Gly
65 70 75 80
Gln Gln Leu Leu Trp Ser Gly Ser Phe Gln Pro Ser Lys His Val Lys
85 90 95
Pro Arg Thr Pro Gly Asn Leu Thr Val His Pro Asn Ile Ser His Thr
100 105 110
Trp Leu Leu Met Trp Thr Asn Pro Tyr Pro Thr Glu Asn His Leu His
115 120 125
Ser Glu Leu Thr Tyr Met Val Asn Val Ser Asn Asp Asn Asp Pro Glu
130 135 140
Asp Phe Lys Val Tyr Asn Val Thr Tyr Met Gly Pro Thr Leu Arg Leu
145 150 155 160
Ala Ala Ser Thr Leu Lys Ser Gly Ala Ser Tyr Ser Ala Arg Val Arg
165 170 175
Ala Trp Ala Gln Thr Tyr Asn Ser
180
<210> 34
<211> 305
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL13R кошачьих
<400> 34
Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn Leu Cys Thr
1 5 10 15
Val Ile Trp Thr Trp Asp Pro Pro Glu Gly Ala Ser Pro Asn Cys Thr
20 25 30
Leu Arg Tyr Phe Ser His Phe Asp Asn Lys Gln Asp Lys Lys Ile Ala
35 40 45
Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu Arg Ile Cys
50 55 60
Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp Asn Pro Ser
65 70 75 80
Ile Leu Val Glu Lys Cys Thr Pro Pro Pro Glu Gly Asp Pro Glu Ser
85 90 95
Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser Tyr Met Lys
100 105 110
Cys Thr Trp Leu Pro Gly Arg Asn Thr Ser Pro Asp Thr Asn Tyr Thr
115 120 125
Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln Cys Glu Asn
130 135 140
Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala Leu Thr Asn
145 150 155 160
Leu Lys Asp Ser Ser Phe Glu Gln His Ser Val Gln Ile Val Val Lys
165 170 175
Asp Asn Ala Gly Lys Ile Arg Pro Ser Phe Asn Ile Val Pro Leu Thr
180 185 190
Ser His Val Lys Pro Asp Pro Pro His Ile Lys Arg Leu Phe Phe Gln
195 200 205
Asn Gly Asn Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn Phe Tyr Ser
210 215 220
Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln Thr Glu Thr
225 230 235 240
His Asp Ile Phe Tyr Val Glu Glu Ala Lys Cys Gln Asn Ser Glu Phe
245 250 255
Glu Gly Asn Leu Glu Gly Thr Ile Cys Phe Met Val Pro Gly Ile Leu
260 265 270
Pro Asp Thr Leu Asn Thr Val Arg Ile Arg Val Arg Thr Asn Lys Leu
275 280 285
Cys Tyr Glu Asp Asp Arg Leu Trp Ser Asn Trp Ser Gln Ala Met Ser
290 295 300
Ile
305
<210> 35
<211> 266
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL4R кошачьих
<400> 35
Lys Val Leu Arg Ala Pro Thr Cys Phe Ser Asp Tyr Phe Ser Thr Ser
1 5 10 15
Val Cys Gln Trp Asn Met Asp Ala Pro Thr Asn Cys Ser Ala Glu Leu
20 25 30
Arg Leu Ser Tyr Gln Leu Asn Phe Met Gly Ser Glu Asn Arg Thr Cys
35 40 45
Val Pro Glu Asn Gly Glu Gly Ala Ala Cys Ala Cys Ser Met Leu Met
50 55 60
Asp Asp Phe Val Glu Ala Asp Val Tyr Gln Leu His Leu Trp Ala Gly
65 70 75 80
Thr Gln Leu Leu Trp Ser Gly Ser Phe Lys Pro Ser Ser His Val Lys
85 90 95
Pro Arg Ala Pro Gly Asn Leu Thr Val His Pro Asn Val Ser His Thr
100 105 110
Trp Leu Leu Arg Trp Ser Asn Pro Tyr Pro Pro Glu Asn His Leu His
115 120 125
Ala Glu Leu Thr Tyr Met Val Asn Ile Ser Ser Glu Asp Asp Pro Thr
130 135 140
Asp Val Ser Val Cys Ala Ser Gly Phe Leu Cys His Leu Leu Gly Leu
145 150 155 160
Arg Arg Val Glu Thr Gly Ala Pro Gly Ala Arg Leu Pro Pro Trp Leu
165 170 175
Cys Ala Pro Arg Pro Arg Arg Val Pro Gly Ser Gln Cys Ala Val Ile
180 185 190
Ser Cys Cys Arg Trp Val Leu Ile Ala Leu Thr Ser Arg Gly Gly Arg
195 200 205
Trp Arg Leu Thr Pro Gly Leu Arg Ser Gln Thr Arg Tyr Val Ser Val
210 215 220
Ala Glu Gly Leu Phe Gly Ala Thr Pro Arg Val Leu Cys Pro Gly Thr
225 230 235 240
Gln Ala Gly Leu Ala Ser Ala Ala Arg Glu Gln Met Ser Pro Asp Pro
245 250 255
Ser Ala Phe His Ser Ile Asp Tyr Glu Pro
260 265
<210> 36
<211> 305
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL13R лошадиных
<400> 36
Gln Pro Pro Val Thr Asn Leu Ser Val Ser Val Glu Asn Leu Cys Thr
1 5 10 15
Val Ile Trp Thr Trp Asn Pro Pro Glu Gly Val Ser Pro Asn Cys Ser
20 25 30
Leu Trp Tyr Phe Ser His Phe Gly Asn Lys Gln Asp Lys Lys Ile Ala
35 40 45
Pro Glu Thr His Arg Ser Lys Glu Val Pro Leu Asn Glu Arg Ile Cys
50 55 60
Leu Gln Val Gly Ser Gln Cys Ser Thr Asn Glu Ser Asp Asn Pro Ser
65 70 75 80
Ile Leu Val Glu Lys Cys Ile Ser Pro Pro Glu Gly Asp Pro Glu Ser
85 90 95
Ala Val Thr Glu Leu Gln Cys Val Trp His Asn Leu Ser Tyr Met Lys
100 105 110
Cys Thr Trp Leu Pro Gly Lys Asn Ala Ser Pro Asp Thr Asn Tyr Thr
115 120 125
Leu Tyr Tyr Trp His Ser Ser Leu Gly Lys Ile Leu Gln Cys Glu Asp
130 135 140
Ile Tyr Arg Glu Gly Gln His Ile Gly Cys Ser Phe Ala Leu Thr Glu
145 150 155 160
Val Lys Asp Ser Ile Phe Glu Gln His Ser Val Gln Ile Met Val Lys
165 170 175
Asp Asn Ala Gly Lys Ile Arg Pro Phe Phe Asn Ile Val Pro Leu Thr
180 185 190
Ser His Val Lys Pro Asp Pro Pro His Ile Lys Lys Leu Phe Phe Gln
195 200 205
Asn Gly Asp Leu Tyr Val Gln Trp Lys Asn Pro Gln Asn Phe Tyr Ser
210 215 220
Arg Cys Leu Ser Tyr Gln Val Glu Val Asn Asn Ser Gln Thr Glu Thr
225 230 235 240
Arg Asp Ile Phe Ser Val Glu Glu Ala Lys Cys Gln Asn Pro Glu Phe
245 250 255
Glu Gly Asp Leu Glu Gly Thr Ile Cys Phe Met Val Pro Gly Val Leu
260 265 270
Pro Asp Thr Val Asn Thr Val Arg Ile Arg Val Lys Thr Asn Lys Leu
275 280 285
Cys Tyr Glu Asp Asp Lys Leu Trp Ser Asn Trp Ser Gln Ala Met Ser
290 295 300
Ile
305
<210> 37
<211> 201
<212> белок
<213> Искусственная последовательность
<220>
<223> ECD мини-IL4R лошадиных
<400> 37
Lys Val Leu His Leu Thr Ala Cys Phe Ser Asp Tyr Ile Ser Ala Ser
1 5 10 15
Thr Cys Glu Trp Lys Met Asp Arg Pro Thr Asn Cys Ser Ala Gln Leu
20 25 30
Arg Leu Ser Tyr Gln Leu Asn Asp Glu Phe Ser Asp Asn Leu Thr Cys
35 40 45
Ile Pro Glu Asn Arg Glu Asp Glu Val Cys Val Cys Arg Met Leu Met
50 55 60
Asp Asn Ile Val Ser Glu Asp Val Tyr Glu Leu Asp Leu Trp Ala Gly
65 70 75 80
Asn Gln Leu Leu Trp Asn Ser Ser Phe Lys Pro Ser Arg His Val Lys
85 90 95
Pro Arg Ala Pro Gln Asn Leu Thr Val His Ala Ile Ser His Thr Trp
100 105 110
Leu Leu Thr Trp Ser Asn Pro Tyr Pro Leu Lys Asn His Leu Trp Ser
115 120 125
Glu Leu Thr Tyr Leu Val Asn Ile Ser Lys Glu Asp Asp Pro Thr Asp
130 135 140
Phe Lys Ile Tyr Asn Val Thr Tyr Met Asp Pro Thr Leu Arg Val Thr
145 150 155 160
Ala Ser Thr Leu Lys Ser Arg Ala Thr Tyr Ser Ala Arg Val Lys Ala
165 170 175
Arg Ala Gln Asn Tyr Asn Ser Thr Trp Ser Glu Trp Ser Pro Ser Thr
180 185 190
Thr Trp His Asn Tyr Tyr Glu Gln Pro
195 200
<210> 38
<211> 4
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 38
Gly Ser Gly Ser
1
<210> 39
<211> 6
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 39
Gly Ser Gly Ser Gly Ser
1 5
<210> 40
<211> 6
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 40
Gly Gly Ser Gly Gly Ser
1 5
<210> 41
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 41
Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5
<210> 42
<211> 4
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 42
Gly Gly Gly Ser
1
<210> 43
<211> 8
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 43
Gly Gly Gly Ser Gly Gly Gly Ser
1 5
<210> 44
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 44
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10
<210> 45
<211> 6
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 45
Gly Ser Ser Gly Ser Ser
1 5
<210> 46
<211> 9
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 46
Gly Ser Ser Gly Ser Ser Gly Ser Ser
1 5
<210> 47
<211> 4
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 47
Gly Gly Ser Ser
1
<210> 48
<211> 8
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 48
Gly Gly Ser Ser Gly Gly Ser Ser
1 5
<210> 49
<211> 12
<212> белок
<213> Искусственная последовательность
<220>
<223> линкер GS
<400> 49
Gly Gly Ser Ser Gly Gly Ser Ser Gly Gly Ser Ser
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА К РЕЦЕПТОРУ IL4 ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2837141C2 |
| ВАРИАНТЫ FC-ОБЛАСТИ С ИЗМЕНЕННЫМ СВЯЗЫВАНИЕМ С НЕОНАТАЛЬНЫМ FC-РЕЦЕПТОРОМ (FCRN) ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2019 |
|
RU2830231C2 |
| АНТИТЕЛО-ПОДОБНЫЕ СВЯЗЫВАЮЩИЕ БЕЛКИ С ДВОЙНЫМИ ВАРИАБЕЛЬНЫМИ ОБЛАСТЯМИ, ИМЕЮЩИЕ ОРИЕНТАЦИЮ СВЯЗЫВАЮЩИХ ОБЛАСТЕЙ КРЕСТ-НАКРЕСТ | 2012 |
|
RU2823693C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ НА ОСНОВЕ ПСЕВДО-FAB | 2019 |
|
RU2820254C2 |
| АНТАГОНИСТЫ NGF ДЛЯ МЕДИЦИНСКОГО ИСПОЛЬЗОВАНИЯ | 2020 |
|
RU2829812C2 |
| БЕЛОК, СВЯЗЫВАЮЩИЙ АНТИГЕН ST2 | 2021 |
|
RU2841164C2 |
| КОНСТРУКЦИИ СЛИТОГО БЕЛКА ДЛЯ ЗАБОЛЕВАНИЯ, СВЯЗАННОГО С КОМПЛЕМЕНТОМ | 2019 |
|
RU2824402C2 |
| ВАРИАНТЫ IgG-FC ДЛЯ ПРИМЕНЕНИЯ В ВЕТЕРИНАРИИ | 2018 |
|
RU2814952C2 |
| СЛИТЫЙ БЕЛОК GDF15 ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2020 |
|
RU2836280C1 |
| T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53 | 2020 |
|
RU2830061C2 |
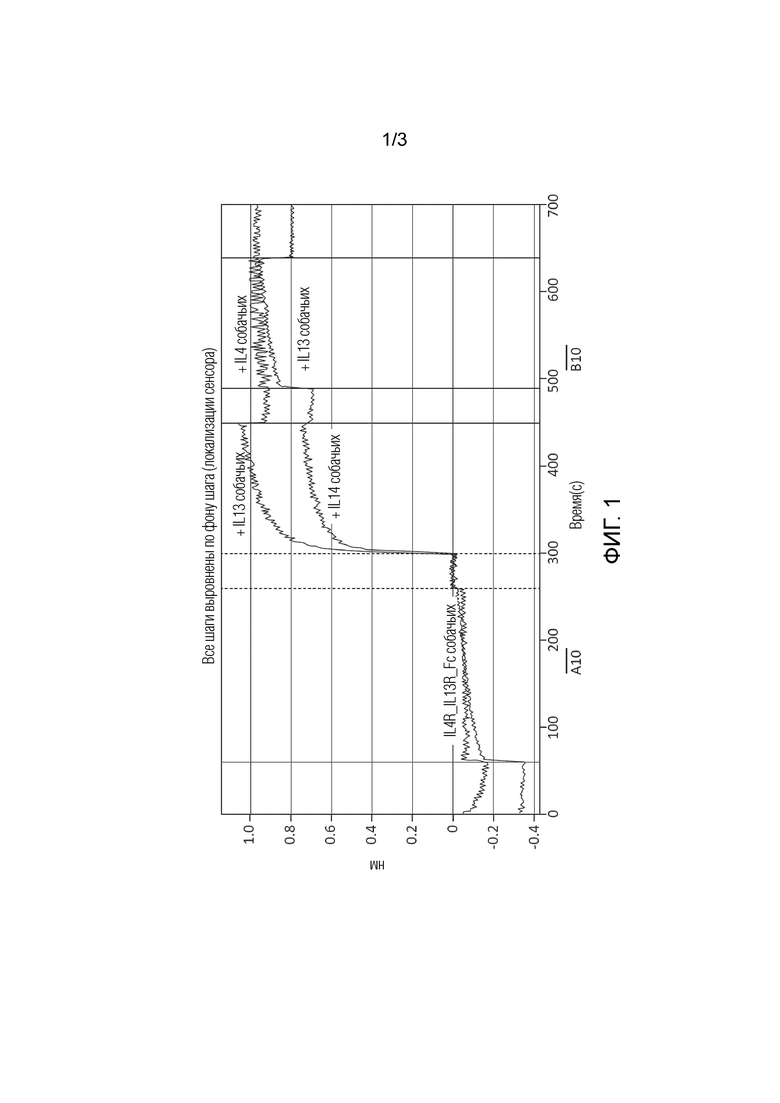
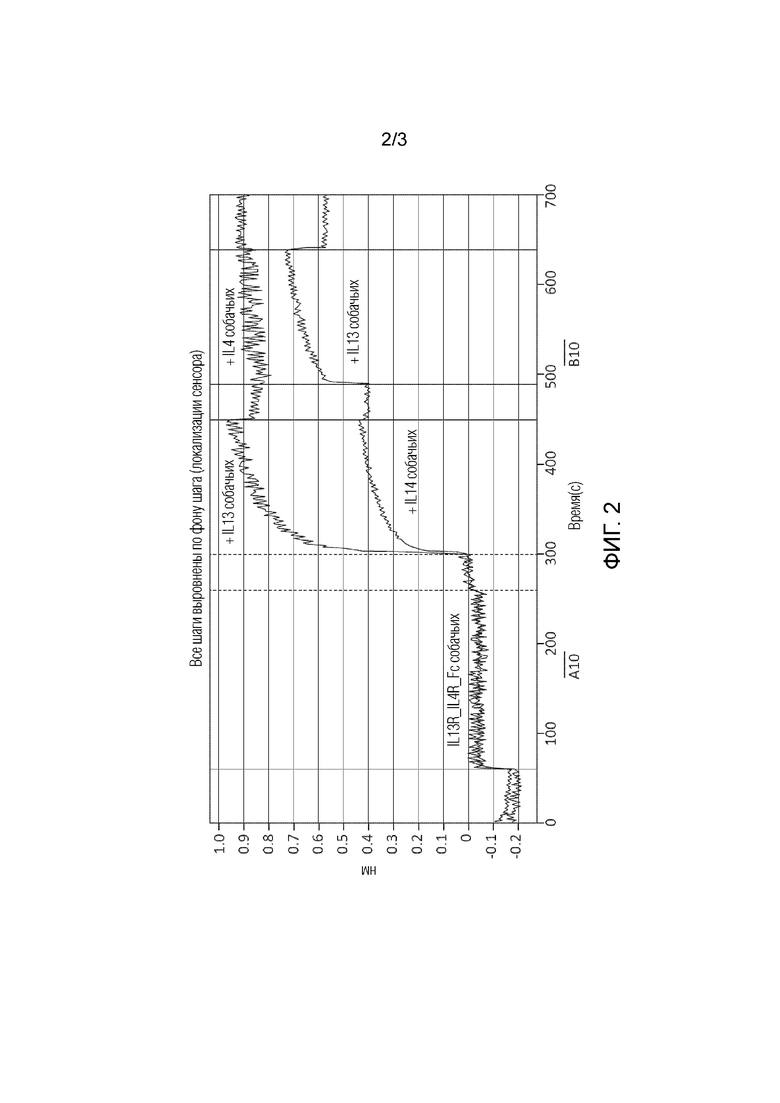
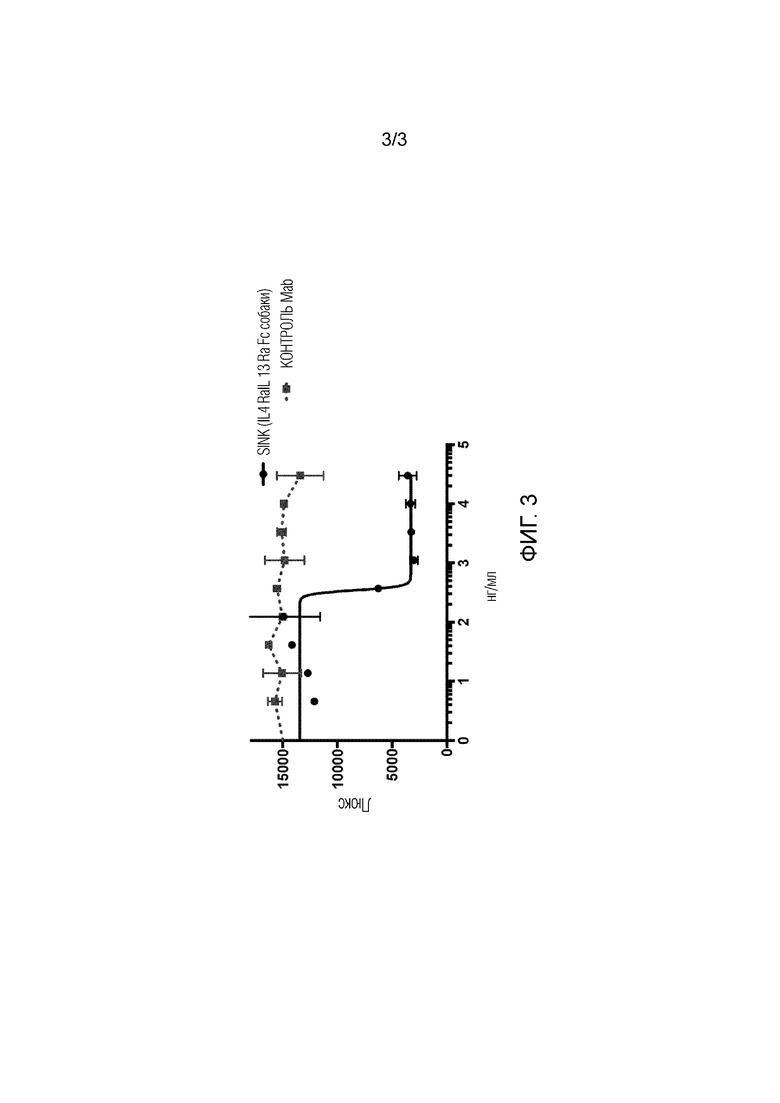
Настоящее изобретение относится к области биотехнологии, в частности новым терапевтическим пептидам, и может быть использовано в медицине. Изобретение раскрывает непрерывный полипептид, способный связываться с IL13 и с IL4. Изобретение применимо в качестве терапевтического агента при лечении индуцированных IL13 и/или IL4 состояний у домашних животных. 9 н. и 16 з.п. ф-лы, 3 ил., 2 табл., 5 пр.
1. Непрерывный полипептид, связывающийся с IL13 и связывающийся с IL4, содержащий
внеклеточный домен полипептида IL13R и
внеклеточный домен полипептида IL4R,
причем внеклеточный домен полипептида IL13R по меньшей мере на 98% идентичен аминокислотной последовательности SEQ ID NO: 22, и
внеклеточный домен полипептида IL4R по меньшей мере на 98% идентичен аминокислотной последовательности SEQ ID NO: 23.
2. Непрерывный полипептид по п. 1, имеющий формулу (I) IL13R–L1–IL4R–L2–FP или формулу (II) IL4R–L1–IL13R–L2–FP, где:
a) IL13R представляет собой внеклеточный домен полипептида IL13R,
b) IL4R представляет собой внеклеточный домен полипептида IL4R,
c) L1 представляет собой первый необязательный пептидный линкер,
d) L2 представляет собой второй необязательный пептидный линкер, и
e) FP представляет собой партнера по слиянию.
3. Непрерывный полипептид по п. 1 или 2, связывающийся с IL13 из вида домашнего животного с константой диссоциации (Kd) менее чем 5×10–6 M, менее чем 1×10–6 M, менее чем 5×10–7 M, менее чем 1×10–7 M, менее чем 5×10–8 M, менее чем 1×10–8 M, менее чем 5×10–9 M, менее чем 1×10–9 M, менее чем 5×10–10 M, менее чем 1×10–10 M, менее чем 5×10-11 M, менее чем 1×10-11 M, менее чем 5×10–12 M или менее чем 1×10–12 M при измерении посредством интерферометрии биослоя.
4. Непрерывный полипептид по любому из пп. 1-3, связывающийся с IL4 из вида домашнего животного с константой диссоциации (Kd) менее чем 5×10–6 M, менее чем 1×10–6 M, менее чем 5×10–7 M, менее чем 1×10–7 M, менее чем 5×10–8 M, менее чем 1×10–8 M, менее чем 5×10–9 M, менее чем 1×10–9 M, менее чем 5×10–10 M, менее чем 1×10–10 M, менее чем 5×10-11 M, менее чем 1×10-11 M, менее чем 5×10–12 M или менее чем 1×10–12 M при измерении посредством интерферометрии биослоя.
5. Непрерывный полипептид по любому из пп. 1-4, уменьшающий передачу сигналов IL13 и/или IL4 у вида домашнего животного.
6. Непрерывный полипептид по любому из пп. 3-5, где вид домашнего животного является представителем семейства собачьих, кошачьих или лошадиных.
7. Непрерывный полипептид по любому из пп. 2-6, где каждый из L1 и L2, если он присутствует, независимо содержит аминокислотную последовательность, выбранную из G, GG, GGG, S, SS, SSS, GS, GSGS (SEQ ID NO: 38), GSGSGS (SEQ ID NO: 39), GGS, GGSGGS (SEQ ID NO: 40), GGSGGSGGS (SEQ ID NO: 41), GGGS (SEQ ID NO: 42), GGGSGGGS (SEQ ID NO: 43), GGGSGGGSGGGS (SEQ ID NO: 44), GSS, GSSGSS (SEQ ID NO: 45), GSSGSSGSS (SEQ ID NO: 46), GGSS (SEQ ID NO: 47), GGSSGGSS (SEQ ID NO: 48) и GGSSGGSSGGSS (SEQ ID NO: 49).
8. Непрерывный полипептид по любому из пп. 2-7, где партнер по слиянию выбран из Fc, альбумина и связывающего альбумин фрагмента.
9. Непрерывный полипептид по п. 8, где Fc представляет собой (a) константную область тяжелой цепи члена семейства собачьих, выбранную из константной области IgG–A, IgG–B, IgG–C и IgG–D; (b) константную область тяжелой цепи члена семейства кошачьих, выбранную из константной области IgG1, IgG2a и IgG2b; или (c) константную область тяжелой цепи члена семейства лошадиных, выбранную из константной области IgG1, IgG2, IgG3, IgG4, IgG5, IgG6 и IgG7.
10. Непрерывный полипептид по любому из пп. 1-9, содержащий последовательность, выбранную из SEQ ID NO: 13, SEQ ID NO: 14, SEQ ID NO: 15, SEQ ID NO: 16, SEQ ID NO: 17, SEQ ID NO: 20 и SEQ ID NO: 21.
11. Выделенная нуклеиновая кислота, кодирующая непрерывный полипептид по любому из пп. 1-10.
12. Клетка–хозяин для получения непрерывного полипептида, содержащая нуклеиновую кислоту по п. 11.
13. Способ получения непрерывного полипептида, включающий культивирование клетки–хозяина по п. 12 и выделение непрерывного полипептида.
14. Фармацевтическая композиция для лечения члена семейства собачьих, кошачьих или лошадиных, имеющего сопровождающееся зудом или аллергическое состояние, такое как атопический дерматит, зуд, астма, псориаз, склеродермия или экзема, содержащая терапевтически эффективное количество непрерывного полипептида по любому из пп. 1-10 и фармацевтически приемлемый носитель.
15. Способ лечения члена семейства собачьих, имеющего сопровождающееся зудом или аллергическое состояние, такое как атопический дерматит, зуд, астма, псориаз, склеродермия или экзема, включающий введение собачьему терапевтически эффективного количества непрерывного полипептида по любому из пп. 1-10 или фармацевтической композиции по п. 14.
16. Способ по п. 15, где непрерывный полипептид или фармацевтическую композицию вводят парентерально.
17. Способ по п. 15 или 16, где непрерывный полипептид или фармацевтическую композицию вводят внутримышечным способом, внутрибрюшинным способом, внутриспинномозговым способом, подкожным способом, внутриартериальным способом, внутрисуставным способом, интратекальным способом или ингаляционным способом.
18. Способ по любому из пп. 15-17, где способ дополнительно включает введение ингибитора Jak, ингибитора PI3K, ингибитора AKT или ингибитора MAPK.
19. Способ по любому из пп. 15-18, где способ дополнительно включает введение одного или нескольких антител, выбранных из антитела к IL17, антитела к IL31, антитела к TNFα, антитела к CD20, антитела к CD19, антитела к CD25, антитела к IL4, антитела к IL13, антитела к IL23, антитела к IgE, антитела к CD11α, антитела к IL6R, антитела к α4–интегрину, антитела к IL12, антитела к IL1β и антитела к BlyS.
20. Способ уменьшения активности передачи сигналов IL4 в клетке, включающий воздействие на клетку непрерывным полипептидом по любому из пп. 1-10 или фармацевтической композицией по п. 14 в условиях, обеспечивающих связывание непрерывного полипептида с IL4, с, таким образом, (a) уменьшением связывания IL/4 с нативным рецептором IL13 и/или нативным рецептором IL–4 и уменьшением опосредованной IL4 передачи сигналов.
21. Способ по п. 20, где клетку подвергают воздействию непрерывного полипептида или фармацевтической композиции ex vivo.
22. Способ по п. 20, где клетку подвергают воздействию непрерывного полипептида или фармацевтической композиции in vivo.
23. Способ по любому из пп. 20-22, где клетка представляет собой клетку члена семейства собачьих, клетку члена семейства кошачьих или клетку члена семейства лошадиных.
24. Способ детекции IL13 в биологическом образце, полученном от члена семейства собачьих, включающий приведение образца в контакт с непрерывным полипептидом по любому из пп. 1-10 или фармацевтической композицией по п. 14 в условиях, обеспечивающих связывание непрерывного полипептида с IL13, и детекцию того, формируется ли комплекс между непрерывным полипептидом и IL13 в образце.
25. Способ детекции IL4 в биологическом образце, полученном от члена семейства собачьих, включающий приведение образца в контакт с непрерывным полипептидом по любому из пп. 1-10 или фармацевтической композицией по п. 14 в условиях, обеспечивающих связывание непрерывного полипептида с IL4, и детекцию того, формируется ли комплекс между непрерывным полипептидом и IL4 в образце.
| US 7410781 B2, 12.08.2008 | |||
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА И СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2017 |
|
RU2674440C1 |
| WO 2017019949 A1, 02.02.2017 | |||
| US 20080287665 A1, 20.11.2008 | |||
| RU 2009120202 A1, 20.01.2011 | |||
| US 20090156421 A1, 18.06.2009. | |||
Авторы
Даты
2023-05-05—Публикация
2018-04-20—Подача