Область техники, к которой относится изобретение
Настоящее раскрытие относится к твердой форме, кристаллической форме и кристаллической форме А соединения формулы (I) как агониста рецептора FXR, способу его получения и применению соединения формулы (I) в производстве лекарственного средства для лечения неалкогольного стеатогепатита (NASH).
Предпосылки создания изобретения
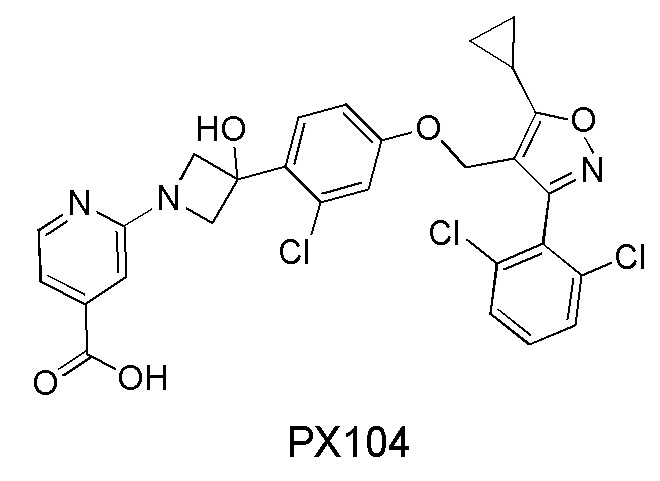
Рецептор фарнезоида Х (FXR) является членом суперсемейства ядерных рецепторов, который впервые клонирован и открыт в библиотеке ДНК печени крысы. FXR имеет типичную структуру ядерного рецептора, состоящую из домена активации лиганд-независимой транскрипции, ДНК-связывающего домена, шарнирного участка и лиганд-связывающего участка. FXR обильно экспрессируется в печени, кишечнике, почках и поджелудочной железе, образует гетеродимер с ретиноидным рецептором Х (RXR) и связывается с ДНК, модулируя транскрипцию гена. Гетродимер FXR/RXR преимущественно связывается с компонентом, состоящим из двух ядерных рецепторных полусайтов консенсуса AG(G/T)TCA, организованных в виде инвертированного повтора и разделенных одним нуклеозидом (мотив IR-1). FXR, как ядерный рецептор, активировнный желчными кислотами, принимает участие в регуляции различных физиологических действий организма, включая такие процессы, как метаболизм желчных кислот, липидный метаболизм, метаболизм глюкозы и защита печени и т.д., и тесно ассоциируется с такими заболеваниями, как метаболический синдром, заболевание гепатобилиарной системы и диабет типа 2, и т.д. Холевые кислоты, которые являются эндогенными лигандами FXR, включают хенодезоксихолевую кислоту (CDCA), дезоксихолевую кислоту (DCA), литохолевую кислоту (LCA) и тауриновые и глициновые конъюгаты этих холевых кислот. PX104 является агонистом рецептора FXR.
Сущность изобретения
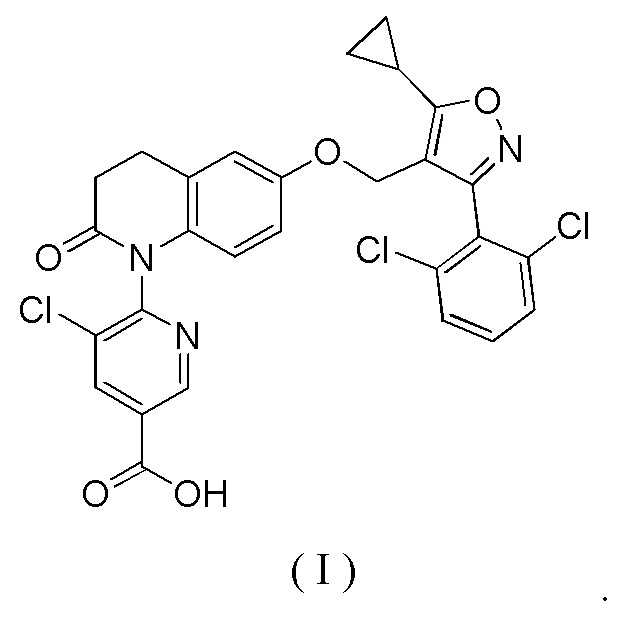
Настоящее раскрытие относится к твердой форме соединения формулы (I).
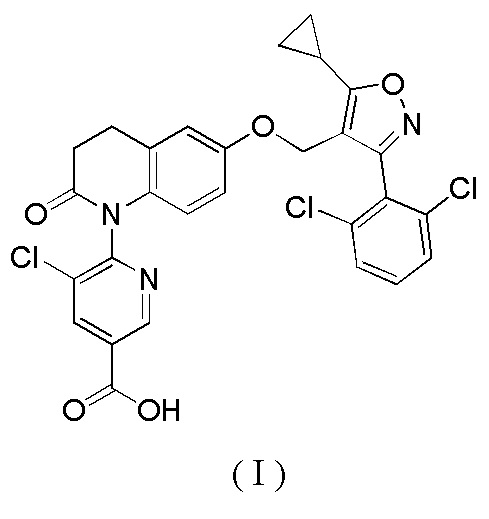
Настоящее раскрытие относится к кристаллической форме соединения формулы (I).
Настоящее раскрытие относится к кристаллической форме А соединения формулы (I), которая характеризуется порошковой рентгенограммой с характеристическими дифракционными пиками при следующих углах 2θ: 3,54±0,2°, 12,72±0,2° и 25,27±0,2°.
В некоторых воплощениях настоящего раскрытия порошковая рентгенограмма кристаллической формы А соединения формулы (I), описанной выше, имеет характеристические дифракционные пики при следующих углах 2θ: 3,54±0,2°, 11,86±0,2°, 12,72±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 24,18±0,2° и 25,27±0,2°.
В некоторых воплощениях настоящего раскрытия порошковая рентгенограмма кристаллической формы А соединения формулы (I), описанной выше, имеет характеристические дифракционные пики при следующих углах 2θ: 3,54±0,2°, 11,86±0,2°, 12,72±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 20,38±0,2°, 22,60±0,2°, 23,80±0,2°, 24,18±0,2° и 25,27±0,2°.
В некоторых воплощениях настоящего раскрытия порошковая рентгенограмма кристаллической формы А соединения формулы (I), описанной выше, имеет характеристические дифракционные пики при следующих углах 2θ: 3,54±0,2°, 11,86±0,2°, 12,72±0,2°, 13,67±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 20,38±0,2°, 22,60±0,2°, 23,80±0,2°, 24,18±0,2°, 25,27±0,2° и 26,57±0,2°.
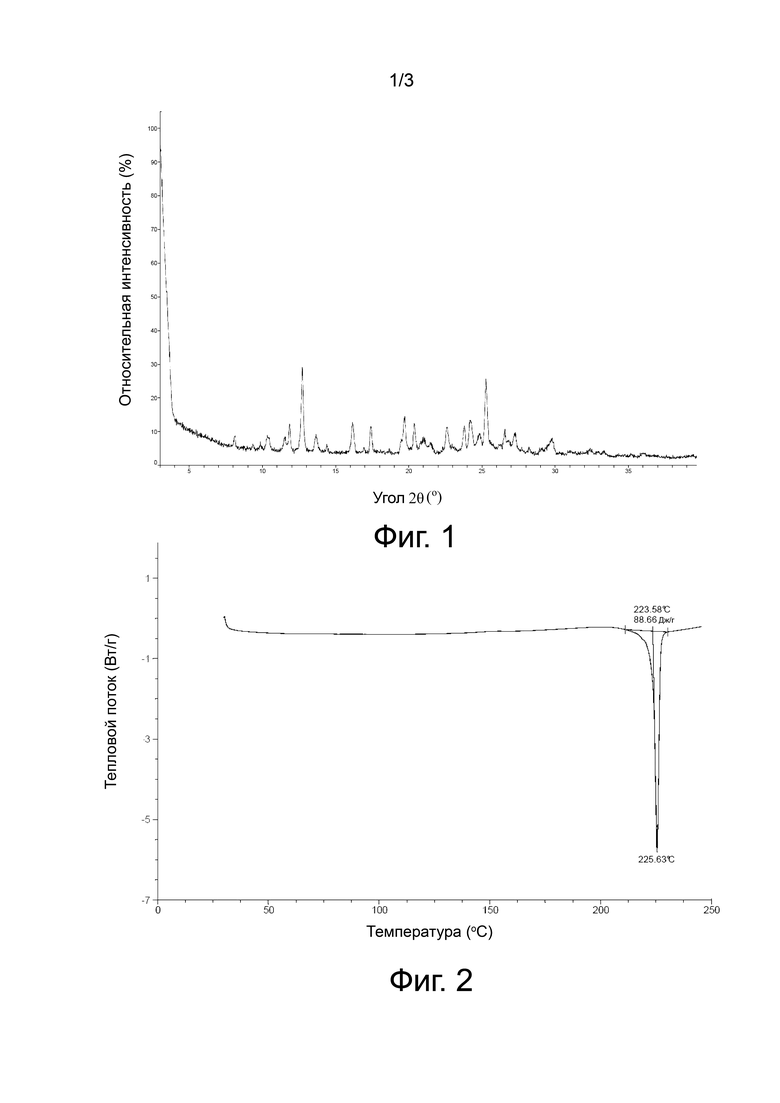
В некоторых воплощениях настоящего раскрытия кристаллическая форма А соединения формулы (I), описанной выше, имеет XRPD, показанную на фиг. 1.
В таблице 1 показан анализ данных XRPD кристаллической формы А соединения формулы (I), описанной выше, в некоторых воплощениях настоящего раскрытия.
Таблица 1
Примечание: 3,541 является базовым пиком.
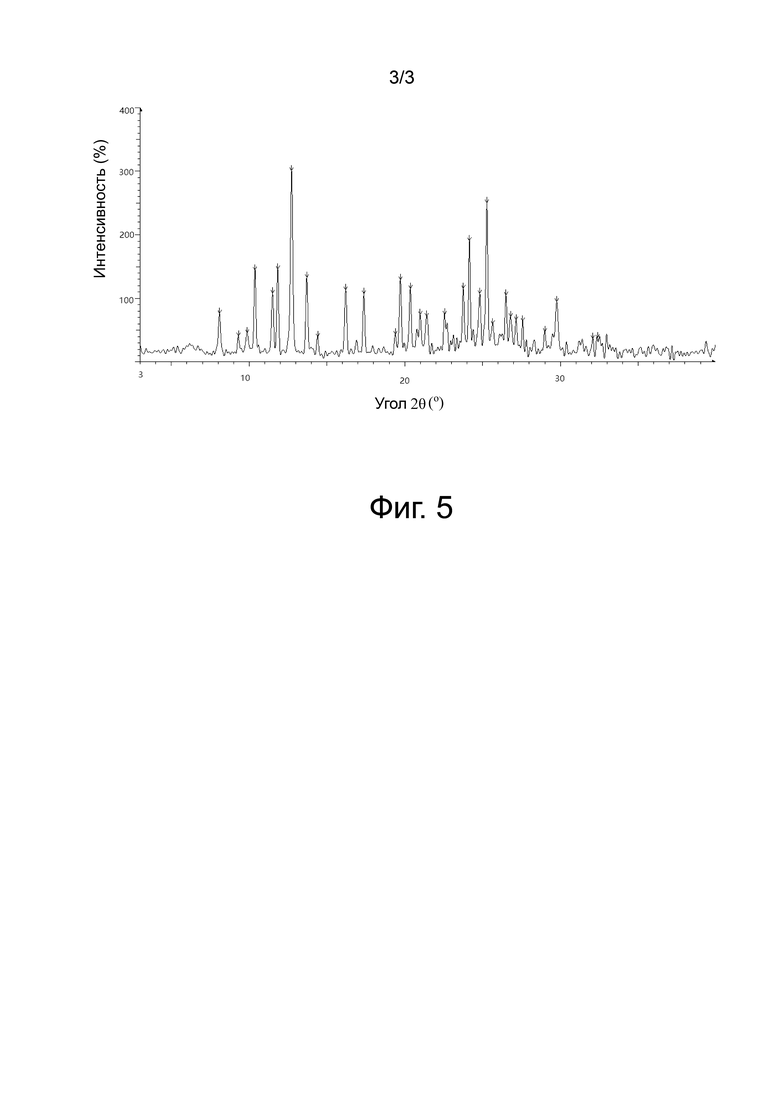
В некоторых воплощениях настоящего раскрытия кристаллическая форма А соединения формулы (I), описанной выше, имеет XRPD, показанную на фиг. 5.
В некоторых воплощениях настоящего раскрытия кривая дифференциальной сканирующей калориметрии кристаллической формы А соединения формулы (I), описанной выше, имеет начальную точку эндотермического пика при 223,58°C±3°C.
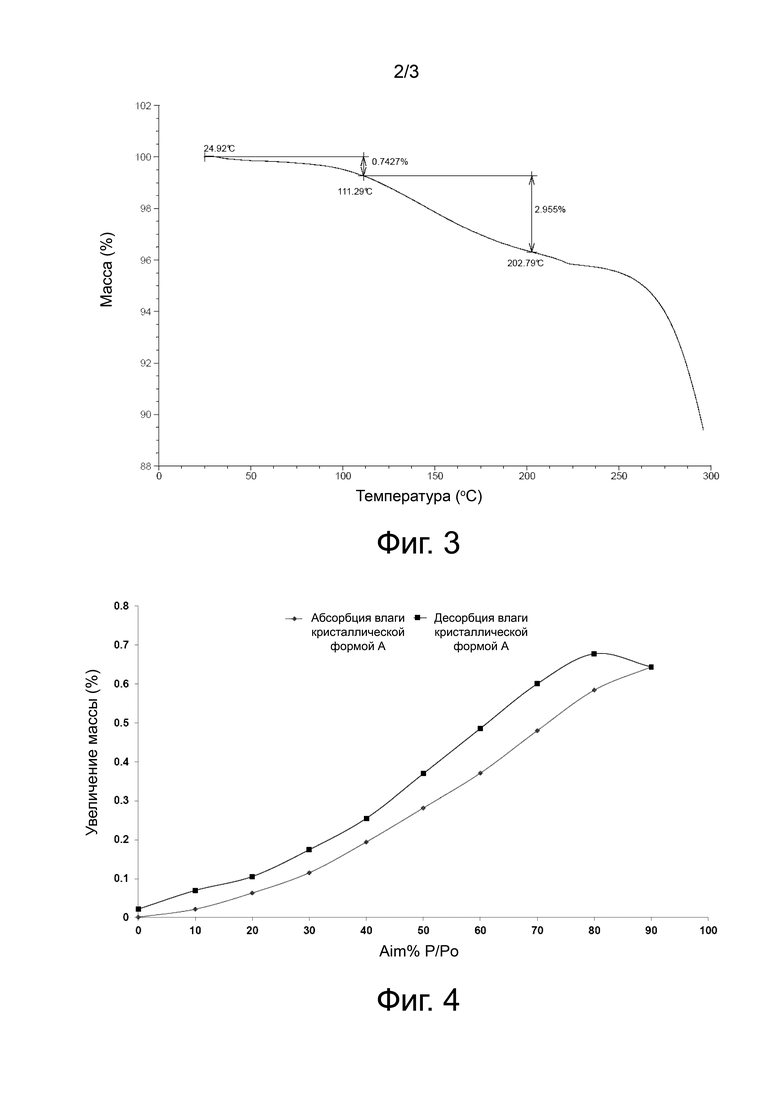
В некоторых воплощениях настоящего раскрытия кристаллическая форма А соединения формулы (I), описанной выше, имеет кривую ДСК, показанную на фиг. 2.
В некоторых воплощениях настоящего раскрытия кривая термогравиметрического анализа кристаллической формы А соединения формулы (I), описанной выше, имеет потерю массы до 0,7427%±0,2% при 111,29°C±3°C и до 3,6977%±0,2% при 202,79°C±3°C.
В некоторых воплощениях настоящего раскрытия кристаллическая форма А соединения формулы (I), описанной выше, имеет кривую ТГА, показанную на фиг. 3.
Настоящее раскрытие также относится к способу получения кристаллической формы А соединения формулы (I), включающему
(а) добавление соединения формулы (I) в растворитель;
(b) перемешивание при 30-50°С в течение 40-55 часов и
(с) центрифугирование и последующее испарение растворителя и получение кристаллической формы А;
причем растворителем является спирт, тетрагидрофуран, вода, ацетон, ацетонитрил, этилацетат, смешанный растворитель из спирта и воды или смешанный растворитель из ацетона и воды.
В некоторых воплощениях настоящего раскрытия вышеуказанный спирт выбирают из метанола, этанола, изопропанола и н-пропанола.
В некоторых воплощениях настоящего раскрытия вышеуказанный растворитель является смешанным растворителем из спирта и воды, причем объемное отношение спирта к воде составляет 1:0,6 – 1:1,5.
В некоторых воплощениях настоящего раскрытия вышеуказанный растворитель является смешанным растворителем из спирта и воды, причем объемное отношение спирта к воде составляет 1:1.
В некоторых воплощениях настоящего раскрытия вышеуказанный растворитель является смешанным растворителем из ацетона и воды, причем объемное отношение ацетона к воде составляет 1:1,5 – 1:2,5.
В некоторых воплощениях настоящего раскрытия вышеуказанный растворитель является смешанным растворителем из ацетона и воды, причем объемное отношение ацетона к воде составляет 1:2.
Настоящее раскрытие также относится к способу получения соединения формулы (I), который включает следующие стадии:
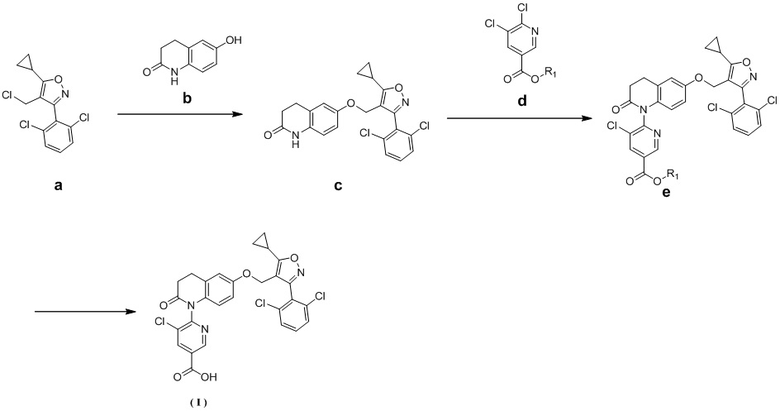
где R1 представляет собой C1-3-алкильную группу.
В некоторых воплощениях настоящего раскрытия вышеуказанный способ получения включает следующие стадии:
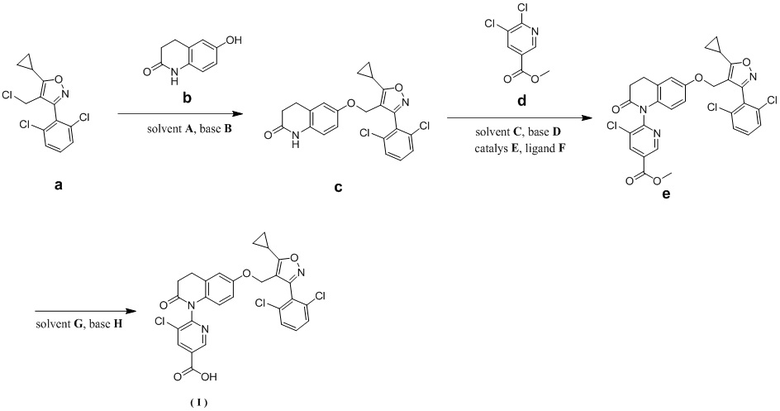
solvent – растворитель, base – основание, catalyst – катализатор, ligand – лиганд,
где
растворитель А представляет собой ДМФА;
основание В представляет собой фосфат калия;
растворитель С представляет собой толуол;
основание D представляет собой карбонат цезия;
катализатор Е представляет собой трис(дибензилиденацетон)дипалладий;
лиганд F представляет собой 2,2'-бис(дифенилфосфино)-1,1'-бинафтил;
растворитель G представляет собой тетрагидрофуран; и
основание Н представляет собой гидроксид натрия.
В некоторых воплощениях настоящего раскрытия в вышеуказанном способе получения отношение объем: масса растворителя С к промежуточному соединению с составляет 10:1, молярное отношение основания D к промежуточному соединению с составляет 2:1, молярное отношение катализатора Е к промежуточному соединению с составляет 0,025:1, и молярное отношение лиганда F к промежуточному соединению с составляет 0,05:1.
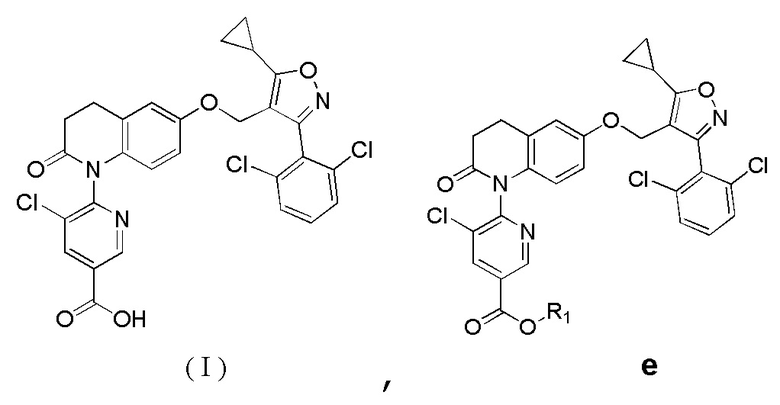
Настоящее раскрытие также относится к соединению, представленному формулой е, или его фармацевтически приемлемой соли,
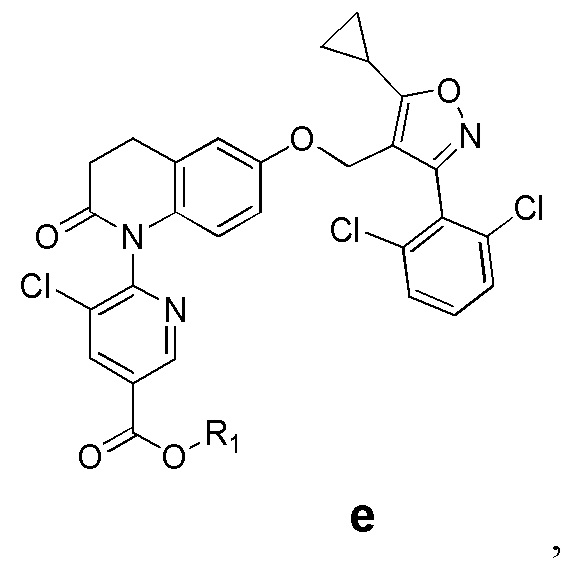
где R1 представляет собой C1-3-алкильную группу.
В некоторых воплощениях настоящего раскрытия R1 представляет собой CН3.
Настоящее раскрытие также относится к применению вышеуказанной твердой формы соединения формулы (I) в производстве лекарственного средства для лечения связанных с FXR заболеваний.
Настоящее раскрытие также относится к применению вышеуказанной кристаллической формы соединения формулы (I) в производстве лекарственного средства для лечения связанных с FXR заболеваний.
Настоящее раскрытие также относится к применению вышеуказанной кристаллической формы А соединения формулы (I) в производстве лекарственного средства для лечения связанных с FXR заболеваний.
В некоторых воплощениях настоящего раскрытия вышеуказанное связанное с FXR заболевание представляет собой заболевание неалкагольное ожирение печени.
Определения и описание
Если не указано иное, предполагается, что перечисленные далее термины и выражения, используемые в настоящем описании, имеют указанные далее значения. Конкретный термин или выражение не должны считаться неопределенными или неясными в отсутствие особого определения, но должны пониматься в общепринятом смысле. Когда в настоящем описании появляется торговое название, оно предназначено для обозначения соответствующего ему товара или активного ингредиента.
Промежуточные соединения по настоящему раскрытию могут быть получены различными методами синтеза, хорошо известными специалистам в данной области техники, включая конкретные воплощения, перечисленные ниже, воплощения, образованные комбинацией конкретных воплощений, перечисленных ниже, с другими методами химического синтеза, и эквивалентные альтернативные методы, хорошо известные специалистам в данной области техники. Альтернативные воплощения включают, но без ограничения, примеры в настоящем раскрытии.
Химические реакции в конкретных воплощениях, раскрытых в настоящем описании, выполняются в подходящем растворителе, который должен подходить для химических изменений в настоящем раскрытии и требуемым реагентам, и материалам. Для того, чтобы получить соединение по настоящему раскрытию, специалистам в данной области техники иногда необходимо модифицировать или выбрать стадии синтеза или реакционные схемы на основе существующих воплощений.
Если не указано иное, термин «С1-3-алкил» используется для обозначения линейной или разветвленной насыщенной углеводородной группы, состоящей из 1-3 атомов углерода. С1-3-Алкильная группа включает С1-2- и С2-3-алкильные группы, и т.д. С1-3-Алкильная группа может быть одновалентной (такой как метил), двухвалентной (такой как метилен) или поливалентной (такой как метин). Примеры С1-3-алкильной группы включают, но без ограничения, метил (Ме), этил (Et), пропил (включая н-пропил и изопропил), и т.п.
Настоящее раскрытие будет подробно описано ниже с помощью примеров, которые не предназначены для ограничения настоящего раскрытия.
Все растворители, используемые в настоящем раскрытии, коммерчески доступны и могут использоваться без дополнительной очистки.
В настоящем раскрытии используются следующие аббревиатуры: r.t. расшифровывается как комнатная температура; TГФ расшифровывается как тетрагидрофуран; NMP расшифровывается как N-метилпирролидон; MeSO3H расшифровывается как метансульфоновая кислота; DME расшифровывается как диметоксиэтан; DCM расшифровывается как дихлорметан; Xphos расшифровывается как 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил; EtOAc расшифровывается как этилацетат; MeOH расшифровывается как метанол; ацетон расшифровывается как ацетон; 2-Me-TГФ расшифровывается как 2-метилтетрагидрофуран; и IPA расшифровывается как изопропанол.
Соединения называют с помощью ручного руководства или программы ChemDraw®, и для коммерчески доступных соединений используют названия по справочнику поставщиков.
Метод порошковой рентгеновской дифракции (XRPD), используемый в настоящем раскрытии
Модель прибора рентгеновский дифрактометр Bruker D8.
Метод испытания: для анализа XRPD используют 10-20 мг образца.
Детализированные параметры XRPD следующие:
рентгеновская трубка: Cu, kα (λ=1,54056Å);
напряжение на рентгеновской трубке 40 кВ, сила электрического тока в трубке 40 мА;
расходящаяся щель 0,60 мм;
щель детектора 10,50 мм;
противорассеивающая щель 7,10 мм;
диапазон сканирования 3-40 град или 4-40 град;
размер шага 0,02 град;
длина шага 0,12 секунд;
скорость вращения диска для образца 15 об/мин.
Метод дифференциальной сканирующей калориметрии (ДСК), используемый в настоящем раскрытии
Модель прибора дифференциальный сканирующий калориметр ТА Q2000.
Метод испытания: для испытания тестовый образец (примерно 1 мг) помещают в алюминиевый тигель для ДСК. В токе 50 мл/мин N2 образец нагревают от 30°С до 300°С (или 350°С) со скоростью нагревания 10°С/мин.
Метод термогравиметрического анализа, используемый в настоящем раскрытии
Модель прибора термогравиметр ТА Q5000IR.
Метод испытания: образец (2-5 мг) для испытания помещают в платиновый тигель для ТГА. В токе 25 мл/мин N2 образец нагревают от комнатной температуры до 350°С или 20% потери массы со скоростью нагревания 10°С/мин.
Метод динамической сорбции паров (DVS), используемый в настоящем раскрытии
Модель прибора анализатор динамической сорбции паров SMS DVS Advantage.
Условия испытания: образец (10-15 мг) для испытания помещают в лодочку для образцов DVS.
Детализированные параметры DVS следующие:
температура 25°С;
равновесие dm/dt=0,01 %/мин (самое короткое время 10 мин и самое длинное время 180 мин);
сушка: сушат в течение 120 мин при 0% RH;
градиент RH (%) при испытании 10%;
интервал градиента RH (%) при испытании: 0% - 90% - 0%.
Классификация оценки гигроскопичности приводится ниже.
Примечание: ΔW% представляет собой увеличение массы образца за счет поглощения влаги при 25 ± 1°C и 80 ± 2% RH.
Технический эффект
Кристаллическая форма А соединения формулы (I) устойчива, слегка гигроскопична и меньше повреждается под действием света и тепла.
Соединение формулы (I) может существенно снизить оценку NAS, улучшить состояние воспаления и иметь некоторую дозозависимость, существенно улучшить состояние стеатоза печени, существенно улучшить функцию печени и уменьшить повреждение печени, улучшить состояние фиброза печени и иметь некоторую дозозависимость.
Краткое описание чертежей
Фиг. 1 представляет собой вид XRPD кристаллической формы А соединения формулы (I) с использованием излучения Cu-Kα.
Фиг. 2 представляет собой кривую ДСК кристаллической формы А соединения формулы (I).
Фиг. 3 представляет собой кривую ТГА кристаллической формы А соединения формулы (I).
Фиг. 4 представляет собой картину DVS кристаллической формы А соединения формулы (I).
Фиг. 5 представляет собой вид XRPD кристаллической формы А соединения формулы (I) с использованием излучения Cu-Kα.
Подробное описание изобретения
Для того, чтобы лучше понимать суть настоящего раскрытия, настоящее раскрытие дополнительно поясняется ниже в сочетании с конкретными примерами, но конкретные примеры не предназначены для ограничения объема настоящего раскрытия.
Пример 1. Получение соединения формулы (I)

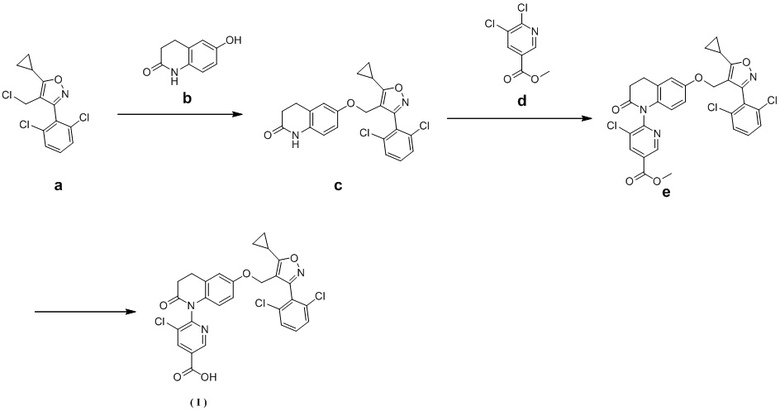
Стадия 1. Синтез промежуточного соединения с
Взвешивают а (500,62 г, 1,65 моль) и b (323,84 г) и добавляют к ДМФА (5,0 л). Смесь перемешивают до прозрачного состояния, и затем добавляют фосфат калия (877,10 г, 4,13 моль). Реакционный раствор нагревают до 50°С, и проводят реакцию при перемешивании в течение 16 часов. Реакционный раствор охлаждают до 20°С. Реакционный раствор медленно выливают в воду (40 л) при перемешивании, и в осадок выпадает большое количество твердого вещества. После перемешивания в течение 15 мин смесь фильтруют, и остаток на фильтре промывают небольшим количеством воды. Остаток на фильтре переносят в роторный испаритель и сушат методом роторного испарения, и получают сырой продукт реакции с (927,65 г). Сырой продукт реакции с (927,65 г) добавляют к этанолу (2,5 л). Смесь нагревают до 100°С и перемешивают в течение 1 часа. Затем смесь медленно охлаждают до 20°С и дополнительно перемешивают в течение 16 часов. Суспензию фильтруют, и получают белое твердое вещество. Твердое вещество переносят в роторный испаритель, сушат методом роторного испарения, и получают промежуточное соединение с (584,63 г). 1H NMR (400 МГц, CDCl3) δ = 8,62 (ушс, 1H), 7,43 – 7,38 (м, 2H), 7,36 - 7,30 (м, 1H), 6,71 - 6,54 (м, 3H), 4,76 (с, 2H), 2,94 - 2,82 (м, 2H), 2,64 - 2,54 (м, 2H), 2,16 (тт, J=5,1, 8,5 Гц, 1H), 1,33 - 1,24 (м, 2H), 1,17 - 1,09 (м, 2H).
Стадия 2. Синтез промежуточного соединения е
В 10-л трехгорлую реакционную колбу в атмосфере азота загружают толуол (5,5 л). При 20°С добавляют промежуточное соединение с (551,12 г, 1,28 моль), d (396, 12 г, 1,92 моль) и затем карбонат цезия (834,98 г, 2,36 моль) с последующим добавлением трис(дибензилиденацетон)дипалладия (29,42 г, 32,13 ммоль) и 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (39,98 г, 64,21 ммоль). Систему греют на масляной бане при температуре масляной бани 115°С, и смесь реагирует при механическом перемешивании в течение 48 часов. Реакционный раствор охлаждают до 20°С и фильтруют через диатомовую землю (1,0 кг). Фильтрат (примерно 5 л) разбавляют этилацетатом (8 л) и промывают водой (6 л × 2) и затем крепким рассолом (6 л × 1). Органическую фазу концентрируют досуха методом роторного испарения, и получают желтое масло (1,12 кг). Желтое масло (1,12 кг) добавляют к метанолу (1,2 л) и перемешивают в течение 2 часов. Появляется большое количество желтого твердого вещества. Желтое твердое вещество отфильтровывают, и остаток на фильтре промывают небольшим количеством холодного метанола. Остаток на фильтре переносят в роторный испаритель и сушат методом роторного испарения, и получают сырой продукт реакции промежуточное соединение е (492 г).
Описанный выше сырой продукт реакции промежуточное соединение е (492 г, сырой продукт) суспендируют в 5,0 л этилацетата. Систему греют на масляной бане при температуре масляной бани 100°С. После перемешивания в течение 2 часов система становится прозрачной. Систему охлаждают естественным путем до 20°С, и затем в осадок выпадает желтое твердое вещество. Смесь перемешивают еще в течение 16 часов. Систему фильтруют, и остаток на фильтре промывают небольшим количеством этилацетата. Твердое вещество сушат методом роторного испарения, и получают желтое твердое вещество 1 (221,56 г).
Полученное выше желтое твердое вещество 1 (221,56 г) растворяют в 2,5 л тетрагидрофурана, и добавляют активированный уголь (110,78 г). Систему перемешивают при 50°С в течение 16 часов. Систему охлаждают до 20°С и затем фильтруют через диатомовую землю (250 г). Фильтрат концентрируют досуха методом роторного испарения, и получают промежуточное соединение е (220,11 г).
ЖХМС (ESI): C29H22Cl3N3O5 [M+H]+: 597.9, 599.8
1H ЯМР (400 МГц, CDCl3) δ = 9,11 (д, J=2,01 Гц, 1 H), 8,49 (д, J=2,01 Гц, 1 H), 7,28 - 7,40 (м, 3 H), 6,69 (д, J=2,76 Гц, 1 H), 6,50 (дд, J=8,91, 2,89 Гц, 1 H), 6,03 (д, J=8,78 Гц, 1 H), 4,74 (с, 2 H), 3,99 (с, 3 H), 2,95 - 3,10 (м, 2 H), 2,75 - 2,85 (м, 2 H), 2,13 (тт, J=8,41, 5,02 Гц, 1 H), 1,62 (с, 1 H), 1,22 - 1,29 (м, 2 H), 1,06 - 1,18 (м, 2 H).
Стадия 3
Промежуточное соединение е (220,11 г, 367,55 ммоль) растворяют в 2,5 л тетрагидрофурана, и раствор охлаждают до 5°С. К вышеупомянутой системе постепенно, по каплям, добавляют раствор гидроксида натрия (13,97 г, 349,17 ммоль) в воде (650 мл) в течение примерно 40 минут, в то же время поддерживая наружную температуру 4-8°С. Смесь реагирует при перемешивании еще в течение 1 часа. К реакционному раствору добавляют 5 л воды. Смесь экстрагируют метил-трет-бутиловым эфиром (3 л × 3). Раствор расслаивается, и органическую фазу отбрасывают. Доводят рН водной фазы до 3-4 1 моль/л хлороводородной кислотой и затем экстрагируют этилацетатом (6 л × 1). Раствор расслаивается, и водную фазу отбрасывают. Органическую фазу концентрируют досуха методом роторного испарения, и получают 237,65 г сырого продукта реакции. Сырой продукт реакции добавляют к 500 мл ацетонитрила и перемешивают при 20°С в течение 24 часов. Смесь фильтруют, и остаток на фильтре промывают ацетонитрилом (200 мл). Остаток на фильтре сушат методом роторного испарения, и получают соединение формулы (I). 1H ЯМР (400 МГц, d4-MeOH) δ = 9,09 (д, J=2,0 Гц, 1H), 8,59 (д, J=2,0 Гц, 1H), 7,52 - 7,41 (м, 3H), 6,75 (д, J=2,8 Гц, 1H), 6,53 (дд, J=2,9, 8,7 Гц, 1H), 6,07 (д, J=9,0 Гц, 1H), 4,85 (с, 2H), 3,10 - 3,00 (м, 2H), 2,83 - 2,72 (м, 2H), 2,30 (квин, J=6,8 Гц, 1H), 1,20 - 1,16 (м, 4H).
Пример 2. Получение кристаллической формы А соединения формулы (I)
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл метанола, и смесь равномерно перемешивают с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл этанола, и смесь равномерно перемешивают с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл ацетона, и смесь равномерно перемешивают с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл ацетонитрила, и смесь равномерно перемешивают с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл этилацетата, и смесь равномерно перемешивают с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 200 мкл тетрагидрофурана, и смесь растворяют с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют 500 мкл воды, и смесь равномерно перемешивают или растворяют с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют раствор смесь (500 мкл) метанола и воды, объемное соотношение 1:1, и смесь равномерно перемешивают или растворяют с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют раствор смесь (500 мкл) этанола и воды, объемное соотношение 1:1, и смесь равномерно перемешивают или растворяют с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Взвешивают 50 мг соединения формулы (I) и добавляют в 1,5-мл флакон для высокоэффективной жидкостной хроматографии. Соответственно, добавляют раствор смесь (500 мкл) ацетона и воды, объемное соотношение 1:2, и смесь равномерно перемешивают или растворяют с помощью ультразвука. Образец суспензии помещают в шейкер с постоянной температурой (40°С) и перемешивают в течение 2 суток. Растворенный образец центрифугируют при высокой скорости, берут супернатант и загружают в центрифужную пробирку. Отверстие пробирки оборачивают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия. Супернатант оставляют испаряться, и получают кристаллическую форму А соединения формулы (I).
Пример 3. Исследование гигроскопичности кристаллической формы А соединения формулы (I)
Материалы анализа:
анализатор динамической сорбции паров SMS DVS Advantage.
Метод анализа:
для испытания берут 10-15 мг кристаллической формы А соединения формулы (I) и помещают в лодочку для образцов DVS.
Результаты анализа
Спектр DVS кристаллической формы А соединения формулы (I) показан на фиг. 4, где ΔW равна 0,5834%.
Выводы из анализа
Увеличение массы кристаллической формы А соединения формулы (I) за счет поглощения влаги при 25°С и 80% RH составляет 0,5834%, что показывает, что кристаллическая форма А соединения формулы (I) слегка гигроскопична.
Пример 4. Испытание на устойчивость твердого вещества кристаллической формы А соединения формулы (I)
Согласно «Guidelines for the Stability Testing of Drug Substances and Drug Products» (Chinese Pharmacopoeia 2015 Edition Part IV general rules 9001), устойчивость кристаллической формы А соединения формулы (I) проверяют при высокой температуре (60°C, открыто), высокой влажности (комнатная температура/относительная влажность 92,5%, открыто) и сильном освещении (5000 люкс, герметезировано).
Взвешивают 5 мг кристаллической формы А соединения формулы (I) и помещают на дно стеклянного сосуда для образцов с образованием тонкого слоя. В случае образцов, помещаемых в условия высокой температуры и высокой влажности, отверстие сосуда закрывают бумагой из алюминиевой фольги, и в бумаге из алюминиевой фольги пробивают небольшие отверстия для уверенности, что образец может полностью контактировать с окружающим воздухом. В случае образцов, помещаемых в условия сильной освещенности, отверстие сосуда закрывают бумагой из алюминиевой фольги. На 5-ый и 10-ый день берут образцы от образцов, помещенных в различные условия, и проверяют XPRD, и результаты испытания сравнивают с результатами в начале испытания в день 0. Результаты испытания приводятся ниже в таблице 2.
Таблица 2. Результаты испытания на устойчивость твердого вещества
Вывод. Кристаллическая форма А соединения формулы (I) имеет хорошую устойчивость в условиях высокой температуры, высокой влажности и сильного освещения.
Пример 5. Анализ соединения формулы (I) на эффективность in vivo
1. План анализа
Построение модели в этом анализе включает две стадии: кормление кормом с высоким содержанием жира и индукция CCl4. Сначала мышей кормят кормом с высоким содержанием жира для того, чтобы индуцировать неалкогольную жирную печень. Отбирают мышей с массой тела >35 г и продолжают кормить кормом с высоким содержанием жира, причем в то же время вводят 25% CCl4 (0,5 мг/кг) интраперитонеальной инъекцией дважды в неделю в течение четырех недель.
День, когда начинают введение CCl4, обозначают как день 0, и время, когда начинают введение CCl4, обозначают как час 0. В день, когда начинают введение CCl4, начинают введение с помощью желудочного зонда. Здоровой контрольной группе, модельной группе, 1% гидроксипропилцеллюлоза (НРМС), и контрольной группе РХ104 вводят объем 5 мл/кг один раз в день в течение 4 недель (28 дней), в то время как группе-модели введения соединения формулы (I) и соответствующего носителя (40% ПЭГ400/10% солютола/50% воды) вводят объем 5 мл/кг в течение первых 13 дней (день 0 – день 12) и 10 мл/кг в течение следующих 15 дней (день 13 – день 27) один раз в день. Момент времени инъекции CCl4 должен отстоять на 4 часа или дольше от момента времени первого ведения в этот день.
Анализ проводят раздельно в 7 группах, а именно, в здоровой контрольной группе, группе-модели с 1% НРМС, группе с эталонным соединением (РХ104), группе с испытываемым соединением (соединение формулы (I), три дозы) и группе-модели с соответствующим носителем.
Здоровая контрольная группа состоит из 6 нормальных мышей, которых на протяжении анализа кормят обычным кормом без инъекции CCl4.
В группе модели и группе введения используют 48 мышей с ожирением. Каждая группа состоит из 8 мышей. После включения в группу мышей инъецируют интраперитонеально CCl4, и вводят различные дозы лекарств или носителя, соответственно.
Данные анализа приводятся в виде среднее ± ст.-кв.ош. Используют программу для анализа Graphpad Prism6 для сравнения между двумя группами. Выбирают анализ методом Т-критерия. #p<0,05, ##p<0,01, ###p<0,001: сравнение со здоровой контрольной группой; *p<0,05, **p<0,01, ***p<0,001: сравнение с группой-моделью, группу с PX-104 сравнивают с группой моделью (1% HPMC), и группу с соединением формулы (I) сравнивают с группой-моделью с носителем.
2. Улучшение оценки NAS с помощью соединения формулы (I)
Для анализа патологии печени на животных моделях неалкогольного стеагепатита всесторонне оценивают терапевтическое действие соединения на NAFLD в трех аспектах: стеатоза гепатоцитов, баллонирующей дистрофии гепатоцитов и накопления клеток воспаления в дольке печени, с учетом клиникопатологического диагноза и критериев оценки для NAFLD и использованием оценки активности NAFLD (NAS).
Таблица 3. Критерии оценки для неалкагольного стеагепатита
При сравнении со здоровой контрольной группой оценки NAS двух групп-моделей существенно возрастают (p<0,001); положительный контроль PX104 в дозе 15 мг/кг (p<0,001 против группы-модели с 1% HPMC) может существенно снизить оценку NAS; при сравнении группы-модели с носителем (40% ПЭГ400/10% солютола/50% воды), испытываемое соединение формулы (I) может существенно снизить оценки NAS в тестовых дозах 7,5 мг/кг, 15 мг/кг и 45 мг/кг. Результаты приводятся в таблице 4.
Таблица 4. Оценка NAS
###
***
###
***
**
***
При сравнении со здоровой контрольной группой оценки воспаления двух групп-моделей существенно возрастают; эталонное соединение PX104 в дозе 15 мг/кг (p<0,001 против группы-модели с 1% HPMC) может существенно улучшить оценку воспаления. При сравнении с группой-моделью с носителем испытываемое соединение формулы (I) во всех тестовых дозах 7,5 мг/кг, 15 мг/кг и 45 мг/кг показывает улучшение при воспалении и имеет некоторую дозозависимость. Результаты приводятся в таблице 5.
Таблица 5. Анализ улучшения при воспалении
###
***
###
**
***
***
При сравнении со здоровой контрольной группой степень стеатоза в двух группах-моделях существенно возрастают; эталонное соединение PX104 показывает существенное улучшение при стеатозе печени в дозе 15 мг/кг (p<0,001 против группы-модели с 1% HPMC). При сравнении с группой-моделью с носителем испытываемое соединение формулы (I) показывает улучшение при стеатозе печени в тестовых дозах 7,5 мг/кг, 15 мг/кг и 45 мг/кг. Результаты приводятся в таблице 6.
Таблица 6. Анализ стеатоза печени
###
***
###
**
***
***
Ни одна из мышей не показала при анализе баллонирующую дистрофию гепатоцитов. Результаты приводятся в таблице 7.
Таблица 7. Анализ баллонирующей дистрофии гепатоцитов
Примечание: результат 0,021@ получают из-за результата по баллонирующей дистрофии у одной мыши из этой группы 0,17. После G-критерия эта величина определяется как анормальная величина.
3. Улучшение при фиброзе печени с помощью соединения формулы (I)
Все срезы, окрашенные сириусом красным, полностью сканируют цифровым слайд-сканером pathoscope 4S. Выбирают произвольно 2 поля зрения в поле зрения 5х, и 2 поля зрения охватывают 85% площади ткани печени. Затем используют программу Image pro-plus 6.0 для количественного анализа, и вычисляют площадь в срезе, охваченную фиброзом. При сравнении со здоровой контрольной группой степень фиброза в двух группах-моделях существенно увеличилась (p<0.001); эталонное соединение PX-104 показывает значительное улучшение в фиброзе печени при дозе 15 мг/кг (p<0,05 против группы-модели с 1% HPMC). При сравнении с группой-моделью с носителем испытываемое соединение формулы (I) в тестовых дозах 7,5 мг/кг, 15 мг/кг и 45 мг/кг показывает улучшение при фиброзе печени и имеет некоторую дозозависимость. Результаты приводятся в таблице 8.
Таблица 8. Анализ фиброза печени
###
*
###
*
**
Вывод
Анализ образованной модели типичной NASH характеризуется существенно повышенной оценкой NAS и явным фиброзом печени.
Результаты этого анализа показывают, что соединение формулы (I) может существенно снизить оценку NAS, улучшает состояние воспаления и имеет некоторую дозозависимость, существенно улучшает состояние стеатоза печени, существенно улучшает функцию печени и уменьшает повреждение печени, улучшает состояние фиброза печени и имеет некоторую дозозависимость.
Пример 6. Анализ биологической активности in vitro соединения формулы (I)
Биохимический анализ FXR
Цель анализа
Активацию реакции связывания FXR соединением обнаруживают амплифицированным люминесцентным бесконтактным гомогенным анализом (альфаскрин).
Материалы для анализа
1. Белок: меченный глутатион-S-трансферазой белок человека FXR (Invitrogen).
2. Соактиватор: меченный биотином соактиватор стероидного рецептора (Anaspec).
3. Реагент для детекции: набор для детекции для амплифицированного люминесцентного бесконтактного гомогенного анализа (альфаскрина) (PerkinElmer).
Метод анализа
1. Разведение соединения. Испытываемое соединение получают в виде 40-мкМ раствора в ДМСО и затем разводят 3-кратно до 10 позиций концентрации. Эталонное соединение готовят в виде 400-мкМ раствора в ДМСО и затем разводят 1,5-кратно до 10 позиций концентрации. Разведенный раствор в ДМСО добавляют в микролунки 384-луночного планшета в объеме 150 мкл на лунку.
2. Меченный глутатион-S-трансферазой белок человека FXR и меченный биотином соактиватор стероидного рецептора получают в смешанном растворе в концентрации 0,4 нМ и 30 нМ, соответственно. Смешанный раствор добавляют в микролунки 384-луночного планшета в объеме 15 мкл на лунку и инкубируют в течение 1 часа при комнатной температуре.
3. Смешанный раствор гранул рецептора из набора для детекции для амплифицированного люминесцентного бесконтактного гомогенного анализа (альфаскрина) разводят 125-кратно и добавляют в микролунки 384-луночного планшета в объеме 7,5 мкл на лунку. Процедуру во время анализа проводят с защитой от света. Инкубацию выполняют при комнатной температуре в течение 1 часа.
4. Раствор смеси донорных гранул из набора для детекции для амплифицированного люминесцентного бесконтактного гомогенного анализа (альфаскрина) разводят 125-кратно и добавляют в микролунки 384-луночного планшета в объеме 7,5 мкл на лунку. Процедуру во время анализа проводят с защитой от света. Инкубацию выполняют при комнатной температуре в течение 1 часа.
5. Анализ ЕС50: используют envision с возбуждением при 680 нм, и считывают сигнал поглощения при 520-620 нм.
6. Анализ данных. Данные анализируют с помощью Prism 5.0, и вычисляют величины ЕС50 активирующего действия соединения.
Таблица 9. Активирующее действие соединения формулы (I) на FXR
Вывод
Результаты этого анализа показывают, что соединение формулы (I) оказывает существенное агонистическое действие на FXR.
| название | год | авторы | номер документа |
|---|---|---|---|
| КРИСТАЛЛИЧЕСКАЯ ИЛИ АМОРФНАЯ ФОРМА АГОНИСТОВ FXR, ПРЕДСТАВЛЯЮЩИХ СОБОЙ ПРОИЗВОДНЫЕ СТЕРОИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2800751C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА И СОЛЕВАЯ ФОРМА ИНГИБИТОРА TGF-βRI И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2018 |
|
RU2750702C1 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ИНГИБИТОРА ATR И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2832707C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА СОЕДИНЕНИЯ, ПРЕДСТАВЛЯЮЩЕГО СОБОЙ ПРОЛЕКАРСТВО ЛАНОСТЕРИНА, И ЕЕ ПРИМЕНЕНИЕ В ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННОГО ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ КАТАРАКТЫ | 2019 |
|
RU2766088C1 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ПРОИЗВОДНОГО ТИОФЕНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2022 |
|
RU2830948C1 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ТРИЦИКЛИЧЕСКОГО СОЕДИНЕНИЯ И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2775753C1 |
| Соединение ингибитора FGFR в твердой форме и способ его получения | 2020 |
|
RU2810067C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА А СОЕДИНЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2016 |
|
RU2699030C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА И СОЛЕВАЯ ФОРМА СОЕДИНЕНИЯ ПИРИДОИМИДАЗОЛА И СООТВЕТСТВУЮЩИЙ СПОСОБ ПОЛУЧЕНИЯ | 2019 |
|
RU2769050C1 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА TLR7/TLR8 | 2019 |
|
RU2792005C2 |
Изобретение относится к кристаллической форме А соединения формулы (I), характеризующейся порошковой рентгенограммой с характеристическими дифракционными пиками при следующих углах 2θ: 11,86±0,2°, 12,72±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 24,18±0,2° и 25,27±0,2°. Способ получения кристаллической формы А соединения формулы (I) по изобретению, осуществляют путем (а) добавления соединения формулы (I) в растворитель; (b) перемешивания при 30-50°С в течение 40-55 часов и (с) центрифугирования, и последующего испарения растворителя и получения кристаллической формы А соединения формулы (I); где растворителем является спирт, тетрагидрофуран, вода, ацетон, ацетонитрил, этилацетат, смешанный растворитель из спирта и воды, где объемное отношение спирта к воде составляет 1:0,6 – 1:1,5, или смешанный растворитель из ацетона и воды, где объемное отношение ацетона к воде составляет 1:1,5 – 1:2,5 и спирт выбирают из метанола, этанола, изопропанола и н-пропанола. Также изобретение относится к способу получения соединения формулы (I), включающему стадии взаимодействия соединений, обозначенных структурами a, b, c, d, e (приведены в формуле изобретения). Изобретение также относится к соединению, представленному формулой е, где R1 представляет собой CН3. Кристаллическую форму А соединения формулы (I) по изобретению применяют в производстве лекарственного средства для лечения связанных с FXR заболеваний, где связанное с FXR заболевание представляет собой неалкагольное ожирение печени. Технический результат – устойчивая, слегка гигроскопичная, и менее подверженная повреждению светом кристаллическая форма А соединения (I). 5 н. и 13 з.п. ф-лы, 5 ил., 9 табл., 6 пр.
1. Кристаллическая форма А соединения формулы (I), характеризующаяся порошковой рентгенограммой с характеристическими дифракционными пиками при следующих углах 2θ: 11,86±0,2°, 12,72±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 24,18±0,2° и 25,27±0,2°;
2. Кристаллическая форма А соединения формулы (I) по п. 1, где порошковая рентгенограмма имеет характеристические дифракционные пики при следующих углах 2θ: 11,86±0,2°, 12,72±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 20,38±0,2°, 22,60±0,2°, 23,80±0,2°, 24,18±0,2° и 25,27±0,2°.
3. Кристаллическая форма А соединения формулы (I) по п. 2, где порошковая рентгенограмма имеет характеристические дифракционные пики при следующих углах 2θ: 11,86±0,2°, 12,72±0,2°, 13,67±0,2°, 16,15±0,2°, 17,40±0,2°, 19,72±0,2°, 20,38±0,2°, 22,60±0,2°, 23,80±0,2°, 24,18±0,2°, 25,27±0,2° и 26,57±0,2°.
4. Кристаллическая форма А соединения формулы (I) по п. 3, где порошковая рентгенограмма является такой, как показано на фиг. 1.
5. Кристаллическая форма А соединения формулы (I) по п. 1, где порошковая рентгенограмма является такой, как показано на фиг. 5.
6. Кристаллическая форма А соединения формулы (I) по любому из пп. 1-5, характеризующаяся кривой дифференциальной сканирующей калориметрии, имеющей начальную точку эндотермического пика при 223,58°C±3°C.
7. Кристаллическая форма А соединения формулы (I) по п. 6, где кривая дифференциальной сканирующей калориметрии является такой, как показано на фиг. 2.
8. Кристаллическая форма А соединения формулы (I) по любому из пп. 1-5, характеризующаяся кривой термогравиметрического анализа, имеющей потерю массы до 0,7427%±0,2% при 111,29°C±3°C и до 3,6977%±0,2% при 202,79°C±3°C.
9. Кристаллическая форма А соединения формулы (I) по п. 8, где кривая термогравиметрического анализа является такой, как показано на фиг. 3.
10. Способ получения кристаллической формы А соединения формулы (I) по любому из пп. 1-9
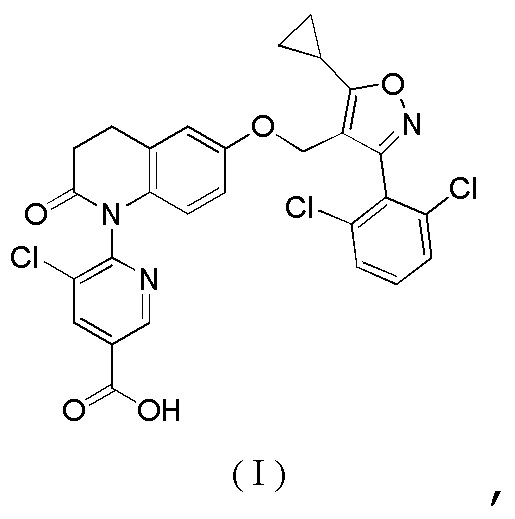
включающий
(а) добавление соединения формулы (I) в растворитель;
(b) перемешивание при 30-50°С в течение 40-55 часов и
(с) центрифугирование и последующее испарение растворителя и получение кристаллической формы А соединения формулы (I);
где растворителем является спирт, тетрагидрофуран, вода, ацетон, ацетонитрил, этилацетат, смешанный растворитель из спирта и воды, где объемное отношение спирта к воде составляет 1:0,6 – 1:1,5, или смешанный растворитель из ацетона и воды, где объемное отношение ацетона к воде составляет 1:1,5 – 1:2,5
и
спирт выбирают из метанола, этанола, изопропанола и н-пропанола.
11. Способ получения по п. 10, где растворитель является смешанным растворителем из спирта и воды, причем объемное отношение спирта к воде составляет 1:1.
12. Способ получения по п. 10, где растворитель является смешанным растворителем из ацетона и воды, причем объемное отношение ацетона к воде составляет 1:2.
13. Способ получения соединения формулы (I), включающий следующие стадии:
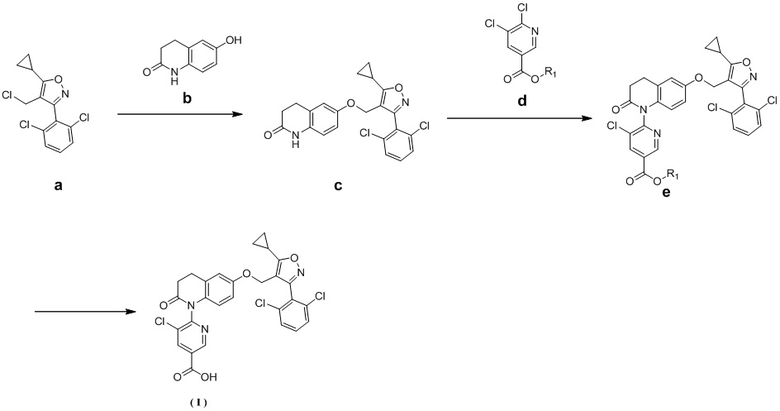
где R1 представляет собой CH3.
14. Способ получения соединения формулы (I) по п. 13, включающий следующие стадии:
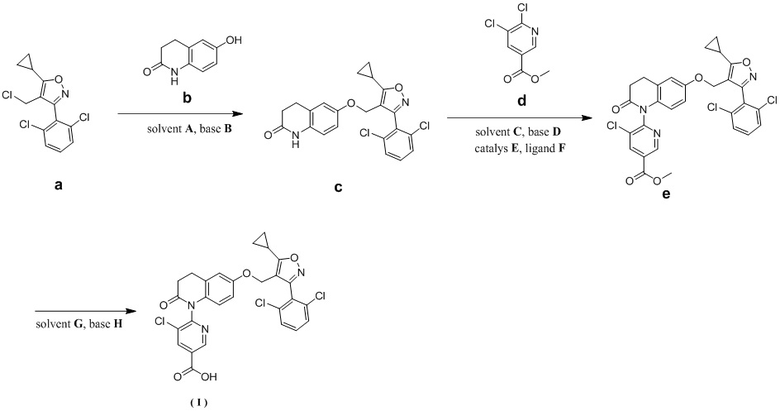
solvent – растворитель, base – основание, catalyst – катализатор, ligand – лиганд,
где
растворитель А представляет собой ДМФА;
основание В представляет собой фосфат калия;
растворитель С представляет собой толуол;
основание D представляет собой карбонат цезия;
катализатор Е представляет собой трис(дибензилиденацетон)дипалладий;
лиганд F представляет собой 2,2'-бис(дифенилфосфино)-1,1'-бинафтил;
растворитель G представляет собой тетрагидрофуран; и
основание Н представляет собой гидроксид натрия.
15. Способ получения соединения формулы (I) по п. 13 или 14, где отношение объем:масса растворителя С к промежуточному соединению с составляет 10:1, молярное отношение основания D к промежуточному соединению с составляет 2:1, молярное отношение катализатора Е к промежуточному соединению с составляет 0,025:1, и молярное отношение лиганда F к промежуточному соединению с составляет 0,05:1.
16. Соединение, представленное формулой е,
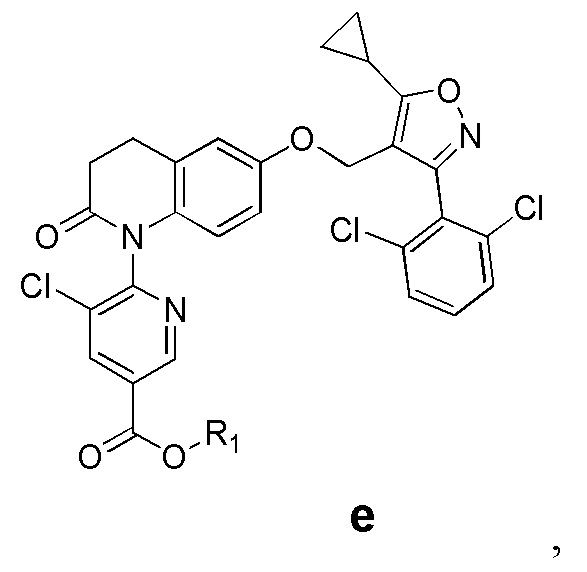
где R1 представляет собой CН3.
17. Применение кристаллической формы А соединения формулы (I) по любому из пп. 1-9 в производстве лекарственного средства для лечения связанных с FXR заболеваний.
18. Применение по п. 17, где связанное с FXR заболевание представляет собой неалкагольное ожирение печени.
| WO 2009005998 A1, 08.01.2009 | |||
| EA 200901662 A, 30.06.2010 | |||
| WO 2017218337 A1, 21.12.2017 | |||
| CN 108341822 A, 31.07.2018 | |||
| Дж | |||
| Бернштейн "Полиморфизм молекулярных кристаллов" Москва, Наука, 2007, гл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Биодоступность, с.324-330 | |||
| MINO R | |||
| CAIRA "Crystalline Polymorphism of Organic Compounds", TOPICS IN CURRENT CHEMISTRY, 1998, vol.198, pp.163-208. | |||
Авторы
Даты
2023-09-27—Публикация
2019-11-26—Подача