Изобретение относится к области органической химии - новым биологически активным соединениям - замещенным пирроло[1,2-а][1,4]диазепинонам, а именно к 7-метил-2-(4-метилфенил)-1,2,4,5-тетрагидро-ЗH-пирроло[1,2-а][1,4]диазепин-3-ону 1 формулы:

соединение 1 обладает антимикотической активностью, что позволяет предположить его использование в медицине в качестве потенциального лекарственного средства с антимикотическими свойствами.
Аналогом по структуре заявляемому соединению является 7-хлор-4-(4-этилфенил)-5,6-дигидро-4H-бензо[f]пирроло[1,2-а][1,4]диазепин 2, обладающий антимикотической активностью [Bioorg. Med. Chem. Lett. 2005, 15, 3453 -3458; doi: 10.1016/j.bmcl.2005.05.007] формулы:

Эталоном сравнения был выбран кетоконазол 3 формулы,

который широко применяется в лечебной практике и является аналогом по действию [Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - с. 918; Мед. Chem. Res. 2013, 22, 211 - 18; doi: 10.1007/s00044-012-0021-2].
Задачей изобретения является поиск в ряду замещенных пирроло[1,2-][1,4]диазепинонов веществ с выраженным антимикотическим действием и низкой токсичностью.
Поставленная задача достигается получением 7-метил-2-(4-[етилфенил)-1,2,4,5-тетрагидро-3H-пирроло[1,2-а][1,4] диазепин-3-она, который обладает антимикотической активностью.
Заявляемое соединение 1 синтезируют обработкой N-[(5-метилфуран-2ил)метил]-N-(4-метилфенил)-3-(1,3-диоксо-1,3-дигидро-2H-изоиндол-2-ил)пропанамида гидразингидратом при кипячении с обратным холодильником в течение 5 минут в этаноле. Затем образовавшийся неочищенный амин обрабатывают смесью ледяной уксусной и концентрированной соляной кислот при комнатной температуре с последующей нейтрализацией соляной кислоты NaHCO3, нагреванием реакционной смеси при 120°С и выделением целевого продукта стандартными методами синтетической органической химии по схеме:
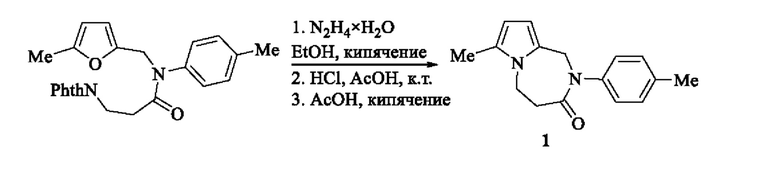
Пример 1. Получение соединения 1. К перемешиваемому раствору 1.206 г (3 ммоль) N/-[(5-метилфуран-2-ил)метил]-N\-(4-метилфенил)-3-(1,3-диоксо-1,3-дигидро-2H-изоиндол-2-ил)пропанамида в 20 мл этанола добавляют 1.3 мл гидразингидрата (50-60%). Реакционную смесь кипятят с обратным холодильником в течение 5 минут и охлаждают до комнатной температуры. Полученный осадок отфильтровывают и промывают холодным этанолом (3 ×5 мл). Растворитель упаривают досуха при пониженном давлении. Полученный остаток разбавляют 10 мл Н2О и экстрагируют СНСl3 (3×5 мл). Объединенные органические фракции промывают насыщенным раствором NaCl (3×5 мл), сушат над безводным Na2SO4 и упаривают досуха при пониженном давлении. К раствору неочищенного амина в 10 мл ледяной уксусной кислоты добавляют 1.5 мл концентрированной соляной кислоты. Реакционную смесь перемешивают в течение 24 ч при комнатной температуре. Затем к реакционной смеси порциями добавляют 1.5 г NaHCO3, кипятят с обратным холодильником в течение 2 минут и выливают в 50 мл насыщенного водного раствора NaHCO3 (50 мл). Образовавшийся осадок отфильтровывают, промывают водой (3 × 10 мл), высушивают и очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента смесь петролейный эфир/этилацетат (9:1). Продукт перекристаллизовывают из смеси петролейный эфир/этилацетат. Выход 30%. Тпл=108-109°С. Найдено, %: С, 75.38; Н, 7.16; N, 10.91. C16H18N2O. Вычислено, %: С, 75.56; Н, 7.13; N, 11. 01. ИК спектр, (КВr), νmax, см-1: 1652, 1510, 1430, 1343, 1227, 1120, 1020, 815, 742. Спектр ЯМР 1Н, (400 МГц, CDCl3), δ, м.д.: 7.19-7.14 (м, 4Н), 5.92 (д, J=3.2 Гц, 1Н), 5.86 (д, J=3.2 Гц, 1H), 4.83 (с, 2Н), 4.13 (т, J=6.4 Гц, 2Н), 3.25 (т, J=6.4 Гц, 3Н), 2.35 (с, 3Н), 2.25 (с, 3Н). Спектр ЯМР 13С (100 МГц, CDCl3), δ, м.д.: 171.4, 140.4, 136.6, 130.9, 129.7 (2С), 126.4, 125.5 (2С), 106.5, 105.6, 49.7, 42.3,34.5,21.1,12.4; m/z(%) (ЭУ, 70 эВ) 254 (70) [М+], 239 (12), 120 (100), 106 (68), 95 (33), 66 (22), 52 (45), 43 (22). Полученное соединение 1 представляет собой светло-бежевое кристаллическое вещество, растворимое в этаноле, ацетоне, хлороформе, этилацетате.

Пример 2. Для характеристики антимикотической активности соединений использовали стандартные параметры: минимальная подавляющая концентрация (МПК), которую определяли модифицированным методом двукратных серийных разведений (Методические рекомендации: Грибы рода Candida. Методы выделения, идентификации на видовом уровне и определение чувствительности к противогрибковым препаратам, Москва, 2009; МУК 4.2.1890-04 Определение чувствительности микроорганизмов к антибактериальным препаратам) и минимальная фунгинидная концентрация (МФК).
Тесты проводили с использованием культуры модельных микроорганизмов Candida albicans АТСС 10231 на питательной среде Мюллера-Хинтона с добавлением 2% глюкозы в 96-луночных полистироловых планшетах. Концентрация микроорганизмов в лунках перед началом культивирования составляла 2,5*105 КОЕ/мл. Культивирование проводили при 37°С без перемешивания. Определение МПК и высевы для определения МФК производили через 24 ч. Исследуемые соединения растворяли в диметилсульфоксиде (ДМСО) до полного растворения в концентрации 20 мг/мл и ниже, в зависимости от растворимости. Вносили в питательную среду так, чтобы количество ДМСО не превышало 5%.
Пример 3. Острую токсичность (ЛД50, мг/мл) соединения 1 определяли по методу Г. Н. Першина [Першин Г.Н. Методы экспериментальной химиотерапии // М., С.100, 1971, 109-117]. Соединение 1 вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемого соединения 1 ЛД50 составляет > 1500 мг/кг.
Согласно классификации токсичности препаратов, соединение 1 относится к V классу практически нетоксичных препаратов [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977, стр. 196]. Результаты испытаний представлены в таблице:

Как видно из таблицы, заявляемое соединение 1 сопоставимо по антимикотической активности с препаратом сравнения (Кетоконазол) по отношению к С.albicans. Таким образом, это делает возможным использование 7-метил-2-(4-метилфенил)-1,2,4,5-тетрагидро-3H-пирроло[1,2-а][1,4]диазепин-3-она 1 для создания новых лекарственных средств в качестве противогрибкового средства в отношении дрожжевых грибов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Применение 2-(4-бромфенил)-7-этил-1,2,4,5-тетрагидро-3H-пирроло[1,2-a][1,4]диазепин-3-она в качестве противогрибкового средства в отношении дрожжевых грибов | 2023 |
|
RU2809051C1 |
| ПРИМЕНЕНИЕ 7-МЕТИЛ-5-[4-(ТРИФТОРМЕТИЛ)ФЕНИЛ]-1,2,4,5-ТЕТРАГИДРО-3H-ПИРРОЛО[1,2-a][1,4]ДИАЗЕПИН-3-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2808981C1 |
| ПРИМЕНЕНИЕ 5-(4-МЕТОКСИФЕНИЛ)-7-МЕТИЛ-1,2,4,5-ТЕТРАГИДРО-3H-ПИРРОЛО[1,2-a][1,4]ДИАЗЕПИН-3-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2810715C1 |
| ПРИМЕНЕНИЕ 10-МЕТИЛ-6,7-ДИГИДРО-5H-ПИРИДО[2,3-b]-ПИРРОЛО[1,2-d][1,4]ДИАЗЕПИНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2803600C1 |
| ПРИМЕНЕНИЕ 1-МЕТИЛ-8,9-ДИМЕТОКСИ-4,5-ДИГИДРО-6H-ПИРРОЛО[1,2-a][1,4]БЕНЗОДИАЗЕПИН-6-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2808993C1 |
| ПРИМЕНЕНИЕ 5-[(1H-ИНДОЛ-3-ИЛ)МЕТИЛ]-7-МЕТИЛ-2,3-ДИГИДРО-1H-ПИРРОЛО[1,2-d][1,4]ДИАЗЕПИН-4(5H)-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2803571C1 |
| ПРИМЕНЕНИЕ 1-МЕТИЛ-5-(4-ХЛОРФЕНИЛ)-4,5-ДИГИДРО-6H-ПИРРОЛО[1,2-a][1,4]БЕНЗОДИАЗЕПИН-6-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2809148C1 |
| ПРИМЕНЕНИЕ 1-МЕТИЛ-4,5-ДИГИДРО-6H-ПИРРОЛО[1,2-a][1,4]БЕНЗОДИАЗЕПИН-6-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2809026C1 |
| ПРИМЕНЕНИЕ 4,6-ДИМЕТИЛ-1,2-ДИГИДРОПИРРОЛО[1,2-a]ПИРАЗИН-3(4H)-ОНА В КАЧЕСТВЕ ПРОТИВОГРИБКОВОГО СРЕДСТВА В ОТНОШЕНИИ ДРОЖЖЕВЫХ ГРИБОВ | 2023 |
|
RU2806191C1 |
| Применение 1-ацетил-5,6-диметил-2-(2-оксопропил)индолин-3-она в качестве противогрибкового средства в отношении дрожжевых грибов | 2023 |
|
RU2809146C1 |
Изобретение относится к области органической химии - новым биологически активным соединениям - замещенным пирроло[1,2-а][1,4]диазепинонам. Предложено применение 7-метил-2-(4-метилфенил)-1,2,4,5-тетрагидро-3H-пирроло[1,2-а][1,4]диазепин-3-она в качестве противогрибкового средства в отношении дрожжевых грибов. Технический результат: получено соединение, обладающее выраженной антимикотической активностью в отношении дрожжевых грибов, а также низкой токсичностью. 1 табл., 3 пр.

Применение 7-метил-2-(4-метилфенил)-1,2,4,5-тетрагидро-3H-пирроло[1,2-a][1,4]диазепин-3-она:
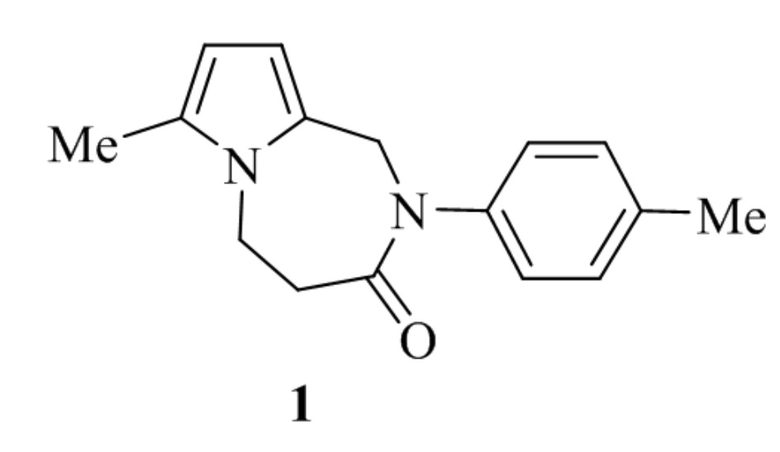
в качестве противогрибкового средства в отношении дрожжевых грибов.
| US 9040524 B2, 26.05.2015 | |||
| WO 2002034752 A1, 02.05.2002 | |||
| 2-ЗАМЕЩЕННЫЕ-1,2,4,5-ТЕТРАГИДРО-3H-ПИРРОЛО[1,2-a][1,4]ДИАЗЕПИН-3-ОНЫ | 2011 |
|
RU2472795C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 7-АЛКИЛ-2,3-ДИГИДРО-1Н-ПИРРОЛО[1,2-d][1,4]ДИАЗЕПИН-4(5Н)-ОНА | 2017 |
|
RU2659390C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИРРОЛО[1,2-а][1,4]ДИАЗЕПИНА | 2006 |
|
RU2323939C1 |
Авторы
Даты
2023-12-06—Публикация
2023-04-27—Подача