Способ относится к области химии и может быть использован для получения метастабильного поликристаллического соединения с формулой Bi2Ge2O7.
Система Bi2O3-GeO2 представляет очень большой научный и практический интерес, благодаря образующимся на ее основе стабильным и метастабильным соединениям.
В области стабильного равновесия известны 3 соединения:
1. Bi12GeO20 с кристаллической структурой силленита (КСС) имеет высокую научную и практическую значимость, благодаря высоким пьезоэлектрическим, фоторефрактивным, фотопроводящим, магнитооптическим и электрооптическим свойствами. Он используется для создания устройств оптической обработки информации, вызывает высокий интерес для получения миниатюрных и пассивных микроволновых керамических компонентов с высокой производительностью для мобильных устройств, а также в качестве перспективного фотокатализатора.
2. Bi4Ge3O12 с кристаллической структурой эвлитина (КСЭ) является уникальным сцинтилляционным материалом, а его высокая радиационная стойкость позволяет применять его в качестве детекторов с актикомптоновской защитой, в рентгеновских и позитронных томографах, в диагностических медицинских устройствах и астрофизике. В последние годы его также рассматривают как перспективный материал для анодов в литий-ионных батареях большой емкости [Т.В. Бермешев, В.П. Жереб, М.П. Бундин, О.В. Юшкова, А.С. Ясинский, Д.С. Ворошилов, В.М. Беспалов, А.Н. Залога, Е.Ю. Подшибякина, О.В. Якивьюк, Е.В. Мазурова. Особенности затвердевания расплава 2Bi2O3 ⋅ 3GeO2 при различных условиях охлаждения // Неорганические материалы. 2022. Т. 58. №4. С.451-463].
3. Bi2Ge3O9 с кристаллической структурой бенитоита (КСБ) представляет интерес в качестве материала для рентгеновских спектрометров и фотоакустических дефлекторных устройств, для генерации стимулированного излучения, а также в качестве перспективного материала керамических подложек для миниатюрных и высокопроизводительных пассивных компонентов в системах СВЧ-связи [Бермешев Т.В., Жереб В.П., Бундин М.П., Ясинский А.С., Юшкова О.В., Ворошилов Д.С., Залога А.Н., Ковалева А.А., Якивьюк О.В., Самойло А.С., Мазурова Е.В. Синтез Bi2Ge3O9 //Неорганические материалы. 2022. Т. 58. №12. С.1320-1330].
В области же метастабильного равновесия известны 2 широкие области соединений:
1. δ-Bi2O3 с гранецентрированной кубической решеткой и структурой типа флюорита - является уникальным суперионным проводником, обладающим рекордно высокой кислородно-ионной проводимостью, превышающей проводимость всех известных твердых электролитов. Оксиды со структурой δ-Bi2O3 являются также фотокатализаторами, перспективными для очистки воздуха и сточных вод от токсичных органических соединений. На их основе предложены эффективные и недорогие адсорбенты для нейтрализации изотопов радиоактивного йода и удаления токсичных соединений селена из водных растворов, для каталитического преобразования нитробензолов в анилины, а также окислители в реакции химического циклического сжигания (CLC). В последнее время, как показали исследования, суперионные твердые электролиты перспективны как механокалорические материалы - вещества, которые можно использовать в устройствах твердотельного охлаждения [Т.В. Бермешев, В.П. Жереб, М.П. Бундин, А.С. Ясинский, О.В. Юшкова, Д.С. Ворошилов, А.С. Самойло, Е.В. Мазурова, А.Н. Залога, О.В. Якивьюк, В.М. Беспалов. Влияние термообработки расплава Bi2O3, содержащего 22 мол. % SiO2, на состояние образующейся при кристаллизации метастабильной δ*-фазы // Неорганические материалы. 2022. Т. 58. №6. С.625-632].
2. Bi2GeO5 со слоистой кристаллической структурой типа Ауривиллиуса - является сегнетоэлектриком с высокой температурой Кюри, обладает высокой ионной проводимостью по кислороду, а также вызывает большой интерес для водородной энергетики и экологии благодаря своим фотокаталитическим свойствам в оптическом диапазоне излучений, в том числе для дезактивации токсичных органических соединений и оксидов азота (NO). Он также рассматривался в качестве катализатора для окислительной димеризации метана и для синтеза перспективных стеклокерамических материалов [Т.В. Бермешев, В.П. Жереб, И.Ю. Губанов, А.Б. Набиулин, В.П. Ченцов, В.В. Рябов, А.С. Ясинский, Н.В. Мердак, О.В. Юшкова, М.П. Бундин, В.М. Беспалов, Е.В. Мазурова, Д.С. Ворошилов, Е.Ю. Подшибякина. Моделирование условий охлаждения германата висмута Bi2GeO5 // Письма в ЖТФ. 2021. Т. 47, №15. С.27-30].
В системе Bi2O3-GeO2 получено соединение с формулой Bi2Ge2O7. Учитывая важность и большое разнообразие возможных сфер применения стабильных и метастабильных соединений, получаемых на базе системы Bi2O3-GeO2, разработка надежного способа получения соединения в данной системе имеет большой научный интерес.
Таким образом, основной задачей изобретения является разработка способа получения соединения с формулой Bi2Ge2O7.
Выбор граничных параметров масс. % Bi2O3 - 32 и GeO2 - 68 обусловлен требованием к максимальной чистоте получаемого продукта от посторонних примесных фаз. При увеличении количества исходного оксида германия, вводимого в сплав, увеличивается и количество примеси GeO2, остающейся в конечном материале. При увеличении же Bi2O3 также идет увеличение примесей, но уже с образованием GeO2 в другой модификации, либо с образованием примесной метастабильной η- Bi2GeO5.
Минимального содержания примеси GeO2 (до 2 масс. %) удается добиться только при указанном содержании исходных компонентов. При увеличении или уменьшении содержания оксида германия в исходной навеске - количество примесных фаз (GeO2, Bi2GeO5, Bi4Ge3O12) будет выше.
Выбор граничных параметров температуры сплавления исходных компонентов 1200±10°С обусловлен температурами границ высокотемпературных областей расплавов в этой системе, каждая из которых имеет свои свойства и строение. Известно, что на фазовой диаграммах систем Bi2O3 - GeO2 [Zhereb V.P., Skorikov V.M. Metastable States in Bismuth-Containing Oxide Systems // Inorganic Materials. 2003. Vol.39. Suppl. 2. P. S121-S145] область расплава может быть разделена на 3 температурные зоны А, В и С (фиг.1, 2). Зона «С» обладает целым рядом неоспоримых преимуществ: низкая вязкость, высокая подвижность атомов, тонкие особенности строения расплава. Все эти факторы обеспечивают максимально быстрое взаимодействие реагентов между собой и предоставляют идеальные условия для сплавления исходных компонентов.
Выбор времени выдержки 60 мин должно обеспечивать полное взаимное растворение исходных компонентов друг в друге, а также обеспечивать переход расплава в однородное и жидкотекучее состояние. Более длительное время выдержки нецелесообразно экономически. Меньшее время выдержки может привести к неполному взаимодействию исходных реагентов между собой.
Первая ступень охлаждения до 1125±5°С обеспечивает снижение градиента температур перед окончательным охлаждением. Выдержка 40 минут при температуре 1125±5°С обеспечивает более полное взаимодействие расплава с оксидами платины на дне и стенках контейнера при указанной температуре.
Вторая ступень - охлаждение с печью до комнатной температуры должна обеспечивать надежное образование соединения Bi2Ge2O7 и сохранение его до комнатной температуры. Более быстрое охлаждение может привести к частичному или полному переходу расплава в аморфное состояние, или же частичному или полному распаду метастабильного соединения Bi2Ge2O7.
Сущность изобретения поясняется результатами рентгенофазового и микроструктурного анализа.
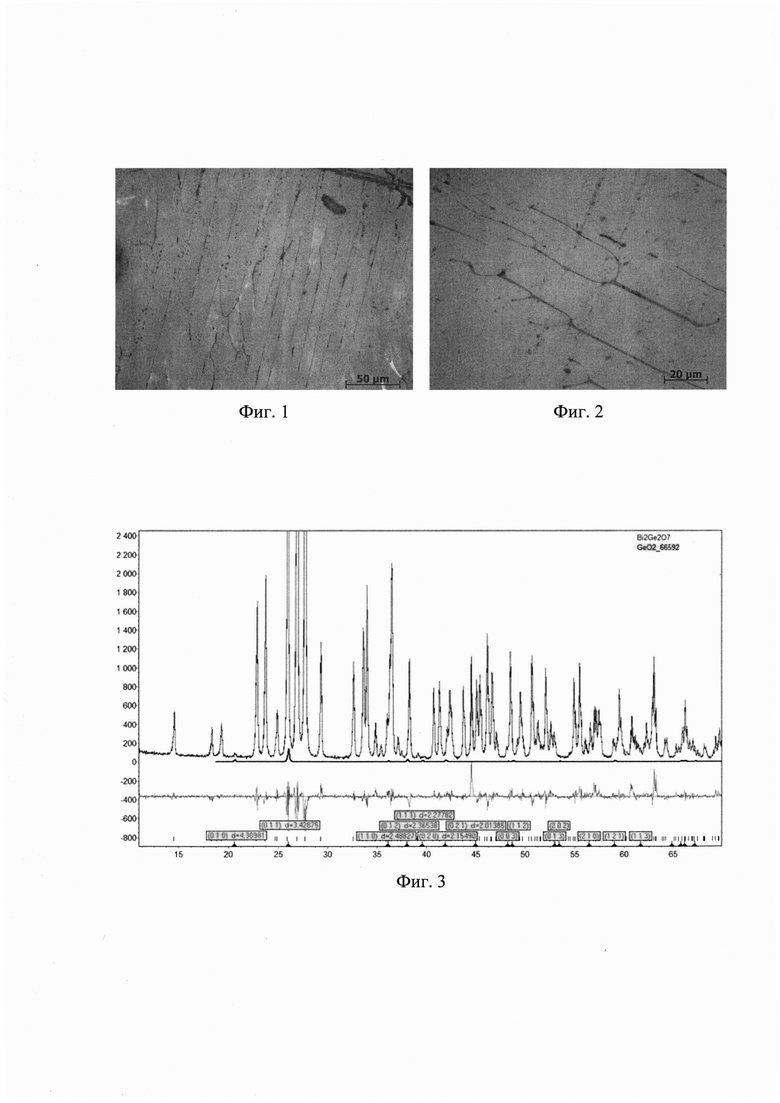
Фиг. 1 - Микроструктура образца Bi2Ge2O7, полученного охлаждением с печью от температуры 1125°С, увеличение х500.
Фиг. 2 - Микроструктура образца Bi2Ge2O7, полученного охлаждением с печью от температуры 1125°С, увеличение х1000.
Фиг. 3 - Дифрактограмма образца Bi2Ge2O7, полученного охлаждением с печью от температуры 1125°С (Bi2Ge2O7 + до 2 масс. % GeO2).
На данном этапе избавиться полностью от небольшой примеси GeO2 не удается. Полученные результаты подтверждаются анализом изображений микроструктуры образцов (фиг.1-2), на которых ясно видно практически полностью однофазное строение полученного материала (фиг.1) с небольшими темными участками по границам зерен (фиг.2), по-видимому, содержащими примесный GeO2. Данный результат также подтверждается рентгенофазовым анализом, приведенным на фиг.3.
По результатам анализов, представленным на фиг.1-3, можно сделать вывод о том, что главными условиями для кристаллизации однофазного соединения Bi2Ge2O7, являются термическая обработка расплава (обеспечивает его полимеризацию с образованием [GeO4-]-тетраэдров) и взаимодействие такого расплава с высокотемпературным оксидом платины (Bi2PtO4 - выступает в качестве «затравки»). Медленное охлаждение расплава (без термических градиентов, вибрационных и ударных воздействий) способствует сохранению полимерной структуры и кристаллизации метастабильных фаз, а также препятствует переходу в аморфное состояние.
Заявляемый способ получения соединения с формулой Bi2Ge2O7 может быть реализован с помощью следующих материальных объектов:
1. печь - нагревательное устройство с рабочей камерой, обеспечивающее нагревание до заданной температуры (1200°С);
2. платиновый контейнер;
3. исходные реагенты: Bi2O3 и GeO2.
Технический результат достигается тем, что получают соединение с формулой Bi2Ge2O7 путем химического присоединения Bi2Q3 и GeO2.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения германата-силиката висмута | 2020 |
|
RU2724760C1 |
| Способ получения германата висмута BiGeO методом литья | 2020 |
|
RU2753671C1 |
| СПОСОБ ПОЛУЧЕНИЯ САМОНАСТРАИВАЮЩЕГОСЯ КАТАЛИЗАТОРА ДЛЯ ОКИСЛИТЕЛЬНОЙ ДИМЕРИЗАЦИИ МЕТАНА В СИСТЕМЕ BiO- SiO | 2020 |
|
RU2753653C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕРМАНАТА ВИСМУТА BiGeO | 2017 |
|
RU2636090C1 |
| Способ получения гетероструктуры, стекло, обогащенное Si/δ* - BiO/стекло, обогащенное Bi, в системе BiO - SiO | 2018 |
|
RU2693062C1 |
| Способ получения керамики | 2022 |
|
RU2791652C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕГУЛИРУЕМОЙ ГЕТЕРОСТРУКТУРЫ СТЕКЛО/δ*-ВiO+BiSiO В СИСТЕМЕ BiO-SiO(Варианты) | 2018 |
|
RU2691334C1 |
| Способ получения соединения δ*-BiO в системе BiO-SiO | 2018 |
|
RU2707598C1 |
| Способ получения германата-силиката висмута со структурой силленита | 2022 |
|
RU2788799C1 |
| Способ получения силиката висмута BiSiO | 2017 |
|
RU2654968C1 |
Изобретение относится к химической промышленности и может быть использовано при изготовлении устройств оптической обработки информации, миниатюрных и пассивных микроволновых керамических компонентов с высокой производительностью для мобильных устройств, а также фотокатализаторов. Сначала смешивают Bi2O3 и GeO2 в соотношении 32:68 масс. %. Полученную смесь помещают в платиновый контейнер, нагревают до 1200±10°С и выдерживают 60 мин. Затем охлаждают до 1125±5°С, выдерживают 40 мин, после чего охлаждают с печью до комнатной температуры. Изобретение позволяет получить однофазное соединение с формулой Bi2Ge2O7. 3 ил.
Способ получения соединения с формулой Bi2Ge2O7, включающий смешивание Bi2O3 и GeO2 в соотношении 32:68 масс. %, помещение полученной смеси в платиновый контейнер, нагревание до 1200±10°С, выдержку 60 мин, охлаждение до 1125±5°С с выдержкой 40 мин и последующее охлаждение с печью до комнатной температуры.
| Способ получения монокристаллов ортогерманата висмута | 1989 |
|
SU1745779A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕРМАНАТА ВИСМУТА BiGeO | 2017 |
|
RU2636090C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕРМАНАТА ВИСМУТА BiGeO | 2017 |
|
RU2654946C1 |
| Способ получения поликристаллического ортогерманата висмута | 2018 |
|
RU2659268C1 |
| Способ получения германата висмута BiGeO | 2018 |
|
RU2687924C1 |
| Способ получения германата висмута BiGeO методом литья | 2020 |
|
RU2753671C1 |
| Способ получения германата висмута BiGeO методом литья | 2021 |
|
RU2753672C1 |
| КОРОЛЕВ Г.М | |||
| и др | |||
| Синтез кристаллических фаз в системе "висмут-германий-кислород", Успехи химии и химической технологии, 2020, т | |||
| XXXIV, no | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| БЕРМЕШЕВ Т.В | |||
Авторы
Даты
2023-12-25—Публикация
2023-02-20—Подача