Настоящее изобретение касается полипептидов и их терапевтического применения, в частности для лечения синдромов стресса, иммунной реакции и инсульта.
Уровень техники
Когда клетки мигрируют в организме, они направляются хемокинами. Клетки, которые привлекаются хемокинами, следуют за сигналом увеличения концентрации хемокинов по направлению к источнику хемокина. В настоящее время известно четыре различных семейства хемокинов, которые различаются по расстоянию между их первыми двумя остатками цистеина. Так называемые хемокины СХС или α-хемокины содержат одну аминокислоту в качестве спейсера между двумя цистеинами, обозначенными в наименовании буквой «X».
Соответственно, благодаря хемокиновым рецепторам на поверхности клеток, хемокины оказывают влияние на клетки. Хемокиновые рецепторы являются интегральными мембранными белками. Хемокиновый рецептор СХС, и в частности хемокиновый рецептор СХС 4 (CXCR4), активирует быстрый рост раковых клеток и миграцию, образуя метастазы по всему телу, преимущественно в легких, костях и печени. Кроме того, ВИЧ может использовать CXCR4 для заражения CD4+ Т-клеток.
CXCR4 участвует в многочисленных процессах развития и физиологии, включая хоуминг стволовых клеток (Mohle and Drost, 2012) и миграцию иммунных клеток (Campbell et al., 2003). Искусственные антагонисты CXCR4 способны мобилизовать гематопоэтические стволовые клетки (HSC), которые используются для восстановления иммунной системы после трансплантации или химиотерапии (Ratajczak and Kim, 2012; Schroeder and DiPersio, 2012). Кроме того, CXCR4 также является основным ко-рецептором для проникновения ВИЧ 1 типа в клетки-мишени (Feng et al., 1996; Bleul et al., 1996). Ко-рецепторное использование CXCR4 является высокоэффективным, и высокая доля CD4+ Т-клеток экспрессируют этот GPCR в лимфатических тканях в условиях in vivo. Тем не менее, почти все варианты ВИЧ 1 типа, использующие С-С хемокиновый рецептор 5 типа (CCR5), передаются и обнаруживаются при хронической инфекции ВИЧ 1 типа (Alkhatib et al., 1996; Deng et al., 1996; Dragic et al., 1996). Было высказано предположение, что множество факторов способствуют неэффективной передаче CXCR4-TponHbix (Х4) штаммов ВИЧ 1 типа (Margolis and Shattock, 2006). Однако механизм(ы), лежащий(ие) в основе эффективного контроля Х4 ВИЧ 1 типа у иммунокомпетентных людей, остаются недостаточно изученными.
Исследования антагонистов CXCR4 в последнее время превратились в обширную область проектов из-за многообразия показаний. В частности, попытки найти стратегию вмешательства в пролиферацию, дифференциацию и метастазирование раковых клеток оказались не столь успешными в клинических исследованиях, как ожидалось. Разработка одной из групп соединений, а именно, AMD3100, антагонистов CXCR4 (соединение бициклама: Hendrix and Flexner 2000), для средств длительного лечения была вынужденно прекращена вследствие токсических побочных эффектов. Хотя AMD3100 зарегистрирован для однократных коротких применений при мобилизации стволовых клеток, тем не менее, трудно найти соответствующие антагонисты для целевого CXCR4.
Zirafi, О. et al. сообщали в J. Leukoc. Biol. 99: 663-868; 2016 об эндогенном пептидном ингибиторе CXCR4 как антагонисте CXCR4. Этот пептид представляет собой фрагмент сывороточного альбумина человека из 16 остатков, и он был выделен в качестве ингибитора CXCR4-тропного вируса иммунодефицита человека типа 1 из библиотеки пептидов, полученных из крови. Эндогенный пептидный ингибитор CXCR4 связывает вторую внеклеточную петлю CXCR4, тем самым предотвращая вовлечение CXCL12 и антагонизируя рецептор. Следовательно, эндогенный пептидный ингибитор CXCR4 ингибирует CXCL12-опосредованную миграцию CXCR4-экспрессирующих клеток in vitro, мобилизует гематопоэтические стволовые клетки и подавляет воспалительные реакции in vivo. Авторы обсуждают создание эндогенного пептидного ингибитора CXCR4, его значение в качестве биомаркера заболевания и его роль в патогенезе вируса иммунодефицита человека / синдрома приобретенного иммунодефицита и рака.
В WO 2009/004054 А2 раскрыт пептид, имеющий аминокислотную последовательность Z1-LVRYTKKVPQVSTPTL-Z2 (ALB-408) и его биологически активные фрагменты и/или варианты и/или производные, в частности амидированные, ацетилированные, сульфатированные, фосфорилированные и/или гликозилированные производные, и пептиды, полученные путем многократного синтеза, которые обладают биологической активностью ALB408-423; где Z представляет собой от 0 до 10 аминокислотных остатков.
В WO 2014/198834 А1 раскрыты пептиды, в частности димеры, эффективные для блокирования инфекции ВИЧ 1 типа NL4-3 (Х4-тропной), опосредованной СХС-хемокиновым рецептором 4 (CXCR4), со значением IC50 менее 50 мкМ.
Следовательно, задачей изобретения является обеспечение пептидов с антагонистической активностью против природного CXCR4. В частности, пептиды должны ингибировать пролиферацию раковых клеток, метастазирование и показывать типы рака, на которые направлены различные аналоги, и реакции противовоспалительных аллергических реакций.
Другой задачей изобретения является обеспечение соединения, которое способно снижать рецепторную активность CXCR4.
Другой задачей настоящего изобретения является обеспечение соединения, которое способно влиять на пролиферацию раковых клеток.
Другой задачей настоящего изобретения является получение соединения, которое способно влиять на миграцию или хоуминг раковых клеток.
Еще одной задачей данного изобретения является получение соединения, которое способно влиять на образование метастазов.
Другой задачей настоящего изобретения является получение соединения, способного лечить высоко агрессивные опухоли таким образом, что рак в значительной степени ингибируется или переходит в хроническую стадию заболевания.
Еще одной задачей данного изобретения является получение соединения, способного регулировать и лечить различные заболевания, такие как иммунные и аллергические заболевания, рост тканей и регуляцию нервной системы.
Краткое описание изобретения
Задачи настоящего изобретения решаются с помощью любого из полипептидов согласно настоящему изобретению. Полипептиды согласно изобретению обладают большим терапевтическим потенциалом.
Полипептид согласно изобретению содержит общую аминокислотную последовательность (записанную в виде однобуквенного кода):
Z1 X1 X2 X3 X4 X5 Х6 X7 А Р X10 X11 S Z3,
где
X1=V, М или L, в частности, L,
X2=V, L или М, в частности, V,
X3=R, K или С, в частности, R,
X4=Y или W, в частности, Y,
X5=S или Т, в частности, Т,
X6=Q или С, в частности, С,
X7=K, С или R, в частности, K,
X10=Q или С, в частности, Q, и
X11=V, М или F, в частности, V;
и
Z1=0, Z2 или пироглутамат, где
Z2=0 или представляет собой модификацию N-концевого атома азота пептидной цепи, причем указанная модификация образует вместе с аминогруппой N-концевой аминокислоты пептида фрагмент, имеющий структуру -NR2R3, где R2 и/или R3 являются независимо друг от друга Н или замещенной или незамещенной ацилалкильной, арильной, аралкильной, циклоалкильной и гетероциклоалкильной группой;
Z3=0 или Z4, где
Z4=0 или является модификацией С-концевой карбоксильной группы пептидной цепи, причем указанная модификация вместе с карбоксильной группой С-концевой аминокислоты пептида образует фрагмент, имеющий структуру -C(O)-O-R1 или -C(O)-NR2R3, где R1 представляет собой замещенную или незамещенную алкильную, арильную, аралкильную, циклоалкильную и гетероциклоалкильную группу.
Когда указано, что группа(ы) Z1 и/или Z2, и/или Z3, и/или Z4=0, это означает в рамках настоящего изобретения, что соответствующая группа не присутствует в этом конкретном варианте реализации.
Неожиданно было обнаружено, что полипептид с неполярным белком на одном конце цепи (X1) и полярным белком на другом конце цепи (S) проявляет антагонистическую активность против природного CXCR4.
В предпочтительном варианте реализации X6 представляет собой Q, так что изобретение относится к полипептиду, содержащему общую аминокислотную последовательность (записанную однобуквенным кодом)
Z1 X1 X2 X3 X4 X5 Q X7 А Р X10 X11 S Z3,
в полипептиде согласно настоящему изобретению пептиды выбраны из следующих:
X1=V, М или L, в частности, L,
X2=V, L или М, в частности, V,
X3=R, K или С, в частности, R,
X4=Y или W, в частности, Y,
X5=S или Т, в частности, Т,
X7=K, С или R, в частности, K,
X10=Q или С, в частности, Q, и
X11=V, М или F, в частности, V;
В предпочтительном варианте реализации изобретения пептид согласно изобретению содержит по меньшей мере одну из следующих аминокислотных последовательностей:

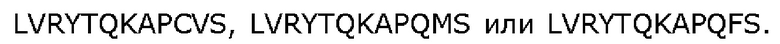 Последовательность
Последовательность 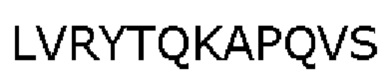 является особенно предпочтительным вариантом реализации.
является особенно предпочтительным вариантом реализации.
Согласно изобретению один или несколько аминокислотных остатков в последовательности могут быть заменены, удалены или добавлены, или могут быть внесены химические модификации на отдельных аминокислотах указанного полипептида, которые приводят к улучшенной биологической или фармакологической активности немодифицированного полипептида согласно изобретению. Специалистам в данной области техники известны соответствующие способы модификации.
Кроме того, по меньшей мере одна боковая цепь аминокислоты указанного полипептида может быть химически модифицирована, в частности фосфорилирована, амидирована, ацетилирована, гликозилирована, пегилирована, гезилирована или модифицирована комбинацией указанных способов.
Выбор подходящей функциональной группы для производного ПЭГ основан на типе доступных реакционноспособных групп на молекуле, которая будет присоединена к ПЭГ. Для белков типичные реакционноспособные аминокислоты включают лизин, цистеин, гистидин, аргинин, аспарагиновую кислоту, глутаминовую кислоту, серин, треонин, тирозин. N-концевая аминогруппа и С-концевая карбоновая кислота также могут быть использованы в качестве специфического соединения путем конъюгации с альдегидными функциональными полимерами.
Полипептид согласно изобретению может содержать по меньшей мере одну D-аминокислоту. В частности, полипептид согласно изобретению может быть составлен из цепи D-аминокислот в ретро-инверсной конфигурации цепи полипептида согласно изобретению.
Таким образом, ретро-инверсные пептиды из пептидов согласно изобретению также входят в объем настоящего изобретения, как и другие производные, стабилизирующие пептидную связь против пептидаз. Термин "производное" означает в рамках настоящей заявки фрагменты любой длины, включая усечения N- и С-концевой части, пептид согласно изобретению, содержащий замены аминокислотных остатков, включая D-аминокислотные остатки и модифицированные аминокислотные остатки, а также пептиды, содержащие дисульфидные связи и удлинение на концах N и С.
Другим объектом настоящего изобретения является лекарственное средство, содержащее по меньшей мере один полипептид согласно изобретению и фармацевтически приемлемый носитель. В одном из простейших вариантов реализации полипептид согласно изобретению можно вводить в воде для инфузии, физиологическом растворе или буферных водных растворах. Также возможны другие составы, например, инкапсулирование в липосомы с формированием наночастиц различных размеров, например, от 20 до 2000 нм.
Обычно пептид согласно изобретению вводят в количествах от 10 до 1000 мг/кг массы тела в течение периода времени, достаточного для остановки роста опухоли. Время введения составляет обычно от двух до десяти недель. Лекарственное средство согласно изобретению предпочтительно подходит для перорального, внутривенного, внутримышечного, внутрикожного, подкожного, интратекального введения или представлен в форме аэрозоля, пригодного для транспульмонального и интраназального введения, в частности, инкапсулирован в липосомы; или для применения в жидкой или липосомальной форме.
Объектом настоящего изобретения является также полинуклеотид, кодирующий полипептид согласно изобретению и/или его фрагменты, варианты, производные и аналоги. Полинуклеотид согласно изобретению может состоять из ДНК, РНК, геномной ДНК или ПНК. Полинуклеотид, гибридизующийся с полинуклеотидом в соответствии с изобретением, который кодирует полипептид согласно изобретению, также является объектом настоящего изобретения.
Другим объектом настоящего изобретения является вектор, содержащий полинуклеотид согласно изобретению, а также генетически сконструированная клетка-хозяин, содержащая вектор согласно изобретению.
Еще одним объектом настоящего изобретения является антитело, направленное против по меньшей мере одного полипептида согласно изобретению.
Еще одним объектом настоящего изобретения является соединение антагониста/ингибитора, направленное против полипептида согласно изобретению.
Объектом настоящего изобретения является также пептид согласно изобретению для применения в лечении неврологических заболеваний, в частности, инсульта, болезни Паркинсона, болезни Альцгеймера, рассеянного склероза; в области иммунологии, в частности, для лечения WHIM-синдрома, красной волчанки и ревматоидного артрита; в области онкологии, в частности, для лечения рака, в частности, рака, проявляющего CRCX-рецептор, такого как рак печени, поджелудочной железы, предстательной железы или груди; для лечения недостаточной мобилизации, пролиферации и миграции стволовых клеток, активации Т-клеток, а также поддержки иммунобластов, таких как CTL/PD-1; при лечении ран, вызванных ожогом; для антифибротического лечения; лечения или предотвращения рубцов; для лечения кардиологических нарушений, в частности, сердечной недостаточности; для лечения метаболических нарушений, в частности, диабета; для лечения вирусных заболеваний, в частности, инфекций ВИЧ 1 типа, ВИЧ 2 типа, цитомегаловируса, вируса простого герпеса (типа 1 и 2), вируса ветряной оспы, вируса гепатита А и вируса гепатита В, вируса гриппа, вируса полиомиелита, риновируса, вируса краснухи, вируса кори, вируса бешенства, вируса саркомы Рауса, вируса Эпштейна-Барр; а также для лечения инфекций, вызванных бактериями и грибами, в частности, Pseudomonas, Candida, S. aureus; для лечения инфекционных процессов, аномальных инфекционных процессов; лечение нарушений роста, лечение неврологических заболеваний, нарушений каскада свертывания крови и кроветворения, сосудистых заболеваний, заболеваний иммунной системы, а также для улучшения заживления ран и костей, легочных нарушений и аллергий.
Другим способом получения полипептида согласно изобретению является твердофазный синтез в соответствии с синтезом Меррифилда или жидкофазный синтез методами, известными специалисту в области техники с использованием защищенных аминокислот, и его очистка.
Еще один способ получения полипептида в соответствии с изобретением может включать методы гетерологичной экспрессии, известные специалисту в области техники, с использованием общепринятых биотехнологических векторов, и при необходимости последующую посттрансляционную или химическую модификацию.
Объектом настоящего изобретения является диагностическое средство, содержащее поли- или моноклональные антитела согласно изобретению или содержащее нуклеиновую кислоту или мРНК, кодирующую полипептид согласно изобретению.
Еще одним объектом настоящего изобретения является диагностическое средство, содержащее полипептид согласно изобретению или полинуклеотид согласно изобретению для тест-систем с целью анализа уровней указанного вещества в ткани, плазме, моче и спинномозговой жидкости, диагностические средства и тест-системы, обнаруживающие полипептид согласно изобретению для анализа уровней указанного вещества в плазме, моче и спинномозговой жидкости масс-спектрометрическими методами, такими как MALDI-MS или ESI-MS, в сочетании с пробоподготовкой методом RP-HPLC, осаждения белка и/или твердофазной экстракции. Предпочтительно методы масс-спектрометрии используются для обнаружения мельчайшего количества молекул в диапазоне Фемто- или Атто-молярных величин.
Также объектом настоящего изобретения является диагностическое средство, содержащее полипептид согласно изобретению в качестве маркеров вирусных заболеваний, бактериальных и грибковых инфекций, воспалительных и неопластических процессов, а также в качестве маркеров воспалительных процессов, нарушенных воспалительных реакций, опухолевых заболеваний, нарушений роста, заболеваний иммунной системы, WHIm-синдрома, красной волчанки и в качестве маркеров заболеваний костей и др.
Изобретение далее описывается более подробно с использованием пептида LVRYTQKAPQVS (SEQ ID No. 1) как типичного представителя пептида по изобретению.
ПРИМЕРЫ
Пептиды
Пептид SEQ ID No. 1 и его различные производные были синтезированы общепринятым твердофазным синтезом на синтезаторе пептидов 9050 (Applied Biosystems) с применением реагентов Fmoc. Пептид очищали путем RP хроматографии, и его идентичность и чистоту определяли с помощью аналитической RP-HPLC и MALDI-MS и LC-ESI-MS.
Анализ инвазии раковых клеток
Анализ инвазии раковых клеток проводили на гуманизированных крысах (Eyol, Е. et al., Oncology Reports, 28:2177-2187, 2012). Имплантировали клетки карциномы поджелудочной железы. Успешный имплантат наблюдался при люминесцентном изображении, а также при увеличении экспрессии CXCR4.
После успешной имплантации клеток карциномы крыс обрабатывали пептидом согласно SEQ ID No. 1. Результаты через 1 неделю терапии (1 н. терапии), через 2 недели терапии (2 н. терапии) и 2 недели после окончания терапии представлены в таблицах ниже.
Результат для пептида SEQ ID No. 1
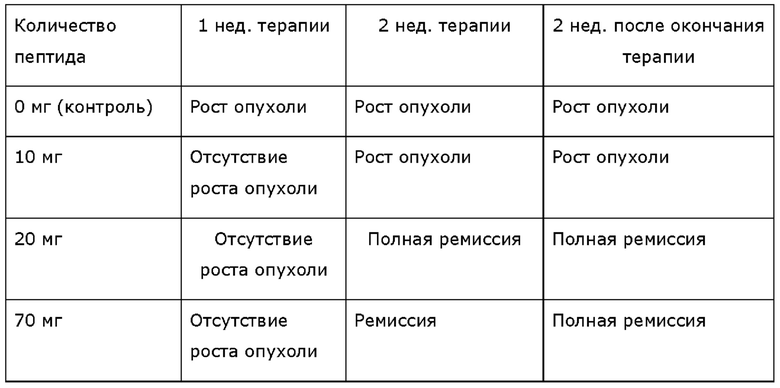
Крысы, не получавшие терапии, умерли после имплантации опухоли в течение нескольких дней.
Крысы, получавшие терапию с применением пептида по настоящему изобретению, выживали в течение по меньшей мере двух недель. Рост опухоли был остановлен, и в зависимости от концентрации наблюдалась частичная или даже полная ремиссия опухоли. Токсического действия пептидов не наблюдалось.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
--->
<110> Neopep Pharma GmbH & Co. KG
<120> Полипептиды для лечения синдромов стресса, иммунореакции и
инсульта
<130> 192153WO
<150> EP18205455.1
<151> 2018-11-09
<160> 15
<170> Патент в версии 3.3
<210> 1
<211> 12
<212> ПРТ
<213> человек
<400> 1
Leu Val Arg Tyr Thr Gln Lys Ala Pro Gln Val Ser
1 5 10
<210> 2
<211> 12
<212> ПРТ
<213> человек
<400> 2
Met Val Arg Tyr Thr Gln Lys Ala Pro Gln Val Ser
1 5 10
<210> 3
<211> 12
<212> ПРТ
<213> человек
<400> 3
Val Val Arg Tyr Thr Gln Lys Ala Pro Gln Val Ser
1 5 10
<210> 4
<211> 12
<212> ПРТ
<213> человек
<400> 4
Leu Met Arg Tyr Thr Gln Lys Gln Pro Gln Val Ser
1 5 10
<210> 5
<211> 12
<212> ПРТ
<213> человек
<400> 5
Leu Leu Arg Tyr Thr Gln Lys Gln Pro Gln Val Ser
1 5 10
<210> 6
<211> 12
<212> ПРТ
<213> человек
<400> 6
Leu Val Lys Tyr Thr Gln Lys Gln Pro Gln Val Ser
1 5 10
<210> 7
<211> 12
<212> ПРТ
<213> человек
<400> 7
Leu Val Cys Tyr Thr Gln Lys Gln Pro Gln Val Ser
1 5 10
<210> 8
<211> 12
<212> ПРТ
<213> человек
<400> 8
Leu Val Arg Trp Thr Gln Lys Ala Pro Gln Val Ser
1 5 10
<210> 9
<211> 12
<212> ПРТ
<213> человек
<400> 9
Leu Val Arg Tyr Ser Gln Lys Gln Pro Gln Val Ser
1 5 10
<210> 10
<211> 12
<212> ПРТ
<213> человек
<400> 10
Leu Val Arg Tyr Thr Cys Lys Ala Pro Gln Val Ser
1 5 10
<210> 11
<211> 12
<212> ПРТ
<213> человек
<400> 11
Leu Val Arg Tyr Thr Gln Cys Ala Pro Gln Val Ser
1 5 10
<210> 12
<211> 12
<212> ПРТ
<213> человек
<400> 12
Leu Val Arg Tyr Thr Gln Arg Ala Pro Gln Val Ser
1 5 10
<210> 13
<211> 12
<212> ПРТ
<213> человек
<400> 13
Leu Val Arg Tyr Thr Gln Lys Ala Pro Cys Val Ser
1 5 10
<210> 14
<211> 12
<212> ПРТ
<213> человек
<400> 14
Leu Val Arg Tyr Thr Gln Lys Ala Pro Gln Met Ser
1 5 10
<210> 15
<211> 12
<212> ПРТ
<213> человек
<400> 15
Leu Val Arg Tyr Thr Gln Lys Ala Pro Gln Phe Ser
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНСТРУИРОВАНИЯ РЕКОМБИНАНТНОГО ПОКСВИРУСА ДЛЯ ТЕРАПЕВТИЧЕСКОЙ ВАКЦИНЫ | 2020 |
|
RU2827444C1 |
| ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ С ВЫСОКОПЛОТНЫМ ПОКРЫТИЕМ ДЛЯ ИНДУКЦИИ ЭКСПРЕССИИ АНТИТЕЛ | 2017 |
|
RU2813282C2 |
| АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ В ОТНОШЕНИИ CD70, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2801093C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА FLT3 | 2018 |
|
RU2820859C2 |
| СПЕЦИФИЧНЫЕ К MUC16 ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2795198C2 |
| ИММУНОГЕНЫ ДЛЯ ВАКЦИНАЦИИ ПРОТИВ ВИЧ | 2013 |
|
RU2721274C2 |
| КОНЪЮГАТЫ АНТИТЕЛА К CCR7 И ЛЕКАРСТВЕННОГО СРЕДСТВА | 2018 |
|
RU2777662C2 |
| CD20 ТЕРАПИЯ, CD22 ТЕРАПИЯ И КОМБИНИРОВАННАЯ ТЕРАПИЯ КЛЕТКАМИ, ЭКСПРЕССИРУЮЩИМИ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) K CD19 | 2016 |
|
RU2752918C2 |
| АДЕНОВИРУСЫ И СПОСОБЫ ПРИМЕНЕНИЯ АДЕНОВИРУСОВ | 2019 |
|
RU2782528C1 |
| Производные слитого с Fc белка с высокой двойной активностью: противовирусной активностью в отношении ВИЧ и иммуномодулирующей активностью | 2018 |
|
RU2774782C2 |
Изобретение относится к биотехнологии, иммунологии и медицине, в частности к полипептидам и их терапевтическому применению для лечения синдромов стресса, иммунной реакции и инсульта. Изобретение обеспечивает пептиды с антагонистической активностью против природного CXCR4. 9 н. и 2 з.п. ф-лы, 1 табл., 1 пр.
1. Терапевтический полипептид, обладающий антагонистической активностью против природного CXCR4, имеющий аминокислотную последовательность, выбранную из группы, состоящей из LVRYTQKAPQVS, MVRYTQKAPQVS, VVRYTQKAPQVS, LMRYTQKQPQVS, LLRYTQKQPQVS, LVKYTQKQPQVS, LVCYTQKQPQVS, LVRWTQKAPQVS, LVRYSQKQPQVS, LVRYTCKAPQVS, LVRYTQCAPQVS, LVRYTQRAPQVS, LVRYTQKAPCVS, LVRYTQKAPQMS или LVRYTQKAPQFS.
2. Лекарственное средство для лечения раковых заболеваний, демонстрирующих рецептор CXCR4, содержащее по меньшей мере один полипептид по п. 1 и фармацевтически приемлемый носитель.
3. Лекарственное средство по п. 2, подходящее для перорального, внутривенного, внутримышечного, внутрикожного, подкожного, интратекального введения или в форме аэрозоля, пригодного для транспульмонального введения, в частности, инкапсулированный в липосомы; или для применения в жидкой или липосомальной форме.
4. Полинуклеотид, кодирующий полипептид по п. 1.
5. Полинуклеотид по п. 4, отличающийся тем, что он состоит из ДНК, РНК, геномной ДНК или РНК.
6. Вектор экспрессии, содержащий полинуклеотид по п. 4.
7. Генетически сконструированная клетка-хозяин для экспрессии полипептида по п. 1, содержащая вектор экспрессии по п. 6.
8. Применение полипептида по любому из пп. 1, 2 в области онкологии, в частности для лечения раковых заболеваний, в частности видов рака, демонстрирующих рецептор CXCR4, таких как рак печени, поджелудочной железы, предстательной железы или молочной железы.
9. Диагностическое средство в качестве маркера опухолевых заболеваний, демонстрирующих рецептор CXCR4, содержащее нуклеиновую кислоту или мРНК, кодирующие полипептид по любому из пп. 1, 2.
10. Диагностическое средство в качестве маркера опухолевых заболеваний, демонстрирующих рецептор CXCR4, содержащее полипептид по любому из пп. 1, 2 или полинуклеотид по п. 4, для тест-систем для анализа уровней адсорбированного вещества в ткани, плазме, моче и спинномозговой жидкости.
11. Диагностическое средство в качестве маркера опухолевых заболеваний, демонстрирующих рецептор CXCR4, содержащее полипептид по любому из пп. 1, 2.
Авторы
Даты
2024-08-12—Публикация
2019-11-08—Подача