ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №62/680,297, поданной 4 июня 2018 г., которая настоящим полностью включена посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит Перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим полностью включен в данную заявку посредством ссылки. Указанная копия ASCII, созданная 23 мая 2019 г., названа 50471-715_201_SL.txt и имеет размер 331880 байт.
УРОВЕНЬ ТЕХНИКИ
[0003] Рекомбинантные полипептиды, такие как химерные полипептиды, представляют ценность для применений в исследованиях, диагностике, производстве и терапии. Модифицированные эффекторные клетки, экспрессирующие связывающие антиген полипептиды, такие как CAR, пригодны для лечения заболеваний и расстройств, таких как инфекционное заболевание, аутоиммунные расстройства и типы рака.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
[0004] Все публикации, патенты и заявки на патент, упомянутые в настоящем описании, включены в данную заявку посредством ссылки в той же степени, как если бы каждые отдельная публикация, патент или заявка на патент были конкретно и отдельно указаны как включенные посредством ссылки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0005] В настоящей заявке предложена выделенная нуклеиновая кислота, кодирующая химерный антигенный рецептор (CAR), причем указанный CAR содержит: (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета. В некоторых вариантах реализации домен, связывающий антиген MUC16, содержит по меньшей мере один из: (а) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 1, 3, 5, 7, 9, 12 и 14; (b) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 2, 4, 6, 8, 10, 11, 13 и 15; и (с) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 27-57.
[0006] В некоторых вариантах реализации домен, связывающий антиген MUC16, представляет собой полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 27-57. В некоторых вариантах реализации домен стебля представляет собой полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 16. В некоторых вариантах реализации костимулирующий сигнальный домен содержит 4-1 ВВ. В некоторых вариантах реализации костимулирующий сигнальный домен 4-1 ВВ содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 22. В некоторых вариантах реализации костимулирующий сигнальный домен содержит CD28. В некоторых вариантах реализации костимулирующий сигнальный домен CD28 содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 23.
[0007] В некоторых вариантах реализации сигнальный домен СО3-дзета содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 26. В некоторых вариантах реализации выделенная нуклеиновая кислота, предложенная в данной заявке, может дополнительно содержать укороченный рецептор эпидермального фактора роста. В некоторых вариантах реализации укороченный рецептор эпидермального фактора роста представляет собой HER.1t и содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 65. В некоторых вариантах реализации укороченный рецептор эпидермального фактора роста представляет собой HER.1t-1 и содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 66.
[0008] В некоторых вариантах реализации указанный CAR содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот, представленной в SEQ ID NO: 27-57.
[0009] В настоящей заявке предложен вектор, содержащий остов и последовательность нуклеиновой кислоты, кодирующую: (1) укороченный рецептор эпидермального фактора роста, содержащий по меньшей мере один из HER1t, HER1t-1 или их функционального варианта; (2) цитокин; и (3) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) ко стимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета.
[0010] В некоторых вариантах реализации цитокин представляет собой IL-15 или IL-12. В некоторых вариантах реализации вектор представляет собой лентивирусный вектор, ретровирусный вектор или невирусный вектор. В некоторых вариантах реализации укороченный рецептор эпидермального фактора роста содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 65 или SEQ ID NO: 66. В некоторых вариантах реализации IL-15 представляет собой связанный с мембраной IL-15. В некоторых вариантах реализации связанный с мембраной IL-15 содержит последовательность нуклеотидов, кодирующую SEQ ID NO: 161.
[0011] В некоторых вариантах реализации любой из векторов, предложенных в данной заявке, может дополнительно содержать последовательность нуклеотидов, кодирующую саморасщепляющийся пептид вируса Thosea asigna (Т2А). В некоторых вариантах реализации остов представляет собой ДНК плазмиду транспозона Спящая красавица или pFUGW. В некоторых вариантах реализации любой из векторов, предложенных в данной заявке, может дополнительно содержать промотор. В некоторых вариантах реализации промотор представляет собой hEF1a1. В некоторых вариантах реализации домен, связывающий антиген MUC16, содержит по меньшей мере один из: (а) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 1, 3, 5, 7, 9, 12 и 14; (b) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 2, 4, 6, 8, 10, 11, 13 и 15; и; (с) полипептида, идентичного по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 27-57. В некоторых вариантах реализации домен, связывающий антиген MUC16, представляет собой полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 27-57. В некоторых вариантах реализации домен стебля содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 16. В некоторых вариантах реализации костимулирующий сигнальный домен содержит 4-1 ВВ. В некоторых вариантах реализации костимулирующий сигнальный домен 4-1 ВВ содержит последовательность нуклеиновой кислоты, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 22.
[0012] В некоторых вариантах реализации костимулирующий сигнальный домен содержит CD28. В некоторых вариантах реализации костимулирующий сигнальный домен CD28 содержит последовательность нуклеиновой кислоты, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 23. В некоторых вариантах реализации сигнальный домен CD3-дзета содержит последовательность нуклеиновой кислоты, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 26.
[0013] В некоторых вариантах реализации вектор содержит плазмиду. В некоторых вариантах реализации каждый вектор содержит плазмиду экспрессии. В некоторых вариантах реализации невирусный вектор представляет собой транспозон Спящая красавица.
[0014] В настоящей заявке предложена эффекторная иммунная клетка, содержащая любой из нуклеотидов, предложенных в данной заявке. В настоящей заявке предложена эффекторная иммунная клетка, содержащая: (1) метку клетки (2) IL-15 и (3) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета.
[0015] В некоторых вариантах реализации IL-15 представляет собой связанный с мембраной IL-15. В некоторых вариантах реализации связанный с мембраной IL-15 содержит полипептидную последовательность, представленную в SEQ ID NO: 161. В некоторых вариантах реализации метка клетки включает HER1t, и HER1t содержит полипептидную последовательность, представленную в SEQ ID NO: 65. В некоторых вариантах реализации метка клетки включает HER1t-1, и HER1t-1 содержит полипептидную последовательность, представленную в SEQ ID NO: 66.
[0016] В настоящей заявке предложена эффекторная иммунная клетка, содержащая любой из векторов, описанных в данной заявке. В некоторых вариантах реализации указанная клетка представляет собой Т-клетку, клетку-естественного киллера (NK), цитотоксический Т-лимфоцит (CTL) или регуляторную Т-клетку. В некоторых вариантах реализации CAR содержит по меньшей мере одну из последовательностей аминокислот SEQ ID NO: 27-57.
[0017] В настоящей заявке предложен способ стимулирования опосредованного Т-клетками иммунного ответа на целевую популяцию клеток или ткань у нуждающегося в этом субъекта, представляющего собой человека, включающий введение указанному субъекту, представляющему собой человека, эффективного количества клетки, генетически модифицированной, чтобы экспрессировать CAR, причем указанный CAR содержит: (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) транс мембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1ВВ или CD28, или и то, и другое; (е) сигнальный домен CD3-дзета и (f) укороченный рецептор эпидермального фактора роста (HER1t). В некоторых вариантах реализации у человека был диагностирован по меньшей мере один из рака яичников и рака молочной железы. В некоторых вариантах реализации рак яичников или молочной железы представляет собой рецидивирующий или рефрактерный рак яичников или молочной железы.
[0018] В настоящей заявке предложена выделенная нуклеиновая кислота, кодирующая химерный антигенный рецептор (CAR), причем CAR содержит: (а) домен, связывающий антиген MUC16, с по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 1-15 или 27-57; (b) домен стебля с последовательностью аминокислот SEQ ID NO: 16; (с) костимулирующий сигнальный домен, содержащий CD28 с последовательностью аминокислот SEQ ID NO: 23; (d) метку HER1, которая содержит по меньшей мере одну из HER1t с последовательностью аминокислот SEQ ID NO: 65 и HER1t-1 с последовательностью аминокислот SEQ ID NO: 66; и (е) сигнальный домен CD3-дзета с последовательностью аминокислот SEQ ID NO: 26.
[0019] В настоящей заявке предложена выделенная нуклеиновая кислота, кодирующая химерный антигенный рецептор (CAR), причем указанный CAR содержит: (а) домен, связывающий антиген MUC16, с по меньшей мере одной из последовательностей аминокислот, представленных в SEQ ID NO: 1-15 или 27-57; (b) домен стебля с последовательностью аминокислот SEQ ID NO: 16; (с) костимулирующий сигнальный домен, содержащий 4-1ВВ, с последовательностью аминокислот SEQ ID NO: 23; (d) метку HER1, которая включает по меньшей мере одну из HER1t с последовательностью аминокислот SEQ ID NO: 65 и HER1t-1 с последовательностью аминокислот SEQ ID NO: 66; (е) сигнальный домен CD3-дзета с последовательностью аминокислот SEQ ID NO: 26.
[0020] В настоящей заявке предложен вектор, содержащий любой один или более из полинуклеотидов, описанных в данной заявке. В некоторых вариантах реализации указанный вектор представляет собой лентивирусный вектор, ретровирусный вектор или невирусный вектор. В некоторых вариантах реализации невирусный вектор представляет собой транспозон Спящая красавица. В некоторых вариантах реализации вектор представляет собой множество векторов.
[0021] В настоящей заявке предложена система экспрессии CAR в эффекторной иммунной клетке, указанная система содержит один или более векторов, кодирующих выделенную нуклеиновую кислоту, предложенную в данной заявке. В некоторых вариантах реализации эффекторная иммунная клетка представляет собой Т-клетку или NK-клетку. В некоторых вариантах реализации система, предложенная в данной заявке, может дополнительно содержать нуклеиновую кислоту, кодирующую по меньшей мере один дополнительный ген. В некоторых вариантах реализации дополнительный ген включает цитокин. В некоторых вариантах реализации цитокин включает по меньшей мере один из IL-2, IL-15, IL-12, IL-21 и слитой молекулы IL-15 и IL-15Rα. В некоторых вариантах реализации цитокин находится в секретированной форме. В некоторых вариантах реализации цитокин находится в связанной с мембраной форме. В некоторых вариантах реализации система содержит один вектор. В некоторых вариантах реализации один или более векторов представляют собой лентивирусный вектор, ретровирусный вектор или невирусный вектор. В некоторых вариантах реализации невирусный вектор представляет собой транспозон Спящая красавица. В некоторых вариантах реализации система, предложенная в данной заявке, может дополнительно содержать транспозазу Спящая красавица. В некоторых вариантах реализации транспозаза Спящая красавица представляет собой SB11, SB100X или SB110. В некоторых вариантах реализации эффекторная иммунная клетка представляет собой клетку млекопитающего.
[0022] В настоящей заявке предложен способ экспрессии CAR в эффекторной иммунной клетке, включающий приведение в контакт эффекторной иммунной клетки с системой, описанной в данной заявке.
[0023] В настоящей заявке предложен способ стимуляции пролиферации и/или выживания сконструированных Т-клеток, включающий: (а) получение образца клеток от субъекта, указанный образец содержит Т-клетки или предшественники Т-клеток; (b) трансфекцию клеток одним или более векторами, кодирующими выделенную нуклеиновую кислоту, предложенную в любом из пп. 1-34 и 47-52, и вектором, кодирующим транспозазу, с получением популяции сконструированных Т-клеток, экспрессирующих MUC16-CAR (MUC16-CAR-T-клеток); (с) и необязательно культивирование популяции MUC16-CAR-T-клеток ex vivo в течение 2 дней или менее.
[0024] В некоторых вариантах реализации способ стимуляции пролиферации и/или выживания сконструированных Т-клеток может дополнительно включать трансфекцию клеток вектором, кодирующим цитокин. В некоторых вариантах реализации цитокин представляет собой слитый белок, содержащий IL-15 и IL-15Ra. В некоторых вариантах реализации один или более векторов представляют собой лентивирусный вектор, ретровирусный вектор или невирусный вектор. В некоторых вариантах реализации невирусный вектор представляет собой транспозон Спящая красавица. В некоторых вариантах реализации способ может дополнительно включать транспозазу Спящая красавица. В некоторых вариантах реализации транспозаза Спящая красавица представляет собой SB11, SB100X или SB110.
[0025] В настоящей заявке предложен способ лечения рака у нуждающегося в этом субъекта, включающий введение указанному субъекту одной или более доз эффективного количества сконструированных Т-клеток, причем сконструированные Т-клетки содержат MUC16-CAR и связанный с мембраной IL-15. В некоторых вариантах реализации первую дозу эффективного количества сконструированных Т-клеток вводят интраперитонеально. В некоторых вариантах реализации вторую дозу эффективного количества сконструированных Т-клеток вводят внутривенно. В некоторых вариантах реализации рак представляет собой рак яичников. В некоторых вариантах реализации рак представляет собой рак молочной железы. В некоторых вариантах реализации MUC16-CAR кодируется любой из последовательностей, представленных в SEQ ID NO: 95-107, 119-149 или 194-195. В некоторых вариантах реализации связанный с мембраной IL-15 кодируется последовательностью SEQ ID NO: 161. В некоторых вариантах реализации эффективное количество сконструированных Т-клеток составляет по меньшей мере 102 клеток/кг. В некоторых вариантах реализации эффективное количество сконструированных Т-клеток составляет по меньшей мере 104 клеток/кг. В некоторых вариантах реализации эффективное количество сконструированных Т-клеток составляет по меньшей мере 105 клеток/кг.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0026] Признаки настоящего изобретения описаны в подробностях в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ настоящего изобретения будет достигнуто исходя из следующего подробного описания, в котором представлены иллюстративные варианты реализации, в которых используют принципы настоящего изобретения, и сопроводительные чертежи, из которых:
[0027] На Фиг. 1 представлен пример схематичного изображения системы транспозонов Спящая красавица. Плазмиды ДНК, полученные из Спящей красавицы, кодирующие MUC16-CAR и цитокин, такой как связанный с мембраной IL15 (mbIL15), транспозоны и плазмиду ДНК, кодирующую транспозазу SB, доставляют в эффекторные иммунные клетки, например, путем электропорации. Сконструированные эффекторные иммунные клетки можно производить с помощью способов, осуществимых в месте оказания медицинских услуг, описанных в данной заявке. В некоторых случаях MUC16-CAR и/или цитокин можно совместно экспрессировать с меткой клетки или меткой уничтожения для условного удаления in vivo.
[0028] На Фиг. 2 изображены примеры кассеты экспрессии генов MUC16-CAR и цитокинов в различных конфигурациях с компонентами переключателя генов.
[0029] На Фиг. 3 представлено изображение MUC16-CAR с различными длинами стебля.
[0030] На Фиг. 4 показана экспрессия трансгенов CAR, mbIL15 и HER1t1. Т-клетки подвергали нуклеофекции транспозоном MUC16-3-CAR-HER1t1 или MUC16-3-CAR-mbIL15-HER1t1 и транспозазой SB. Экспрессию трансгенов измеряли в 1 день после нуклеофекции. Дискриминационное окно для клеток устанавливали на живые CD3+ клетки. Результаты представлены в виде среднего значения ± стандартная ошибка среднего для трех здоровых доноров.
[0031] На Фиг. 5 показана экспрессия MUC16-CAR с различными длинами спейсеров, полученных из шарнирных областей С08-альфа в CAR-T-клетках. MUC16-CAR-T-клетки получали путем электропорации Т-клеток здоровых доноров плазмидами с системой SB (№ донора D133098). CAR-T-клетки размножали ex vivo путем совместного культивирования с экспрессирующими MUC16t АаРС путем стимуляции раз в неделю. Экспрессию CAR измеряли с помощью многопараметрической проточной цитометрии в 1 день и 8 день после нуклеофекции. Испытуемые образцы представлены в Таблице 6.
[0032] На Фиг. 6 показаны CAR-Т-клетки, экспрессирующие MUC16-CAR с различными длинами спейсеров, полученных из шарнирных областей CD8-альфа. CAR-T-клетки получали путем электропорации Т-клеток здоровых доноров плазмидами с системой SB (№ донора D132552). CAR-T-клетки размножали ex vivo путем совместного культивирования с экспрессирующими MUC16t АаРС путем стимуляции раз в неделю. Экспрессию CAR измеряли с помощью многопараметрической проточной цитометрии в 1 день и 8 день после нуклеофекции. Испытуемые образцы представлены в Таблице 7.
[0033] На Фиг. 7 показан анализ методом вестерн-блоттинга экспрессии MUC16-CAR. Экспрессию MUC16-CAR измеряли путем окрашивания антителом мыши против CD3ζ человека. Дорожка 1: маркер молекулярной массы белков; дорожка 2: MUC16-3-CAR-HER1t1 Т-клетки; и 3: MUC16-3-CAR-mbIL15-HER1t1 Т-клетки.
[0034] На Фиг. 8 показан анализ методом вестерн-блоттинга экспрессии mbIL15. Экспрессию mbIL15 измеряли путем окрашивания антителом против IL-15. Дорожка 1: маркер молекулярной массы белков; дорожка 2: MUC16-3-CAR-HER1t1 Т-клетки, и дорожка 3: MUC16-3-CAR-mbIL15-HER1t1 Т-клетки.
[0035] На Фиг. 9 показан анализ методом вестерн-блоттинга экспрессии HER1t1. Экспрессию HER1t1 измеряли с помощью способа иммунопреципитации с последующим вестерн-блоттингом. Дорожка 1: MUC16-3-CAR-HER1t1 Т-клетки; дорожка 2: MUC16-3-CAR-mbIL15-HER1t1 Т-клетки; дорожка 3: контроль иммунопреципитации без лизата; дорожка 4: лизат линии клеток А431; и дорожка 5: маркер молекулярной массы белков.
[0036] На Фиг. 10А показан анализ методом проточной цитометрии экспрессии MUC16 в различных исследованных линиях опухолевых клеток.
[0037] На Фиг. 10В показана специфичная цитотоксичность MUC16-CAR-T-клеток. Цитотоксичность MUC16-3-CAR-HER1t1 Т-клеток и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток в отношении различных линий опухолевых клеток при различных соотношениях эффектора и мишени (Э:М). Контрольные CAR-mbIL15-HER1t1 Т-клетки использовали в качестве отрицательного контроля. Представлено среднее значение ± стандартная ошибка среднего для трех повторных лунок из 3 доноров.
[0038] На Фиг. 11 показана продукция цитокинов MUC16-CAR-T-клетками при совместном культивировании с различными линиями опухолевых клеток. CAR-T-клетки, полученные с использованием Т-клеток трех здоровых доноров, совместно культивировали с определенными линиями опухолевых клеток при соотношении Э:М 1:1 в течение семи дней. Представлено среднее значение ± стандартная ошибка среднего для трех повторных лунок из 3 доноров.
[0039] На Фиг. 12 показана цитотоксичность MUC16-CAR-T-клеток в люциферазном анализе. CAR-T-клетки, полученные из Т-клеток двух здоровых доноров, культивировали с линиями опухолевых клеток. Испытуемые образцы представлены в Таблице 8.
[0040] На Фиг. 13А показана биологическая функция mbIL15 в MUC16-CAR-T-клетках. CAR-T-клетки получали из Т-клеток трех здоровых доноров. Сохранение MUC16-3-CAR-HER1t1 Т-клеток и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток в культуре in vitro в отсутствие антигена и экзогенных цитокинов. Каждый символ представляет CAR-T-клетки отдельного донора. Показано среднее значение ± стандартная ошибка среднего для трех доноров.
[0041] На Фиг. 13В показана биологическая функция mbIL15 в MUC16-CAR-T-клетках. CAR-T-клетки получали из Т-клеток трех здоровых доноров. Показана пролиферация CAR-T-клеток. Каждый символ представляет CAR-T-клетки отдельного донора. Показано среднее значение ± стандартная ошибка среднего для трех доноров.
[0042] На Фиг. 13С показана биологическая функция mbIL15 в MUC16-CAR-T-клетках. CAR-T-клетки получали из Т-клеток трех здоровых доноров. Показан анализ маркеров памяти MUC16-3-CAR-mbIL15-HER1t1 Т-клеток. Каждый символ представляет CAR-T-клетки отдельного донора. Показано среднее значение ± стандартная ошибка среднего для трех доноров.
[0043] На Фиг. 14 показано сохранение in vitro MUC16-CAR-T-клеток в отсутствие экзогенных цитокинов. MUC16-2-CAR-HER1t1 Т-клетки и MUC16-2-CAR-mbIL15-HER1t1 Т-клетки из Т-клеток трех здоровых доноров культивировали в присутствии или отсутствие экзогенных цитокинов в течение 2 недель. Представляли на графике жизнеспособные Т-клетки в культуре без цитокинов как долю Т-клеток в культуре с цитокинами. Результаты представлены в виде среднего значения ± стандартная ошибка среднего для трех доноров.
[0044] На Фиг. 15 показана опосредованная цетуксимабом активность антителозависимой клеточной цитотоксичности (АЗКЦ) (выраженная в виде % цитотоксичности; ось у) в отношении MUC16-CAR-T-клеток, коэкспрессирующих HER1t1. Аллогенные NK-клетки использовали в качестве эффекторных клеток при отношении Э:М, равном 10:1. Цетуксимаб проявил специфичную цитотоксичность по отношению к экспрессирующим HER1t1 MUC16-CAR-Τ-клеткам. Результаты представлены в виде среднего значения±стандартная ошибка среднего.
[0045] На Фиг. 16 показан количественный анализ опухолевой нагрузки SKOV3-fLUC-MUC16, измеренной с помощью биолюминесцентной визуализации (IVIS) in vivo. Мышам NSG (Ν=5-7 мышей на группу) вводили линию опухолевых клеток SKOV3-fLUC-MUC16 путем интраперитонеальной (и/п) инъекции в 0 день. Несущих опухоль мышей лечили различной терапией MUC16-CAR-T путем однократной и/п или в/в инъекции и проводили количественный анализ опухолевой нагрузки посредством IVIS в ходе лечения. Результаты представлены в виде среднего значения ± стандартная ошибка среднего. Стрелка указывает на день, в который осуществляли введение CAR-T.
[0046] На Фиг. 17 показан количественный анализ опухолевой нагрузки SKOV3-fLUC-MUC16, измеренной с помощью биолюминесцентной визуализации (IVIS) in vivo. Мышам NSG (Ν=5-7 мышей на группу) вводили линию опухолевых клеток SKOV3-fLUC-MUC16 путем и/п инъекции в 0 день. Несущих опухоль мышей лечили различной терапией MUC16-CAR-T путем однократной и/п инъекции через пять дней после введения опухолевых клеток, и проводили количественный анализ опухолевой нагрузки посредством IVIS в ходе лечения. Результаты представлены в виде среднего значения ± стандартная ошибка среднего.
[0047] На Фиг. 18А и на Фиг. 18В показан количественный анализ MUC16-CAR-T-клеток в крови получивших лечение несущих опухоль мышей NSG. Мышам NSG (N=5-7 мышей на группу) вводили линию опухолевых клеток SKOV3-fLUC-MUC16 путем и/п инъекции. Несущих опухоль мышей лечили различной терапией MUC16-CAR-T путем однократной и/п инъекции через пять дней после введения опухолевых клеток, и проводили количественный анализ CAR-T-клеток (количество CAR-Т-клеток на мл крови; ось у) путем измерения CD8+ HER1t1+ (Фиг. 18А) и CD4+ HER1t1+ (Фиг. 18В) Т-клеток в образцах крови мыши. Результаты представлены в виде среднего значения ± стандартная ошибка среднего; n=5-7 мышей в каждый момент времени.
[0048] На Фиг. 19 показан количественный анализ опухолевой нагрузки SKOV3-fLUC-MUC16, измеренной с помощью биолюминесцентной визуализации (IVIS) in vivo. Мышам NSG (Ν=5 мыши на группу) вводили линию опухолевых клеток SKOV3-fLUC-MUC16 путем и/п инъекции в 0 день. Несущих опухоль мышей лечили одной из трех различных доз MUC16-2-CAR-Т-клеток путем однократной и/п инъекции через пять дней после введения опухолевых клеток, и проводили количественный анализ опухолевой нагрузки посредством IVIS в ходе лечения. Испытуемые образцы представлены в Таблице 9. Результаты представлены в виде среднего значения ± стандартная ошибка среднего.
[0049] На Фиг. 20 показан количественный анализ опухолевой нагрузки SKOV3-fLUC-MUC16, измеренной с помощью биолюминесцентной визуализации (IVIS) in vivo. Мышам NSG (Ν=5 мыши на группу) вводили линию опухолевых клеток SKOV3-fLUC-MUC16 путем и/п инъекции в 0 день. Несущих опухоль мышей лечили одной из трех различных доз MUC16-3-CAR-Τ-клеток путем однократной и/п инъекции через пять дней после введения опухолевых клеток, и проводили количественный анализ опухолевой нагрузки посредством IVIS в ходе лечения. Испытуемые образцы представлены в Таблице 9. Результаты представлены в виде среднего значения ± стандартная ошибка среднего.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0050] Следующее описание и примеры подробно иллюстрируют варианты реализации настоящего изобретения. Должно быть понятно, что настоящее изобретение не ограничено конкретными вариантами реализации, описанными в данной заявке, и по этой причине может изменяться. Для специалистов в данной области понятно, что существует множество вариантов и модификаций настоящего изобретения, которые входят в объем настоящего изобретения.
[0051] Все термины следует понимать так, как их будет понимать специалист в данной области. Если не указано иначе, все технические и научные термины, используемые в данной заявке, имеют те же значения, которые обычно понимает средний специалист в области, к которой относится настоящее изобретение.
[0052] Заголовки разделов, используемые в данной заявке, предназначены только для организационных целей и не должны толковаться как ограничивающие описанный объект изобретения.
[0053] Хотя различные признаки настоящего изобретения могут быть описаны в контексте одного варианта реализации, указанные признаки также могут быть представлены отдельно или в любой подходящей комбинации. Напротив, хотя настоящее изобретение может быть описано в данной заявке в контексте отдельных вариантов реализации для ясности, настоящее изобретение также можно осуществить в одном варианте реализации.
[0054] Следующие определения дополняют определения в данной области и относятся к настоящей заявке, и не должны приписываться какому-либо связанному или несвязанному случаю, например, любому совместному патенту или заявке на патент. Хотя любые способы и материалы, сходные или эквивалентные описанным в данной заявке, можно применять на практике для тестирования настоящего изобретения, предпочтительные материалы и способы описаны в данной заявке. Соответственно, терминология, используемая в данной заявке, предназначена лишь для цели описания конкретных вариантов реализации и не предназначена для ограничения.
[0055] В данном описании использование форм единственного числа включает формы множественного числа, если не указано иначе. Следует отметить, что, как используется в настоящем описании, формы единственного числа включают ссылку на множественное число, если в контексте явно не указано иное. В данной заявке использование «или» означает «и/или», если не указано иное. Более того, использование термина «включая», а также других форм, таких как «включать», «включает» и «включен», не является ограничивающим.
[0056] Упоминание в настоящем описании «некоторых вариантов реализации», «варианта реализации», «одного варианта реализации» или «других вариантов реализации» означает, что конкретный признак, структура или свойство, описанные в отношении вариантов реализации, входят в по меньшей мере некоторые варианты реализации, но не обязательно во все варианты реализации настоящего изобретения.
[0057] В настоящем описании и пункте(-ах) формулы изобретения термины «включающий» (и любая форма термина включающий, такая как «включают» и «включает»), «обладающий» (и любая форма термина обладающий, такая как «обладают» и «обладает»), «состоящий» (и любая форма термина состоящий, такая как «состоит» и «состоят») или «содержащий» (и любая форма термина содержащий, такая как «содержит» и «содержат») являются включительными или неограничивающими и не исключают дополнительные, не перечисленные элементы или этапы способа. Предполагается, что любой вариант реализации, обсуждаемый в описании настоящего изобретения, можно осуществить в отношении любого способа или композиции согласно настоящему изобретению, и наоборот. Более того, композиции согласно настоящему изобретению можно применять, чтобы осуществить способы согласно настоящему изобретению.
[0058] Термин «приблизительно» в отношении упомянутого числового значения и его грамматические эквиваленты в данной заявке могут включать само числовое значение и диапазон значений плюс или минус 10% от указанного числового значения. Например, количество «приблизительно 10» включает 10 и любые количества от 9 до 11. Например, термин «приблизительно» в отношении упомянутого числового значения может также включать диапазон значений плюс или минус 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% или 1% от указанного значения.
[0059] Под термином «выделенный» подразумевают удаление нуклеиновой кислоты из ее природного окружения. Под термином «очищенный» подразумевают, что повысили чистоту данной нуклеиновой кислоты, которую либо удалили из природного окружения (включая геномную ДНК и мРНК), либо синтезировали (включая кДНК), и/или амплифицировали в лабораторных условиях, причем «чистота» является относительным термином, не «абсолютной чистотой». Следует понимать, тем не менее, что нуклеиновые кислоты и белки могут находиться в составе с разбавителями или адъювантами, но все же для практических целей быть выделенными. Например, нуклеиновые кислоты обычно смешивают с приемлемым носителем или разбавителем, когда их применяют для внедрения в клетки.
[0060] «Полинуклеотид» или «олигонуклеотид» в данной заявке относится к полимерной форме нуклеотидов любой длины, либо рибонуклеотидов, либо дезоксирибонуклеотидов. Данный термин относится только к первичной структуре молекулы. Таким образом, данный термин включает двух- и одноцепочечную ДНК, триплексную ДНК, а также двух- и одноцепочечную РНК. Он также включает модифицированные, например, путем метилирования и/или путем кэппирования, и немодифицированные формы полинуклеотида. Также подразумевают, что указанный термин включает молекулы, которые содержат не встречающиеся в природе или синтетические нуклеотиды, а также аналоги нуклеотидов.
[0061] Термин «полипептид» используют взаимозаменяемо с терминами «полипептиды» и «белок(-ки)», и он относится к полимеру из аминокислотных остатков. «Зрелый белок» представляет собой белок, который является полноразмерным и который необязательно содержит гликозилирование или другие модификации, обычные для белка в данном клеточном окружении.
[0062] Нуклеиновые кислоты и/или последовательности нуклеиновых кислот «гомологичны», когда они происходят, в природе или искусственно, из общего предшественника нуклеиновой кислоты или последовательности нуклеиновой кислоты. Белки и/или белковые последовательности гомологичны, когда кодирующие их ДНК происходят, в природе или искусственно, из общего предшественника нуклеиновой кислоты или последовательности нуклеиновой кислоты. Гомологичные молекулы можно назвать гомологами. Например, любые встречающиеся в природе белки, описанные в данной заявке, можно модифицировать с помощью любого доступного способа мутагенеза. При экспрессии данная подвергнутая мутагенезу нуклеиновая кислота кодирует полипептид, который гомологичен белку, кодируемому исходной нуклеиновой кислотой. Гомология, как правило, является следствием идентичности последовательностей между двумя или более нуклеиновыми кислотами или белками (или их последовательностями). Точный процент идентичности между последовательностями, который пригоден для установления гомологии, изменяется в зависимости от обсуждаемой нуклеиновой кислоты и белка, но всего лишь 25% идентичности последовательностей обычно используют для установления гомологии. Более высокие уровни идентичности последовательностей, например, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 99% или более, также можно использовать для установления гомологии.
[0063] Термины «идентичный» или «идентичность последовательностей» в контексте двух последовательностей нуклеиновых кислот или аминокислотных последовательностей полипептидов относится к остаткам в двух последовательностях, которые одинаковы при выравнивании для максимального соответствия в определенном окне сравнения. В одном классе вариантов реализации полипептиды в данной заявке по меньшей мере на 80%, 85%, 90%, 98% 99% или 100% идентичны эталонному полипептиду, или его фрагменту, например, что измеряют с помощью BLASTP (или CLUSTAL, или любого другого доступного программного обеспечения для выравнивания), используя параметры по умолчанию. Аналогично, нуклеиновые кислоты также можно описать относительно исходной нуклеиновой кислоты, например, они могут быть на 50%, 60%, 70%, 75%, 80%, 85%, 90%, 98%, 99% или 100% идентичны эталонной нуклеиновой кислоте или ее фрагменту, например, что измеряют с помощью BLASTN (или CLUSTAL, или любого другого доступного программного обеспечения для выравнивания), используя параметры по умолчанию. Когда у одной молекулы есть некоторый процент идентичности последовательности с большей молекулой, это означает, что когда две молекулы оптимально выровнены, у указанного процента остатков в меньшей молекуле находится совпадающий остаток в большей молекуле в соответствии с порядком, в котором две молекулы оптимально выровнены.
[0064] «Транспозон» или «мобильный элемент» (ТЕ) представляет собой векторную последовательность ДНК, которая может изменять свое положение в геноме, иногда создавая или обращая мутации и изменяя размер генома клетки. Транспозиция часто приводит к дупликации ТЕ. ТЕ I класса копируют двумя этапами: сначала их транскрибируют с ДНК в РНК, и полученную РНК затем обратно транскрибируют в ДНК. Данную скопированную ДНК затем вставляют в новое положение в геноме. Этап обратной транскрипции катализируется обратной транскриптазой, которая может кодироваться самим ТЕ. Свойства ретротранспозонов сходны с таковыми у ретровирусов, таких как ВИЧ. Механизм транспозиции копировать-вставить ТЕ II класса не включает стадию РНК-интермедиата. Транспозиции катализируются несколькими ферментами транс поз азами. Некоторые транспозазы неспецифично связываются с любым целевым сайтом в ДНК, тогда как другие связываются с определенными целевыми последовательностями ДНК. Транспозаза делает ступенчатый разрез в целевом сайте, приводя к образованию одноцепочечных 5’- или 3’-выступов ДНК (липких концов). Данный этап вырезает транспозон ДНК, который затем лигируется в новый целевой сайт; данный процесс включает активность ДНК-полимеразы, которая заполняет гэпы, и ДНК-лигазы, которая замыкает сахарофосфатный остов. Это приводит к дупликации целевого сайта. Сайты вставки транспозонов ДНК можно идентифицировать по коротким прямым повторам, которые могут быть созданы ступенчатым разрезом в целевой ДНК и заполнением ДНК-полимеразой, за которыми следует серия инвертированных повторов, важных для вырезания ТЕ транспозазой. Копированные-вставленные ТЕ могут дуплицироваться, если их транспозиция происходит во время S-фазы клеточного цикла, когда донорный сайт уже был реплицирован, но целевой сайт еще не был реплицирован. Транспозицию можно классифицировать либо как «автономную», либо как «неавтономную» в ТЕ как I класса, так и II класса. Автономные ТЕ могут сами перемещаться, тогда как для неавтономных ТЕ требуется присутствие других ТЕ для перемещения. Причиной этого часто является то, что у неавтономных ТЕ отсутствует транспозаза (для II класса) или обратная транскриптаза (для I класса).
[0065] «Транспозаза» относится к ферменту, который связывается с концом транспозона и катализирует перемещение транспозона в другую часть генома посредством механизма копировать-вставить или репликационного механизма транспозиции. В некоторых вариантах реализации каталитическую активность транспозазы можно использовать для перемещения гена(-ов) из вектора в геном.
[0066] Последовательности нуклеиновых кислот и векторы, описанные или предложенные в данной заявке, можно ввести в клетку путем «трансфекции», «трансформации», «нуклеофекции» или «трансдукции». «Трансфекция», «трансформация» или «трансдукция» в данной заявке относится к внедрению одного или более экзогенных полинуклеотидов в клетку-хозяина путем применения физических или химических способов. Множество методик трансфекции известны в данной области и включают, например, копреципитацию ДНК фосфатом кальция (см., например, Murray Ε. J. (ред.), Methods in Molecular Biology, том 7, протоколы переноса и экспрессии генов, Humana Press (1991)); DEAE-декстран; электропорацию; опосредованную катионными липосомами трансфекцию; бомбардировку микрочастицами, осуществленную частицами вольфрама (Johnston, Nature, 346: 776-777 (1990)); и копреципитацию ДНК фосфатом стронция (Brash и др., Mol. Cell Biol., 7: 2031-2034 (1987)); и нуклеофекцию (Trompeter и др., J. Immonol. Methods 274:245-256 (2003). Фаговые или вирусные векторы можно внедрить в клетки хозяева после выращивания инфекционных частиц в подходящих пакующих клетках, множество из которых доступны для приобретения.
[0067] «Промотор» относится к участку полинуклеотида, который инициирует транскрипцию кодирующей последовательности. Промоторы расположены рядом с сайтами начала транскрипции генов на той же цепи и против хода транскрипции на ДНК (по направлению к 5’-области смысловой цепи). Некоторые промоторы являются конститутивными, так как они активны при всех обстоятельствах в клетке, тогда как другие являются регулируемыми, становясь активными в ответ на определенные стимулы, например, индуцируемый промотор.
[0068] Термин «активность промотора» относится к уровню экспрессии последовательности нуклеотидов, которая функционально связана с промотором, активность которого измеряют. Активность промотора можно измерить непосредственно путем определения количества полученного транскрипта РНК, например, с помощью анализа нозерн-блот, или опосредованно путем определения количества продукта, кодируемого связанной последовательностью нуклеиновой кислоты, такой как репортерная последовательность нуклеиновой кислоты, связанная с промотором.
[0069] «Индуцируемый промотор» в данной заявке относится к промотору, который индуцируется в активное состояние присутствием или отсутствием регуляторов транскрипции, например, биотических или абиотических факторов. Индуцируемые промоторы полезны, так как экспрессию генов, функционально связанных с ними, можно включить или выключить на некоторых стадиях развития организма или в определенной ткани. Примеры индуцируемых промоторов представляют собой регулируемые спиртом промоторы, регулируемые тетрациклином промоторы, регулируемые стероидами промоторы, регулируемые металлами промоторы, регулируемые патогенезом промоторы, регулируемые температурой промоторы и регулируемые светом промоторы. В одном варианте реализации индуцируемый промотор является частью генетического переключателя.
[0070] Термин «энхансер» в данной заявке относится к последовательности ДНК, которая повышает транскрипцию, например, последовательности нуклеиновой кислоты, с которой она функционально связана. Энхансеры могут быть расположены во множестве тысяч пар нуклеотидов от кодирующей области последовательности нуклеиновой кислоты и могут опосредовать связывание регуляторных факторов, паттерны метилирования ДНК или изменения в структуре ДНК. Большое количество энхансеров из множества различных источников хорошо известны в данной области и доступны в виде или внутри клонированных полинуклеотидов (например, из депозитариев, таких как Американская коллекция типовых культур (АТСС), а также других коммерческих или частных источников). Множество полинуклеотидов, содержащих промоторы (такие как широко используемый промотор CMV), также содержат последовательности энхансеров. Энхансеры могут быть расположены против хода транскрипции, внутри или по ходу транскрипции от кодирующей последовательности. Термин «энхансеры Ig» относится к энхансерным элементам, происходящим из энхансерных областей, картированных в локусе иммуноглобулинов (Ig) (такие энхансеры включают, например, 5’-энхансеры тяжелой цепи (мю), 5’-энхансеры легкой цепи (каппа), интронные энхансеры каппа и мю и 3’-энхансеры (см., как правило, Paul W. Ε. (ред.), Fundamental immunology, 3е издание, Raven Press, Нью-Йорк (1993), страницы 353-363; и патент США номер 5,885,827).
[0071] «Кодирующая последовательность» в данной заявке относится к фрагменту полинуклеотида, который кодирует полипептид. Область или последовательность ограничена вблизи 5’-конца старт-кодоном и вблизи 3’-конца стоп-кодоном. Кодирующие последовательности также могут называть открытыми рамками считывания.
[0072] «Функционально связанный» в данной заявке относится к физической и/или функциональной связи фрагмента ДНК с другим фрагментом ДНК таким образом, чтобы позволить фрагментам функционировать предполагаемым образом. Последовательность ДНК, кодирующая продукт гена, функционально связана с регуляторной последовательностью, когда она связана с регуляторной последовательностью, такой как, например, промоторы, энхансеры и/или сайленсеры, таким образом, который позволяет модуляцию транскрипции последовательности ДНК, непосредственно или опосредованно. Например, последовательность ДНК функционально связана с промотором, когда она лигирована с промотором по ходу транскрипции относительно сайта инициации транскрипции от промотора, в правильной рамке считывания относительно сайта инициации транскрипции, и позволяет происходить элонгации транскрипции вдоль последовательности ДНК. Энхансер или сайленсер функционально связан с последовательностью ДНК, кодирующей продукт гена, когда он лигирован с последовательностью ДНК таким образом, чтобы повысить или снизить, соответственно, транскрипцию последовательности ДНК. Энхансеры и сайленсеры могут быть расположены против хода транскрипции, по ходу транскрипции или находиться внутри кодирующих областей последовательности ДНК. ДНК сигнальной последовательности функционально связана с ДНК, кодирующей полипептид, если сигнальная последовательность экспрессируется в виде пребелка, который участвует в секреции полипептида. Связь последовательностей ДНК с регуляторными последовательностями обычно осуществляют путем лигирования в подходящих сайтах рестрикции или посредством адаптеров или линкеров, которые вставляют в последовательность, применяя эндонуклеазы рестрикции, известные специалисту в данной области.
[0073] Термин «регулятор транскрипции» относится к биохимическому элементу, который действует, чтобы предотвратить или ингибировать транскрипцию управляемой промотором последовательности ДНК при некоторых условиях окружающей среды (например, репрессору или ядерному ингибиторному белку), или позволить или стимулировать транскрипцию управляемой промотором последовательности ДНК при некоторых условиях окружающей среды (например, индуктору или энхансеру).
[0074] Термин «индукция» относится к повышению транскрипции последовательности нуклеиновой кислоты, активности промотора и/или экспрессии, вызванному регулятором транскрипции, относительно некоторого основного уровня транскрипции.
[0075] «Целевой» ген, или «гетерологичный» ген, или «интересующий ген (ИГ)» относится к гену, введенному в клетку-хозяина путем переноса генов.
[0076] «Рекомбиназа» в данной заявке относится к группе ферментов, которая может способствовать сайт-специфичной рекомбинации между определенными сайтами, когда указанные сайты физически разделены на одной молекуле ДНК или когда сайты находятся на отдельных молекулах ДНК. Последовательности ДНК определенных сайтов рекомбинации не обязательно идентичны. Инициация рекомбинации зависит от взаимодействия белок-ДНК, в данной группе существует большое количество белков, которые катализируют встраивание и вырезание фага (например, интеграза λ, фС31), расщепление кольцевых плазмид (например, Tn3, гамма дельта, Cre, Flp), инверсию ДНК для экспрессии альтернативных генов (например, Hin, Gin, Pin), сборку генов во время развития (например, гена фиксация азота Anabaena) и транспозицию (например, транспозона IS607). Большинство сайт-специфичеких рекомбиназ относятся к одному из двух семейств, на основании эволюционного и механистического родства. Они представляют собой семейство интеграз λ или тирозин-рекомбиназы (например, Cre, Flp, Xer D) и семейство резолваз/интеграз или семейство серин-рекомбиназ (например, фС31, ТР901-1, Tn3, гамма дельта).
[0077] «Сайты присоединения рекомбиназ» представляют собой специфичные полинуклеотидные последовательности, которые узнаются ферментами рекомбиназы, описанными в данной заявке. Обычно вовлечены два различных сайта (названные «комплементарными сайтами»), один присутствует на целевой нуклеиновой кислоте (например, хромосоме или эписоме эукариот или прокариот), а другой на нуклеиновой кислоте, которую нужно встроить в целевой сайт рекомбинации. Термины «attB» и «attP», которые относятся к сайтам присоединения (или рекомбинации), изначально полученным из бактериальной мишени и донора фага, соответственно, используют в данной заявке, хотя у сайтов рекомбинации для конкретных ферментов могут быть различные названия. Сайты рекомбинации обычно содержат левое и правое плечи, разделенные коровым или спейсерным участком. Таким образом, сайт рекомбинации attB состоит из ВОВ', где В и В' представляют собой левое и правое плечи, соответственно, и О представляет собой коровый участок. Аналогично, attP представляет собой POP', где Ρ и Р' представляют собой плечи и О снова представляет собой коровый участок. При рекомбинации между сайтами attB и attP и одновременном встраивании нуклеиновой кислоты в мишень, сайты рекомбинации, которые фланкируют встроенную ДНК, называют «attL» и «attR». Сайты attL и attR, с использованием указанной выше терминологии, таким образом, состоят из ВОР’ и РОВ’, соответственно. В некоторых представлениях в данной заявке «О» опускают и attB и attP, например, называют ВВ' и РР', соответственно.
[0078] «Вектор экспрессии» или «вектор» представляет собой любой генетический элемент, например, плазмиду, хромосому, вирус, транспозон, ведущий себя либо как автономная единица репликации полинуклеотида внутри клетки (т.е., способная реплицироваться под собственным контролем), либо который сделали способным реплицироваться путем вставки в хромосому клетки-хозяина, присоединив его к другому фрагменту полинуклеотида, чтобы вызвать репликацию и/или экспрессию присоединенного фрагмента. Подходящие векторы включают, но не ограничены перечисленными: плазмиды, транспозоны, бактериофаги и космиды. Векторы могут содержать полинуклеотидные последовательности, которые необходимы для осуществления лигирования или вставки вектора в желательную клетку-хозяина и для осуществления экспрессии присоединенного фрагмента. Такие последовательности отличаются в зависимости от организма хозяина; они включают последовательности промотора, чтобы осуществить транскрипцию, последовательности энхансера, чтобы повысить транскрипцию, последовательности сайта связывания рибосом и последовательности терминации транскрипции и трансляции. В качестве альтернативы, векторы экспрессии могут быть способны непосредственно экспрессировать продукты последовательности нуклеиновой кислоты, кодированные в них, без лигирования или встраивания вектора в последовательности ДНК клетки-хозяина.
[0079] Вектор также может содержать «ген селектируемого маркера». Термин «ген селектируемого маркера» в данной заявке относится к последовательности нуклеиновой кислоты, которая позволяет клеткам, экспрессирующим указанную последовательность нуклеиновой кислоты, быть специфично выбранными или отброшенными в присутствии соответствующего селективного агента. Подходящие гены селектируемого маркера известны в данной области и описаны, например, в международной публикации заявки на патент WO 1992/08796 и WO 1994/28143; Wigler и др., Proc. Natl. Acad. Sci. USA, 77: 3567 (1980); O'Hare и др., Proc. Natl. Acad. Sci. USA, 78: 1527 (1981); Mulligan & Berg, Proc. Natl. Acad. Sci. USA, 78: 2072 (1981); Colberre-Garapin и др., J. Mol. Biol., 150:1 (1981); Santerre и др., Gene, 30: 147 (1984); Kent и др., Science, 237: 901-903 (1987); Wigler и др., Cell, 11: 223 (1977); Szybalska & Szybalski, Proc. Natl. Acad. Sci. USA, 48: 2026 (1962); Lowy и др., Cell, 22: 817 (1980); и в патентах США №5,122,464 и 5,770,359.
[0080] В некоторых вариантах реализации вектор представляет собой «эписомальный вектор экспрессии» или «эписому», которая способна реплицироваться в клетке-хозяине и сохраняется в виде внехромосомного фрагмента ДНК внутри клетки-хозяина в присутствии подходящего селективного давления (см., например, Conese и др., Gene Therapy, 11:1735-1742 (2004)). Примеры доступных для приобретения эписомальных векторов экспрессии включают, но не ограничены эписомальными плазмидами, в которых используется ядерный антиген вируса Эпштейна-Барр (EBNA1) и точка начала репликации вируса Эпштейна-Барр (EBV) (oriP). Векторы pREP4, рСЕР4, pREP7 и pcDNA3.1 от Invitrogen (Карлсбад, Калифорния) и pBK-CMV от Stratagene (Ла-Хойя, Калифорния) представляют собой лишь некоторые из примеров эписомального вектора, в которых используется Т-антиген и точка начала репликации SV40 вместо EBNA1 и oriP.
[0081] «Клетка рака» относится к клетке, проходящей раннюю, промежуточную или распространенную стадии многоэтапного неопластического прогрессирования, как описано ранее (Pitot и др., Fundamentals of Oncology, 15-28 (1978)). Она включает клетки на ранней, промежуточной и распространенной стадиях неопластического развития, включая «преднеопластические» клетки (т.е. «гиперпластические» клетки и диспластические клетки), и неопластические клетки на распространенных стадиях неопластического развития диспластической клетки.
[0082] «Метастатическая» клетка рака относится к клетке рака, которая переместилась из первичного очага рака (т.е. места, где указанная клетка рака изначально образовалась из нормальной, гиперпластической или диспластической клетки) в место, отличное от первичного места, где перемещенная клетка рака оседает и пролиферирует.
[0083] «Рак» относится к множеству раковых клеток, которые могут быть или не быть метастатическими, такой как рак яичников, рак молочной железы, рак легких, рак предстательной железы, рак шейки матки, рак поджелудочной железы, рак толстого кишечника, рак желудка, рак пищевода, рак рта, рак языка, рак десны, рак кожи (например, меланома, базально-клеточная карцинома, саркома Капоши и т.д.), рак мышцы, рак сердца, рак печени, бронхиальный рак, рак хряща, рак кости, рак яичка, рак почки, рак эндометрия, рак матки, рак мочевого пузыря, рак костного мозга, рак лимфомы, рак селезенки, рак тимуса, рак щитовидной железы, рак головного мозга, рак нейрона, мезотелиома, рак желчного пузыря, рак глаза (например, рак роговицы, рак сосудистой оболочки глаза, рак хориоида, рак макулы, рак стекловидного тела и т.д.), рак сустава (такой как рак синовиальной оболочки), глиобластома, лимфома и лейкоз.
MUC16
[0084] Также известный как СА-125 (раковый антиген 125, антиген 125 карциномы или углеводный антиген 125) или муцин 16, MUC16 является представителем семейства гликопротеинов муцинов. Было показано, что MUC16 играет роль в распространении онкогенеза и пролиферации опухоли посредством нескольких различных механизмов. Подходы, основанные на антителах против MUC16, имели лишь незначительный успех. Соответственно, необходимы другие стратегии лечения.
[0085] MUC16 представляет собой большой углеводный антиген, также известный как СА-125. MUC16 кодируется геном MUC16, расположенным на хромосоме 19 человека. MUC16 представляет собой многодоменный трансмембранный белок I типа с высоким уровнем гликозилирования, содержащий 3 домена. С-концевой домен содержит множество внеклеточных элементов SEA (белок спермы морского ежа, энтерокиназа и агрин), которые обладают аутопротеолитической активностью. SEA содержит два протеолитических сайта, проксимальных трансмембранному (ТМ) домену. Большой отщепленный домен, названный СА-125, высвобождается в кровоток при кислом рН. СА-125 широко используют в качестве биомаркера заболевания раком яичников. Высоко консервативный укороченный внеклеточный связанный с мембраной домен белка, названный эктодоменом MUC16. Было обнаружено антитело MUC16, которое специфично связывается с эктодоменом MUC16, который сохраняется на поверхности опухолевой клетки. «Сверхэкспрессия MUC16» интересующей клеткой (такой как клетка рака) относится к более высокому уровню белка и/или мРНК MUC16, который экспрессируется интересующей клеткой, по сравнению с контрольной клеткой (такой как нераковая клетка, нормальная клетка и т.д.).
Химерные антигенные рецепторы.
[0086] В вариантах реализации, описанных в данной заявке, CAR может содержать внеклеточный происходящий из антитела одноцепочечный вариабельный домен (scFv) для распознавания мишени, причем scFv может быть соединен гибким линкером с трансмембранным доменом и/или внутриклеточным(и) сигнальным(и) доменом(-ами), который включает, например, CD3ζ, для активации Т-клеток. Обычно, когда Т-клетки активируются in vivo, они получают первичный вызванный антигеном сигнал TCR со вторичным костимулирующим сигналом от CD28, который вызывает продукцию цитокинов (т.е. IL-2 и IL-21), которые затем по типу обратной связи попадают в сигнальную петлю аутокринным/паракринным образом. По этой причине, CAR могут содержать сигнальный домен, например, цитоплазматический сигнальный домен CD28 или сигнальные домены другой костимулирующей молекулы, такие как сигнальный домен 4-1ВВ. Костимуляция химерного CD28 улучшает сохранение Т-клеток путем повышения экспрессии антиапоптических молекул и продукции IL-2, а также размножение Т-клеток, полученных из мононуклеарных клеток периферической крови (МКПК).
[0087] В одном варианте реализации CAR представляют собой слитые одноцепочечные вариабельные фрагменты (scFv), полученные из моноклональных антител, специфичных к различным эпитопам MUC16, например, слитые с трансмембранным доменом и эндодоменом CD3-дзета. Такие молекулы приводят к передаче сигнала дзета в ответ на распознавание scFv его мишени.
[0088] В варианте реализации CAR может содержать эктодомен (внеклеточный), трансмембранный домен и эндодомен (внутриклеточный). В одном варианте реализации эктодомена CAR, сигнальный пептид направляет образующийся белок в эндоплазматический ретикулум. Это происходит, например, если рецептор должен быть гликозилирован и заякорен в мембрану клетки. Предусмотрено, что любая последовательность эукариотического сигнального пептида функциональна. Как правило, используют сигнальный пептид, в природе присоединенный к наиболее аминоконцевому компоненту (например, в scFv с ориентацией легкая цепь - линкер - тяжелая цепь используют нативный сигнальный пептид легкой цепи). В вариантах реализации сигнальный пептид представляет собой GM-CSFRa (SEQ ID NO: 58) или IgK (SEQ ID NO: 59). Другие сигнальные пептиды, которые можно применять, включают сигнальные пептиды из CDS-альфа и CD28.
[0089] Домен распознавания антигена может представлять собой scFv. Тем не менее, могут быть альтернативы. Предложен домен распознавания антигена из отдельных цепей альфа и бета нативного Т-клеточного рецептора (TCR), так как они содержат простые эктодомены (например, эктодомен CD4), а также другие компоненты распознавания, такие как связанный, например, цитокин (что приводит к распознаванию клеток, несущих рецептор цитокина). Почти все, что связывает данную мишень, такую как, например, ассоциированный с вирусом антиген, с высокой аффинностью можно применять в качестве участка распознавания антигена.
[0090] Обычно, CAR существуют в димеризованной форме и экспрессируются в виде слитого белка, в котором соединены внеклеточная область scFv (VH, связанный с VL), домен стебля, трансмембранный домен и внутриклеточные сигнальные мотивы. Эндодомен из CAR первого поколения вызывает активацию Т-клеток исключительно посредством передачи сигналов CD3-ζ. CAR второго поколения обуславливает активирующую передачу сигналов через CD3-ζ и CD28, или другие эндодомены, такие как 4-1ВВ или ОХ40. CAR третьего поколения активирует Т-клетки посредством содержащей CD3-ζ комбинации трех сигнальных мотивов, таких как CD28, 4-1ВВ или ОХ40.
[0091] В вариантах реализации в соответствии с настоящим изобретением предложен химерный антигенный рецептор (CAR), содержащий внеклеточный домен, трансмембранный домен и внутриклеточный сигнальный домен. В вариантах реализации внеклеточный домен содержит специфичный к мишени связывающий элемент, иначе называемый связывающей антиген группой или scFv, и домен стебля. В вариантах реализации внутриклеточный сигнальный домен или иначе цитоплазматический сигнальный домен содержит ко стимулирующую сигнальную область и часть цепи дзета.
[0092] Костимулирующая сигнальная область относится к части CAR, содержащей внутриклеточный сигнальный домен костимулирующей молекулы. Костимулирующие молекулы представляют собой молекулы поверхности клетки, отличные от рецепторов антигенов или их лигандов, которые необходимы для эффективного ответа лимфоцитов на антиген.
[0093] В вариантах реализации между внеклеточным доменом и трансмембранным доменом CAR находится домен стебля или участок стебля. В данной заявке термин «домен стебля» или «участок стебля», как правило, означает любой олигонуклеотид или полипептид, функция которого состоит в связывании трансмембранного домена либо с scFv, либо с цитоплазматическим доменом в полипептидной цепи. Домен стебля может содержать гибкий шарнир, такой как шарнир Fc, и необязательно один или два константных домена Fc. В некоторых случаях участок стебля содержит шарнирную область из IgG1. В альтернативных случаях участок стебля содержит участок СН2СН3 иммуноглобулина и необязательно части CD3. В некоторых случаях участок стебля содержит шарнирную область CD8α, шарнирную область IgG4-Fc из 12 аминокислот (ESKYGPPCPPCP) (SEQ ID NO: 196) или шарнирные области IgG4, описанные в WO/2016/073755.
[0094] В других вариантах реализации между внеклеточным доменом и трансмембранным доменом CAR находится спейсер. Спейсер может содержать участок стебля и участок удлинения стебля, изображенный на Фиг. 3. В одном варианте реализации спейсер может содержать один участок стебля. В другом варианте реализации спейсер может содержать участок стебля (обозначенный «s») и участок(-ки) удлинения стебля, который в данной заявке обозначен «s-n'». Например, спейсер может содержать один (1) участок стебля и s'-n, где n может представлять собой 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. В дополнительных вариантах реализации участок стебля может быть связан с участком удлинения стебля s'-n посредством линкера.
[0095] Трансмембранный домен может быть получен либо из природного, либо из синтетического источника. Если источник природный, то домен может происходить из любого связанного с мембраной или трансмембранного белка. Подходящие трансмембранные домены могут содержать трансмембранный(-е) участок(-ки) цепи альфа, бета или дзета Т-клеточного рецептора; или трансмембранный участок CD28, CD3-эпсилон, CD3ζ, CD45, CD4, CD5, CD8-альфа, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137 или CD154. В качестве альтернативы трансмембранный домен может быть синтетическим и может содержать гидрофобные остатки, такие как лейцин и валин. В некоторых вариантах реализации триплет фенилаланина, триптофана и валина находится на одном или обоих концах синтетического трансмембранного домена. Необязательно короткий олигонуклеотидный или полипептидный линкер, в некоторых вариантах реализации, длиной от 2 до 10 аминокислот может образовать связь между трансмембранным доменом и цитоплазматическим сигнальным доменом CAR. В некоторых вариантах реализации линкер представляет собой глицин-сериновый линкер. В некоторых вариантах реализации трансмембранный домен включает трансмембранный домен CD8a или трансмембранный домен CD3ζ. В некоторых вариантах реализации трансмембранный домен включает трансмембранный домен CD8α. В других вариантах реализации трансмембранный домен включает трансмембранный домен CD3ζ.
[0096] Внутриклеточный домен может содержать один или более костимулирующих доменов. Примеры костимулирующих доменов включают, но не ограничены перечисленными: CD8, CD27, CD28, 4-1ВВ (CD137), ICOS, DAP10, DAP12, ОХ40 (CD134), CD3-дзета или их фрагмент или комбинацию. В некоторых случаях CAR, описанный в данной заявке, содержит один или более, или два или более костимулирующих доменов, выбранных из CD8, CD27, CD28, 4-1ВВ (CD137), ICOS, DAP10, DAP12, ОХ40 (CD134) или их фрагмента или комбинации. В некоторых случаях CAR, описанный в данной заявке, содержит один или более, или два или более костимулирующих доменов, выбранных из CD27, CD28, 4-1ВВ (CD137), ICOS, ОХ40 (CD134) или их фрагмента или комбинации. В некоторых случаях CAR, описанный в данной заявке, содержит один или более, или два или более костимулирующих доменов, выбранных из CD8, CD28, 4-1ВВ (CD137), DAP10, DAP12 или их фрагмента или комбинации. В некоторых случаях CAR, описанный в данной заявке, содержит один или более, или два или более костимулирующих доменов, выбранных из CD28, 4-1ВВ (CD137), или их фрагмента или комбинации. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены CD28 и 4-1ВВ (CD137) или их соответствующие фрагменты. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены CD28 и ОХ40 (CD134) или их соответствующие фрагменты. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены CD8 и CD28 или их соответствующие фрагменты. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены CD28 или его фрагмент. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены 4-1ВВ (CD137) или его фрагмент.В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены ОХ40 (CD134) или его фрагмент. В некоторых случаях CAR, описанный в данной заявке, содержит костимулирующие домены CD8 или его фрагмент. В некоторых случаях CAR, описанный в данной заявке, содержит по меньшей мере один ко стимулирующий домен DAP10 или его фрагмент. В некоторых случаях CAR, описанный в данной заявке, содержит по меньшей мере один костимулирующий домен DAP12 или его фрагмент.
[0097] Внутриклеточный сигнальный домен, также известный как цитоплазматический домен, CAR согласно настоящему изобретению отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, в которую поместили CAR. Термин «эффекторная функция» относится к специализированной функции клетки. Эффекторная функция Т-клетки, например, может представлять собой цитолитическую активность или хелперную активность, включая секрецию цитокинов. Таким образом, термин «внутриклеточный сигнальный домен» относится к части белка, которая передает сигнал эффекторной функции и направляет клетку на осуществление специализированной функции. Хотя обычно может быть использован весь внутриклеточный сигнальный домен, во множестве случаев не обязательно использовать полноразмерную цепь. В случае если используют укороченную часть внутриклеточного сигнального домена, такую укороченную часть можно использовать вместо интактной цепи при условии, что она передает сигнал эффекторной функции. Следовательно, подразумевают, что термин внутриклеточный сигнальный домен включает любую укороченную часть внутриклеточного сигнального домена, достаточную для передачи сигнала эффекторной функции. В некоторых вариантах реализации внутриклеточный домен дополнительно содержит сигнальный домен для активации Т-клеток. В некоторых случаях сигнальный домен для активации Т-клеток содержит домен, полученный из TCR-дзета, FcR-гамма, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b или CD66d. В некоторых случаях сигнальный домен для активации Т-клеток содержит домен, полученный из CD3ζ.
[0098] В вариантах реализации в настоящей заявке предложена выделенная нуклеиновая кислота, кодирующая химерный антигенный рецептор (CAR), причем указанный CAR содержит: (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1ВВ или CD28, или и то, и другое; (е) сигнальный домен CD3-дзета; и необязательно (f) укороченный рецептор эпидермального фактора роста (HER1t или HER1t1).
[0099] В объем настоящего изобретения входят последовательности нуклеиновых кислот, которые кодируют функциональные части CAR, описанные в данной заявке. Функциональные части включают, например, такие части CAR, которые сохраняют способность распознавать клетки-мишени, или обнаруживать, лечить или предотвращать заболевание в сходной степени, такой же степени или в большей степени, чем исходный CAR. В отношении последовательности нуклеиновой кислоты, кодирующей исходный CAR, последовательность нуклеиновой кислоты, кодирующая функциональную часть CAR, может кодировать белок, содержащий, например, приблизительно 10%, 25%, 30%, 50%, 68%, 80%, 90%, 95% или более от исходного CAR.
[00100] В вариантах реализации CAR содержит дополнительные аминокислоты на амино- или карбоксиконце указанной части, или на обоих концах, указанные дополнительные аминокислоты не обнаруживаются в последовательности аминокислот исходного CAR. Желательно, дополнительные аминокислоты не препятствуют биологической функции функциональной части, например, распознаванию клеток-мишеней, обнаружению рака, лечению или предотвращению рака и т.д. Более желательно, дополнительные аминокислоты повышают биологическую активность CAR по сравнению с биологической активностью исходного CAR.
[00101] Термин «функциональный вариант» в данной заявке относится к полипептиду или белку, обладающему существенной или значительной идентичностью или подобием последовательностей с эталонным полипептидом, и сохраняет биологическую активность эталонного полипептида, вариантом которого он является. Функциональные варианты включают, например, такие варианты CAR, описанные в данной заявке (исходного CAR), которые сохраняют способность распознавать клетки-мишени в сходной степени, такой же степени или в большей степени, чем исходный CAR. В отношении последовательности нуклеиновой кислоты, кодирующей исходный CAR, последовательность нуклеиновой кислоты, кодирующая функциональный вариант CAR, может быть, например, приблизительно на 10% идентична, приблизительно на 25% идентична, приблизительно на 30% идентична, приблизительно на 50% идентична, приблизительно на 65% идентична, приблизительно на 80% идентична, приблизительно на 90% идентична, приблизительно на 95% идентична или приблизительно на 99% идентична последовательности нуклеиновой кислоты, кодирующей исходный CAR.
[00102] CAR, описанный в данной заявке, включает (включая его функциональные части и функциональные варианты) гликозилированные, амидированные, карбоксилированные, фосфорилированные, этерифицированные, N-ацилированные, циклизированные посредством, например, дисульфидного мостика, или превращенные в соль присоединения кислоты и/или необязательно димеризованные, или полимеризованные, или конъюгированные варианты.
Связывающая антиген группа.
[00103] В вариантах реализации CAR, описанный в данной заявке, содержит специфичный к мишени связывающий элемент, иначе называемый антигенсвязывающей группой. В вариантах реализации CAR, описанный в данной заявке, сконструирован для нацеливания на интересующий антиген посредством конструирования желательной связывающей антиген группы, которая специфично связывается с антигеном на клетке.
[00104] В вариантах реализации связывающая антиген группа CAR, описанного в данной заявке, специфична к MUC16 (MUC16-CAR). MUC16-специфичный CAR, когда экспрессирован на поверхности клетки, перенацеливает специфичность Т-клеток на MUC16 человека. В вариантах реализации связывающий антиген домен включает одноцепочечный фрагмент антитела (scFv), содержащий вариабельный домен легкой цепи (VL) и вариабельный домен тяжелой цепи (VH) моноклонального антитела против MUC16, специфичного к целевому антигену, соединенные гибким линкером, таким как глицин-сериновый линкер или линкер Уитлоу. В вариантах реализации scFv представляет собой MUC16-1 scFv, MUC16-2 scFv, MUC16-3 scFv, MUC16-4 scFv, MUC16-5 scFv, MUC16-6 scFv или MUC16-7 scFv. В вариантах реализации scFv гуманизирован. В некоторых вариантах реализации связывающая антиген группа может содержать VH и VL, которые направленно связаны, например, от N к С концу, VH-линкер-VL или VL-линкер-VH.
[00105] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% любой из последовательностей аминокислот, представленных в SEQ ID NO: 1, 3, 5, 7, 9, 12 и 14 (MUC16 VL).
[00106] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% любой из последовательностей аминокислот, представленных в SEQ ID NO: 2, 4, 6, 8, 10, 11, 13 и 15 (MUC16 VH).
[00107] В вариантах реализации CAR, описанный в данной заявке, содержит связывающие антиген группы VL (последовательности SEQ ID NO: 1, 3, 5, 7, 9, 12 или 14) и VH (последовательности SEQ ID NO: 2, 4, 6, 8, 10, 11 или 15) с Gly-Ser линкером (SEQ ID NO: 83 или SEQ ID NO: 197) или функциональными вариантами линкера.
[00108] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% любой из последовательностей аминокислот, представленных в SEQ ID NO: 27-57 (VH, VL и линкер).
[00109] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 2 (MUC16-1 VH).
[00110] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 1 (MUC16-1 VL).
[00111] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 4 (MUC16-2 VH).
[00112] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 3 (MUC16-2 VL).
[00113] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 6 (MUC16-3 VH).
[00114] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 5 (MUC16-3 VL).
[00115] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 8 (MUC16-4 VH).
[00116] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 7 (MUC16-4 VL).
[00117] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 10 (MUC16-5 VH-L).
[00118] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 11 (MUC16-5 VH-F).
[00119] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 9 (MUC16-5 VL).
[00120] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 13 (MUC16-6 VH).
[00121] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 12 (MUC16-6 VL).
[00122] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VH, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 15 (MUC16-7 VH).
[00123] В вариантах реализации CAR, описанный в данной заявке, содержит связывающую антиген группу, содержащую полипептид VL, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 14 (MUC16-7 VL).
[00124] В вариантах реализации связывающая антиген группа содержит сигнальный пептид GM-CSFRa, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 58.
[00125] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 27. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 28. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 29.
[00126] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 30.
[00127] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 31. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 32. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 33.
[00128] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 34. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 35. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 36.
[00129] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 37. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 38. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 39.
[00130] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 40. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 41. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 42.
[00131] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 43. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 44. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 45.
[00132] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 46. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 47. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 48.
[00133] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 49. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 50. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 51.
[00134] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 52. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 53. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 54.
[00135] В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 55. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 56. В вариантах реализации CAR, описанный в данной заявке, содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 57.
Домен стебля.
[00136] В вариантах реализации MUC16-CAR согласно настоящему изобретению содержит домен стебля, который обеспечивает разделение связывающей антиген группы и мембраны Т-клетки. В вариантах реализации домен стебля создает оптимальное межмембранное расстояние между эффектором и мишенью. В вариантах реализации домен стебля обеспечивает гибкость связывающего антиген домена, чтобы он достиг своей мишени. В одном варианте реализации домен стебля представляет собой шарнирный домен CDS-альфа.
[00137] В вариантах реализации шарнирный домен CD8-альфа содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 16.
Спенсеры.
[00138] В других вариантах реализации между внеклеточным доменом и трансмембранным доменом CAR присутствует спейсер. В данной заявке описано, что спейсер может содержать участок стебля и участок удлинения стебля, изображенные на Фиг. 3. В одном варианте реализации спейсер может содержать один участок стебля. В другом варианте реализации спейсер может содержать участок стебля (обозначенный «s») и участок(-ки) удлинения стебля, который в данной заявке обозначен «s-n'». Например, спейсер может содержать один (1) участок стебля и s'-n, где n может представлять собой 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20. В дополнительных вариантах реализации участок стебля может быть связан с участком удлинения стебля s'-n посредством линкера. Линкер, описанный в данной заявке, может включать, например, линкер GSG (SEQ ID NO: 85), линкер SGSG (SEQ ID NO: 86), линкер (G4S)3 (SEQ ID NO: 83), линкер (G4S)4 (SEQ ID NO: 200) и/или линкер Уитлоу.
[00139] В одном варианте реализации участок стебля и участок(-ки) удлинения стебля может происходить или может быть сконструирован из полипептида природного или синтетического происхождения. Участок стебля и/или участок(-ки) удлинения стебля могут содержать шарнирный(-е) домен(ы), полученный(-е) из белка поверхности клетки или его производных или вариантов. В некоторых вариантах реализации участок стебля и/или участок(-ки) удлинения стебля могут содержать шарнирный домен, полученный из CD28 или CDS-альфа (CD8a). В некоторых вариантах реализации каждый из участка стебля и участка(-ов) удлинения стебля может быть получен из по меньшей мере одного из шарнирного домена CDS-альфа, шарнирного домена CD28, шарнирного домена CTLA-4, внеклеточного домена LNGFR, шарнира IgG1, шарнира IgG4 и домена СН2-СН3. Стебель и участок(-ки) удлинения стебля можно отдельно получить из любой комбинации шарнирного домена CDS-альфа, шарнирного домена CD28, шарнирного домена CTLA-4, внеклеточного домена LNGFR, шарнира IgG1, шарнира IgG4 или домена СН2-СН3. В качестве примера, участок стебля можно получить из шарнирного домена CDS-альфа, и по меньшей мере один участок удлинения стебля можно получить из шарнирного домена CD28, таким образом, создавая гибридный спейсер. В качестве другого примера, участок стебля можно получить из шарнира IgG1 или шарнира IgG4, и по меньшей мере один участок удлинения стебля можно получить из домена СН2-СН3 IgG.
[00140] В некоторых вариантах реализации участок стебля может содержать один или более сайтов димеризации для образования гомо- или гетер одимер изо ванных химерных полипептидов. В других вариантах реализации участок стебля или один или более участков удлинения стебля могут содержать мутации, которые устраняют сайты димеризации вообще. В некоторых вариантах реализации участок(-ки) удлинения стебля может(-гут) содержать по меньшей мере на один сайт димеризации меньше по сравнению с участком стебля. Например, если участок стебля содержит два сайта димеризации, то участок удлинения стебля может содержать один или ноль сайтов димеризации. В качестве другого примера, если участок стебля содержит один сайт димеризации, то участок удлинения стебля может содержать ноль сайтов димеризации. В некоторых примерах на участке(-ах) удлинения стебля отсутствует сайт димеризации.
[00141] В некоторых аспектах вариантов реализации, описанных в данной заявке, участок стебля обсуждаемого связывающего антиген полипептида содержит последовательность с идентичностью по меньшей мере приблизительно на 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или более шарнирному домену CDS-альфа. Шарнирный домен CD8-альфа может содержать полипептидную последовательность с идентичностью по меньшей мере приблизительно на 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% или больше последовательности, представленной в SEQ ID NO: 16. В некоторых случаях, участок удлинения стебля содержит полипептидную последовательность с идентичностью по меньшей мере на 65%, 70%, 75%, 80%, 85%, 90%, 95% или более последовательности, представленной в SEQ ID NO: 16. В некоторых случаях, участок удлинения стебля содержит последовательность нуклеотидов с идентичностью по меньшей мере на 65%, 70%, 75%, 80%, 85%, 90%, 95% или более последовательности, представленной в SEQ ID NO: 108. В некоторых примерах участок стебля и участок удлинения стебля могут вместе содержать полинуклеотидную последовательность с идентичностью по меньшей мере на 65%, 70%, 75%, 80%, 85%, 90%, 95% или более последовательности, представленной в SEQ ID NO: 16.
Трансмембранный домен.
[00142] В вариантах реализации CAR содержит трансмембранный домен, который слит с внеклеточным доменом домена стебля CAR. В одном варианте реализации используют трансмембранный домен, который в природе связан с одним из доменов в CAR. В вариантах реализации транс мембранный домен представляет собой гидрофобную альфа-спираль, которая пронизывает мембрану.
[00143] Трансмембранный домен можно получить либо из природного, либо из синтетического источника. Если источник природный, домен можно получить из любого связанного с мембраной или трансмембранного белка. Транс мембранные участки, особенно пригодные для настоящего изобретения, могут происходить (т.е., содержать по меньшей мере трансмембранный(-е) участок(-ки)) из альфа-, бета- или дзета-цепи Т-клеточного рецептора, CD28, CD3-эпсилон, CD45, CD4, CD5, CD8-альфа, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154. В качестве альтернативы, трансмембранный домен может быть синтетическим, в указанном случае он будет содержать преимущественно гидрофобные остатки, такие как лейцин и валин. В вариантах реализации триплет фенилаланина, триптофана и валина будет находиться на каждом конце синтетического трансмембранного домена. Необязательно короткий олигонуклеотидный или полипептидный линкер, в вариантах реализации длиной от 2 до 10 аминокислот, может создать связь между трансмембранным доменом и цитоплазматическим сигнальным доменом CAR. В вариантах реализации линкер представляет собой глицин-сериновый линкер.
[00144] В вариантах реализации трансмембранный домен в CAR, описанный в данной заявке, представляет собой транс мембранный домен CDS-альфа. В вариантах реализации трансмембранный домен CDS-альфа содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 20.
[00145] В вариантах реализации трансмембранный домен в CAR, описанный в данной заявке, представляет собой трансмембранный домен CD28. В вариантах реализации трансмембранный домен CD28 содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 21.
Цитоплазматический домен (костимулирующий домен и сигнальный домен).
[00146] Цитоплазматический домен, также известный как внутриклеточный сигнальный домен CAR, описанный в данной заявке, отвечает за активацию по меньшей мере одной из нормальных эффекторных функций иммунной клетки, в которую поместили CAR. Термин «эффекторная функция» относится к специализированной функции клетки. Эффекторная функция Т-клетки, например, может представлять собой цитолитическую активность или хелперную активность, включая секрецию цитокинов. Таким образом, термин «внутриклеточный сигнальный домен» относится к части белка, которая передает сигнал эффекторной функции и направляет клетку на осуществление специализированной функции. Хотя обычно может быть использован весь внутриклеточный сигнальный домен, во множестве случаев не обязательно использовать полноразмерную цепь. В случае если используют укороченную часть внутриклеточного сигнального домена, такую укороченную часть можно использовать вместо интактной цепи при условии, что она передает сигнал эффекторной функции. Следовательно, подразумевают, что термин внутриклеточный сигнальный домен включает любую укороченную часть внутриклеточного сигнального домена, достаточную для передачи сигнала эффекторной функции.
[00147] Примеры внутриклеточных сигнальных доменов для применения в CAR, описанных в данной заявке, могут включать цитоплазматические последовательности Т-клеточного рецептора (TCR) и корецепторов, которые действуют согласованно, чтобы начать передачу сигнала после связывания рецептором антигена, а также любое производное или вариант данных последовательностей и любую синтетическую последовательность, которая обладает такой же функциональной способностью.
[00148] Сигналов, выработанных через TCR отдельно, как правило, недостаточно для полной активации Т-клетки, и также требуется вторичный или костимулирующий сигнал. Таким образом, активация Т-клетки может быть опосредована двумя различными классами цитоплазматических сигнальных последовательностей: теми, которые инициируют антиген-зависимую первичную активацию через TCR (первичные цитоплазматические сигнальные последовательности), и теми, которые действуют независимым от антигена образом, чтобы создать вторичный или костимулирующий сигнал (вторичные цитоплазматические сигнальные последовательности).
[00149] Первичные цитоплазматические сигнальные последовательности регулируют первичную активацию комплекса TCR либо стимулирующим путем, либо ингибирующим путем. Первичные цитоплазматические сигнальные последовательности, которые действуют стимулирующим путем, могут содержать сигнальные мотивы, которые известны как иммунорецепторные тирозиновые активирующие мотивы, или ITAM.
[00150] Примеры содержащих ITAM первичных цитоплазматических сигнальных последовательностей, которые особенно пригодны в настоящем изобретении, включают таковые, происходящие из TCR-дзета, FcR-гамма, FcR-бета, CD3-гамма, CD3-дельта, CD3-эпсилон, CD5, CD22, CD79a, CD79b и CD66d. В вариантах реализации цитоплазматическая сигнальная молекула в CAR, описанном в данной заявке, содержит цитоплазматическую сигнальную последовательность, полученную из CD3-дзета.
[00151] В вариантах реализации цитоплазматический домен CAR может быть разработан таким образом, чтобы он содержал сигнальный домен CD3-дзета сам по себе или в комбинации с любым(и) другим(и) желательным(и) цитоплазматическим(и) доменом(-ами), полезным(и) в контексте CAR, описанного в данной заявке. Например, цитоплазматический домен CAR может содержать часть цепи CD3-дзета и костимулирующую сигнальную область. Костимулирующая сигнальная область относится к части CAR, содержащей внутриклеточный домен костимулирующей молекулы. Костимулирующая молекула представляет собой молекулу поверхности клетки, отличную от рецептора антигена или его лигандов, которые необходимы для эффективного ответа лимфоцитов на антиген. Примеры таких молекул включают CD27, CD28, 4-1ВВ (CD137), ОХ40, CD30, CD40, PD-1, ICOS, связанный с функцией лимфоцитов антиген 1 (LFA-1), CD2, CD7, LIGHT, NKG2C, В7-Н3, DAP10, DAP12 и лиганд, который специфично связывается с CD83, и тому подобные молекулы. В вариантах реализации костимулирующие молекулы можно использовать вместе, например, CD28 и 4-1ВВ или CD28 и ОХ40. Таким образом, хотя в настоящем изобретении приведен пример, главным образом, 4-1ВВ и CD28 в качестве костимулирующего сигнального элемента, другие костимулирующие элементы входят в объем настоящего изобретения.
[00152] Цитоплазматические сигнальные последовательности внутри цитоплазматической сигнальной части CAR, описанного в данной заявке, могут быть связаны друг с другом в произвольном или определенном порядке. Необязательно короткий олиго- или полипептидный линкер длиной от 2 до 10 аминокислот может образовать указанную связь. Дублет глицин-серин представляет собой особенно подходящий линкер.
[00153] В одном варианте реализации цитоплазматический домен содержит сигнальный домен CD3-дзета и сигнальный домен CD28. В другом варианте реализации цитоплазматический домен содержит сигнальный домен CD3-дзета и сигнальный домен 4-1ВВ. В еще одном варианте реализации цитоплазматический домен содержит сигнальный домен CD3-дзета и сигнальные домены CD28 и 4-1ВВ.
[00154] В одном варианте реализации цитоплазматический домен в CAR, описанный в данной заявке, содержит сигнальный домен 4-1ВВ и сигнальный домен CD3-дзета, причем сигнальный домен 4-1ВВ содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% полипептидной последовательности, представленной в SEQ ID NO: 22, и сигнальный домен CD3-дзета содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% нуклеотидной последовательности, представленной в SEQ ID NO: 26.
[00155] В одном варианте реализации цитоплазматический домен в CAR, описанный в данной заявке, разработан таким образом, чтобы он содержал сигнальный домен CD28 и сигнальный домен CD3-дзета, причем указанный сигнальный домен CD28 содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% полипептидной последовательности, представленной в SEQ ID NO: 23, и сигнальный домен CD3-дзета содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% полипептидной последовательности, представленной в SEQ ID NO: 26.
[00156] В одном варианте реализации цитоплазматический домен в CAR, описанном в данной заявке, содержит сигнальный домен 4-1ВВ и сигнальный домен CD3-дзета, причем сигнальный домен 4-1ВВ содержит последовательность аминокислот, представленную в SEQ ID NO: 22, и сигнальный домен CD3-дзета содержит последовательность аминокислот, представленную в SEQ ID NO: 26.
Дополнительные генетические элементы.
[00157] Хотя клеточные методы лечения подают большие надежды для лечения заболеваний человека, значительная токсичность от самих клеток или от продуктов их трансгенов препятствовали клиническому исследованию. В вариантах реализации, описанных в данной заявке, эффекторные иммунные клетки, содержащие CAR, описанный в данной заявке, которые вводили путем инфузии млекопитающему субъекту, например, человеку, можно удалить, чтобы регулировать действие таких эффекторных иммунных клеток, если в результате их применения возникает токсичность. Следовательно, в некоторых вариантах реализации дополнительно к терапевтическому специфичному к MUC16 химерному антигенному рецептору, описанному в данной заявке, в сконструированную эффекторную иммунную клетку, описанную в данной заявке, также внедряют второй ген. Второй ген, по сути, является «переключателем уничтожения», который позволяет осуществить удаление содержащих MUC16-CAR или MUC16-CAR/mbIL-15 клеток. В некоторых вариантах реализации «переключатель уничтожения» представляет собой метку HER1 или метку CD20, которая содержит полипептид HER1 или полипептид CD20, который содержит по меньшей мере связывающий антитело эпитоп HER1 или CD20 или его функциональный фрагмент и необязательно сигнальную полипептидную последовательность или ее фрагмент.
[00158] В некоторых вариантах реализации второй ген представляет собой метку HER1, которая представляет собой рецептор эпидермального фактора роста (HER1) или его фрагмент или вариант. В вариантах реализации второй ген представляет собой метку HER1, которая представляет собой укороченный рецептор эпидермального фактора роста 1 человека (например, HER1t или HER1t1). В некоторых случаях второй ген представляет собой вариант укороченного рецептора эпидермального фактора роста 1 человека. В вариантах реализации по меньшей мере один из HER1, HER1t и HER1t1 обеспечивает механизм безопасности, позволяя осуществить удаление введенных путем инфузии CAR-Т-клеток посредством введения одобренного FDA цетуксимаба или любого антитела, которое распознает HER1, HER1t и/или HER1t1. В вариантах реализации ген HER1t содержит последовательность нуклеотидов, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 65. В вариантах реализации ген HER1t1 содержит последовательность нуклеотидов, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 66. Укороченная последовательность HER1, например, HER1t и HER1t1, устраняет возможность связывания лиганда EGF, гомо- и гетеродимеризацию EGFR и опосредованную EGFR передачу сигналов, при этом сохраняя незатронутым связывание цетуксимаба с рецептором (Ferguson, K., 2008. A structure-based view of Epidermal Growth Factor Receptor regulation. Annu Rev Biophys, том 37, стр. 353-373).
[00159] В дополнительных вариантах реализации дополнительно к терапевтическому специфичному к MUC16 химерному антигенному рецептору согласно настоящему изобретению второй введенный ген представляет собой метку CD20. В некоторых случаях метка CD20 представляет собой полноразмерный полипептид CD20 или укороченный полипептид CD20 (CD20t-1). В некоторых случаях метка CD20, например, CD20 или CD20t-1, также обеспечивает механизм безопасности, позволяя удалить введенные путем инфузии CAR-T-клетки посредством введения одобренной FDA терапии ритуксимабом. В некоторых вариантах реализации метка CD20 содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 36. В некоторых вариантах реализации метка CD20 представляет собой метку CD20t-1 и содержит полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 68. В некоторых вариантах реализации метка CD20 кодируется геном CD20, который содержит последовательность нуклеотидов, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 160. В некоторых вариантах реализации метка CD20 кодируется геном CD20t-1, который содержит последовательность нуклеотидов, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 160.
[00160] В вариантах реализации вектор CAR, содержащий CAR, описанный в данной заявке, дополнительно содержит полноразмерную метку CD20, содержащую последовательность нуклеиновой кислоты, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 159.
[00161] В вариантах реализации ген, кодирующий метку уничтожения, например, метку HER1t, HER1t-1, CD20 или CD20M, соединяют генетически с MUC16-CAR на 3'-конце в одной рамке считывания с саморасщепляющимся пептидом, например, но не ограничиваясь пептидом вируса Thosea asigna (Т2А). В вариантах реализации пептид Т2А содержит последовательность аминокислот, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 72.
[00162] В вариантах реализации ген метки уничтожения клонирован в остов лентивирусной плазмиды в одной рамке считывания с геном MUC16-CAR. В других вариантах реализации метка уничтожения клонирована в отдельный лентивирусный вектор. В других вариантах реализации оба гена клонированы в вектор транспозона Спящая красавица. В еще других вариантах реализации метка уничтожения, такая как HER1t, HER1t-1, CD20 или CD20t-1, клонирована в отдельный вектор транспозона Спящая красавица. В некоторых вариантах реализации метки уничтожения содержат сигнальный пептид, например, сигнальный пептид GM-CSFRa, причем сигнальный пептид GM-CSFRa идентичен по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 58. В некоторых вариантах реализации сигнальный пептид представляет собой IgK с последовательностью, по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичной последовательности нуклеиновой кислоты, представленной в SEQ ID NO: 59. В некоторых случаях сигнальный пептид можно выбрать из IgE и CD8α и их вариантов и фрагментов.
[00163] Примеры кассет экспрессии генов, кодирующих CAR и метку уничтожения, описанные в данной заявке, показаны на Фиг. 1 и 2.
Примеры открытых рамок считывания CAR
[00164] Примеры открытых рамок считывания CAR и рецептора MUC16 человека, входящих в способы и композиции, описанные в данной заявке, представлены в Таблице 1.
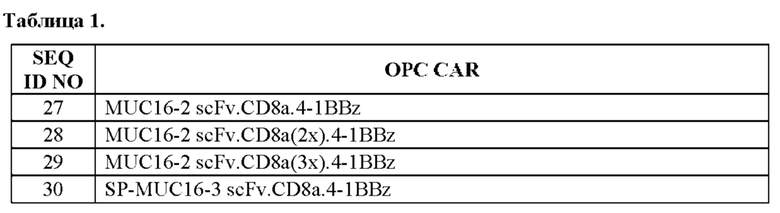
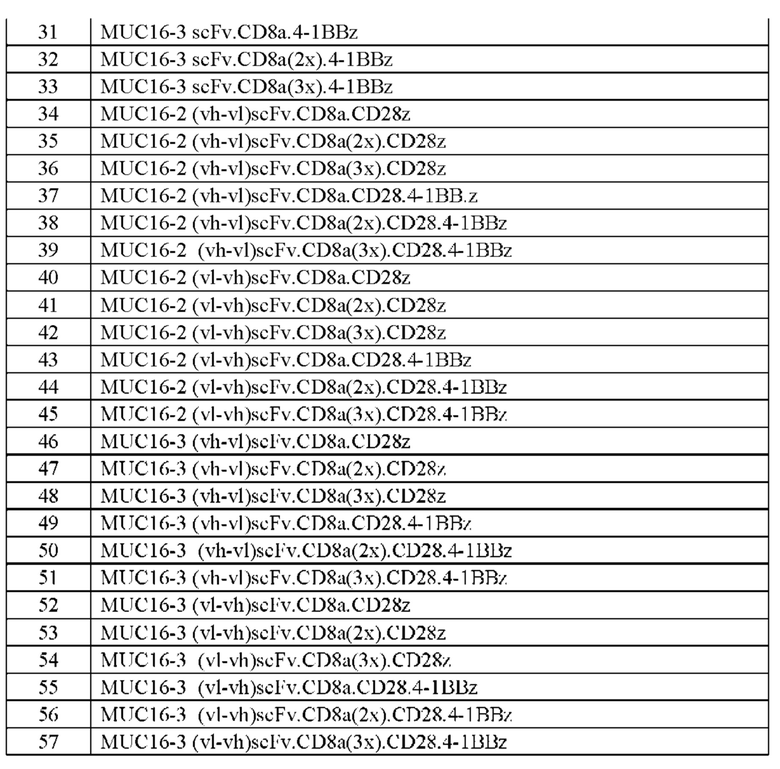
[00165] В вариантах реализации в настоящей заявке предложена выделенная нуклеиновая кислота, кодирующая CAR, причем CAR содержит полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот, представленной в SEQ ID NO: 3-4 или SEQ ID NO: 5-6. [00166] В каждом из вариантов реализации, перечисленных в Таблице 1, с «MUC16-2 scFv», связывающая антиген CAR группа представляет собой MUC16-2 scFv, содержащий полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 3-4. В вариантах реализации MUC16-3 scFv содержит сигнальный пептид GM-CSFRa, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 58.
[00167] В каждом из вариантов реализации в Таблице 1 с «CD8a», транс мембранный участок CAR содержит трансмембранный домен CD8-альфа, содержащий полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 20, и домен стебля представляет собой CD8a, содержащий полипептид, идентичный по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 16.
[00168] В каждом из вариантов реализации в Таблице 1 с «CD28m», внутриклеточный домен CAR содержит CD28 с последовательностью аминокислот, идентичной по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 21.
[00169] В каждом из вариантов реализации в Таблице 1 с «Т2А», ОРС CAR содержит саморасщепляющийся пептид вируса Thosea asigna (Т2А), который позволяет получить множество продуктов генов с одного вектора. В вариантах реализации пептид Т2А содержит последовательность аминокислот, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 72.
[00170] В вариантах реализации в Таблице 1 с «HER1t», ОРС CAR содержит укороченный рецептор эпидермального фактора роста 1 человека (HER1t), который обеспечивает механизм безопасности, позволяя удалить введенные путем инфузии CAR-T-клетки посредством введения одобренной FDA терапии цетуксимабом. Ген HER1t, описанный в данной заявке, может содержать полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 65. Если не указано иное в Таблице 1, метки HER1t содержат сигнальный пептид GM-CSFRa («GM-CSFRsp») (SEQ ID NO: 58). В некоторых вариантах реализации HER1t можно заменить другой меткой, например, HER1t-1. Ген HER1t-1, описанный в данной заявке, может содержать полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 66. В вариантах реализации в Таблице 1 с «IgKsp», сигнальный пептид представляет собой IgK, содержащий последовательность аминокислот, по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичную последовательности аминокислот SEQ ID NO: 59.
[00171] В вариантах реализации в Таблице 1 с «4-1ВВ», ОРС CAR содержит костимулирующую молекулу, содержащую полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 22.
[00172] В вариантах реализации в Таблице 1 с «FL CD20», ОРС CAR содержит полноразмерную метку CD20, содержащую полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 67. CD20 обеспечивает механизм безопасности, позволяя удалить введенные путем инфузии CAR-T-клетки посредством введения одобренной FDA терапии ритуксимабом. В других вариантах реализации FL CD20 можно заменить CD20t-1, содержащим полипептидную последовательность, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 68.
[00173] В некоторых вариантах реализации в Таблице 1, ОРС CAR может находиться под контролем индуцируемого промотора для транскрипции генов. В одном аспекте, индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®. В некоторых вариантах реализации ОРС CAR и компоненты переключателя генов можно сконфигурировать, как изображено на Фиг. 1-2.
Цитокины.
[00174] В некоторых вариантах реализации CAR, описанный в данной заявке, вводят субъекту с одним или более дополнительными терапевтическими агентами, которые включают, но не ограничены цитокинами. В некоторых случаях цитокин включает по меньшей мере один хемокин, интерферон, интерлейкин, лимфокин, фактор некроза опухоли или его вариант или комбинацию. В некоторых случаях цитокин представляет собой интерлейкин. В некоторых случаях интерлейкин представляет собой по меньшей мере один из IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-14, IL-15, IL-16, IL-17, IL-18, IL-19, IL-20, IL-21, IL-22, IL-23, IL-24, IL-25, IL-26, IL-27, IL-28, IL-29, IL-30, IL-31, IL-32, IL-33 и его функциональных вариантов и фрагментов. В некоторых вариантах реализации цитокины могут быть связаны с мембраной или секретированы. В вариантах реализации цитокин представляет собой растворимый IL-15, растворимый комплекс IL-15/IL-15Rα (например, ALT-803). В некоторых случаях интерлейкин может включать связанный с мембраной IL-15 (mbIL-15) или слитые IL-15 и IL-15Rα. В некоторых вариантах реализации mbIL-15 представляет собой связанный с мембраной химерный IL-15, который может совместно экспрессироваться с модифицированной эффекторной иммунной клеткой, описанной в данной заявке. В некоторых вариантах реализации mbIL-15 включает полноразмерный IL-15 (например, нативный полипептид IL-15) или его фрагмент или вариант, слитый в одной рамке считывания с полноразмерным IL-15Rα, его функциональным фрагментом или вариантом. В некоторых случаях IL-15 опосредованно связан с IL-15Rα с помощью линкера. В некоторых случаях mbIL-15 такой, как описано в Hurton и др. «Tethered IL-15 augments antitumor activity and promotes a stem-cell memory subset in tumor-specific T cells», PNAS 2016. В некоторых случаях цитокин экспрессируется в той же эффекторной иммунной клетке, что и CAR.
[00175] В дополнительных вариантах реализации эффекторная иммунная клетка, экспрессирующая CAR, описанный в данной заявке, экспрессирует связанный с мембраной IL-15 («mIL-15 или mbIL-15»). В аспектах настоящего изобретения mbIL-15 включает слитый белок IL-15 с IL-15Rα. В дополнительных вариантах реализации mbIL-15 содержит последовательность аминокислот, идентичную по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности аминокислот SEQ ID NO: 69. В некоторых случаях CAR и цитокин экспрессируются в отдельных векторах. В определенных случаях векторы могут представлять собой лентивирусные векторы, ретровирусные векторы или транспозоны Спящая красавица.
[00176] В некоторых вариантах реализации mbIL-15 экспрессируется с меткой клетки, такой как HER1t, HER-It-1, CD20t-1 или CD20, описанная в данной заявке. mbIL-15 может экспрессироваться в одной рамке считывания с HER1t, HER-It-1, CD20t-1 или CD20.
[00177] В некоторых вариантах реализации mbIL-15 может находиться под контролем индуцируемого промотора для транскрипции генов. В одном аспекте индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®.
[00178] В другом аспекте интерлейкин может включать IL-12. В некоторых вариантах реализации IL-12 представляет собой одно цепочечный IL-12 (scIL-12), чувствительный к протеазе IL-12, дестабилизированный IL-12, связанный с мембраной IL-12, интеркалированный IL-12. В некоторых случаях варианты IL-12 представляют собой варианты, описанные в WO 2015/095249, WO 2016/048903, WO 2017/062953, все из которых полностью включены в данную заявку посредством ссылки.
[00179] В некоторых вариантах реализации цитокины, описанные выше, могут находиться под контролем индуцируемого промотора для транскрипции генов. В одном аспекте индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®.
Переключатель генов.
[00180] В данной заявке предложены полипептиды переключателей генов, полинуклеотиды, кодирующие полипептиды индуцируемых лигандами переключателей генов, и способы и системы, включающие данные полипептиды и/или полинуклеотиды. Термин «переключатель генов» относится к комбинации элемента ответа, связанного с промотором, и, например, системы на основе рецептора экдизона (EcR), который в присутствии одного или более лигандов модулирует экспрессию гена, в который входят элемент ответа и промотор. Строго регулируемые индуцируемые системы экспрессии генов или переключателей генов пригодны для различных применений, таких как генотерапия, крупномасштабная продукция белков в клетках, основанные на клеточной системе высокопроизводительные скрининговые анализы, функциональная геномика и регуляция признаков в трансгенных растениях и животных. Такие индуцируемые системы экспрессии генов могут включать индуцируемые лигандом гетерологичные системы экспрессии генов.
[00181] В ранней версии переключателя генов на основе EcR используют полипептиды EcR Drosophila melanogaster (DmEcR) и RXR Mus musculus (MmRXR), и показали, что данные рецепторы в присутствии стероида понастерона А трансактивируют репортерные гены в линиях клеток млекопитающих и трансгенных мышах (Christopherson и др., 1992; No и др., 1996). Позже Suhr и др., 1998, показали, что нестероидный агонист экдизона тебуфенозид вызывает высокий уровень трансактивации репортерных генов в клетках млекопитающих посредством EcR Bombyx mori (BmEcR) в отсутствие экзогенного гетеродимерного партнера.
[00182] В международной заявке на патент №PCT/US97/05330 (WO 97/38117) и PCT/US99/08381 (WO 99/58155) описаны способы модуляции экспрессии экзогенного гена, в которых конструкция ДНК, содержащая экзогенный ген и элемент ответа на экдизон, активируется второй конструкцией ДНК, содержащей рецептор экдизона, который в присутствии его лиганда и необязательно в присутствии рецептора способен действовать как молчаливый партнер, связывается с элементом ответа на экдизон, чтобы вызвать экспрессию гена. В данном примере рецептор экдизона выделяли из Drosophila melanogaster. Обычно, в таких системах требуется присутствие молчаливого партнера, предпочтительно рецептора ретиноида X (RXR), чтобы обеспечить оптимальную активацию. В клетках млекопитающих рецептор экдизона (EcR) насекомого способен гетеродимеризоваться с рецептором ретиноида X (RXR) млекопитающего и, таким образом, может применяться для регуляции экспрессии целевых генов или гетерологичных генов лиганд-зависимым образом. В международной заявке на патент №PCT/US98/14215 (WO 99/02683) описано, что рецептор экдизона, выделенный из тутового шелкопряда Bombyx mori, функционален в системах млекопитающих без потребности в экзогенном партнере по димеризации.
[00183] В патенте США №6,265,173 описано, что различных представителей суперсемейства рецепторов стероидных гормонов/гормонов щитовидной железы можно комбинировать с рецептором ultraspiracle (USP) Drosophila melanogaster или его фрагментами, содержащими по меньшей мере домен димеризации USP, для применения в системе экспрессии генов. В патенте США №5,880,333 описана гетеродимерная система EcR и ultraspiracle (USP) Drosophila melanogaster, применяемая в растениях, в которой трансактивирующий домен и связывающий ДНК домен расположены на двух различных гибридных белках. В каждом из данных случаев трансактивирующий домен и связывающий ДНК домен (либо в виде нативного EcR, как в международной заявке на патент №PCT/US98/14215, либо в виде модифицированного EcR, как в международной заявке на патент №PCT/US97/05330) были включены в состав одной молекулы, а других гетеродимерных партнеров, либо USP, либо RXR, использовали в их нативном состоянии.
[00184] В международной заявке на патент №PCT/US01/0905 описана индуцируемая система экспрессии генов на основе рецептора экдизона, в которой трансактивирующий и связывающий ДНК домены отделены друг от друга путем их размещения на двух различных белках, что приводит к сильно сниженной фоновой активности в отсутствие лиганда и значительно повышенной активности по сравнению с фоновой в присутствии лиганда. Данная двугибридная система представляет собой значительно улучшенную индуцируемую систему модуляции экспрессии генов по сравнению с двумя системами, описанными в заявках PCT/US97/05330 и PCT/US98/14215. Полагают, что в двугибридной системе используется способность пары взаимодействующих белков привести домен активации транскрипции в более благоприятное положение по сравнению со связывающим ДНК доменом так, что когда связывающий ДНК домен связывается с сайтом связывания ДНК на гене, трансактивирующий домен более эффективно активирует промотор (см., например, патент США №5,283,173). Двугибридная система экспрессии генов содержит две кассеты экспрессии генов: первую, кодирующую связывающий ДНК домен, слитый с полипептидом ядерного рецептора, и вторую, кодирующую трансактивирующий домен, слитый с отличным полипептидом ядерного рецептора. Полагают, что в присутствии лиганда происходит конформационное изменение, которое вызывает взаимодействие первого полипептида со вторым полипептидом, тем самым приводя к димеризации связывающего ДНК домена и трансактивирующего домена. Поскольку связывающий ДНК и трансактивирующий домены находятся на двух различных молекулах, фоновая активность в отсутствие лиганда сильно снижается.
[00185] Некоторые модификации указанной двугибридной системы также могут обеспечить улучшенную чувствительность к нестероидным лигандам, например, диацилгидразинам, по сравнению со стероидными лигандами, например, понастероном А («PonA») или муристероном А («MurA»). То есть, по сравнению со стероидами, нестероидные лиганды вызывали более высокую активность транскрипции гена при более низкой концентрации лиганда. Более того, двугибридная система позволяет избежать некоторых побочных эффектов вследствие сверхэкспрессии RXR, которые могут произойти при применении немодифицированного RXR в качестве переключающего партнера. В предпочтительной двугибридной системе нативные связывающий ДНК и трансактивирующий домены EcR или RXR удаляют, и, в результате, уменьшается вероятность, что данные гибридные молекулы будут взаимодействовать с другими рецепторами стероидных гормонов, присутствующими в клетке, тем самым приводя к уменьшению побочных эффектов.
[00186] Рецептор экдизона (EcR) является представителем суперсемейства ядерных рецепторов и относится к подсемейству 1, группе Н (в данной заявке называют «ядерными рецепторами группы Н»). Представители каждой группы на 40-60% идентичны по последовательности аминокислот в домене Е (лиганд-связывающем домене) (Laudet и др., A Unified Nomenclature System for the Nuclear Receptor Subfamily, 1999; Cell 97: 161-163). Дополнительно к рецептору экдизона, другие представители данной группы Н подсемейства 1 ядерных рецепторов включают: вездесущий рецептор (UR), орфанный рецептор 1 (OR-1), ядерный рецептор 1 стероидных гормонов (NER-1), RXR-взаимодействующий белок 15 (RIP-15), β-рецептор X печени (LXRβ), белок, подобный рецептору стероидных гормонов (RLD-1), рецептор X печени (LXR), α-рецептор X печени (LXRα), фарнезоидный рецептор X (FXR), взаимодействующий с рецептором белок 14 (RIP-14) и рецептор фарнезола (HRR-1).
[00187] В некоторых случаях индуцируемый промотор («1Р») может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH® Intrexon Corporation. В некоторых случаях переключатель генов можно выбрать из компонентов рецептора на основе экдизона, описанных, без ограничения, в любой из систем, описанных в: PCT/US2001/009050 (WO 2001/070816); патентах США№7,091,038; 7,776,587; 7,807,417; 8,202,718; PCT/US2001/030608 (WO 2002/029075); патентах США №8,105,825; 8,168,426; PCT/1J52002/005235 (WO 2002/066613); заявке на патент США №10/468,200 (публикация заявки на патент США №20120167239); PCT/US2002/005706 (WO 2002/066614); патентах США №7,531,326; 8,236,556; 8,598,409; PCT/U52002/005090 (WO 2002/066612); патенте США номер 8,715,959 (публикация заявки на патент США №20060100416); PCT/US2002/005234 (WO 2003/027266); патентах США №7,601,508; 7,829,676; 7,919,269; 8,030,067; PCT/U52002/005708 (WO 2002/066615); заявке на патент США №10/468,192 (публикация заявки на патент США №20110212528); PCT/US2002/005026 (WO 2003/027289); патентах США №7,563,879; 8,021,878; 8,497,093; PCT/US2005/015089 (WO 2005/108617); патенте США номер 7,935,510; 8,076,454; PCT/U52008/011270 (WO 2009/045370); заявке на патент США№12/241,018 (публикация заявки на патент США №20090136465); PCT/US2008/011563 (WO 2009/048560); заявке на патент США №12/247,738 (публикация заявки на патент США №20090123441); PCT/US2009/005510 (WO 2010/042189); заявке на патент США №13/123,129 (публикация заявки на патент США №20110268766); PCT/US2011/029682 (WO 2011/119773); заявке на патент США №13/636,473 (публикация заявки на патент США №20130195800); PCT/US2012/027515 (WO 2012/122025); и патенте США №9,402,919; каждый из которых полностью включен в данную заявку посредством ссылки.
[00188] Предложены системы модуляции экспрессии CAR и/или цитокина в клетке-хозяине, содержащие полинуклеотиды, кодирующие полипептиды переключателей генов, описанные в данной заявке. Дополнительно в данной заявке предложены полинуклеотиды, кодирующие полипептиды переключателей генов для индуцируемого лигандом контроля экспрессии генов, причем указанные полипептиды переключателей генов содержат (а) первый полипептид переключателя генов, содержащий ДНК-связывающий домен (DBD), слитый с лиганд-связывающим доменом ядерного рецептора; и (b) второй полипептид переключателя генов, содержащий трансактивирующий домен, слитый с лиганд-связывающим доменом ядерного рецептора; причем указанные первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером. В некоторых вариантах реализации линкер представляет собой расщепляемую линкерную последовательность или вызывающую проскок рибосомы линкерную последовательность, выбранную из группы, состоящей из 2А, GSG-2A, линкера GSG (SEQ ID NO: 85), линкера SGSG (SEQ ID NO: 86), вариантов furinlink и его производных. В некоторых вариантах реализации линкер 2А представляет собой линкер р2А, линкер Т2А, линкер F2A или линкер Е2А.
[00189] В некоторых вариантах реализации связывающий ДНК домен (DBD) включает по меньшей мере один из GAL4 (DBD GAL4), DBD LexA, DBD фактора транскрипции, DBD представителя суперсемейства ядерных рецепторов стероидных гормонов/гормонов щитовидной железы, DBD бактериального LacZ и DBD дрожжей. В некоторых случаях трансактивирующий домен включает по меньшей мере один из трансактивирующего домена VP16 и трансактивирующего домена кислого активатора В42. В других случаях лиганд-связывающий домен ядерного рецептора включает по меньшей мере один из рецептора экдизона (EcR), вездесущего рецептора, орфанного рецептора 1, NER-1, ядерного рецептора 1 стероидных гормонов, взаимодействующего с рецептором ретиноида X белка 15, β-рецептора X печени, белка, подобного рецептору стероидных гормонов, рецептора X печени, α-рецептора X печени, фарнезоидного рецептора X, взаимодействующего с рецептором белка 14 и рецептора фарнезола. В некоторых вариантах реализации лиганд-связывающий домен ядерного рецептора происходит из полипептидной последовательности рецептора экдизона, представленной в SEQ ID NO: 91 и 92.
[00190] В еще одном варианте реализации первый полипептид переключателя генов содержит DBD GAL4, слитый с лиганд-связывающим доменом ядерного рецептора EcR, и второй полипептид переключателя генов содержит трансактивирующий домен VP16, слитый с лиганд-связывающим доменом ядерного рецептора X ретиноидов (RXR). В некоторых случаях первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером, который выбран из группы, состоящей из 2А, GSG-2A, линкера GSG (SEQ ID NO: 85), линкера SGSG (SEQ ID NO: 86), вариантов furinlink и их производных.
[00191] В некоторых вариантах реализации два или более полипептидов, кодируемых полинуклеотидом, описанным в данной заявке, могут быть разделены встроенной последовательностью, кодирующей линкерный полипептид. В некоторых случаях линкер представляет собой поддающийся расщеплению линкер. В некоторых вариантах реализации интересующие полипептиды экспрессированы в виде слитых белков, связанных поддающимся расщеплению линкерным полипептидом. В некоторых вариантах реализации поддающийся(-еся) расщеплению линкерный(-е) полипептид(ы) может(-гут) представлять собой любой один или более из: F/T2A, Т2А, р2А, 2А, GSG-p2A, линкера GSG (SEQ ID NO: 85) и вариантов furinlink. В некоторых вариантах реализации линкерный полипептид содержит последовательности SEQ ID NO: 72-86 или 197-199.
[0126] В некоторых случаях можно использовать последовательность 2А из вируса. Элементы 2А могут быть короче, чем IRES, содержащие от 5 до 100 пар оснований. В некоторых случаях длина последовательности 2А может составлять 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90 или 100 нуклеотидов. Связанные с 2А гены могут экспрессироваться в одной открытой рамке считывания, и «саморасщепление» может происходить котрансляционно между двумя последними аминокислотами GP на С-конце полипептида 2А, что приводит к равным количествам совместно экспрессированных белков.
[0127] Длина последовательности 2А из вируса может составлять приблизительно 20 аминокислот. В некоторых случаях последовательность 2А из вируса может содержать консенсусный мотив Asp-Val/Ile-Glu-X-Asn-Pro-Gly-Pro (SEQ ID NO: 201). Последовательность консенсусного мотива может действовать котрансляционно. Например, можно предотвратить образование обычной пептидной связи между остатками глицина и пролина, что может привести к проскоку рибосомы и расщеплению образующегося полипептида. Данный эффект позволяет получить множество генов на эквимолярных уровнях.
[0128] Пептид 2А может позволить трансляцию множества белков в одной открытой рамке считывания с образованием полипептида, которые могут впоследствии расщепиться на отдельные полипептиды посредством механизма проскока рибосомы (Funston, Kallioinen и др. 2008). В некоторых вариантах реализации последовательность 2А может включать: F/T2A, Т2А, р2А, 2А, Т2А, Е2А, F2A и BmCPV2A, BmIFV2A и любую их комбинацию.
[0129] В некоторых случаях вектор может содержать последовательность IRES и линкерную последовательность 2А. В других случаях экспрессии множества генов, связанных с пептидами 2А, может способствовать последовательность спейсера (GSG (SEQ ID NO: 85)) перед пептидами 2А. В некоторых случаях в конструкциях могут сочетаться спейсеры, линкеры, адапторы, промоторы или их комбинации. Например, конструкция может содержать спейсер (SGSG (SEQ ID NO: 86) или GSG (SEQ ID NO: 85)) и сайт расщепления фурином линкера (R-A-K-R (SEQ ID NO: 81)) с различными пептидами 2А. Спейсер может представлять собой I-Ceui. В некоторых случаях линкер может быть сконструированным. Например, линкер может быть разработан таким образом, чтобы он обладал такими химическими свойствами, как гидрофобность. В некоторых случаях, по меньшей мере две линкерные последовательности могут образовывать один белок. В других случаях, в векторе можно использовать множество линкеров. Например, интересующие гены могут быть разделены по меньшей мере двумя линкерами.
[0130] В некоторых вариантах реализации два или более полипептидов, кодируемых полинуклеотидом, описанным в данной заявке, могут быть разделены встроенной последовательностью, кодирующей линкерный полипептид. В некоторых случаях линкер представляет собой поддающийся расщеплению линкер. В некоторых вариантах реализации интересующие полипептиды экспрессированы в виде слитых белков, связанных поддающимся расщеплению линкерным полипептидом. В некоторых вариантах реализации поддающийся(-еся) расщеплению линкерный(-е) полипептид(ы) может(-гут) представлять собой любой один или два из: Furinlink, fmdv, р2а, GSG-p2a и/или fp2a, описанных в последовательностях SEQ ID NO: 72-86 или 197-199.
[0131] В некоторых вариантах реализации линкер можно использовать в полинуклеотиде, описанном в данной заявке. Линкер может представлять собой гибкий линкер, жесткий линкер, расщепляемый in vivo линкер или любую их комбинацию. В некоторых случаях линкер может соединять друг с другом функциональные домены (как в гибких и жестких линкерах) или высвобождать свободный функциональный домен in vivo как в расщепляемых линкерах in vivo.
[0132] Линкеры могут улучшать биологическую активность, повышать выход экспрессии и способствовать достижению желательных фармакокинетических профилей. Линкер также может включать гидразон, пептид, дисульфид или сложный тиоэфир.
[0133] В некоторых случаях линкерная последовательность, описанная в данной заявке, может включать гибкий линкер. Гибкие линкеры можно применять, когда для соединенного домена требуется некоторая степень подвижности или взаимодействия. Гибкие линкеры могут состоять из малых, неполярных (например, Gly) или полярных (например, Ser или Thr) аминокислот. Гибкие линкеры могут содержать последовательности, состоящие, главным образом, из участков из остатков Gly и Ser (линкер «GS»). Примером гибкого линкера может служить последовательность (Gly-Gly-Gly-Gly-Ser)n (SEQ ID NO: 197). Регулируя число копий «п», длину данного типичного линкера GS можно оптимизировать, чтобы добиться подходящего разделения функциональных доменов, или для сохранения необходимых взаимодействий между доменами. Помимо линкеров GS, можно применять другие гибкие линкеры для рекомбинантных слитых белков. В некоторых случаях гибкие линкеры также могут быть богаты малыми или полярными аминокислотами, такими как Gly и Ser, но могут содержать аминокислоты, такие как Thr и Ala, для сохранения гибкости. В других случаях можно использовать полярные аминокислоты, такие как Lys и Glu, чтобы улучшить растворимость.
[0134] Гибкие линкеры, содержащиеся в линкерных последовательностях, описанных в данной заявке, могут быть богаты малыми или полярными аминокислотами, такими как Gly и Ser, чтобы обеспечить хорошую гибкость и растворимость. Гибкие линкеры могут быть подходящим вариантом, когда требуется некоторая подвижность или взаимодействия слитых доменов белков. Кроме того, хотя у гибких линкеров нет жестких структур, в некоторых случаях они могут служить в качестве пассивного линкера, чтобы держать на расстоянии функциональные домены. Длину гибких линкеров можно изменять, чтобы позволить правильную укладку или чтобы добиться оптимальной биологической активности слитых белков.
[0135] Линкер, описанный в данной заявке, в некоторых случаях может дополнительно включать жесткий линкер. Жесткий линкер можно применять для сохранения фиксированного расстояния между доменами полипептида. Примеры жестких линкеров могут представлять собой: образующие альфа-спираль линкеры, Pro-богатую последовательность, (ХР)n, остов Х-Pro, А(EAAAK)nA (n=2-5) (SEQ ID NO: 202), в качестве нескольких примеров. Жесткие линкеры могут иметь относительно негибкие структуры, принимая α-спиральные конформации или содержа множество остатков Pro в некоторых случаях.
[0136] Линкер, описанный в данной заявке, может быть расщепляемым в некоторых случаях. В других случаях линкер не расщепляемый. Линкеры, которые являются нерасщепляемыми, могут ковалентно соединять друг с другом функциональные домены, чтобы они действовали как одна молекула в процессах in vivo или процессе ex vivo. Линкер также может быть расщепляемым in vivo. Расщепляемый линкер можно ввести, чтобы высвободить функциональные домены in vivo. Расщепляемый линкер может быть расщеплен в присутствии восстанавливающих реагентов, протеаз, в качестве нескольких примеров. Например, для получения расщепляемого линкера можно использовать восстановление дисульфидной связи. В случае дисульфидного линкера, акт расщепления может происходить посредством дисульфидного обмена с тиолом, таким как глутатион. В других случаях расщепление линкера in vivo в рекомбинантном слитом белке также можно осуществить с помощью протеаз, которые могут экспрессироваться in vivo при патологических состояниях (например, раке или воспалении), в специфичных клетках или тканях или ограниченно внутри некоторых компартментов клетки. В некоторых случаях расщепляемый линкер может позволить направленное расщепление. Например, специфичность множества протеаз может привести к более медленному расщеплению линкера в ограниченных компартментах. Расщепляемый линкер также может включать гидразон, пептиды, дисульфид или сложный тиоэфир. Например, гидразон может придать стабильность в сыворотке. В других случаях гидразон может позволить расщепление в кислом компартменте. рН кислого компартмента может составлять до 7. Линкер также может включать тиоэфир. Тиоэфир может быть невосстанавливаемым. Тиоэфир может быть разработан для внутриклеточной протеолитической деградации.
[0137] В некоторых вариантах реализации линкерный полипептид fmdv содержит последовательность, которая может быть по меньшей мере приблизительно на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентична последовательности SEQ ID NO: 82. В некоторых вариантах реализации линкерный полипептид fmdv представляет собой один или более линкеров, кодируемых в одном векторе, соединяющих два или более слитых белков. В некоторых случаях линкерный полипептид fmdv может кодироваться последовательностью нуклеиновой кислоты открытой рамки считывания (ОРС) полинуклеотида. В некоторых случаях ОРС, кодирующая fmdv, включает или состоит из последовательности SEQ ID NO: 173. В некоторых вариантах реализации полинуклеотид, кодирующий fmdv, по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 173.
[0138] В некоторых случаях линкерный полипептид может представлять собой линкер «р2а». В некоторых вариантах реализации полипептид р2А может содержать последовательность, которая может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентична последовательности SEQ ID NO: 75. В некоторых вариантах реализации линкерный полипептид р2А может представлять собой один или более линкеров, кодируемых в одном векторе, соединяющем два или более слитых белков. В некоторых случаях линкерный полипептид р2А может кодироваться последовательностью нуклеиновой кислоты открытой рамки считывания (ОРС) полинуклеотида. В некоторых вариантах реализации ОРС, кодирующая р2а, включает или состоит из последовательности, представленной в SEQ ID NO: 167. В некоторых случаях полинуклеотид, кодирующий р2а, может быть или может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 167.
[0139] В некоторых случаях линкерный полипептид может представлять собой линкер «GSG-p2a». В некоторых вариантах реализации линкерный полипептид GSG-p2A может содержать последовательность, которая может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентична последовательности SEQ ID NO: 76. В некоторых вариантах реализации линкерный полипептид GSG-p2A может представлять собой один или более линкеров, кодируемых в одном векторе, соединяющем два или более слитых белков. В некоторых случаях линкерный полипептид GSG-p2A может кодироваться последовательностью нуклеиновой кислоты открытой рамки считывания (ОРС) полинуклеотида. ОРС, кодирующая GSG р2а, может содержать последовательность, представленную в SEQ ID NO: 168. В некоторых случаях полинуклеотид, кодирующий GSG-p2a, может быть или может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 168.
[0140] Линкерный полипептид может представлять собой линкер «fp2a», предложенный в данной заявке. В некоторых вариантах реализации линкерный полипептид fp2a может содержать последовательность, которая может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентична последовательности SEQ ID NO: 77. В некоторых случаях, линкерный полипептид fp2a может представлять собой один или более линкеров, кодируемых в одном векторе, соединяющем два или более слитых белков. В некоторых случаях, линкерный полипептид fp2a может кодироваться последовательностью нуклеиновой кислоты открытой рамки считывания (ОРС) полинуклеотида. В некоторых вариантах реализации полинуклеотид, кодирующий линкер fp2a, может быть или может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 169.
[0141] В некоторых случаях линкер может быть сконструированным. Например, линкер может быть разработан таким образом, чтобы он обладал такими химическими свойствами как гидрофобность. В некоторых случаях по меньшей мере две линкерные последовательности могут позволить получить один и тот же белок. Последовательность может быть или может быть приблизительно на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или 100% идентична последовательности, представленной в SEQ ID NO: 72 - SEQ ID NO: 86 или SEQ ID NO: 197 - SEQ ID NO: 199. В других случаях в векторе можно использовать множество линкеров. Например, полипептидные последовательности интересующих генов и одного или более переключателей генов, описанных в данной заявке, могут быть разделены по меньшей мере двумя линкерами. В некоторых случаях гены могут быть разделены 2, 3, 4, 5, 6, 7, 8, 9 или до 10 линкерами.
[0142] Линкер может представлять собой сконструированный линкер. Способы разработки линкеров могут быть вычислительными. В некоторых случаях, вычислительные способы могут включать графические методики. Вычислительные способы можно применять для поиска подходящих пептидов в библиотеках трехмерных пептидных структур, полученных из баз данных. Например, банк данных белков Brookhaven Protein Data Bank (PDB) можно использовать для измерения расстояния в пространстве между выбранными аминокислотами линкера.
[0143] В некоторых вариантах реализации предложены полинуклеотиды, кодирующие полипептидную конструкцию, содержащую полипептид фурина и полипептид 2А, причем указанные полипептид фурина и полипептид 2А соединены полипептидным линкером, содержащим по меньшей мере три гидрофобные аминокислоты. В некоторых случаях по меньшей мере три гидрофобные аминокислоты выбраны из перечня, состоящего из глицина (Gly, G), аланина (Ala, А), валина (Val, V), лейцина (Leu, L), изолейцина (Ile, I), пролина (Pro, Р), фенилаланина (Phe, F), метионина (Met, М), триптофана (Trp, W). В некоторых случаях полипептидный линкер также может содержать одну или более последовательностей GS-линкера, например, (GS)n (SEQ ID NO: 203), (SG)n (SEQ ID NO: 204), (GSG)n (SEQ ID NO: 198) и (SGSG)n (SEQ ID NO: 199), где n может представлять собой любое число от нуля до пятнадцати.
[0144] Предложены способы получения улучшенной экспрессии полипептидной конструкции, включающие: предоставление полинуклеотида, кодирующего указанную полипептидную конструкцию, содержащую первый функциональный полипептид и второй функциональный полипептид, причем указанные первый функциональный полипептид и второй функциональный полипептид соединены линкерным полипептидом, содержащим последовательность, по меньшей мере на 60% идентичную последовательности APVKQ (SEQ ID NO: 205); и экспрессию указанного полинуклеотида в клетке-хозяине, причем указанная экспрессия приводит к улучшенной экспрессии полипептидной конструкции по сравнению с соответствующей полипептидной конструкцией, которая не содержит линкерный полипептид, содержащий последовательность, по меньшей мере на 60% идентичную последовательности APVKQ (SEQ ID NO: 205).
[0145] В других случаях линкер может представлять собой IRES. Термин «внутренний участок посадки рибосомы (IRES)» в данной заявке может быть предназначен для обозначения внутреннего участка посадки рибосомы. В векторе, содержащем последовательность IRES, первый ген может быть транслирован зависимым от кэпирования механизмом сканирования рибосомой с собственной 5'-НТО, тогда как трансляция последующего гена может осуществляться непосредственным привлечением рибосомы на IRES независимым от кэпирования образом. Последовательность IRES может позволить эукариотическим рибосомам связаться и начать трансляцию без связывания с 5'-кэпированным концом. Последовательность IRES может позволить экспрессию множества генов с одного транскрипта (Mountford и Smith 1995).
[00192] Примеры последовательностей IRES можно найти в SEQ ID NO: 192 и 193. В некоторых случаях полинуклеотид, кодирующий IRES 2xRbm3, может быть или может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 192. В некоторых случаях полинуклеотид, кодирующий IRES EMCV, может быть или может быть приблизительно по меньшей мере на 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% или 100% идентичен последовательности SEQ ID NO: 193.
[00193] В некоторых вариантах реализации предложены системы модуляции экспрессии CAR и цитокина в клетке-хозяине, содержащие первую кассету экспрессии генов, содержащую первый полинуклеотид, кодирующий первый полипептид; вторую кассету экспрессии генов, содержащую второй полинуклеотид, кодирующий второй полипептид; и лиганд; причем указанные первый и второй полипептиды содержат один или более из: (i) трансактивирующего домена; (ii) ДНК-связывающего домена; и (iii) лиганд-связывающего домена; (iv) CAR; (vi) цитокина и/или (vii) метки клетки, так что при приведении в контакт клетки-хозяина с первой кассетой экспрессии генов и второй кассетой экспрессии генов в присутствии лиганда, CAR и цитокин экспрессируются в клетке-хозяине. В некоторых случаях CAR представляет собой MUC16-CAR и цитокин представляет собой mbIL-15. В некоторых случаях MUC16-CAR, mbIL-15 совместно экспрессируются с одной меткой клетки. В некоторых случаях каждый из MUC16-CAR и mbIL-15 совместно экспрессируется с меткой клетки. В других случаях MUC16-CAR экспрессируется с меткой клетки и mbIL-15 экспрессируется со второй меткой клетки. Примеры конфигураций кассет экспрессии генов изображены на Фиг. 1 и 2. В других случаях CAR представляет собой MUC16-CAR и цитокин представляет собой IL-12. В некоторых случаях MUC16CAR, IL-12 совместно экспрессируются с одной меткой клетки. В некоторых случаях каждый из MUC16-CAR и IL-12 совместно экспрессируется с меткой клетки. В других случаях MUC16-CAR экспрессируется с меткой клетки и IL-12 экспрессируется со второй меткой клетки.
[00194] В некоторых вариантах реализации предложены системы модуляции экспрессии CAR и цитокина в клетке-хозяине, содержащие первую кассету экспрессии генов, содержащую первый полинуклеотид, кодирующий первый полипептид; вторую кассету экспрессии генов, содержащую второй полинуклеотид, кодирующий второй полипептид; и лиганд; причем указанный первый полипептид содержит один или более из: (i) трансактивирующего домена; (ii) ДНК-связывающего домена; и (iii) лиганд-связывающего домена и второй полипептид содержит один или более из: (i) CAR; (ii) цитокина и/или (iii) метки клетки, так что при приведении в контакт клетки-хозяина с первой кассетой экспрессии генов и второй кассетой экспрессии генов в присутствии лиганда, CAR и/или цитокин экспрессируются в клетке-хозяине. В некоторых случаях CAR представляет собой MUC16-CAR и цитокин представляет собой mbIL-15. В некоторых случаях каждый из MUC16-CAR и mbIL-15 совместно экспрессируются с меткой клетки. В других случаях MUC16-CAR экспрессируется с первой меткой клетки и mbIL-15 экспрессируется со второй меткой клетки.
[00195] Примеры конфигураций систем модуляции экспрессии MUC16-CAR и цитокина в клетке-хозяине изображены на Фиг. 1-2. В некоторых вариантах реализации кассеты экспрессии генов внедряют в эффекторную иммунную клетку, применяя вирусные системы или системы на основе вирусов. Примеры не основанных на вирусах систем доставки, описанных в данной заявке, включают систему транспозона SB11, систему транспозона SB100X, систему транспозона SB110, систему транспозона piggyBac. В одном варианте реализации кассеты экспрессии генов внедряют в эффекторную иммунную клетку в одном или более транспозонах Спящая красавица.
[00196] Примеры вариантов реализации кассет экспрессии генов, которые кодируют конститутивную экспрессию MUC16-CAR, цитокина (такого как mbIL-15 или IL-12) и метки клетки, изображены на Фиг. 1. На Фиг. 1a-b изображены примеры дизайнов кассеты экспрессии генов для MUC16-CAR, mbIL-15 и метки клетки в различных конфигурациях. В данном варианте реализации кассету экспрессии генов внедряют в эффекторную иммунную клетку в одном транспозоне Спящая красавица. На Фиг. 1с-d изображены конфигурации кассеты экспрессии генов, в которых MUC16-CAR может находиться в одной кассете экспрессии генов, a mbIL-15 и метка клетки могут находиться во второй кассете экспрессии генов. В данном варианте реализации кассету экспрессии генов внедряют в эффекторную иммунную клетку в одном или более транспозонах Спящая красавица.
[00197] Примеры вариантов реализации кассет экспрессии генов, которые кодируют индуцируемую экспрессию MUC16-CAR, цитокина (такого как mbIL-15) и/или метки клетки, изображены на Фиг. 2. На Фиг. 2а-d изображены примеры дизайнов кассеты экспрессии генов для MUC16-CAR, mbIL-15 и метки клетки в различных конфигурациях под контролем индуцируемого промотора. На Фиг. 2е представлен типичный вариант реализации кассеты экспрессии генов, кодирующей полипептиды переключателя генов, описанные в данной заявке. В данном варианте реализации кассету(-ы) экспрессии генов внедряют в эффекторную иммунную клетку в одном или более транспозонах Спящая красавица.
Лиганды
[00198] В некоторых вариантах реализации лиганд, используемый для индуцируемой регуляции переключения генов, можно выбрать из любого, но не ограниченного перечисленными, лиганда: N-[(1R)-1-(1,1-диметилэтил)бутил]-N'-(2-этил-3-метоксибензоил)-3,5-диметилбензогидразид (также называемый веледимекс), (2S,3R,5R,9R,10R,13R,14S,17R)-17-[(2S,3R)-3,6-дигидрокси-6-метилгептан-2-ил]-2,3,14-тригидрокси-10,13-диметил-2,3,4,5,9,11,12,15,16,17-декагидро-1H-циклопента[а]фенантрен-6-он; N'-(3,5-диметилбензоил)-N'-[(3R)-2,2-диметил-3-гексанил]-2-этил-3-метоксибензогидразид; 5-метил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(3,5-диметилбензоил)-N-(1-этил-2,2-диметилпропил)гидразид; 5-метил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(3,5-диметокси-4-метилбензоил)-N'-(1-этил-2,2-диметилпропил)гидразид; 5-метил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N-(1-трет-бутилбутил)-N-(3,5-диметилбензоил)гидразид; 5-метил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(1-трет-бутилбутил)-N'-(3,5-диметокси-4-метилбензоил)гидразид; 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(3,5-диметилбензоил)-N'-(1-этил-2,2-диметилпропил)гидразид; 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(3,5-диметокси-4-метилбензоил)-N'-(1-этил-2,2-диметилпропил)гидразид; 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N-(1-трет-бутилбутил)-N-(3,5-диметилбензоил)гидразид; 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты N'-(1-трет-бутилбутил)-N'-(3,5-диметокси-4-метилбензоил)гидразид; 3,5-диметилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N-(3-метокси-2-метилбензоил)гидразид; 3,5-диметокси-4-метилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N-(3-метокси-2-метилбензоил)гидразид; 3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(3-метокси-2-метилбензоил)гидразид; 3,5-диметокси-4-метилбензойной кислоты N-(1-трет-бутилбутил)-N'-(3-метокси-2-метилбензоил)гидразид; 3,5-диметилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N-(2-этил-3-метоксибензоил)гидразид; 3,5-диметокси-4-метилбензойной кислоты N-(1-этил-2,2-диметилпропил)-N'-(2-этил-3-метоксибензоил)гидразид; 3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид; 3,5-диметокси-4-метилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид; 2-метоксиникотиновой кислоты N-(1-трет-бутилпентил)-N'-(4-этилбензоил)гидразид; 3,5-диметилбензойной кислоты N-(2,2-диметил-1-фенилпропил)-N'-(4-этилбензоил)гидразид; 3,5-диметилбензойной кислоты N-(1-трет-бутилпентил)-Н'-(3-метокси-2-метилбензоил)гидразид; и 3,5-диметокси-4-метилбензойной кислоты N-(1-трет-бутилпентил)-N'-(3-метокси-2-метилбензоил)гидразид.
[00199] В некоторых случаях лиганд, используемый для регулируемого дозой контроля индуцируемого переключателя генов на основе рецептора экдизона, можно выбрать из любого, не ограничиваясь перечисленными, из: экдистероида, такого как экдизон, 20-гидроксиэкдизона, понастерона А, муристерона А и тому подобных, 9-цис-ретиноевой кислоты, синтетических аналогов ретиноевой кислоты, М,N'-диацилгидразинов, таких как описанные в патентах США №6,013,836; 5,117,057; 5,530,028 и 5,378,726 и публикациях заявок на патент США №2005/0209283 и 2006/0020146; оксадиазолинов, описанных в публикации заявки на патент США №2004/0171651; дибензоилалкилцианогидразинов, таких как описанные в Европейской заявке на патент №461,809; N-алкил-N,N'-диароилгидразинов, таких как описанные в патенте США №5,225,443; N-ацил-N-алкилкарбонилгидразинов, таких как описанные в Европейской заявке на патент №234,994; N-ароил-N-алкил-N'-ароилгидразинов, таких как описанные в патенте США №4,985,461; арнидокетонов, таких как описанные в публикации заявки на патент США № 2004/0049037; каждая из которых включена в данную заявку посредством ссылки, и в других сходных материалах, включая 3,5-ди-трет-бутил-4-гидрокси-N-изобутилбензамид, 8-О-ацетилхарпагид, оксистеролы, 22(R)-гидроксихолестерин, 24(S)-гидроксихолестерин, 25-эпоксихолестерин, Т0901317, 5-альфа-6-альфа-эпоксихолестерин-3-сульфат (ECHS), 7-кетохолестерин-3-сульфат, фарнезол, желчные кислоты, эфиры 1,1-бифосфоната, ювенильный гормон III и тому подобные. Примеры диацилгидразиновых лигандов, пригодных в настоящем изобретении, включают RG-115819 (3,5-диметилбензойной кислоты К-(1-этил-2,2-диметилпропил)-Н'-(2-метил-3-метоксибензоил)гидразид), RG-115932 ((11)-3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид) и RG-115830 (3,5-диметилбензойной кислоты N-(1-трет-бутилбутил)-N'-(2-этил-3-метоксибензоил)гидразид). См., например, заявку на патент США №12/155,111 и заявку РСТ №PCT/US2008/006757, обе из которых полностью включены в данную заявку посредством ссылки.
Не основанные на вирусах системы доставки
[00200] Нуклеиновую кислоту, кодирующую CAR, описанный в настоящем изобретении, также можно внедрить в эффекторные иммунные клетки, применяя не основанные на вирусах системы доставки, такие как «система транспозонов Спящая красавица (SB)», которая относится к синтетической системе транспозонов ДНК для внедрения последовательностей ДНК в хромосомы позвоночных. Типичная система транспозона SB описана, например, в патентах США №6,489,458 и 8,227,432, и показана на Фиг. 3. Система транспозонов Спящая красавица содержит транспозазу Спящая красавица (SB) и транспозон(ы) SB. В данной заявке система транспозонов Спящая красавица может включать полипептиды транспозазы Спящая красавица, а также производные, варианты и/или фрагменты, которые сохраняют активность, и полинуклеотиды транспозона Спящая красавица, производные, варианты и/или фрагменты, которые сохраняют активность. В некоторых вариантах реализации транспозаза Спящая красавица предложена в виде мРНК. В некоторых аспектах мРНК кодирует транспозазу SB10, SB11, SB100x или SB110. В некоторых аспектах мРНК содержит кэп и поли(А)-хвост.
[00201] Транспозоны ДНК транслоцируются из одного сайта ДНК в другой простым способом копирования/вставки. Транспозиция представляет собой точный процесс, в котором определенный фрагмент ДНК вырезают из одной молекулы ДНК и перемещают в другой сайт в той же или отличной молекуле ДНК или геноме. Как и с другими транспозазами Tc1/типа маринер, транспозаза SB встраивает транспозон в динуклеотидную пару оснований ТА в реципиентной последовательности ДНК. Сайт встраивания может быть в любом месте в той же молекуле ДНК или в другой молекуле ДНК (или хромосоме). В геномах млекопитающих, включая людей, присутствует приблизительно 200 миллионов сайтов ТА. Сайт встраивания ТА дуплицируется в процессе встраивания транспозона. Такая дупликация последовательности ТА является отличительным признаком транспозиции и используются для установления механизма в некоторых экспериментах. Транспозаза может либо кодироваться транспозоном, либо транспозаза может быть предоставлена другим источником, в последнем случае транспозон становится неавтономным элементом. Неавтономные транспозоны наиболее пригодны в качестве генетических инструментов, так как после встраивания они не могут независимо продолжать вырезать и снова вставлять. Транспозоны SB предусмотрены для применения в качестве невирусных векторов для внедрения генов в геномы позвоночных животных и для генотерапии. Вкратце, систему Спящая красавица (SB) (Hackett и др., Mol Ther 18:674-83, (2010)) приспособили для генетической модификации эффекторных иммунных клеток (Cooper и др., Blood 105:1622-31, (2005)). В одном варианте реализации это включало два этапа: (i) электроперенос плазмид ДНК, экспрессирующих транспозон SB (т.е., химерный антигенный рецептор (CAR), чтобы перенаправлять специфичность Т-клеток (Jin и др., Gene Ther 18:849-56, (2011); Kebriaei и др., Hum Gene Ther 23:444-50, (2012)) и транспозазу SB, и (ii) размножение и распространение Т-клеток, стабильно экспрессирующих встроенные элементы на сконструированных искусственных антигенпрезентирующих клетках (АаРС), полученных из линии клеток К562 (также известных как АаРС (активирующие и размножающие клетки). В другом варианте реализации второй этап (ii) опускают и генетически модифицированные Т-клетки криоконсервируют или незамедлительно вводят путем инфузии пациенту. [00202] В одном варианте реализации системы транспозона SB описаны, например, в Hudecek и др., Critical Reviews in Biochemistry and Molecular Biology, 52:4, 355-380 (2017), Singh и др., Cancer Res (8):68 (2008). 15 апреля 2008 г. и Maiti и др., J Immunother. 36(2): 112 123 (2013), полностью включенном в данную заявку посредством ссылки. [00203] В некоторых вариантах реализации MUC16-С AR и mbIL-15 кодируются в векторе плазмидной ДНК транспозона, а транспозаза SB кодируется в отдельном векторе. В некоторых вариантах реализации MUC16-CAR, описанный в данной заявке, кодируется в векторе плазмидной ДНК транспозона, mb-IL15 кодируется во втором векторе плазмидной ДНК транспозона, а транспозаза SB кодируется в третьем векторе плазмидной ДНК. В некотором варианте реализации CAR кодируется с меткой уничтожения, например, HER1t, HER1t1, CD20 или CD20t-1. В некоторых вариантах реализации mbIL-15 кодируется с меткой уничтожения, например, HER1t, HER1t1, CD20 или CD20t-1.
[00204] В вариантах реализации MUC16-CAR можно совместно экспрессировать с mblL-15 и меткой клетки из вектора плазмидной ДНК транспозона. В дополнительных вариантах реализации MUC16-CAR может находиться под контролем индуцируемого промотора. В другом варианте реализации mbIL-15 может находиться под контролем индуцируемого промотора. В одном аспекте индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®. В некоторых вариантах реализации MUC16-CAR, mbIL-15 и метку уничтожения можно сконфигурировать в одном, двух или более транспозонах. Примеры конфигураций MUC16-CAR или mbIL15 под контролем индуцируемого промотора изображены на Фиг. 2.
[00205] В вариантах реализации MUC16-CAR и другие генетические элементы доставляют в клетку, применяя систему транспозона SB11, систему транспозона SB100X, систему транспозона SB110, систему транспозона piggyBac (см., например, патентСША№9,228,180, Wilson и др., «PiggyBac Transposon-mediated Gene Transfer in Human Cells», Molecular Therapy 15:139-145 (2007), полностью включены в данную заявку посредством ссылки) и/или систему транспозона piggyBat (см., например, Mitra и др., «Functional characterization of piggyBat from the bat Myotis lucifugus unveils an active mammalian DNA transposon», Proc. Natl. Acad. Sci USA 110:234-239 (2013). Дополнительные транспозазы и системы транспозонов предложены в патентах США №7,148,203; 8,227,432; публикации заявки на патент США №2011/0117072; Mates и др., Nat Genet, 41(6):753-61 (2009). doi: 10.1038/ng.343. Epub, 3 мая 2009, Gene Ther., 18(9):849-56 (2011). doi: 10.1038/gt.2011.40. Epub, 31 марта 2011 и in Ivicsnflp., Cell. 91(4):501-10, (1997), каждый из которых полностью включен в данную заявку посредством ссылки.
[00206] В других вариантах реализации MUC16-CAR и другие генетические элементы, такие как цитокины, mbIL-15 и/или метка HER1t/HER1t1/CD20/CD20t-l, можно встроить в ДНК иммунной эффекторной клетки посредством рекомбиназы и встраивания векторов экспрессии. Такие векторы могут произвольно встраиваться в ДНК клетки-хозяина или могут содержать сайт рекомбинации, чтобы позволить специфичную рекомбинацию между вектором экспрессии и хромосомой клетки-хозяина. В таких встраивающихся векторах экспрессии можно использовать эндогенные контролирующие экспрессию последовательности хромосом клетки-хозяина, чтобы влиять на экспрессию желательного белка. В некоторых вариантах реализации направленное встраивание вызывается присутствием последовательностей на донорном полинуклеотиде, которые гомологичны последовательностям, фланкирующим сайт встраивания. Например, направленного встраивания с применением донорных полинуклеотидов, описанных в данной заявке, можно добиться, следуя обычным методикам трансфекции, например, методикам, применяемым для создания нокаутов или нокинов генов путем гомологичной рекомбинации. В других вариантах реализации направленное встраивание вызывается как присутствием последовательностей на донорном полинуклеотиде, которые гомологичны последовательностям, фланкирующим сайт встраивания, так и приведением в контакт клеток с донорным полинуклеотидом в присутствии сайт-специфичной рекомбиназы. Под сайт-специфичной рекомбиназой, или просто рекомбиназой, подразумевают полипептид, который катализирует консервативную сайт-специфичную рекомбинацию между совместимыми с ним сайтами рекомбинации. В данной заявке сайт-специфичная рекомбиназа включает нативные полипептиды, а также их производные, варианты и/или фрагменты, которые сохраняют активность, и нативные полинуклеотиды, производные, варианты и/или фрагменты, которые кодируют рекомбиназу, которая сохраняет активность.
[00207] Указанные рекомбиназы можно ввести в целевую клетку до, одновременно или после введения нацеливающего вектора. Рекомбиназу можно непосредственно ввести в клетку в виде белка, например, применяя липосомы, покрытые частицы или микроинъекцию. В качестве альтернативы, полинуклеотид, либо ДНК, либо информационную РНК, кодирующую рекомбиназу, можно ввести в клетку, применяя подходящий вектор экспрессии. Компоненты нацеливающего вектора, описанные выше, пригодны для конструирования кассет экспрессии, содержащих последовательности, кодирующие интересующую рекомбиназу. Тем не менее, экспрессию рекомбиназы можно регулировать другими способами, например, поместив экспрессию рекомбиназы под контроль регулируемого промотора (т.е., промотора, экспрессию с которого можно селективно индуцировать или репрессировать).
[00208] Рекомбиназа может быть из семейства интеграз или резолваз. В семейство рекомбиназ интеграз входит более ста представителей, и они включают, например, FLP, Cre и лямбда-интегразу. Семейство интеграз, также называемое семейством тирозиновых рекомбиназ или семейством лямбда-интеграз, использует каталитическую гидроксильную группу тирозина для нуклеофильной атаки на фосфодиэфирную связь ДНК. Обычно, представители семейства тирозиновых рекомбиназ изначально делают одноцепочечный разрыв (ник) на ДНК, из которого позже образуется двухцепочечный разрыв. Примеры интеграз из семейства тирозиновых рекомбиназ включают Cre, FLP, SSV1 и лямбда (X)-интегразу. В семействе резолваз, также известном как семейство сериновых рекомбиназ, консервативный остаток серина образует ковалентную связь с целевым сайтом ДНК (Grindley, и др., (2006) Ann Rev Biochem 16:16).
[00209] В одном варианте реализации рекомбиназа представляет собой выделенную полинуклеотидную последовательность, содержащую последовательность нуклеиновой кислоты, которая кодирует рекомбиназу, выбранную из группы, состоящей из рекомбиназы SPβc2, рекомбиназы SF370.1, рекомбиназы Bxb1, рекомбиназы А118 и рекомбиназы φRv1. Примеры сериновых рекомбиназ подробно описаны в патенте США №9,034,652, который настоящим полностью включен в данную заявку посредством ссылки.
[00210] Рекомбиназы для применения для осуществления настоящего изобретения можно получить рекомбинантно или очистить, как описано ранее. Полипептиды, обладающие желательной рекомбиназной активностью, можно очистить до желательной степени чистоты с помощью способов, известных в данной области, таких как преципитация белка сульфатом аммония, очистка, включая, но не ограничиваясь фракционированием по размеру, аффинной хроматографией, ВЭЖХ, ионообменной хроматографией, аффинной хроматографией на гепарин-агарозе (например, Thorpe & Smith, Proc. Nat. Acad. Sci. 95:5505-5510, 1998).
[00211] В одном варианте реализации рекомбиназы можно внедрить в эукариотические клетки, которые содержат сайты присоединения рекомбиназ, в которых необходимо осуществить рекомбинацию с помощью любого подходящего способа. Способы внедрения функциональных белков в клетки, например, с помощью микроинъекции или других способов, хорошо известны в данной области. Внедрение очищенного белка рекомбиназы гарантирует временное присутствие белка и его функции, что часто является предпочтительным вариантом реализации. В качестве альтернативы, ген, кодирующий рекомбиназу, можно встроить в вектор экспрессии, применяемый для трансформации клетки, в котором кодирующий рекомбиназу полинуклеотид функционально связан с промотором, который опосредует экспрессию полинуклеотид а в эукариотической клетке. Полипептид рекомбиназы также можно внедрить в эукариотическую клетку с помощью информационной РНК, которая кодирует полипептид рекомбиназы. Как правило, предпочтительно, чтобы рекомбиназа присутствовала в течение лишь такого времени, которое необходимо для встраивания фрагментов нуклеиновых кислот в геном, который модифицируют. Следовательно, не ожидается, что отсутствие стабильности, присущее большинству векторов экспрессии, будет оказывать негативное влияние. Можно ввести ген рекомбиназы в клетку до, после или одновременно с внедрением интересующего экзогенного полинуклеотида. В одном варианте реализации ген рекомбиназы присутствует внутри вектора, который несет полинуклеотид, который необходимо встроить; ген рекомбиназы может даже содержаться внутри указанного полинуклеотида.
[00212] В одном варианте реализации способ сайт-специфичной рекомбинации включает предоставление первого сайта рекомбинации и второго сайта рекомбинации; приведение в контакт первого и второго сайтов рекомбинации с полипептидом прокариотической рекомбиназы, что приводит к рекомбинации между сайтами рекомбинации, причем полипептид рекомбиназы может опосредовать рекомбинацию между первым и вторым сайтами рекомбинации, уазанный первый сайт рекомбинации представляет собой attP или attB, второй сайт рекомбинации представляет собой attB или attP, и рекомбиназа выбрана из группы, состоящей из рекомбиназы фага Listeria monocytogenes, рекомбиназы фага Streptococcus pyogenes, рекомбиназы фага Bacillus subtilis, рекомбиназы фага Mycobacterium tuberculosis и рекомбиназы фага Mycobacterium smegmatis, при этом если первый сайт присоединения рекомбиназ представляет собой attB, то второй сайт присоединения рекомбиназ представляет собой attP, и если первый сайт присоединения рекомбиназ представляет собой attP, то второй сайт присоединения рекомбиназ представляет собой attB.
[00213] В дополнительных вариантах реализации предложено внедрение сайт-специфичной рекомбиназы в клетку, геном которой нужно модифицировать. В одном варианте реализации предложен способ осуществления сайт-специфичной рекомбинации в эукариотической клетке, включающий предоставление эукариотической клетки, которая содержит первый сайт присоединения рекомбиназ и второй сайт присоединения рекомбиназ; приведение в контакт первого и второго сайтов присоединения рекомбиназ с полипептидом прокариотической рекомбиназы, что приводит к рекомбинации между сайтами присоединения рекомбиназ, причем полипептид рекомбиназы может опосредовать рекомбинацию между первым и вторым сайтами присоединения рекомбиназ, указанный первый сайт присоединения рекомбиназ представляет собой сайт присоединения рекомбиназ (attP) генома фага или сайт присоединения рекомбиназ (attB) генома бактерий, второй сайт присоединения рекомбиназ представляет собой attB или attP, и рекомбиназа выбрана из группы, состоящей из рекомбиназы фага Listeria monocytogenes, рекомбиназы фага Streptococcus pyogenes, рекомбиназы фага Bacillus subtilis, рекомбиназы фага Mycobacterium tuberculosis и рекомбиназы фага Mycobacterium smegmatis, при этом если первый сайт присоединения рекомбиназ представляет собой attB, то второй сайт присоединения рекомбиназ представляет собой attP, и если первый сайт присоединения рекомбиназ представляет собой attP, то второй сайт присоединения рекомбиназ представляет собой attB. В варианте реализации рекомбиназа выбрана из группы, состоящей из рекомбиназы А118, рекомбиназы SF370.1, рекомбиназы SPβc2, рекомбиназы φRv1 и рекомбиназы Bxb1. В одном варианте реализации рекомбинация приводит к встраиванию.
[00214] Независимо от способа, применяемого для внедрения экзогенных нуклеиновых кислот в клетку-хозяина, для того чтобы подтвердить присутствие рекомбинантной последовательности ДНК в клетке-хозяине, можно провести различные анализы. Такие анализы включают, например, «молекулярно-биологические» анализы, хорошо известные специалистам в данной области, такие как саузерн- и нозерн-блоттинг, ОТ-ПЦР и ПЦР; «биохимические» анализы, такие как обнаружение присутствия или отсутствия определенного пептида, например, с помощью иммунологических способов (ELISA и вестерн-блотов) или с помощью анализов, описанных в данной заявке, для идентификации пептидов, или белков, или нуклеиновых кислот, входящих в объем настоящего изобретения.
Системы доставки на основе вирусов.
[00215] Также в данной заявке предложены системы доставки на основе вирусов, в которые встроена нуклеиновая кислота согласно настоящему изобретению. Примеры вирусных векторов экспрессии включают, но не ограничены перечисленными: векторы на основе аденовируса (например, систему на основе аденовируса Per.С6, доступную от Crucell, Inc. (Лейден, Нидерланды)), векторы на основе лентивируса (например, на основе лентивируса pLPI от Life Technologies (Карлсбад, Калифорния)) и ретровирусные векторы (например, pFB-ERV плюс pCFB-EGSH), вирусы герпеса. В варианте реализации вирусный вектор представляет собой лентивирусный вектор. Векторы, происходящие из ретровирусов, таких как лентивирус, являются подходящими инструментами, чтобы добиться долгосрочного переноса генов, поскольку они позволяют длительное стабильное встраивание трансгена и его воспроизводство в дочерних клетках. Лентивирусные векторы обладают дополнительным преимуществом над векторами, происходящими из онкоретровирусов, таких как вирусы лейкоза мыши, состоящим в том, что они могут трансдуцировать непролиферирующие клетки, такие как гепатоциты. Они также могут обладать дополнительным преимуществом низкой иммуногенности. Вообще и в вариантах реализации подходящий вектор содержит точку начала репликации, функциональную в по меньшей мере одном организме, последовательность промотора, удобные сайты рестрикции эндонуклеазами и один или более селектируемых маркеров, (например, WO 01/96584; WO 01/29058 и патент США №6,326,193).
[00216] В вариантах реализации предложен лентивирусный вектор, содержащий остов и последовательность нуклеиновой кислоты, кодирующую химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; (е) сигнальный домен CD3-дзета. Необязательно вектор дополнительно содержит нуклеиновую кислоту, кодирующую укороченный рецептор эпидермального фактора роста (HER1t или HER1t1), CD20t-1 или полноразмерный CD20. [00217] В некоторых случаях предложен вектор, содержащий остов и последовательность нуклеиновой кислоты, кодирующую (1) укороченный рецептор эпидермального фактора роста например, HER1t или HERt-1 или его функциональный вариант; и (2) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета. [00218] В некоторых случаях предложен вектор, содержащий остов и последовательность нуклеиновой кислоты, кодирующую (1) полноразмерный CD20, укороченный CD20 или его функциональные варианты, и (2) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета.
[00219] В вариантах реализации нуклеиновая кислота, кодирующая специфичный к MUC16 CAR, клонирована в вектор, содержащий компоненты лентивирусного остова. Типичные компоненты остова включают, но не ограничены pFUGW и pSMPUW. Остов лентивирусного вектора pFUGW представляет собой самоинактивирующийся (SIN) остов лентивирусного вектора, и из него удалены ненужные последовательности вируса ВИЧ-1, что приводит к меньшей вероятности развития неоплазии, вредных мутаций и регенерирования инфекционных частиц. В вариантах реализации вектор, кодирующий MUC16-CAR, также кодирует mbIL-15 в единой конструкции. В вариантах реализации MUC16-CAR и mbIL-15 кодируются двумя отдельными лентивирусными векторами. В некоторых вариантах реализации mbIL-15 экспрессируется с укороченной меткой рецептора эпидермального фактора роста. В вариантах реализации MUC16-CAR может совместно экспрессироваться с mbIL-15 и меткой клетки с единого лентивирусного вектора. В дополнительных вариантах реализации MUC16-CAR может находиться под контролем индуцируемого промотора. В другом варианте реализации mbIL-15 может находиться под контролем индуцируемого промотора. В одном аспекте индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®.
[00220] В одном варианте реализации MUC16-CAR, описанный в данной заявке, содержит scFv против MUC16, шарнирный и трансмембранный домен CD8 человека и сигнальные домены 4-1 ВВ человека и CD3-дзета. В другом варианте реализации MUC16-CAR согласно настоящему изобретению содержит scFv против MUC16, шарнирный и трансмембранный домен CD8 человека, сигнальные домены 4-1 ВВ человека и CD3-дзета и необязательно метку укороченного рецептора эпидермального фактора роста (HER1t или HER1t-1). Другие подходящие векторы включают встраивающиеся векторы экспрессии, которые могут произвольно встраиваться в ДНК клетки-хозяина или могут содержать сайт рекомбинации, чтобы позволить специфичную рекомбинацию между вектором экспрессии и хромосомой клетки-хозяина. В таких встраивающихся векторах экспрессии могут использоваться эндогенные контролирующие экспрессию последовательности хромосом клетки-хозяина, которые влияют на экспрессию желательного белка. Примеры векторов, которые встраиваются сайт-специфичным образом, включают, например, компоненты системы Flp-In от Invitrogen (Карлсбад, Калифорния) (например, pcDNA™5/FRT) или системы cre-lox, например, которые можно найти в pExchange-6 Core Vectors или Stratagene (Ла-Хойя, Калифорния). Примеры векторов, которые произвольно встраиваются в хромосомы клетки-хозяина, включают, например, pcDNA3.1 (при введении в отсутствие Т-антигена) от Invitrogen (Карлсбад, Калифорния) и pCI или pFNIOA (ACT) FLEXI™ от Promega (Мадисон, Висконсин). Дополнительные промоторные элементы, например, энхансеры, регулируют частоту инициации транскрипции. Обычно, они расположены на участке 30 - 110 п.о. против хода транскрипции от сайта инициации, хотя недавно было показано, что множество промоторов также содержат функциональные элементы по ходу транскрипции от сайта инициации. Расстояние между элементами промотора часто можно легко менять, так что функция промотора сохраняется, когда элементы инвертируются или перемещаются относительно друг друга. В промоторе тимидинкиназы (tk) расстояние между элементами промотора можно увеличить до 50 п.о. до того, как активность начнет снижаться. В зависимости от промотора, судя по всему, отдельные элементы могут действовать либо совместно, либо независимо, чтобы активировать транскрипцию.
[00221] Одним примером подходящего промотора является последовательность промотора немедленно-ранних генов цитомегаловируса (CMV). Данная последовательность промотора представляет собой последовательность сильного конститутивного промотора, способного запускать высокие уровни экспрессии любой полинуклеотидной последовательности, функционально связанной с ним.
[00222] Другой пример подходящего промотора представляет собой фактор элонгации 1-альфа 1 человека (hEF1a1). В вариантах реализации векторная конструкция, содержащая CAR, описанный в данной заявке, содержит функциональные варианты hEF1a1.
[00223] Тем не менее, также можно применять другие последовательности конститутивного промотора, включая, но не ограничиваясь перечисленными: ранний промотор вируса обезьян 40 (SV40), промотор вируса опухоли молочной железы мыши (MMTV), промотор длинного концевого повтора (LTR) вируса иммунодефицита человека (ВИЧ), промотор MoMuLV, промотор вируса лейкоза птиц, немедленно-ранний промотор вируса Эпштейна-Барр, промотор вируса саркомы Рауса, а также промоторы генов человека, такие как, но не ограничиваясь перечисленными: промотор актина, промотор миозина, промотор гемоглобина и промотор креатинкиназы. Кроме того, настоящее изобретение не должно быть ограничено применением конститутивных промоторов. Предполагается, что индуцируемые промоторы также входят в объем настоящего изобретения, как описано ранее. Применение индуцируемого промотора создает молекулярный переключатель, способный включать экспрессию полинуклеотидной последовательности, с которой он функционально связан, когда такая экспрессия желательна, или выключать экспрессию, когда экспрессия нежелательна. Примеры индуцируемых промоторов включают, но не ограничены перечисленными: промотор металлотионеина, промотор глюкокортикоидов, промотор прогестерона и промотор тетрациклина. В одном аспекте индуцируемый промотор может представлять собой промотор, индуцируемый лигандом переключателя генов. В некоторых случаях индуцируемый промотор может представлять собой состоящий из двух полипептидов индуцируемый низкомолекулярным лигандом переключатель генов на основе рецептора экдизона, такой как переключатель генов RHEOSWITCH®.
[00224] Для того чтобы оценить экспрессию CAR, описанного в данной заявке, или его частей, вектор экспрессии, который предназначен для введения в клетку, также может содержать либо ген селектируемого маркера, либо репортерный ген, либо и то, и другое, чтобы способствовать идентификации и селекции экспрессирующих клеток из популяции клеток, в которой ищут клетки, трансфицированные или инфицированные вирусными векторами или невирусными векторами. В других аспектах селектируемый маркер может находиться на отдельном участке ДНК и использоваться в процедуре котрансфекции. Как селектируемые маркеры, так и репортерные гены могут быть фланкированы подходящими регуляторными последовательностями, чтобы позволить экспрессию в клетках-хозяевах. Полезные селектируемые маркеры включают, например, гены устойчивости к антибиотикам, такие как ген устойчивости к неомицину (пео) и ген устойчивости к ампициллину, и тому подобные гены. В некоторых вариантах реализации метку укороченного рецептора эпидермального фактора роста (HER1t или HER1t-1) можно применять в качестве гена селектируемого маркера.
[00225] Репортерные гены можно применять для идентификации потенциально трансфицированных клеток и для оценки функциональности регуляторных последовательностей. Обычнорепортерный ген представляет собой ген, который не присутствует или не экспрессируется реципиентным организмом или тканью и который кодирует полипептид, экспрессия которого проявляется некоторым легко детектируемым свойством, например, ферментативной активностью. Экспрессию репортерного гена анализируют через подходящее время после внедрения ДНК в реципиентные клетки. Подходящие репортерные гены включают гены, кодирующие люциферазу, бета-галактозидазу, хлорамфеникол-ацетилтрансферазу, секретируемую щелочную фосфатазу или зеленый флуоресцентный белок (например, Ui-Tei и др., FEBS Letters 479: 79-82 (2000)). Подходящие системы экспрессии хорошо известны, и их можно получить, применяя известные методики, или получить из коммерческих источников. Обычно в конструкции минимальную 5'-фланкирующую область, при которой выявляют наибольший уровень экспрессии репортерного гена, идентифицируют как промотор. Такие промоторные области могут быть связаны с репортерным геном, и их можно применять для оценки способности агентов модулировать управляемую промотором транскрипцию.
[00226] В вариантах реализации вирусный вектор, описанный в данной заявке, может содержать промотор hEF1a1 для запуска экспрессии трансгенов, последовательность поли(А) бычьего гормона роста для усиления транскрипции, посттранскрипционный регуляторный элемент вируса гепатита сурка (WPRE), а также последовательности LTR, полученные из плазмиды pFUGW.
[00227] Способы внедрения и экспрессии генов в клетку хорошо известны. В контексте вектора экспрессии, вектор можно легко внедрить в клетку-хозяина, например, клетку млекопитающего, бактерий, дрожжей или насекомых, с помощью любого способа, описанного в данной области. Например, вектор экспрессии можно перенести в клетку-хозяина с помощью физических, химических или биологических способов.
[00228] Физические способы внедрения полинуклеотида в клетку-хозяина, например, эффекторную иммунную клетку, включают преципитацию фосфатом кальция, липофекцию, бомбардировку частицами, микроинъекцию, электропорацию и тому подобные способы. Способы получения клеток, содержащих векторы и/или экзогенные нуклеиновые кислоты, хорошо известны в данной области. См., например, Sambrook и др. (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Нью-Йорк (2001)). В вариантах реализации способ внедрения полинуклеотида в клетку-хозяина представляет собой трансфекцию фосфатом кальция или трансфекцию полиэтиленимином (PEI). В некоторых вариантах реализации способ внедрения полинуклеотида в клетку-хозяина представляет собой электропорацию.
[00229] Биологические способы внедрения интересующего полинуклеотида в клетку-хозяина, например, эффекторную иммунную клетку, включают применение ДНК- и РНК-векторов. Вирусные векторы, и особенно ретровирусные векторы, стали наиболее широко применяемым способом внедрения генов в млекопитающее, например, в клетки человека. Другие вирусные векторы могут происходить из лентивируса, поксвирусов, вируса простого герпеса I, аденовирусов и аденоассоциированных вирусов, и тому подобных вирусов. См., например, патенты США№5,350,674 и 5,585,362.
[00230] Химические средства для внедрения полинуклеотида в клетку-хозяина включают коллоидные дисперсные системы, такие как комплексы макромолекул, нанокапсулы, микросферы, гранулы и системы на основе липидов, включая эмульсии типа масло в воде, мицеллы, смешанные мицеллы и липосомы. Типичная коллоидная система для применения в качестве средства доставки in vitro и in vivo представляет собой липосому (например, искусственную мембранную везикулу).
[00231] В случае если используется вирусная система доставки, типичным средством доставки является липосома. Липидные составы можно применять для внедрения нуклеиновых кислот в клетку-хозяина (in vitro, ex vivo или in vivo). В другом аспекте, нуклеиновая кислота может быть связана с липидом. Нуклеиновая кислота, связанная с липидом, может быть инкапсулирована в водное внутреннее пространство липосомы, рассеяна внутри липидного бислоя липосомы, присоединена к липосоме посредством соединяющей молекулы, которая связана как с липосомой, так и с олигонуклеотидом, заключенным в липосому, может образовывать комплекс с липосомой, быть диспергирована в растворе, содержащем липид, смешана с липидом, объединена с липидом, содержаться в виде суспензии в липиде, содержаться или образовывать комплекс с мицеллой или иным образом связана с липидом. Композиции с липидом, липидом/ДНК или липидом/вектором экспрессии не ограничены любой конкретной структурой в растворе. Например, они могут присутствовать в бислойной структуре, в виде мицелл или в «схлопнутой» структуре. Они также могут быть просто рассеяны в растворе, необязательно образуя агрегаты, которые не однородны по размеру или форме. Липиды представляют собой жирные вещества, которые могут представлять собой встречающиеся в природе или синтетические липиды. Например, липиды включают жировые капли, которые в природе встречаются в цитоплазме, а также класс соединений, которые содержат длинноцепочечные алифатические углеводороды и их производные, такие как жирные кислоты, спирты, амины, аминоспирты и альдегиды.
[00232] Липиды, подходящие для применения, можно получить из коммерчески доступных источников. Например, димиристилфосфатидилхолин («DMPC») можно получить от Sigma, Сент-Луис, Миссури; дицетилфосфат («DCP») можно получить от K & K Laboratories (Плейнвью, Нью-Йорк); холестерин («Chol») можно получить от Calbiochem-Behring; димиристилфосфатидилглицерин («DMPG») и другие липиды можно получить от Avanti Polar Lipids, Inc. (Бирмингем, Алабама). Исходные растворы липидов в хлороформе или хлороформе/метаноле можно хранить при приблизительно -20°С. Хлороформ используют в качестве единственного растворителя, поскольку его легче выпаривать, чем метанол. «Липосома» представляет собой родовой термин, в объем которого входят различные однослойные и многослойные липидные среды, образованные путем получения замкнутых липидных бислоев или агрегатов. Липосомы можно охарактеризовать как имеющие везикулярные структуры с фосфолипидной бислойной мембраной и внутренней водной средой. Многослойные липосомы содержат множество липидных слоев, разделенных водной средой. Они образуются спонтанно, когда фосфолипиды суспендируют в избытке водного раствора. Компоненты липидов претерпевают самоперестройку перед образованием замкнутых структур и захватом воды и растворенных веществ между липидными бислоями (Ghosh и др., Glycobiology 5: 505-10 (1991)). Тем не менее, также в объем входят композиции со структурами в растворе, отличными от нормальной структуры везикул. Например, липиды могут принимать мицеллярную структуру или существуют лишь в виде неоднородных агрегатов липидных молекул. Также предложены комплексы липофектамина-нуклеиновой кислоты.
Клетки, содержащие MUC16-CAR и векторы
[00233] В данной заявке предложены сконструированные клетки, экспрессирующие CAR, описанный в данной заявке. В некоторых вариантах реализации сконструированная клетка, описанная в данной заявке, представляет собой эффекторную иммунную клетку. В вариантах реализации в настоящей заявке предложена эффекторная иммунная клетка, содержащая вектор, содержащий остов и последовательность нуклеиновой кислоты, кодирующую (1) укороченный рецептор эпидермального фактора роста (HER1t или HER1t1) и (2) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и е) сигнальный домен CD3-дзета.
[00234] В некоторых вариантах реализации предложена эффекторная иммунная клетка, содержащая химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; е) сигнальный домен CD3-дзета и (1) укороченный рецептор эпидермального фактора роста (HER1t или HER1t1).
[00235] В вариантах реализации в настоящей заявке предложена эффекторная иммунная клетка, содержащая (1) метку клетки для применения в качестве переключателя уничтожения, селективный маркер, биомаркер или их комбинацию, и (2) химерный антигенный рецептор (CAR), причем CAR содержит (а) домен, связывающий антиген MUC16; (b) домен стебля; (с) трансмембранный домен; (d) костимулирующий сигнальный домен, содержащий 4-1 ВВ или CD28, или и то, и другое; и (е) сигнальный домен CD3-дзета. В вариантах реализации метка клетки представляет собой HER1t, HER1t1, CD20t-1 или CD20.
[00236] В вариантах реализации эффекторная иммунная клетка представляет собой Т-клетку, клетку-естественного киллера (NK), цитотоксический Т-лимфоцит (CTL) и регуляторную Т-клетку. В вариантах реализации клетка проявляет противоопухолевую активность, когда домен, связывающий антиген MUC16, связывается с MUC16.
Модифицированные эффекторные иммунные клетки
[00237] Предложены эффекторные иммунные клетки, модифицированные для экспрессии одного или более гетерологичных генов или полипептидов, описанных в данной заявке. Предложены эффекторные иммунные клетки, модифицированные для экспрессии MUC16-CAR, описанного в данной заявке, и по меньшей мере одной из меток HER1t, HER1tl, CD20 и CD20t-1. В некоторых случаях предложена эффекторная иммунная клетка, модифицированная для экспрессии MUC16-CAR, mbIL-15 и по меньшей мере одной из меток HER1t, HER1t1, CD20 и CD20t-1, описанных в данной заявке.
[00238] «Т-клетка» или «Т-лимфоцит» в данной заявке представляет собой тип лимфоцита, который играет центральную роль в клеточно-опосредованном иммунитете. Их можно отличить от других лимфоцитов, таких как В-клетки и клетки-естественные киллеры (NK-клетки), по присутствию Т-клеточного рецептора (TCR) на поверхности клетки.
[00239] В некоторых вариантах реализации модифицированные эффекторные иммунные клетки представляют собой модифицированные иммунные клетки, которые включают Т-клетки и/или клетки-естественные киллеры. Т-клетки или Т-лимфоциты представляют собой подтип белых кровяных клеток, которые участвуют в клеточно-опосредованном иммунитете. Примеры Т-клеток включают хелперные Т-клетки, цитотоксические Т-клетки, клетки ТН17, стволовые Т-клетки памяти (TSCM), необученные Т-клетки, Т-клетки памяти, эффекторные Т-клетки, регуляторные Т-клетки или Т-клетки-естественные киллеры.
[00240] Хелперные Т-клетки (ТН-клетки) помогают другим белым кровяным клеткам в иммунологических процессах, включая созревание В-клеток с образованием плазматических клеток и В-клеток памяти и активацию цитотоксических Т-клеток и макрофагов. В некоторых случаях ТН-клетки известны как CD4+Т-клетки благодаря экспрессии гликопротеина CD4 на поверхностях клеток. Хелперные Т-клетки активируются, когда им презентируют пептидные антигены молекулы ГКГС II класса, которые экспрессируются на поверхности антигенпрезентирующих клеток (АПК). После активации они быстро делятся и секретируют малые белки, названные цитокинами, которые регулируют или способствуют активному иммунному ответу. Данные клетки могут дифференцироваться в один из нескольких подтипов, включая ТН1, ТН2, ТН3, ТН17, Th9 или TFH, который секретирует различные цитокины, чтобы способствовать различным типам иммунных ответов. Передача сигналов от АПК направляет Т-клетки на образование определенных подтипов.
[00241] Цитотоксические Т-клетки (ТС-клетки или CTL) уничтожают инфицированные вирусом клетки и опухолевые клетки, а также участвуют в отторжении трансплантата. Данные клетки также известны как CD8+ Т-клетки, поскольку они экспрессируют гликопротеин CD8 на своей поверхности. Данные клетки распознают свои мишени путем связывания с антигеном, связанным с молекулами ГКГС I класса, которые присутствуют на поверхностях всех содержащих ядра клеток. Посредством IL-10, аденозина и других молекул, секретированных регуляторными Т-клетками, CD8+клетки могут инактивироваться и перейти в анергическое состояние, что предотвращает аутоиммунные заболевания.
[00242] Т-клетки памяти представляют собой субтипантигенспецифичных Т-клеток, которые сохраняются длительное время после устранения инфекции. Они быстро размножаются с образованием больших количеств эффекторных Т-клеток после повторного контакта со знакомым антигеном, таким образом, обеспечивая иммунную систему «памятью» о последней инфекции. Т-клетки памяти включают следующие субтипы: стволовые Т-клетки памяти (TSCM), Т-клетки центральной памяти (клетки ТСМ) и два типа эффекторных Т-клеток памяти (клетки ТЕМ и клетки TEMRA). Клетки памяти могут быть либо CD4+, либо CD8+. Т-клетки памяти могут экспрессировать белки поверхности клетки CD45RO, CD45RA и/или CCR7.
[00243] Регуляторные Т-клетки (клетки Treg), ранее известные как супрессорные Т-клетки, играют роль в поддержании иммунологической толерантности. Их основная роль заключается в остановке опосредованного Т-клетками иммунитета для окончания иммунной реакции и подавления аутореактивных Т-клеток, которые избежали процесса отрицательной селекции в тимусе.
[00244] Т-клетки-естественные киллеры (NKT-клетки) связывают адаптивную иммунную систему с врожденной иммунной системой. В отличие от обычных Т-клеток, которые распознают пептидные антигены, презентированные молекулами главного комплекса гистосовместимости (ГКГС), NKT-клетки распознают гликолипидный антиген, презентированный молекулой, названной CD Id. После активации данные клетки могут осуществлять функции, приписываемые как Th-, так и Тс-клеткам (т.е. продукцию цитокинов и высвобождение цитолитических/уничтожающих клетки молекул). Они также способны распознавать и уничтожать некоторые опухолевые клетки и клетки, инфицированные вирусами герпеса.
[00245] Клетки-естественные киллеры (NK) представляют собой тип цитотоксических лимфоцитов врожденной иммунной системы. В некоторых случаях NK-клетки обеспечивают первую линию защиты от вирусных инфекций и/или образования опухоли. NK-клетки могут обнаруживать ГКГС, презентированные на инфицированных или раковых клетках, запуская высвобождение цитокинов, и впоследствии вызывать лизис и апоптоз. NK-клетки могут дополнительно обнаруживать подвергнутые стрессу клетки в отсутствие антител и/или ГКГС, тем самым позволяя осуществить быстрый иммунный ответ.
Дозы модифицированных эффекторных иммунных клеток
[00246] В некоторых вариантах реализации некоторое количество модифицированных эффекторных иммунных клеток вводят нуждающемуся в этом субъекту, и указанное количество определяют на основании эффективности и способности вызывать ассоциированную с цитокинами токсичность. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 102 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 103 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 104 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 105 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 105 до приблизительно 108 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 105 до приблизительно 107 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 106 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 106 до приблизительно 108 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 107 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 105 до приблизительно 106 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 106 до приблизительно 107 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 107 до приблизительно 108 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 108 до приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 109 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 108 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 107 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 106 модифицированных эффекторных иммунных клеток/кг. В некоторых случаях количество модифицированных эффекторных иммунных клеток включает от приблизительно 105 модифицированных эффекторных иммунных клеток/кг.
[00247] В некоторых вариантах реализации предложены CAR-T-клетки, которые представляют собой специфичные к MUC16 CAR-T-клетки. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 102 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 103 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 104 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 105 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 105 до приблизительно 108 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 105 до приблизительно 107 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 106 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 106 до приблизительно 108 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 107 до приблизительно 109 CAR-T клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-Т-клеток включает от приблизительно 105 до приблизительно 106 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-Т-клеток включает от приблизительно 106 до приблизительно 107 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 107 до приблизительно 108 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает от приблизительно 108 до приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-Т-клеток включает приблизительно 109 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-Т-клеток включает приблизительно 108 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 107 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 106 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 105 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 104 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 103 CAR-T-клеток/кг. В некоторых случаях количество специфичных к MUC16 CAR-T-клеток включает приблизительно 102 CAR-T-клеток/кг.
Источники эффекторных иммунных клеток
[00248] В некоторых аспектах варианты реализации, описанные в данной заявке, включают способы получения и/или размножения антигенспецифичных перенацеленных эффекторных иммунных клеток (например, Т-клеток, Treg, NK-клеток или NK-T-клеток), которые включают трансфекцию клеток вектором экспрессии, содержащим конструкцию ДНК (или РНК), кодирующую CAR, затем необязательно стимуляцию клеток питающими клетками, рекомбинантным антигеном или антителом к указанному рецептору, чтобы вызвать пролиферацию клеток. В некоторых аспектах клетка (или популяция клеток), сконструированная для экспрессии CAR, представляет собой стволовую клетку, клетку iPS, Т-клетку, дифференцированную из клетки iPS, эффекторную иммунную клетку или предшественника данных клеток.
[00249] Источники эффекторных иммунных клеток могут включать как аллогенные, так и аутологические источники. В некоторых случаях эффекторные иммунные клетки могут быть дифференцированы из стволовых клеток или индуцированных плюрипотентных стволовых клеток (иПСК). Таким образом, клетку для конструирования согласно вариантам реализации можно выделить из пуповинной крови, периферической крови, эмбриональных стволовых клеток человека или иПСК. Например, аллогенные Т-клетки можно модифицировать, чтобы они содержали химерный антигенный рецептор (и необязательно не содержали функциональный TCR). В некоторых аспектах эффекторные иммунные клетки представляют собой первичные Т-клетки человека, такие как Т-клетки, полученные из мононуклеарных клеток периферической крови (МКПК) человека. МКПК можно собрать из периферической крови или после стимуляции G-CSF (колониестимулирующий фактор гранулоцитов) из костного мозга, или из пуповинной крови. В одном аспекте эффекторные иммунные клетки представляют собой общую популяцию Т-клеток. После трансфекции или трансдукции (например, конструкцией экспрессии CAR) клетки можно незамедлительно вводить путем инфузии или можно криоконсервировать. В некоторых аспектах после трансфекции или трансдукции клетки можно сохранить в растворе цитокинов, который может содержать IL-2 и/или IL-21, до того как они будут готовы к инфузии. В некоторых аспектах после трансфекции клетки можно размножать в течение дней, недель или месяцев ex vivo в виде общей популяции в течение приблизительно 1, 2, 3, 4, 5 дней или более после переноса генов в клетки. В дополнительном аспекте после трансфекции трансфектантов клонируют, и клон, демонстрирующий присутствие одной встроенной или эписомально поддерживаемой кассеты экспрессии или плазмиды и экспрессию химерного антигенного рецептора, размножали ex vivo. Клон, выбранный для размножения, проявлял способность специфично распознавать и лизировать экспрессирующие антиген клетки-мишени. Рекомбинантные Т-клетки можно нарастить путем стимуляции IL-2 или другими цитокинами, которые связываются с общей гамма-цепью (например, IL-7, IL-12, IL-15, IL-21 и другими). Рекомбинантные Т-клетки можно размножить путем стимуляции искусственными антигенпрезентирующими клетками. Рекомбинантные Т-клетки можно размножить на искусственных антигенпрезентирующих клетках или с антителом, таким как ОКТЗ, которое перекрестно связывает CD3 на поверхности Т-клеток. Можно дополнительно осуществить селекцию субпопуляций рекомбинантных Т-клеток с применением способов выделения на основе магнитных гранул и/или технологии сортировки клеток с возбуждением флуоресценции и дополнительно культивировать их с АаРС. В дополнительном аспекте генетически модифицированные клетки можно криоконсервировать.
[00250] Т-клетки также можно получить из множества источников, включая костный мозг, ткань лимфатического узла, пуповинную кровь, ткань тимуса, ткань из очага инфекции, асцит, плевральный выпот, ткань селезенки и опухоли. В некоторых вариантах реализации настоящего изобретения можно использовать любое количество линий Т-клеток, доступных в данной области. В некоторых вариантах реализации настоящего изобретения Т-клетки можно получить из единицы крови, собранной от субъекта, применяя любое количество методик, известных квалифицированному специалисту, таких как разделение фиколлом®. В вариантах реализации клетки из циркулирующей крови из индивида получают с помощью афереза. Продукт афереза обычно содержит лимфоциты, включая Т-клетки, моноциты, гранулоциты, В-клетки, другие содержащие ядро белые кровяные клетки, красные кровяные клетки и тромбоциты. В одном варианте реализации клетки, собранные путем афереза, можно промыть, чтобы удалить плазматическую фракцию и чтобы поместить клетки в подходящий буфер или среды для последующих этапов обработки. В одном варианте реализации настоящего изобретения клетки промывают фосфатно-солевым буферным раствором (ФБР). В альтернативном варианте реализации в растворе для промывки отсутствует кальций и может отсутствовать магний или могут отсутствовать многие, если не все двухвалентные катионы. Исходные этапы активации в отсутствие кальция приводят к усиленной активации. Специалисты со средней квалификацией в данной области легко поймут, что этап промывки можно осуществить с помощью способов, известных специалистам в данной области, например, применяя полуавтоматизированную «проточную» центрифугу (например, устройство для обработки клеток Cobe 2991, Baxter CytoMate или Haemonetics Cell Saver 5), следуя инструкциям производителя. После промывки клетки можно ресуспендировать в различных биосовместимых буферах, таких как, например, ФБР без Са2+ и без Mg2+, PlasmaLyte А или другой солевой раствор с буфером или без него. В качестве альтернативы нежелательные компоненты образца афереза можно удалить и клетки непосредственно ресуспендировать в культуральной среде.
[00251] В другом варианте реализации Т-клетки выделяют из лимфоцитов периферической крови путем лизирования красных кровяных клеток и удаления моноцитов, например, путем центрифугирования через градиент перколла® или путем противоточного элютриациоиного центрифугирования. Определенную субпопуляцию Т-клеток, например, CD3+, CD28+, CD4+, CD8+, CD45RA+ и CD45RO+ Т-клетки, можно затем выделить с помощью методик положительной или отрицательной селекции. В другом варианте реализации CD14+ клетки удаляют из популяции Т-клеток. Например, в одном варианте реализации Т-клетки выделяют путем инкубации с конъюгированными с антителами против CD3/против CD28 (т.е. 3x28) гранулами, такими как DYNABEADS® М-450 CD3/CD28 Т, в течение периода времени, достаточного для положительной селекции желательных Т-клеток. В одном варианте реализации период времени составляет приблизительно 30 минут. В дополнительном варианте реализации период времени находится в диапазоне от 30 минут до 36 часов или более и все целые значения между указанными значениями. В дополнительном варианте реализации период времени составляет по меньшей мере 1, 2, 3, 4, 5 или 6 часов. В еще одном варианте реализации период времени составляет от 10 до 24 часов. В одном варианте реализации период времени инкубации составляет 24 часа. Для выделения Т-клеток из пациентов с лейкозом использование более длительных периодов инкубации, например, в течение 24 часов, может увеличить количество полученных клеток. Более длительные периоды инкубации можно использовать для выделения Т-клеток в любой ситуации, когда Т-клеток мало по сравнению с другими типами клеток, например, при выделении инфильтрирующих опухоль лимфоцитов (TIL) из опухолевой ткани или из индивидов с нарушенным иммунитетом. Кроме того, использование более длительных периодов инкубации может повысить эффективность захвата CD8+ Т-клеток. Таким образом, путем всего лишь укорачивания или удлинения времени, которое Т-клеткам позволяют связываться с гранулами CD3/CD28, и/или путем увеличения или уменьшения отношения гранул к Т-клеткам (как описано далее в данной заявке), субпопуляции Т-клеток можно в соответствии с предпочтениями подвергнуть положительной или отрицательной селекции при инициации культуры или в другие моменты времени в течение указанного процесса. Кроме того, путем увеличения или уменьшения отношения антител против CD3 и/или против CD28 на гранулах или другой поверхности, субпопуляции Т-клеток можно в соответствии с предпочтениями подвергнуть положительной или отрицательной селекции при инициации культуры или в другие желательные моменты времени. Квалифицированный специалист поймет, что также можно использовать множество раундов селекции в контексте настоящего изобретения. В некоторых вариантах реализации может быть желательно осуществить процедуру селекции и использовать «невыбранные» клетки для процесса активации и размножения. «Невыбранные» клетки также можно подвергнуть дополнительным раундам селекции.
[00252] Обогащение популяции Т-клеток путем отрицательной селекции можно осуществить с помощью комбинации антител, направленных на маркеры на поверхности, уникальные для прошедших отрицательную селекцию клеток. Одним способом является сортировка клеток и/или селекция с помощью отрицательной магнитной иммунной адгезии или проточной цитометрии, в которых применяют коктейль моноклональных антител, направленных на маркеры на поверхности клетки, присутствующие на клетках, прошедших отрицательную селекцию. Например, чтобы обогатить популяцию CD4+ клетками путем отрицательной селекции, коктейль моноклональных антител обычно содержит антитела против CD14, CD20, CD11b, CD16, HLA-DR и CD8. В некоторых вариантах реализации может быть желательно обогатить или провести положительную селекцию регуляторных Т-клеток, которые обычно экспрессируют CD4+, CD25+, CD62Lhi, GITR+ и FoxP3+. В качестве альтернативы, в некоторых вариантах реализации регуляторные Т-клетки удаляют с помощью гранул, конъюгированных с антителами против CD25, или другим сходным способом селекции.
[00253] Для выделения желательной популяции клеток путем положительной или отрицательной селекции, концентрацию клеток и поверхности (например, частиц, таких как гранулы) можно изменять. В некоторых вариантах реализации может потребоваться значительно уменьшить объем, в котором смешивают гранулы и клетки (т.е. увеличить концентрацию клеток), чтобы гарантировать максимальный контакт клеток и гранул. Например, в одном варианте реализации используют концентрацию, составляющую 2 миллиарда клетки/мл. В одном варианте реализации используют концентрацию, составляющую 1 миллиард клеток/мл. В дополнительном варианте реализации используют более 100 миллионов клеток/мл. В дополнительном варианте реализации используют концентрацию клеток, составляющую 10, 15, 20, 25, 30, 35, 40, 45 или 50 миллионов клеток/мл. В еще одном варианте реализации используют концентрацию клеток, составляющую 75, 80, 85, 90, 95 или 100 миллионов клеток/мл. В дополнительных вариантах реализации можно использовать концентрации, составляющие 125 или 150 миллионов клеток/мл. Использование высоких концентраций может привести к повышенному выходу клеток, активации клеток и размножению клеток. Кроме того, использование высоких концентраций клеток позволяет более эффективный захват клеток, которые могут слабо экспрессировать целевые интересующие антигены, таких как CD28-отрицательные Т-клетки, или из образцов, в которых присутствует множество опухолевых клеток (т.е. лейкемической крови, опухолевой ткани и т.д.). Такие популяции клеток могут иметь терапевтическое значение, и будет желательно их получить. Например, использование высокой концентрации клеток позволяет более эффективную селекцию CD8+ Т-клеток, у которых обычно более слабая экспрессия CD28.
[00254] В сходном варианте реализации может потребоваться использовать более низкие концентрации клеток. При значительном разбавлении смеси Т-клеток и поверхности (например, частиц, таких как гранулы), взаимодействия между частицами и клетками минимизируются. Это позволяет осуществить селекцию клеток, которые экспрессируют большие количества желательных антигенов, которые будут связаны с частицами. Например, CD4+ Т-клетки экспрессируют более высокие уровни CD28 и более эффективно захватываются, чем CD8+ Т-клетки в разбавленных концентрациях. В одном варианте реализации используемая концентрация клеток составляет 5×106/мл. В других вариантах реализации используемая концентрация может составлять приблизительно от 1×105/мл до 1×106/мл, и любое целое значение между указанными значениями.
[00255] В других вариантах реализации клетки можно инкубировать на вращающем устройстве в течение различных интервалов времени при различных скоростях либо при 2-10°С, либо при комнатной температуре.
[00256] Т-клетки для стимуляции также можно заморозить после этапа промывки. После этапа промывки, который удаляет плазму и тромбоциты, клетки можно суспендировать в растворе для замораживания. Хотя множество растворов для замораживания и параметров замораживания известны в данной области и будут пригодны в данном контексте, один способ включает применение ФБР, содержащего 20% ДМСО и 8% сывороточного альбумина человека, или культуральной среды, содержащей 10% декстрана 40 и 5% декстрозы, 20% сывороточного альбумина человека и 7,5% ДМСО, или 31,25% PlasmaLyte-А, 31,25% декстрозы 5%, 0,45% NaCl, 10% декстрана 40 и 5% декстрозы, 20% сывороточного альбумина человека и 7,5% ДМСО, или других подходящих сред для замораживания клеток, содержащих, например, Hespan и PlasmaLyte А, указанные клетки затем замораживают до -80°С при скорости 1°С в минуту и хранят в резервуаре для хранения в паровой фазе жидкого азота. Можно применять другие способы контролируемого замораживания, а также неконтролируемое замораживание сразу при -20°С или в жидком азоте. В некоторых вариантах реализации криоконсервированные клетки размораживают и промывают, как описано в данной заявке, и оставляют на один час при комнатной температуре перед активацией с применением способов согласно настоящему изобретению.
[00257] Также в некоторых вариантах реализации предложен сбор образцов крови или продукта афереза от субъекта в период времени перед тем, как могут потребоваться размноженные клетки, описанные в данной заявке. Соответственно, источник клеток, которые нужно размножить, можно собрать в любой необходимый момент времени, и желательные клетки, такие как Т-клетки, можно выделить и заморозить для последующего применения в Т-клеточной терапии любого количества заболеваний или состояний, при которых будет польза от Т-клеточной терапии, таких как описанные в данной заявке. В одном варианте реализации образец крови или продукт афереза берут из в целом здорового субъекта. В некоторых вариантах реализации образец крови или продукт афереза берут из в целом здорового субъекта, у которого есть риск развития заболевания, но у которого еще не развилось заболевание, и интересующие клетки выделяют и замораживают для последующего применения. В некоторых вариантах реализации Т-клетки можно размножить, заморозить и применять позже. В некоторых вариантах реализации образцы собирают из пациента вскоре после диагностики конкретного заболевания, описанного в данной заявке, но перед любой терапией. В дополнительном варианте реализации клетки выделяют из образца крови или продукта афереза субъекта перед любым количеством подходящих способов лечения, включая, но не ограничиваясь лечением такими агентами, как натализумаб, эфализумаб, противовирусные агенты, химиотерапия, радиация, иммуносупрессивные агенты, такие как циклоспорин, азатиоприн, метотрексат, микофенолат и FK506, антитела или другие иммунодеструктивные агенты, такие как КЭМПАС, антитела против CD3, цитоксан, флударабин, циклоспорин, FK506, рапамицин, микофеноловая кислота, стероиды, FR901228 и облучение. Данные лекарственные средства либо ингибируют кальций-зависимую фосфатазу - кальциневрин (циклоспорин и FK506), либо ингибируют киназу p70S6, которая важна для сигнального пути, вызванного фактором роста (рапамицин) (Liu и др., Cell 66:807-815, (1991); Henderson и др., Immun 73:316-321, (1991); Bierer и др., Curr. Opin. Immun 5:763-773, (1993)). В дополнительном варианте реализации клетки выделяют из пациента и замораживают для последующего применения в сочетании с (например, до, одновременно или после) трансплантацией костного мозга или стволовых клеток, разрушающей Т-клетки терапией с применением либо химиотерапевтических агентов, таких как флударабин, либо наружной дистанционной лучевой терапии (XRT), либо циклофосфамида, либо антител, таких как ОКТЗ или КЭМПАС. В другом варианте реализации клетки выделяют до, и их можно заморозить для последующего применения для лечения после разрушающей В-клетки терапии, например, агентами, которые реагируют с CD20, например, ритуксаном.
[00258] В дополнительном варианте реализации настоящего изобретения Т-клетки получают из пациента непосредственно после лечения. В этом отношении, наблюдали, что после некоторых способов лечения рака, в частности, после лечения лекарственными средствами, которые повреждают иммунную систему, вскоре после лечения во время периода, когда пациенты обычно будут восстанавливаться от лечения, качество полученных Т-клеток может быть оптимальным, или их способность разрастаться ex vivo может улучшиться. Аналогичным образом, после манипуляции ex vivo с применением способов, описанных в данной заявке, данные клетки могут находиться в предпочтительном состоянии для улучшенного приживления и размножения in vivo. Таким образом, в контексте настоящего изобретения предполагается собирать клетки крови, включая Т-клетки, дендритные клетки или другие клетки гематопоэтического происхождения, во время данной фазы восстановления. Кроме того, в некоторых вариантах реализации можно применять активацию (например, активацию с помощью GM-CSF) и режимы подготовки к трансплантации, чтобы создать состояние у субъекта, которое благоприятствует репопуляции, рециркуляции, регенерации и/или размножению конкретных типов клеток, особенно в течение определенного периода времени после терапии. Типичные типы клеток включают Т-клетки, В-клетки, дендритные клетки и другие клетки иммунной системы.
Активация и увеличение количества Т-клеток
[00259] Либо до, либо после конструирования Т-клеток для экспрессии CAR, описанного в данной заявке, Т-клетки можно активировать и размножить, как правило, применяя способы, описанные, например, в патентах США №6,352,694; 6,534,055; 6,905,680; 6,692,964; 5,858,358; 6,887,466; 6,905,681; 7,144,575; 7,067,318; 7,172,869; 7,232,566; 7,175,843; 5,883,223; 6,905,874; 6,797,514; 6,867,041; и в публикации заявки на патент США №20060121005.
[00260] Как правило, Т-клетки, описанные в данной заявке, наращивают путем приведения в контакт с поверхностью, к которой присоединен агент, который стимулирует сигнал, связанный с комплексом CD3/TCR, и лиганд, который стимулирует костимулирующую молекулу на поверхности Т-клеток. В частности, популяции Т-клеток можно стимулировать, как описано в данной заявке, например посредством контакта с антителом против CD3, или его антигенсвязывающим фрагментом, или антителом против CD2, иммобилизованным на поверхности, или посредством контакта с активатором протеинкиназы С (например, бриостатином) в сочетании с ионофором кальция. Для костимуляции вспомогательной молекулы на поверхности Т-клеток применяют лиганд, который связывает вспомогательную молекулу. Например, популяцию Т-клеток можно привести в контакт с антителом против CD3 и антителом против CD28 при условиях, подходящих для стимуляции пролиферации Т-клеток. Для стимуляции пролиферации либо CD4+ Т-клеток, либо CD8+ Т-клеток, можно применять антитело против CD3 и антитело против CD28. Примеры антитела против CD28, которое можно применять, включают 9.3, В-Т3, XR-CD28 (Diaclone, Безансон, Франция), а также можно применять другие способы, широко известные в данной области (Berg и др., Transplant Ргос.30(8):3975-3977, (1998); Haanen и др., J. Exp. Med. 190(9):13191328, (1999); Garland и др., J. Immonol Meth. 227(1-2):53-63, (1999)).
[00261] В некоторых вариантах реализации первичный стимулирующий сигнал и костимулирующий сигнал для Т-клетки может предоставляться в соответствии с различными протоколами. Например, агенты, предоставляющие каждый сигнал, могут находиться в растворе или могут быть связаны с поверхностью. Когда они связаны с поверхностью, указанные агенты могут быть связаны с единой поверхностью (т.е. в «цис»-расположении) или с отдельными поверхностями (т.е. в «транс»-расположении). В качестве альтернативы, один агент может быть связан с поверхностью, а другой агент может находиться в растворе. В одном варианте реализации агент, предоставляющий костимулирующий сигнал, связан с поверхностью клетки, а агент, предоставляющий первичный активирующий сигнал, находится в растворе или связан с поверхностью. В некоторых вариантах реализации и то, и другое агента могут находиться в растворе. В другом варианте реализации агенты могут находиться в растворимой форме, а затем перекрестно связываться с поверхностью, например, клетка, экспрессирующая Fc-рецепторы, или антитело, или другой связывающий агент, который будет связываться с указанными агентами. В этом отношении, см., например, в публикациях заявок на патент США №20040101519 и 20060034810 описание искусственных антигенпрезентирующих клеток (иАПК), которые предназначены для применения для активации и размножения Т-клеток в настоящем изобретении.
[00262] В одном варианте реализации два агента иммобилизованы на гранулах, либо на одной и той же грануле, т.е. «цис», либо на отдельных гранулах, т.е. «транс». В качестве примера, агент, предоставляющий первичный активирующий сигнал, представляет собой антитело против CD3 или его антигенсвязывающий фрагмент, и агент, предоставляющий костимулирующий сигнал, представляет собой антитело против CD28 или его антигенсвязывающий фрагмент; и оба агента совместно иммобилизованы на одной и той же грануле в эквивалентных молекулярных количествах. В одном варианте реализации используют отношение 1:1 каждого антитела, связанного с гранулами, для размножения CD4+ Т-клеток и роста Т-клеток. В некоторых аспектах настоящего изобретения используют такое отношение антител против CD3:CD28, связанных с гранулами, что наблюдается повышение размножения Т-клеток по сравнению с размножением, наблюдаемым при использовании отношения 1:1. В одном конкретном варианте реализации наблюдают повышение в от приблизительно 1 до приблизительно 3 раз по сравнению с размножением, наблюдаемым при использовании отношения 1:1. В одном варианте реализации отношение антител против CD3:CD28, связанных с гранулами, находится в диапазоне от 100:1 до 1:100 и все целые значения между указанными значениями. В одном аспекте настоящего изобретения большее количество антитела против CD28 связано с частицами, чем количество антитела против CD3, т.е., отношение CD3:CD28 меньше единицы. В некоторых вариантах реализации настоящего изобретения отношение антитела против CD28 к антителу против CD3, связанных с гранулами, больше чем 2:1. В одном конкретном варианте реализации используют отношение 1:100 антител против CD3:CD28, связанных с гранулами. В другом варианте реализации используют отношение 1:75 антител против CD3:CD28, связанных с гранулами. В дополнительном варианте реализации используют отношение 1:50 антител против CD3:CD28, связанных с гранулами. В другом варианте реализации используют отношение 1:30 антител против CD3:CD28, связанных с гранулами. В вариантах реализации используют отношение 1:10 антител против CD3:CD28, связанных с гранулами. В другом варианте реализации используют отношение 1:3 антител против CD3:CD28, связанных с гранулами. В еще одном варианте реализации используют отношение 3:1 антител против CD3:CD28, связанных с гранулами.
[00263] Отношения частицы к клеткам от 1:500 до 500:1 и любые целые значения между указанными значениями можно использовать, чтобы стимулировать Т-клетки или другие клетки-мишени. Для специалистов со средней квалификацией в данной области будет понятно, что отношение частиц к клеткам может зависеть от размера частиц относительно целевой клетки. Например, гранулы малого размера могут связываться лишь с несколькими клетками, тогда как гранулы большего размера могут связываться с множеством клеток. В некоторых вариантах реализации отношение клеток к частицам в диапазоне от 1:100 до 100:1, и любые целые значения между указанными значениями, и в дополнительных вариантах реализации отношение от 1:9 до 9:1, и любые целые значения между указанными значениями, также можно использовать, чтобы стимулировать Т-клетки. Отношение частиц, связанных с антителами против CD3 и против CD28, к Т-клеткам, которое приводит к стимуляции Т-клеток, может изменяться, как отмечено выше, тем не менее, некоторые значения включают 1:100, 1:50, 1:40, 1:30, 1:20, 1:10, 1:9, 1:8, 1:7, 1:6, 1:5, 1:4, 1:3, 1:2, 1:1, 2:1, 3:1, 4:1, 5:1, 6:1, 7:1, 8:1, 9:1, 10:1 и 15:1, причем одно отношение составляет по меньшей мере 1:1 частиц на Т-клетку. В одном варианте реализации используют отношение частиц к клеткам, составляющее 1:1 или менее. В одном конкретном варианте реализации отношение частицы:клетки составляет 1:5. В дополнительных вариантах реализации отношение частиц к клеткам можно изменять в зависимости от дней стимуляции. Например, в одном варианте реализации отношение частиц к клеткам составляет от 1:1 до 10:1 в первый день, и дополнительные частицы добавляют к клеткам каждый день или каждый второй день после этого в течение вплоть до 10 дней, при конечных соотношениях от 1:1 до 1:10 (на основании количества клеток в день добавления). В одном конкретном варианте реализации отношение частиц к клеткам составляет 1:1 в первый день после стимуляции, и его подводят до 1:5 на третий и пятый день после стимуляции. В другом варианте реализации частицы добавляют ежедневно или через день до конечного отношения, составляющего 1:1 в первый день и 1:5 на третий и пятый день после стимуляции. В другом варианте реализации отношение частиц к клеткам составляет 2:1 в первый день после стимуляции, и его подводят до 1:10 на третий и пятый день после стимуляции. В другом варианте реализации частицы добавляют ежедневно или через день до конечного отношения, составляющего 1:1 в первый день и 1:10 на третий и пятый день после стимуляции. Для специалиста в данной области должно быть понятно, что различные другие отношения могут подходить для применения в настоящем изобретении. В частности, отношения будут изменяться в зависимости от размера частиц и от размера и типа клеток.
[00264] В дополнительных вариантах реализации, описанных в данной заявке, эффекторные иммунные клетки, такие как Т-клетки, комбинируют с покрытыми агентом гранулами, указанные гранулы и клетки впоследствии разделяют, а затем культивируют клетки. В альтернативном варианте реализации перед культивированием покрытые агентом гранулы и клетки не разделяют, а культивируют вместе. В дополнительном варианте реализации гранулы и клетки сначала концентрируют путем применения некоторой силы, такой как магнитная сила, что приводит к повышенному лигированию маркеров поверхности клетки, тем самым вызывая стимуляцию клеток.
[00265] В качестве примера, белки на поверхности клетки можно лигировать, позволяя парамагнитным гранулам, к которым присоединены антитела против CD3 и против CD28 (гранулы 3x28), контактировать с Т-клетками. В одном варианте реализации клетки (например, от 104 до 109 Т-клеток) и гранулы (например, парамагнитные гранулы М-450 CD3/CD28 Т DYNABEADS® при отношении 1:1, или MicroBeads MACS® от Miltenyi Biotec) объединяют в буфере, например, ФБР (без двухвалентных катионов, таких как кальций и магний). Снова, специалисты со средней квалификацией в данной области легко поймут, что можно использовать любую концентрацию клеток. Например, целевая клетка может быть очень редкой в образце и может составлять лишь 0,01% образца, или весь образец (т.е. 100%) может содержать интересующую целевую клетку. Соответственно, любое количество клеток находится в рамках контекста настоящего изобретения. В некоторых вариантах реализации может потребоваться значительно уменьшить объем, в котором смешивают частицы и клетки (т.е. увеличить концентрацию клеток), чтобы гарантировать максимальный контакт клеток и частиц. Например, в одном варианте реализации используют концентрацию, составляющую приблизительно 2 миллиарда клеток/мл. В другом варианте реализации используют более 100 миллионов клеток/мл. В дополнительном варианте реализации используют концентрацию клеток, составляющую 10, 15, 20, 25, 30, 35, 40, 45 или 50 миллионов клеток/мл. В еще одном варианте реализации используют концентрацию клеток, составляющую 75, 80, 85, 90, 95 или 100 миллионов клеток/мл. В дополнительных вариантах реализации можно использовать концентрации, составляющие 125 или 150 миллионов клеток/мл. Использование высоких концентраций может привести к повышенному выходу клеток, активации клеток и размножению клеток. Кроме того, использование высоких концентраций клеток позволяет более эффективный захват клеток, которые могут слабо экспрессировать целевые интересующие антигены, таких как CD28-отрицательные Т-клетки. Такие популяции клеток могут представлять терапевтическую ценность, и может потребоваться их получить в некоторых вариантах реализации. Например, использование высокой концентрации клеток позволяет более эффективную селекцию CD8+ Т-клеток, у которых обычно более слабая экспрессия CD28.
[00266] В одном варианте реализации, описанном в данной заявке, смесь можно культивировать в течение от нескольких часов (приблизительно 3 часов) до приблизительно 14 дней, или любое кратное часу целое значение между указанными значениями. В другом варианте реализации смесь можно культивировать в течение 21 дня. В одном варианте реализации настоящего изобретения гранулы и Т-клетки культивируют совместно в течение приблизительно восьми дней. В другом варианте реализации гранулы и Т-клетки культивируют совместно в течение 2-3 дней. Также может потребоваться несколько циклов стимуляции, так что время культивирования Т-клеток может составить 60 дней или более. Условия, подходящие для культивирования Т-клеток, включают подходящие среды (например, минимальную питательную среду, или среду RPMI 1640, или Х-vivo 15 (Lonza)), которые могут содержать факторы, необходимые для пролиферации и поддержания жизнеспособности, включая сыворотку (например, эмбриональную бычью сыворотку или сыворотку человека), интерлейкин-2 (IL-2), инсулин, IFN-гамма, IL-4, IL-7, GM-CSF, IL-10, IL-12, IL-15, TGF-бета и TNF-альфа, или любые другие вспомогательные вещества для роста клеток, известные квалифицированному специалисту. Другие вспомогательные вещества для роста клеток включают, но не ограничены перечисленными: поверхностно-активное вещество, плазманат и восстанавливающие агенты, такие как N-ацетилцистеин и 2-меркаптоэтанол. Среды могут включать RPMI 1640, AIM-V, DMEM, MEM, альфа-MEM, F-12, Х-Vivo 15 и Х-Vivo 20, Optimizer, с добавленными аминокислотами, пируватом натрия и витаминами, либо бессывороточные, либо дополненные подходящим количеством сыворотки (или плазмы) или определенным набором гормонов, и/или количеством цитокина(-ов), достаточным для роста и размножения Т-клеток. Антибиотики, например, пенициллин и стрептомицин, добавляют только в экспериментальные культуры, но не в культуры клеток, которые предназначены для введения путем инфузии субъекту. Клетки-мишени поддерживаются при условиях, необходимых для поддержания роста, например, при подходящей температуре (например, 37°С) и атмосфере (например, воздух плюс 5% СО2).
[00267] Т-клетки, которые подвергли стимуляции в течение различных периодов времени, могут проявлять различные свойства. Например, обычная кровь или продукты афереза - мононуклеарные клетки периферической крови - содержат популяцию хелперных Т-клеток (Тн, CD4+), которая больше, чем популяция цитотоксических или супрессорных Т-клеток (Тс, CD8+). Размножение Т-клеток ex vivo путем стимуляции рецепторов CD3 и CD28 приводит к получению популяции Т-клеток, которая до приблизительно 8-9 дня состоит преимущественно из ТН-клеток, тогда как после приблизительно 8-9 дня указанная популяция Т-клеток содержит все возрастающую популяцию ТС-клеток. Соответственно, в зависимости от цели лечения, введение путем инфузии субъекту популяции Т-клеток, содержащей преимущественно Тн-клетки, может быть предпочтительным. Аналогично, если была выделена субпопуляция антигенспецифичных ТС-клеток, может быть предпочтительным размножить данную субпопуляцию до большей степени.
[00268] Кроме того, дополнительно к маркерам CD4 и CD8, другие фенотипические маркеры значительно изменяются, но, по большей части, воспроизводимо в ходе процесса размножения клеток. Следовательно, такая воспроизводимость дает возможность приспособить продукт активированных Т-клеток для определенных целей.
[00269] В некоторых случаях эффекторные иммунные клетки согласно вариантам реализации (например, Т-клетки) культивируют совместно с активирующими и размножающими клетками (АиРК), чтобы способствовать размножению клеток. АиРК также могут называть искусственными антигенпрезентирующими клетками (иАПК). Например, антигенпрезентирующие клетки (АПК) пригодны для получения терапевтических композиций и продуктов клеточной терапии согласно вариантам реализации. В одном аспекте АиРК могут представлять собой генетически модифицированные клетки К562. Общее руководство, касающееся получения и применения антигенпрезентирующих систем, см., например, в патентах США №6,225,042, 6,335,479, 6,362,001 и 6,790,662; публикациях заявок на патент США №2009/0017000 и 2009/0004142; и международной публикации №WO2007/103009, каждый из которых включен в данную заявку посредством ссылки. В еще одном дополнительном аспекте вариантов реализации культивирование генетически модифицированных CAR-клеток включает культивирование генетически модифицированных CAR-клеток в присутствии дендритных клеток или активирующих и размножающих клеток (АиРК), которые стимулируют размножение экспрессирующих CAR эффекторных иммунных клеток. В еще дополнительных аспектах АиРК содержат связывающее CAR антитело или фрагмент антитела, экспрессированный на поверхности АиРК. АиРК могут содержать дополнительные молекулы, которые активируют или костимулируют Т-клетки в некоторых случаях. Дополнительные молекулы могут в некоторых случаях включать связанные с мембраной цитокины Сγ. В еще дополнительных аспектах АиРК инактивируют или облучают, или исследуют на наличие и подтверждают отсутствие инфекционного материала. В еще дополнительных аспектах культивирование генетически модифицированных CAR-клеток в присутствии АиРК включает культивирование генетически модифицированных CAR-клеток в среде, содержащей растворимые цитокины, такие как IL-15, IL-21 и/или IL-2. Клетки можно культивировать при отношении, составляющем от приблизительно 10:1 до приблизительно 1:10; от приблизительно 3:1 до приблизительно 1:5; от приблизительно 1:1 до приблизительно 1:3 (эффекторных иммунных клеток к АиРК); или любой диапазон, который можно вывести из него. Например, совместную культуру Т-клеток и АиРК можно вести при отношении, равном приблизительно 1:1, приблизительно 1:2 или приблизительно 1:3.
[00270] В одном аспекте АиРК могут экспрессировать CD137L. В некоторых аспектах АиРК могут дополнительно экспрессировать антиген, на который нацелена CAR-клетка, например, MUC16 (полноразмерный, укороченный или любой его вариант). В других аспектах АиРК могут дополнительно экспрессировать CD64, CD86 или mIL15. В некоторых аспектах АиРК могут экспрессировать по меньшей мере один клон антитела против CD3, такой как, например, ОКТЗ и/или UCHT1. В одном аспекте АиРК могут быть инактивированы (например, облучены). В одном аспекте АиРК могли исследовать на наличие и подтвердили отсутствие инфекционного материала. Способы получения таких АиРК известны в данной области. В одном аспекте культивирование CAR-модифицированной популяции Т-клеток с АиРК может включать культивирование клеток при отношении от приблизительно 10:1 до приблизительно 1:10; от приблизительно 3:1 до приблизительно 1:5; от приблизительно 1:1 до приблизительно 1:3 (Т-клетокк АиРК); или любой диапазон, полученный из указанных. Например, совместная культура Т-клеток и АиРК может быть при отношении приблизительно 1:1, приблизительно 1:2 или приблизительно 1:3. В одном аспекте этап культивирования может дополнительно включать культивирование с аминобисфосфонатом (например, золедроновой кислотой).
[00271] В одном аспекте популяцию генетически модифицированных CAR-клеток незамедлительно вводят путем инфузии субъекту или криоконсервируют. В другом аспекте популяцию генетически модифицированных CAR-клеток помещают в раствор цитокинов перед инфузией субъекту. В дополнительном аспекте популяцию генетически модифицированных CAR-клеток культивируют и/или стимулируют в течение не более 1, 2, 3, 4, 5, 6, 7, 14, 21, 28, 35 42 дней, 49, 56, 63 или 70 дней. В варианте реализации стимуляция включает совместное культивирование генетически модифицированных CAR-Т-клеток с АиРК, чтобы вызвать рост CAR-положительных Т-клеток. В другом аспекте популяцию генетически модифицированных CAR-клеток стимулируют не более чем: 1X стимуляцией, 2Х стимуляцией, 3Х стимуляцией, 4Х стимуляцией, 5Х стимуляцией, 5Х стимуляцией, 6Х стимуляцией, 7Х стимуляцией, 8Х стимуляцией, 9Х стимуляцией или 10Х стимуляцией. В некоторых случаях генетически модифицированные клетки не культивируют ex vivo в присутствии АиРК. В некоторых конкретных случаях способ согласно варианту реализации дополнительно включает обогащение популяции клеток экспрессирующими CAR эффекторными иммунными клетками (например, Т-клетками) после этапа трансфекции и/или культивирования. Обогащение может включать сортировку клеток с возбуждением флуоресценции (FACS), чтобы отсортировать экспрессирующие CAR клетки. В дополнительном аспекте сортировка экспрессирующих CAR клеток включает применение связывающего CAR антитела. Обогащение также может включать обеднение CD56+ клетками. В еще одном дополнительном аспекте варианта реализации способ дополнительно включает криоконсервирование образца популяции генетически модифицированных CAR-клеток.
[00272] В некоторых случаях АиРК инкубируют с пептидом оптимальной длины, которая позволяет непосредственное связывание пептида с молекулой ГКГС без дополнительного процессинга. В качестве альтернативы клетки могут экспрессировать интересующий антиген (т.е. в случае ГКГС-независимого распознавания антигена). Более того, в некоторых случаях АПК могут экспрессировать антитело, которое связывается либо с определенным полипептидом CAR, либо с полипептидами CAR вообще (например, универсальная активирующая и размножающая клетка (уАиРК)). Такие способы описаны в WO/2014/190273, который включен в данную заявку посредством ссылки. Дополнительно к молекулам пептид-ГКГС или интересующим антигенам, системы АиРК также могут содержать по меньшей мере одну экзогенную вспомогательную молекулу. Можно использовать любое подходящее количество и комбинацию вспомогательных молекул. Вспомогательную молекулу можно выбрать из таких вспомогательных молекул, как костимулирующие молекулы и молекулы адгезии. Примеры костимулирующих молекул включают CD70 и В7.1 (В7.1 ранее был известен как В7 и также известен как CD80), которые, среди прочих, связываются с молекулами CD28 и/или CTLA-4 на поверхности Т-клеток, тем самым влияя, например, на размножение Т-клеток, дифференцировку ТЫ, кратковременное выживание Т-клеток и секрецию цитокина, такого как интерлейкин (IL)-2. Молекулы адгезии могут включать связывающие углеводы гликопротеины, такие как селектины, транс мембранные связывающие гликопротеины, такие как интегрины, кальций-зависимые белки, такие как кадгерины, и однократно пронизывающие мембрану трансмембранные белки суперсемейства иммуноглобулинов (Ig), такие как молекулы межклеточной адгезии (ICAM), которые вызывают, например, контакт клеток с клетками или клеток с матриксом. Примеры молекул адгезии включают LFA-3 и 1С AM, такие как ICAM-1. Методики, способы и реагенты, пригодные для селекции, клонирования, получения и экспрессии типичных вспомогательных молекул, включая костимулирующие молекулы и молекулы адгезии, приведены в качестве примера, например, в патентах США №6,225,042, 6,355,479 и 6,362,001, включенных в данную заявку посредством ссылки.
[00273] Клетки, которые выбирают для получения АиРК, предпочтительно имеют дефекты во внутриклеточном процессинге антигенов, внутриклеточном транспорте пептидов и/или внутриклеточной загрузке пептидов на молекулы ГКГС I класса или II класса, или являются пойкилотермическими (т.е. менее чувствительны к температурному воздействию, чем линии клеток млекопитающих), или проявляют как дефекты, так и пойкилотермические свойства. Предпочтительно, у клеток, которые выбирают для получения АиРК, также отсутствует способность экспрессировать по меньшей мере один эндогенный эквивалент (например, эндогенную молекулу ГКГС I класса или II класса и/или эндогенные вспомогательные молекулы, описанные выше) компонентов экзогенной молекулы ГКГС I класса или II класса и вспомогательной молекулы, которые внедряют в клетки. Более того, АиРК предпочтительно сохраняют дефекты и пойкилотермические свойства, которыми обладали клетки перед их модификацией для получения АиРК. Примеры АиРК либо представляют собой, либо получены из линии клеток с дефектом в транспортерах, связанных с процессингом антигена (ТАР), такой как линия клеток насекомого. Типичной пойкилотермической линией клеток насекомого является линия клеток Drosophila, такая как линия клеток Schneider 2 (см., например, Schneider 1972, Illustrative methods for the preparation, growth, and culture of Schneider 2 cells, предложены в патентах США №6,225,042, 6,355,479 и 6,362,001).
[00274] В одном варианте реализации АиРК также подвергают циклу замораживания-размораживания. В типичном цикле замораживания-размораживания, АиРК можно заморозить путем приведения в контакт подходящей емкости, содержащей АиРК, с подходящим количеством жидкого азота, твердого диоксида углерода (т.е. сухого льда) или аналогичного низкотемпературного материала, так что быстро происходит замораживание. Замороженные АПК затем размораживают, либо путем удаления АиРК из низкотемпературного материала и воздействия условий комнатной температуры, либо путем содействия процессу размораживания, при котором используют баню с водой комнатной температуры или тепло рук, чтобы способствовать меньшему времени размораживания. Кроме того, АиРК можно заморозить и хранить в течение более длительного периода времени перед размораживанием. Замороженные АиРК также можно разморозить, а затем лиофилизировать перед дальнейшим применением. Предпочтительно, консерванты, которые могут негативно влиять на процедуры замораживания-размораживания, такие как диметилсульфоксид (ДМСО), полиэтиле нглико л и (ПЭГ) и другие консерванты, отсутствуют в средах, содержащих АиРК, которые подвергают циклу замораживания-размораживания, или по существу удалены, например, путем переноса АиРК в среды, которые по существу не содержат такие консерванты.
[00275] В дополнительных вариантах реализации ксеногенная нуклеиновая кислота и нуклеиновая кислота, эндогенная для АиРК, может быть инактивирована путем перекрестного связывания, так что по существу не происходит рост клетки, репликация или экспрессия нуклеиновой кислоты после инактивации. В одном варианте реализации АиРК инактивируют в момент времени после экспрессии экзогенных молекул ГКГС и вспомогательных молекул, представления таких молекул на поверхности АиРК и нагрузки представленных молекул ГКГС выбранным пептидом или пептидами. Соответственно, такие инактивированные и нагруженные выбранным пептидом АиРК, хотя их сделали по существу неспособными пролиферировать или реплицироваться, сохраняют функцию представления выбранного пептида. Предпочтительно, перекрестное связывание также позволяет получить АиРК, которые по существу свободны от контаминирующих микроорганизмов, таких как бактерии и вирусы, без значительного снижения функции АиРК как антигенпрезентирующих клеток. Таким образом, перекрестное связывание позволяет сохранить важные функции АиРК, при этом помогая уменьшить опасения относительно безопасности продукта клеточной терапии, разработанного с применением АиРК. Способы, относящиеся к перекрестному связыванию и АиРК, см., например, в публикации заявки на патент США №20090017000, которая включена в данную заявку посредством ссылки.
[00276] В некоторых вариантах реализации дополнительно предложена сконструированная антигенпрезентирующая клетка (АПК). Такие клетки можно применять, например, как описано выше, для размножения эффекторных иммунных клеток ex vivo. В дополнительных аспектах сконструированные АПК можно сами по себе вводить пациенту и тем самым стимулировать размножение эффекторных иммунных клеток in vivo. Сконструированные АПК согласно вариантам реализации настоящего изобретения можно сами по себе применять в качестве терапевтического агента. В других вариантах реализации сконструированные АПК можно применять в качестве терапевтического агента, который может стимулировать активацию эндогенных эффекторных иммунных клеток, специфичных к целевому антигену, и/или повышать активность или сохранение адоптивно перенесенных эффекторных иммунных клеток, специфичных к целевому антигену.
[00277] В данной заявке термин «сконструированная АПК» относится к клетке(-ам), которая(-ые) содержит(-ат) по меньшей мере первый трансген, причем указанный первый трансген кодирует HLA. Такие сконструированные АПК могут дополнительно содержать второй трансген для экспрессии антигена, так что указанный антиген представлен на поверхности АПК в комплексе с HLA. В некоторых аспектах сконструированная АПК может относиться к типу клеток, который представляет антигены (например, дендритным клеткам). В дополнительных аспектах сконструированную АПК можно получить из типа клеток, который обычно не представляет антигены, такого как Т-клетка или предшественник Т-клетки (называют «Т-АПК»). Таким образом, в некоторых аспектах сконструированная АПК согласно вариантам реализации содержит первый трансген, кодирующий целевой антиген, и второй трансген, кодирующий антиген лейкоцитов человека (HLA), так что HLA экспрессируется на поверхности сконструированной АПК в комплексе с эпитопом целевого антигена. В некоторых конкретных аспектах HLA, который экспрессируется в сконструированной АПК, представляет собой HLA-A2.
[00278] В некоторых аспектах сконструированная АПК согласно вариантам реализации может дополнительно содержать по меньшей мере третий трансген, кодирующий костимулирующую молекулу. Ко стимулирующая молекула может представлять собой костимулирующий цитокин, который может представлять собой связанный с мембраной цитокин Сγ. В некоторых аспектах костимулирующий цитокин представляет собой IL-15, такой как связанный с мембраной IL-15. В некоторых дополнительных аспектах сконструированная АПК может содержать отредактированный ген (или ген может быть удален). Например, ингибиторный ген, такой как PD-1, LIM-3, CTLA-4 или TCR, может быть отредактирован, чтобы снизить или устранить экспрессию гена. Сконструированная АПК согласно вариантам реализации может дополнительно содержать трансген, кодирующий любой интересующий целевой антиген.
Место предоставления медицинских услуг
[00279] В одном варианте реализации настоящего изобретения эффекторные иммунные клетки, описанные в данной заявке, модифицируют на месте предоставления медицинских услуг. В некоторых случаях модифицированные эффекторные иммунные клетки также называют сконструированными Т-клетками. В некоторых случаях место предоставления медицинских услуг находится в больнице или в учреждении (например, в медицинском учреждении) поблизости от нуждающегося в лечении субъекта. Субъекта подвергают аферезу, и мононуклеарные клетки периферической крови (МКПК) или субпопуляцию МКПК можно обогатить, например, путем элютриации или разделения в фиколле. Обогащенные МКПК или субпопуляцию МКПК можно криоконсервировать в любом подходящем растворе для криоконсервации перед дальнейшей обработкой. В одном случае процесс элютриации осуществляют, применяя буферный раствор, содержащий сывороточный альбумин человека. Эффекторные иммунные клетки, такие как Т-клетки, можно выделить с помощью способов селекции, описанных в данной заявке. В одном случае способ селекции Т-клеток включает использование гранул, специфичных к CD3, или гранул, специфичных к CD4 и CD8 на Т-клетках. В одном случае гранулы могут представлять собой парамагнитные гранулы. Собранные эффекторные иммунные клетки можно криоконсервировать в любом подходящем растворе для криоконсервации перед модификацией. Эффекторные иммунные клетки можно разморозить за 24 часа, 36 часов, 48 часов. 72 часа или 96 часов до инфузии. Размороженные клетки можно поместить в буфер для культивирования клеток, например, в буфер для культивирования клеток (например, RPMI), дополненный фетальной бычьей сывороткой (ФБС) или сывороткой АВ человека, или поместить в буфер, который содержит цитокины, такие как IL-2 и IL-21, перед модификацией. В другом аспекте собранные эффекторные иммунные клетки можно модифицировать незамедлительно, без необходимости криоконсервации.
[00280] В некоторых случаях эффекторные иммунные клетки модифицируют путем конструирования/внедрения химерного рецептора, одной или более меток клетки и/или цитокинов в эффекторные иммунные клетки, а затем быстро вводят путем инфузии субъекту. В некоторых случаях источники эффекторных иммунных клеток могут включать как аллогенные, так и аутологические источники. В одном случае эффекторные иммунные клетки могут представлять собой Т-клетки или NK-клетки. В одном случае химерный рецептор может представлять собой MUC16-CAR. В другом случае цитокин может представлять собой mbIL-15. В одном случае mbIL-15 имеет последовательность SEQ ID NO: 69, или ее вариант или фрагмент. В еще одном случае экспрессия mbIL-15 модулируется системами экспрессии на основе индуцируемого лигандом переключателя генов, описанными в данной заявке. Например, лиганд, такой как веледимекс, можно доставить субъекту, чтобы модулировать экспрессию mbIL-15. В другом случае цитокин может представлять собой IL-12. В еще одном случае экспрессия IL-12 модулируется системами экспрессии на основе индуцируемого лигандом переключателя генов, описанными в данной заявке. Например, лиганд, такой как веледимекс, можно доставить субъекту, чтобы модулировать экспрессию IL-12.
[00281] В другом аспекте веледимекс предоставлен в дозе 5 мг, 10 мг, 15 мг, 20 мг, 30 мг, 40 мг, 50 мг, 60 мг, 70 мг, 80 мг, 90 мг или 100 мг. В дополнительном аспекте предусмотрены более низкие дозы веледимекса, например, 0,5 мг, 1 мг, 5 мг, 10 мг, 15 мг или 20 мг. В одном варианте реализации веледимекс вводят субъекту за 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или 21 дней до инфузии модифицированных эффекторных иммунных клеток. В дополнительном варианте реализации веледимекс вводят субъекту приблизительно раз в 12 часов, приблизительно раз в 24 часа, приблизительно раз в 36 часов или приблизительно раз в 48 часов, в течение эффективного периода времени после инфузии модифицированных эффекторных иммунных клеток. В одном варианте реализации эффективный период времени для введения веледимекса составляет приблизительно: 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 дней. В других вариантах реализации веледимекс можно повторно вводить после периода отдыха, после перерыва в применении лекарств или когда у субъекта случается рецидив.
[00282] В некоторых случаях, когда наблюдается нежелательное явление у субъекта или когда нет потребности в лечении, метку клетки можно активировать, например, посредством цетуксимаба, для условного удаления in vivo модифицированных эффекторных иммунных клеток, содержащих метки клетки, такие как метки укороченного рецептора эпидермального фактора роста, описанные в данной заявке.
[00283] В некоторых вариантах реализации такие эффекторные иммунные клетки модифицируют с помощью конструкций, описанных на Фиг. 1-2, посредством электропорации. В одном случае электропорацию осуществляют с помощью устройства для электропорации, такого как устройства для электропорации Nucleofector™ от Lonza. В других вариантах реализации вектор, содержащий упомянутые выше конструкции, представляет собой невирусный или вирусный вектор. В одном случае невирусный вектор содержит систему транспозон-транспозаза Спящая красавица. В одном случае осуществляют электропорацию эффекторных иммунных клеток, применяя определенную последовательность. Например, в эффекторные иммунные клетки можно внедрить путем электропорации один транспозон, а затем ДНК, кодирующую транспозазу, а затем второй транспозон. В другом случае в эффекторные иммунные клетки можно внедрить путем электропорации все транспозоны и транспозазу одновременно. В другом случае в эффекторные иммунные клетки можно внедрить путем электропорации транспозазу, а затем оба транспозона или один транспозон за один раз. При проведении последовательных электропорации, эффекторные иммунные клетки могут находиться в покое в течение периода времени перед следующим этапом электропорации.
[00284] В некоторых случаях модифицированные эффекторные иммунные клетки не подвергают этапу размножения и активации. В некоторых случаях модифицированные эффекторные иммунные клетки не подвергают этапу инкубации или культивирования (например, размножения ex vivo). В некоторых случаях модифицированные эффекторные иммунные клетки помещают в буфер, который содержит IL-2 и IL21, перед инфузией. В других случаях модифицированные эффекторные иммунные клетки помещают в буфер или дают отдохнуть в буфере для культивирования клеток, например, в буфере для культивирования клеток (например, RPMI), дополненном фетальной бычьей сывороткой (ФБС), перед инфузией. Перед инфузией модифицированные эффекторные иммунные клетки можно собрать, промыть и поместить в солевой буфер при подготовке к инфузии субъекту.
[00285] В одном случае субъекту проводят лимфодеплецию (противолимфоцитарную терапию) перед инфузией. В других случаях лимфодеплеция не требуется, и модифицированные эффекторные иммунные клетки быстро вводят путем инфузии субъекту. Примеры режимов лимфодеплеции перечислены в Таблицах 2 и 3 ниже:


[00286] В дополнительном случае субъекта подвергали минимальной лимфодеплеции. Минимальная лимфодеплеция в данной заявке относится к сокращенному протоколу лимфодеплеции, такому что субъекту можно осуществлять введение путем инфузии в течение 1 дня, 2 дней или 3 дней после режима лимфодеплеции. В одном случае сокращенный протокол лимфодеплеции может включать более низкие дозы флударабина и/или циклофосфамида. В другом случае сокращенный протокол лимфодеплеции может включать более короткий период лимфодеплеции, например, 1 день или 2 дня.
[00287] В одном варианте реализации эффекторные иммунные клетки модифицируют путем конструирования/внедрения химерного рецептора и цитокина в указанные эффекторные иммунные клетки, а затем быстро вводят путем инфузии субъекту. В других случаях эффекторные иммунные клетки модифицируют путем конструирования/внедрения химерного рецептора и цитокина в указанные клетки, а затем вводят субъекту путем инфузии в течение по меньшей мере: 0, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23,24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49 или 50 часов. В других случаях эффекторные иммунные клетки модифицируют путем конструирования/внедрения химерного рецептора и цитокина в эффекторные иммунные клетки, а затем вводят субъекту путем инфузии в течение 0 дня, <1 дня, <2 дней, <3 дней, <4 дней, <5 дней, <6 дней или <7 дней.
[00288] В некоторых вариантах реализации некоторое количество модифицированных эффекторных клеток вводят нуждающемуся в этом субъекту, и указанное количество определяют на основании эффективности и способности вызывать связанную с цитокинами токсичность. В другом варианте реализации модифицированные эффекторные клетки представляют собой CAR+ и CD3+ клетки. В некоторых случаях количество модифицированных эффекторных клеток включает от приблизительно 104 до приблизительно 109 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает от приблизительно 104 до приблизительно 105 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает от приблизительно 105 до приблизительно 106 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает от приблизительно 106 до приблизительно 107 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает >104, но ≤105 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает >105, но ≤106 модифицированных эффекторных клеток/кг. В некоторых случаях количество модифицированных эффекторных клеток включает >106, но ≤107 модифицированных эффекторных клеток/кг.
[00289] В одном варианте реализации модифицированные эффекторные иммунные клетки нацелены на рак посредством региональной доставки непосредственно в опухолевую ткань. Например, при раке яичников модифицированные эффекторные иммунные клетки можно доставлять интраперитонеально (и/и) в живот или перитонеальную полость. Такую и/п доставку можно осуществить через порт или заранее установленный порт, помещенный для доставки химиотерапевтических средств. Другие способы региональной доставки модифицированных эффекторных иммунных клеток могут включать инфузию через катетер в полость резекции, внутриопухолевую инъекцию под контролем ультразвука, инфузию через печеночную артерию или внутриплевральную доставку.
[00290] В одном варианте реализации нуждающийся в этом субъект может начать терапию первой дозой модифицированных эффекторных иммунных клеток, доставленной и/п путем, а затем второй дозой модифицированных эффекторных иммунных клеток, доставленной в/в. В дополнительном варианте реализации за второй дозой модифицированных эффекторных иммунных клеток могут следовать последующие дозы, которые можно доставить в/в или и/п. В одном варианте реализации период времени между первой и второй или дополнительными последующими дозами может составлять приблизительно: 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 дней. В одном варианте реализации период времени между первой и второй или дополнительными последующими дозами может составлять приблизительно: 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35 или 36 месяцев. В другом варианте реализации период времени между первой и второй или дополнительными последующими дозами может составлять приблизительно: 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 лет.
[00291] В другом варианте реализации катетер можно поместить в очаг опухоли или метастазирования для дополнительного введения 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 доз модифицированных эффекторных иммунных клеток. В некоторых случаях дозы модифицированных эффекторных клеток могут содержать от приблизительно 102 до приблизительно 109 модифицированных эффекторных клеток/кг. В случаях, когда наблюдается токсичность, дозы модифицированных эффекторных клеток могут содержать от приблизительно 102 до приблизительно 105 модифицированных эффекторных клеток/кг. В некоторых случаях дозы модифицированных эффекторных клеток могут начинаться с приблизительно 102 модифицированных эффекторных клеток/кг и последующие дозы могут быть увеличены до приблизительно: 104, 105, 106, 107, 108 или 109 модифицированных эффекторных клеток/кг.
[00292] В других вариантах реализации способ стимуляции пролиферации и/или выживания сконструированных клеток включает получение образца клеток от субъекта и трансфекцию клеток из образца клеток одним или более полинуклеотидами, которые содержат один или более транспозонов. В одном варианте реализации транспозоны кодируют химерный антигенный рецептор (CAR), цитокин, один или более меток клетки и транспозазу, способную эффективно встраивать указанный один или более полинуклеотидов в геном указанных клеток с получением популяции сконструированных клеток. В варианте реализации транспозоны кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки, полипептиды переключателей генов для индуцируемого лигандом контроля цитокина и транспозазу, способную эффективно встраивать указанный один или более полинуклеотидов в геном указанных клеток с получением популяции сконструированных клеток. В варианте реализации полипептиды переключателей генов содержат i) первый полипептид переключателя генов, который содержит связывающий ДНК домен, слитый с первым лиганд-связывающим доменом ядерного рецептора, и ii) второй полипептид переключателя генов, который содержит трансактивирующий домен, слитый со вторым лиганд-связывающим доменом ядерного рецептора. В некоторых вариантах реализации первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером. В одном случае лимфодеплеция не требуется перед введением сконструированных клеток субъекту.
[00293] В одном случае способ размножения in vivo сконструированных клеток включает получение образца клеток от субъекта и трансфекцию клеток из образца клеток одним или более полинуклеотидами, которые содержат один или более транспозонов. В одном варианте реализации транспозоны кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки и транспозазу, способную эффективно встраивать указанный один или более полинуклеотидов в геном указанных клеток с получением популяции сконструированных клеток. В варианте реализации транспозоны кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки, полипептиды переключателей генов для индуцируемого лигандом контроля цитокинов и транспозазу, способную эффективно встраивать указанный один или более полинуклеотидов в геном указанных клеток, с получением популяции сконструированных клеток. В варианте реализации полипептиды переключателей генов содержат i) первый полипептид переключателя генов, который содержит связывающий ДНК домен, слитый с первым лиганд-связывающим доменом ядерного рецептора, и ii) второй полипептид переключателя генов, который содержит трансактивирующий домен, слитый со вторым лиганд-связывающим доменом ядерного рецептора. В некоторых вариантах реализации первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером. В одном случае лимфодеплеция не требуется перед введением сконструированных клеток субъекту.
[00294] В другом варианте реализации способ повышения сохранения сконструированных клеток in vivo у нуждающегося в этом субъекта включает получение образца клеток от субъекта и трансфекцию клеток из образца клеток одним или более полинуклеотидами, которые содержат один или более транспозонов. В некоторых случаях один или более транспозонов кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки и транспозазу, способную эффективно встраивать ДНК в геном указанных клеток с получением популяции сконструированных клеток. В некоторых случаях один или более транспозонов кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки, полипептиды переключателей генов для индуцируемого лигандом контроля цитокинов и транспозазу, способную эффективно встраивать ДНК в геном указанных клеток с получением популяции сконструированных клеток. В некоторых случаях полипептиды переключателей генов содержат: i) первый полипептид переключателя генов, который содержит связывающий ДНК домен, слитый с первым лиганд-связывающим доменом ядерного рецептора, и ii) второй полипептид переключателя генов, который содержит трансактивирующий домен, слитый со вторым лиганд-связывающим доменом ядерного рецептора, причем указанный первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером. В одном случае, лимфодеплеция не требуется перед введением сконструированных клеток субъекту.
[00295] В другом варианте реализации способ лечения субъекта с солидной опухолью включает получение образца клеток от субъекта, трансфекцию клеток из образца одним или более полинуклеотидами, которые содержат один или более транспозонов, и введение популяции сконструированных клеток субъекту. В одном случае лимфодеплеция не требуется перед введением сконструированных клеток субъекту. В некоторых случаях один или более транспозонов кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки и транспозазу, способную эффективно встраивать ДНК в геном клеток. В некоторых случаях один или более транспозонов кодируют химерный антигенный рецептор (CAR), цитокин, одну или более меток клетки, полипептиды переключателей генов для индуцируемого лигандом контроля цитокинов и транспозазу, способную эффективно встраивать ДНК в геном клеток. В некоторых случаях полипептиды переключателей генов содержат: i) первый полипептид переключателя генов, который содержит связывающий ДНК домен, слитый с первым лиганд-связывающим доменом ядерного рецептора, и ii) второй полипептид переключателя генов, который содержит трансактивирующий домен, слитый со вторым лиганд-связывающим доменом ядерного рецептора, причем указанный первый полипептид переключателя генов и второй полипептид переключателя генов соединены линкером. В некоторых случаях клетки трансфицируют посредством электропорации. В некоторых случаях полинуклеотиды, кодирующие полипептиды переключателей генов, модулируются промотором. В некоторых случаях промотор представляет собой тканеспецифичный промотор или промотор EF1A или его функциональный вариант. В некоторых случаях тканеспецифичный промотор содержит специфичный для Т-клеток элемент ответа или элемент ответа NFAT. В некоторых случаях цитокин включает по меньшей мере один из IL-1, IL-2, IL-15, IL-12, IL-21, слитый IL-15, IL-15R или вариант IL-15. В некоторых случаях цитокин находится в секретируемой форме. В некоторых случаях цитокин находится в связанной с мембраной форме. В некоторых случаях клетки представляют собой NK-клетки, NKT-клетки, Т-клетки или предшественники Т-клеток. В некоторых случаях клетки вводят субъекту (например, путем введения путем инфузии субъекту сконструированных клеток). В некоторых случаях способ дополнительно включает введение эффективного количества лиганда (например, веледимекса), чтобы индуцировать экспрессию цитокина. В некоторых случаях CAR способен связывать по меньшей мере MUC-16. В некоторых случаях транспозаза представляет собой Тс1-подобную транспозазу лососевых. В некоторых случаях транспозаза представляет собой транспозазу SB11 или SB100x. В других случаях транспозаза представляет собой PiggyBac. В некоторых случаях метка клетки включает по меньшей мере один из укороченного варианта HER1 или укороченного варианта CD20.
Применения в терапии.
[00296] В вариантах реализации, описанных в данной заявке, предложена эффекторная иммунная клетка (например, Т-клетка), трансдуцированная транспозоном(-ами) Спящая красавица и транспозазой Спящая красавица. Например, транспозон или транспозоны Спящая красавица могут содержать CAR, в котором объединен домен распознавания антигена MUC16 с доменом стебля шарнира CD8-альфа и его вариантами, внутриклеточным доменом CD3-дзета, CD28, 4-1ВВ или любыми их комбинациями и внутриклеточным доменом CD3-дзета, одной или более меток клетки, одним или более цитокинами и необязательно компонентами системы переключения генов, описанными в данной заявке. Следовательно, в некоторых случаях трансдуцированная Т-клетка может вызывать опосредованный CAR Т-клеточный ответ.
[00297] В вариантах реализации, описанных в данной заявке, предложено применение CAR для перенаправления специфичности первичной Т-клетки на антиген поверхности MUC16. Таким образом, в соответствии с настоящим изобретением также предложен способ стимулирования опосредованного Т-клетками иммунного ответа на целевую популяцию клеток или ткань у млекопитающего, включающий этап введения млекопитающему Т-клетки, которая экспрессирует CAR, причем CAR содержит связывающую группу, которая специфично взаимодействует с MUC16, домен стебля, часть цепи дзета, содержащую например, внутриклеточный домен CD3-дзета человека, и костимулирующую сигнальную область.
[00298] В одном варианте реализации настоящего изобретения предложена клеточная терапия, при которой Т-клетки генетически модифицируют, чтобы они экспрессировали специфичные к MUC16 CAR согласно настоящему изобретению, и CAR-T-клетку вводят путем инфузии нуждающемуся в этом реципиенту. Введенная путем инфузии клетка способна уничтожать клетки с повышенной экспрессией MUC16 у реципиента. В отличие от терапии антителами, CAR-T-клетки, описанные в данной заявке, способны реплицироваться in vivo, приводя к длительному их сохранению, что может приводить к продолжительному действию на опухолевые клетки.
[00299] Согласно настоящему изобретению дополнительно предложен способ обнаружения заболевания, при котором наблюдается сверхэкспрессия MUC16 у субъекта, включающий а) предоставление i) образца от субъекта, и ii) любого одного или более антител или их антигенсвязывающих фрагментов, которые описаны в данной заявке, b) приведение в контакт образца с антителом при условиях, подходящих для специфичного связывания антитела с его антигеном, и с) обнаружение повышенного уровня связывания антитела с образцом по сравнению с контрольным образцом, в котором нет заболевания, таким образом, приводя к обнаружению заболевания у субъекта. В одном варианте реализации заболевание представляет собой рак. В предпочтительном варианте реализации рак выбран из группы, состоящей из рака яичников и рака молочной железы. Без ограничения способа детектирования, в одном варианте реализации детектирование связывания антитела с образцом осуществляют иммуногистохимическим способом, твердофазным иммуноферментным анализом (ELISA), сортировкой клеток с возбуждением флуоресценции (FACS), вестерн-блоттингом, иммунопреципитацией и/или рентгенографической визуализацией.
[00300] Также в настоящей заявке предложен способ лечения заболевания, при котором наблюдается сверхэкспрессия MUC16, включающий введение субъекту, страдающему указанным заболеванием, терапевтически эффективного количества любого одного или более антител, или их антигенсвязывающих фрагментов, которые описаны в данной заявке. В одном варианте реализации заболевание представляет собой рак, например, рак яичников и рак молочной железы.
[00301] В одном варианте реализации MUC16-CAR-Т-клетки, описанные в данной заявке, могут претерпеть сильное размножение in vivo и могут сохраняться в течение более длительного периода времени. В другом варианте реализации CAR-T-клетки, описанные в данной заявке, могут развиться в специфичные Т-клетки памяти, которые могут повторно активироваться.
[00302] Модифицированные CAR Т-клетки, описанные в данной заявке, также могут служить в качестве типа вакцины для иммунизации ex vivo и/или терапии in vivo у млекопитающего. В вариантах реализации млекопитающее представляет собой человека. В отношении иммунизации ex vivo, перед введением эффекторной иммунные клетки млекопитающему происходит in vitro по меньшей мере одно из следующих: i) размножение клеток, ii) внедрение нуклеиновой кислоты, кодирующей CAR, в клетки, и/или iii) криоконсервация клеток.
[00303] Процедуры ex vivo хорошо известны и более подробно обсуждаются ниже. Вкратце, клетки выделяют из млекопитающего (например, человека) и генетически модифицируют (т.е., трансдуцируют или трансфицируют in vitro) вектором, экспрессирующим CAR, описанный в данной заявке. Модифицированную CAR клетку можно вводить млекопитающему реципиенту, чтобы предоставить терапевтическую пользу. Млекопитающий реципиент может представлять собой человека, и модифицированная CAR клетка может быть аутологичной по отношению к реципиенту. В качестве альтернативы, клетки могут быть аллогенными, сингенными или ксеногенными по отношению к реципиенту.
[00304] Процедуру размножения ex vivo гематопоэтических стволовых клеток и клеток предшественников, описанную в патенте США №5,199,942, включенном в данную заявку посредством ссылки, можно применять по отношению к клеткам согласно настоящему изобретению. Другие подходящие способы известны в данной области, следовательно, настоящее изобретение не ограничено каким-либо конкретным способом размножения клеток ex vivo. Вкратце, культивирование и размножение Т-клеток ex vivo включает: (1) сбор CD34+ гематопоэтических стволовых клеток и клеток предшественников из млекопитающего из собранной периферической крови или эксплантата костного мозга; и (2) размножение таких клеток ex vivo. Дополнительно к клеточным факторам роста, описанным в патенте США №5,199,942, другие факторы, такие как flt3-L, IL-1, IL-3 и лиганд c-kit, можно применять для культивирования и размножения клеток. [00305] Дополнительно к применению вакцины, основанной на клеточной системе, с точки зрения иммунизации ex vivo, в соответствии с настоящим изобретением также предложены композиции и способы иммунизации in vivo, чтобы вызвать иммунный ответ, направленный против антигена у пациента.
[00306] Как правило, клетки, активированные и размноженные, как описано в данной заявке, можно применять для лечения и предотвращения заболеваний, которые возникают у индивидов с иммунной недостаточностью. В частности, модифицированные CAR Т клетки согласно настоящему изобретению применяют для лечения MUC16-положительных злокачественных новообразований, таких как, например, MUC16. В некоторых вариантах реализации клетки согласно настоящему изобретению применяют для лечения пациентов, имеющих риск развития MUC16. Таким образом, способы лечения или предотвращения MUC16 включают введение нуждающемуся в этом субъекту терапевтически эффективного количества модифицированных CAR Т-клеток согласно настоящему изобретению. В вариантах реализации клетки, активированные и размноженные, как описано в данной заявке, можно применять для лечения MUC16.
[00307] Вкратце, фармацевтические композиции, описанные в данной заявке, могут содержать популяцию целевых клеток, описанных в данной заявке, в комбинации с одним или более фармацевтически или физиологически приемлемыми носителями, разбавителями или вспомогательными веществами. Такие композиции могут содержать буферы, такие как нейтральный буферный солевой раствор, фосфатно-солевой буферный раствор и тому подобные; углеводы, такие как глюкоза, манноза, сахароза или декстраны, маннит; белки; полипептиды или аминокислоты, такие как глицин; антиоксиданты; хелатирующие агенты, такие как ЭДТА или глутатион; адъюванты (например, гидроксид алюминий) и консерванты. В вариантах реализации композиции согласно настоящему изобретению находятся в форме для внутривенного введения.
[00308] Фармацевтические композиции, описанные в данной заявке, можно вводить способом, подходящим для заболевания, которое лечат (или которое предотвращают). Количество и частоту введения будут определять по таким факторам, как состояние пациента и тип и тяжесть заболевания пациента, хотя подходящие дозировки можно определить с помощью клинических испытаний.
[00309] Если указано «иммунологически эффективное количество» или «терапевтическое количество», то точное количество композиций, описанных в данной заявке, которое будут вводить, может определить врач с учетом индивидуальных различий в возрасте, массе тела и состоянии пациента (субъекта). В общем, может быть указано, что фармацевтическую композицию, содержащую Т-клетки, описанные в данной заявке, можно вводить при дозировке, равной от 104 до 109 клеток/кг массы тела, от 105 до 106 клеток/кг массы тела, включая все целые значения в данных диапазонах. Композиции Т-клеток также можно вводить множество раз в данных дозировках. Указанные клетки можно вводить, применяя методики инфузии, которые широко известны в иммунотерапии (см., например, Rosenberg и др., New Eng. J. of Med. 319:1676, (1988)). Оптимальную дозировку и схему лечения для конкретного пациента может легко определить специалист в области медицины путем контролирования признаков заболевания у пациента и соответствующей корректировки лечения.
[00310] В некоторых вариантах реализации может потребоваться вводить активированные Т-клетки субъекту, а затем впоследствии повторно брать кровь (или осуществлять аферез), активировать Т-клетки из нее и обратно вливать пациенту данные активированные и размноженные Т-клетки. Данный процесс можно осуществить множество раз каждые несколько недель. В некоторых вариантах реализации Т-клетки можно активировать из собранной крови от 10 см3 до 400 см3. В некоторых вариантах реализации Т-клетки активируют из собранной крови 20 см3, 30 см3, 40 см3, 50 см3, 60 см3, 70 см3, 80 см3, 90 см3 или 100 см3. Без привязки к теории, использование данного протокола множества сборов крови/множества повторных инфузии может привести к селективному удалению некоторых популяций Т-клеток. В другом варианте реализации может потребоваться вводить активированные Т-клетки из обсуждаемой композиции после лимфодеплеции у пациента, либо путем облучения, либо путем химиотерапии.
[00311] Введение композиций, описанных в данной заявке, можно осуществить любым удобным способом, например, путем аэрозольной ингаляции, инъекции, приема внутрь, переливания, имплантации или трансплантации. Композиции, описанные в данной заявке, можно вводить пациенту подкожно, внутрикожно, внутрь опухоли, внутрь лимфоузла, внутримедуллярно, внутримышечно, путем внутривенной (в/в) инъекции или интраперитонеально. В одном варианте реализации композиции Т-клеток согласно настоящему изобретению вводят пациенту путем внутрикожной или подкожной инъекции. В другом варианте реализации композиции MUC16-CAR-T-клеток согласно настоящему изобретению вводят путем в/в инъекции. Композиции Т-клеток можно вводить путем инъекции непосредственно в лимфатический узел или очаг первичной опухоли или метастаза.
[00312] Дозировка указанных выше способов лечения для введения пациенту будет изменяться в зависимости от точной природы состояния, которое лечат, и реципиента лечения. Масштабирование дозировок для введения человеку можно осуществить согласно общепринятой в данной области практике. Например, доза указанной выше терапии может находиться в диапазоне от 1×104 CAR+ клеток/кг до 5×106 CAR+ клеток/кг. Типичные дозы могут составлять 1×102 CAR+ клеток/кг, 1×103 CAR+ клеток/кг, 1×104 CAR+ клеток/кг, 1×105 CAR+ клеток/кг, 3×105 CAR+ клеток/кг, 1×106 CAR+ клеток/кг, 5×106 CAR+ клеток/кг, 1×107 CAR+ клеток/кг, 1×108 CAR+ клеток/кг или 1×109 CAR+ клеток/кг. Подходящую дозу можно скорректировать соответственно для взрослого пациента или ребенка.
[00313] В качестве альтернативы, обычное количество эффекторных иммунных клеток, которые вводят млекопитающему (например, человеку), может находиться, например, в диапазоне от ста, тысячи, десяти тысяч, миллиона до 100 миллиардов клеток; тем не менее количества ниже или выше данного типичного диапазона входят в объем настоящего изобретения. Например, доза клеток-хозяев согласно настоящему изобретению может составлять от приблизительно 1 миллиона до приблизительно 50 миллиардов клеток (например, приблизительно 5 миллионов клеток, приблизительно 25 миллионов клеток, приблизительно 500 миллионов клеток, приблизительно 1 миллиард клеток, приблизительно 5 миллиардов клеток, приблизительно 20 миллиардов клеток, приблизительно 30 миллиардов клеток, приблизительно 40 миллиардов клеток или диапазон, определяемый любыми двумя из предшествующих значений), от приблизительно 10 миллионов до приблизительно 100 миллиардов клеток (например, приблизительно 20 миллионов клеток, приблизительно 30 миллионов клеток, приблизительно 40 миллионов клеток, приблизительно 60 миллионов клеток, приблизительно 70 миллионов клеток, приблизительно 80 миллионов клеток, приблизительно 90 миллионов клеток, приблизительно 10 миллиардов клеток, приблизительно 25 миллиардов клеток, приблизительно 50 миллиардов клеток, приблизительно 75 миллиардов клеток, приблизительно 90 миллиардов клеток или диапазон, определяемый любыми двумя из предшествующих значений), от приблизительно 100 миллионов клеток до приблизительно 50 миллиардов клеток (например, приблизительно 120 миллионов клеток, приблизительно 250 миллионов клеток, приблизительно 350 миллионов клеток, приблизительно 450 миллионов клеток, приблизительно 650 миллионов клеток, приблизительно 800 миллионов клеток, приблизительно 900 миллионов клеток, приблизительно 3 миллиарда клеток, приблизительно 30 миллиардов клеток, приблизительно 45 миллиардов клеток или диапазон, определяемый любыми двумя из предшествующих значений).
[00314] Терапевтическую или профилактическую эффективность можно отслеживать путем периодической оценки получающих лечение пациентов. Для повторных введений в течение нескольких дней или более, в зависимости от состояния, лечение повторяют до того, как происходит желательное подавление симптомов заболевания. Тем не менее другие схемы введения доз могут быть пригодны и входят в объем настоящего изобретения. Желательную дозировку можно доставить путем разового болюсного введения композиции, путем множества болюсных введений композиции или путем непрерывного введения композиции путем инфузии.
[00315] Композицию, содержащую эффекторные иммунные клетки, экспрессирующие описанные последовательности нуклеиновых кислот, или вектор, содержащий указанные последовательности нуклеиновых кислот, можно вводить с одним или более дополнительными терапевтическими агентами, которые можно совместно вводить млекопитающему. Под «совместным введением» понимают введение одного или более дополнительных терапевтических агентов и композиции, содержащей клетки-хозяева согласно настоящему изобретению или вектор согласно настоящему изобретению, достаточно близко по времени, чтобы усилить эффект одного или более дополнительных терапевтических агентов, или наоборот. В этом отношении, композицию, содержащую эффекторные иммунные клетки, описанные в данной заявке, или вектор, описанный в данной заявке, можно вводить одновременно с одним или более дополнительными терапевтическими агентами, или первым, и один или более дополнительных терапевтических агентов можно вводить вторыми, или наоборот. В качестве альтернативы, композицию, содержащую описанные эффекторные иммунные клетки или векторы, описанные в данной заявке, и один или более дополнительных терапевтических агентов можно вводить одновременно.
[00316] Примерами терапевтических агентов, которые можно включить в состав или совместно вводить с композицией (или включить в наборы), содержащей клетки-хозяева согласно настоящему изобретению и/или векторы согласно настоящему изобретению, являются интерлейкины, цитокины, интерфероны, адъюванты и химиотерапевтические агенты. В вариантах реализации дополнительные терапевтические агенты представляют собой IFN-альфа, IFN-бета, IFN-гамма, GM-CSF, G-CSF, M-CSF, LT-бета, TNF-альфа, факторы роста и hGH, лиганд Toll-подобного рецептора человека TLR1, TLR2, TLR3, TLR4, TLR5, TLR6, TLR7, TLR8, TLR9 и TLR10.
[00317] «Противовспенивающие агенты» уменьшают вспенивание во время обработки, которое может привести к свертыванию водных дисперсий, пузырькам в готовой пленке или в целом нарушает обработку. Примеры противовспенивающих агентов включают кремниевые эмульсии или сорбитансесквиолеат.
[00318] «Антиоксиданты» включают, например, бутилированный гидрокситолуол (ВНТ), аскорбат натрия, аскорбиновую кислоту, метабисульфит натрия и токоферол. В некоторых вариантах реализации антиоксиданты повышают химическую стабильность, когда требуется.
[00319] В составах, описанных в данной заявке, могут быть полезны антиоксиданты, хелатирующие металл агенты, содержащие тиол соединения и другие общепринятые стабилизирующие агенты. Примеры таких стабилизирующих агентов включают, но не ограничены перечисленными: (а) от приблизительно 0,5% до приблизительно 2% (масса/объем) глицерина, (b) от приблизительно 0,1% до приблизительно 1% (масса/объем) метионина, (с) от приблизительно 0,1% до приблизительно 2% (масса/объем) монотиоглицерина, (d) от приблизительно 1 мМ до приблизительно 10 мМ ЭДТА, (е) от приблизительно 0,01% до приблизительно 2% (масса/объем) аскорбиновой кислоты, (f) от 0,003% до приблизительно 0,02% (масса/объем) полисорбата 80, (g) от 0,001% до приблизительно 0,05% (масса/объем) полисорбата 20, (h) аргинин, (i) гепарин, (j) сульфат декстрана, (k) циклодекстрины, (l) полисульфат пентозана и другие гепариноиды, (m) двухвалентные катионы, такие как магний и цинк; или (n) их комбинации.
[00320] «Связующие вещества» придают связующие свойства и включают, например, альгиновую кислоту и ее соли; производные целлюлозы, такие как карбоксиметилцеллюлоза, метилцеллюлоза (например, Метоцел®), гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза (например, Клуцел®), этилцеллюлоза (например, Этоцел®) и микрокристаллическая целлюлоза (например, Авицел®); микрокристаллическую декстрозу; амилозу; алюмосиликат магния; полисахаридные кислоты; бентониты; желатин; сополимер поливинилпирролидона/винилацетата; кросповидон; повидон; крахмал; прежелатинизированный крахмал; трагакант, декстрин, сахар, такой как сахароза (например, Дипак®), глюкоза, декстроза, меласса, маннит, сорбит, ксилит (например, Ксилитаб®) и лактоза; природную или синтетическую камедь, такую как акация, трагакант, камедь гхатти, слизь из шелухи семян подорожника, поливинилпирролидон (например, Поливидон® CL, Коллидон® CL, Полипласдон® XL-10), арабиногалактан лиственницы, Вигум®, полиэтиленгликоль, воски, альгинат натрия и тому подобные связующие вещества.
[00321] «Носитель» или «материалы-носители» включают любые широко применяемые в фармацевтике вспомогательные вещества, и их следует выбирать на оновании совместимости с соединениями, описанными в данной заявке, такими как соединения ибрутиниба и противораковый агент, и особенностей профиля высвобождения желательной лекарственной формы. Примеры материалов-носителей включают, например, связующие вещества, суспендирующие агенты, разрыхляющие агенты, наполнители, поверхностно-активные вещества, солюбилизаторы, стабилизаторы, лубриканты, смачивающие агенты, разбавители и тому подобные вещества. «Фармацевтически совместимые материалы-носители» могут включать, но не ограничены перечисленными: акацию, желатин, коллоидный диоксид кремния, глиуерофосфат кальция, лактат кальция, мальтодекстрин, глицерин, силикат магния, поливинилпирролидон (PVP), холестерин, эфиры холестерина, казеинат натрия, соевый лецитин, таурохолевую кислоту, фосфатидилхолин, хлорид натрия, трикальцийфосфат, дикалийфосфат, целлюлозу и конъюгаты целлюлозы, сахара, стеароиллактилат натрия, каррагенан, моноглицерид, диглицерид, прежелатинизированный крахмал и тому подобные носители. См., например, Remington: The Science and Practice of Pharmacy, 19 изд. (Истон, Пенсильвания: Mack Publishing Company, 1995); Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Истон, Пенсильвания 1975; Liberman, H.A. и Lachman, L., ред., Pharmaceutical Dosage Forms, Marcel Decker, Нью-Йорк, Нью-Йорк, 1980; и Pharmaceutical Dosage Forms and Drug Delivery Systems, седьмое изд. (Lippincott Williams & Wilkins, 1999).
[00322] «Диспергирующие агенты» и/или «модификаторы вязкости» включают материалы, которые контролируют диффузию и гомогенное состояние лекарственного средства посредством жидких сред, или способа гранулирования, или способа смешивания. В некоторых вариантах реализации данные агенты также способствуют эффективности покрывающей или размывающей матрицы. Примеры агентов, спопобствующих диффузии/диспергирующих агентов включают, например, гидрофильные полимеры, электролиты, твин® 60 или 80, ПЭГ, поливинилпирролидон (ПВП; коммерчески доступный под наименованием Пласдон®), и диспергирующие агенты на основе углеводов, такие как, например, гидроксипропилцеллюлозы (например, ГПЦ, ГПЦ-SL и ГПЦ-L), гидроксипропилметилцеллюлозы (например, ГПМЦ К100, ГПМЦ К4М, ГПМЦ К15М и ГПМЦ К100М), карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, фталат гидроксипропилметилцеллюлозы, стеарат ацетата гидроксипропилметилцеллюлозы (HPMCAS), некристаллическая целлюлоза, алюмосиликат магния, триэтаноламин, поливиниловый спирт (PVA), сополимер винилпирролидона/винилацетата (S630), полимер 4-(1,1,3,3-тетраметилбутил)фенола с оксидом этилена и формальдегидом (также известный как тилоксапол), полоксамеры (например, плюроники F68®, F88® и F108®, которые представляют собой блоксополимеры оксида этилена и оксида пропилена); и полоксамины (например, Тетроник 908®, также известный как Полоксамин 908®, который представляет собой тетрафункциональный блоксополимер, полученный путем последовательного добавления оксида пропилена и оксида этилена к этилендиамину (BASF Corporation, Парсиппани, Нью-Джерси)), поливинилпирролидон K12, поливинилпирролидон K17, поливинилпирролидон K25 или поливинилпирролидон K30, сополимер поливинилпирролидона/винилацетата (S-630), полиэтиленгликоль, например, полиэтиленгликоль с молекулярной массой от приблизительно 300 до приблизительно 6000, или от приблизительно 3350 до приблизительно 4000, или от приблизительно 7000 до приблизительно 5400, карбоксиметилцеллюлозу натрия, метилцеллюлозу, полисорбат-80, альгинат натрия, камеди, такие как, например, трагакант и гуммиарабик, гуаровая камедь, ксантаны, включая ксантановую камедь, сахара, целлюлозные полимеры, такие как, например, карбоксиметилцеллюлоза натрия, метилцеллюлоза натрия, карбоксиметилцеллюлоза, полисорбат-80, альгинат натрия, полиэтоксилированный сорбитанмонолаурат, полиэтоксилированный сорбитанмонолаурат, повидон, карбомеры, поливиниловый спирт (PVA), альгинаты, хитозаны и их комбинации. Пластификаторы, такие как целлюлоза или триэтилцеллюлоза, также можно применять в качестве диспергирующих агентов. Диспергирующие агенты, особенно пригодные в липосомальных дисперсиях и самоэмульгирующих дисперсиях, представляют собой димиристоилфосфатидилхолин, природный фосфатидилхолин из яиц, природный фосфатидилглицерин из яиц, холестерин и изопропилмиристат.
[00323] Комбинации одного или более веществ, способствующих размыванию, с одним или более веществом, способствующим диффузии, также можно применять в композициях согласно настоящему изобретению.
[00324] Термин «разбавитель» относится к химическим соединениям, которые применяют для разбавления интересующего соединения перед доставкой. Разбавители также можно применять для стабилизации соединений, так как они могут обеспечить более стабильную среду. Соли, растворенные в буферных растворах (которые также могут обеспечивать контроль или поддержание рН), применяют в качестве разбавителей в данной области, включая, но не ограничиваясь фосфатно-солевым буферным раствором. В некоторых вариантах реализации разбавители увеличивают объем композиции, чтобы способствовать прессованию или создать достаточный объем для гомогенной смеси для заполнения капсулы. Такие соединения включают, например, лактозу, крахмал, маннит, сорбит, декстрозу, микрокристаллическую целлюлозу, такую как Авицел®; двухосновный фосфат кальция, дигидрат дикальцийфосфата; трикальцийфосфат, фосфат кальция; безводную лактозу, высушенную распылением лактозу; прежелатинизированный крахмал, прессованный сахар, такой как ди-пак® (Amstar); маннит, гидроксипропилметилцеллюлозу, стеарат ацетата гидроксипропилметилцеллюлозы, разбавители на основе сахарозы, кондитерский сахар; одноосновный кальция сульфат моногидрат, кальция сульфат дигидрат; кальция лактат тригидрат, декстраты; гидролизированную твердую клетчатку, амилозу; измельченную в порошок целлюлозу, карбонат кальция; глицин, каолин; маннит, хлорид натрия; инозит, бентонит и тому подобные соединения.
[00325] «Наполнители» включают такие соединения, как лактоза, карбонат кальция, фосфат кальция, двхосновный фосфат кальция, сульфат кальция, микрокристаллическая целлюлоза, порошок целлюлозы, декстроза, декстраты, декстран, крахмалы, прежелатинизированный крахмал, сахароза, ксилит, лактитол, маннит, сорбит, хлорид натрия, полиэтиленгликоль и тому подобные соединения.
[00326] «Лубриканты» и «скользящие вещества» представляют собой соединения, которые предотвращают, уменьшают или ингибируют адгезию или трение материалов. Типичные лубриканты включают, например, стеариновую кислоту, гидроксид кальция, тальк, стеарилфумарат натрия, углеводород, такой как минеральное масло, или гидрогенизированное растительное масло, такое как гидрогенизированное соевое масло (Стеротекс®), высшие жирные кислоты и соли щелочных металлов и щелочно-земельных металлов, таких как алюминий, кальций, магний, цинк, стеариновую кислоту, стеараты натрия, глицерин, тальк, воски, Стеаровет®, борную кислоту, бензоат натрия, ацетат натрия, хлорид натрия, лейцин, полиэтиленгликоль (например, ПЭГ-4000) или метоксиполиэтиленгликоль, такой как Карбовакс™, олеат натрия, бензоат натрия, бегенат глицерина, полиэтиленгликоль, лаурилсульфат магния или натрия, коллоидный кремний, такой как Силоид™, Cab-O-Sil®, крахмал, такой как кукурузный крахмал, кремниевое масло, поверхностно-активное вещество и тому подобные лубриканты.
[00327] «Пластификаторы» представляют собой соединения, применяемые для размягчения микрокапсулирующего материала или пленочных покрытий, чтобы сделать их менее ломкими. Подходящие пластификаторы включают, например, полиэтиленгликоли, такие как ПЭГ 300, ПЭГ 400, ПЭГ 600, ПЭГ 1450, ПЭГ 3350 и ПЭГ 800, стеариновая кислота, пропиленгликоль, олеиновая кислота, триэтилцеллюлоза и триацетин. В некоторых вариантах реализации пластификаторы также могут функционировать как диспергирующие агенты или смачивающие агенты.
[00328] «Солюбилизаторы» включают такие соединения, как триацетин, триэтилцитрат, этилолеат, этилкаприлат, лаурилсульфат натрия, докузат натрия, витамин Е ТПГС, диметилацетамид, N-метилпирролидон, N-гидроксиэтилпирролидон, поливинилпирролидон, гидроксипропилметилцеллюлоза, гидроксипропилциклодекстрины, этанол, н-бутанол, изопропиловый спирт, холестерин, соли желчных кислот, полиэтиленгликоль 200-600, гликофурол, транскутол, пропиленгликоль и диметилизосорбид и тому подобные соединения.
[00329] «Стабилизаторы» включают такие соединения, как любые антиокислительные агенты, буферы, кислоты, консерванты и тому подобные соединения.
[00330] «Суспендирующие агенты» включают такие соединения, как поливинилпирролидон, например, поливинилпирролидон K12, поливинилпирролидон K17, поливинилпирролидон K25 или поливинилпирролидон K30, сополимер винилпирролидона/винил ацетата (S630), полиэтиленгликоль, например, молекулярная масса полиэтиленгликоля может составлять от приблизительно 300 до приблизительно 6000, или от приблизительно 3350 до приблизительно 4000, или от приблизительно 7000 до приблизительно 5400, карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, стеарат ацетата гидроксиметилцеллюлозы, полисорбат-80, гидроксиэтилцеллюлоза, альгинат натрия, камеди, такие как, например, трагакантовая камедь и гуммиарабик, гуаровая камедь, ксантаны, включая ксантановую камедь, сахара, целлюлозные полимеры, такие как, например, карбоксиметилцеллюлоза натрия, метилцеллюлоза, карбоксиметилцеллюлоза натрия, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза, полисорбат-80, альгинат натрия, полиэтоксилированный сорбитанмонолаурат, полиэтоксилированный сорбитанмонолаурат, повидон и тому подобные соединения.
[00331] «Поверхностно-активные вещества» включают такие соединения, как лаурилсульфат натрия, докузат натрия, твин 60 или 80, триацетин, витамин Е ТПГС, сорбитанмоноолеат, полиоксиэтиленсорбитана моноолеат, полисорбаты, полоксамеры, соли желчных кислот, глицерилмоностеарат, сополимеры оксида этилена и оксида пропилена, например, Плюроник® (BASF) и тому подобные соединения. Некоторые другие поверхностно-активные вещества включают полиоксиэтиленовые глицериды жирных кислот и растительные масла, например, полиоксиэтиленовое (60) гидрогенизированное касторовое масло; и полиоксиэтиленовые алкилэфиры и алкилфенилэфиры, например, октоксинол 10, октоксинол 40. В некоторых вариантах реализации поверхностно-активные вещества можно добавить, чтобы повысить физическую стабильность, или для других целей.
[00332] «Повышающие вязкость агенты» включают, например, метилцеллюлозу, ксантановую камедь, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, стеарат ацетата гидроксипропилметилцеллюлозы, фталат гидроксипропилметилцеллюлозы, карбомер, поливиниловый спирт, альгинаты, акацию, хитозаны и их комбинации.
[00333] «Смачивающие агенты» включают такие соединения, как олеиновая кислота, глицерилмоностеарат, сорбитанмоноолеат, сорбитанмонолаурат, триэтаноламинолеат, моноолеат полиоксиэтиленсорбитана, полиоксиэтиленсорбитанмонолаурат, докузат натрия, олеат натрия, лаурилсульфат натрия, докузат натрия, триацетин, твин 80, витамин Е ТПГС, соли аммония и тому подобные соединения.
НАБОРЫ И КОМПОЗИЦИИ
[00334] В одном аспекте настоящего изобретения предложены наборы и композиции, содержащие первый вектор, содержащий кодирующие области, которые кодируют специфичные к MUC16 CAR согласно настоящему изобретению, и необязательно гены, внедренные из соображений безопасности, например, HER1t или HER1t-1 и их функциональные варианты, или CD20 или CD20t-1, и их функциональные варианты. Наборы и композиции могут дополнительно содержать цитокины. В другом аспекте наборы и композиции могут содержать компоненты переключателя генов RHEOSWITCH®. Данные наборы и композиции могут содержать множество векторов, каждый из которых кодирует различные белки или субпопуляции белков. Данные векторы могут быть вирусными, невирусными, эписомальными или встраивающимися. В некоторых вариантах реализации векторы представляют собой транспозоны, например, транспозоны Спящая красавица.
[00335] В некоторых вариантах реализации наборы и композиции содержат не только векторы, но также клетки и агенты, такие как интерлейкины, цитокины, интерлейкины и химиотерапевтические вещества, адъюванты, смачивающие агенты или эмульгирующие агенты. В одном варианте реализации клетки представляют собой Т-клетки. В одном варианте реализации наборы и композиция содержат IL-2. В одном варианте реализации наборы и композиции содержат IL-21. В одном варианте реализации наборы и композиции содержат ингибиторы Bcl-2, STAT3 или STAT5. В вариантах реализации набор содержит IL-15 или mbIL-15.
[00336] В некоторых вариантах реализации предложены наборы и изделия для применения в одном или более способах, описанных в данной заявке. Такие наборы содержат носитель, упаковку или контейнер, который разделен на отсеки для вмещения одного или более контейнеров, таких как флаконы, пробирки и тому подобные контейнеры, каждый из контейнеров содержит один из отдельных элементов для применения в способе, описанном в данной заявке. Подходящие контейнеры включают, например, бутыли, флаконы, шприцы и пробирки. В одном варианте реализации контейнеры получают из различных материалов, таких как стекло или пластик.
[00337] Изделия, предложенные в данной заявке, содержат упаковочные материалы. Примеры фармацевтических упаковочных материалов включают, но не ограничены перечисленными: блистерные упаковки, бутыли, пробирки, мешки, контейнеры, бутыли и любой упаковочный материал, подходящий для выбранного состава и предполагаемого способа введения и лечения.
[00338] Например, контейнер(ы) содержит(-ат) CAR-T-клетки (например, специфичные к MUC16 CAR-T-клетки, описанные в данной заявке) и необязательно дополнительно содержит(-ат) цитокины и/или химиотерапевтические агенты, описанные в данной заявке. Такие наборы необязательно содержат идентифицирующее описание или этикетку или инструкции, касающиеся их применения в способах, описанных в данной заявке.
[00339] Набор обычно содержит этикетки, на которых перечислено содержание и/или инструкции по применению, и листок-вкладыш с инструкциями по применению. Комплект инструкций так же, как правило, входит в набор.
[00340] В некоторых вариантах реализации этикетка находится на контейнере или связана с контейнером. В одном варианте реализации этикетка находится на контейнере, когда буквы, цифры или другие символы, образующие этикетку, присоединены, отпрессованы или выгравированы на самом контейнере; этикетка связана с контейнером, когда она присутствует внутри емкости или держателя, который также удерживает контейнер, например, в виде листка-вкладыша. В одном варианте реализации этикетку используют для указания того, что содержимое следует применять для конкретного терапевтического применения. На этикетке также указаны руководства по применению содержимого, например, в способах, описанных в данной заявке.
ПРИМЕРЫ
[00341] Данные примеры предложены исключительно с целью пояснения и не предназначены для ограничения объема формулы изобретения, предложенной в данной заявке.
Пример 1. Нуклеофекция Т-клеток системой Спящая красавица.
[00342] Для получения генетически модифицированных Т-клеток, криоконсервированную общую популяцию Т-клеток размораживали, промывали и ресуспендировали в предварительно нагретой среде RPMI 1640 без фенолового красного, дополненной ФБС и Glutamax (среда R20), и помещали в термостат с контролем влажности при 37°С с 5% CO2. Клетки подсчитывали, центрифугировали и ресуспендировали в буфере для нуклеофекции. Для получения CAR-Т-клеток, всего 15 мкг плазмид(ы) с транспозонами, содержащих(-ей) конструкции CAR, объединяли с 5 мкг плазмиды, кодирующей транспозазу SB, в каждой реакции в кювете для нуклеофекции, содержащей определенное количество Т-клеток (обычно в диапазоне 5-40×106 на кювету). Электропорации Т-клеток добивались, применяя устройство для нуклеофекции Amaxa 2b или нуклеофектор 4D (Lonza, Уолкерсвилл, Мэриленд). После электропорации содержимое из каждой кюветы переносили в предварительно нагретые среды R20 и помещали в термостат при 37°С. Образец каждой культуры Т-клеток брали для анализа методом проточной цитометрии, чтобы охарактеризовать экспрессию CAR, HERlt и mbIL-15, в соответствующих случаях, в определенный момент времени. Для некоторых экспериментов CAR+ Т-клетки размножали ex vivo для дальнейшего определения характеристик. Для размножения ex vivo полученных CAR+ Т-клеток, Т-клетки дополнительно совместно культивировали с активирующими и размножающими клетками (АиРК). Вкратце, облученные АиРК, полученные из линии клеток K562, сконструированной для экспрессии CD86, 41BBL, mbIL15, наряду с укороченным антигеном MUC16 (MUC16t), совместно культивировали с CAR+T-клетками в полных средах с IL-21 и IL-2 с последующими еженедельными добавлениями АиРК.
[00343] Анализ методом проточной цитометрии экспрессии CAR, HER1t1 и mbIL15 проводили в день 1 после электропорации и перед каждой стимуляцией АиРК, применяя конъюгированный с Fluor 647 HiLyte™ рекомбинантный слитый белок MUC16t-Fc или белок L, меченый AF647, конъюгированный с фикоэритрином (РЕ) цетуксимаб и конъюгированные с флуоресцеинизотиоцианатом (FITC) антитела против IL-15 и против IL-15RA, соответственно.
Пример 2. Получение М1ТС16-САК-Т-клеток.
[00344] CAR-T-клетки, экспрессирующие MUC16-2 CAR, получали путем электропорации плазмидами с системой SB, как описано в примере 1. MUC16-2-CAR-HER1t1 Т-клетки получали путем электропорации Т-клеток человека плазмидой с транспозоном SB, кодирующей MUC16-2 CAR и HER1t1, и плазмидой с транспозазой SB11. MUC16-2-CAR-mbIL15-HER1t1 Т-клетки получали путем электропорации Т-клеток человека (1) плазмидой с транспозоном SB, кодирующей MUC16-2 CAR, mbIL15 и HER1t1, и (2) аплазмидой с транспозазой SB11. Проводили количественный анализ экспрессии CAR, mbIL15 и HER1t1, применяя многопараметрическую проточную цитометрию, в 1 день после нуклеофекции.
[00345] В Таблице 4 показана эффективность трансфекции, измеренная по % клеток, экспрессирующих трансгены в различных донорных Т-клетках после нуклеофекции плазмидами с системой SB, с применением транспозонов, экспрессирующих гены MUC16-2 CAR и HER1t1 (MUC16-2-CAR-HER1t1 Т-клетки) или MUC16-2 CAR, mbIL15 и HER1t1 (MUC16-2-CAR-mbIL15-HER1t1 Т-клетки), в 1 день после нуклеофекции. Дискриминационные окна устанавливали на популяции живых CD3+ клеток.
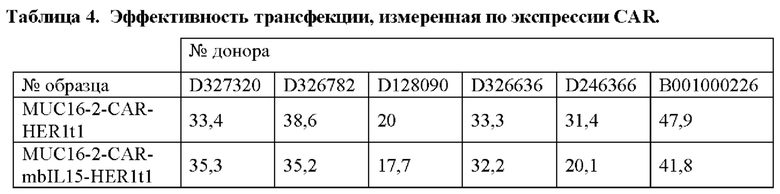
[00346] CAR-T-клетки, экспрессирующие MUC16-3-CAR, получали путем электропорации плазмидами с системой SB, как показано в примере 1. MUC16-3-CAR-HER1t1 Т-клетки получали путем электропорации Т-клеток человека плазмидой с транспозоном SB, кодирующей MUC16-3-CAR и HER1t1, и плазмидой с транспозазой SB11. MUC16-3-CAR-mbIL15-HER1t1 Т-клетки получали путем электропорации Т-клеток человека плазмидой с транспозоном SB, кодирующей MUC16-3-CAR, mbIL15 и HER1t1, и плазмидой с транспозазой SB11. Проводили количественный анализ экспрессии CAR, mbIL15 и HER1t1, применяя многопараметрическую проточную цитометрию, в 1 день после нуклеофекции.
[00347] По Фиг. 4 понятно, что Т-клетки, подвергнутые нуклеофекции либо плазмидой MUC16-3-HER1t1, либо плазмидой MUC16-3-mbIL15-HER1t1, экспрессируют трансгены, что подтверждают по экспрессии HER1t1 после инкубации в течение ночи после нуклеофекции. Отдельные экспериментальные точки для каждого донора показаны в Таблице 5.

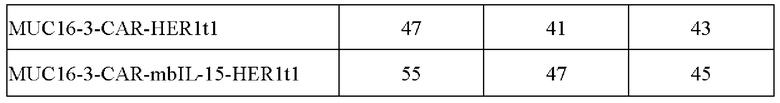
Пример 3. MUC16-CAR с различными длинами спейсера.
[00348] CAR-T-клетки, экспрессирующие MUC16-CAR с различными длинами спейсеров, полученных из шарнирных областей CD8-альфа, получали путем электропорации Т-клеток здоровых доноров плазмидами с системой SB (№ донора D133098), как описано в Примере 1. CAR-T-клетки размножали ex vivo путем совместного культивирования с экспрессирующими MUC16t АиРК путем стимуляции раз в неделю, как описано в Примере 1. Экспрессию CAR измеряли с помощью многопараметрической проточной цитометрии в 1 день и 8 день после нуклеофекции. Проанализированные испытуемые образцы CAR-T приведены в Таблице 6. На Фиг. 5 показаны результаты проточной цитометрии в отношении экспрессии MUC16-CAR различными MUC16-CAR-Т-клетками. Дискриминационные окна устанавливали на живые CD3+ клетки. На Фиг. 5 показано, что наблюдали изменяющиеся степени экспрессии MUC16-CAR через один день после переноса генов в зависимости от MUC16 scFv и спейсера, используемого для конструирования молекулы CAR. Обогащение CAR+ Т-клетками наблюдали при совместном культивировании CAR+ Т-клеток с линией клеток MUC16t+ АиРК in vitro. Для MUC16-CAR-Т-клеток, полученных из донора №D133098, лучшее обогащение CAR+T-клетками наблюдали с 1 дня по 8 день после электропорации с применением спейсера CD8a(3x) для MUC16-2 CAR и применением спейсера CD8a(2x) для MUC16-7 CAR.

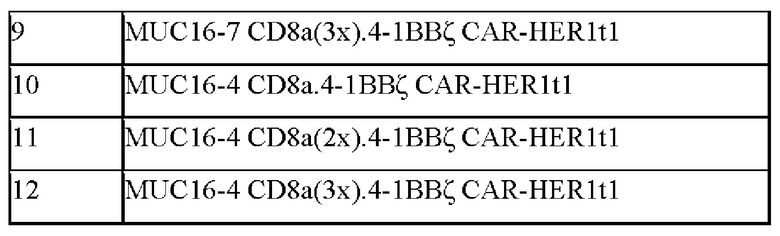
[00349] MUC16-3-CAR-HER1t1 и MUC16-3-mbIL15-HER1t1 Т-клетки, экспрессирующие MUC16-3-CAR с различными спейсерами, полученными из шарнирных областей CD8-альфа, получали путем электропорации Т-клеток здоровых доноров плазмидами с системой SB (№ донора D132552). CAR+Т-клетки размножали ex vivo путем совместного культивирования с экспрессирующими MUC16t АиРК путем стимуляции раз в неделю, как описан ранее. Экспрессию MUC16-3-CAR измеряли по окрашиванию белка MUC16-Fc, применяя многопараметрическую проточную цитометрию, в 1 день и 8 день после нуклеофекции. Конструкции CAR-T, которые оценивали, приведены в Таблице 7. На Фиг. 6 показаны результаты проточной цитометрии в отношении экспрессии MUC16-CAR различными MUC16-3-CAR-T-клетками. На Фиг. 6 показано, что наблюдали изменяющуюся степень экспрессии MUC16-CAR через один день после переноса генов в зависимости от спейсера, используемого для конструирования молекулы CAR. Наблюдали изменяющуюся степень обогащения CAR+T-клетками через восемь дней после переноса генов при совместном культивировании CAR+T-клеток с линией клеток MUC16t+ АиРК in vitro в зависимости от спейсера, используемого для конструирования молекулы CAR.

Пример 4. Вестерн-блоттинг.
[00350] Лизаты Т-клеток получали путем ресуспендирования осадков клеток в анализе методом радиоиммунопреципитации с добавлением ингибиторов протеаз. Осветленный лизат отделяли от клеточного экстракта и хранили криоконсервированным. Анализ с помощью бицинхониновой кислоты (ВСА) проводили, чтобы определить общую концентрацию белка и для нормировки среди образцов. Всего 10 мкг образца белка анализировали путем электрофореза в восстанавливающих условиях. Белковый материал из геля переносили на поливинилиденфторидные (ПВДФ) мембраны. Мембраны с перенесенным белком блокировали, а затем инкубировали с первичным антителом мыши против CD3ζ человека или против IL-15 на качающейся платформе. Мембрану промывали перед добавлением подходящего меченого пероксидазой хрена (HRP) вторичного антитела. Блоты получали, используя детектирование с помощью хемилюминесценции (ECL). Изображения вестерн-блоттинга получали с помощью системы визуализации FluorChem™ Е Imager.
[00351] Для обнаружения HER1t1 осуществляли способ иммунопреципитации с последующим вестерн-блоттингом. Анализировали дополнительные контроли, которые включали лизат клеток А431 (положительный контроль) и контроль иммунопреципитации (иммунопреципитация без лизата; отрицательный контроль). Белковый материал из геля переносили на мембраны ПВДФ. Мембраны с перенесенным белком блокировали, а затем инкубировали с первичным антителом мыши против EGFR человека. Мембрану промывали перед добавлением меченого пероксидазой хрена (HRP) антитела козы против антитела мыши. Изображения вестерн-блоттинга получали с помощью системы визуализации FluorChem™ Е Imager.
[00352] На Фиг. 7-9 показаны изображения вестерн-блотов с применением лизатов MUC16-3-CAR-HER1t1 Т-клеток и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток. Как показано на Фиг. 7, полосы MUC16-3-CAR детектировали в лизатах MUC16-3-CAR-HER1t1 Т-клеток и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток. Полосы нативного CD3ζ с более низкой молекулярной массой также детектировали, как и ожидалось, в лизатах CAR-T-клеток. Как показано на Фиг. 8, экспрессия белка mbIL15 была обнаружена только в лизате MUC16-3-CAR-mbIL15-HER1t1 Т-клеток, которые коэкспрессируют mbIL15 (Фиг. 8). На Фиг. 9 показана экспрессия HER1t1 с ожидаемой молекулярной массой приблизительно 40 кДа в MUC16-3-CAR-HER1U Т-клетках и MUC16-3-CAR-mbIL15-HER1t1 Т-клетках. Вкратце, полученные результаты демонстрируют, что Т-клетки, экспрессирующие MUC16-CAR, mbIL15 и HER1t, можно получить, применяя систему SB.
Пример 5. Цитотоксичность MUC16-3-CAR-T-клеток.
[00353] Цитотоксическую активность Т-клеток определили, применяя люминесцентный анализ жизнеспособности клеток. Специфичную цитотоксичность MUC16-3-CAR-mbIL15-HER1t1 клеток оценивали, применяя CAR+ Т-клетки, полученные, как описано выше. В MUC16-3-CAR-mbIL15-HER1t1, контрольных MUC16-3-CAR-HER1t1 Т-клетках и контрольных CAR-mbIL15-HER1t1 Т-клетках без MUC16 оценивали экспрессию MUC16-CAR, HER1t1 и mbIL-15. Эффекторные CAR-T-клетки идентифицировали по экспрессии HER1t1. Различные соотношения эффектор : мишень (Э:М) оценивали для линии клеток яичников, SKVO3 с эктопической экспрессией MUC16t (SKOV3- MUC16t), исходной линии клеток SKVO3, которая не экспрессирует MUC16, OVCAR3 с природной экспрессией MUC16 и не экспрессирующей MUC16 линии клеток А549. Супернатанты из культуры клеток хранили при -80°С до проведения анализа цитокинов. Процент цитотоксичности определяли, используя формулу ниже:
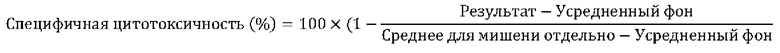
[00354] Специфичную цитотоксичность MUC16-3-CAR-T-клеток, полученных из Т-клеток трех здоровых доноров, по отношению к экспрессирующим MUC16 опухолевым мишеням продемонстрировали путем сравнения цитотоксической активности различных линий опухолевых клеток при различных соотношениях Э:М. CAR-T-клетки, экспрессирующие контрольные CAR, использовали в качестве отрицательного контроля. На Фиг. 10А показано, что MUC16t экспрессируется только опухолевыми клетками SKOV3-MUC16t. Эффекторные CAR-T-клетки (нормированные на основании клеточной экспрессии HER1t1) совместно культивировали с целевыми опухолевыми клетками при различных соотношениях Э:М. На Фиг. 10В показано, что как MUC16-3-CAR-HER1t1 Т-клетки (в которых нет mbIL15), так и MUC16-3-CAR-mbIL15-HER1t1 продемонстрировали сходную дозозависимую цитотоксичность против линий опухолевых клеток SKOV3-MUC16t и OVCAR3. Тем не менее, только MUC16-3-CAR-mbIL15-HER1t1 убивали OVCAR3 при более высоком отношении Э:М. Селективное уничтожение клеток OVCAR3 посредством MUC16-3-CAR-mbIL15-HER1t1 дает возможность предположить повышенную активацию Т-клеток среди модифицированных Т-клеток. Фоновый сигнал не был обнаружен в культуре меченых целевых клеток отдельно. Более того, специфичные к MUC16 CAR-T-клетки не уничтожали линии MUC16отр опухолевых клеток (SKOV3 и А549) и не наблюдали уничтожения какой-либо линии опухолевых клеток контрольными CAR-mbIL15-HER1t Т-клетками. В совокупности данные результаты демонстрируют, что MUC16-3-CAR-mbIL15-HER1t1 специфично опосредовали уничтожение экспрессирующих MUC16 линий опухолевых клеток.
Пример 6. Продукция цитокинов MUC16-3-CAR-Т-клетками.
[00355] Культуральные супернатанты из анализа цитотоксичности из Примера 5 подвергали скринингу, применяя специально изготовленные наборы множества аналитов для продукции цитокинов, включая IFNγ и гранзим В.
[00356] Перенацеленную специфичность MUC16-3-CAR-HER1t1 Т-клеток (без mbIL15) и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток в отношении экспрессирующих MUC16 опухолевых клеток дополнительно исследовали путем исследования секреции цитокинов при совместном культивировании с не экспрессирующими MUC16 и экспрессирующими MUC16 линиями опухолевых клеток. В данных исследованиях оценивали продукцию цитокинов MUC16-3-CAR-mbIL15-HER1t1 Т-клетками из 3 различных доноров при отношении Э:М 1:1 после совместного культивирования с линиями опухолевых клеток. На Фиг. 11 показано, что повышенные уровни провоспалительных цитокинов наблюдали только для линий опухолевых клеток, экспрессирующих MUC16t. Кроме того, экспрессия mbIL15 в MUC16-3-CAR-mbIL15-HER1t1 Т приводила к низкой продукции цитокинов по сравнению с уровнями, наблюдаемыми после тестирования MUC16-3-CAR-HER1t1 Т-клеток без mbIL15. Полученные результаты продемонстрировали, что MUC16-3-CAR-mbIL15-HER1t1 Т-клетки проявляют специфичную цитотоксическую функцию по отношению к экспрессирующим MUC16 опухолевым клеткам и показали, что коэкспрессия mbIL15 может снижать продукцию провоспалительных цитокинов, не нарушая цитотоксическое действие MUC16-3-CAR-mbIL15-HER1t1.
Пример 7. Специфичность MUC16-3-CAR-Т-клеток.
[00357] Цитотоксическую активность Т-клеток определяли, применяя люциферазный анализ. MUC16-CAR-Т-клетки (Таблица 8) наряду с контрольными CAR-T-клетками получали путем электропорации плазмидами с системой SB Т-клеток двух здоровых доноров (D326782 и D132552) и размножали путем совместного культивирования ex vivo с АиРК, как описано в Примере 1. Цитотоксичность оценивали при различных отношениях Э:М, используя линии клеток SKOV3-MUC16t, OVCAR3 и MUC16отр А549 в качестве клеток-мишеней в трех повторных лунках. Процент цитотоксичности определяли, используя формулу, описанную выше.

[00358] На Фиг. 12 показано, что MUC16-3-CAR-Т-клетки, коэкспрессирующие mbIL15 и HER1t1, проявляли специфичную цитотоксичность по отношению к линиям опухолевых клеток MUC16+ зависимым от концентрации образом. Ни одна из исследованных MUC16-CAR-T-клеток не проявляла значительную цитотоксичность по отношению к MUC16отр линиям опухолевых клеток А549. Клетки MUC16-3-CAR-mbIL15-HER1t1 со спейсером CD8a(2x) проявляли более высокую специфичную цитотоксичность по отношению к MUC16+ линиям опухолевых клеток по сравнению со спейсером CD8a в CAR-T-клетках, полученных из Т-клеток здоровых доноров, как показано.
Пример 8. Сохранение и отсутствие автономной пролиферации MUC16-CAR-T-клеток, экспрессирующих mbIL15.
[00359] Чтобы оценить влияние mbIL15 на сохранение CAR-Т-клеток, MUC16-3-CAR-HER1t1 Т- и MUC16-3-CAR-mbIL15-HER1t1 Т-клетки метили CellTrace™ Violet и совместно культивировали с аутологическими МКПК. Совместные культуры поддерживали в течение 14 дней. Во время культивирования клеток, образцы клеток оценивали для измерения жизнеспособности и окрашивали для проточной цитометрии для оценки CAR-Т-клеток и фенотипа памяти. Пролиферацию определяли путем разбавления красителя.
[00360] Оценка сохранения клеток показала, что MUC16-3-CAR-HER1t (без mbIL15) не сохранялись в культуре через две недели и только MUC16-3-CAR-mbIL15-HER1t1 Т-клетки были обнаружены в культуре, в которой нет цитокинов в день 14 (Фиг. 13А), демонстрируя роль mbIL15 в улучшенном сохранении CAR-T-клеток. Оценка возможности автономной пролиферации показала, что хотя MUC16-3-CAR-mbIL15-HER1t1 Т-клетки обнаружены в день 14, они не смогли пролиферировать, что продемонстрировали отсутствием дочерних клеток (Фиг. 13В). Более того, в день 14 в сохранившихся MUC16-3-CAR-mbIL15-HER1t1 Т-клетках выявили обогащение популяциями Т-клеток, подобными клеткам памяти или подобными клеткам в покоящемся состоянии, что определяли по более высоким уровням CD45RA+/CD45RO+ клеток по сравнению с днем -1 (Фиг. 13С).
[00361] MUC16-2-CAR-HER1t1 Т-клетки (которые не экспрессируют mbIL15) и MUC16-2-CAR-mbIL15-HER1t1 Т-клетки получали путем электропорации плазмидами с системой SB Т-клеток трех здоровых доноров. CAR-T-клетки размножали ex vivo путем еженедельной стимуляции АиРК. CAR-T-клетки культивировали в среде без экзогенных цитокинов в течение 2 недель. Рассчитывали количество жизнеспособных Т-клеток в культуре как часть исходного количества клеток, чтобы показать их сохранение.
[00362] На Фиг. 14 показано, что MUC16-2-CAR-mbIL15-HER1t1 Т-клетки, экспрессирующие mbIL15, могут сохраняться в культуре ex vivo в 15 день после удаления цитокинов, тогда как MUC16-2-CAR-HER1t1 Т-клетки, не экспрессирующие mbIL15, не выживали более 7 дней в отсутствие цитокинов.
[00363] Полученные результаты показали улучшенное сохранение MUC16-CAR-T-клеток, когда mbIL15 совместно экспрессировали с CAR.
Пример 9. Анализ АЗКЦ.
[00364] Аутологические клетки-естественные киллеры (NK) использовали в качестве эффекторных клеток в анализе АЗКЦ. Размноженные ex vivo MUC16-2-CAR-mbIL15-HER1t1 клетки использовали в качестве клеток-мишеней в данном анализе. Совместные культуры эффекторных клеток и клеток-мишеней создавали при отношении Э:М 10:1 в присутствии 10 мкг/мл цетуксимаба или ритуксимаба или без антитела. Жизнеспособность оценивали после совместного культивирования, применяя проточную цитометрию. Для того чтобы определить % АЗКЦ в отношении CAR+ Т-клеток, частичную утрату меченых CD3+ клеток определяли путем сравнения с исходной популяцией CAR+ Т-клеток.
[00365] На Фиг. 15 продемонстрировали, что MUC16-2-CAR-mbIL15-HER1t1 Т-клетки, полученные из Т-клеток трех различных здоровых доноров, эффективно уничтожались посредством АЗКЦ, когда цетуксимаб добавляли в культуру. Добавление антитела против CD20 - ритуксимаба (неспецифичного контроля) в культуру показало низкие фоновые уровни цитотоксичности, подтверждая специфичность опосредованной цетуксимабом АЗКЦ в отношении CAR-T-клеток. Результаты представлены в виде среднего +/- стандартная ошибка среднего.
Пример 10. Функциональная оценка MUC16-2-CAR-Т-клеток в модели рака яичников in vivo.
[00366] SKOV3-fLUC-MUC16 вводили и/п мышам NSG (сутки 0). На 6 день мышей с прижившейся опухолевой нагрузкой, что подтверждали посредством визуализации IVIS, произвольно делили на группы (n=5-7 мышей на группу) для введения однократной и/п инъекции либо: солевого раствора (HBSS), MUC16-2-CAR-HER1t1 Т-клеток (2×106 клеток/мышь), MUC16-2-CAR-mbIL15-HER1t1 Т-клеток (2×106 клеток/мышь), либо однократной в/в инъекции MUC16-2-CAR-mbIL15-HER1t1 Т-клеток (2×106 клеток/мышь). Эффективность против роста опухоли оценивали с помощью биолюминесцентной визуализации (IVIS) in vivo, которую проводили каждые 3-4 дней после введения дозы CAR-T-клеток, чтобы оценить опухолевую нагрузку. Общую безопасность оценивали путем оценки массы тела и с помощью клинических наблюдений, проводимых на протяжении всего исследования минимум 2-3 раза в неделю после введения CAR-T-клеток.
[00367] На Фиг. 16 показано, что однократная и/п или в/в инъекция MUC16-2-CAR-T-клеток эффективно уничтожала опухоль SKOV3-fLUC-MUC16 у мышей. Противоопухолевый ответ CAR-T-клеток, введенных путем в/в инъекции, был более поздним по сравнению с и/п инфузией.
Пример 11. Функциональная оценка MUC16-2-CAR-Т-клеток в модели рака яичников in vivo.
[00368] Опухолевые клетки SKOV3-fLUC-MUC16 вводили и/п мышам NSG в 0 день. На 5 день мышей с прижившейся опухолевой нагрузкой (что подтверждали посредством визуализации IVIS) произвольно делили на группы (n=5-7 мышей на группу) для введения однократной и/п инъекции либо: солевого раствора (HBSS), MUC16-3-CAR-HER1t1 Т-клеток (2×106 клеток/мышь), либо MUC16-3-CAR-mbIL15-HER1t1 Т-клеток (2×106 клеток/мышь). Эффективность против роста опухоли оценивали с помощью биолюминесцентной визуализации (IVIS) in vivo, которую проводили каждые 3-4 дней после введения дозы CAR-T-клеток, чтобы оценить опухолевую нагрузку. Образцы цельной крови в ЭДТА собирали раз в неделю и подвергали многопараметрической проточной цитометрии для оценки сохранения, размножения MUC16-CAR-Т-клеток и определения различных субпопуляций Т-клеток. В образцах плазмы анализировали цитокины человека как показатель активности Т-клеток. Общую безопасность оценивали путем оценки массы тела и с помощью клинических наблюдений, проводимых на протяжении всего исследования минимум 2-3 раза в неделю после введения CAR-T-клеток.
[00369] На Фиг. 17 показано, что и/п введение MUC16-3-CAR-mbIL15-HER1t1 Т-клеток мышам NSG, несущим экспрессирующие MUC16 опухоли SKOV-3, приводило к значимому уменьшению (уменьшению >3 log значения общего потока) опухолевой нагрузки по сравнению с контрольной группой, которой вводили солевой раствор. Коэкспрессия mbIL15 в MUC16-3-CAR-mbIL15-HER1t1 Т-клетках была связана со значительно большим уменьшением опухолевой нагрузки по сравнению с MUC16-3-CAR-HER1t1 Т-клетками без экспрессии mbIL15.
[00370] Показали улучшенное сохранение и размножение in vivo MUC16-3-CAR-mbIL15-HER1t1 Т-клеток, что продемонстрировали по повышенным количествам Т-клеток, экспрессирующих HER1t1 в крови по сравнению с MUC16-3-CAR-mbIL15-HER1t1 Т-клетками. Более того, как для CD4+, так и для CD8+ CAR-T-клеток показали размножение и сохранение in vivo. См. Фиг. 18А-В.
Пример 12. Ответ на дозу MUC16-CAR-Т-клеток в модели рака яичников in vivo.
[00371] SKOV3-fLUC-MUC16 вводили и/п мышам NSG в 0 день. На 6 день мышей с прижившейся опухолевой нагрузкой (что подтверждали посредством визуализации IVIS) произвольно делили на группы (n=5 мышей на группу) для введения однократной и/п инъекции либо: солевого раствора (HBSS), трех различных доз MUC16-2-CAR-mbIL15-HER1t1 Т-клеток (1×105, 5×105 или 1×106 клеток/мышь) и MUC16-3-CAR-mbIL15-HER1t1 Т-клеток (1×105, 5×105 или 1×106 клеток/мышь), либо однократной дозы MUC16-3-CAR-HER1t1 Т-клеток (1×106 клеток/мышь). Все MUC16-2-CAR-mbIL15-HER1t1 Т-клетки, MUC16-3-CAR-HER1t1 Т-клетки и MUC16-3-CAR-mbIL15-HER1t1 Т-клетки получали из одного донора и производили в течение <2 дней. Эффективность против роста опухоли оценивали с помощью биолюминесцентной визуализации (IVIS) in vivo, которую проводили каждые 3-4 дня после введения дозы CAR-T-клеток, чтобы оценить опухолевую нагрузку.
[00372] На Фиг. 19-20 показано, что как MUC16-2-CAR-mbIL15-HER1t1 Т-клетки, так и MUC16-3-CAR-mbIL15-HER1t1 Т-клетки проявили зависимое от дозы CAR-T элиминирование опухолевых клеток SKOV3-fLUC-MUC16 у мышей. MUC16-3-CAR-mbIL15-HER1t1 Т-клетки проявляли эффективный противоопухолевый ответ даже при дозе 1×105 CAR-T-клеток/мышь по сравнению с MUC16-3-CAR-HER1t1 Т-клетками без mbIL15 при дозе 1×106 CAR-T клеток/мышь.

Пример 13. Аффинность связывания моноклональных антител против MUC16.
[00373] Аффинность связывания различных моноклональных антител против MUC16 (МАТ) оценивали с помощью анализа методом поверхностного плазмонного резонанса (ППР), применяя Biacore 3000. МАТ против MUC16 получали путем временной трансфекции клеток HEK-293 соответствующими плазмидами легкой и тяжелой цепей. Вариабельные области МАТ против MUC16 соединяли с константными областями цепи мыши с получением химерного MAT IgG1 мыши. Укороченный MUC16, слитый с Fc-областью человека, был иммобилизован на сенсорном чипе СМ5. Различные концентрации МАТ впрыскивали в жидкую фазу, и результаты анализировали, применяя BIAevaluation, чтобы рассчитать KD МАТ.
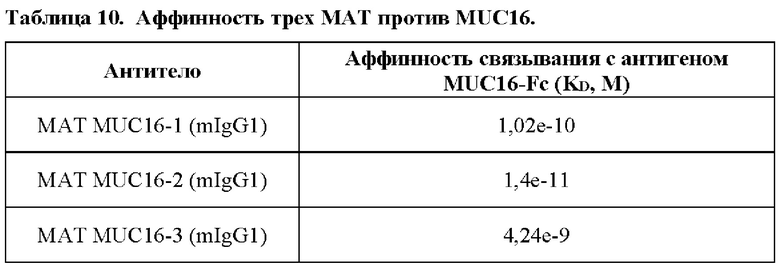
[00374] Если не указано иначе, все технические и научные термины и любые аббревиатуры, использованные в данной заявке, имеют те же значения, которые обычно понимает средний специалист в области, к которой относится настоящее изобретение.
[00375] Хотя в данной заявке были показаны и описаны предпочтительные варианты реализации настоящего изобретения, для специалиста в данной области будет понятно, что такие варианты реализации предложены исключительно в качестве примера. Множество вариантов, изменений и замен придут на ум специалистам в данной области, без отклонения от настоящего описания. Должно быть понятно, что различные альтернативы вариантов реализации, описанных в данной заявке, или комбинации одного или более данных вариантов реализации или аспектов, описанных в них, можно применять для осуществления настоящего изобретения. Предполагается, что следующая формула изобретения определяет объем настоящего изобретения и что способы и структуры, входящие в объем данной формулы изобретения, и их эквиваленты входят объем настоящего изобретения.
ПОСЛЕДОВАТЕЛЬНОСТИ
[00376] В Таблице 11 предложен типичный перечень некоторых последовательностей, входящих в варианты реализации, предложенные в данной заявке.
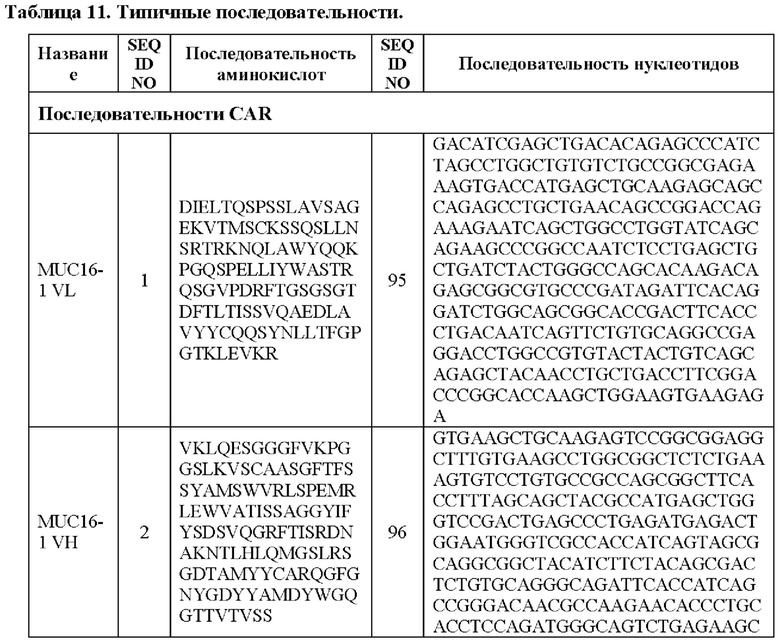
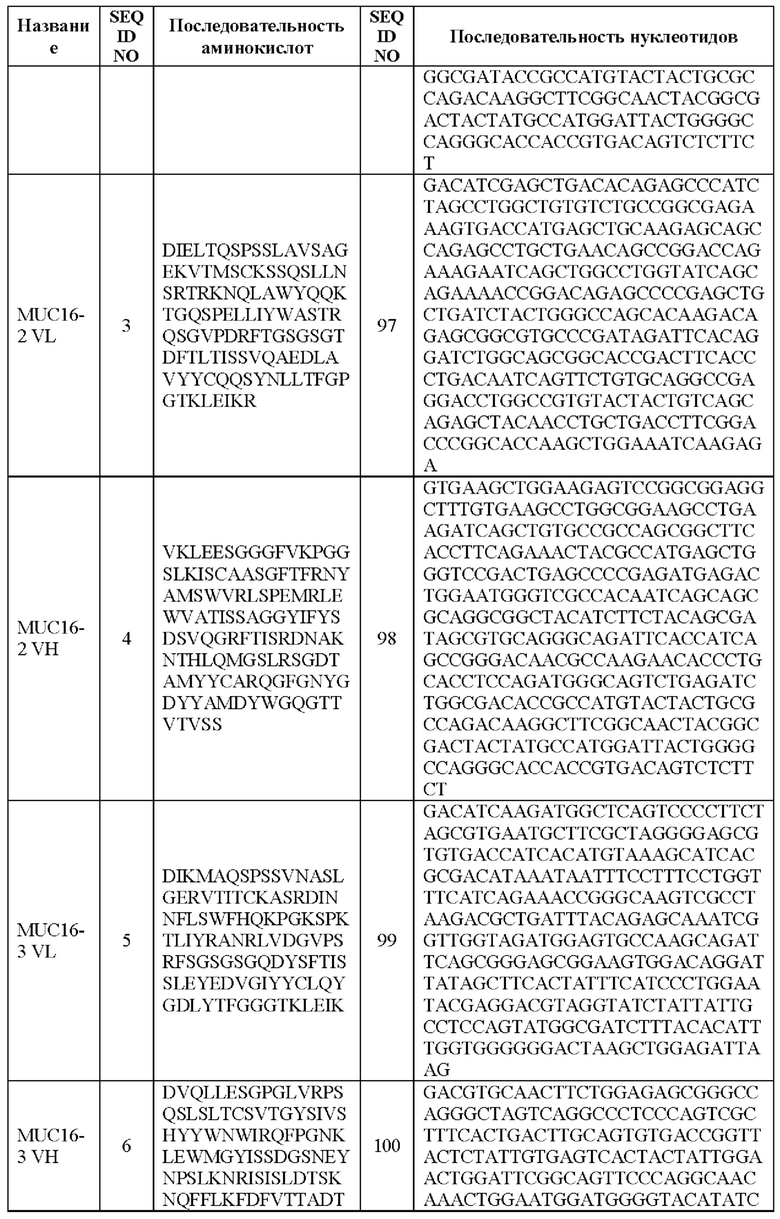
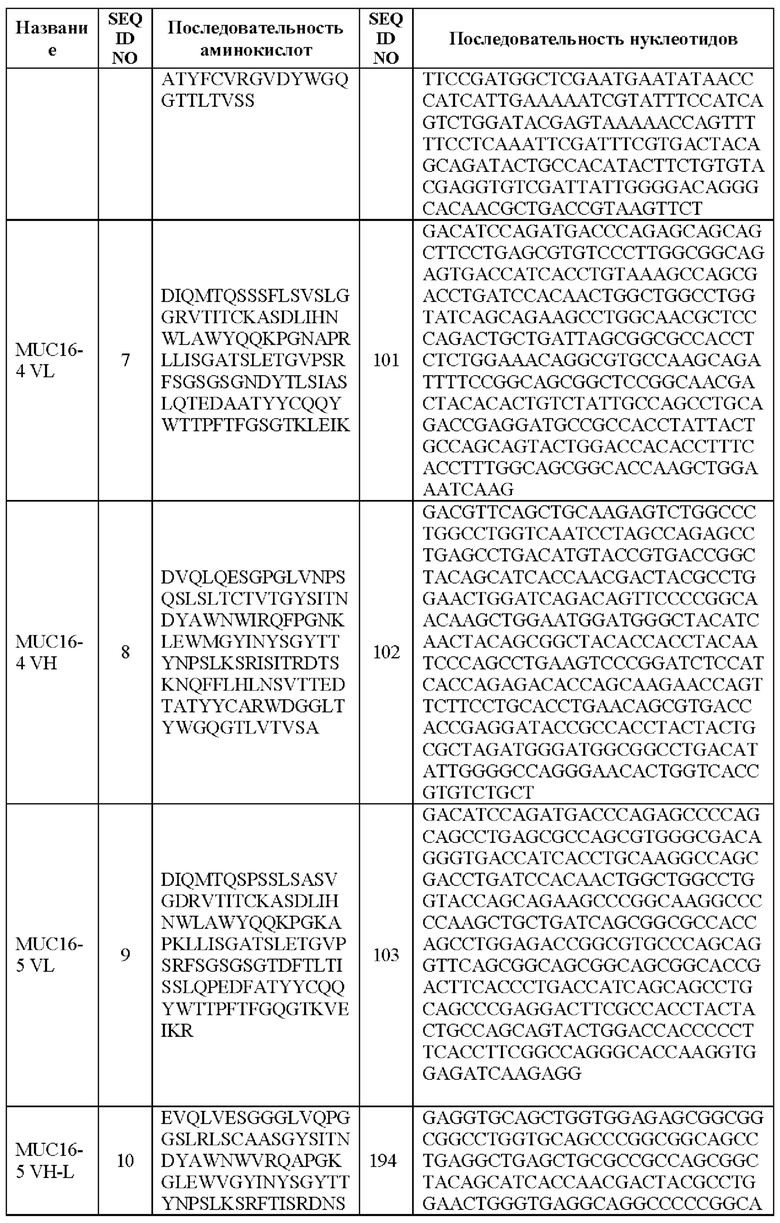
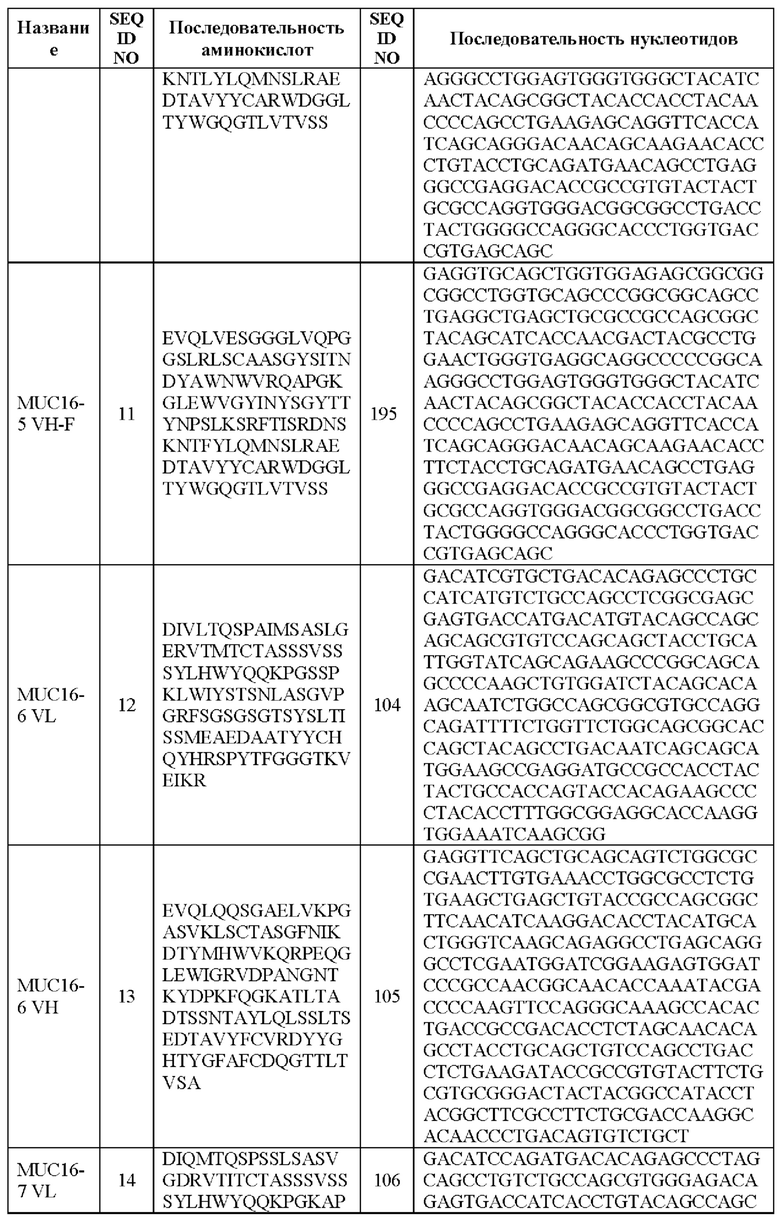
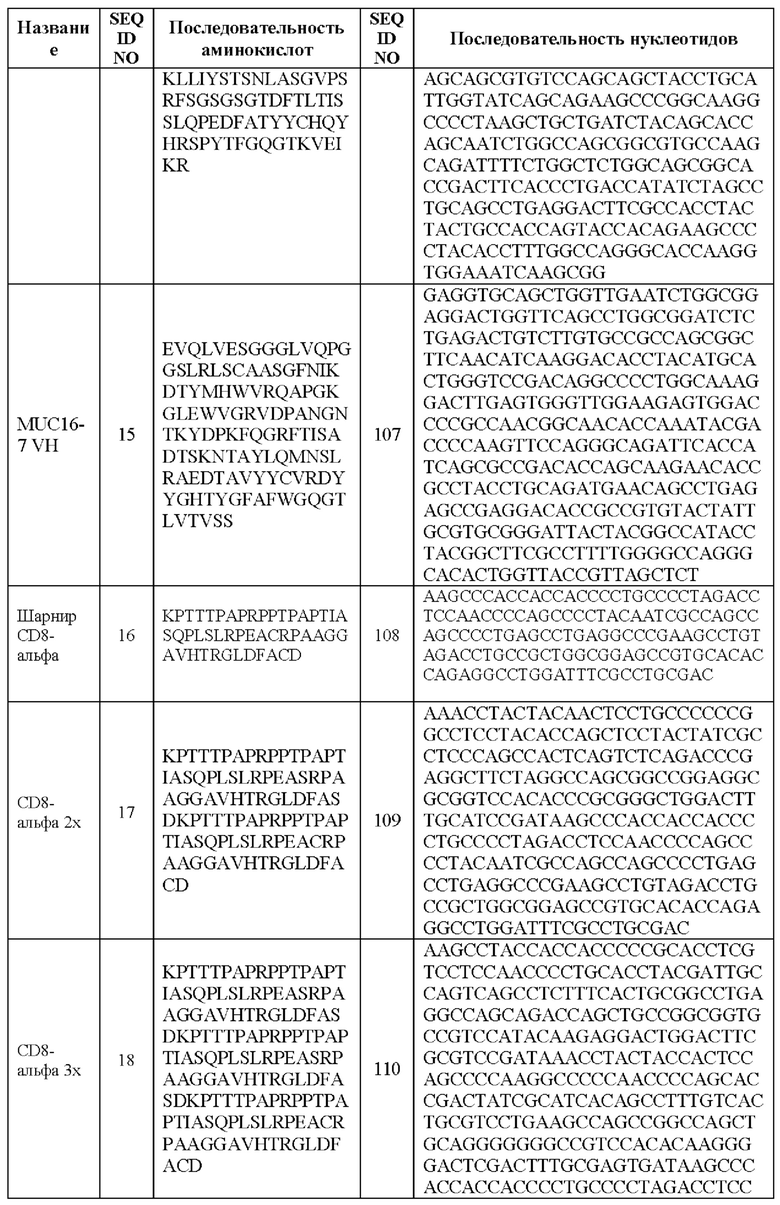
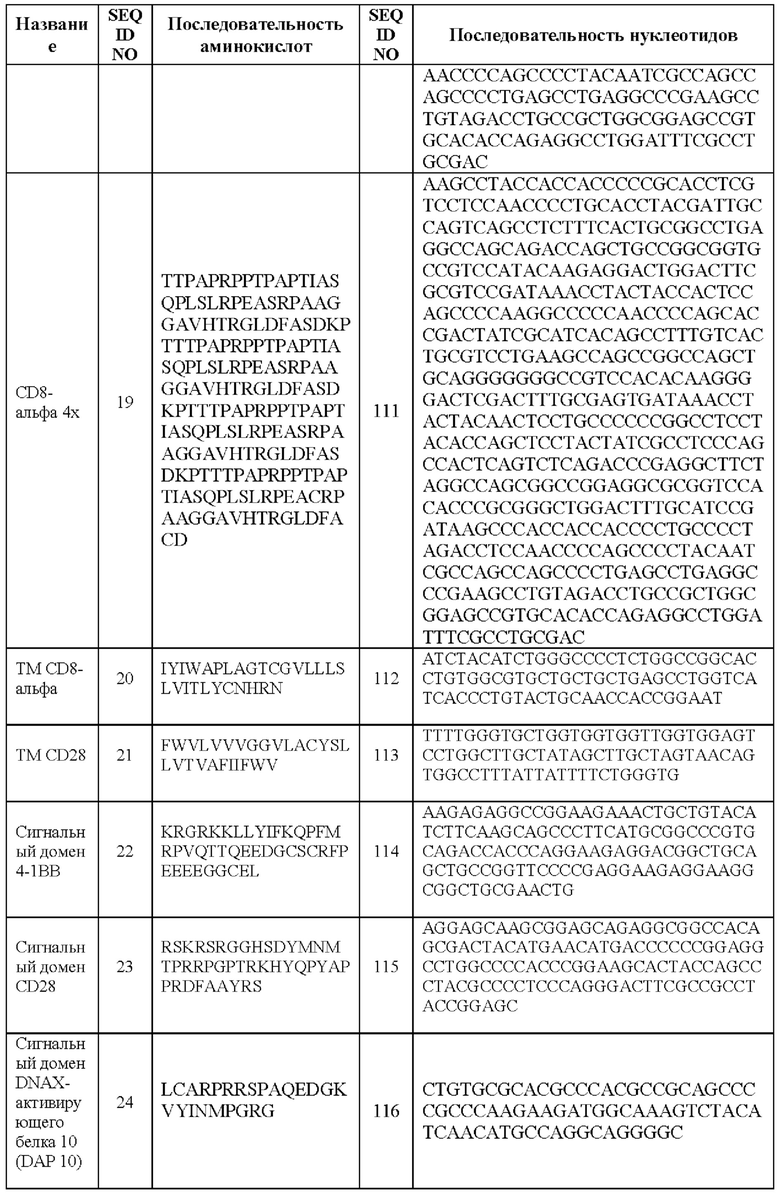
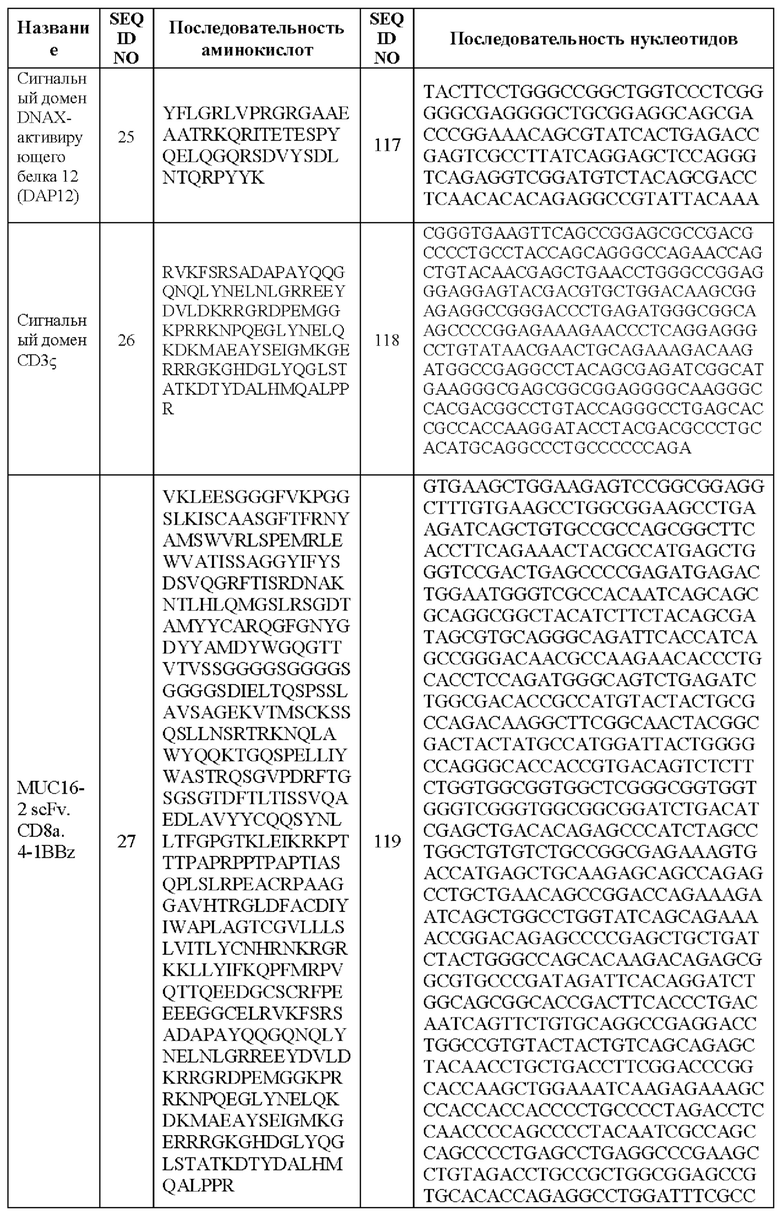
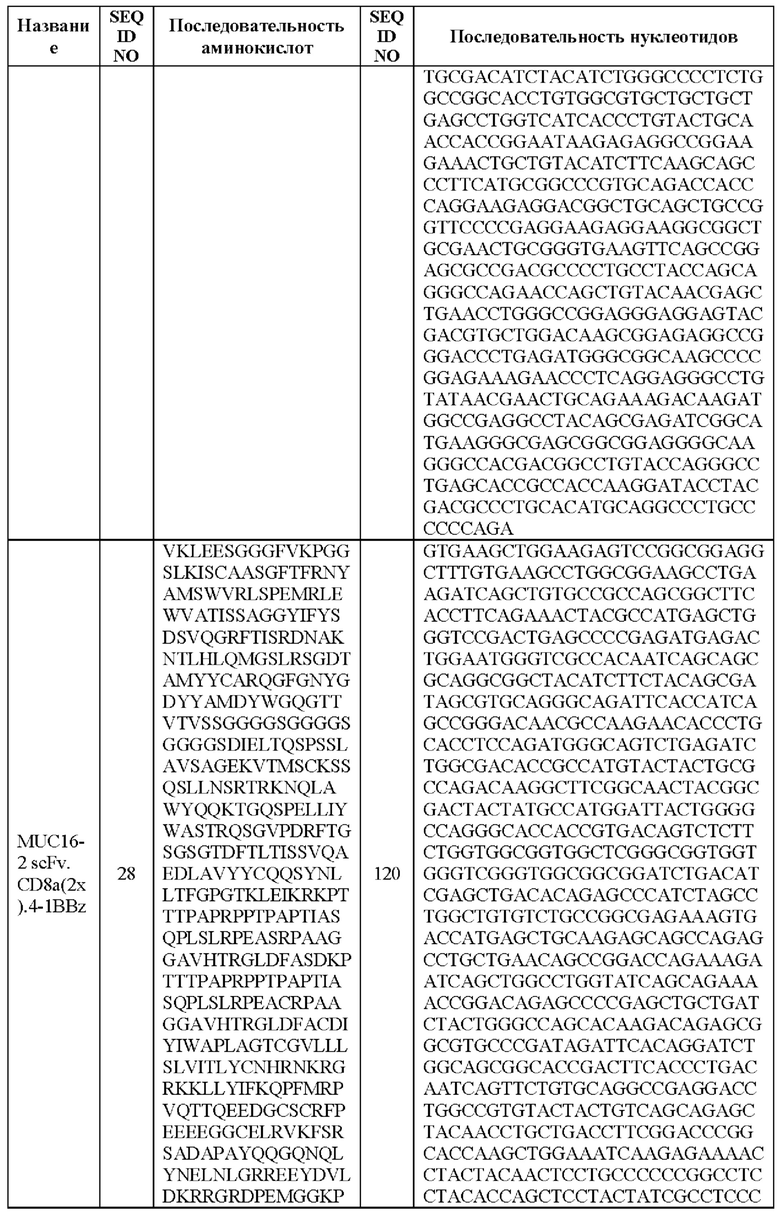




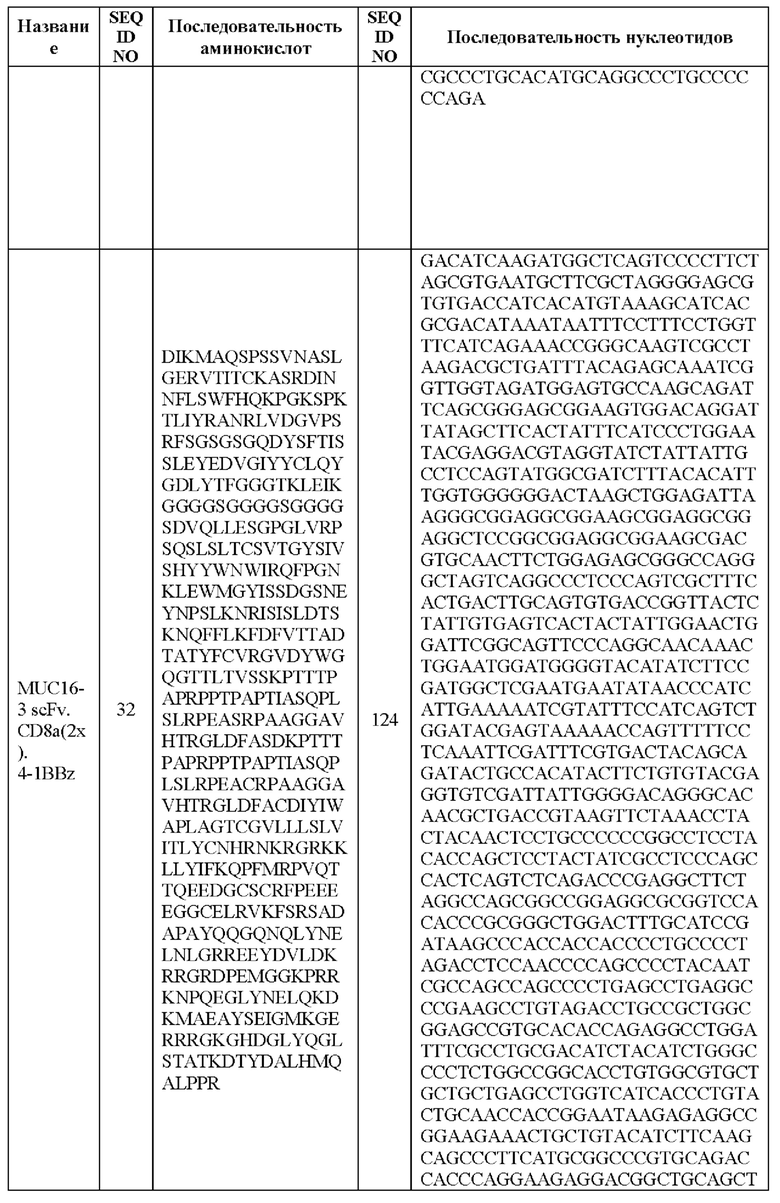
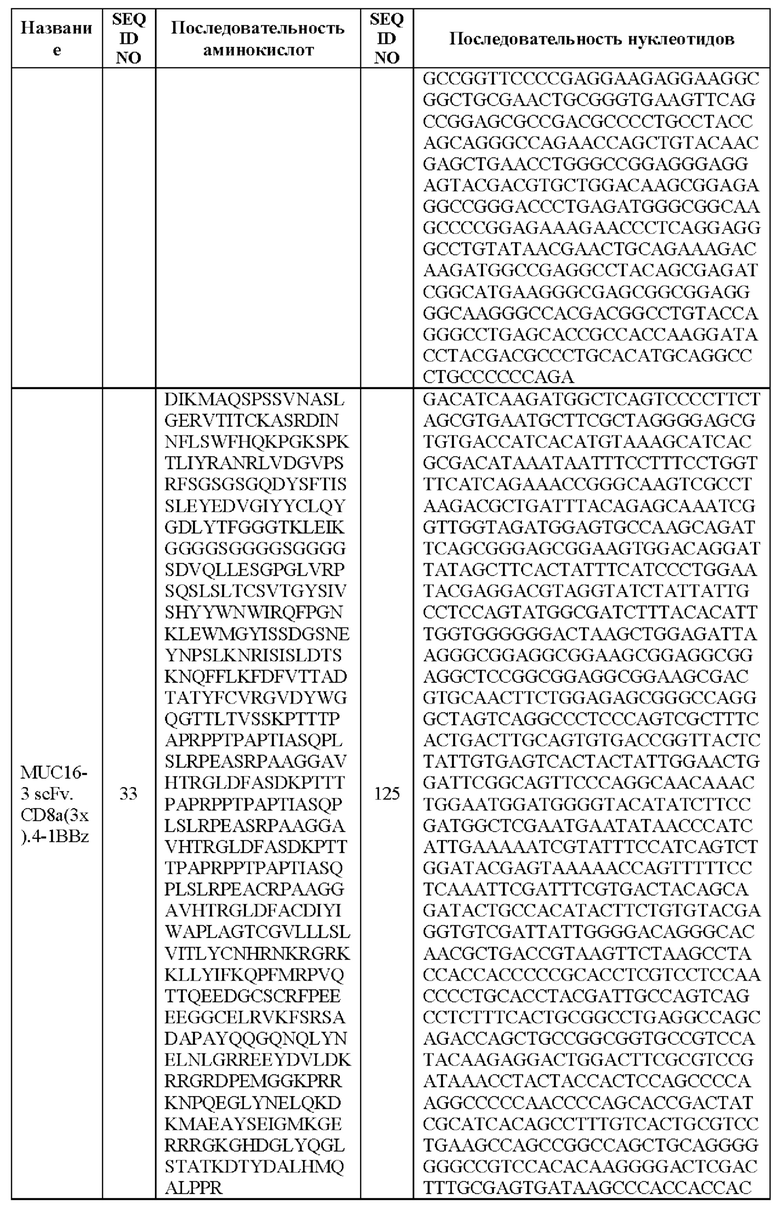

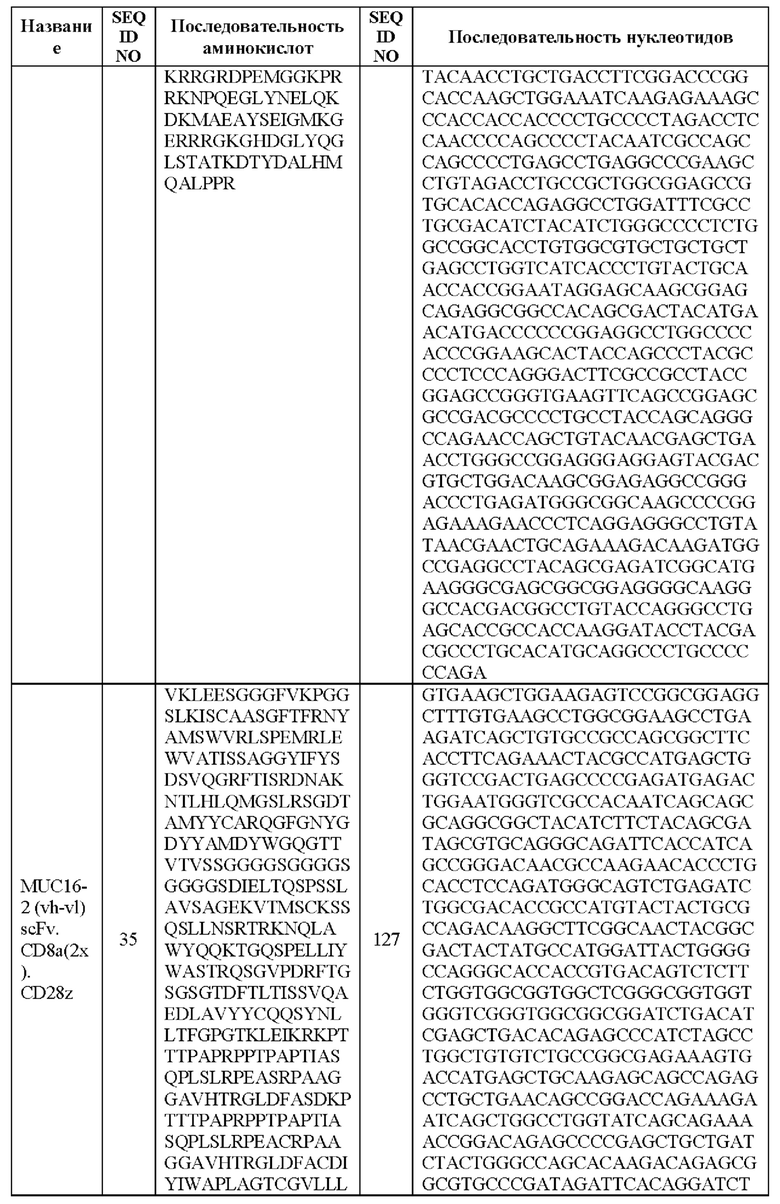
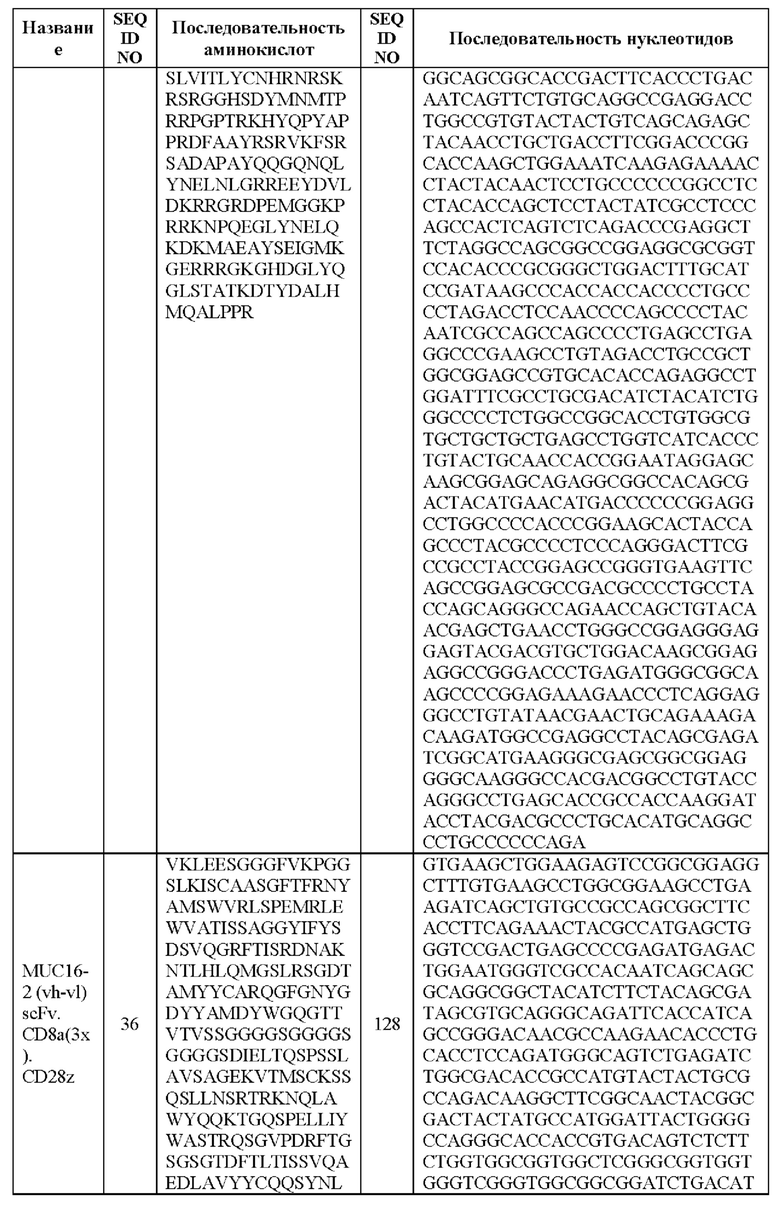



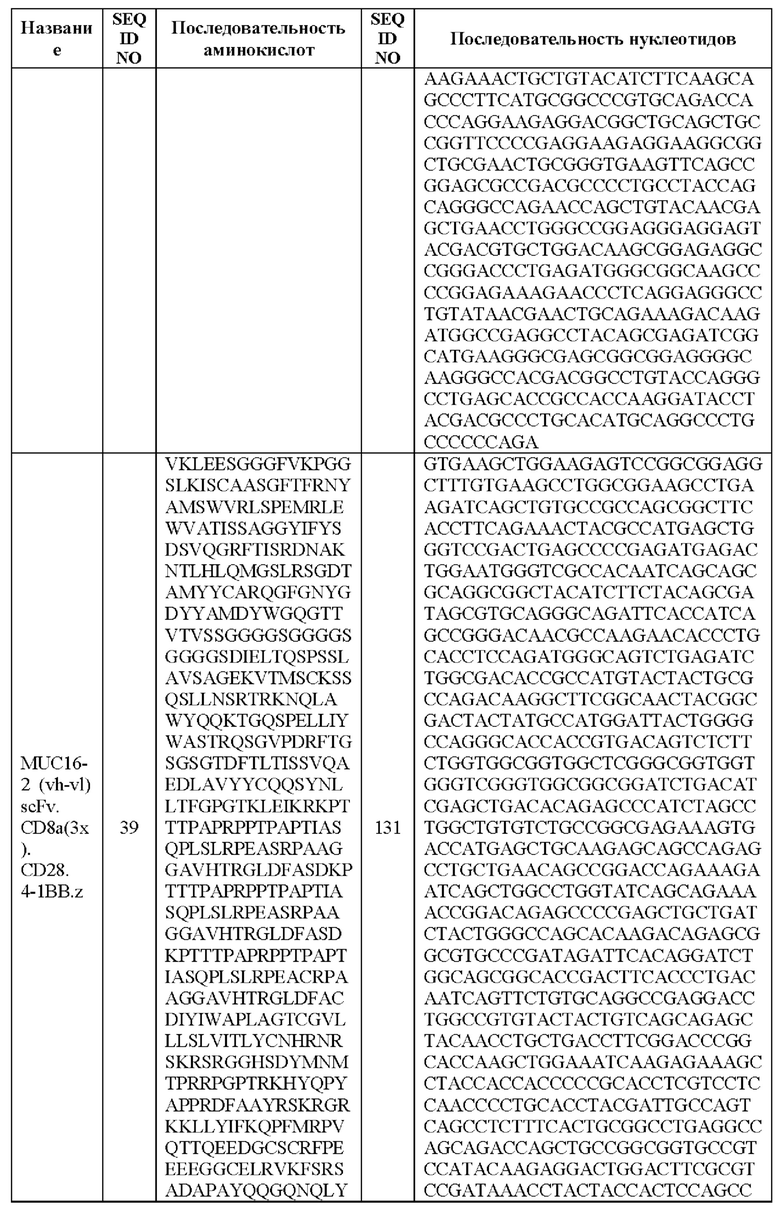



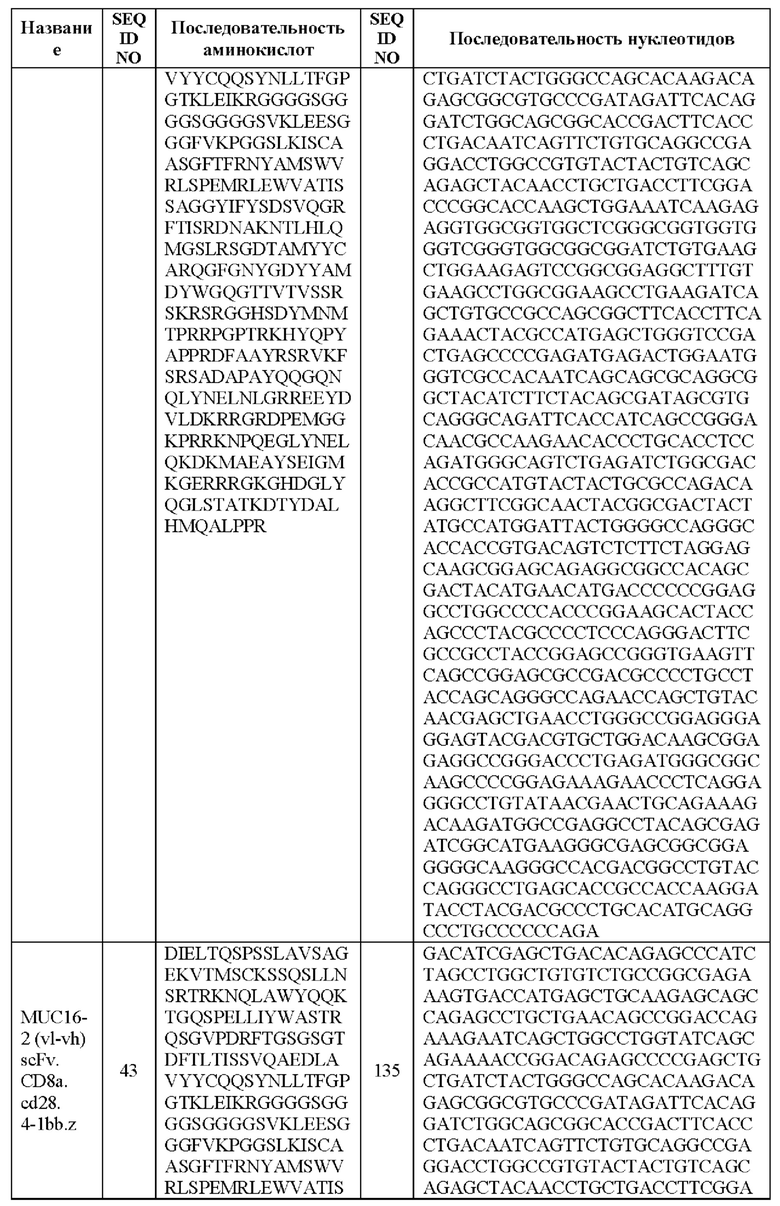



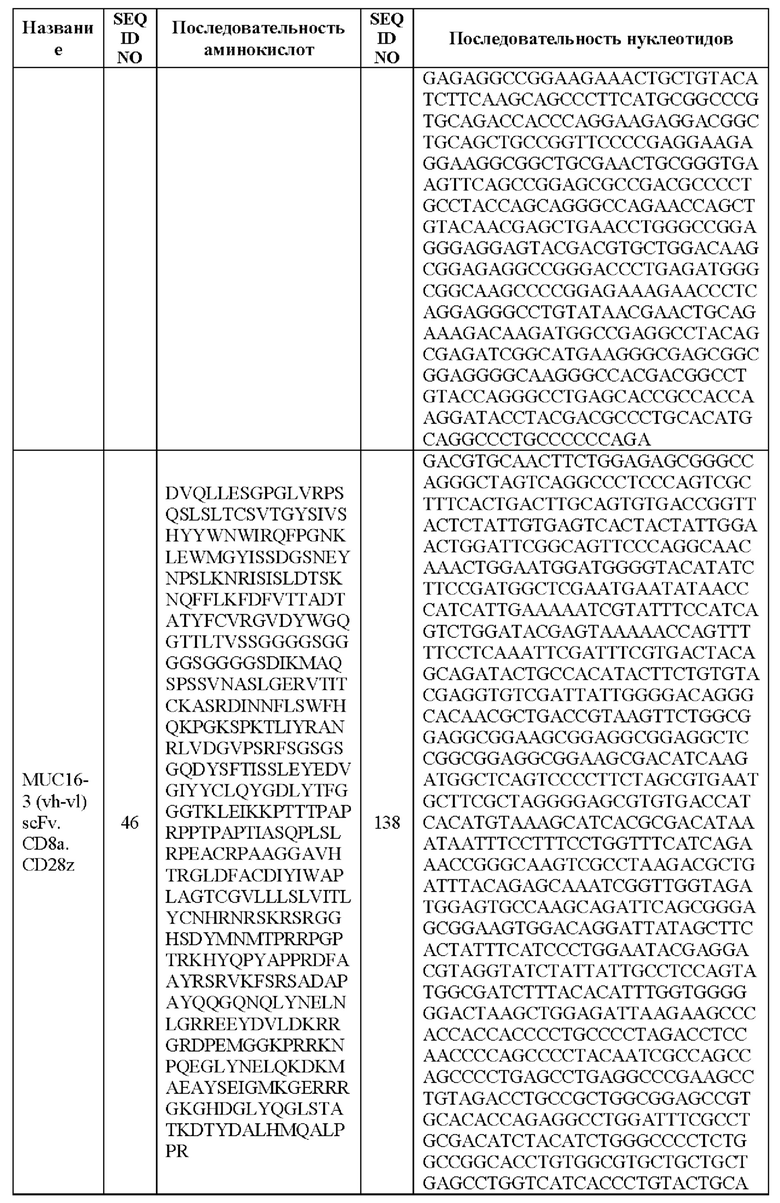
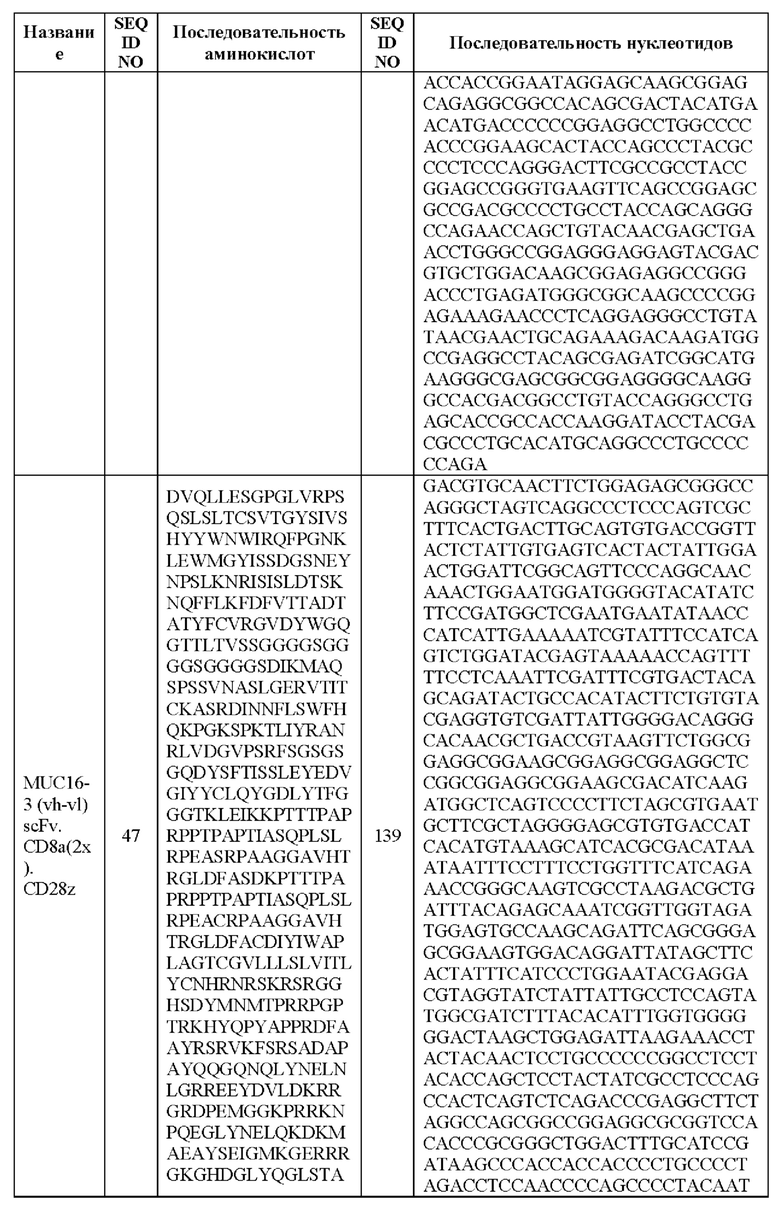

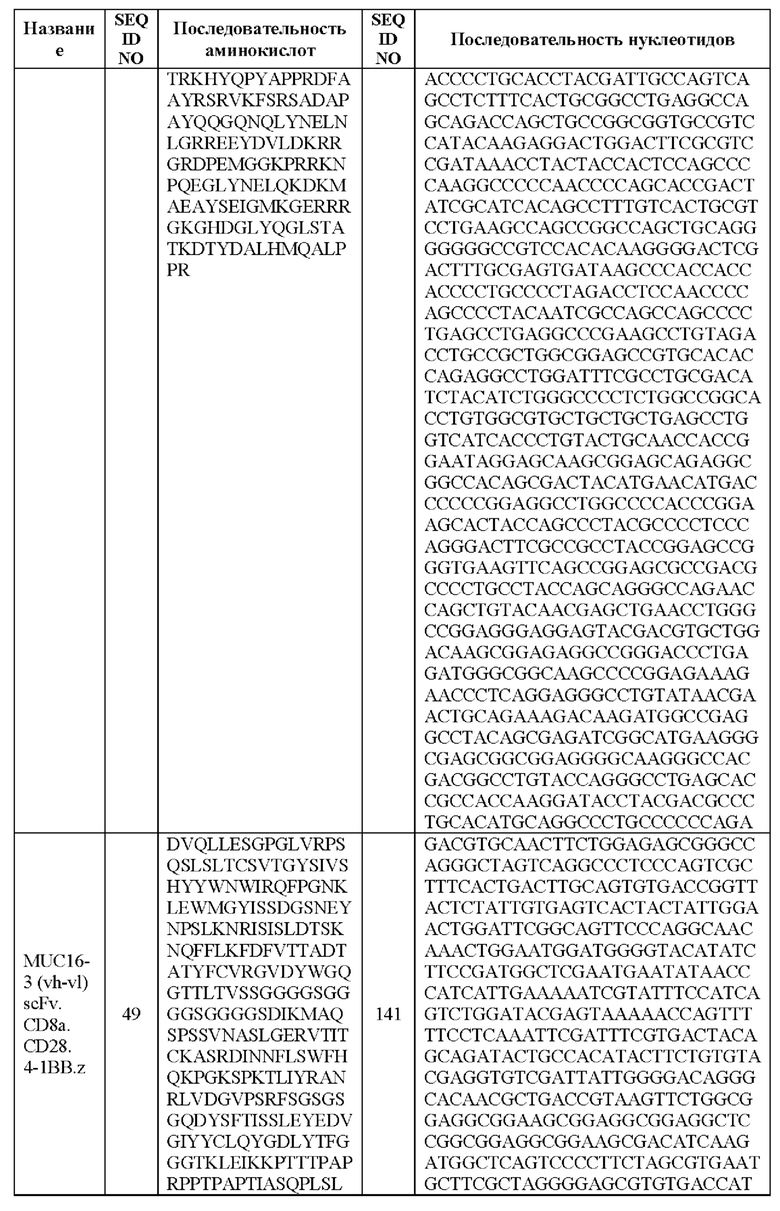
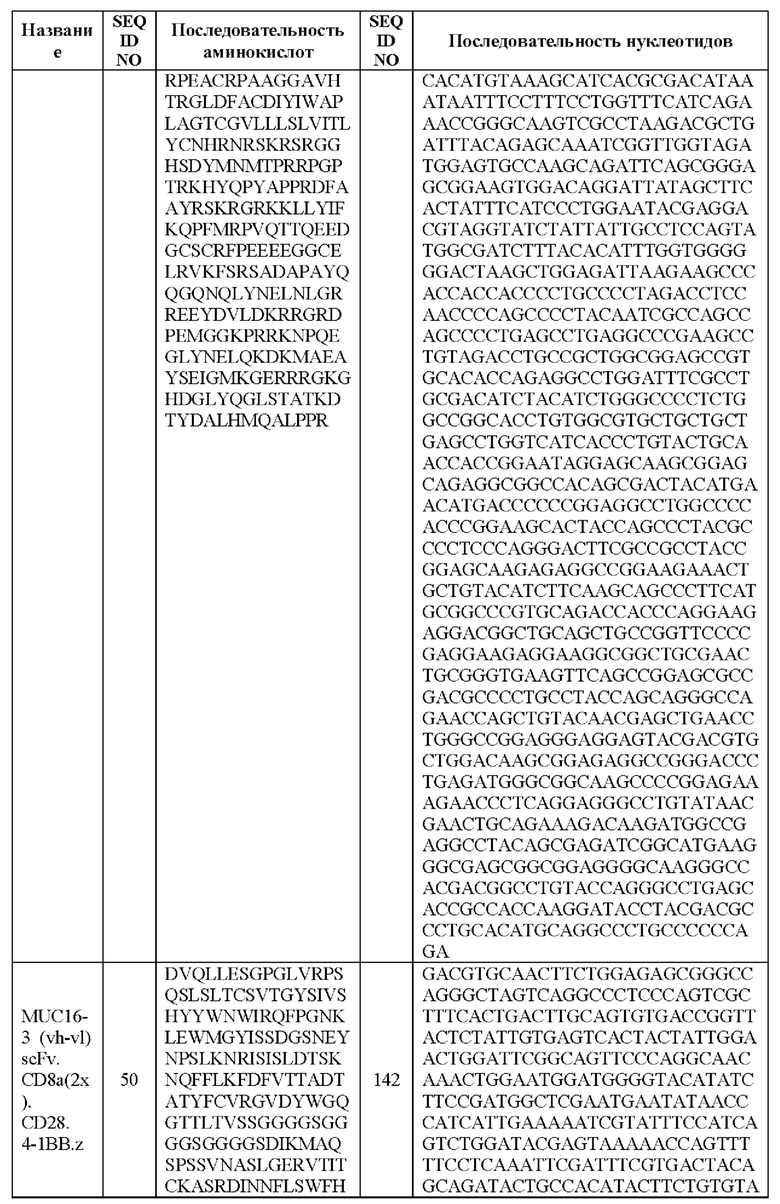


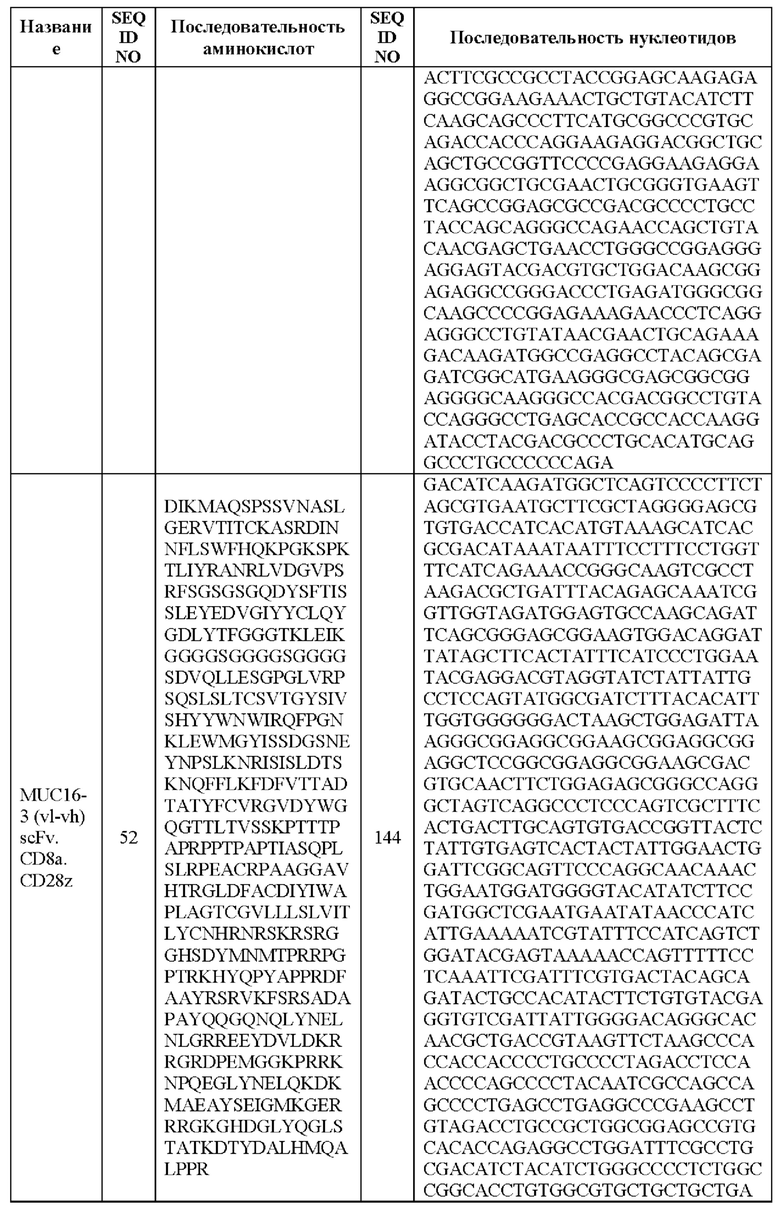
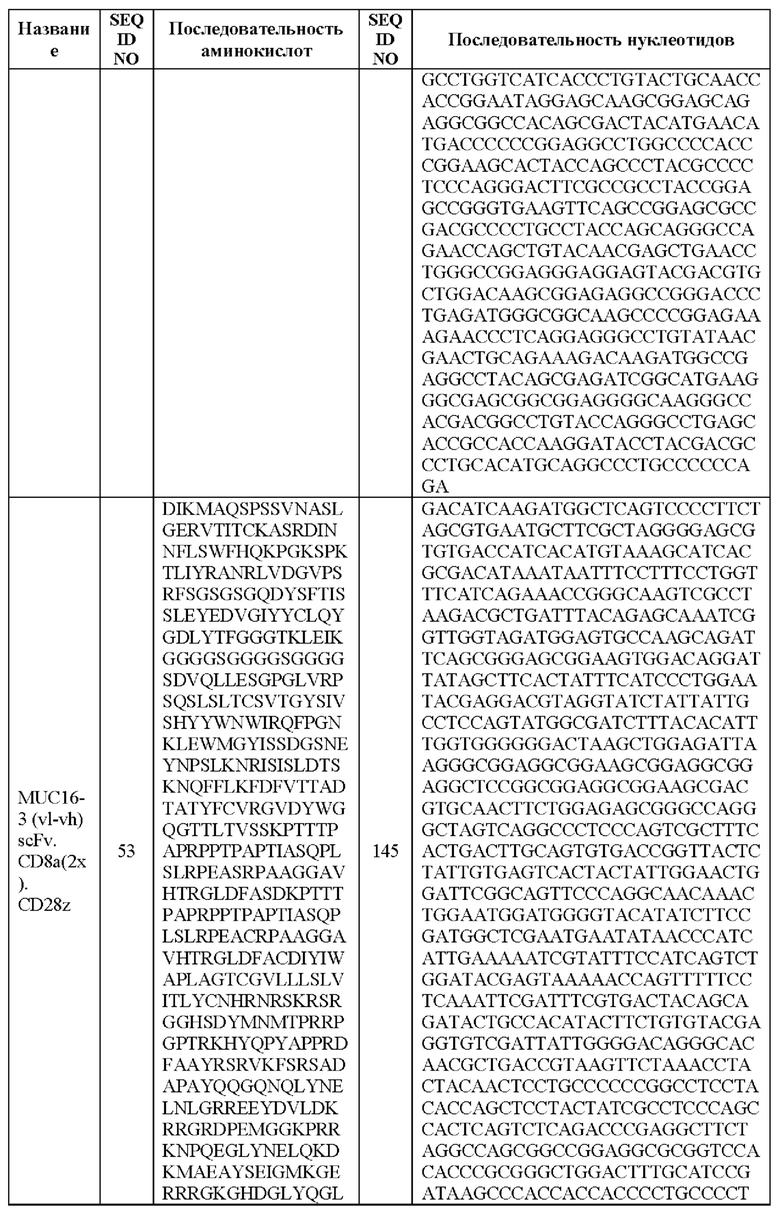
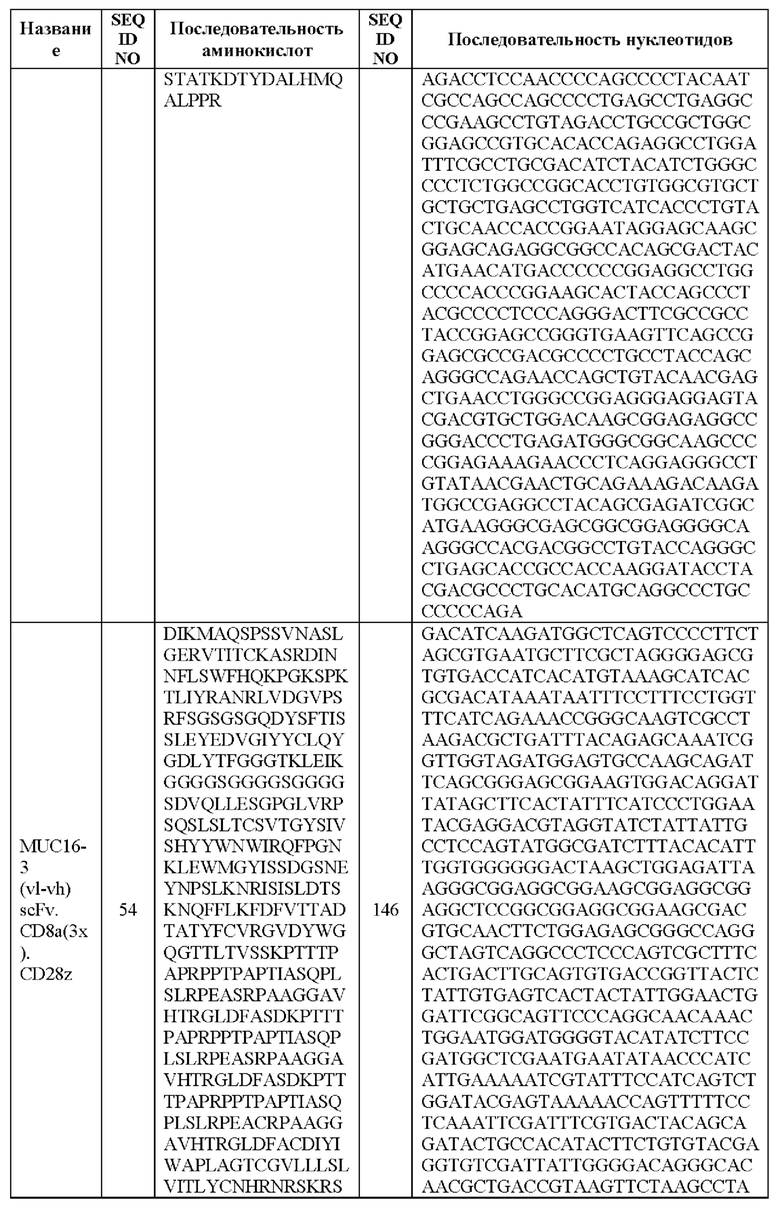
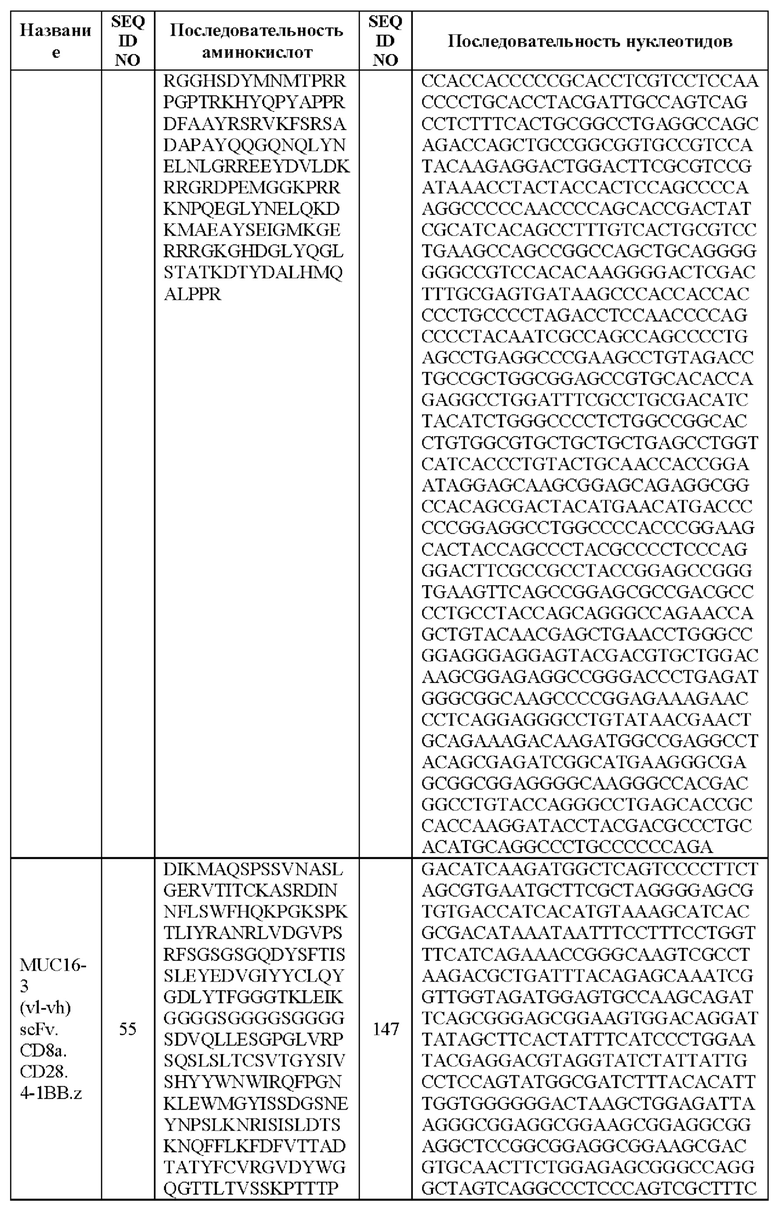



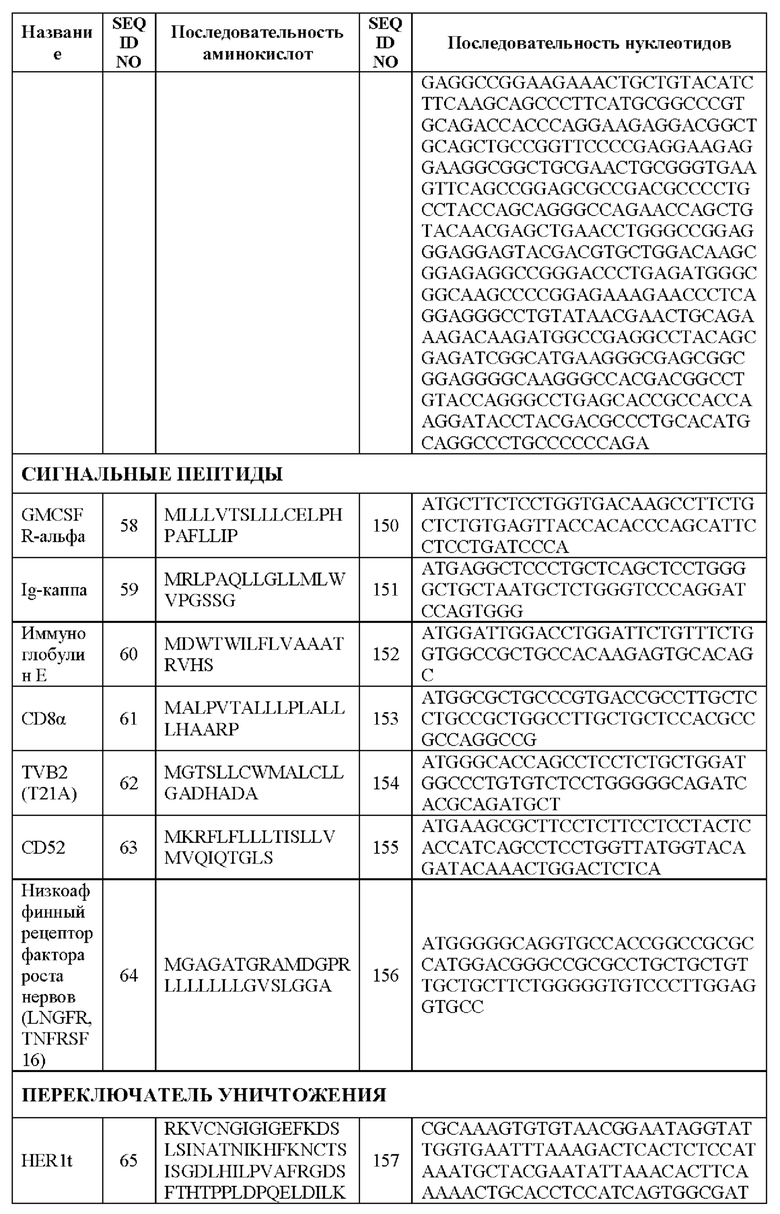


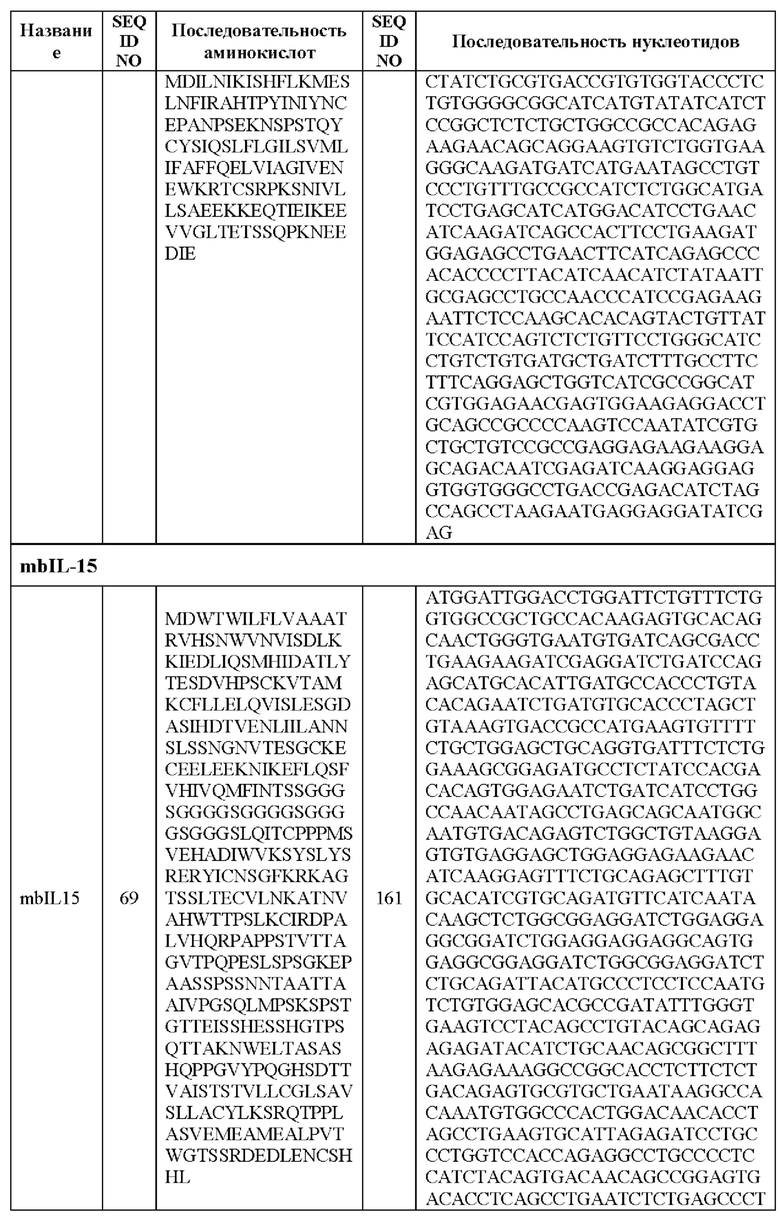
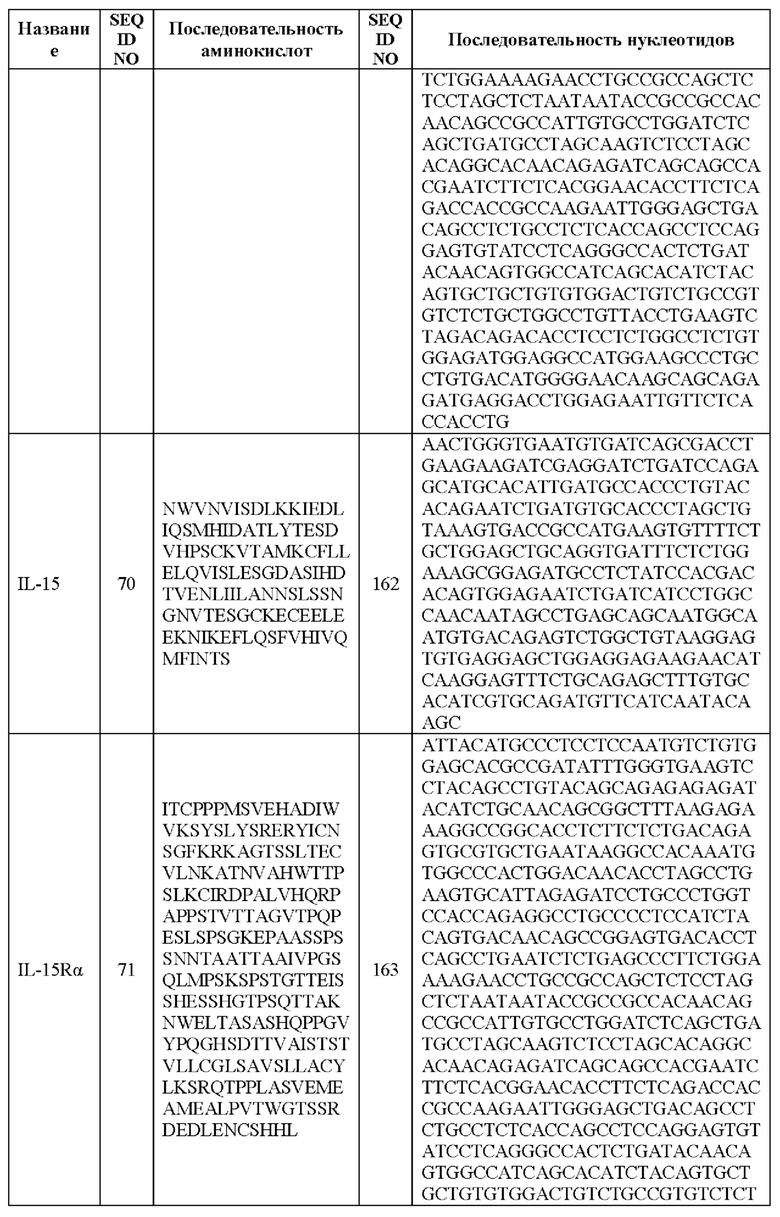
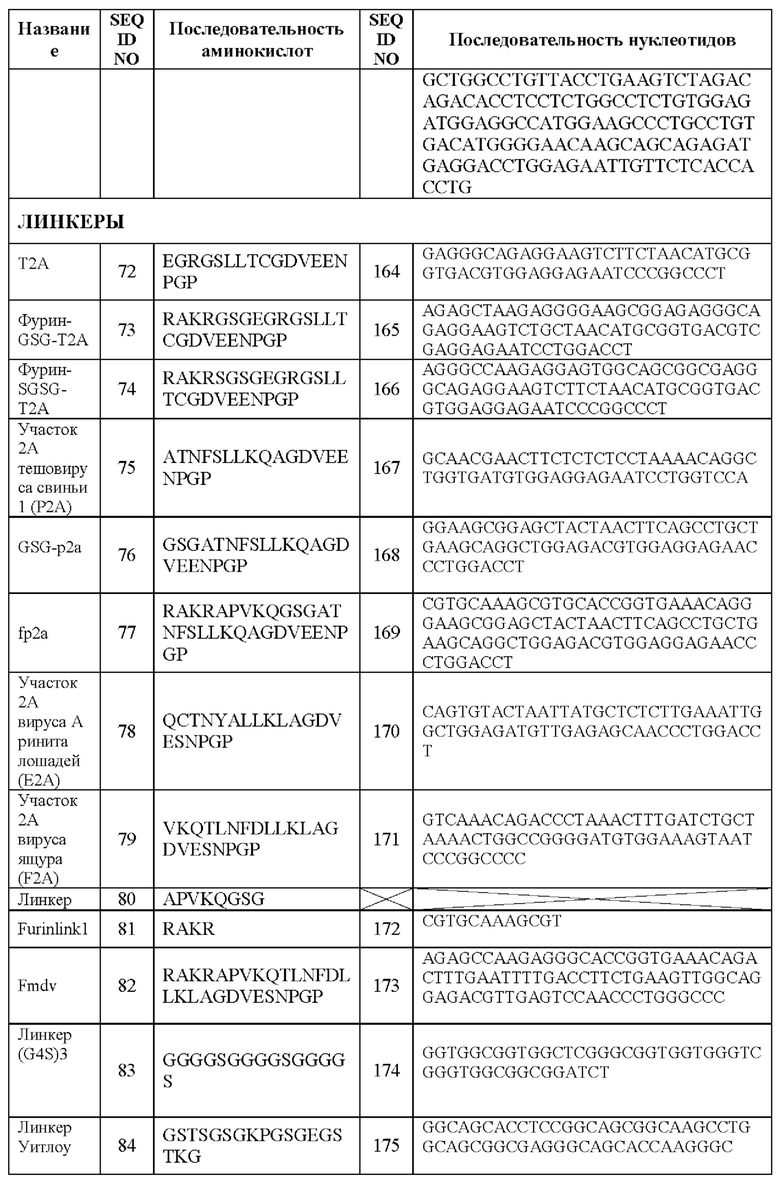
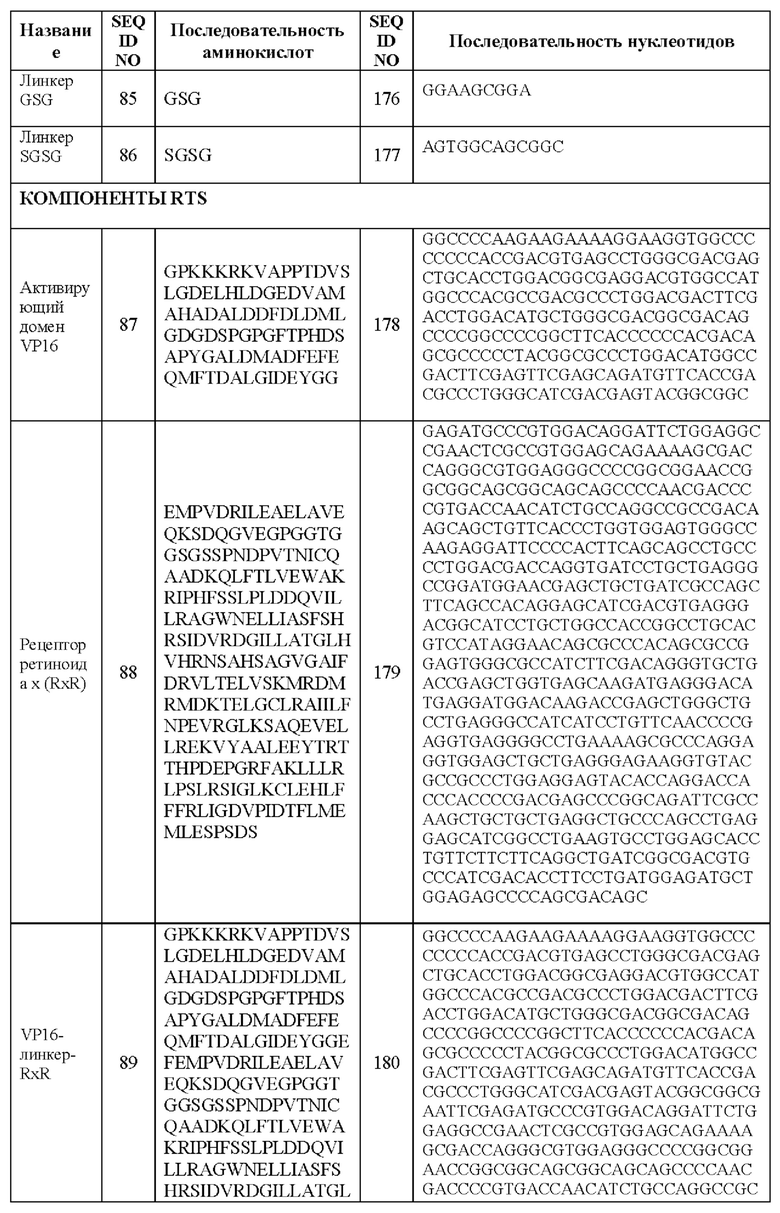
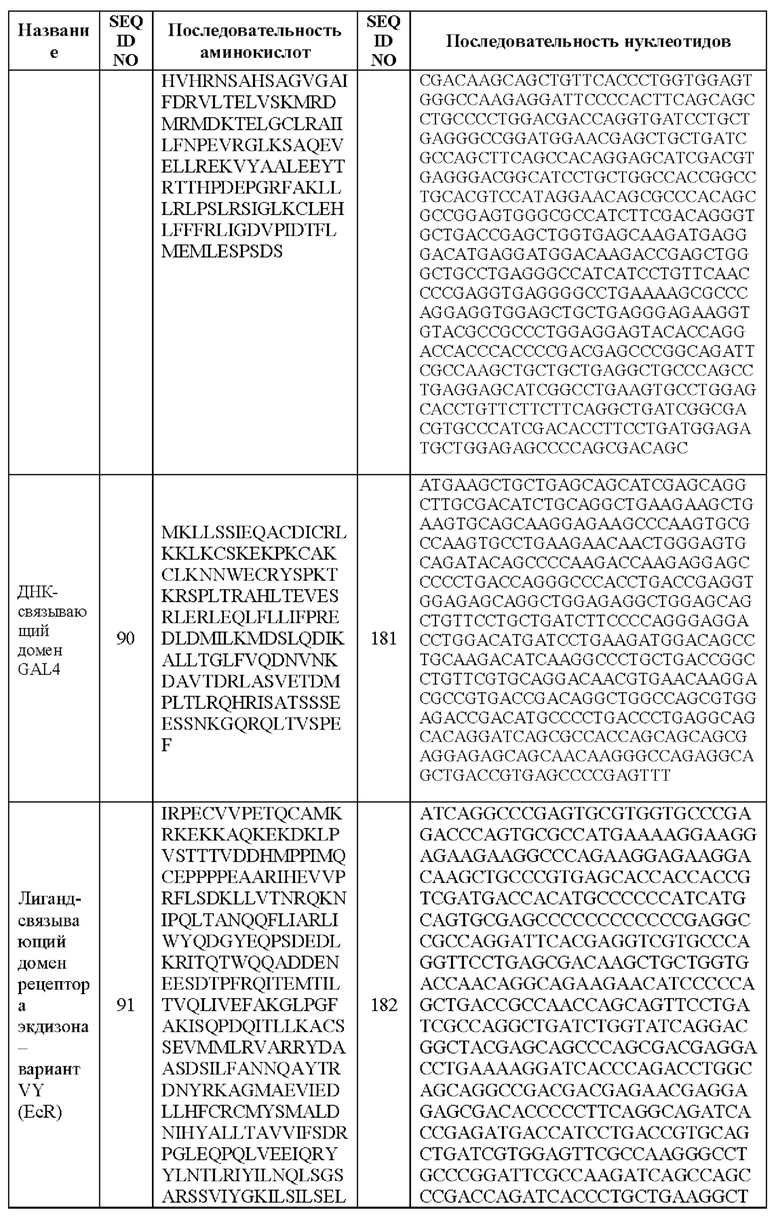
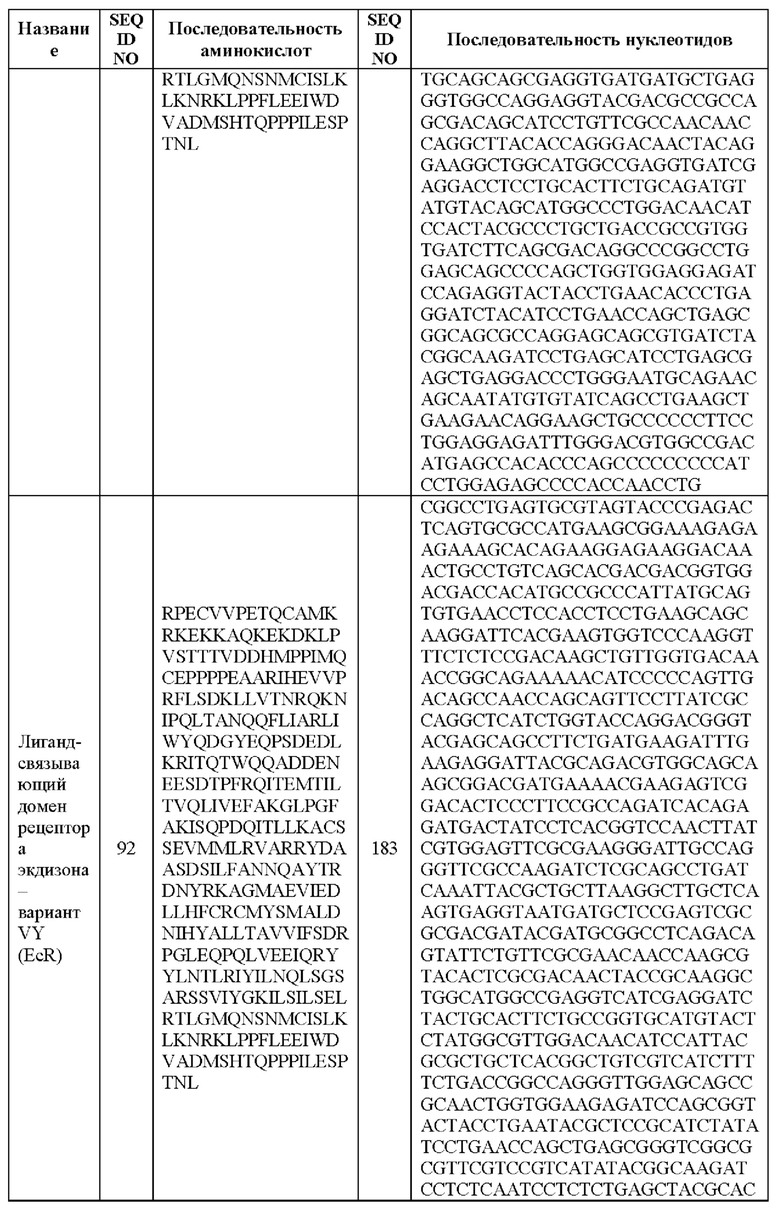


--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> INTREXON CORPORATION
<120> СПЕЦИФИЧНЫЕ К MUC16 ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И ИХ ПРИМЕНЕНИЯ
<130> 50471-715.601
<140> PCT/US2019/035384
<141> 2019-06-04
<150> 62/680,297
<151> 2018-06-04
<160> 205
<170> PatentIn версии 3.5
<210> 1
<211> 113
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 1
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Val Lys
100 105 110
Arg
<210> 2
<211> 122
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 2
Val Lys Leu Gln Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Val Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 3
<211> 113
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 3
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg
<210> 4
<211> 121
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 4
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr His Leu Gln
65 70 75 80
Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala Arg
85 90 95
Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 5
<211> 106
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 5
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 6
<211> 113
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 6
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser
<210> 7
<211> 107
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 7
Asp Ile Gln Met Thr Gln Ser Ser Ser Phe Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser Asp Leu Ile His Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Ser Ile Ala Ser Leu Gln Thr
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Thr Thr Pro Phe
85 90 95
Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 8
<211> 116
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 8
Asp Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Asn Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Thr Val Thr Gly Tyr Ser Ile Thr Asn Asp
20 25 30
Tyr Ala Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Asn Tyr Ser Gly Tyr Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu His Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg Trp Asp Gly Gly Leu Thr Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ala
115
<210> 9
<211> 108
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 9
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Asp Leu Ile His Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Thr Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 10
<211> 116
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 10
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Ile Thr Asn Asp
20 25 30
Tyr Ala Trp Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Val Gly Tyr Ile Asn Tyr Ser Gly Tyr Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Asp Gly Gly Leu Thr Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 11
<211> 116
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Ser Ile Thr Asn Asp
20 25 30
Tyr Ala Trp Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Val Gly Tyr Ile Asn Tyr Ser Gly Tyr Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Phe Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Trp Asp Gly Gly Leu Thr Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 12
<211> 109
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 12
Asp Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Met Thr Cys Thr Ala Ser Ser Ser Val Ser Ser Ser
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Gly Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu
65 70 75 80
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys His Gln Tyr His Arg Ser Pro
85 90 95
Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 13
<211> 120
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 13
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Val Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Val Arg Asp Tyr Tyr Gly His Thr Tyr Gly Phe Ala Phe Cys Asp Gln
100 105 110
Gly Thr Thr Leu Thr Val Ser Ala
115 120
<210> 14
<211> 109
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 14
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Thr Ala Ser Ser Ser Val Ser Ser Ser
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys His Gln Tyr His Arg Ser Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg
100 105
<210> 15
<211> 120
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 15
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Asn Ile Lys Asp Thr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Val Asp Pro Ala Asn Gly Asn Thr Lys Tyr Asp Pro Lys Phe
50 55 60
Gln Gly Arg Phe Thr Ile Ser Ala Asp Thr Ser Lys Asn Thr Ala Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Val Arg Asp Tyr Tyr Gly His Thr Tyr Gly Phe Ala Phe Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 16
<211> 47
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 16
Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
1 5 10 15
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
20 25 30
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 17
<211> 94
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 17
Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
1 5 10 15
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala
20 25 30
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys
35 40 45
Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
50 55 60
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
65 70 75 80
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
85 90
<210> 18
<211> 141
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 18
Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
1 5 10 15
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala
20 25 30
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys
35 40 45
Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
50 55 60
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala
65 70 75 80
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro
85 90 95
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
100 105 110
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
115 120 125
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
130 135 140
<210> 19
<211> 185
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 19
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
1 5 10 15
Gln Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly
20 25 30
Ala Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr
35 40 45
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
50 55 60
Pro Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala
65 70 75 80
Val His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr
85 90 95
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
100 105 110
Leu Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val
115 120 125
His Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro
130 135 140
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
145 150 155 160
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
165 170 175
Thr Arg Gly Leu Asp Phe Ala Cys Asp
180 185
<210> 20
<211> 28
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 20
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys Asn His Arg Asn
20 25
<210> 21
<211> 27
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 21
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 22
<211> 42
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 22
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 23
<211> 41
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 23
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 24
<211> 24
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 24
Leu Cys Ala Arg Pro Arg Arg Ser Pro Ala Gln Glu Asp Gly Lys Val
1 5 10 15
Tyr Ile Asn Met Pro Gly Arg Gly
20
<210> 25
<211> 52
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 25
Tyr Phe Leu Gly Arg Leu Val Pro Arg Gly Arg Gly Ala Ala Glu Ala
1 5 10 15
Ala Thr Arg Lys Gln Arg Ile Thr Glu Thr Glu Ser Pro Tyr Gln Glu
20 25 30
Leu Gln Gly Gln Arg Ser Asp Val Tyr Ser Asp Leu Asn Thr Gln Arg
35 40 45
Pro Tyr Tyr Lys
50
<210> 26
<211> 112
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 26
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 27
<211> 479
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 27
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
290 295 300
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
305 310 315 320
Cys Asn His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
325 330 335
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
340 345 350
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
355 360 365
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
370 375 380
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
385 390 395 400
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
405 410 415
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
420 425 430
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
435 440 445
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
450 455 460
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 28
<211> 526
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 28
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Asn His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
370 375 380
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
385 390 395 400
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
405 410 415
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
420 425 430
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
435 440 445
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
450 455 460
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
465 470 475 480
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
485 490 495
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
500 505 510
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 29
<211> 573
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 29
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
405 410 415
His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
420 425 430
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
435 440 445
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
450 455 460
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
465 470 475 480
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
485 490 495
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
500 505 510
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
515 520 525
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
530 535 540
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
545 550 555 560
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 30
<211> 485
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 30
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro Asp Ile Lys Met Ala Gln Ser Pro Ser Ser
20 25 30
Val Asn Ala Ser Leu Gly Glu Arg Val Thr Ile Thr Cys Lys Ala Ser
35 40 45
Arg Asp Ile Asn Asn Phe Leu Ser Trp Phe His Gln Lys Pro Gly Lys
50 55 60
Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu Val Asp Gly Val
65 70 75 80
Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr
85 90 95
Ile Ser Ser Leu Glu Tyr Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln
100 105 110
Tyr Gly Asp Leu Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
130 135 140
Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln Ser
145 150 155 160
Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His Tyr
165 170 175
Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp Met
180 185 190
Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys
195 200 205
Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu
210 215 220
Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val
225 230 235 240
Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser
245 250 255
Lys Pro Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr
260 265 270
Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala
275 280 285
Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile
290 295 300
Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser
305 310 315 320
Leu Val Ile Thr Leu Tyr Cys Asn His Arg Asn Lys Arg Gly Arg Lys
325 330 335
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
340 345 350
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
355 360 365
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
370 375 380
Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
385 390 395 400
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
405 410 415
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
420 425 430
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
435 440 445
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
450 455 460
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
465 470 475 480
Ala Leu Pro Pro Arg
485
<210> 31
<211> 463
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 31
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
275 280 285
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
290 295 300
Cys Asn His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
305 310 315 320
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
325 330 335
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
340 345 350
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln
355 360 365
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
370 375 380
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
385 390 395 400
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
405 410 415
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
420 425 430
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
435 440 445
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 32
<211> 510
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 32
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
325 330 335
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
340 345 350
Asn His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
355 360 365
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
370 375 380
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
385 390 395 400
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
405 410 415
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
420 425 430
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
435 440 445
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
450 455 460
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
465 470 475 480
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
485 490 495
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
500 505 510
<210> 33
<211> 557
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 33
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
325 330 335
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
340 345 350
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
355 360 365
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
370 375 380
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
385 390 395 400
His Arg Asn Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
405 410 415
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
420 425 430
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
435 440 445
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
450 455 460
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
465 470 475 480
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
485 490 495
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
500 505 510
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
515 520 525
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
530 535 540
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
545 550 555
<210> 34
<211> 478
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 34
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
290 295 300
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
305 310 315 320
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
325 330 335
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
340 345 350
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 35
<211> 525
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 35
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
370 375 380
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
385 390 395 400
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
405 410 415
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
420 425 430
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
435 440 445
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
450 455 460
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
465 470 475 480
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
485 490 495
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
500 505 510
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 36
<211> 572
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 36
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
405 410 415
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
420 425 430
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
435 440 445
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe
450 455 460
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
465 470 475 480
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
485 490 495
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
500 505 510
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
515 520 525
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
530 535 540
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
545 550 555 560
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
565 570
<210> 37
<211> 520
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 37
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
290 295 300
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
305 310 315 320
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
325 330 335
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
340 345 350
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg
355 360 365
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
370 375 380
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
385 390 395 400
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
405 410 415
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
420 425 430
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
435 440 445
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
450 455 460
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
465 470 475 480
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
485 490 495
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
500 505 510
His Met Gln Ala Leu Pro Pro Arg
515 520
<210> 38
<211> 567
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 38
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
370 375 380
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
385 390 395 400
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly
405 410 415
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
420 425 430
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
435 440 445
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
450 455 460
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
465 470 475 480
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
485 490 495
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
500 505 510
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
515 520 525
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
530 535 540
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
545 550 555 560
Met Gln Ala Leu Pro Pro Arg
565
<210> 39
<211> 614
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 39
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
1 5 10 15
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
20 25 30
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
35 40 45
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
65 70 75 80
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Glu Leu Thr Gln Ser
130 135 140
Pro Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys
145 150 155 160
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Gln Leu
165 170 175
Ala Trp Tyr Gln Gln Lys Thr Gly Gln Ser Pro Glu Leu Leu Ile Tyr
180 185 190
Trp Ala Ser Thr Arg Gln Ser Gly Val Pro Asp Arg Phe Thr Gly Ser
195 200 205
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu
210 215 220
Asp Leu Ala Val Tyr Tyr Cys Gln Gln Ser Tyr Asn Leu Leu Thr Phe
225 230 235 240
Gly Pro Gly Thr Lys Leu Glu Ile Lys Arg Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
405 410 415
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
420 425 430
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
435 440 445
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg
450 455 460
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
465 470 475 480
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
485 490 495
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
500 505 510
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
515 520 525
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
530 535 540
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
545 550 555 560
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
565 570 575
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
580 585 590
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
595 600 605
Gln Ala Leu Pro Pro Arg
610
<210> 40
<211> 478
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 40
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
290 295 300
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
305 310 315 320
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
325 330 335
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
340 345 350
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 41
<211> 525
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 41
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
370 375 380
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
385 390 395 400
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
405 410 415
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
420 425 430
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
435 440 445
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
450 455 460
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
465 470 475 480
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
485 490 495
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
500 505 510
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
515 520 525
<210> 42
<211> 403
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 42
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Arg Ser Lys Arg Ser Arg
245 250 255
Gly Gly His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro
260 265 270
Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala
275 280 285
Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr
290 295 300
Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg
305 310 315 320
Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met
325 330 335
Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu
340 345 350
Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys
355 360 365
Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu
370 375 380
Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu
385 390 395 400
Pro Pro Arg
<210> 43
<211> 445
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 43
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Arg Ser Lys Arg Ser Arg
245 250 255
Gly Gly His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro
260 265 270
Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala
275 280 285
Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
290 295 300
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
305 310 315 320
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
325 330 335
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
340 345 350
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
355 360 365
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
370 375 380
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
385 390 395 400
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
405 410 415
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
420 425 430
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
435 440 445
<210> 44
<211> 567
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 44
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
340 345 350
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
355 360 365
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
370 375 380
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
385 390 395 400
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly
405 410 415
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
420 425 430
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
435 440 445
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
450 455 460
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
465 470 475 480
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
485 490 495
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
500 505 510
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
515 520 525
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
530 535 540
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
545 550 555 560
Met Gln Ala Leu Pro Pro Arg
565
<210> 45
<211> 614
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 45
Asp Ile Glu Leu Thr Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Gln Leu Ala Trp Tyr Gln Gln Lys Thr Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gln Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Ser Tyr Asn Leu Leu Thr Phe Gly Pro Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Val Lys Leu Glu Glu Ser Gly Gly Gly Phe Val Lys Pro Gly Gly Ser
130 135 140
Leu Lys Ile Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Asn Tyr Ala
145 150 155 160
Met Ser Trp Val Arg Leu Ser Pro Glu Met Arg Leu Glu Trp Val Ala
165 170 175
Thr Ile Ser Ser Ala Gly Gly Tyr Ile Phe Tyr Ser Asp Ser Val Gln
180 185 190
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu His Leu
195 200 205
Gln Met Gly Ser Leu Arg Ser Gly Asp Thr Ala Met Tyr Tyr Cys Ala
210 215 220
Arg Gln Gly Phe Gly Asn Tyr Gly Asp Tyr Tyr Ala Met Asp Tyr Trp
225 230 235 240
Gly Gln Gly Thr Thr Val Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
245 250 255
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
260 265 270
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
275 280 285
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
290 295 300
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
305 310 315 320
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
325 330 335
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
340 345 350
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
355 360 365
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
370 375 380
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
385 390 395 400
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
405 410 415
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
420 425 430
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
435 440 445
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg
450 455 460
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
465 470 475 480
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
485 490 495
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
500 505 510
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
515 520 525
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
530 535 540
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
545 550 555 560
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
565 570 575
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
580 585 590
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
595 600 605
Gln Ala Leu Pro Pro Arg
610
<210> 46
<211> 462
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 46
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
275 280 285
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
290 295 300
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
305 310 315 320
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
325 330 335
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
340 345 350
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
355 360 365
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
370 375 380
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
385 390 395 400
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
405 410 415
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
420 425 430
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
435 440 445
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 47
<211> 509
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 47
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
325 330 335
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
340 345 350
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
355 360 365
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
370 375 380
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
385 390 395 400
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
405 410 415
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
420 425 430
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
435 440 445
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
450 455 460
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
465 470 475 480
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
485 490 495
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
500 505
<210> 48
<211> 556
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 48
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
325 330 335
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
340 345 350
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
355 360 365
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
370 375 380
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
385 390 395 400
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
405 410 415
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
420 425 430
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe
435 440 445
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
450 455 460
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
465 470 475 480
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
485 490 495
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
500 505 510
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
515 520 525
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
530 535 540
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
545 550 555
<210> 49
<211> 504
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 49
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
275 280 285
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
290 295 300
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
305 310 315 320
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
325 330 335
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg
340 345 350
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
355 360 365
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
370 375 380
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
385 390 395 400
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
405 410 415
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
420 425 430
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
435 440 445
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
450 455 460
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
465 470 475 480
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
485 490 495
His Met Gln Ala Leu Pro Pro Arg
500
<210> 50
<211> 551
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 50
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
325 330 335
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
340 345 350
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
355 360 365
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
370 375 380
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly
385 390 395 400
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
405 410 415
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
420 425 430
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
435 440 445
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
450 455 460
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
465 470 475 480
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
485 490 495
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
500 505 510
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
515 520 525
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
530 535 540
Met Gln Ala Leu Pro Pro Arg
545 550
<210> 51
<211> 598
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 51
Asp Val Gln Leu Leu Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Tyr Ser Ile Val Ser His
20 25 30
Tyr Tyr Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Ser Asp Gly Ser Asn Glu Tyr Asn Pro Ser Leu
50 55 60
Lys Asn Arg Ile Ser Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Lys Phe Asp Phe Val Thr Thr Ala Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Val Arg Gly Val Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
130 135 140
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
145 150 155 160
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
165 170 175
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
180 185 190
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
195 200 205
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
210 215 220
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
325 330 335
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
340 345 350
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
355 360 365
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
370 375 380
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
385 390 395 400
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
405 410 415
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
420 425 430
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg
435 440 445
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
450 455 460
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
465 470 475 480
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
485 490 495
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
500 505 510
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
515 520 525
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
530 535 540
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
545 550 555 560
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
565 570 575
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
580 585 590
Gln Ala Leu Pro Pro Arg
595
<210> 52
<211> 462
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 52
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
275 280 285
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
290 295 300
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
305 310 315 320
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
325 330 335
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val
340 345 350
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn
355 360 365
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
370 375 380
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
385 390 395 400
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
405 410 415
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
420 425 430
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
435 440 445
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 53
<211> 509
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 53
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
325 330 335
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
340 345 350
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
355 360 365
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
370 375 380
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys
385 390 395 400
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
405 410 415
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
420 425 430
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
435 440 445
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
450 455 460
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
465 470 475 480
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
485 490 495
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
500 505
<210> 54
<211> 556
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 54
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
325 330 335
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
340 345 350
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
355 360 365
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
370 375 380
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
385 390 395 400
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
405 410 415
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
420 425 430
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe
435 440 445
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu
450 455 460
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
465 470 475 480
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
485 490 495
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
500 505 510
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
515 520 525
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
530 535 540
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
545 550 555
<210> 55
<211> 504
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 55
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
275 280 285
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
290 295 300
Cys Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp
305 310 315 320
Tyr Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr
325 330 335
Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg
340 345 350
Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro
355 360 365
Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu
370 375 380
Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala
385 390 395 400
Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu
405 410 415
Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly
420 425 430
Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu
435 440 445
Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser
450 455 460
Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly
465 470 475 480
Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu
485 490 495
His Met Gln Ala Leu Pro Pro Arg
500
<210> 56
<211> 551
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 56
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
325 330 335
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
340 345 350
Asn His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr
355 360 365
Met Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln
370 375 380
Pro Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly
385 390 395 400
Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val
405 410 415
Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu
420 425 430
Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp
435 440 445
Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
450 455 460
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
465 470 475 480
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
485 490 495
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
500 505 510
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
515 520 525
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
530 535 540
Met Gln Ala Leu Pro Pro Arg
545 550
<210> 57
<211> 598
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 57
Asp Ile Lys Met Ala Gln Ser Pro Ser Ser Val Asn Ala Ser Leu Gly
1 5 10 15
Glu Arg Val Thr Ile Thr Cys Lys Ala Ser Arg Asp Ile Asn Asn Phe
20 25 30
Leu Ser Trp Phe His Gln Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile
35 40 45
Tyr Arg Ala Asn Arg Leu Val Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Gln Asp Tyr Ser Phe Thr Ile Ser Ser Leu Glu Tyr
65 70 75 80
Glu Asp Val Gly Ile Tyr Tyr Cys Leu Gln Tyr Gly Asp Leu Tyr Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Val Gln Leu Leu Glu Ser
115 120 125
Gly Pro Gly Leu Val Arg Pro Ser Gln Ser Leu Ser Leu Thr Cys Ser
130 135 140
Val Thr Gly Tyr Ser Ile Val Ser His Tyr Tyr Trp Asn Trp Ile Arg
145 150 155 160
Gln Phe Pro Gly Asn Lys Leu Glu Trp Met Gly Tyr Ile Ser Ser Asp
165 170 175
Gly Ser Asn Glu Tyr Asn Pro Ser Leu Lys Asn Arg Ile Ser Ile Ser
180 185 190
Leu Asp Thr Ser Lys Asn Gln Phe Phe Leu Lys Phe Asp Phe Val Thr
195 200 205
Thr Ala Asp Thr Ala Thr Tyr Phe Cys Val Arg Gly Val Asp Tyr Trp
210 215 220
Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Pro Thr Thr Thr Pro
225 230 235 240
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
245 250 255
Ser Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His
260 265 270
Thr Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala
275 280 285
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
290 295 300
Leu Arg Pro Glu Ala Ser Arg Pro Ala Ala Gly Gly Ala Val His Thr
305 310 315 320
Arg Gly Leu Asp Phe Ala Ser Asp Lys Pro Thr Thr Thr Pro Ala Pro
325 330 335
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
340 345 350
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
355 360 365
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
370 375 380
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Asn
385 390 395 400
His Arg Asn Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met
405 410 415
Asn Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro
420 425 430
Tyr Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg
435 440 445
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
450 455 460
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
465 470 475 480
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
485 490 495
Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
500 505 510
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
515 520 525
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
530 535 540
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
545 550 555 560
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
565 570 575
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
580 585 590
Gln Ala Leu Pro Pro Arg
595
<210> 58
<211> 22
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 58
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro
20
<210> 59
<211> 20
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 59
Met Arg Leu Pro Ala Gln Leu Leu Gly Leu Leu Met Leu Trp Val Pro
1 5 10 15
Gly Ser Ser Gly
20
<210> 60
<211> 18
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 60
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser
<210> 61
<211> 21
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 61
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro
20
<210> 62
<211> 21
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 62
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Ala
20
<210> 63
<211> 24
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 63
Met Lys Arg Phe Leu Phe Leu Leu Leu Thr Ile Ser Leu Leu Val Met
1 5 10 15
Val Gln Ile Gln Thr Gly Leu Ser
20
<210> 64
<211> 28
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 64
Met Gly Ala Gly Ala Thr Gly Arg Ala Met Asp Gly Pro Arg Leu Leu
1 5 10 15
Leu Leu Leu Leu Leu Gly Val Ser Leu Gly Gly Ala
20 25
<210> 65
<211> 335
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 65
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp Lys Cys Asn Leu
195 200 205
Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser Glu Cys Ile Gln
210 215 220
Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile Thr Cys Thr Gly
225 230 235 240
Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly Pro
245 250 255
His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly Glu Asn Asn Thr
260 265 270
Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys His
275 280 285
Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu Glu Gly Cys Pro
290 295 300
Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly Met Val Gly Ala
305 310 315 320
Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly Leu Phe Met
325 330 335
<210> 66
<211> 243
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 66
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
195 200 205
Gly Gly Ser Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys
210 215 220
Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val Arg Ser
225 230 235 240
Lys Arg Ser
<210> 67
<211> 297
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 67
Met Thr Thr Pro Arg Asn Ser Val Asn Gly Thr Phe Pro Ala Glu Pro
1 5 10 15
Met Lys Gly Pro Ile Ala Met Gln Ser Gly Pro Lys Pro Leu Phe Arg
20 25 30
Arg Met Ser Ser Leu Val Gly Pro Thr Gln Ser Phe Phe Met Arg Glu
35 40 45
Ser Lys Thr Leu Gly Ala Val Gln Ile Met Asn Gly Leu Phe His Ile
50 55 60
Ala Leu Gly Gly Leu Leu Met Ile Pro Ala Gly Ile Tyr Ala Pro Ile
65 70 75 80
Cys Val Thr Val Trp Tyr Pro Leu Trp Gly Gly Ile Met Tyr Ile Ile
85 90 95
Ser Gly Ser Leu Leu Ala Ala Thr Glu Lys Asn Ser Arg Lys Cys Leu
100 105 110
Val Lys Gly Lys Met Ile Met Asn Ser Leu Ser Leu Phe Ala Ala Ile
115 120 125
Ser Gly Met Ile Leu Ser Ile Met Asp Ile Leu Asn Ile Lys Ile Ser
130 135 140
His Phe Leu Lys Met Glu Ser Leu Asn Phe Ile Arg Ala His Thr Pro
145 150 155 160
Tyr Ile Asn Ile Tyr Asn Cys Glu Pro Ala Asn Pro Ser Glu Lys Asn
165 170 175
Ser Pro Ser Thr Gln Tyr Cys Tyr Ser Ile Gln Ser Leu Phe Leu Gly
180 185 190
Ile Leu Ser Val Met Leu Ile Phe Ala Phe Phe Gln Glu Leu Val Ile
195 200 205
Ala Gly Ile Val Glu Asn Glu Trp Lys Arg Thr Cys Ser Arg Pro Lys
210 215 220
Ser Asn Ile Val Leu Leu Ser Ala Glu Glu Lys Lys Glu Gln Thr Ile
225 230 235 240
Glu Ile Lys Glu Glu Val Val Gly Leu Thr Glu Thr Ser Ser Gln Pro
245 250 255
Lys Asn Glu Glu Asp Ile Glu Ile Ile Pro Ile Gln Glu Glu Glu Glu
260 265 270
Glu Glu Thr Glu Thr Asn Phe Pro Glu Pro Pro Gln Asp Gln Glu Ser
275 280 285
Ser Pro Ile Glu Asn Asp Ser Ser Pro
290 295
<210> 68
<211> 263
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 68
Met Thr Thr Pro Arg Asn Ser Val Asn Gly Thr Phe Pro Ala Glu Pro
1 5 10 15
Met Lys Gly Pro Ile Ala Met Gln Ser Gly Pro Lys Pro Leu Phe Arg
20 25 30
Arg Met Ser Ser Leu Val Gly Pro Thr Gln Ser Phe Phe Met Arg Glu
35 40 45
Ser Lys Thr Leu Gly Ala Val Gln Ile Met Asn Gly Leu Phe His Ile
50 55 60
Ala Leu Gly Gly Leu Leu Met Ile Pro Ala Gly Ile Tyr Ala Pro Ile
65 70 75 80
Cys Val Thr Val Trp Tyr Pro Leu Trp Gly Gly Ile Met Tyr Ile Ile
85 90 95
Ser Gly Ser Leu Leu Ala Ala Thr Glu Lys Asn Ser Arg Lys Cys Leu
100 105 110
Val Lys Gly Lys Met Ile Met Asn Ser Leu Ser Leu Phe Ala Ala Ile
115 120 125
Ser Gly Met Ile Leu Ser Ile Met Asp Ile Leu Asn Ile Lys Ile Ser
130 135 140
His Phe Leu Lys Met Glu Ser Leu Asn Phe Ile Arg Ala His Thr Pro
145 150 155 160
Tyr Ile Asn Ile Tyr Asn Cys Glu Pro Ala Asn Pro Ser Glu Lys Asn
165 170 175
Ser Pro Ser Thr Gln Tyr Cys Tyr Ser Ile Gln Ser Leu Phe Leu Gly
180 185 190
Ile Leu Ser Val Met Leu Ile Phe Ala Phe Phe Gln Glu Leu Val Ile
195 200 205
Ala Gly Ile Val Glu Asn Glu Trp Lys Arg Thr Cys Ser Arg Pro Lys
210 215 220
Ser Asn Ile Val Leu Leu Ser Ala Glu Glu Lys Lys Glu Gln Thr Ile
225 230 235 240
Glu Ile Lys Glu Glu Val Val Gly Leu Thr Glu Thr Ser Ser Gln Pro
245 250 255
Lys Asn Glu Glu Asp Ile Glu
260
<210> 69
<211> 395
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 69
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp
20 25 30
Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp
35 40 45
Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu
50 55 60
Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr
65 70 75 80
Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly
85 90 95
Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys
100 105 110
Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe
115 120 125
Ile Asn Thr Ser Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Leu Gln Ile Thr
145 150 155 160
Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val Lys Ser
165 170 175
Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly Phe Lys
180 185 190
Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn Lys Ala
195 200 205
Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile Arg Asp
210 215 220
Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val Thr Thr
225 230 235 240
Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly Lys Glu
245 250 255
Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr Thr Ala
260 265 270
Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro Ser Thr
275 280 285
Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr Pro Ser
290 295 300
Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser His Gln
305 310 315 320
Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr Val Ala Ile
325 330 335
Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val Ser Leu Leu
340 345 350
Ala Cys Tyr Leu Lys Ser Arg Gln Thr Pro Pro Leu Ala Ser Val Glu
355 360 365
Met Glu Ala Met Glu Ala Leu Pro Val Thr Trp Gly Thr Ser Ser Arg
370 375 380
Asp Glu Asp Leu Glu Asn Cys Ser His His Leu
385 390 395
<210> 70
<211> 114
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 70
Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys Ile Glu Asp Leu Ile
1 5 10 15
Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr Glu Ser Asp Val His
20 25 30
Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe Leu Leu Glu Leu Gln
35 40 45
Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile His Asp Thr Val Glu
50 55 60
Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser Ser Asn Gly Asn Val
65 70 75 80
Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu Glu Glu Lys Asn Ile
85 90 95
Lys Glu Phe Leu Gln Ser Phe Val His Ile Val Gln Met Phe Ile Asn
100 105 110
Thr Ser
<210> 71
<211> 237
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 71
Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp Val
1 5 10 15
Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser Gly
20 25 30
Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu Asn
35 40 45
Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys Ile
50 55 60
Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr Val
65 70 75 80
Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser Gly
85 90 95
Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala Thr
100 105 110
Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser Pro
115 120 125
Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly Thr
130 135 140
Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala Ser
145 150 155 160
His Gln Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr Val
165 170 175
Ala Ile Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val Ser
180 185 190
Leu Leu Ala Cys Tyr Leu Lys Ser Arg Gln Thr Pro Pro Leu Ala Ser
195 200 205
Val Glu Met Glu Ala Met Glu Ala Leu Pro Val Thr Trp Gly Thr Ser
210 215 220
Ser Arg Asp Glu Asp Leu Glu Asn Cys Ser His His Leu
225 230 235
<210> 72
<211> 18
<212> ПРТ
<213> Вирус Thosea asigna
<400> 72
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 73
<211> 25
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 73
Arg Ala Lys Arg Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys
1 5 10 15
Gly Asp Val Glu Glu Asn Pro Gly Pro
20 25
<210> 74
<211> 26
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 74
Arg Ala Lys Arg Ser Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr
1 5 10 15
Cys Gly Asp Val Glu Glu Asn Pro Gly Pro
20 25
<210> 75
<211> 19
<212> ПРТ
<213> Тешовирус свиньи 1
<400> 75
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 76
<211> 22
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 76
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 77
<211> 31
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 77
Arg Ala Lys Arg Ala Pro Val Lys Gln Gly Ser Gly Ala Thr Asn Phe
1 5 10 15
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
20 25 30
<210> 78
<211> 20
<212> ПРТ
<213> Вирус A ринита лошадей
<400> 78
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 79
<211> 22
<212> ПРТ
<213> Вирус ящура
<400> 79
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 80
<211> 8
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 80
Ala Pro Val Lys Gln Gly Ser Gly
1 5
<210> 81
<211> 4
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 81
Arg Ala Lys Arg
1
<210> 82
<211> 28
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 82
Arg Ala Lys Arg Ala Pro Val Lys Gln Thr Leu Asn Phe Asp Leu Leu
1 5 10 15
Lys Leu Ala Gly Asp Val Glu Ser Asn Pro Gly Pro
20 25
<210> 83
<211> 15
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 83
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 84
<211> 18
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 84
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 85
<211> 3
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 85
Gly Ser Gly
1
<210> 86
<211> 4
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 86
Ser Gly Ser Gly
1
<210> 87
<211> 86
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 87
Gly Pro Lys Lys Lys Arg Lys Val Ala Pro Pro Thr Asp Val Ser Leu
1 5 10 15
Gly Asp Glu Leu His Leu Asp Gly Glu Asp Val Ala Met Ala His Ala
20 25 30
Asp Ala Leu Asp Asp Phe Asp Leu Asp Met Leu Gly Asp Gly Asp Ser
35 40 45
Pro Gly Pro Gly Phe Thr Pro His Asp Ser Ala Pro Tyr Gly Ala Leu
50 55 60
Asp Met Ala Asp Phe Glu Phe Glu Gln Met Phe Thr Asp Ala Leu Gly
65 70 75 80
Ile Asp Glu Tyr Gly Gly
85
<210> 88
<211> 235
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 88
Glu Met Pro Val Asp Arg Ile Leu Glu Ala Glu Leu Ala Val Glu Gln
1 5 10 15
Lys Ser Asp Gln Gly Val Glu Gly Pro Gly Gly Thr Gly Gly Ser Gly
20 25 30
Ser Ser Pro Asn Asp Pro Val Thr Asn Ile Cys Gln Ala Ala Asp Lys
35 40 45
Gln Leu Phe Thr Leu Val Glu Trp Ala Lys Arg Ile Pro His Phe Ser
50 55 60
Ser Leu Pro Leu Asp Asp Gln Val Ile Leu Leu Arg Ala Gly Trp Asn
65 70 75 80
Glu Leu Leu Ile Ala Ser Phe Ser His Arg Ser Ile Asp Val Arg Asp
85 90 95
Gly Ile Leu Leu Ala Thr Gly Leu His Val His Arg Asn Ser Ala His
100 105 110
Ser Ala Gly Val Gly Ala Ile Phe Asp Arg Val Leu Thr Glu Leu Val
115 120 125
Ser Lys Met Arg Asp Met Arg Met Asp Lys Thr Glu Leu Gly Cys Leu
130 135 140
Arg Ala Ile Ile Leu Phe Asn Pro Glu Val Arg Gly Leu Lys Ser Ala
145 150 155 160
Gln Glu Val Glu Leu Leu Arg Glu Lys Val Tyr Ala Ala Leu Glu Glu
165 170 175
Tyr Thr Arg Thr Thr His Pro Asp Glu Pro Gly Arg Phe Ala Lys Leu
180 185 190
Leu Leu Arg Leu Pro Ser Leu Arg Ser Ile Gly Leu Lys Cys Leu Glu
195 200 205
His Leu Phe Phe Phe Arg Leu Ile Gly Asp Val Pro Ile Asp Thr Phe
210 215 220
Leu Met Glu Met Leu Glu Ser Pro Ser Asp Ser
225 230 235
<210> 89
<211> 323
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 89
Gly Pro Lys Lys Lys Arg Lys Val Ala Pro Pro Thr Asp Val Ser Leu
1 5 10 15
Gly Asp Glu Leu His Leu Asp Gly Glu Asp Val Ala Met Ala His Ala
20 25 30
Asp Ala Leu Asp Asp Phe Asp Leu Asp Met Leu Gly Asp Gly Asp Ser
35 40 45
Pro Gly Pro Gly Phe Thr Pro His Asp Ser Ala Pro Tyr Gly Ala Leu
50 55 60
Asp Met Ala Asp Phe Glu Phe Glu Gln Met Phe Thr Asp Ala Leu Gly
65 70 75 80
Ile Asp Glu Tyr Gly Gly Glu Phe Glu Met Pro Val Asp Arg Ile Leu
85 90 95
Glu Ala Glu Leu Ala Val Glu Gln Lys Ser Asp Gln Gly Val Glu Gly
100 105 110
Pro Gly Gly Thr Gly Gly Ser Gly Ser Ser Pro Asn Asp Pro Val Thr
115 120 125
Asn Ile Cys Gln Ala Ala Asp Lys Gln Leu Phe Thr Leu Val Glu Trp
130 135 140
Ala Lys Arg Ile Pro His Phe Ser Ser Leu Pro Leu Asp Asp Gln Val
145 150 155 160
Ile Leu Leu Arg Ala Gly Trp Asn Glu Leu Leu Ile Ala Ser Phe Ser
165 170 175
His Arg Ser Ile Asp Val Arg Asp Gly Ile Leu Leu Ala Thr Gly Leu
180 185 190
His Val His Arg Asn Ser Ala His Ser Ala Gly Val Gly Ala Ile Phe
195 200 205
Asp Arg Val Leu Thr Glu Leu Val Ser Lys Met Arg Asp Met Arg Met
210 215 220
Asp Lys Thr Glu Leu Gly Cys Leu Arg Ala Ile Ile Leu Phe Asn Pro
225 230 235 240
Glu Val Arg Gly Leu Lys Ser Ala Gln Glu Val Glu Leu Leu Arg Glu
245 250 255
Lys Val Tyr Ala Ala Leu Glu Glu Tyr Thr Arg Thr Thr His Pro Asp
260 265 270
Glu Pro Gly Arg Phe Ala Lys Leu Leu Leu Arg Leu Pro Ser Leu Arg
275 280 285
Ser Ile Gly Leu Lys Cys Leu Glu His Leu Phe Phe Phe Arg Leu Ile
290 295 300
Gly Asp Val Pro Ile Asp Thr Phe Leu Met Glu Met Leu Glu Ser Pro
305 310 315 320
Ser Asp Ser
<210> 90
<211> 150
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 90
Met Lys Leu Leu Ser Ser Ile Glu Gln Ala Cys Asp Ile Cys Arg Leu
1 5 10 15
Lys Lys Leu Lys Cys Ser Lys Glu Lys Pro Lys Cys Ala Lys Cys Leu
20 25 30
Lys Asn Asn Trp Glu Cys Arg Tyr Ser Pro Lys Thr Lys Arg Ser Pro
35 40 45
Leu Thr Arg Ala His Leu Thr Glu Val Glu Ser Arg Leu Glu Arg Leu
50 55 60
Glu Gln Leu Phe Leu Leu Ile Phe Pro Arg Glu Asp Leu Asp Met Ile
65 70 75 80
Leu Lys Met Asp Ser Leu Gln Asp Ile Lys Ala Leu Leu Thr Gly Leu
85 90 95
Phe Val Gln Asp Asn Val Asn Lys Asp Ala Val Thr Asp Arg Leu Ala
100 105 110
Ser Val Glu Thr Asp Met Pro Leu Thr Leu Arg Gln His Arg Ile Ser
115 120 125
Ala Thr Ser Ser Ser Glu Glu Ser Ser Asn Lys Gly Gln Arg Gln Leu
130 135 140
Thr Val Ser Pro Glu Phe
145 150
<210> 91
<211> 336
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 91
Ile Arg Pro Glu Cys Val Val Pro Glu Thr Gln Cys Ala Met Lys Arg
1 5 10 15
Lys Glu Lys Lys Ala Gln Lys Glu Lys Asp Lys Leu Pro Val Ser Thr
20 25 30
Thr Thr Val Asp Asp His Met Pro Pro Ile Met Gln Cys Glu Pro Pro
35 40 45
Pro Pro Glu Ala Ala Arg Ile His Glu Val Val Pro Arg Phe Leu Ser
50 55 60
Asp Lys Leu Leu Val Thr Asn Arg Gln Lys Asn Ile Pro Gln Leu Thr
65 70 75 80
Ala Asn Gln Gln Phe Leu Ile Ala Arg Leu Ile Trp Tyr Gln Asp Gly
85 90 95
Tyr Glu Gln Pro Ser Asp Glu Asp Leu Lys Arg Ile Thr Gln Thr Trp
100 105 110
Gln Gln Ala Asp Asp Glu Asn Glu Glu Ser Asp Thr Pro Phe Arg Gln
115 120 125
Ile Thr Glu Met Thr Ile Leu Thr Val Gln Leu Ile Val Glu Phe Ala
130 135 140
Lys Gly Leu Pro Gly Phe Ala Lys Ile Ser Gln Pro Asp Gln Ile Thr
145 150 155 160
Leu Leu Lys Ala Cys Ser Ser Glu Val Met Met Leu Arg Val Ala Arg
165 170 175
Arg Tyr Asp Ala Ala Ser Asp Ser Ile Leu Phe Ala Asn Asn Gln Ala
180 185 190
Tyr Thr Arg Asp Asn Tyr Arg Lys Ala Gly Met Ala Glu Val Ile Glu
195 200 205
Asp Leu Leu His Phe Cys Arg Cys Met Tyr Ser Met Ala Leu Asp Asn
210 215 220
Ile His Tyr Ala Leu Leu Thr Ala Val Val Ile Phe Ser Asp Arg Pro
225 230 235 240
Gly Leu Glu Gln Pro Gln Leu Val Glu Glu Ile Gln Arg Tyr Tyr Leu
245 250 255
Asn Thr Leu Arg Ile Tyr Ile Leu Asn Gln Leu Ser Gly Ser Ala Arg
260 265 270
Ser Ser Val Ile Tyr Gly Lys Ile Leu Ser Ile Leu Ser Glu Leu Arg
275 280 285
Thr Leu Gly Met Gln Asn Ser Asn Met Cys Ile Ser Leu Lys Leu Lys
290 295 300
Asn Arg Lys Leu Pro Pro Phe Leu Glu Glu Ile Trp Asp Val Ala Asp
305 310 315 320
Met Ser His Thr Gln Pro Pro Pro Ile Leu Glu Ser Pro Thr Asn Leu
325 330 335
<210> 92
<211> 335
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 92
Arg Pro Glu Cys Val Val Pro Glu Thr Gln Cys Ala Met Lys Arg Lys
1 5 10 15
Glu Lys Lys Ala Gln Lys Glu Lys Asp Lys Leu Pro Val Ser Thr Thr
20 25 30
Thr Val Asp Asp His Met Pro Pro Ile Met Gln Cys Glu Pro Pro Pro
35 40 45
Pro Glu Ala Ala Arg Ile His Glu Val Val Pro Arg Phe Leu Ser Asp
50 55 60
Lys Leu Leu Val Thr Asn Arg Gln Lys Asn Ile Pro Gln Leu Thr Ala
65 70 75 80
Asn Gln Gln Phe Leu Ile Ala Arg Leu Ile Trp Tyr Gln Asp Gly Tyr
85 90 95
Glu Gln Pro Ser Asp Glu Asp Leu Lys Arg Ile Thr Gln Thr Trp Gln
100 105 110
Gln Ala Asp Asp Glu Asn Glu Glu Ser Asp Thr Pro Phe Arg Gln Ile
115 120 125
Thr Glu Met Thr Ile Leu Thr Val Gln Leu Ile Val Glu Phe Ala Lys
130 135 140
Gly Leu Pro Gly Phe Ala Lys Ile Ser Gln Pro Asp Gln Ile Thr Leu
145 150 155 160
Leu Lys Ala Cys Ser Ser Glu Val Met Met Leu Arg Val Ala Arg Arg
165 170 175
Tyr Asp Ala Ala Ser Asp Ser Ile Leu Phe Ala Asn Asn Gln Ala Tyr
180 185 190
Thr Arg Asp Asn Tyr Arg Lys Ala Gly Met Ala Glu Val Ile Glu Asp
195 200 205
Leu Leu His Phe Cys Arg Cys Met Tyr Ser Met Ala Leu Asp Asn Ile
210 215 220
His Tyr Ala Leu Leu Thr Ala Val Val Ile Phe Ser Asp Arg Pro Gly
225 230 235 240
Leu Glu Gln Pro Gln Leu Val Glu Glu Ile Gln Arg Tyr Tyr Leu Asn
245 250 255
Thr Leu Arg Ile Tyr Ile Leu Asn Gln Leu Ser Gly Ser Ala Arg Ser
260 265 270
Ser Val Ile Tyr Gly Lys Ile Leu Ser Ile Leu Ser Glu Leu Arg Thr
275 280 285
Leu Gly Met Gln Asn Ser Asn Met Cys Ile Ser Leu Lys Leu Lys Asn
290 295 300
Arg Lys Leu Pro Pro Phe Leu Glu Glu Ile Trp Asp Val Ala Asp Met
305 310 315 320
Ser His Thr Gln Pro Pro Pro Ile Leu Glu Ser Pro Thr Asn Leu
325 330 335
<210> 93
<211> 488
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 93
Met Lys Leu Leu Ser Ser Ile Glu Gln Ala Cys Asp Ile Cys Arg Leu
1 5 10 15
Lys Lys Leu Lys Cys Ser Lys Glu Lys Pro Lys Cys Ala Lys Cys Leu
20 25 30
Lys Asn Asn Trp Glu Cys Arg Tyr Ser Pro Lys Thr Lys Arg Ser Pro
35 40 45
Leu Thr Arg Ala His Leu Thr Glu Val Glu Ser Arg Leu Glu Arg Leu
50 55 60
Glu Gln Leu Phe Leu Leu Ile Phe Pro Arg Glu Asp Leu Asp Met Ile
65 70 75 80
Leu Lys Met Asp Ser Leu Gln Asp Ile Lys Ala Leu Leu Thr Gly Leu
85 90 95
Phe Val Gln Asp Asn Val Asn Lys Asp Ala Val Thr Asp Arg Leu Ala
100 105 110
Ser Val Glu Thr Asp Met Pro Leu Thr Leu Arg Gln His Arg Ile Ser
115 120 125
Ala Thr Ser Ser Ser Glu Glu Ser Ser Asn Lys Gly Gln Arg Gln Leu
130 135 140
Thr Val Ser Pro Glu Phe Pro Gly Ile Arg Pro Glu Cys Val Val Pro
145 150 155 160
Glu Thr Gln Cys Ala Met Lys Arg Lys Glu Lys Lys Ala Gln Lys Glu
165 170 175
Lys Asp Lys Leu Pro Val Ser Thr Thr Thr Val Asp Asp His Met Pro
180 185 190
Pro Ile Met Gln Cys Glu Pro Pro Pro Pro Glu Ala Ala Arg Ile His
195 200 205
Glu Val Val Pro Arg Phe Leu Ser Asp Lys Leu Leu Val Thr Asn Arg
210 215 220
Gln Lys Asn Ile Pro Gln Leu Thr Ala Asn Gln Gln Phe Leu Ile Ala
225 230 235 240
Arg Leu Ile Trp Tyr Gln Asp Gly Tyr Glu Gln Pro Ser Asp Glu Asp
245 250 255
Leu Lys Arg Ile Thr Gln Thr Trp Gln Gln Ala Asp Asp Glu Asn Glu
260 265 270
Glu Ser Asp Thr Pro Phe Arg Gln Ile Thr Glu Met Thr Ile Leu Thr
275 280 285
Val Gln Leu Ile Val Glu Phe Ala Lys Gly Leu Pro Gly Phe Ala Lys
290 295 300
Ile Ser Gln Pro Asp Gln Ile Thr Leu Leu Lys Ala Cys Ser Ser Glu
305 310 315 320
Val Met Met Leu Arg Val Ala Arg Arg Tyr Asp Ala Ala Ser Asp Ser
325 330 335
Ile Leu Phe Ala Asn Asn Gln Ala Tyr Thr Arg Asp Asn Tyr Arg Lys
340 345 350
Ala Gly Met Ala Glu Val Ile Glu Asp Leu Leu His Phe Cys Arg Cys
355 360 365
Met Tyr Ser Met Ala Leu Asp Asn Ile His Tyr Ala Leu Leu Thr Ala
370 375 380
Val Val Ile Phe Ser Asp Arg Pro Gly Leu Glu Gln Pro Gln Leu Val
385 390 395 400
Glu Glu Ile Gln Arg Tyr Tyr Leu Asn Thr Leu Arg Ile Tyr Ile Leu
405 410 415
Asn Gln Leu Ser Gly Ser Ala Arg Ser Ser Val Ile Tyr Gly Lys Ile
420 425 430
Leu Ser Ile Leu Ser Glu Leu Arg Thr Leu Gly Met Gln Asn Ser Asn
435 440 445
Met Cys Ile Ser Leu Lys Leu Lys Asn Arg Lys Leu Pro Pro Phe Leu
450 455 460
Glu Glu Ile Trp Asp Val Ala Asp Met Ser His Thr Gln Pro Pro Pro
465 470 475 480
Ile Leu Glu Ser Pro Thr Asn Leu
485
<210> 94
<211> 487
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 94
Met Lys Leu Leu Ser Ser Ile Glu Gln Ala Cys Asp Ile Cys Arg Leu
1 5 10 15
Lys Lys Leu Lys Cys Ser Lys Glu Lys Pro Lys Cys Ala Lys Cys Leu
20 25 30
Lys Asn Asn Trp Glu Cys Arg Tyr Ser Pro Lys Thr Lys Arg Ser Pro
35 40 45
Leu Thr Arg Ala His Leu Thr Glu Val Glu Ser Arg Leu Glu Arg Leu
50 55 60
Glu Gln Leu Phe Leu Leu Ile Phe Pro Arg Glu Asp Leu Asp Met Ile
65 70 75 80
Leu Lys Met Asp Ser Leu Gln Asp Ile Lys Ala Leu Leu Thr Gly Leu
85 90 95
Phe Val Gln Asp Asn Val Asn Lys Asp Ala Val Thr Asp Arg Leu Ala
100 105 110
Ser Val Glu Thr Asp Met Pro Leu Thr Leu Arg Gln His Arg Ile Ser
115 120 125
Ala Thr Ser Ser Ser Glu Glu Ser Ser Asn Lys Gly Gln Arg Gln Leu
130 135 140
Thr Val Ser Pro Glu Phe Pro Gly Arg Pro Glu Cys Val Val Pro Glu
145 150 155 160
Thr Gln Cys Ala Met Lys Arg Lys Glu Lys Lys Ala Gln Lys Glu Lys
165 170 175
Asp Lys Leu Pro Val Ser Thr Thr Thr Val Asp Asp His Met Pro Pro
180 185 190
Ile Met Gln Cys Glu Pro Pro Pro Pro Glu Ala Ala Arg Ile His Glu
195 200 205
Val Val Pro Arg Phe Leu Ser Asp Lys Leu Leu Val Thr Asn Arg Gln
210 215 220
Lys Asn Ile Pro Gln Leu Thr Ala Asn Gln Gln Phe Leu Ile Ala Arg
225 230 235 240
Leu Ile Trp Tyr Gln Asp Gly Tyr Glu Gln Pro Ser Asp Glu Asp Leu
245 250 255
Lys Arg Ile Thr Gln Thr Trp Gln Gln Ala Asp Asp Glu Asn Glu Glu
260 265 270
Ser Asp Thr Pro Phe Arg Gln Ile Thr Glu Met Thr Ile Leu Thr Val
275 280 285
Gln Leu Ile Val Glu Phe Ala Lys Gly Leu Pro Gly Phe Ala Lys Ile
290 295 300
Ser Gln Pro Asp Gln Ile Thr Leu Leu Lys Ala Cys Ser Ser Glu Val
305 310 315 320
Met Met Leu Arg Val Ala Arg Arg Tyr Asp Ala Ala Ser Asp Ser Ile
325 330 335
Leu Phe Ala Asn Asn Gln Ala Tyr Thr Arg Asp Asn Tyr Arg Lys Ala
340 345 350
Gly Met Ala Glu Val Ile Glu Asp Leu Leu His Phe Cys Arg Cys Met
355 360 365
Tyr Ser Met Ala Leu Asp Asn Ile His Tyr Ala Leu Leu Thr Ala Val
370 375 380
Val Ile Phe Ser Asp Arg Pro Gly Leu Glu Gln Pro Gln Leu Val Glu
385 390 395 400
Glu Ile Gln Arg Tyr Tyr Leu Asn Thr Leu Arg Ile Tyr Ile Leu Asn
405 410 415
Gln Leu Ser Gly Ser Ala Arg Ser Ser Val Ile Tyr Gly Lys Ile Leu
420 425 430
Ser Ile Leu Ser Glu Leu Arg Thr Leu Gly Met Gln Asn Ser Asn Met
435 440 445
Cys Ile Ser Leu Lys Leu Lys Asn Arg Lys Leu Pro Pro Phe Leu Glu
450 455 460
Glu Ile Trp Asp Val Ala Asp Met Ser His Thr Gln Pro Pro Pro Ile
465 470 475 480
Leu Glu Ser Pro Thr Asn Leu
485
<210> 95
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 95
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaagcccgg ccaatctcct gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa gtgaagaga 339
<210> 96
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 96
gtgaagctgc aagagtccgg cggaggcttt gtgaagcctg gcggctctct gaaagtgtcc 60
tgtgccgcca gcggcttcac ctttagcagc tacgccatga gctgggtccg actgagccct 120
gagatgagac tggaatgggt cgccaccatc agtagcgcag gcggctacat cttctacagc 180
gactctgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagaag cggcgatacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttct 366
<210> 97
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 97
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagaga 339
<210> 98
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 98
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttct 366
<210> 99
<211> 318
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 99
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaag 318
<210> 100
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 100
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttct 339
<210> 101
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 101
gacatccaga tgacccagag cagcagcttc ctgagcgtgt cccttggcgg cagagtgacc 60
atcacctgta aagccagcga cctgatccac aactggctgg cctggtatca gcagaagcct 120
ggcaacgctc ccagactgct gattagcggc gccacctctc tggaaacagg cgtgccaagc 180
agattttccg gcagcggctc cggcaacgac tacacactgt ctattgccag cctgcagacc 240
gaggatgccg ccacctatta ctgccagcag tactggacca cacctttcac ctttggcagc 300
ggcaccaagc tggaaatcaa g 321
<210> 102
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 102
gacgttcagc tgcaagagtc tggccctggc ctggtcaatc ctagccagag cctgagcctg 60
acatgtaccg tgaccggcta cagcatcacc aacgactacg cctggaactg gatcagacag 120
ttccccggca acaagctgga atggatgggc tacatcaact acagcggcta caccacctac 180
aatcccagcc tgaagtcccg gatctccatc accagagaca ccagcaagaa ccagttcttc 240
ctgcacctga acagcgtgac caccgaggat accgccacct actactgcgc tagatgggat 300
ggcggcctga catattgggg ccagggaaca ctggtcaccg tgtctgct 348
<210> 103
<211> 324
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 103
gacatccaga tgacccagag ccccagcagc ctgagcgcca gcgtgggcga cagggtgacc 60
atcacctgca aggccagcga cctgatccac aactggctgg cctggtacca gcagaagccc 120
ggcaaggccc ccaagctgct gatcagcggc gccaccagcc tggagaccgg cgtgcccagc 180
aggttcagcg gcagcggcag cggcaccgac ttcaccctga ccatcagcag cctgcagccc 240
gaggacttcg ccacctacta ctgccagcag tactggacca cccccttcac cttcggccag 300
ggcaccaagg tggagatcaa gagg 324
<210> 104
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 104
gacatcgtgc tgacacagag ccctgccatc atgtctgcca gcctcggcga gcgagtgacc 60
atgacatgta cagccagcag cagcgtgtcc agcagctacc tgcattggta tcagcagaag 120
cccggcagca gccccaagct gtggatctac agcacaagca atctggccag cggcgtgcca 180
ggcagatttt ctggttctgg cagcggcacc agctacagcc tgacaatcag cagcatggaa 240
gccgaggatg ccgccaccta ctactgccac cagtaccaca gaagccccta cacctttggc 300
ggaggcacca aggtggaaat caagcgg 327
<210> 105
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 105
gaggttcagc tgcagcagtc tggcgccgaa cttgtgaaac ctggcgcctc tgtgaagctg 60
agctgtaccg ccagcggctt caacatcaag gacacctaca tgcactgggt caagcagagg 120
cctgagcagg gcctcgaatg gatcggaaga gtggatcccg ccaacggcaa caccaaatac 180
gaccccaagt tccagggcaa agccacactg accgccgaca cctctagcaa cacagcctac 240
ctgcagctgt ccagcctgac ctctgaagat accgccgtgt acttctgcgt gcgggactac 300
tacggccata cctacggctt cgccttctgc gaccaaggca caaccctgac agtgtctgct 360
<210> 106
<211> 327
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 106
gacatccaga tgacacagag ccctagcagc ctgtctgcca gcgtgggaga cagagtgacc 60
atcacctgta cagccagcag cagcgtgtcc agcagctacc tgcattggta tcagcagaag 120
cccggcaagg cccctaagct gctgatctac agcaccagca atctggccag cggcgtgcca 180
agcagatttt ctggctctgg cagcggcacc gacttcaccc tgaccatatc tagcctgcag 240
cctgaggact tcgccaccta ctactgccac cagtaccaca gaagccccta cacctttggc 300
cagggcacca aggtggaaat caagcgg 327
<210> 107
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 107
gaggtgcagc tggttgaatc tggcggagga ctggttcagc ctggcggatc tctgagactg 60
tcttgtgccg ccagcggctt caacatcaag gacacctaca tgcactgggt ccgacaggcc 120
cctggcaaag gacttgagtg ggttggaaga gtggaccccg ccaacggcaa caccaaatac 180
gaccccaagt tccagggcag attcaccatc agcgccgaca ccagcaagaa caccgcctac 240
ctgcagatga acagcctgag agccgaggac accgccgtgt actattgcgt gcgggattac 300
tacggccata cctacggctt cgccttttgg ggccagggca cactggttac cgttagctct 360
<210> 108
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 108
aagcccacca ccacccctgc ccctagacct ccaaccccag cccctacaat cgccagccag 60
cccctgagcc tgaggcccga agcctgtaga cctgccgctg gcggagccgt gcacaccaga 120
ggcctggatt tcgcctgcga c 141
<210> 109
<211> 282
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 109
aaacctacta caactcctgc cccccggcct cctacaccag ctcctactat cgcctcccag 60
ccactcagtc tcagacccga ggcttctagg ccagcggccg gaggcgcggt ccacacccgc 120
gggctggact ttgcatccga taagcccacc accacccctg cccctagacc tccaacccca 180
gcccctacaa tcgccagcca gcccctgagc ctgaggcccg aagcctgtag acctgccgct 240
ggcggagccg tgcacaccag aggcctggat ttcgcctgcg ac 282
<210> 110
<211> 423
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 110
aagcctacca ccacccccgc acctcgtcct ccaacccctg cacctacgat tgccagtcag 60
cctctttcac tgcggcctga ggccagcaga ccagctgccg gcggtgccgt ccatacaaga 120
ggactggact tcgcgtccga taaacctact accactccag ccccaaggcc cccaacccca 180
gcaccgacta tcgcatcaca gcctttgtca ctgcgtcctg aagccagccg gccagctgca 240
gggggggccg tccacacaag gggactcgac tttgcgagtg ataagcccac caccacccct 300
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 360
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 420
gac 423
<210> 111
<211> 564
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 111
aagcctacca ccacccccgc acctcgtcct ccaacccctg cacctacgat tgccagtcag 60
cctctttcac tgcggcctga ggccagcaga ccagctgccg gcggtgccgt ccatacaaga 120
ggactggact tcgcgtccga taaacctact accactccag ccccaaggcc cccaacccca 180
gcaccgacta tcgcatcaca gcctttgtca ctgcgtcctg aagccagccg gccagctgca 240
gggggggccg tccacacaag gggactcgac tttgcgagtg ataaacctac tacaactcct 300
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 360
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 420
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 480
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 540
agaggcctgg atttcgcctg cgac 564
<210> 112
<211> 84
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 112
atctacatct gggcccctct ggccggcacc tgtggcgtgc tgctgctgag cctggtcatc 60
accctgtact gcaaccaccg gaat 84
<210> 113
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 113
ttttgggtgc tggtggtggt tggtggagtc ctggcttgct atagcttgct agtaacagtg 60
gcctttatta ttttctgggt g 81
<210> 114
<211> 126
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 114
aagagaggcc ggaagaaact gctgtacatc ttcaagcagc ccttcatgcg gcccgtgcag 60
accacccagg aagaggacgg ctgcagctgc cggttccccg aggaagagga aggcggctgc 120
gaactg 126
<210> 115
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 115
aggagcaagc ggagcagagg cggccacagc gactacatga acatgacccc ccggaggcct 60
ggccccaccc ggaagcacta ccagccctac gcccctccca gggacttcgc cgcctaccgg 120
agc 123
<210> 116
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 116
ctgtgcgcac gcccacgccg cagccccgcc caagaagatg gcaaagtcta catcaacatg 60
ccaggcaggg gc 72
<210> 117
<211> 156
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 117
tacttcctgg gccggctggt ccctcggggg cgaggggctg cggaggcagc gacccggaaa 60
cagcgtatca ctgagaccga gtcgccttat caggagctcc agggtcagag gtcggatgtc 120
tacagcgacc tcaacacaca gaggccgtat tacaaa 156
<210> 118
<211> 336
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 118
cgggtgaagt tcagccggag cgccgacgcc cctgcctacc agcagggcca gaaccagctg 60
tacaacgagc tgaacctggg ccggagggag gagtacgacg tgctggacaa gcggagaggc 120
cgggaccctg agatgggcgg caagccccgg agaaagaacc ctcaggaggg cctgtataac 180
gaactgcaga aagacaagat ggccgaggcc tacagcgaga tcggcatgaa gggcgagcgg 240
cggaggggca agggccacga cggcctgtac cagggcctga gcaccgccac caaggatacc 300
tacgacgccc tgcacatgca ggccctgccc cccaga 336
<210> 119
<211> 1437
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 119
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcccacca ccacccctgc ccctagacct 780
ccaaccccag cccctacaat cgccagccag cccctgagcc tgaggcccga agcctgtaga 840
cctgccgctg gcggagccgt gcacaccaga ggcctggatt tcgcctgcga catctacatc 900
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 960
tgcaaccacc ggaataagag aggccggaag aaactgctgt acatcttcaa gcagcccttc 1020
atgcggcccg tgcagaccac ccaggaagag gacggctgca gctgccggtt ccccgaggaa 1080
gaggaaggcg gctgcgaact gcgggtgaag ttcagccgga gcgccgacgc ccctgcctac 1140
cagcagggcc agaaccagct gtacaacgag ctgaacctgg gccggaggga ggagtacgac 1200
gtgctggaca agcggagagg ccgggaccct gagatgggcg gcaagccccg gagaaagaac 1260
cctcaggagg gcctgtataa cgaactgcag aaagacaaga tggccgaggc ctacagcgag 1320
atcggcatga agggcgagcg gcggaggggc aagggccacg acggcctgta ccagggcctg 1380
agcaccgcca ccaaggatac ctacgacgcc ctgcacatgc aggccctgcc ccccaga 1437
<210> 120
<211> 1578
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 120
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aaacctacta caactcctgc cccccggcct 780
cctacaccag ctcctactat cgcctcccag ccactcagtc tcagacccga ggcttctagg 840
ccagcggccg gaggcgcggt ccacacccgc gggctggact ttgcatccga taagcccacc 900
accacccctg cccctagacc tccaacccca gcccctacaa tcgccagcca gcccctgagc 960
ctgaggcccg aagcctgtag acctgccgct ggcggagccg tgcacaccag aggcctggat 1020
ttcgcctgcg acatctacat ctgggcccct ctggccggca cctgtggcgt gctgctgctg 1080
agcctggtca tcaccctgta ctgcaaccac cggaataaga gaggccggaa gaaactgctg 1140
tacatcttca agcagccctt catgcggccc gtgcagacca cccaggaaga ggacggctgc 1200
agctgccggt tccccgagga agaggaaggc ggctgcgaac tgcgggtgaa gttcagccgg 1260
agcgccgacg cccctgccta ccagcagggc cagaaccagc tgtacaacga gctgaacctg 1320
ggccggaggg aggagtacga cgtgctggac aagcggagag gccgggaccc tgagatgggc 1380
ggcaagcccc ggagaaagaa ccctcaggag ggcctgtata acgaactgca gaaagacaag 1440
atggccgagg cctacagcga gatcggcatg aagggcgagc ggcggagggg caagggccac 1500
gacggcctgt accagggcct gagcaccgcc accaaggata cctacgacgc cctgcacatg 1560
caggccctgc cccccaga 1578
<210> 121
<211> 1719
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 121
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcctacca ccacccccgc acctcgtcct 780
ccaacccctg cacctacgat tgccagtcag cctctttcac tgcggcctga ggccagcaga 840
ccagctgccg gcggtgccgt ccatacaaga ggactggact tcgcgtccga taaacctact 900
accactccag ccccaaggcc cccaacccca gcaccgacta tcgcatcaca gcctttgtca 960
ctgcgtcctg aagccagccg gccagctgca gggggggccg tccacacaag gggactcgac 1020
tttgcgagtg ataagcccac caccacccct gcccctagac ctccaacccc agcccctaca 1080
atcgccagcc agcccctgag cctgaggccc gaagcctgta gacctgccgc tggcggagcc 1140
gtgcacacca gaggcctgga tttcgcctgc gacatctaca tctgggcccc tctggccggc 1200
acctgtggcg tgctgctgct gagcctggtc atcaccctgt actgcaacca ccggaataag 1260
agaggccgga agaaactgct gtacatcttc aagcagccct tcatgcggcc cgtgcagacc 1320
acccaggaag aggacggctg cagctgccgg ttccccgagg aagaggaagg cggctgcgaa 1380
ctgcgggtga agttcagccg gagcgccgac gcccctgcct accagcaggg ccagaaccag 1440
ctgtacaacg agctgaacct gggccggagg gaggagtacg acgtgctgga caagcggaga 1500
ggccgggacc ctgagatggg cggcaagccc cggagaaaga accctcagga gggcctgtat 1560
aacgaactgc agaaagacaa gatggccgag gcctacagcg agatcggcat gaagggcgag 1620
cggcggaggg gcaagggcca cgacggcctg taccagggcc tgagcaccgc caccaaggat 1680
acctacgacg ccctgcacat gcaggccctg ccccccaga 1719
<210> 122
<211> 1455
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 122
atgctgctgc tggtgaccag cctgctgctg tgtgagctgc cccaccccgc ctttctgctg 60
atccccgaca tcaagatggc tcagtcccct tctagcgtga atgcttcgct aggggagcgt 120
gtgaccatca catgtaaagc atcacgcgac ataaataatt tcctttcctg gtttcatcag 180
aaaccgggca agtcgcctaa gacgctgatt tacagagcaa atcggttggt agatggagtg 240
ccaagcagat tcagcgggag cggaagtgga caggattata gcttcactat ttcatccctg 300
gaatacgagg acgtaggtat ctattattgc ctccagtatg gcgatcttta cacatttggt 360
ggggggacta agctggagat taagggcgga ggcggaagcg gaggcggagg ctccggcgga 420
ggcggaagcg acgtgcaact tctggagagc gggccagggc tagtcaggcc ctcccagtcg 480
ctttcactga cttgcagtgt gaccggttac tctattgtga gtcactacta ttggaactgg 540
attcggcagt tcccaggcaa caaactggaa tggatggggt acatatcttc cgatggctcg 600
aatgaatata acccatcatt gaaaaatcgt atttccatca gtctggatac gagtaaaaac 660
cagtttttcc tcaaattcga tttcgtgact acagcagata ctgccacata cttctgtgta 720
cgaggtgtcg attattgggg acagggcaca acgctgaccg taagttctaa gcccaccacc 780
acccctgccc ctagacctcc aaccccagcc cctacaatcg ccagccagcc cctgagcctg 840
aggcccgaag cctgtagacc tgccgctggc ggagccgtgc acaccagagg cctggatttc 900
gcctgcgaca tctacatctg ggcccctctg gccggcacct gtggcgtgct gctgctgagc 960
ctggtcatca ccctgtactg caaccaccgg aataagagag gccggaagaa actgctgtac 1020
atcttcaagc agcccttcat gcggcccgtg cagaccaccc aggaagagga cggctgcagc 1080
tgccggttcc ccgaggaaga ggaaggcggc tgcgaactgc gggtgaagtt cagccggagc 1140
gccgacgccc ctgcctacca gcagggccag aaccagctgt acaacgagct gaacctgggc 1200
cggagggagg agtacgacgt gctggacaag cggagaggcc gggaccctga gatgggcggc 1260
aagccccgga gaaagaaccc tcaggagggc ctgtataacg aactgcagaa agacaagatg 1320
gccgaggcct acagcgagat cggcatgaag ggcgagcggc ggaggggcaa gggccacgac 1380
ggcctgtacc agggcctgag caccgccacc aaggatacct acgacgccct gcacatgcag 1440
gccctgcccc ccaga 1455
<210> 123
<211> 1389
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 123
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcccac caccacccct 720
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 780
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 840
gacatctaca tctgggcccc tctggccggc acctgtggcg tgctgctgct gagcctggtc 900
atcaccctgt actgcaacca ccggaataag agaggccgga agaaactgct gtacatcttc 960
aagcagccct tcatgcggcc cgtgcagacc acccaggaag aggacggctg cagctgccgg 1020
ttccccgagg aagaggaagg cggctgcgaa ctgcgggtga agttcagccg gagcgccgac 1080
gcccctgcct accagcaggg ccagaaccag ctgtacaacg agctgaacct gggccggagg 1140
gaggagtacg acgtgctgga caagcggaga ggccgggacc ctgagatggg cggcaagccc 1200
cggagaaaga accctcagga gggcctgtat aacgaactgc agaaagacaa gatggccgag 1260
gcctacagcg agatcggcat gaagggcgag cggcggaggg gcaagggcca cgacggcctg 1320
taccagggcc tgagcaccgc caccaaggat acctacgacg ccctgcacat gcaggccctg 1380
ccccccaga 1389
<210> 124
<211> 1530
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 124
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaaacctac tacaactcct 720
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 780
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 840
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 900
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 960
agaggcctgg atttcgcctg cgacatctac atctgggccc ctctggccgg cacctgtggc 1020
gtgctgctgc tgagcctggt catcaccctg tactgcaacc accggaataa gagaggccgg 1080
aagaaactgc tgtacatctt caagcagccc ttcatgcggc ccgtgcagac cacccaggaa 1140
gaggacggct gcagctgccg gttccccgag gaagaggaag gcggctgcga actgcgggtg 1200
aagttcagcc ggagcgccga cgcccctgcc taccagcagg gccagaacca gctgtacaac 1260
gagctgaacc tgggccggag ggaggagtac gacgtgctgg acaagcggag aggccgggac 1320
cctgagatgg gcggcaagcc ccggagaaag aaccctcagg agggcctgta taacgaactg 1380
cagaaagaca agatggccga ggcctacagc gagatcggca tgaagggcga gcggcggagg 1440
ggcaagggcc acgacggcct gtaccagggc ctgagcaccg ccaccaagga tacctacgac 1500
gccctgcaca tgcaggccct gccccccaga 1530
<210> 125
<211> 1671
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 125
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcctac caccaccccc 720
gcacctcgtc ctccaacccc tgcacctacg attgccagtc agcctctttc actgcggcct 780
gaggccagca gaccagctgc cggcggtgcc gtccatacaa gaggactgga cttcgcgtcc 840
gataaaccta ctaccactcc agccccaagg cccccaaccc cagcaccgac tatcgcatca 900
cagcctttgt cactgcgtcc tgaagccagc cggccagctg cagggggggc cgtccacaca 960
aggggactcg actttgcgag tgataagccc accaccaccc ctgcccctag acctccaacc 1020
ccagccccta caatcgccag ccagcccctg agcctgaggc ccgaagcctg tagacctgcc 1080
gctggcggag ccgtgcacac cagaggcctg gatttcgcct gcgacatcta catctgggcc 1140
cctctggccg gcacctgtgg cgtgctgctg ctgagcctgg tcatcaccct gtactgcaac 1200
caccggaata agagaggccg gaagaaactg ctgtacatct tcaagcagcc cttcatgcgg 1260
cccgtgcaga ccacccagga agaggacggc tgcagctgcc ggttccccga ggaagaggaa 1320
ggcggctgcg aactgcgggt gaagttcagc cggagcgccg acgcccctgc ctaccagcag 1380
ggccagaacc agctgtacaa cgagctgaac ctgggccgga gggaggagta cgacgtgctg 1440
gacaagcgga gaggccggga ccctgagatg ggcggcaagc cccggagaaa gaaccctcag 1500
gagggcctgt ataacgaact gcagaaagac aagatggccg aggcctacag cgagatcggc 1560
atgaagggcg agcggcggag gggcaagggc cacgacggcc tgtaccaggg cctgagcacc 1620
gccaccaagg atacctacga cgccctgcac atgcaggccc tgccccccag a 1671
<210> 126
<211> 1434
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 126
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcccacca ccacccctgc ccctagacct 780
ccaaccccag cccctacaat cgccagccag cccctgagcc tgaggcccga agcctgtaga 840
cctgccgctg gcggagccgt gcacaccaga ggcctggatt tcgcctgcga catctacatc 900
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 960
tgcaaccacc ggaataggag caagcggagc agaggcggcc acagcgacta catgaacatg 1020
accccccgga ggcctggccc cacccggaag cactaccagc cctacgcccc tcccagggac 1080
ttcgccgcct accggagccg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1140
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1200
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1260
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1320
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1380
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc caga 1434
<210> 127
<211> 1575
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 127
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aaacctacta caactcctgc cccccggcct 780
cctacaccag ctcctactat cgcctcccag ccactcagtc tcagacccga ggcttctagg 840
ccagcggccg gaggcgcggt ccacacccgc gggctggact ttgcatccga taagcccacc 900
accacccctg cccctagacc tccaacccca gcccctacaa tcgccagcca gcccctgagc 960
ctgaggcccg aagcctgtag acctgccgct ggcggagccg tgcacaccag aggcctggat 1020
ttcgcctgcg acatctacat ctgggcccct ctggccggca cctgtggcgt gctgctgctg 1080
agcctggtca tcaccctgta ctgcaaccac cggaatagga gcaagcggag cagaggcggc 1140
cacagcgact acatgaacat gaccccccgg aggcctggcc ccacccggaa gcactaccag 1200
ccctacgccc ctcccaggga cttcgccgcc taccggagcc gggtgaagtt cagccggagc 1260
gccgacgccc ctgcctacca gcagggccag aaccagctgt acaacgagct gaacctgggc 1320
cggagggagg agtacgacgt gctggacaag cggagaggcc gggaccctga gatgggcggc 1380
aagccccgga gaaagaaccc tcaggagggc ctgtataacg aactgcagaa agacaagatg 1440
gccgaggcct acagcgagat cggcatgaag ggcgagcggc ggaggggcaa gggccacgac 1500
ggcctgtacc agggcctgag caccgccacc aaggatacct acgacgccct gcacatgcag 1560
gccctgcccc ccaga 1575
<210> 128
<211> 1716
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 128
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcctacca ccacccccgc acctcgtcct 780
ccaacccctg cacctacgat tgccagtcag cctctttcac tgcggcctga ggccagcaga 840
ccagctgccg gcggtgccgt ccatacaaga ggactggact tcgcgtccga taaacctact 900
accactccag ccccaaggcc cccaacccca gcaccgacta tcgcatcaca gcctttgtca 960
ctgcgtcctg aagccagccg gccagctgca gggggggccg tccacacaag gggactcgac 1020
tttgcgagtg ataagcccac caccacccct gcccctagac ctccaacccc agcccctaca 1080
atcgccagcc agcccctgag cctgaggccc gaagcctgta gacctgccgc tggcggagcc 1140
gtgcacacca gaggcctgga tttcgcctgc gacatctaca tctgggcccc tctggccggc 1200
acctgtggcg tgctgctgct gagcctggtc atcaccctgt actgcaacca ccggaatagg 1260
agcaagcgga gcagaggcgg ccacagcgac tacatgaaca tgaccccccg gaggcctggc 1320
cccacccgga agcactacca gccctacgcc cctcccaggg acttcgccgc ctaccggagc 1380
cgggtgaagt tcagccggag cgccgacgcc cctgcctacc agcagggcca gaaccagctg 1440
tacaacgagc tgaacctggg ccggagggag gagtacgacg tgctggacaa gcggagaggc 1500
cgggaccctg agatgggcgg caagccccgg agaaagaacc ctcaggaggg cctgtataac 1560
gaactgcaga aagacaagat ggccgaggcc tacagcgaga tcggcatgaa gggcgagcgg 1620
cggaggggca agggccacga cggcctgtac cagggcctga gcaccgccac caaggatacc 1680
tacgacgccc tgcacatgca ggccctgccc cccaga 1716
<210> 129
<211> 1560
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 129
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcccacca ccacccctgc ccctagacct 780
ccaaccccag cccctacaat cgccagccag cccctgagcc tgaggcccga agcctgtaga 840
cctgccgctg gcggagccgt gcacaccaga ggcctggatt tcgcctgcga catctacatc 900
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 960
tgcaaccacc ggaataggag caagcggagc agaggcggcc acagcgacta catgaacatg 1020
accccccgga ggcctggccc cacccggaag cactaccagc cctacgcccc tcccagggac 1080
ttcgccgcct accggagcaa gagaggccgg aagaaactgc tgtacatctt caagcagccc 1140
ttcatgcggc ccgtgcagac cacccaggaa gaggacggct gcagctgccg gttccccgag 1200
gaagaggaag gcggctgcga actgcgggtg aagttcagcc ggagcgccga cgcccctgcc 1260
taccagcagg gccagaacca gctgtacaac gagctgaacc tgggccggag ggaggagtac 1320
gacgtgctgg acaagcggag aggccgggac cctgagatgg gcggcaagcc ccggagaaag 1380
aaccctcagg agggcctgta taacgaactg cagaaagaca agatggccga ggcctacagc 1440
gagatcggca tgaagggcga gcggcggagg ggcaagggcc acgacggcct gtaccagggc 1500
ctgagcaccg ccaccaagga tacctacgac gccctgcaca tgcaggccct gccccccaga 1560
<210> 130
<211> 1701
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 130
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aaacctacta caactcctgc cccccggcct 780
cctacaccag ctcctactat cgcctcccag ccactcagtc tcagacccga ggcttctagg 840
ccagcggccg gaggcgcggt ccacacccgc gggctggact ttgcatccga taagcccacc 900
accacccctg cccctagacc tccaacccca gcccctacaa tcgccagcca gcccctgagc 960
ctgaggcccg aagcctgtag acctgccgct ggcggagccg tgcacaccag aggcctggat 1020
ttcgcctgcg acatctacat ctgggcccct ctggccggca cctgtggcgt gctgctgctg 1080
agcctggtca tcaccctgta ctgcaaccac cggaatagga gcaagcggag cagaggcggc 1140
cacagcgact acatgaacat gaccccccgg aggcctggcc ccacccggaa gcactaccag 1200
ccctacgccc ctcccaggga cttcgccgcc taccggagca agagaggccg gaagaaactg 1260
ctgtacatct tcaagcagcc cttcatgcgg cccgtgcaga ccacccagga agaggacggc 1320
tgcagctgcc ggttccccga ggaagaggaa ggcggctgcg aactgcgggt gaagttcagc 1380
cggagcgccg acgcccctgc ctaccagcag ggccagaacc agctgtacaa cgagctgaac 1440
ctgggccgga gggaggagta cgacgtgctg gacaagcgga gaggccggga ccctgagatg 1500
ggcggcaagc cccggagaaa gaaccctcag gagggcctgt ataacgaact gcagaaagac 1560
aagatggccg aggcctacag cgagatcggc atgaagggcg agcggcggag gggcaagggc 1620
cacgacggcc tgtaccaggg cctgagcacc gccaccaagg atacctacga cgccctgcac 1680
atgcaggccc tgccccccag a 1701
<210> 131
<211> 1842
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 131
gtgaagctgg aagagtccgg cggaggcttt gtgaagcctg gcggaagcct gaagatcagc 60
tgtgccgcca gcggcttcac cttcagaaac tacgccatga gctgggtccg actgagcccc 120
gagatgagac tggaatgggt cgccacaatc agcagcgcag gcggctacat cttctacagc 180
gatagcgtgc agggcagatt caccatcagc cgggacaacg ccaagaacac cctgcacctc 240
cagatgggca gtctgagatc tggcgacacc gccatgtact actgcgccag acaaggcttc 300
ggcaactacg gcgactacta tgccatggat tactggggcc agggcaccac cgtgacagtc 360
tcttctggtg gcggtggctc gggcggtggt gggtcgggtg gcggcggatc tgacatcgag 420
ctgacacaga gcccatctag cctggctgtg tctgccggcg agaaagtgac catgagctgc 480
aagagcagcc agagcctgct gaacagccgg accagaaaga atcagctggc ctggtatcag 540
cagaaaaccg gacagagccc cgagctgctg atctactggg ccagcacaag acagagcggc 600
gtgcccgata gattcacagg atctggcagc ggcaccgact tcaccctgac aatcagttct 660
gtgcaggccg aggacctggc cgtgtactac tgtcagcaga gctacaacct gctgaccttc 720
ggacccggca ccaagctgga aatcaagaga aagcctacca ccacccccgc acctcgtcct 780
ccaacccctg cacctacgat tgccagtcag cctctttcac tgcggcctga ggccagcaga 840
ccagctgccg gcggtgccgt ccatacaaga ggactggact tcgcgtccga taaacctact 900
accactccag ccccaaggcc cccaacccca gcaccgacta tcgcatcaca gcctttgtca 960
ctgcgtcctg aagccagccg gccagctgca gggggggccg tccacacaag gggactcgac 1020
tttgcgagtg ataagcccac caccacccct gcccctagac ctccaacccc agcccctaca 1080
atcgccagcc agcccctgag cctgaggccc gaagcctgta gacctgccgc tggcggagcc 1140
gtgcacacca gaggcctgga tttcgcctgc gacatctaca tctgggcccc tctggccggc 1200
acctgtggcg tgctgctgct gagcctggtc atcaccctgt actgcaacca ccggaatagg 1260
agcaagcgga gcagaggcgg ccacagcgac tacatgaaca tgaccccccg gaggcctggc 1320
cccacccgga agcactacca gccctacgcc cctcccaggg acttcgccgc ctaccggagc 1380
aagagaggcc ggaagaaact gctgtacatc ttcaagcagc ccttcatgcg gcccgtgcag 1440
accacccagg aagaggacgg ctgcagctgc cggttccccg aggaagagga aggcggctgc 1500
gaactgcggg tgaagttcag ccggagcgcc gacgcccctg cctaccagca gggccagaac 1560
cagctgtaca acgagctgaa cctgggccgg agggaggagt acgacgtgct ggacaagcgg 1620
agaggccggg accctgagat gggcggcaag ccccggagaa agaaccctca ggagggcctg 1680
tataacgaac tgcagaaaga caagatggcc gaggcctaca gcgagatcgg catgaagggc 1740
gagcggcgga ggggcaaggg ccacgacggc ctgtaccagg gcctgagcac cgccaccaag 1800
gatacctacg acgccctgca catgcaggcc ctgcccccca ga 1842
<210> 132
<211> 1434
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 132
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aagcccacca ccacccctgc ccctagacct 780
ccaaccccag cccctacaat cgccagccag cccctgagcc tgaggcccga agcctgtaga 840
cctgccgctg gcggagccgt gcacaccaga ggcctggatt tcgcctgcga catctacatc 900
tgggcccctc tggccggcac ctgtggcgtg ctgctgctga gcctggtcat caccctgtac 960
tgcaaccacc ggaataggag caagcggagc agaggcggcc acagcgacta catgaacatg 1020
accccccgga ggcctggccc cacccggaag cactaccagc cctacgcccc tcccagggac 1080
ttcgccgcct accggagccg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1140
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1200
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1260
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1320
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1380
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc caga 1434
<210> 133
<211> 1575
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 133
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aaacctacta caactcctgc cccccggcct 780
cctacaccag ctcctactat cgcctcccag ccactcagtc tcagacccga ggcttctagg 840
ccagcggccg gaggcgcggt ccacacccgc gggctggact ttgcatccga taagcccacc 900
accacccctg cccctagacc tccaacccca gcccctacaa tcgccagcca gcccctgagc 960
ctgaggcccg aagcctgtag acctgccgct ggcggagccg tgcacaccag aggcctggat 1020
ttcgcctgcg acatctacat ctgggcccct ctggccggca cctgtggcgt gctgctgctg 1080
agcctggtca tcaccctgta ctgcaaccac cggaatagga gcaagcggag cagaggcggc 1140
cacagcgact acatgaacat gaccccccgg aggcctggcc ccacccggaa gcactaccag 1200
ccctacgccc ctcccaggga cttcgccgcc taccggagcc gggtgaagtt cagccggagc 1260
gccgacgccc ctgcctacca gcagggccag aaccagctgt acaacgagct gaacctgggc 1320
cggagggagg agtacgacgt gctggacaag cggagaggcc gggaccctga gatgggcggc 1380
aagccccgga gaaagaaccc tcaggagggc ctgtataacg aactgcagaa agacaagatg 1440
gccgaggcct acagcgagat cggcatgaag ggcgagcggc ggaggggcaa gggccacgac 1500
ggcctgtacc agggcctgag caccgccacc aaggatacct acgacgccct gcacatgcag 1560
gccctgcccc ccaga 1575
<210> 134
<211> 1209
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 134
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aggagcaagc ggagcagagg cggccacagc 780
gactacatga acatgacccc ccggaggcct ggccccaccc ggaagcacta ccagccctac 840
gcccctccca gggacttcgc cgcctaccgg agccgggtga agttcagccg gagcgccgac 900
gcccctgcct accagcaggg ccagaaccag ctgtacaacg agctgaacct gggccggagg 960
gaggagtacg acgtgctgga caagcggaga ggccgggacc ctgagatggg cggcaagccc 1020
cggagaaaga accctcagga gggcctgtat aacgaactgc agaaagacaa gatggccgag 1080
gcctacagcg agatcggcat gaagggcgag cggcggaggg gcaagggcca cgacggcctg 1140
taccagggcc tgagcaccgc caccaaggat acctacgacg ccctgcacat gcaggccctg 1200
ccccccaga 1209
<210> 135
<211> 1335
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 135
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aggagcaagc ggagcagagg cggccacagc 780
gactacatga acatgacccc ccggaggcct ggccccaccc ggaagcacta ccagccctac 840
gcccctccca gggacttcgc cgcctaccgg agcaagagag gccggaagaa actgctgtac 900
atcttcaagc agcccttcat gcggcccgtg cagaccaccc aggaagagga cggctgcagc 960
tgccggttcc ccgaggaaga ggaaggcggc tgcgaactgc gggtgaagtt cagccggagc 1020
gccgacgccc ctgcctacca gcagggccag aaccagctgt acaacgagct gaacctgggc 1080
cggagggagg agtacgacgt gctggacaag cggagaggcc gggaccctga gatgggcggc 1140
aagccccgga gaaagaaccc tcaggagggc ctgtataacg aactgcagaa agacaagatg 1200
gccgaggcct acagcgagat cggcatgaag ggcgagcggc ggaggggcaa gggccacgac 1260
ggcctgtacc agggcctgag caccgccacc aaggatacct acgacgccct gcacatgcag 1320
gccctgcccc ccaga 1335
<210> 136
<211> 1701
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 136
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aaacctacta caactcctgc cccccggcct 780
cctacaccag ctcctactat cgcctcccag ccactcagtc tcagacccga ggcttctagg 840
ccagcggccg gaggcgcggt ccacacccgc gggctggact ttgcatccga taagcccacc 900
accacccctg cccctagacc tccaacccca gcccctacaa tcgccagcca gcccctgagc 960
ctgaggcccg aagcctgtag acctgccgct ggcggagccg tgcacaccag aggcctggat 1020
ttcgcctgcg acatctacat ctgggcccct ctggccggca cctgtggcgt gctgctgctg 1080
agcctggtca tcaccctgta ctgcaaccac cggaatagga gcaagcggag cagaggcggc 1140
cacagcgact acatgaacat gaccccccgg aggcctggcc ccacccggaa gcactaccag 1200
ccctacgccc ctcccaggga cttcgccgcc taccggagca agagaggccg gaagaaactg 1260
ctgtacatct tcaagcagcc cttcatgcgg cccgtgcaga ccacccagga agaggacggc 1320
tgcagctgcc ggttccccga ggaagaggaa ggcggctgcg aactgcgggt gaagttcagc 1380
cggagcgccg acgcccctgc ctaccagcag ggccagaacc agctgtacaa cgagctgaac 1440
ctgggccgga gggaggagta cgacgtgctg gacaagcgga gaggccggga ccctgagatg 1500
ggcggcaagc cccggagaaa gaaccctcag gagggcctgt ataacgaact gcagaaagac 1560
aagatggccg aggcctacag cgagatcggc atgaagggcg agcggcggag gggcaagggc 1620
cacgacggcc tgtaccaggg cctgagcacc gccaccaagg atacctacga cgccctgcac 1680
atgcaggccc tgccccccag a 1701
<210> 137
<211> 1842
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 137
gacatcgagc tgacacagag cccatctagc ctggctgtgt ctgccggcga gaaagtgacc 60
atgagctgca agagcagcca gagcctgctg aacagccgga ccagaaagaa tcagctggcc 120
tggtatcagc agaaaaccgg acagagcccc gagctgctga tctactgggc cagcacaaga 180
cagagcggcg tgcccgatag attcacagga tctggcagcg gcaccgactt caccctgaca 240
atcagttctg tgcaggccga ggacctggcc gtgtactact gtcagcagag ctacaacctg 300
ctgaccttcg gacccggcac caagctggaa atcaagagag gtggcggtgg ctcgggcggt 360
ggtgggtcgg gtggcggcgg atctgtgaag ctggaagagt ccggcggagg ctttgtgaag 420
cctggcggaa gcctgaagat cagctgtgcc gccagcggct tcaccttcag aaactacgcc 480
atgagctggg tccgactgag ccccgagatg agactggaat gggtcgccac aatcagcagc 540
gcaggcggct acatcttcta cagcgatagc gtgcagggca gattcaccat cagccgggac 600
aacgccaaga acaccctgca cctccagatg ggcagtctga gatctggcga caccgccatg 660
tactactgcg ccagacaagg cttcggcaac tacggcgact actatgccat ggattactgg 720
ggccagggca ccaccgtgac agtctcttct aagcctacca ccacccccgc acctcgtcct 780
ccaacccctg cacctacgat tgccagtcag cctctttcac tgcggcctga ggccagcaga 840
ccagctgccg gcggtgccgt ccatacaaga ggactggact tcgcgtccga taaacctact 900
accactccag ccccaaggcc cccaacccca gcaccgacta tcgcatcaca gcctttgtca 960
ctgcgtcctg aagccagccg gccagctgca gggggggccg tccacacaag gggactcgac 1020
tttgcgagtg ataagcccac caccacccct gcccctagac ctccaacccc agcccctaca 1080
atcgccagcc agcccctgag cctgaggccc gaagcctgta gacctgccgc tggcggagcc 1140
gtgcacacca gaggcctgga tttcgcctgc gacatctaca tctgggcccc tctggccggc 1200
acctgtggcg tgctgctgct gagcctggtc atcaccctgt actgcaacca ccggaatagg 1260
agcaagcgga gcagaggcgg ccacagcgac tacatgaaca tgaccccccg gaggcctggc 1320
cccacccgga agcactacca gccctacgcc cctcccaggg acttcgccgc ctaccggagc 1380
aagagaggcc ggaagaaact gctgtacatc ttcaagcagc ccttcatgcg gcccgtgcag 1440
accacccagg aagaggacgg ctgcagctgc cggttccccg aggaagagga aggcggctgc 1500
gaactgcggg tgaagttcag ccggagcgcc gacgcccctg cctaccagca gggccagaac 1560
cagctgtaca acgagctgaa cctgggccgg agggaggagt acgacgtgct ggacaagcgg 1620
agaggccggg accctgagat gggcggcaag ccccggagaa agaaccctca ggagggcctg 1680
tataacgaac tgcagaaaga caagatggcc gaggcctaca gcgagatcgg catgaagggc 1740
gagcggcgga ggggcaaggg ccacgacggc ctgtaccagg gcctgagcac cgccaccaag 1800
gatacctacg acgccctgca catgcaggcc ctgcccccca ga 1842
<210> 138
<211> 1386
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 138
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaagcccac caccacccct 720
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 780
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 840
gacatctaca tctgggcccc tctggccggc acctgtggcg tgctgctgct gagcctggtc 900
atcaccctgt actgcaacca ccggaatagg agcaagcgga gcagaggcgg ccacagcgac 960
tacatgaaca tgaccccccg gaggcctggc cccacccgga agcactacca gccctacgcc 1020
cctcccaggg acttcgccgc ctaccggagc cgggtgaagt tcagccggag cgccgacgcc 1080
cctgcctacc agcagggcca gaaccagctg tacaacgagc tgaacctggg ccggagggag 1140
gagtacgacg tgctggacaa gcggagaggc cgggaccctg agatgggcgg caagccccgg 1200
agaaagaacc ctcaggaggg cctgtataac gaactgcaga aagacaagat ggccgaggcc 1260
tacagcgaga tcggcatgaa gggcgagcgg cggaggggca agggccacga cggcctgtac 1320
cagggcctga gcaccgccac caaggatacc tacgacgccc tgcacatgca ggccctgccc 1380
cccaga 1386
<210> 139
<211> 1527
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 139
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaaacctac tacaactcct 720
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 780
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 840
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 900
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 960
agaggcctgg atttcgcctg cgacatctac atctgggccc ctctggccgg cacctgtggc 1020
gtgctgctgc tgagcctggt catcaccctg tactgcaacc accggaatag gagcaagcgg 1080
agcagaggcg gccacagcga ctacatgaac atgacccccc ggaggcctgg ccccacccgg 1140
aagcactacc agccctacgc ccctcccagg gacttcgccg cctaccggag ccgggtgaag 1200
ttcagccgga gcgccgacgc ccctgcctac cagcagggcc agaaccagct gtacaacgag 1260
ctgaacctgg gccggaggga ggagtacgac gtgctggaca agcggagagg ccgggaccct 1320
gagatgggcg gcaagccccg gagaaagaac cctcaggagg gcctgtataa cgaactgcag 1380
aaagacaaga tggccgaggc ctacagcgag atcggcatga agggcgagcg gcggaggggc 1440
aagggccacg acggcctgta ccagggcctg agcaccgcca ccaaggatac ctacgacgcc 1500
ctgcacatgc aggccctgcc ccccaga 1527
<210> 140
<211> 1668
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 140
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaagcctac caccaccccc 720
gcacctcgtc ctccaacccc tgcacctacg attgccagtc agcctctttc actgcggcct 780
gaggccagca gaccagctgc cggcggtgcc gtccatacaa gaggactgga cttcgcgtcc 840
gataaaccta ctaccactcc agccccaagg cccccaaccc cagcaccgac tatcgcatca 900
cagcctttgt cactgcgtcc tgaagccagc cggccagctg cagggggggc cgtccacaca 960
aggggactcg actttgcgag tgataagccc accaccaccc ctgcccctag acctccaacc 1020
ccagccccta caatcgccag ccagcccctg agcctgaggc ccgaagcctg tagacctgcc 1080
gctggcggag ccgtgcacac cagaggcctg gatttcgcct gcgacatcta catctgggcc 1140
cctctggccg gcacctgtgg cgtgctgctg ctgagcctgg tcatcaccct gtactgcaac 1200
caccggaata ggagcaagcg gagcagaggc ggccacagcg actacatgaa catgaccccc 1260
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 1320
gcctaccgga gccgggtgaa gttcagccgg agcgccgacg cccctgccta ccagcagggc 1380
cagaaccagc tgtacaacga gctgaacctg ggccggaggg aggagtacga cgtgctggac 1440
aagcggagag gccgggaccc tgagatgggc ggcaagcccc ggagaaagaa ccctcaggag 1500
ggcctgtata acgaactgca gaaagacaag atggccgagg cctacagcga gatcggcatg 1560
aagggcgagc ggcggagggg caagggccac gacggcctgt accagggcct gagcaccgcc 1620
accaaggata cctacgacgc cctgcacatg caggccctgc cccccaga 1668
<210> 141
<211> 1512
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 141
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaagcccac caccacccct 720
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 780
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 840
gacatctaca tctgggcccc tctggccggc acctgtggcg tgctgctgct gagcctggtc 900
atcaccctgt actgcaacca ccggaatagg agcaagcgga gcagaggcgg ccacagcgac 960
tacatgaaca tgaccccccg gaggcctggc cccacccgga agcactacca gccctacgcc 1020
cctcccaggg acttcgccgc ctaccggagc aagagaggcc ggaagaaact gctgtacatc 1080
ttcaagcagc ccttcatgcg gcccgtgcag accacccagg aagaggacgg ctgcagctgc 1140
cggttccccg aggaagagga aggcggctgc gaactgcggg tgaagttcag ccggagcgcc 1200
gacgcccctg cctaccagca gggccagaac cagctgtaca acgagctgaa cctgggccgg 1260
agggaggagt acgacgtgct ggacaagcgg agaggccggg accctgagat gggcggcaag 1320
ccccggagaa agaaccctca ggagggcctg tataacgaac tgcagaaaga caagatggcc 1380
gaggcctaca gcgagatcgg catgaagggc gagcggcgga ggggcaaggg ccacgacggc 1440
ctgtaccagg gcctgagcac cgccaccaag gatacctacg acgccctgca catgcaggcc 1500
ctgcccccca ga 1512
<210> 142
<211> 1653
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 142
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaaacctac tacaactcct 720
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 780
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 840
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 900
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 960
agaggcctgg atttcgcctg cgacatctac atctgggccc ctctggccgg cacctgtggc 1020
gtgctgctgc tgagcctggt catcaccctg tactgcaacc accggaatag gagcaagcgg 1080
agcagaggcg gccacagcga ctacatgaac atgacccccc ggaggcctgg ccccacccgg 1140
aagcactacc agccctacgc ccctcccagg gacttcgccg cctaccggag caagagaggc 1200
cggaagaaac tgctgtacat cttcaagcag cccttcatgc ggcccgtgca gaccacccag 1260
gaagaggacg gctgcagctg ccggttcccc gaggaagagg aaggcggctg cgaactgcgg 1320
gtgaagttca gccggagcgc cgacgcccct gcctaccagc agggccagaa ccagctgtac 1380
aacgagctga acctgggccg gagggaggag tacgacgtgc tggacaagcg gagaggccgg 1440
gaccctgaga tgggcggcaa gccccggaga aagaaccctc aggagggcct gtataacgaa 1500
ctgcagaaag acaagatggc cgaggcctac agcgagatcg gcatgaaggg cgagcggcgg 1560
aggggcaagg gccacgacgg cctgtaccag ggcctgagca ccgccaccaa ggatacctac 1620
gacgccctgc acatgcaggc cctgcccccc aga 1653
<210> 143
<211> 1794
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 143
gacgtgcaac ttctggagag cgggccaggg ctagtcaggc cctcccagtc gctttcactg 60
acttgcagtg tgaccggtta ctctattgtg agtcactact attggaactg gattcggcag 120
ttcccaggca acaaactgga atggatgggg tacatatctt ccgatggctc gaatgaatat 180
aacccatcat tgaaaaatcg tatttccatc agtctggata cgagtaaaaa ccagtttttc 240
ctcaaattcg atttcgtgac tacagcagat actgccacat acttctgtgt acgaggtgtc 300
gattattggg gacagggcac aacgctgacc gtaagttctg gcggaggcgg aagcggaggc 360
ggaggctccg gcggaggcgg aagcgacatc aagatggctc agtccccttc tagcgtgaat 420
gcttcgctag gggagcgtgt gaccatcaca tgtaaagcat cacgcgacat aaataatttc 480
ctttcctggt ttcatcagaa accgggcaag tcgcctaaga cgctgattta cagagcaaat 540
cggttggtag atggagtgcc aagcagattc agcgggagcg gaagtggaca ggattatagc 600
ttcactattt catccctgga atacgaggac gtaggtatct attattgcct ccagtatggc 660
gatctttaca catttggtgg ggggactaag ctggagatta agaagcctac caccaccccc 720
gcacctcgtc ctccaacccc tgcacctacg attgccagtc agcctctttc actgcggcct 780
gaggccagca gaccagctgc cggcggtgcc gtccatacaa gaggactgga cttcgcgtcc 840
gataaaccta ctaccactcc agccccaagg cccccaaccc cagcaccgac tatcgcatca 900
cagcctttgt cactgcgtcc tgaagccagc cggccagctg cagggggggc cgtccacaca 960
aggggactcg actttgcgag tgataagccc accaccaccc ctgcccctag acctccaacc 1020
ccagccccta caatcgccag ccagcccctg agcctgaggc ccgaagcctg tagacctgcc 1080
gctggcggag ccgtgcacac cagaggcctg gatttcgcct gcgacatcta catctgggcc 1140
cctctggccg gcacctgtgg cgtgctgctg ctgagcctgg tcatcaccct gtactgcaac 1200
caccggaata ggagcaagcg gagcagaggc ggccacagcg actacatgaa catgaccccc 1260
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 1320
gcctaccgga gcaagagagg ccggaagaaa ctgctgtaca tcttcaagca gcccttcatg 1380
cggcccgtgc agaccaccca ggaagaggac ggctgcagct gccggttccc cgaggaagag 1440
gaaggcggct gcgaactgcg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1500
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1560
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1620
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1680
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1740
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc caga 1794
<210> 144
<211> 1386
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 144
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcccac caccacccct 720
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 780
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 840
gacatctaca tctgggcccc tctggccggc acctgtggcg tgctgctgct gagcctggtc 900
atcaccctgt actgcaacca ccggaatagg agcaagcgga gcagaggcgg ccacagcgac 960
tacatgaaca tgaccccccg gaggcctggc cccacccgga agcactacca gccctacgcc 1020
cctcccaggg acttcgccgc ctaccggagc cgggtgaagt tcagccggag cgccgacgcc 1080
cctgcctacc agcagggcca gaaccagctg tacaacgagc tgaacctggg ccggagggag 1140
gagtacgacg tgctggacaa gcggagaggc cgggaccctg agatgggcgg caagccccgg 1200
agaaagaacc ctcaggaggg cctgtataac gaactgcaga aagacaagat ggccgaggcc 1260
tacagcgaga tcggcatgaa gggcgagcgg cggaggggca agggccacga cggcctgtac 1320
cagggcctga gcaccgccac caaggatacc tacgacgccc tgcacatgca ggccctgccc 1380
cccaga 1386
<210> 145
<211> 1527
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 145
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaaacctac tacaactcct 720
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 780
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 840
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 900
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 960
agaggcctgg atttcgcctg cgacatctac atctgggccc ctctggccgg cacctgtggc 1020
gtgctgctgc tgagcctggt catcaccctg tactgcaacc accggaatag gagcaagcgg 1080
agcagaggcg gccacagcga ctacatgaac atgacccccc ggaggcctgg ccccacccgg 1140
aagcactacc agccctacgc ccctcccagg gacttcgccg cctaccggag ccgggtgaag 1200
ttcagccgga gcgccgacgc ccctgcctac cagcagggcc agaaccagct gtacaacgag 1260
ctgaacctgg gccggaggga ggagtacgac gtgctggaca agcggagagg ccgggaccct 1320
gagatgggcg gcaagccccg gagaaagaac cctcaggagg gcctgtataa cgaactgcag 1380
aaagacaaga tggccgaggc ctacagcgag atcggcatga agggcgagcg gcggaggggc 1440
aagggccacg acggcctgta ccagggcctg agcaccgcca ccaaggatac ctacgacgcc 1500
ctgcacatgc aggccctgcc ccccaga 1527
<210> 146
<211> 1668
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 146
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcctac caccaccccc 720
gcacctcgtc ctccaacccc tgcacctacg attgccagtc agcctctttc actgcggcct 780
gaggccagca gaccagctgc cggcggtgcc gtccatacaa gaggactgga cttcgcgtcc 840
gataaaccta ctaccactcc agccccaagg cccccaaccc cagcaccgac tatcgcatca 900
cagcctttgt cactgcgtcc tgaagccagc cggccagctg cagggggggc cgtccacaca 960
aggggactcg actttgcgag tgataagccc accaccaccc ctgcccctag acctccaacc 1020
ccagccccta caatcgccag ccagcccctg agcctgaggc ccgaagcctg tagacctgcc 1080
gctggcggag ccgtgcacac cagaggcctg gatttcgcct gcgacatcta catctgggcc 1140
cctctggccg gcacctgtgg cgtgctgctg ctgagcctgg tcatcaccct gtactgcaac 1200
caccggaata ggagcaagcg gagcagaggc ggccacagcg actacatgaa catgaccccc 1260
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 1320
gcctaccgga gccgggtgaa gttcagccgg agcgccgacg cccctgccta ccagcagggc 1380
cagaaccagc tgtacaacga gctgaacctg ggccggaggg aggagtacga cgtgctggac 1440
aagcggagag gccgggaccc tgagatgggc ggcaagcccc ggagaaagaa ccctcaggag 1500
ggcctgtata acgaactgca gaaagacaag atggccgagg cctacagcga gatcggcatg 1560
aagggcgagc ggcggagggg caagggccac gacggcctgt accagggcct gagcaccgcc 1620
accaaggata cctacgacgc cctgcacatg caggccctgc cccccaga 1668
<210> 147
<211> 1512
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 147
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcccac caccacccct 720
gcccctagac ctccaacccc agcccctaca atcgccagcc agcccctgag cctgaggccc 780
gaagcctgta gacctgccgc tggcggagcc gtgcacacca gaggcctgga tttcgcctgc 840
gacatctaca tctgggcccc tctggccggc acctgtggcg tgctgctgct gagcctggtc 900
atcaccctgt actgcaacca ccggaatagg agcaagcgga gcagaggcgg ccacagcgac 960
tacatgaaca tgaccccccg gaggcctggc cccacccgga agcactacca gccctacgcc 1020
cctcccaggg acttcgccgc ctaccggagc aagagaggcc ggaagaaact gctgtacatc 1080
ttcaagcagc ccttcatgcg gcccgtgcag accacccagg aagaggacgg ctgcagctgc 1140
cggttccccg aggaagagga aggcggctgc gaactgcggg tgaagttcag ccggagcgcc 1200
gacgcccctg cctaccagca gggccagaac cagctgtaca acgagctgaa cctgggccgg 1260
agggaggagt acgacgtgct ggacaagcgg agaggccggg accctgagat gggcggcaag 1320
ccccggagaa agaaccctca ggagggcctg tataacgaac tgcagaaaga caagatggcc 1380
gaggcctaca gcgagatcgg catgaagggc gagcggcgga ggggcaaggg ccacgacggc 1440
ctgtaccagg gcctgagcac cgccaccaag gatacctacg acgccctgca catgcaggcc 1500
ctgcccccca ga 1512
<210> 148
<211> 1653
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 148
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaaacctac tacaactcct 720
gccccccggc ctcctacacc agctcctact atcgcctccc agccactcag tctcagaccc 780
gaggcttcta ggccagcggc cggaggcgcg gtccacaccc gcgggctgga ctttgcatcc 840
gataagccca ccaccacccc tgcccctaga cctccaaccc cagcccctac aatcgccagc 900
cagcccctga gcctgaggcc cgaagcctgt agacctgccg ctggcggagc cgtgcacacc 960
agaggcctgg atttcgcctg cgacatctac atctgggccc ctctggccgg cacctgtggc 1020
gtgctgctgc tgagcctggt catcaccctg tactgcaacc accggaatag gagcaagcgg 1080
agcagaggcg gccacagcga ctacatgaac atgacccccc ggaggcctgg ccccacccgg 1140
aagcactacc agccctacgc ccctcccagg gacttcgccg cctaccggag caagagaggc 1200
cggaagaaac tgctgtacat cttcaagcag cccttcatgc ggcccgtgca gaccacccag 1260
gaagaggacg gctgcagctg ccggttcccc gaggaagagg aaggcggctg cgaactgcgg 1320
gtgaagttca gccggagcgc cgacgcccct gcctaccagc agggccagaa ccagctgtac 1380
aacgagctga acctgggccg gagggaggag tacgacgtgc tggacaagcg gagaggccgg 1440
gaccctgaga tgggcggcaa gccccggaga aagaaccctc aggagggcct gtataacgaa 1500
ctgcagaaag acaagatggc cgaggcctac agcgagatcg gcatgaaggg cgagcggcgg 1560
aggggcaagg gccacgacgg cctgtaccag ggcctgagca ccgccaccaa ggatacctac 1620
gacgccctgc acatgcaggc cctgcccccc aga 1653
<210> 149
<211> 1794
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 149
gacatcaaga tggctcagtc cccttctagc gtgaatgctt cgctagggga gcgtgtgacc 60
atcacatgta aagcatcacg cgacataaat aatttccttt cctggtttca tcagaaaccg 120
ggcaagtcgc ctaagacgct gatttacaga gcaaatcggt tggtagatgg agtgccaagc 180
agattcagcg ggagcggaag tggacaggat tatagcttca ctatttcatc cctggaatac 240
gaggacgtag gtatctatta ttgcctccag tatggcgatc tttacacatt tggtgggggg 300
actaagctgg agattaaggg cggaggcgga agcggaggcg gaggctccgg cggaggcgga 360
agcgacgtgc aacttctgga gagcgggcca gggctagtca ggccctccca gtcgctttca 420
ctgacttgca gtgtgaccgg ttactctatt gtgagtcact actattggaa ctggattcgg 480
cagttcccag gcaacaaact ggaatggatg gggtacatat cttccgatgg ctcgaatgaa 540
tataacccat cattgaaaaa tcgtatttcc atcagtctgg atacgagtaa aaaccagttt 600
ttcctcaaat tcgatttcgt gactacagca gatactgcca catacttctg tgtacgaggt 660
gtcgattatt ggggacaggg cacaacgctg accgtaagtt ctaagcctac caccaccccc 720
gcacctcgtc ctccaacccc tgcacctacg attgccagtc agcctctttc actgcggcct 780
gaggccagca gaccagctgc cggcggtgcc gtccatacaa gaggactgga cttcgcgtcc 840
gataaaccta ctaccactcc agccccaagg cccccaaccc cagcaccgac tatcgcatca 900
cagcctttgt cactgcgtcc tgaagccagc cggccagctg cagggggggc cgtccacaca 960
aggggactcg actttgcgag tgataagccc accaccaccc ctgcccctag acctccaacc 1020
ccagccccta caatcgccag ccagcccctg agcctgaggc ccgaagcctg tagacctgcc 1080
gctggcggag ccgtgcacac cagaggcctg gatttcgcct gcgacatcta catctgggcc 1140
cctctggccg gcacctgtgg cgtgctgctg ctgagcctgg tcatcaccct gtactgcaac 1200
caccggaata ggagcaagcg gagcagaggc ggccacagcg actacatgaa catgaccccc 1260
cggaggcctg gccccacccg gaagcactac cagccctacg cccctcccag ggacttcgcc 1320
gcctaccgga gcaagagagg ccggaagaaa ctgctgtaca tcttcaagca gcccttcatg 1380
cggcccgtgc agaccaccca ggaagaggac ggctgcagct gccggttccc cgaggaagag 1440
gaaggcggct gcgaactgcg ggtgaagttc agccggagcg ccgacgcccc tgcctaccag 1500
cagggccaga accagctgta caacgagctg aacctgggcc ggagggagga gtacgacgtg 1560
ctggacaagc ggagaggccg ggaccctgag atgggcggca agccccggag aaagaaccct 1620
caggagggcc tgtataacga actgcagaaa gacaagatgg ccgaggccta cagcgagatc 1680
ggcatgaagg gcgagcggcg gaggggcaag ggccacgacg gcctgtacca gggcctgagc 1740
accgccacca aggataccta cgacgccctg cacatgcagg ccctgccccc caga 1794
<210> 150
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 150
atgcttctcc tggtgacaag ccttctgctc tgtgagttac cacacccagc attcctcctg 60
atccca 66
<210> 151
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 151
atgaggctcc ctgctcagct cctggggctg ctaatgctct gggtcccagg atccagtggg 60
<210> 152
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 152
atggattgga cctggattct gtttctggtg gccgctgcca caagagtgca cagc 54
<210> 153
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 153
atggcgctgc ccgtgaccgc cttgctcctg ccgctggcct tgctgctcca cgccgccagg 60
ccg 63
<210> 154
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 154
atgggcacca gcctcctctg ctggatggcc ctgtgtctcc tgggggcaga tcacgcagat 60
gct 63
<210> 155
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 155
atgaagcgct tcctcttcct cctactcacc atcagcctcc tggttatggt acagatacaa 60
actggactct ca 72
<210> 156
<211> 84
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 156
atgggggcag gtgccaccgg ccgcgccatg gacgggccgc gcctgctgct gttgctgctt 60
ctgggggtgt cccttggagg tgcc 84
<210> 157
<211> 1005
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 157
cgcaaagtgt gtaacggaat aggtattggt gaatttaaag actcactctc cataaatgct 60
acgaatatta aacacttcaa aaactgcacc tccatcagtg gcgatctcca catcctgccg 120
gtggcattta ggggtgactc cttcacacat actcctcctc tggatccaca ggaactggat 180
attctgaaaa ccgtaaagga aatcacaggg tttttgctga ttcaggcttg gcctgaaaac 240
aggacggacc tccatgcctt tgagaaccta gaaatcatac gcggcaggac caagcaacat 300
ggtcagtttt ctcttgcagt cgtcagcctg aacataacat ccttgggatt acgctccctc 360
aaggagataa gtgatggaga tgtgataatt tcaggaaaca aaaatttgtg ctatgcaaat 420
acaataaact ggaaaaaact gtttgggacc tccggtcaga aaaccaaaat tataagcaac 480
agaggtgaaa acagctgcaa ggccacaggc caggtctgcc atgccttgtg ctcccccgag 540
ggctgctggg gcccggagcc cagggactgc gtctcttgcc ggaatgtcag ccgaggcagg 600
gaatgcgtgg acaagtgcaa ccttctggag ggtgagccaa gggagtttgt ggagaactct 660
gagtgcatac agtgccaccc agagtgcctg cctcaggcca tgaacatcac ctgcacagga 720
cggggaccag acaactgtat ccagtgtgcc cactacattg acggccccca ctgcgtcaag 780
acctgcccgg caggagtcat gggagaaaac aacaccctgg tctggaagta cgcagacgcc 840
ggccatgtgt gccacctgtg ccatccaaac tgcacctacg gatgcactgg gccaggtctt 900
gaaggctgtc caacgaatgg gcctaagatc ccgtccatcg ccactgggat ggtgggggcc 960
ctcctcttgc tgctggtggt ggccctgggg atcggcctct tcatg 1005
<210> 158
<211> 732
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 158
cgcaaagtgt gtaacggaat aggtattggt gaatttaaag actcactctc cataaatgct 60
acgaatatta aacacttcaa aaactgcacc tccatcagtg gcgatctcca catcctgccg 120
gtggcattta ggggtgactc cttcacacat actcctcctc tggatccaca ggaactggat 180
attctgaaaa ccgtaaagga aatcacaggg tttttgctga ttcaggcttg gcctgaaaac 240
aggacggacc tccatgcctt tgagaaccta gaaatcatac gcggcaggac caagcaacat 300
ggtcagtttt ctcttgcagt cgtcagcctg aacataacat ccttgggatt acgctccctc 360
aaggagataa gtgatggaga tgtgataatt tcaggaaaca aaaatttgtg ctatgcaaat 420
acaataaact ggaaaaaact gtttgggacc tccggtcaga aaaccaaaat tataagcaac 480
agaggtgaaa acagctgcaa ggccacaggc caggtctgcc atgccttgtg ctcccccgag 540
ggctgctggg gcccggagcc cagggactgc gtctctggtg gcggtggctc gggcggtggt 600
gggtcgggtg gcggcggatc tggtggcggt ggctcgtttt gggtgctggt ggtggttggt 660
ggagtcctgg cttgctatag cttgctagta acagtggcct ttattatttt ctgggtgagg 720
agtaagagga gc 732
<210> 159
<211> 891
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 159
atgacaacac ccagaaattc agtaaatggg actttcccgg cagagccaat gaaaggccct 60
attgctatgc aatctggtcc aaaaccactc ttcaggagga tgtcttcact ggtgggcccc 120
acgcaaagct tcttcatgag ggaatctaag actttggggg ctgtccagat tatgaatggg 180
ctcttccaca ttgccctggg gggtcttctg atgatcccag cagggatcta tgcacccatc 240
tgtgtgactg tgtggtaccc tctctgggga ggcattatgt atattatttc cggatcactc 300
ctggcagcaa cggagaaaaa ctccaggaag tgtttggtca aaggaaaaat gataatgaat 360
tcattgagcc tctttgctgc catttctgga atgattcttt caatcatgga catacttaat 420
attaaaattt cccatttttt aaaaatggag agtctgaatt ttattagagc tcacacacca 480
tatattaaca tatacaactg tgaaccagct aatccctctg agaaaaactc cccatctacc 540
caatactgtt acagcataca atctctgttc ttgggcattt tgtcagtgat gctgatcttt 600
gccttcttcc aggaacttgt aatagctggc atcgttgaga atgaatggaa aagaacgtgc 660
tccagaccca aatctaacat agttctcctg tcagcagaag aaaaaaaaga acagactatt 720
gaaataaaag aagaagtggt tgggctaact gaaacatctt cccaaccaaa gaatgaagaa 780
gacattgaaa ttattccaat ccaagaagag gaagaagaag aaacagagac gaactttcca 840
gaacctcccc aagatcagga atcctcacca atagaaaatg acagctctcc t 891
<210> 160
<211> 789
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 160
atgaccacac cacggaactc tgtgaatggc accttcccag cagagccaat gaagggacca 60
atcgcaatgc agagcggacc caagcctctg tttcggagaa tgagctccct ggtgggccca 120
acccagtcct tctttatgag agagtctaag acactgggcg ccgtgcagat catgaacgga 180
ctgttccaca tcgccctggg aggactgctg atgatcccag ccggcatcta cgcccctatc 240
tgcgtgaccg tgtggtaccc tctgtggggc ggcatcatgt atatcatctc cggctctctg 300
ctggccgcca cagagaagaa cagcaggaag tgtctggtga agggcaagat gatcatgaat 360
agcctgtccc tgtttgccgc catctctggc atgatcctga gcatcatgga catcctgaac 420
atcaagatca gccacttcct gaagatggag agcctgaact tcatcagagc ccacacccct 480
tacatcaaca tctataattg cgagcctgcc aacccatccg agaagaattc tccaagcaca 540
cagtactgtt attccatcca gtctctgttc ctgggcatcc tgtctgtgat gctgatcttt 600
gccttctttc aggagctggt catcgccggc atcgtggaga acgagtggaa gaggacctgc 660
agccgcccca agtccaatat cgtgctgctg tccgccgagg agaagaagga gcagacaatc 720
gagatcaagg aggaggtggt gggcctgacc gagacatcta gccagcctaa gaatgaggag 780
gatatcgag 789
<210> 161
<211> 1185
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 161
atggattgga cctggattct gtttctggtg gccgctgcca caagagtgca cagcaactgg 60
gtgaatgtga tcagcgacct gaagaagatc gaggatctga tccagagcat gcacattgat 120
gccaccctgt acacagaatc tgatgtgcac cctagctgta aagtgaccgc catgaagtgt 180
tttctgctgg agctgcaggt gatttctctg gaaagcggag atgcctctat ccacgacaca 240
gtggagaatc tgatcatcct ggccaacaat agcctgagca gcaatggcaa tgtgacagag 300
tctggctgta aggagtgtga ggagctggag gagaagaaca tcaaggagtt tctgcagagc 360
tttgtgcaca tcgtgcagat gttcatcaat acaagctctg gcggaggatc tggaggaggc 420
ggatctggag gaggaggcag tggaggcgga ggatctggcg gaggatctct gcagattaca 480
tgccctcctc caatgtctgt ggagcacgcc gatatttggg tgaagtccta cagcctgtac 540
agcagagaga gatacatctg caacagcggc tttaagagaa aggccggcac ctcttctctg 600
acagagtgcg tgctgaataa ggccacaaat gtggcccact ggacaacacc tagcctgaag 660
tgcattagag atcctgccct ggtccaccag aggcctgccc ctccatctac agtgacaaca 720
gccggagtga cacctcagcc tgaatctctg agcccttctg gaaaagaacc tgccgccagc 780
tctcctagct ctaataatac cgccgccaca acagccgcca ttgtgcctgg atctcagctg 840
atgcctagca agtctcctag cacaggcaca acagagatca gcagccacga atcttctcac 900
ggaacacctt ctcagaccac cgccaagaat tgggagctga cagcctctgc ctctcaccag 960
cctccaggag tgtatcctca gggccactct gatacaacag tggccatcag cacatctaca 1020
gtgctgctgt gtggactgtc tgccgtgtct ctgctggcct gttacctgaa gtctagacag 1080
acacctcctc tggcctctgt ggagatggag gccatggaag ccctgcctgt gacatgggga 1140
acaagcagca gagatgagga cctggagaat tgttctcacc acctg 1185
<210> 162
<211> 342
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 162
aactgggtga atgtgatcag cgacctgaag aagatcgagg atctgatcca gagcatgcac 60
attgatgcca ccctgtacac agaatctgat gtgcacccta gctgtaaagt gaccgccatg 120
aagtgttttc tgctggagct gcaggtgatt tctctggaaa gcggagatgc ctctatccac 180
gacacagtgg agaatctgat catcctggcc aacaatagcc tgagcagcaa tggcaatgtg 240
acagagtctg gctgtaagga gtgtgaggag ctggaggaga agaacatcaa ggagtttctg 300
cagagctttg tgcacatcgt gcagatgttc atcaatacaa gc 342
<210> 163
<211> 711
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 163
attacatgcc ctcctccaat gtctgtggag cacgccgata tttgggtgaa gtcctacagc 60
ctgtacagca gagagagata catctgcaac agcggcttta agagaaaggc cggcacctct 120
tctctgacag agtgcgtgct gaataaggcc acaaatgtgg cccactggac aacacctagc 180
ctgaagtgca ttagagatcc tgccctggtc caccagaggc ctgcccctcc atctacagtg 240
acaacagccg gagtgacacc tcagcctgaa tctctgagcc cttctggaaa agaacctgcc 300
gccagctctc ctagctctaa taataccgcc gccacaacag ccgccattgt gcctggatct 360
cagctgatgc ctagcaagtc tcctagcaca ggcacaacag agatcagcag ccacgaatct 420
tctcacggaa caccttctca gaccaccgcc aagaattggg agctgacagc ctctgcctct 480
caccagcctc caggagtgta tcctcagggc cactctgata caacagtggc catcagcaca 540
tctacagtgc tgctgtgtgg actgtctgcc gtgtctctgc tggcctgtta cctgaagtct 600
agacagacac ctcctctggc ctctgtggag atggaggcca tggaagccct gcctgtgaca 660
tggggaacaa gcagcagaga tgaggacctg gagaattgtt ctcaccacct g 711
<210> 164
<211> 54
<212> ДНК
<213> Вирус Thosea asigna
<400> 164
gagggcagag gaagtcttct aacatgcggt gacgtggagg agaatcccgg ccct 54
<210> 165
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 165
agagctaaga ggggaagcgg agagggcaga ggaagtctgc taacatgcgg tgacgtcgag 60
gagaatcctg gacct 75
<210> 166
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 166
agggccaaga ggagtggcag cggcgagggc agaggaagtc ttctaacatg cggtgacgtg 60
gaggagaatc ccggccct 78
<210> 167
<211> 57
<212> ДНК
<213> Тешовирус свиньи 1
<400> 167
gcaacgaact tctctctcct aaaacaggct ggtgatgtgg aggagaatcc tggtcca 57
<210> 168
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 168
ggaagcggag ctactaactt cagcctgctg aagcaggctg gagacgtgga ggagaaccct 60
ggacct 66
<210> 169
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 169
cgtgcaaagc gtgcaccggt gaaacaggga agcggagcta ctaacttcag cctgctgaag 60
caggctggag acgtggagga gaaccctgga cct 93
<210> 170
<211> 60
<212> ДНК
<213> Вирус A ринита лошадей
<400> 170
cagtgtacta attatgctct cttgaaattg gctggagatg ttgagagcaa ccctggacct 60
<210> 171
<211> 66
<212> ДНК
<213> Вирус ящура
<400> 171
gtcaaacaga ccctaaactt tgatctgcta aaactggccg gggatgtgga aagtaatccc 60
ggcccc 66
<210> 172
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 172
cgtgcaaagc gt 12
<210> 173
<211> 84
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 173
agagccaaga gggcaccggt gaaacagact ttgaattttg accttctgaa gttggcagga 60
gacgttgagt ccaaccctgg gccc 84
<210> 174
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 174
ggtggcggtg gctcgggcgg tggtgggtcg ggtggcggcg gatct 45
<210> 175
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 175
ggcagcacct ccggcagcgg caagcctggc agcggcgagg gcagcaccaa gggc 54
<210> 176
<211> 9
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 176
ggaagcgga 9
<210> 177
<211> 12
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 177
agtggcagcg gc 12
<210> 178
<211> 258
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 178
ggccccaaga agaaaaggaa ggtggccccc cccaccgacg tgagcctggg cgacgagctg 60
cacctggacg gcgaggacgt ggccatggcc cacgccgacg ccctggacga cttcgacctg 120
gacatgctgg gcgacggcga cagccccggc cccggcttca ccccccacga cagcgccccc 180
tacggcgccc tggacatggc cgacttcgag ttcgagcaga tgttcaccga cgccctgggc 240
atcgacgagt acggcggc 258
<210> 179
<211> 705
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 179
gagatgcccg tggacaggat tctggaggcc gaactcgccg tggagcagaa aagcgaccag 60
ggcgtggagg gccccggcgg aaccggcggc agcggcagca gccccaacga ccccgtgacc 120
aacatctgcc aggccgccga caagcagctg ttcaccctgg tggagtgggc caagaggatt 180
ccccacttca gcagcctgcc cctggacgac caggtgatcc tgctgagggc cggatggaac 240
gagctgctga tcgccagctt cagccacagg agcatcgacg tgagggacgg catcctgctg 300
gccaccggcc tgcacgtcca taggaacagc gcccacagcg ccggagtggg cgccatcttc 360
gacagggtgc tgaccgagct ggtgagcaag atgagggaca tgaggatgga caagaccgag 420
ctgggctgcc tgagggccat catcctgttc aaccccgagg tgaggggcct gaaaagcgcc 480
caggaggtgg agctgctgag ggagaaggtg tacgccgccc tggaggagta caccaggacc 540
acccaccccg acgagcccgg cagattcgcc aagctgctgc tgaggctgcc cagcctgagg 600
agcatcggcc tgaagtgcct ggagcacctg ttcttcttca ggctgatcgg cgacgtgccc 660
atcgacacct tcctgatgga gatgctggag agccccagcg acagc 705
<210> 180
<211> 969
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 180
ggccccaaga agaaaaggaa ggtggccccc cccaccgacg tgagcctggg cgacgagctg 60
cacctggacg gcgaggacgt ggccatggcc cacgccgacg ccctggacga cttcgacctg 120
gacatgctgg gcgacggcga cagccccggc cccggcttca ccccccacga cagcgccccc 180
tacggcgccc tggacatggc cgacttcgag ttcgagcaga tgttcaccga cgccctgggc 240
atcgacgagt acggcggcga attcgagatg cccgtggaca ggattctgga ggccgaactc 300
gccgtggagc agaaaagcga ccagggcgtg gagggccccg gcggaaccgg cggcagcggc 360
agcagcccca acgaccccgt gaccaacatc tgccaggccg ccgacaagca gctgttcacc 420
ctggtggagt gggccaagag gattccccac ttcagcagcc tgcccctgga cgaccaggtg 480
atcctgctga gggccggatg gaacgagctg ctgatcgcca gcttcagcca caggagcatc 540
gacgtgaggg acggcatcct gctggccacc ggcctgcacg tccataggaa cagcgcccac 600
agcgccggag tgggcgccat cttcgacagg gtgctgaccg agctggtgag caagatgagg 660
gacatgagga tggacaagac cgagctgggc tgcctgaggg ccatcatcct gttcaacccc 720
gaggtgaggg gcctgaaaag cgcccaggag gtggagctgc tgagggagaa ggtgtacgcc 780
gccctggagg agtacaccag gaccacccac cccgacgagc ccggcagatt cgccaagctg 840
ctgctgaggc tgcccagcct gaggagcatc ggcctgaagt gcctggagca cctgttcttc 900
ttcaggctga tcggcgacgt gcccatcgac accttcctga tggagatgct ggagagcccc 960
agcgacagc 969
<210> 181
<211> 450
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 181
atgaagctgc tgagcagcat cgagcaggct tgcgacatct gcaggctgaa gaagctgaag 60
tgcagcaagg agaagcccaa gtgcgccaag tgcctgaaga acaactggga gtgcagatac 120
agccccaaga ccaagaggag ccccctgacc agggcccacc tgaccgaggt ggagagcagg 180
ctggagaggc tggagcagct gttcctgctg atcttcccca gggaggacct ggacatgatc 240
ctgaagatgg acagcctgca agacatcaag gccctgctga ccggcctgtt cgtgcaggac 300
aacgtgaaca aggacgccgt gaccgacagg ctggccagcg tggagaccga catgcccctg 360
accctgaggc agcacaggat cagcgccacc agcagcagcg aggagagcag caacaagggc 420
cagaggcagc tgaccgtgag ccccgagttt 450
<210> 182
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 182
atcaggcccg agtgcgtggt gcccgagacc cagtgcgcca tgaaaaggaa ggagaagaag 60
gcccagaagg agaaggacaa gctgcccgtg agcaccacca ccgtcgatga ccacatgccc 120
cccatcatgc agtgcgagcc cccccccccc gaggccgcca ggattcacga ggtcgtgccc 180
aggttcctga gcgacaagct gctggtgacc aacaggcaga agaacatccc ccagctgacc 240
gccaaccagc agttcctgat cgccaggctg atctggtatc aggacggcta cgagcagccc 300
agcgacgagg acctgaaaag gatcacccag acctggcagc aggccgacga cgagaacgag 360
gagagcgaca cccccttcag gcagatcacc gagatgacca tcctgaccgt gcagctgatc 420
gtggagttcg ccaagggcct gcccggattc gccaagatca gccagcccga ccagatcacc 480
ctgctgaagg cttgcagcag cgaggtgatg atgctgaggg tggccaggag gtacgacgcc 540
gccagcgaca gcatcctgtt cgccaacaac caggcttaca ccagggacaa ctacaggaag 600
gctggcatgg ccgaggtgat cgaggacctc ctgcacttct gcagatgtat gtacagcatg 660
gccctggaca acatccacta cgccctgctg accgccgtgg tgatcttcag cgacaggccc 720
ggcctggagc agccccagct ggtggaggag atccagaggt actacctgaa caccctgagg 780
atctacatcc tgaaccagct gagcggcagc gccaggagca gcgtgatcta cggcaagatc 840
ctgagcatcc tgagcgagct gaggaccctg ggaatgcaga acagcaatat gtgtatcagc 900
ctgaagctga agaacaggaa gctgcccccc ttcctggagg agatttggga cgtggccgac 960
atgagccaca cccagccccc ccccatcctg gagagcccca ccaacctg 1008
<210> 183
<211> 1008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 183
cggcctgagt gcgtagtacc cgagactcag tgcgccatga agcggaaaga gaagaaagca 60
cagaaggaga aggacaaact gcctgtcagc acgacgacgg tggacgacca catgccgccc 120
attatgcagt gtgaacctcc acctcctgaa gcagcaagga ttcacgaagt ggtcccaagg 180
tttctctccg acaagctgtt ggtgacaaac cggcagaaaa acatccccca gttgacagcc 240
aaccagcagt tccttatcgc caggctcatc tggtaccagg acgggtacga gcagccttct 300
gatgaagatt tgaagaggat tacgcagacg tggcagcaag cggacgatga aaacgaagag 360
tcggacactc ccttccgcca gatcacagag atgactatcc tcacggtcca acttatcgtg 420
gagttcgcga agggattgcc agggttcgcc aagatctcgc agcctgatca aattacgctg 480
cttaaggctt gctcaagtga ggtaatgatg ctccgagtcg cgcgacgata cgatgcggcc 540
tcagacagta ttctgttcgc gaacaaccaa gcgtacactc gcgacaacta ccgcaaggct 600
ggcatggccg aggtcatcga ggatctactg cacttctgcc ggtgcatgta ctctatggcg 660
ttggacaaca tccattacgc gctgctcacg gctgtcgtca tcttttctga ccggccaggg 720
ttggagcagc cgcaactggt ggaagagatc cagcggtact acctgaatac gctccgcatc 780
tatatcctga accagctgag cgggtcggcg cgttcgtccg tcatatacgg caagatcctc 840
tcaatcctct ctgagctacg cacgctcggc atgcaaaact ccaacatgtg catctccctc 900
aagctcaaga acagaaagct gccgcctttc ctcgaggaga tctgggatgt ggcggacatg 960
tcgcacaccc aaccgccgcc tatcctcgag tcccccacga atctctag 1008
<210> 184
<211> 1467
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 184
atgaagctac tgtcttctat cgaacaagca tgcgatattt gccgacttaa aaagctcaag 60
tgctccaaag aaaaaccgaa gtgcgccaag tgtctgaaga acaactggga gtgtcgctac 120
tctcccaaaa ccaaaaggtc tccgctgact agggcacatc tgacagaagt ggaatcaagg 180
ctagaaagac tggaacagct atttctactg atttttcctc gagaagacct tgacatgatt 240
ttgaaaatgg attctttaca ggatataaaa gcattgttaa caggattatt tgtacaagat 300
aatgtgaata aagatgccgt cacagataga ttggcttcag tggagactga tatgcctcta 360
acattgagac agcatagaat aagtgcgaca tcatcatcgg aagagagtag taacaaaggt 420
caaagacagt tgactgtatc gccggaattc ccggggatcc ggcctgagtg cgtagtaccc 480
gagactcagt gcgccatgaa gcggaaagag aagaaagcac agaaggagaa ggacaaactg 540
cctgtcagca cgacgacggt ggacgaccac atgccgccca ttatgcagtg tgaacctcca 600
cctcctgaag cagcaaggat tcacgaagtg gtcccaaggt ttctctccga caagctgttg 660
gtgacaaacc ggcagaaaaa catcccccag ttgacagcca accagcagtt ccttatcgcc 720
aggctcatct ggtaccagga cgggtacgag cagccttctg atgaagattt gaagaggatt 780
acgcagacgt ggcagcaagc ggacgatgaa aacgaagagt cggacactcc cttccgccag 840
atcacagaga tgactatcct cacggtccaa cttatcgtgg agttcgcgaa gggattgcca 900
gggttcgcca agatctcgca gcctgatcaa attacgctgc ttaaggcttg ctcaagtgag 960
gtaatgatgc tccgagtcgc gcgacgatac gatgcggcct cagacagtat tctgttcgcg 1020
aacaaccaag cgtacactcg cgacaactac cgcaaggctg gcatggccga ggtcatcgag 1080
gatctactgc acttctgccg gtgcatgtac tctatggcgt tggacaacat ccattacgcg 1140
ctgctcacgg ctgtcgtcat cttttctgac cggccagggt tggagcagcc gcaactggtg 1200
gaagagatcc agcggtacta cctgaatacg ctccgcatct atatcctgaa ccagctgagc 1260
gggtcggcgc gttcgtccgt catatacggc aagatcctct caatcctctc tgagctacgc 1320
acgctcggca tgcaaaactc caacatgtgc atctccctca agctcaagaa cagaaagctg 1380
ccgcctttcc tcgaggagat ctgggatgtg gcggacatgt cgcacaccca accgccgcct 1440
atcctcgagt cccccacgaa tctctag 1467
<210> 185
<211> 1464
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 185
atgaagctgc tgagcagcat cgagcaggct tgcgacatct gcaggctgaa gaagctgaag 60
tgcagcaagg agaagcccaa gtgcgccaag tgcctgaaga acaactggga gtgcagatac 120
agccccaaga ccaagaggag ccccctgacc agggcccacc tgaccgaggt ggagagcagg 180
ctggagaggc tggagcagct gttcctgctg atcttcccca gggaggacct ggacatgatc 240
ctgaagatgg acagcctgca agacatcaag gccctgctga ccggcctgtt cgtgcaggac 300
aacgtgaaca aggacgccgt gaccgacagg ctggccagcg tggagaccga catgcccctg 360
accctgaggc agcacaggat cagcgccacc agcagcagcg aggagagcag caacaagggc 420
cagaggcagc tgaccgtgag ccccgagttt cccgggcggc ctgagtgcgt agtacccgag 480
actcagtgcg ccatgaagcg gaaagagaag aaagcacaga aggagaagga caaactgcct 540
gtcagcacga cgacggtgga cgaccacatg ccgcccatta tgcagtgtga acctccacct 600
cctgaagcag caaggattca cgaagtggtc ccaaggtttc tctccgacaa gctgttggtg 660
acaaaccggc agaaaaacat cccccagttg acagccaacc agcagttcct tatcgccagg 720
ctcatctggt accaggacgg gtacgagcag ccttctgatg aagatttgaa gaggattacg 780
cagacgtggc agcaagcgga cgatgaaaac gaagagtcgg acactccctt ccgccagatc 840
acagagatga ctatcctcac ggtccaactt atcgtggagt tcgcgaaggg attgccaggg 900
ttcgccaaga tctcgcagcc tgatcaaatt acgctgctta aggcttgctc aagtgaggta 960
atgatgctcc gagtcgcgcg acgatacgat gcggcctcag acagtattct gttcgcgaac 1020
aaccaagcgt acactcgcga caactaccgc aaggctggca tggccgaggt catcgaggat 1080
ctactgcact tctgccggtg catgtactct atggcgttgg acaacatcca ttacgcgctg 1140
ctcacggctg tcgtcatctt ttctgaccgg ccagggttgg agcagccgca actggtggaa 1200
gagatccagc ggtactacct gaatacgctc cgcatctata tcctgaacca gctgagcggg 1260
tcggcgcgtt cgtccgtcat atacggcaag atcctctcaa tcctctctga gctacgcacg 1320
ctcggcatgc aaaactccaa catgtgcatc tccctcaagc tcaagaacag aaagctgccg 1380
cctttcctcg aggagatctg ggatgtggcg gacatgtcgc acacccaacc gccgcctatc 1440
ctcgagtccc ccacgaatct ctag 1464
<210> 186
<211> 244
<212> ДНК
<213> Homo sapiens
<400> 186
gagcgtgcgt gaggctccgg tgcccgtcag tgggcagagc gcacatcgcc cacagtcccc 60
gagaagttgg ggggaggggg tcggcgattg aaccggtgcc tagagaaggt ggcgcggggt 120
aaactgggaa agtgatgtcg tgtactggct ccgccttttt cccgagggtg ggggagaacc 180
gtatataagt gcagtagtcg ccgtgaacgt tctttttcgc aacgggtttg ccgccagaac 240
acag 244
<210> 187
<211> 148
<212> ДНК
<213> Неизвестно
<220>
<223> Описание неизвестного:
Последовательность индуцируемого GAL4 проксимального элемента связывания
факторов (PFB) из 6 сайтов
<400> 187
attgttcgga gcagtgcggc gcgtttagcg gagtactgtc ctccgatatt aatcggggca 60
gactattccg gggtttaccg gcgcactctc gcccgaactt caccggcggt ctttcgtccg 120
tgctttatcg gggcggatca ctccgaac 148
<210> 188
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 188
aggtctatat aagcagagct cgtttagtga accctcattc tggagacgga tcccgagccg 60
agtgttttga cctccataga a 81
<210> 189
<211> 31
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
олигонуклеотид
<400> 189
cagccgctaa atccaaggta aggtcagaag a 31
<210> 190
<211> 132
<212> ДНК
<213> Вирус обезьян 40
<400> 190
aacttgttta ttgcagctta taatggttac aaataaagca atagcatcac aaatttcaca 60
aataaagcat ttttttcact gcattctagt tgtggtttgt ccaaactcat caatgtatct 120
tatcatgtct gg 132
<210> 191
<211> 275
<212> ДНК
<213> Неизвестно
<220>
<223> Описание неизвестного:
Последовательность двунаправленного поли(А) aCA
[двунаправленный поли(А)]
<400> 191
atcgattaat ctagcggccc tagacgagca gacatgataa gatacattga tgagtttgga 60
caaaccacaa ctagaatgca gtgaaaaaaa tgctttattt gtgaaatttg tgatgctatt 120
gctttatttg taaccattat aagctgcaat aaacaagtta acaacaacaa ttgcattcat 180
tttatgtttc aggttcaggg ggagatgtgg gaggtttttt aaagcaagta aaacctctac 240
aaatgtggta aaatccgata agcgtaccta gaggc 275
<210> 192
<211> 73
<212> ДНК
<213> Неизвестно
<220>
<223> Описание неизвестного:
Последовательность IRES 2xRbm3
<400> 192
actagtttta taatttcttc ttccagaatt tctgacattt tataatttct tcttccagaa 60
gactcacaac ctc 73
<210> 193
<211> 570
<212> ДНК
<213> Неизвестно
<220>
<223> Описание неизвестного:
Последовательность IRES EMCV
<400> 193
ccccctctcc ctcccccccc cctaacgtta ctggccgaag ccgcttggaa taaggccggt 60
gtgcgtttgt ctatatgtta ttttccacca tattgccgtc ttttggcaat gtgagggccc 120
ggaaacctgg ccctgtcttc ttgacgagca ttcctagggg tctttcccct ctcgccaaag 180
gaatgcaagg tctgttgaat gtcgtgaagg aagcagttcc tctggaagct tcttgaagac 240
aaacaacgtc tgtagcgacc ctttgcaggc agcggaaccc cccacctggc gacaggtgcc 300
tctgcggcca aaagccacgt gtataagata cacctgcaaa ggcggcacaa ccccagtgcc 360
acgttgtgag ttggatagtt gtggaaagag tcaaatggct ctcctcaagc gtattcaaca 420
aggggctgaa ggatgcccag aaggtacccc attgtatggg atctgatctg gggcctcggt 480
gcacatgctt tacatgtgtt tagtcgaggt taaaaaacgt ctaggccccc cgaaccacgg 540
ggacgtggtt ttcctttgaa aaacacgatc 570
<210> 194
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 194
gaggtgcagc tggtggagag cggcggcggc ctggtgcagc ccggcggcag cctgaggctg 60
agctgcgccg ccagcggcta cagcatcacc aacgactacg cctggaactg ggtgaggcag 120
gcccccggca agggcctgga gtgggtgggc tacatcaact acagcggcta caccacctac 180
aaccccagcc tgaagagcag gttcaccatc agcagggaca acagcaagaa caccctgtac 240
ctgcagatga acagcctgag ggccgaggac accgccgtgt actactgcgc caggtgggac 300
ggcggcctga cctactgggg ccagggcacc ctggtgaccg tgagcagc 348
<210> 195
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полинуклеотид
<400> 195
gaggtgcagc tggtggagag cggcggcggc ctggtgcagc ccggcggcag cctgaggctg 60
agctgcgccg ccagcggcta cagcatcacc aacgactacg cctggaactg ggtgaggcag 120
gcccccggca agggcctgga gtgggtgggc tacatcaact acagcggcta caccacctac 180
aaccccagcc tgaagagcag gttcaccatc agcagggaca acagcaagaa caccttctac 240
ctgcagatga acagcctgag ggccgaggac accgccgtgt actactgcgc caggtgggac 300
ggcggcctga cctactgggg ccagggcacc ctggtgaccg tgagcagc 348
<210> 196
<211> 12
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 196
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 197
<211> 5
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 197
Gly Gly Gly Gly Ser
1 5
<210> 198
<211> 45
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<220>
<221> MISC_FEATURE
<222> (1)..(45)
<223> Данная последовательность может содержать 0-15 повторяющихся единиц
"Gly Ser Gly"
<400> 198
Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly
1 5 10 15
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
20 25 30
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly
35 40 45
<210> 199
<211> 60
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<220>
<221> MISC_FEATURE
<222> (1)..(60)
<223> Данная последовательность может содержать 0-15 повторяющихся единиц
"Ser Gly Ser Gly"
<400> 199
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10 15
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
20 25 30
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
35 40 45
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
50 55 60
<210> 200
<211> 20
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 200
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 201
<211> 8
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Val или Ile
<220>
<221> MOD_RES
<222> (4)..(4)
<223> Любая аминокислота
<400> 201
Asp Xaa Glu Xaa Asn Pro Gly Pro
1 5
<210> 202
<211> 27
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> MISC_FEATURE
<222> (2)..(26)
<223> Данная область может содержать 2-5 повторяющихся единиц
"Glu Ala Ala Ala Lys"
<400> 202
Ala Glu Ala Ala Ala Lys Glu Ala Ala Ala Lys Glu Ala Ala Ala Lys
1 5 10 15
Glu Ala Ala Ala Lys Glu Ala Ala Ala Lys Ala
20 25
<210> 203
<211> 30
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<220>
<221> MISC_FEATURE
<222> (1)..(30)
<223> Данная последовательность может содержать 0-15 повторяющихся единиц
"Gly Ser"
<400> 203
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10 15
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
20 25 30
<210> 204
<211> 30
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<220>
<221> MISC_FEATURE
<222> (1)..(30)
<223> Данная последовательность может содержать 0-15 повторяющихся единиц
"Ser Gly"
<400> 204
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
1 5 10 15
Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser Gly
20 25 30
<210> 205
<211> 5
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 205
Ala Pro Val Lys Gln
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛЕННЫЕ НА АНТИГЕН СОЗРЕВАНИЯ В-КЛЕТОК, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2829097C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1, ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗА AL | 2018 |
|
RU2774895C2 |
| Т-КЛЕТКИ С КОСТИМУЛИРУЮЩИМ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ, НАЦЕЛЕННЫЕ НА IL13Rα2 | 2015 |
|
RU2749922C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ И СВЯЗЫВАЮЩИЕ АГЕНТЫ, НАЦЕЛЕННЫЕ НА DLL3 | 2020 |
|
RU2822366C2 |
| CD20 ТЕРАПИЯ, CD22 ТЕРАПИЯ И КОМБИНИРОВАННАЯ ТЕРАПИЯ КЛЕТКАМИ, ЭКСПРЕССИРУЮЩИМИ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) K CD19 | 2016 |
|
RU2752918C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ИЗБИРАТЕЛЬНОЙ ЭКСПРЕССИИ БЕЛКА | 2017 |
|
RU2795467C2 |
| CD123-СПЕЦИФИЧЕСКИЕ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ ДЛЯ ИММУНОТЕРАПИИ РАКА | 2015 |
|
RU2727290C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР | 2018 |
|
RU2770002C2 |
| КОМПОЗИЦИИ И СПОСОБЫ СЕЛЕКТИВНОЙ ДЕГРАДАЦИИ БЕЛКА | 2018 |
|
RU2811700C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, НАЦЕЛИВАЮЩИЕСЯ НА ВАРИАНТ III РЕЦЕПТОРА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА | 2017 |
|
RU2751662C2 |
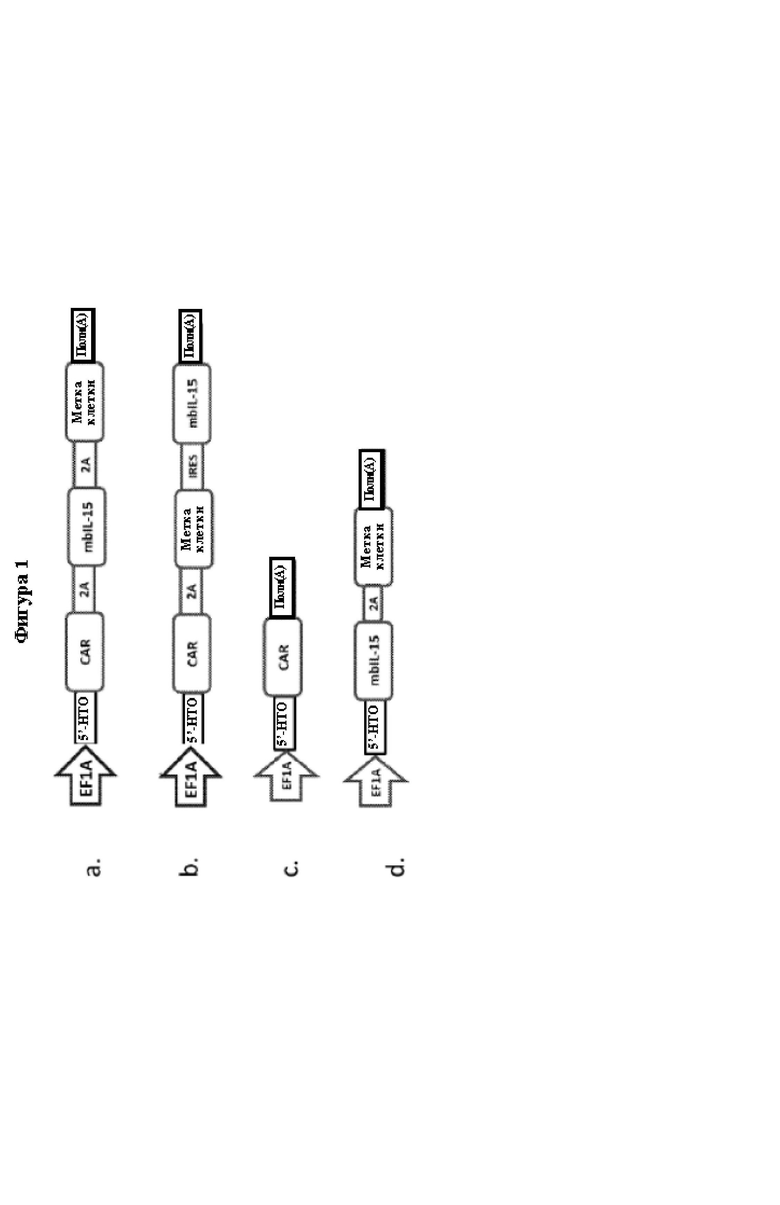
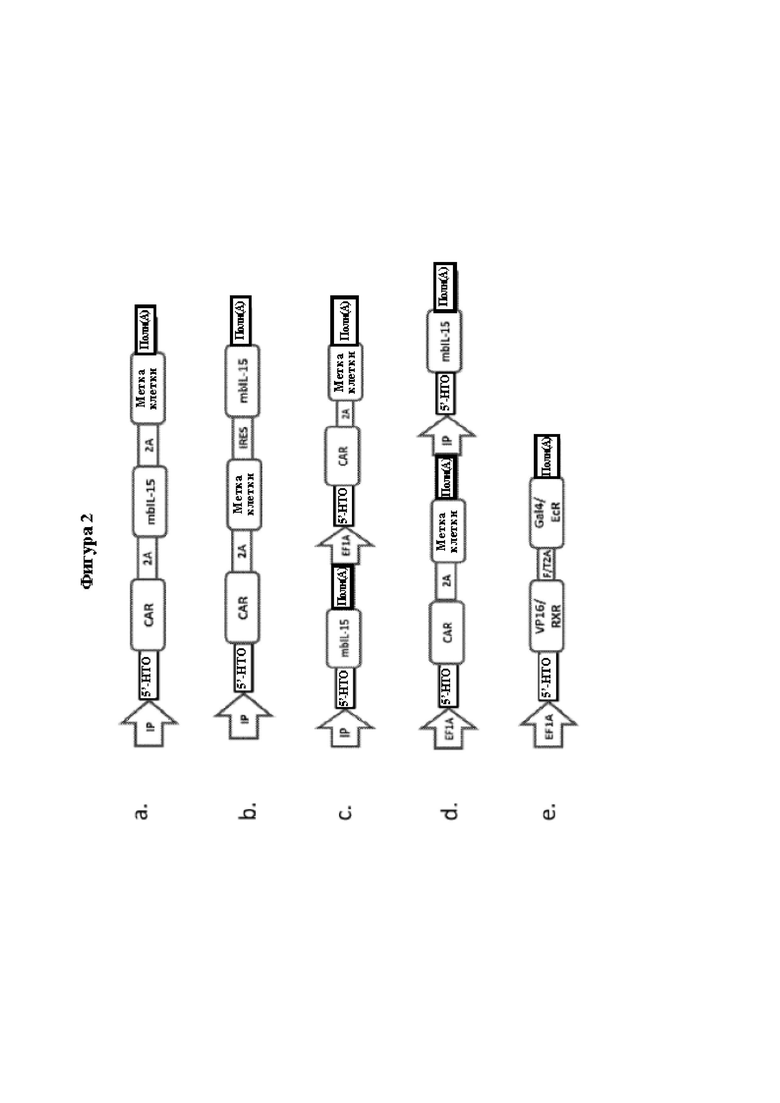

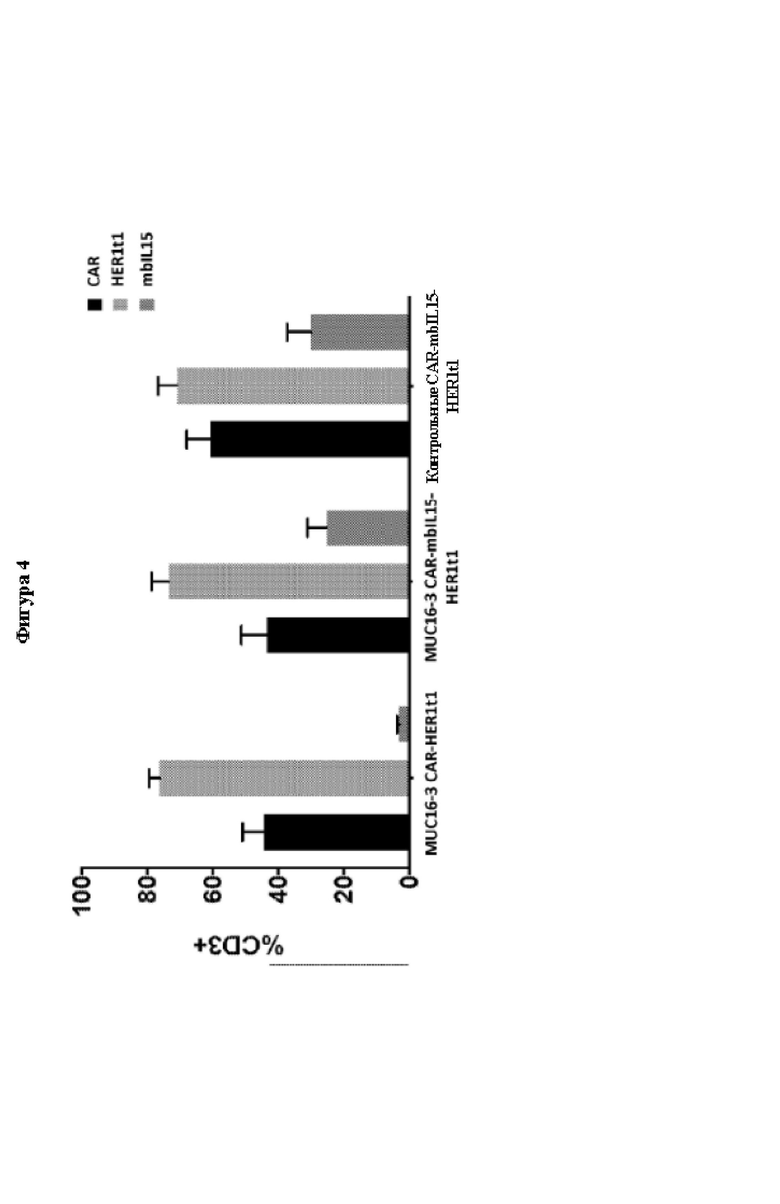

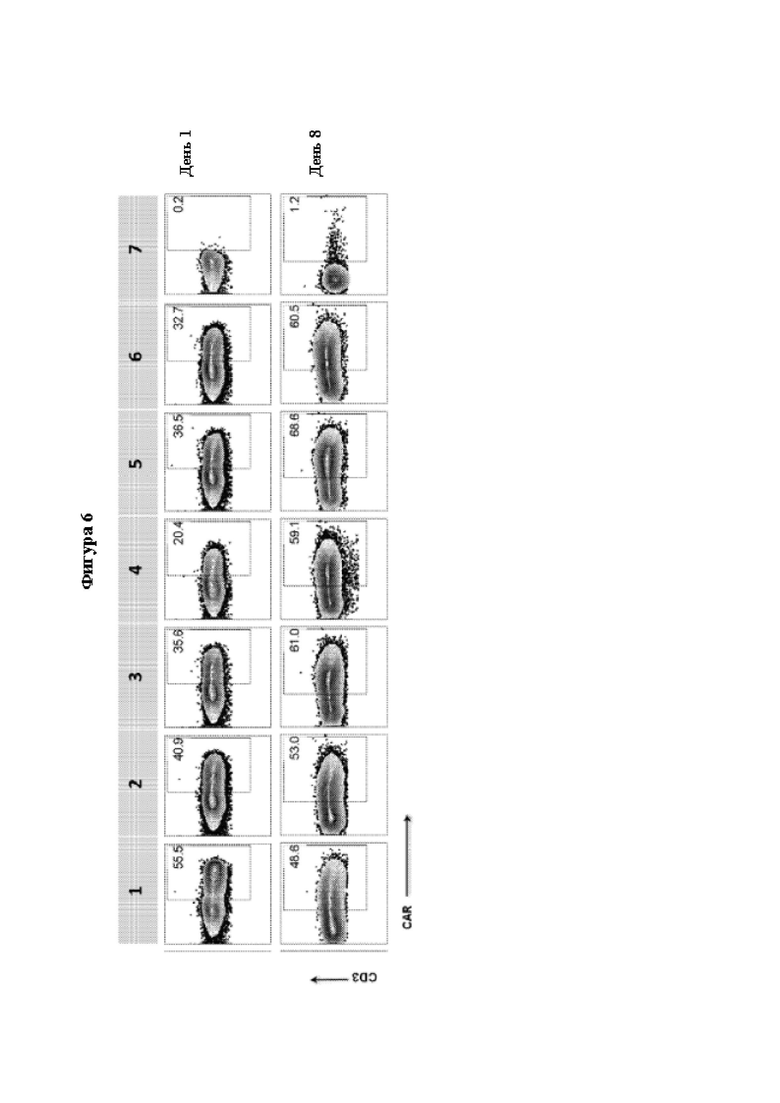
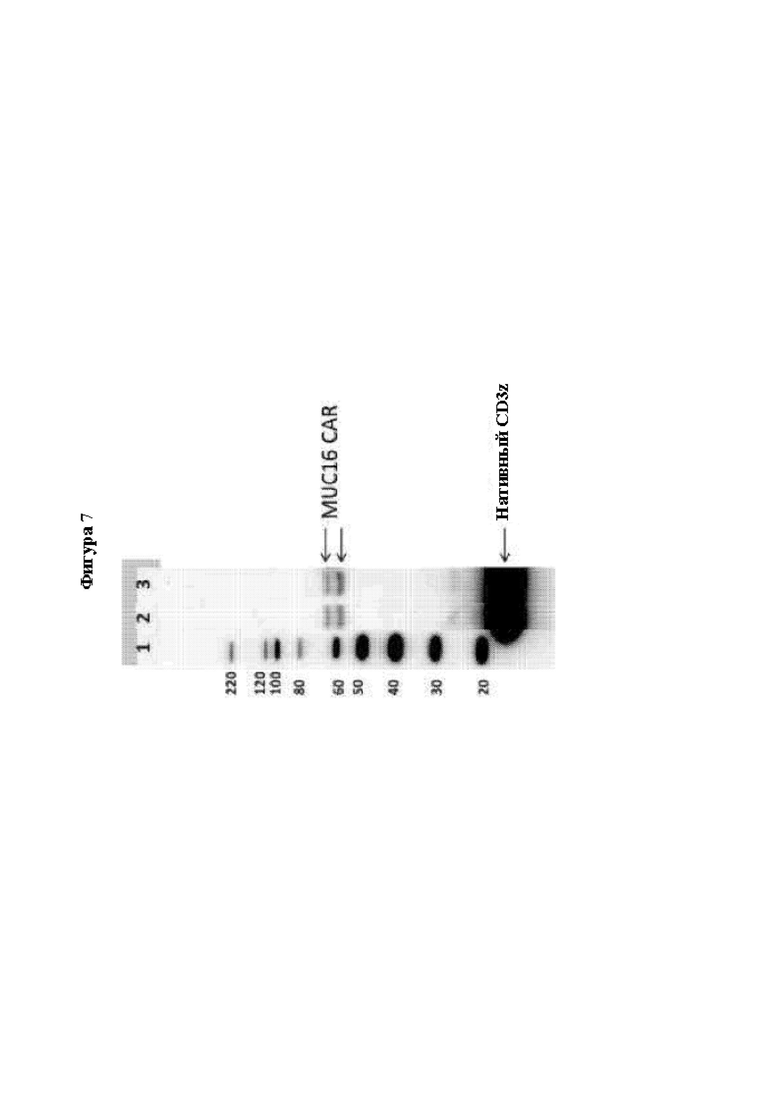
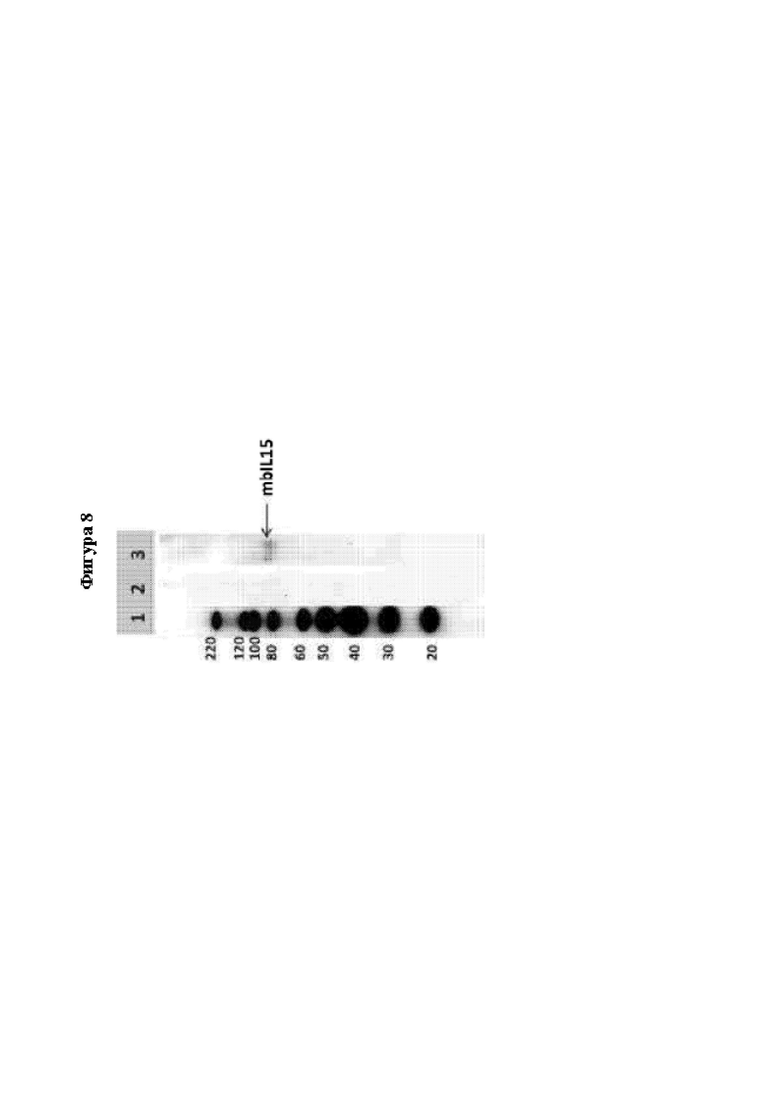
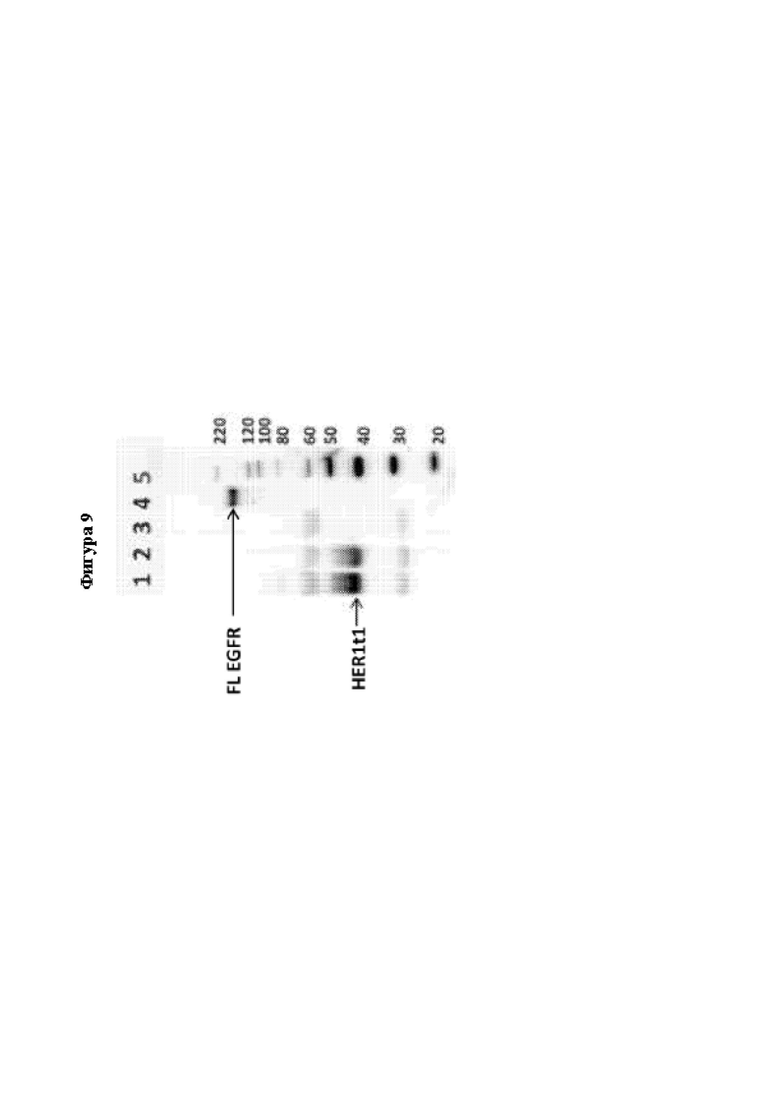
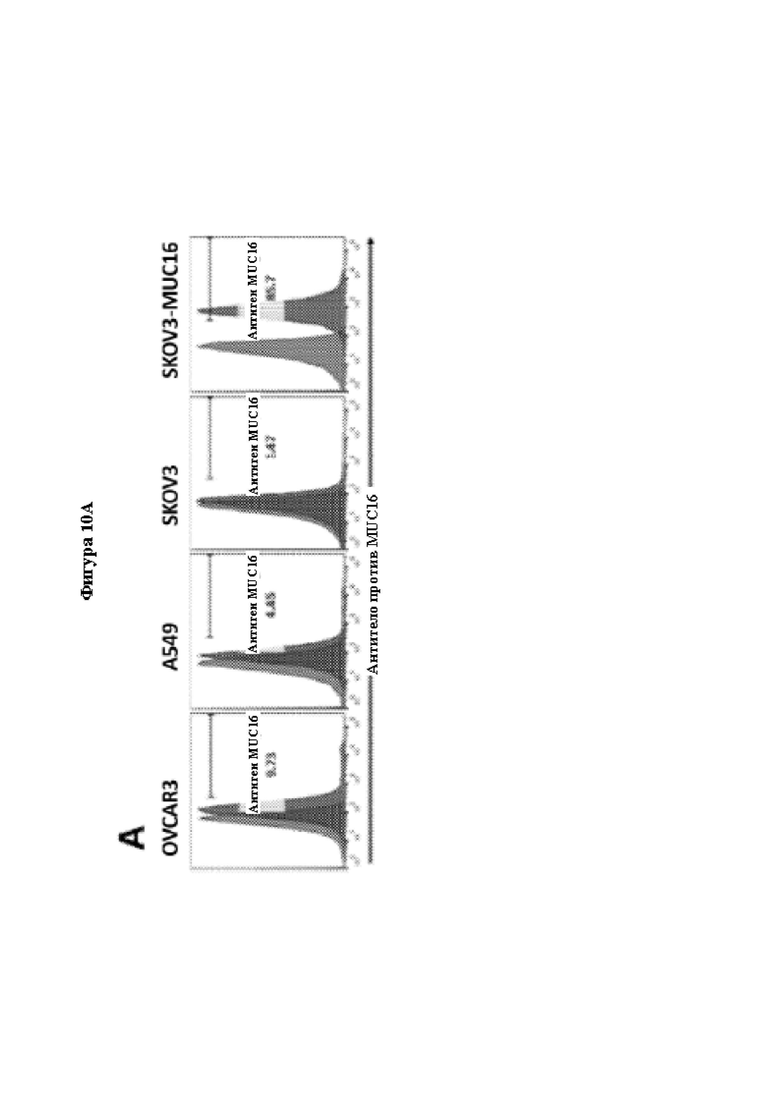
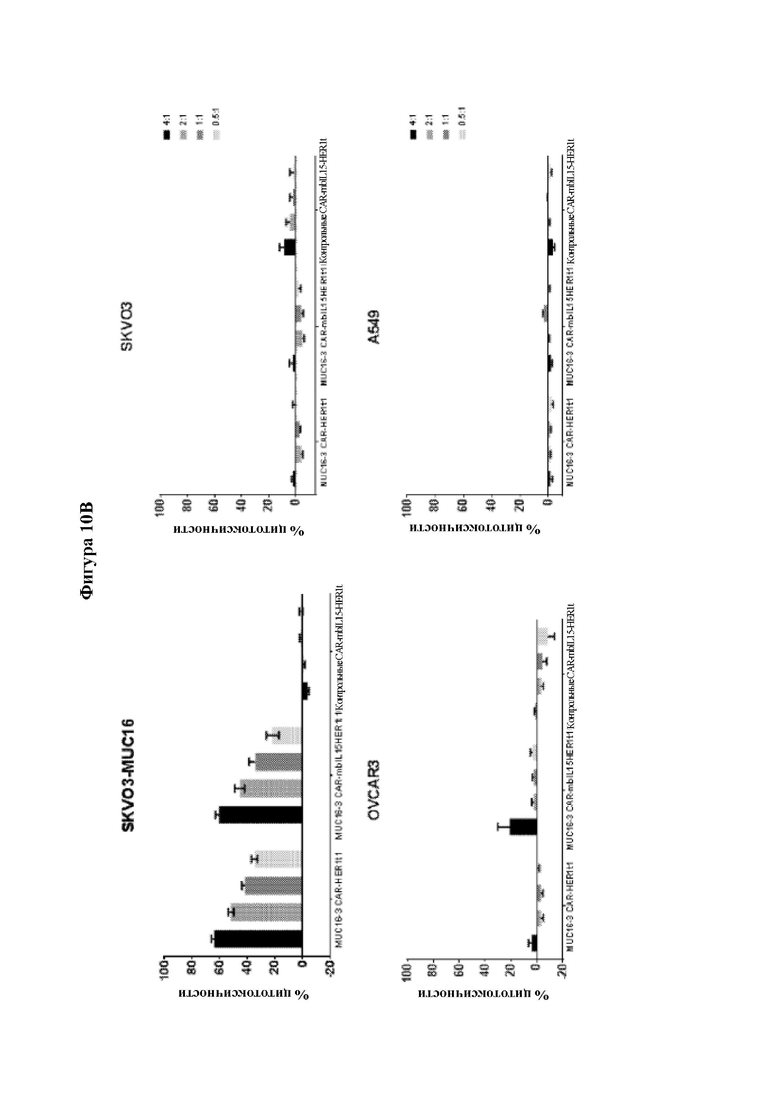
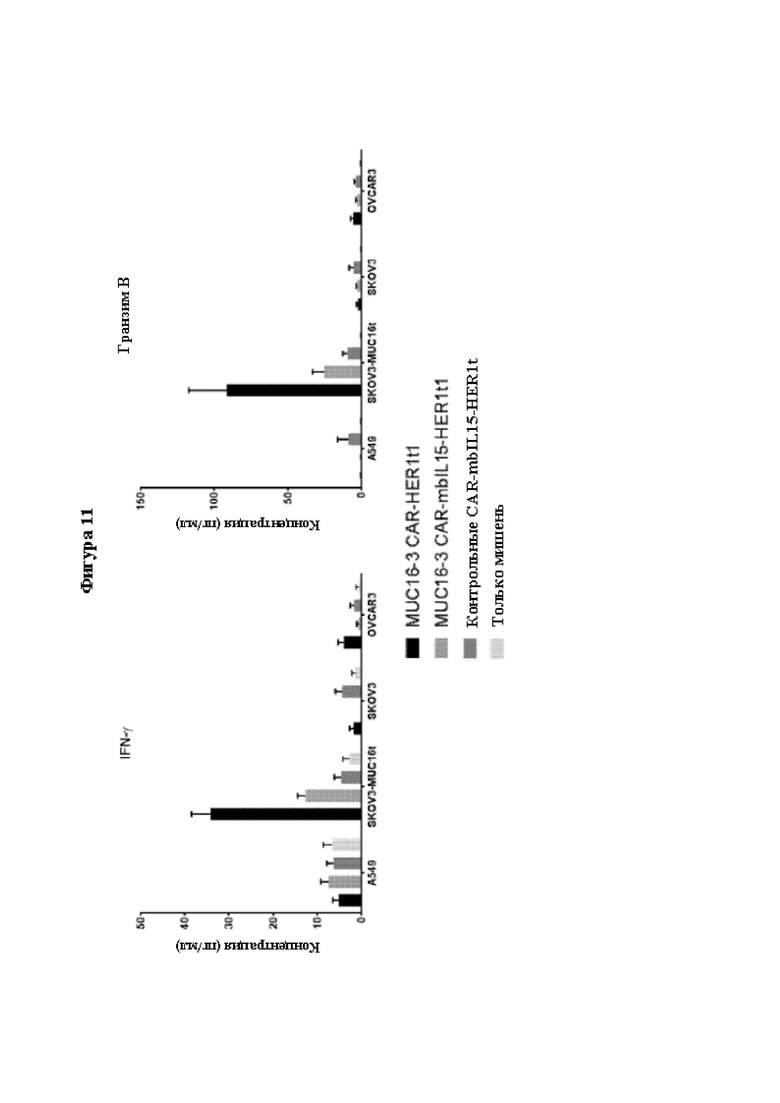
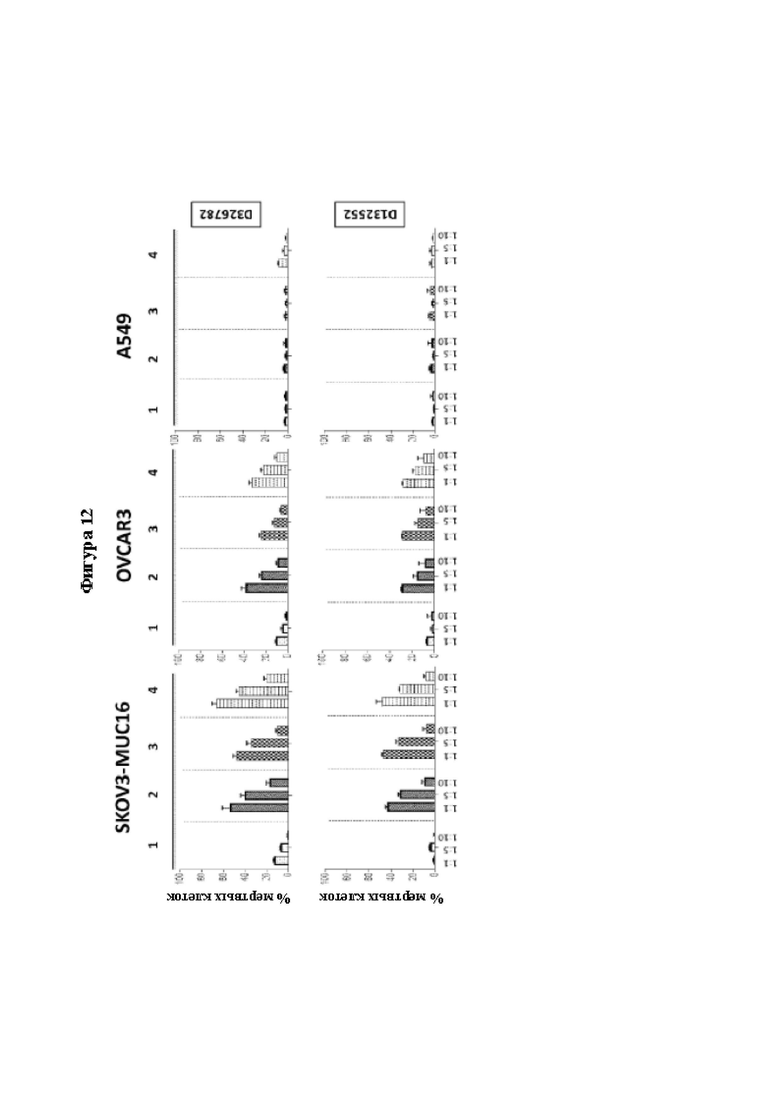
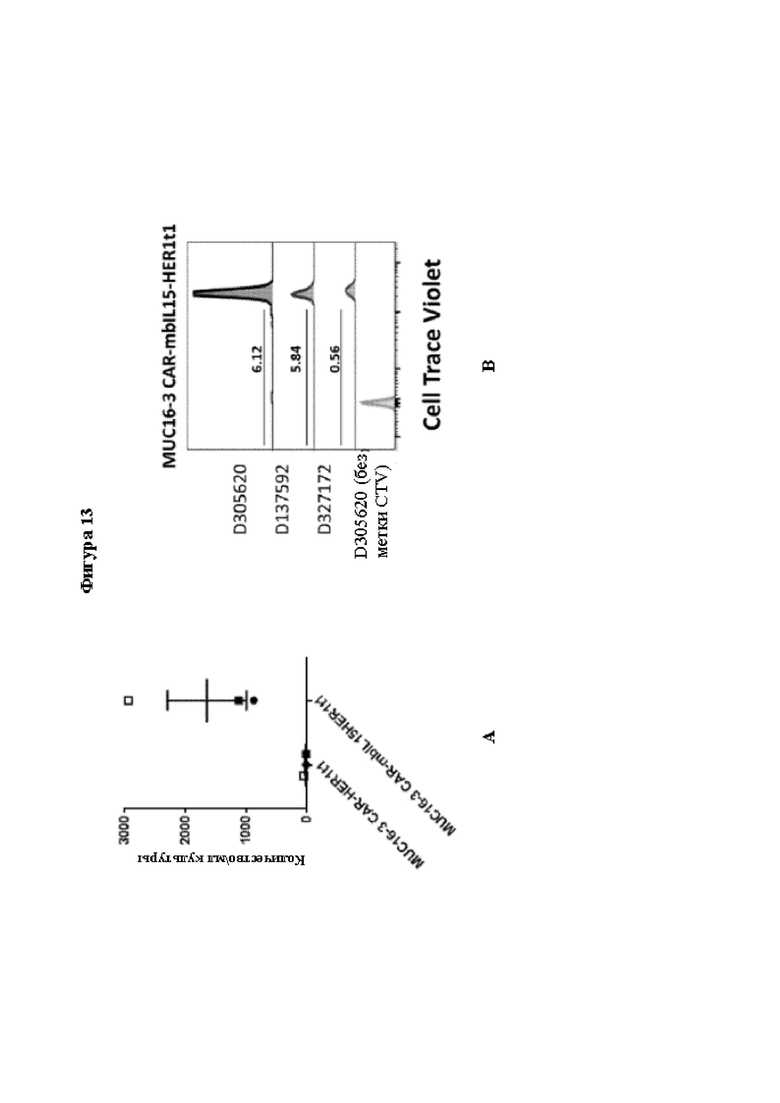

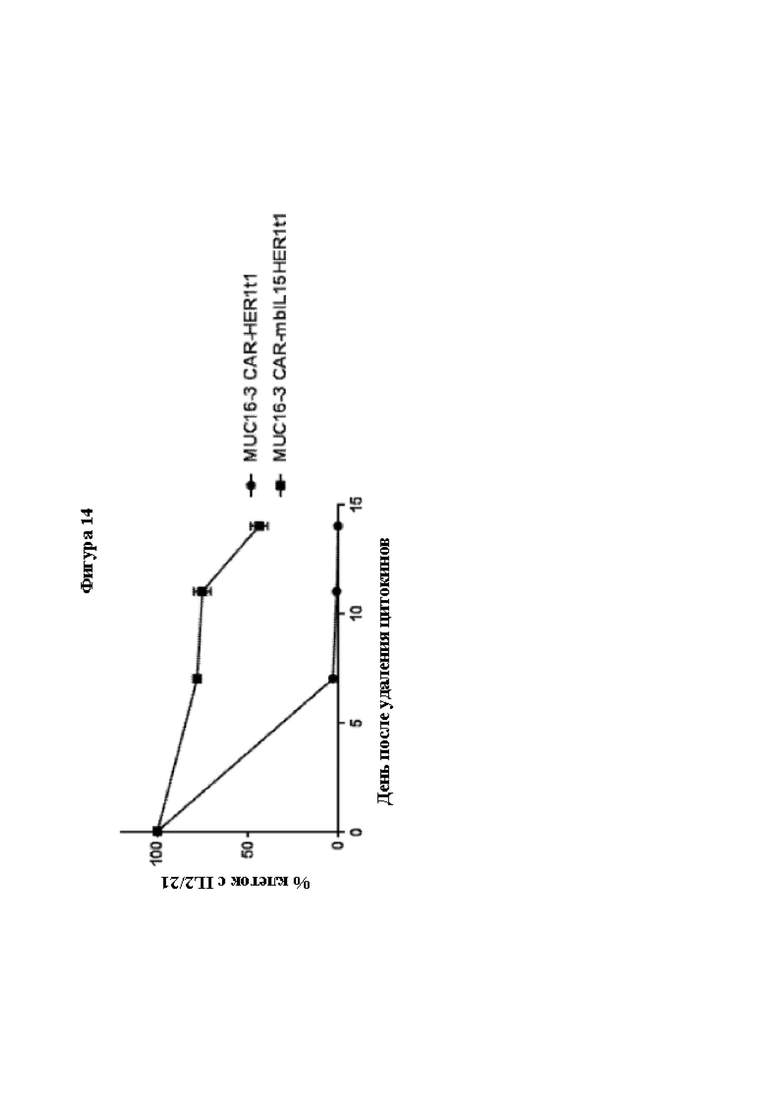
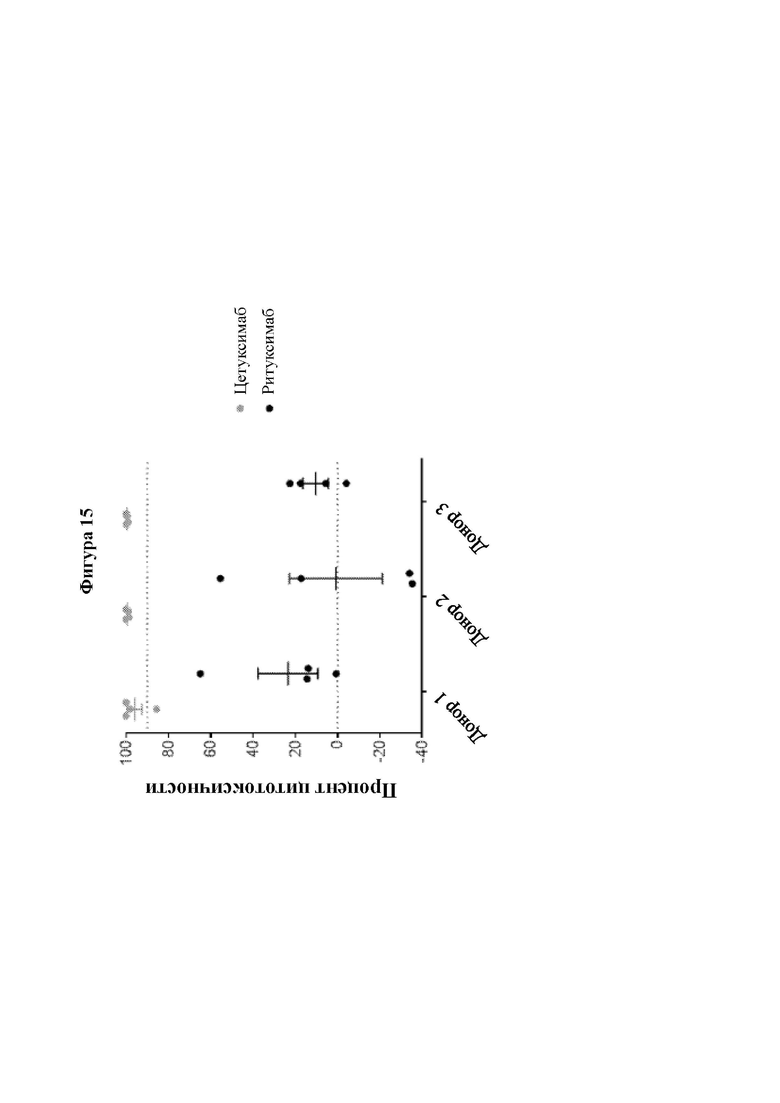
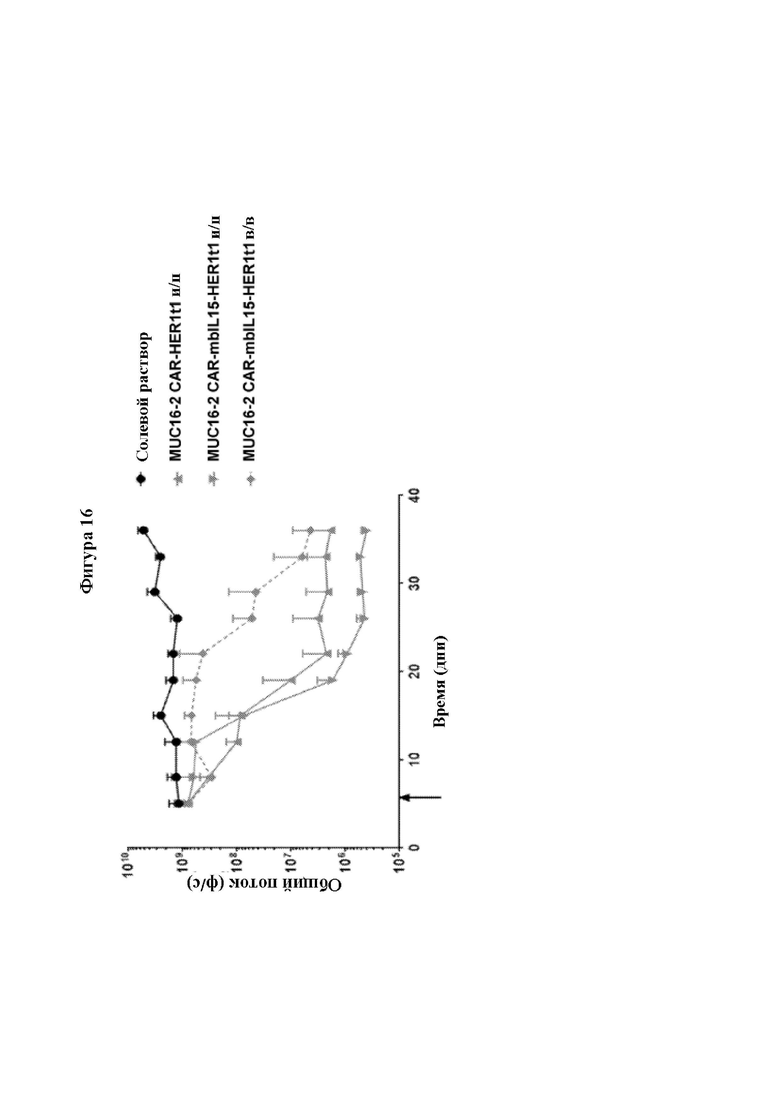
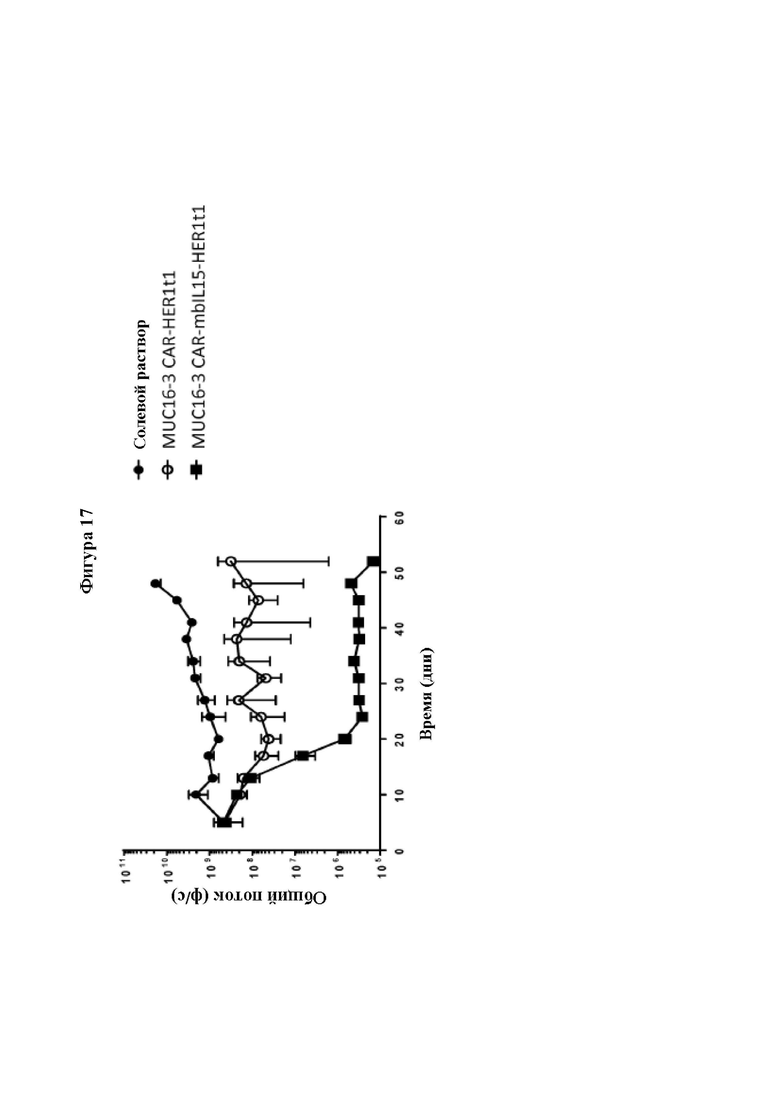
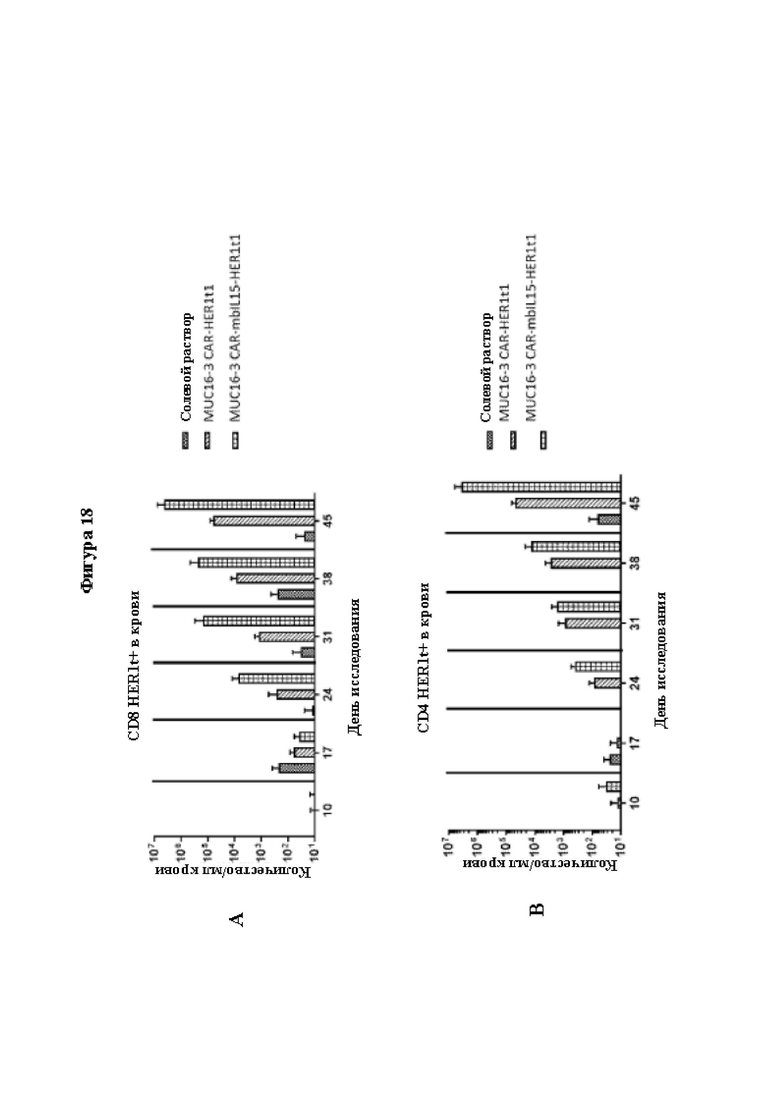
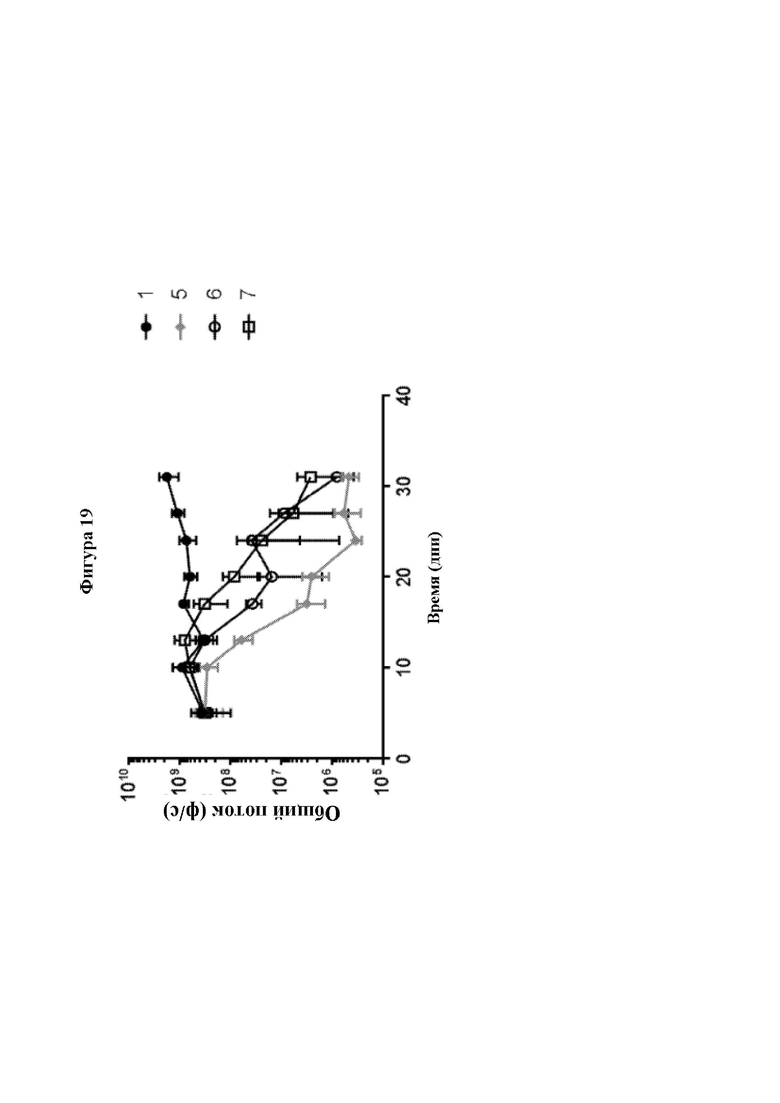
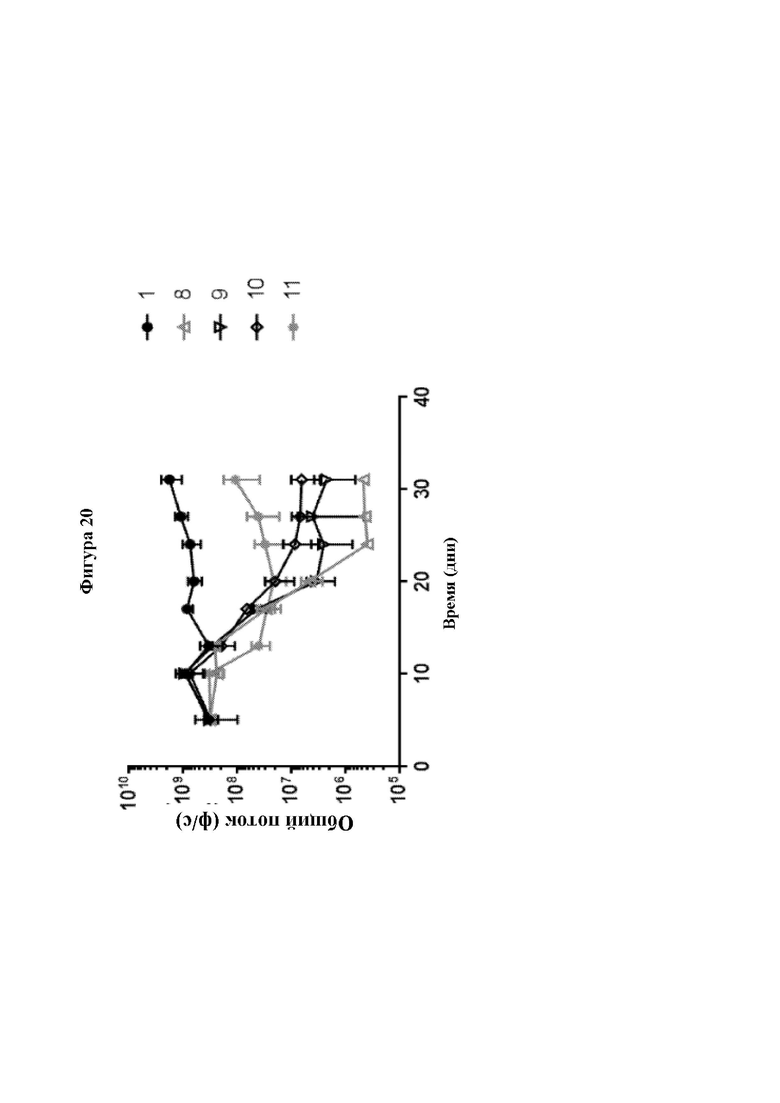
Изобретение относится к области биотехнологии, в частности к нуклеиновой кислоте, кодирующей химерный антигенный рецептор (CAR), содержащий домен, связывающий антиген MUC16, трансмембранный домен и внутриклеточный сигнальный домен, а также к вектору и клетке, ее содержащей. Также раскрыт способ стимуляции пролиферации и/или выживания сконструированных T-клеток, предусматривающий использование вышеуказанной нуклеиновой кислоты. Изобретение эффективно для лечения рака у субъекта. 5 н. и 14 з.п. ф-лы, 20 ил., 11 табл., 13 пр.
1. Нуклеиновая кислота, кодирующая химерный антигенный рецептор (CAR), причем указанный CAR содержит:
(a) домен, связывающий антиген MUC16, содержащий:
(i) первый полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 5, и второй полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 6;
(ii) первый полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 12, и второй полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 13; или
(iii) первый полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 14, и второй полипептид, который имеет по меньшей мере 90% идентичности последовательности аминокислот SEQ ID NO: 15;
(b) трансмембранный домен; и
(с) внутриклеточный сигнальный домен.
2. Нуклеиновая кислота по п. 1, отличающаяся тем, что указанный CAR содержит домен стебля, который содержит полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 16.
3. Нуклеиновая кислота по п. 1, отличающаяся тем, что указанный внутриклеточный сигнальный домен указанного CAR содержит полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 22.
4. Нуклеиновая кислота по п. 1, отличающаяся тем, что указанный внутриклеточный сигнальный домен указанного CAR содержит полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 23.
5. Нуклеиновая кислота по п. 1, отличающаяся тем, что указанный внутриклеточный сигнальный домен указанного CAR содержит полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 26.
6. Нуклеиновая кислота по п. 1, которая дополнительно кодирует укороченный рецептор эпидермального фактора роста.
7. Нуклеиновая кислота по п. 6, которая кодирует полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 65 или SEQ ID NO: 66.
8. Вектор для экспрессии химерного антигенного рецептора (CAR), где указанный вектор содержит: (а) остов; (b) нуклеиновую кислоту по любому из пп. 1-7; и (c) нуклеиновую кислоту, которая кодирует цитокин.
9. Вектор по п. 8, отличающийся тем, что указанный цитокин представляет собой IL-15 или IL-12.
10. Вектор по п. 8, отличающийся тем, что указанный вектор представляет собой лентивирусный вектор, ретровирусный вектор или невирусный вектор.
11. Вектор по п. 9, отличающийся тем, что указанный IL-15 представляет собой связанный с мембраной IL-15.
12. Вектор по п. 11, отличающийся тем, что указанный вектор кодирует полипептид, который имеет по меньшей мере 90% идентичности с последовательностью аминокислот SEQ ID NO: 69.
13. Вектор по п. 8, дополнительно содержащий нуклеиновую кислоту, кодирующую саморасщепляющийся пептид вируса Thosea asigna (T2A).
14. Эффекторная иммунная клетка для лечения рака, клетки которого экспрессируют MUC16, при этом указанная клетка представляет собой T-клетку, клетку-естественный киллер (NK), цитотоксический T-лимфоцит (CTL) или регуляторную T-клетку, и при этом указанная эффекторная иммунная клетка содержит вектор по п. 8.
15. Способ стимуляции пролиферации и/или выживания сконструированных T-клеток, указанный способ включает осуществление трансфекции T-клеток или предшественников T-клеток, полученных от субъекта: (а) вектором, содержащим нуклеиновую кислоту согласно любому из пп. 1-7; и (b) вектором, кодирующим транспозазу, с получением тем самым популяции сконструированных T-клеток или предшественников Т-клеток.
16. Способ по п. 15, дополнительно включающий культивирование указанной популяции сконструированных T-клеток ex vivo в течение 2 дней или менее.
17. Способ лечения рака у субъекта, имеющего рак, указанный способ включает введение указанному субъекту одной или более доз, содержащих по меньшей мере 102 клеток/кг сконструированных T-клеток, содержащих CAR, который кодирует нуклеиновая кислота согласно любому из пп. 1-7 и связанный с мембраной IL-15.
18. Способ по п. 17, отличающийся тем, что первую дозу эффективного количества сконструированных T-клеток вводят интраперитонеально или внутривенно.
19. Способ по п. 17, отличающийся тем, что указанная одна или более доз эффективного количества сконструированных T-клеток содержит по меньшей мере 102 клеток/кг.
| MYTHILI KONERU et al., IL-12 secreting tumor-targeted chimeric antigen receptor T cells eradicate ovarian tumors in vivo, OncoImmunology, 2015, Vol | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| WO2016205176 A1, 22.12.2016 | |||
| WO2017172981 A2, 05.10.2017 | |||
| LENKA V | |||
| HURTON et al., Tethered IL-15 augments antitumor activity and promotes a stem-cell memory subset in tumor-specific | |||
Авторы
Даты
2023-05-02—Публикация
2019-06-04—Подача