Изобретение относится к области органической химии, а именно к 5-(4-метоксифенил)-4-спиро-2,4-дигидро-3H-пиразол-3-онам формулы 1а, б:
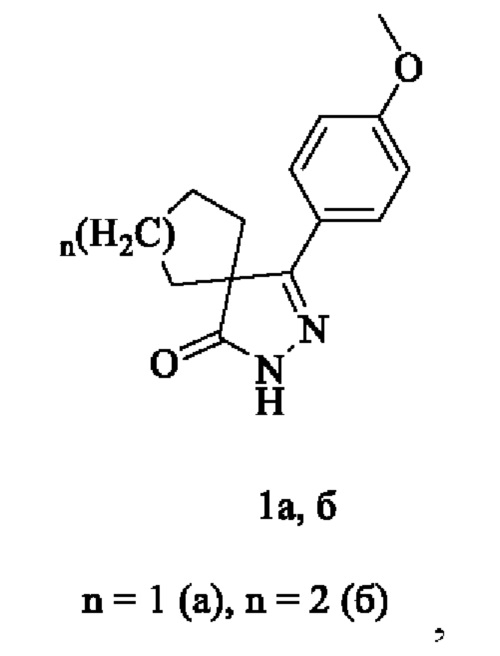
обладающим антиоксидантной активностью, которые могут быть использованы в фармакологии.
Аналогом по структуре заявляемым соединениям является 3-фенил-4-этил-1H-пиразол-5(4H)-он, обладающий биологической активностью [R.V. Ragavan, К.М. Kumar, V. Vijayakumar, S. Sarveswari, S. Ramaiah, A. Anbarasu, S. Karthikeyan, P. Giridharan, N.S. Kumari / beta-Keto esters from ketones and ethyl chloroformate: a rapid, general, efficient synthesis of pyrazolones and their antimicrobial, in silico and in vitro cytotoxicity studies // Org Med Chem Lett. 2013. Vol.3. №1. P. 6. DOI: 10.1186/2191-2858-3-6], формулы:
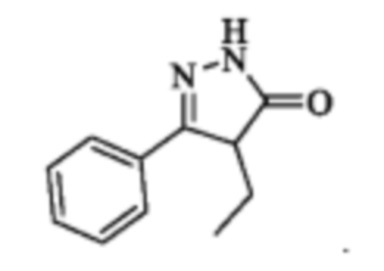
Задачей изобретения является изыскание в ряду 5-арил-4-замещенных-2,4-дигидро-3H-пиразол-3-онов новых соединений, обладающих биологической активностью и расширение арсенала средств воздействия на живой организм.
Поставленная задача решается синтезом 5-метоксифенил-4-спиро-2,4-дигидро-3H-пиразол-3-онов 1а, б, которые обладают умеренной антиоксидантной активностью.
Синтезируют заявляемые соединения 1а, б путем взаимодействия 2,5-метоксифенил-1,3,4-оксадазола 2 с метил 1-бромциклоалканкарбоксилатами 3а, б и цинком в среде растворителя с последующим выделением целевых продуктов, по следующей схеме:
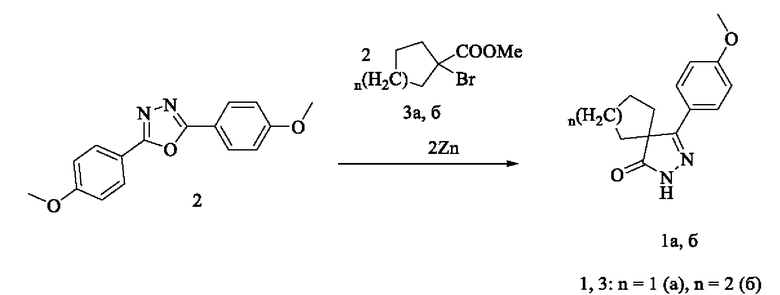
Процесс ведут при температуре 105-115°С, а в качестве растворителя используют толуол.
Изобретение иллюстрируется следующими примерами.
Пример 1. 4-(4-Метоксифенил)-2,3-диазаспиро[4.4]нон-3-ен-1-он (1а).
К смеси 2,0 г измельченного в мелкую стружку цинка, каталитического количества сулемы, 2.82 г (0.01 моль) 2,5-бис(4-метоксифенил)-1,3,4-оксадиазола 2, 20 мл безводного толуола и 2 мл ГМФТА добавляли по каплям при перемешивании смесь 4.55 г (0.022 моль) метилового эфира 1-бромциклопентанкарбоновой кислоты 3а в 10 мл безводного толуола. Затем реакционную смесь кипятили 4 ч, охлаждали, декантировали, гидролизовали 5%-ным раствором уксусной кислоты, органический слой отделяли, из водного слоя продукты реакции дважды экстрагировали толуолом. После сушки органической фазы безводным сульфатом натрия толуол отгоняли, продукт дважды перекристаллизовывали из этанола. Выход 45%, Т. пл. 190-192°С.
Спектр ИК, v, см-1: 3168 (NH), 1691 (СО). Спектр ЯМР 1Н, δ, м.д.: 1.95-2.05 м (2Н), 2.10-2.21 м (6Н) [(СН2)4], 3.85 с (3Н, МеО), 6.93 д (2Наром., J 8.8 Гц), 7.68 д (2Наром., J 8.8 Гц) (4-МеОС6Н4), 8.65 с (1Р, NH).
Соединение 1а представляет собой белое кристаллическое вещество, легкорастворимое в ДМСО, хлороформе, ацетоне, трудно растворимое в спирте и алканах, нерастворимое в воде. Устойчиво при хранении в обычных условиях.
Пример 2. 4-(4-Метоксифенил)-2,3-диазаспиро[4.5]дец-3-ен-1-он (1б).
К смеси 2,0 г измельченного в мелкую стружку цинка, каталитического количества сулемы, 2.82 г (0.01 моль) 2,5-бис(4-метоксифенил)-1,3,4-оксадиазола 2, 20 мл безводного толуола и 2 мл ГМФТА добавляли по каплям при перемешивании смесь 4.86 г (0.022 моль) метилового эфира 1-бромциклогексанкарбоновой кислоты 36 в 10 мл безводного толуола. Затем реакционную смесь кипятили 4 ч, охлаждали, декантировали, гидролизовали 5%-ным раствором уксусной кислоты, органический слой отделяли, из водного слоя продукты реакции дважды экстрагировали толуолом. После сушки органической фазы безводным сульфатом натрия толуол отгоняли, продукт дважды перекристаллизовывали из этанола. Выход 49%, Т.пл. 190-191°С.
ИК спектр, v, см-1: 3198 (NH), 1685 (С=O). Спектр ЯМР 1Н, δ, м.д.: 1.24-2.34 м [10Н, (СН2)5], 3.84 с (3Н, ОСН3), 6.93 д (2Наром., J 8.7 Гц), 7.75 д (2Наром., J 8.7 Гц) (4-МеОС6Н4), 9.23 с (1Н, NH).
Соединение 1б представляет собой белое кристаллическое вещество, легкорастворимое в ДМСО, хлороформе, ацетоне, трудно растворимое в спирте и алканах, нерастворимое в воде. Устойчиво при хранении в обычных условиях.
Пример 3. Исследование соединений (1а, б) на наличие антиоксидантной активности.
Антиоксидантная активность изучалась спектрофотометрическим методом по способности растворов исследуемых веществ улавливать ярко окрашенные радикалы 2,2-дифенил-1-пикрилгидразила (DPPH) [Moore J.С, Liangli L.Yu. P. 118-172. DOI: 10.1002/9780470228333.CH9 в [Wheat Antioxidants (ed. Liangli Yu). Wiley. 2007. DOI: 10.1002/9780470228333]].
Фотометрический DPPH реагент содержал 0.2 мМ раствор DPPH в метаноле. Растворы (концентрация 15 мкмоль/мл) исследуемых соединений и эталонов (агидол-1, аскорбиновая кислота) в ДМСО в количестве 100 мкл добавлялись к DPPH реагенту (100 мкл) в лунки 96-луночного планшета. Реакционная смесь выдерживалась при 20°С в течение 20 мин. в темноте. Оптическую плотность реакционных смесей измеряли при 517 нм. Калибровка проводилась по свежеприготовленному раствору DPPH в смеси ДМСО-метанол, 1 к 1. Убыль радикала рассчитывали по формуле:
Убыль радикала (%)=[(А0 - A1)/A0]⋅100, где А0 поглощение раствора DPPH без исследуемого образца, A1 поглощение раствора DPPH в присутствии исследуемого образца.
Результаты представлены в таблице.

Как видно из таблицы, заявляемые соединения 1а, 6 проявляют умеренную антиоксидантную активность. Следовательно, заявляемые соединения могут найти применение в фармакологии.
Изобретение относится к области органической химии, а именно к применению производных 5-(4-метоксифенил)-4-спиро-2,4-дигидро-3H-пиразол-3-онов формулы 1а, б в качестве средств, обладающих антиоксидантной активностью. Технический результат – умеренная антиоксидантная активность, проявляемая соединениями формулы 1а, б. 1 табл., 3 пр.
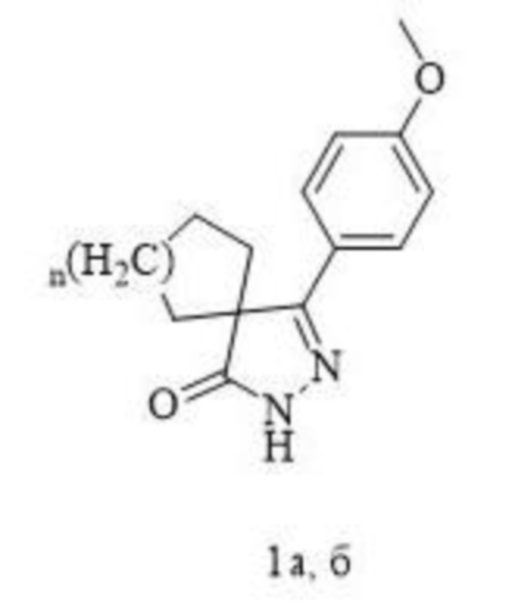
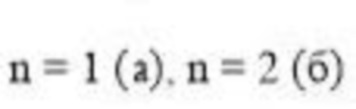
Применение 5-(4-метоксифенил)-4-спиро-2,4-дигидро-3H-пиразол-3-онов формулы 1а, б
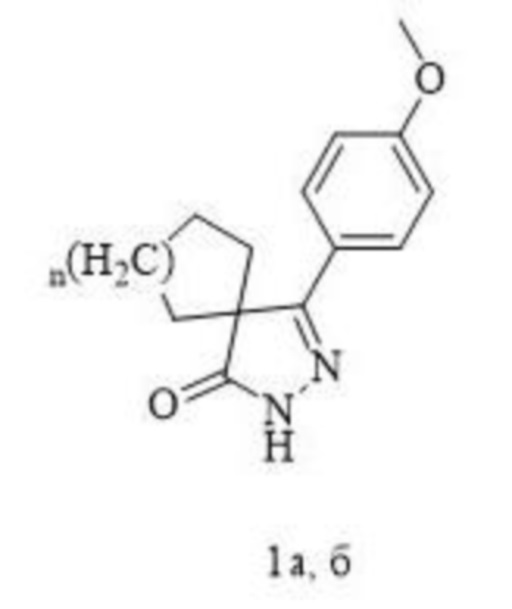
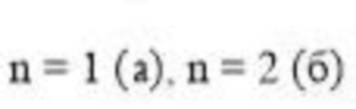
в качестве средств, обладающих антиоксидантной активностью.
| Способ армировки бронзовых вкладышей сталью | 1927 |
|
SU33049A1 |
| Шушакова Е.Ю | |||
| и др., Взаимодействие метил 1-бромциклоалканкарбоксилатов с цинком и 2,5-диарил-1,3,4-оксадиазолами | |||
| Современные аспекты химии | |||
| Материалы IV молодежной школы-конференции, Пермь, 2017, с.57 | |||
| Nikiforova Е.А | |||
| et al., Reaction of Reformatsky reagents with 2,5-diphenyl-1,3,4-oxadiazole | |||
| Mendeleev Communications, | |||
Авторы
Даты
2023-12-07—Публикация
2023-05-03—Подача