ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к фармацевтической области, в частности к соединениям, содержащим структуру дигидроизохинолинон/изоиндолинон и структуру пиримидин/пиридин, и способам их получения, а также к способам и применениям для лечения и/или предотвращения заболеваний.
УРОВЕНЬ ТЕХНИКИ
Семейство белков циклин-зависимых киназ (CDK) состоит из представителей, которые являются ключевыми регуляторами цикла деления клеток (CDK клеточного цикла), представителей, которые участвуют в регуляции транскрипции генов (CDK транскрипции), и представителей с другими функциями. Для активации CDK требуется ассоциация с регуляторной субъединицей - циклином. CDK клеточного цикла - CDKl/циклин В, СОК2/циклин А, СОК2/циклин Е, СОК4/циклин D и СЭКб/циклин D - среди CDK клеточного цикла активируются в последовательном порядке, чтобы запустить цикл деления клеток и провести клетку через него. Транскрипционные CDK - СОК9/циклин Т и СОК7/циклин Н -регулируют активность РНК-полимер азы II за счет фосфорилирования карбоксиконцевого домена (CTD). Положительный фактор транскрипции b (P-TEFb) является гетеродимером CDK9 и одного из четырех партнеров-циклинов (циклина Т1, циклина К, циклина Т2а или T2b).
В то время как CDK9 (идентификационный номер в базе данных NCBI GenBank Gene ID: 1025) участвует исключительно в регуляции транскрипции, CDK7 дополнительно участвует в регуляции клеточного цикла в качестве CDK-активирующей киназы (САК).
Транскрипция генов РНК-полимеразой II инициируется сборкой преинициаторного комплекса в промоторной области и фосфорилированием Ser 5 и Ser 7 CTD комплексом СОК7/циклин Н. Для большей части генов РНК-полимераза II останавливает транскрипцию мРНК после того, как она перемещается на 20 - 40 нуклеотидов по матрице ДНК. Эта остановка РНК-полимеразы II вблизи промотора опосредована отрицательными факторами элонгации и признана основным механизмом контроля для регуляции экспрессии быстро индуцируемых генов в ответ на различные стимулы (Cho et al., Cell Cycle 9, 1697, 2010). P-TEFb играет решающую роль в преодолении остановки РНК-полимеразы II вблизи промотора и переходе в состояние продуктивной элонгации путем фосфорилирования Ser2 CTD, а также путем фосфорилирования и инактивации негативных факторов элонгации.
Активность самого P-TEFb регулируется несколькими механизмами. Около половины клеточного P-TEFb существует в неактивном комплексе с 7SK малой ядерной РНК (7SK мяРНК), La-родственным белком 7 (LARP7/PIP7S) и индуцируемыми гексаметилен-бис-ацетамидом белками 1/2 (HEXIM1/2, Не et al., Mol Cell 29, 588, 2008). Оставшаяся половина P-TEFb существует в активном комплексе, содержащем бромдомен-содержащий белок Brd4 (Yang et al., Mol Cell 19, 535, 2005). Brd4 привлекает P-TEFb посредством взаимодействия с ацетилированными гистонами в области хроматина, инициированными для транскрипции генов. Посредством поочередного взаимодействия со своими полржительными и отрицательными регуляторами P-TEFb поддерживается в функциональном равновесии: P-TEFb, связанный с комплексом 7SK мяРНК, представляет собой запас, из которого может высвобождаться активный P-TEFb при необходимости транскрипции и пролиферации клеток. Кроме того, активность P-TEFb регулируется посттрансляционными модификациями, включая фосфорилирование/дефосфорилирование, убиквитинирование и ацетилирование.
Нарушенная регуляция активности киназы CDK9 гетеродимера P-TEFb связана с различными патологическими состояниями у человека, такими как гиперпролиферативные заболевания (например, рак), вызванные вирусами инфекционные заболевания или сердечно-сосудистые заболевания.
Рак рассматривается как гиперпролиферативное нарушение, опосредованное дисбалансом пролиферации и гибели клеток (апоптоза). Высокие уровни антиапоптотических белков семейства Вс1-2 обнаруживаются в различных опухолях человека и служат причиной длительной выживаемости опухолевых клеток и резистентности к терапии. Было показано, что ингибирование активности киназы P-TEFb снижает транскрипционную активность РНК-полимеразы II, что приводит к снижению количества короткоживущих антиапоптотических белков (особенно Мс1-1 и XIAP), восстанавливая способность опухолевых клеток подвергаться апоптозу. Ряд других белков, связанных с трансформированным фенотипом опухоли (таких как транскрипты чувствительных к Мус, NF-kB генов, митотические киназы), либо представляют собой короткоживущие белки, либо кодируются короткоживущими транскриптами (чувствительными к сниженной активности РНК-полимеразы II, опосредованной ингибированием P-TEFb).
Исследования лекарственной устойчивости к ингибитору CDK9 не проводились. В настоящем изобретении линии клеток, устойчивые к ингибитору CDK9, получали путем длительного введения, и было обнаружено, что соединения в соответствии с настоящим изобретением ингибируют линии клеток, которые обладают лекарственной устойчивостью вследствие длительного введения ингибитора CDK9. После дополнительной экспрессии мутантного белка CDK9 в линиях клеток с лекарственной устойчивостью и детектирования было обнаружено, что соединения в соответствии с настоящим изобретением могут преодолевать приводящую к лекарственной устойчивости мутацию CDK9.
Кроме того, многие вирусы используют транскрипционный аппарат клетки-хозяина для транскрипции своего собственного генома. В случае ВИЧ-1 РНК-полимераза II привлекается в промоторную область в вирусных LTR. Вирусный белок-активатор транскрипции (Tat) связывается с образующимися вирусными транскриптами и преодолевает остановку РНК-полимеразы II вблизи промотора путем привлечения P-TEFb, который, в свою очередь, способствует элонгации транскриптов. Кроме того, белок Tat увеличивает долю активного P-TEFb путем замещения ингибирующих P-TEFb белков HEXIM1/2 в комплексе 7SK мяРНК. Недавно полученные данные показали, что ингибирование активности киназы P-TEFb является достаточным для блокирования репликации ВИЧ-1 при концентрациях ингибитора киназы, которые не являются цитотоксичными для клеток-хозяев (обзор приведен в Wang & Fischer, Trends Pharmacol Sci 29, 302, 2008). Аналогичным образом, привлечение P-TEFb вирусными белками было описано для других вирусов, таких как вирус Эпштейна-Барр, ассоциированный с В-клеточным раком, в котором белок ядерного антигена EBNA2 взаимодействует с P-TEFb (Bark-Jones et al., Oncogene, 25, 1775, 2006), и Т-лимфотропный вирус человека 1 типа (HTLV-1), в котором активатор транскрипции Tax привлекает P-TEFb (Zhou et al., J Virol. 80, 4781, 2006).
Гипертрофия сердца - адаптивная реакция сердца на механическую перегрузку и давление (гемодинамический стресс, например, гипертония, инфаркт миокарда) - может привести в долгосрочной перспективе к сердечной недостаточности и смерти. Было показано, что гипертрофия сердца связана с повышенной транскрипционной активностью и фосфорилированием CTD РНК-полимеразы II в клетках сердечной мышцы. Было обнаружено, что P-TEFb активируется в результате диссоциации из неактивного комплекса 7SK мяРНК/НЕХ1М1/2. Эти обнаруженные факты позволяют рассматривать фармакологическое ингибирование активности киназы P-TEFb в качестве терапевтического подхода для лечения гипертрофии сердца (обзор приведен в Dey et al., Cell Cycle 6, 1856, 2007).
Таким образом, многочисленные линии свидетельств указывают на то, что селективное ингибирование активности киназы CDK9 гетеродимера P-TEFb (=CDK9 и один из четырех партнеров-циклинов: циклин Т1, циклин К, циклин Т2а или T2b) представляет собой инновационный подход к лечению таких заболеваний, как рак, вирусные заболевания и/или заболевания сердца. CDK9 относится к семейству из по меньшей мере 13 близкородственных киназ, из которых подгруппа CDK клеточного цикла выполняет несколько ролей в регуляции пролиферации клеток. Таким образом, ожидается, что одновременное ингибирование CDK клеточного цикла (например, CDK1/циклин В, CDK2/циклин А, CDK2/циклин Е, CDK4/циклин D, СЭКб/циклин D) и CDK9 будет влиять на нормальные пролиферирующие ткани, такие как слизистая оболочка кишечника, лимфатические и гемопоэтические органы и репродуктивные органы. Для максимизации широты терапевтического действия ингибиторов киназы CDK9 требуются молекулы с высокой селективностью по отношению к CDK9.
В целом, хотя известны различные ингибиторы CDK, все еще требуются селективные ингибиторы CDK9 для лечения заболеваний, таких как гиперпролиферативные заболевания, вирусные заболевания и/или заболевания сердца, которые могут обеспечить одно или более преимуществ по сравнению с соединениями, известными из уровня техники.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к ингибитору киназы, содержащему соединение формулы (I) или его фармацевтически приемлемую соль, сольват, сложный эфир, кислоту, метаболит или пролекарство,
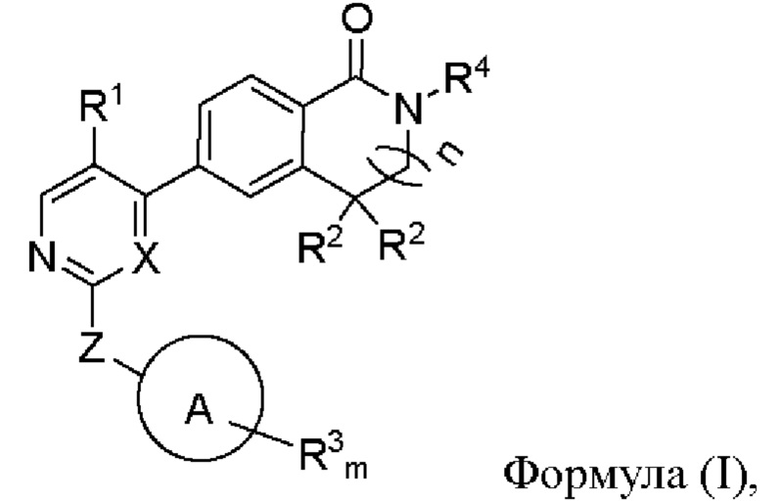
где А выбран из группы, состоящей из циклогексила, фенила, пиридинила и пиперидила;
X представляет собой СН или N;
Z представляет собой -NH- или -NH-C(=0)-;
п представляет собой 0 или 1;
R1 выбран из группы, состоящей из водорода, галогена, циано, (С1-С6)алкила и (С1-С6)галогеналкила;
R2 выбраны из группы, состоящей из водорода и (С1-С6)алкила, или два R2 вместе образуют (С3-С6)циклоалкил;
m выбран из целого числа 1 - 3, и каждый R3 независимо выбран из группы, состоящей из водорода, -NH-(С1-С3)алкил-(С1-С3)алкокси, галогена, (С1-С6)алкила, (С1-С6)алкокси, (С1-С6)галогеналкила, (С1-С6)алкилациламино, (С1-С6)алкилсульфонила, (С1-С6)алкилсульфонамидо, аминосульфонила, (С1-С6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (С 1-С6)алкилом, карбоксил(С1-С3)алкилом, аминосульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С1-С3)алкилом,
(С1-С3)алкилсульфонил(С3-С6)циклоалкилом, гетероциклиламиноацила в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, гетероциклилом, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, -S(=O)(=NH)(С1-С3)алкилом и -(С1-С3)алкил-S(=O)(=NH)(С1-С3)алкилом;
R4 выбран из группы, состоящей из водорода и (С1-С6)алкила.
В предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ia) или его фармацевтически приемлемой соли, сольвату сложному эфиру, кислоте, метаболиту или пролекарству,
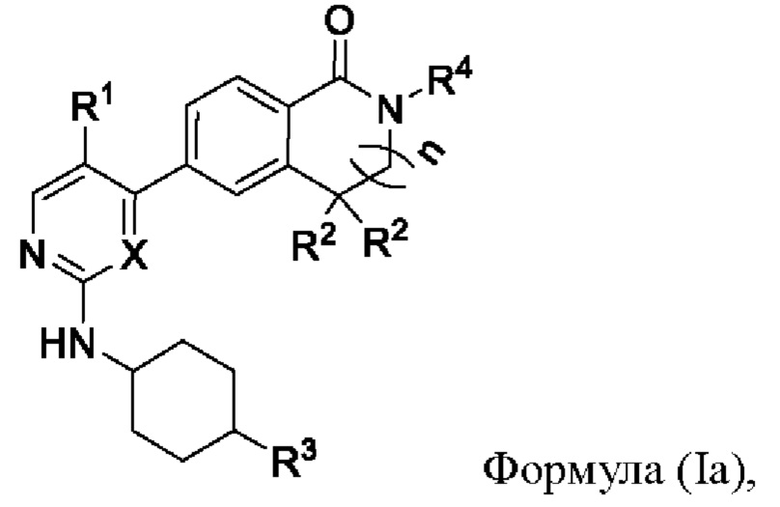
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В этом варианте реализации X предпочтительно представляет собой N; в другом варианте реализации R3 предпочтительно представляет собой -NH-(С1-С3)алкил-(С1-С3)алкокси или карбоксил(С1-С3)алкил.
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ib) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
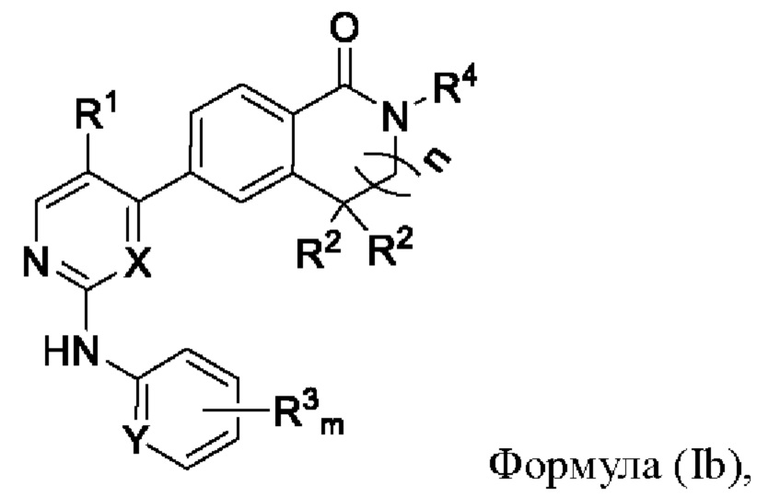
где Y представляет собой СН или N; X, m, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В более предпочтительном аспекте X представляет собой N; в другом предпочтительном аспекте Y представляет собой СН.
В другом предпочтительном аспекте каждый R3 независимо выбран из группы, состоящей из галогена, (С1-С6)алкила, (С1-С6)алкокси, (С1-С6)галогеналкила, (С1-С6)алкилсульфонила, (С1-С6)алкилсульфонамидо, аминосульфонила, (С1-С6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, аминосульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С1-С3)алкилом,
(С1-С3)алкилсульфонил(С3-С6)циклоалкилом, гетероциклиламиноацила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, гетероциклила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, -S(=O)(=NH)(С1-С3)алкиломи -(С1-С3)алкил-S(=O)(=ХН)(С1-С3)алкилом.
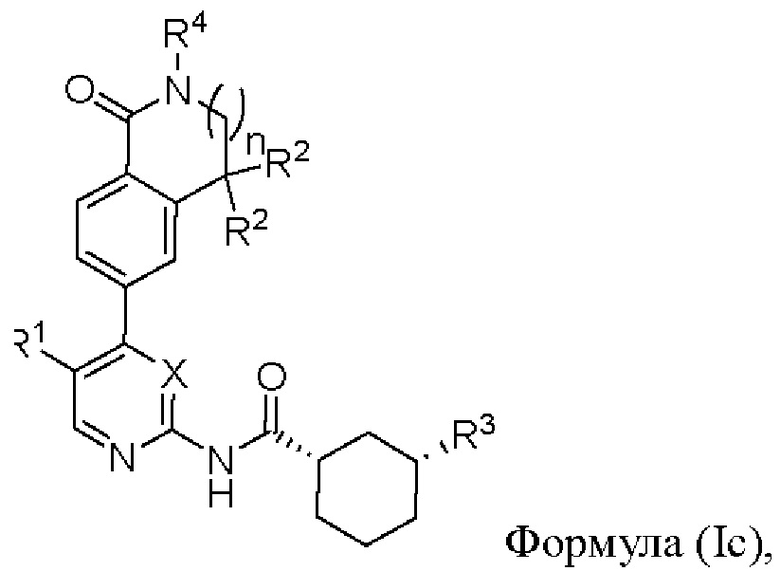
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ic) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
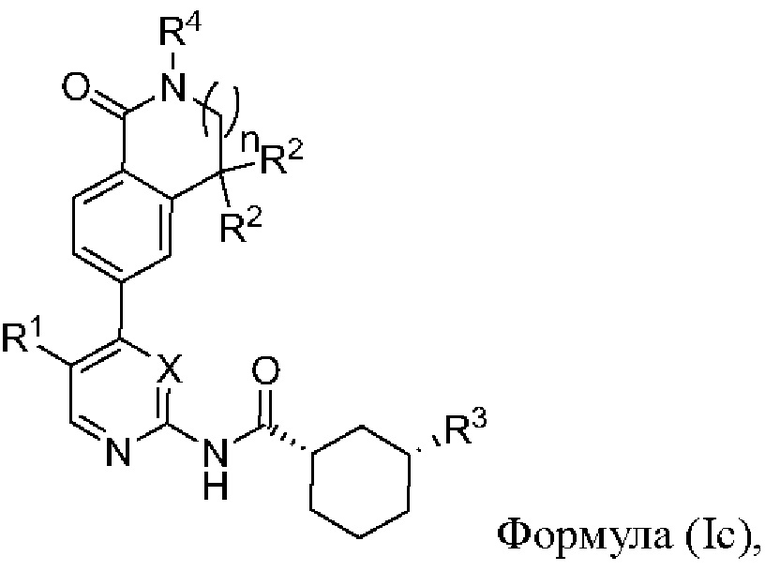
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В более предпочтительном аспекте R3 представляет собой (С1-С6)алкилациламино.
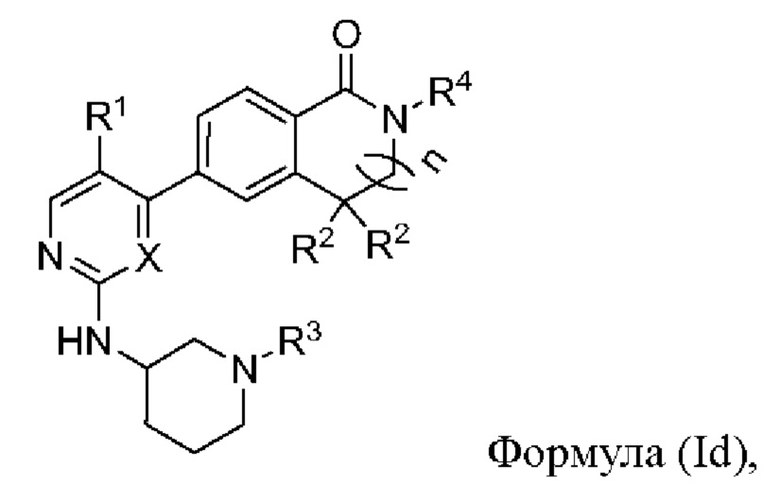
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Id) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
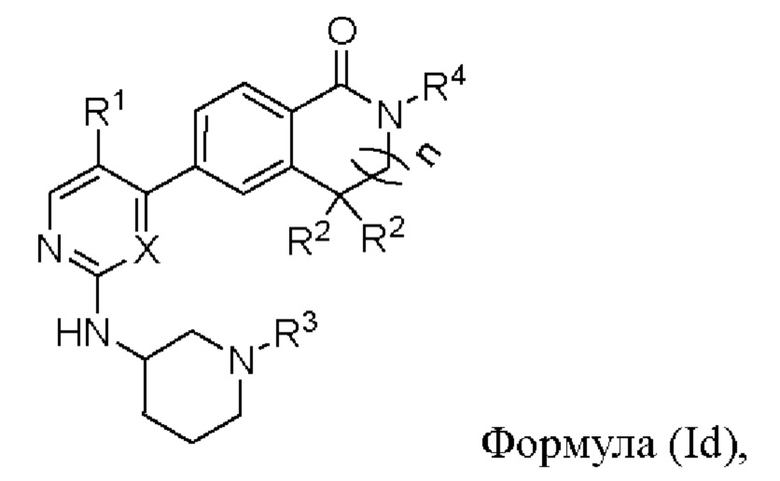
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В этом варианте реализации X предпочтительно представляет собой N; в более предпочтительном аспекте R3 представляет собой (С1-С6)алкилсульфонил.
В другом аспекте настоящее изобретение также относится к фармацевтической композиции, содержащей ингибитор киназы в соответствии с настоящим изобретением и фармацевтически приемлемый разбавитель или носитель.
В другом аспекте настоящее изобретение относится к применению ингибитора киназы в соответствии с настоящим изобретением для получения лекарственного средства для лечения гиперпролиферативных нарушений, инфекционных заболеваний, вызванных вирусом, и сердечно-сосудистых заболеваний.
В другом аспекте настоящее изобретение также относится к способу лечения гиперпролиферативных нарушений, инфекционных заболеваний, вызванных вирусом, и сердечно-сосудистых заболеваний путем применения ингибитора киназы в соответствии с настоящим изобретением.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Если не указано иное, все технические и научные термины, применяемые в настоящем описании, имеют то же значение, которое обычно имеют в виду специалисты средней квалификации в области техники, к которой относится настоящее изобретение. В настоящем описании формы единственного числа также включают множественное число, если в контексте явно не указано иное. Все публикации, заявки на патент, патенты и другие источники, упомянутые в настоящем документе, включены в настоящую заявку посредством ссылки. В случае противоречия настоящее описание, включая определения, будет иметь преимущественную силу. Кроме того, материалы, методы и примеры являются лишь иллюстративными и не предназначены для ограничения.
Если не указано иное, в настоящем изобретении используют общепринятые методы масс-спектроскопии, ЯМР, ВЭЖХ, химии белков, биохимии, технологий рекомбинантной ДНК и фармакологии, которые находятся в рамках компетенции в данной области техники. Если конкретные определения не приведены, номенклатура, используемая применительно к аналитической химии, синтетической органической химии и медицинской и фармацевтической химии, а также их лабораторные процедуры и методики, описанные в настоящем документе, являются такими, которые известны в данной области техники. Как правило, вышеупомянутые методики и процедуры могут быть выполнены обычными методами, хорошо известными в данной области техники, а также методами, описанными в различных общих и более специализированных источниках, которые цитируются и рассматриваются по всему тексту настоящего описания.
Термин «алкил» относится к алифатической углеводородной группе, которая может представлять собой разветвленный или линейный алкил. В зависимости от структуры алкильная группа может представлять собой монорадикал или дирадикал (то есть, алкиленовую группу). В настоящем изобретении алкильная группа предпочтительно представляет собой алкил, содержащий от 1 до 8 атомов углерода, более предпочтительно «низший алкил», содержащий от 1 до 6 атомов углерода, и еще более предпочтительно алкил, содержащий от 1 до 3 атомов углерода. Типичные алкильные группы включают, но не ограничены перечисленными: метил, этил, пропил, бутил, пентил, гексил и тому подобное. Следует понимать, что в объем термина «алкил», упоминаемого в настоящем документе, входят все конфигурации и конформации алкила, которые могут существовать, например предполагается, что в объем термина «пропил», упоминаемого в настоящем документе, входят н-пропил и изопропил, в объем термина «бутил», упоминаемого в настоящем документе, входят н-бутил, изобутил и третичный бутил, а в объем термина «пентил», упоминаемого в настоящем документе, входят н-пентил, изопентил, неопентил, трет-пентил, пент-3-ил и т.д.
Термин «алкокси» относится к -О-алкильной группе, где алкил соответствует определению, приведенному в настоящем документе. Типичные алкоксигруппы включают, но не ограничены перечисленными: метокси, этокси, пропокси, бутокси, пентилокси, гексилокси и тому подобное.
Термин «алкоксиалкил» относится к алкильной группе в соответствии с определением в настоящем документе, которая замещена алкокси в соответствии с определением в настоящем документе.
Термин «циклоалкил» относится к моноциклическому или полициклическому радикалу, который содержит только углерод и водород. Циклоалкильные группы включают группы, содержащие от 3 до 12 кольцевых атомов. В зависимости от структуры циклоалкильная группа может представлять собой монорадикал или дирадикал (например, циклоалкиленовую группу). В настоящем изобретении циклоалкильная группа предпочтительно представляет собой циклоалкил, содержащий от 3 до 8 атомов углерода, и более предпочтительно «низший циклоалкил», содержащий от 3 до 6 атомов углерода. Примеры циклоалкила включают, но не ограничены перечисленными: циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклопентенил, циклогексенил, циклогептенил и адамантил.
Термин «алкил(циклоалкил)» или «циклоалкилалкил» относится к алкильной группе в соответствии с определением в настоящем документе, которая замещена циклоалкилом в соответствии с определением в настоящем документе. Неограничивающие примеры циклоалкилалкила включают циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил и т.д.
Термин «ароматический» относится к плоскому кольцу, имеющему систему делокализованных пи-электронов, содержащую 4п+2 пи-электронов, где п представляет собой целое число. Ароматические кольца могут состоять из пяти, шести, семи, восьми, девяти или более чем девяти атомов. Ароматические соединения могут быть необязательно замещены. Термин «ароматический» включает как карбоциклические арильные (например, фенил), так и гетероциклические арильные (или «гетероарильные», или «гетероароматические») группы (например, пиридин). Указанный термин включает моноциклические группы или полициклические группы с конденсированными кольцами (то есть кольцами, которые имеют общие пары смежных атомов углерода).
Используемый в настоящем документе термин «арил» относится к ароматическому кольцу, где каждый из атомов, образующих кольцо, представляет собой атом углерода. Арильные кольца могут быть образованы пятью, шестью, семью, восемью, девятью или более чем девятью атомами углерода. Арильные группы могут быть необязательно замещены. Примеры арильных групп включают, но не ограничены перечисленными: фенил, нафталенил, фенантреонил, антраценил, флуоренил и инденил. В зависимости от структуры арильная группа может представлять собой монорадикал или дирадикал (то есть, ариленовую группу).
Термин «арилокси» относится к -О-арилу, где арил соответствует определению, приведенному в настоящем документе.
Термин «гетероарил» относится к арильной группе, которая содержит один или более кольцевых гетероатомов, выбранных из азота, кислорода и серы. N-содержащий «гетероарильный» фрагмент относится к ароматической группе, в которой по меньшей мере один из скелетных атомов кольца представляет собой атом азота. В зависимости от структуры гетероарильная группа может представлять собой монорадикал или дирадикал (то есть, гетероариленовую группу). Примеры гетероарильных групп включают, но не ограничены перечисленными: пиридинил, имидазолил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофурил, индазолил, индолизинил, фталазинил, пиридазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, нафтиридинил, фуропиридинил и тому подобные.
В настоящем документе термин «гетероалкил» относится к алкилу в соответствии с определением в настоящем документе, в котором один или более атомов основной цепи представляют собой гетероатомы, такие как кислород, азот, сера, кремний, фосфор или их комбинация. Гетероатомы (один или более) могут быть расположены в любом положении в гетероалкиле или в положении, в котором гетероалкил соединен с остальной частью молекулы.
В настоящем документе термин «гетероциклоалкил» или «гетероциклил» относится к неароматическому кольцу, где один или более атомов, образующих кольцо, представляют собой гетероатом, выбранный из группы, состоящей из азота, кислорода и серы. Гетероциклоалкильные кольца могут представлять собой моноциклические или бициклические кольца, образованные тремя, четырьмя, пятью, шестью, семью, восемью, девятью или более чем девятью атомами. Гетероциклоалкильные кольца могут быть необязательно замещены. Примеры гетероциклоалкилов включают, но не ограничены перечисленными: лактамы, лактоны, циклические имиды, циклические тиоимиды, циклические карбаматы, тетрагидротиопиран, 4Н-пиран, тетрагидропиран, пиперидин, 1,3-диоксин, 1.3- диоксан, 1,4-диоксин, 1,4-диоксан, пиперазин,1,3-оксатиан, 1,4-оксатиин, 1.4- оксатиан, тетрагидро-1,4-тиазин, 2Н-1,2-оксазин, малеимид, сукцинимид, барбитуровую кислоту, тиобарбитуровую кислоту, диоксопиперазин, гидантоин, дигидроурацил, морфолин, триоксан, гексагидро-1,3,5-триазин, тетрагидротиофен, тетрагидрофуран, пирролин, пирролидин, имидазолидин, пирролидон, пиразолин, пиразолидин, имидазолин, имидазолидин, 1,3-диоксол, 1,3-диоксолан, 1,3-дитиол, 1,3-дитиолан, изоксазолин, изоксазолидин, оксазолин, оксазолидин, оксазолидинон, тиазолин, тиазолидин, 1,3-оксатиолан. В зависимости от структуры гетероциклоалкильная группа может представлять собой монорадикал или дирадикал (то есть гетероциклоалкиленовую группу).
Термин «алкил(гетероциклоалкил)» или «гетероциклоалкилалкил» относится к алкильной группе в соответствии с определением в настоящем документе, которая замещена гетероциклоалкилом в соответствии с определением в настоящем документе.
Термин «гало-» («halo») или «галоген» («halogen») относится к фтору, хлору, брому и йоду.
Термины «галогеналкил», «галогеналкокси» и «галогенгетероалкил» включают алкильные, алкокси или гетероалкильные структуры, в которых по меньшей мере один водород заменен на атом галогена. В некоторых вариантах реализации, в которых два или более атомов водорода заменены на атомы галогена, атомы галогена одинаковы или отличаются друг от друга.
Термин «гидрокси» относится к группе -ОН.
Термин «циано» относится к группе -CN.
Термин «карбоксил» относится к группе -СООН.
Термин «сложный эфир» относится к химическому фрагменту формулы -COOR, где R выбран из группы, состоящей из алкила, циклоалкила, арила, гетероарила (связанного через кольцевой атом углерода) и гетероциклила (связанного через кольцевой атом углерода).
Термин «амино» относится к группе -NH2.
Термин «аминоацил» относится к группе -CO-NH2.
Термин «алкиламиноацил» относится к группе -CO-NH-R, где R представляет собой алкил в соответствии с определением в настоящей заявке.
Термин «амид» или «амидо» относится к -NR-CO-R', где R и R' независимо представляют собой водород или алкил.
Термин «алкиламино» относится к аминозаместителю, который дополнительно замещен одной или двумя алкильными группами, конкретно относится к группе -NRR', где каждый из R и R' независимо выбран из группы, состоящей из водорода или низшего алкила, при условии, что -NRR' не является -NH2. «Алкиламино» включает группы соединений, в которых атом азота -NH2 присоединен по меньшей мере к одной алкильной группе. Примеры алкиламиногрупп включают, но не ограничены перечисленными: метиламино, этиламино и тому подобное. «Диалкиламино» включает группы, в которых атом азота -NH2 присоединен по меньшей мере к двум другим алкильным группам. Примеры диалкиламино групп включают, но не ограничены перечисленными: диметиламино, диэтиламино и тому подобное.
Термин «циклоалкиламино» относится к аминозаместителю, дополнительно замещенному одной или двумя циклоалкильными группами в соответствии с определением в настоящем документе.
Термин «гетероциклоалкиламино» относится к аминорадикалу в соответствии с определением в настоящем документе, замещенному гетероциклоалкильной группой в соответствии с определением в настоящем документе.
Термин «алкиламино алкил» относится к алкильному радикалу в соответствии с определением в настоящем документе, замещенному алкиламиногруппой в соответствии с определением в настоящем документе.
Термин «аминоалкил» относится к алкильному заместителю, дополнительно замещенному одной или более аминогруппами.
Термин «аминоалкокси» относится к алкоксизаместителю, дополнительно замещенному одной или более аминогруппами.
Термин «гидроксиалкил» или «гидроксилалкил» относится к алкильному заместителю, дополнительно замещенному одной или более гидроксигруппами.
Термин «цианоалкил» относится к алкильному заместителю, дополнительно замещенному одной или более цианогруппами.
Термин «карбоксилалкил» относится к алкильным заместителям, дополнительно замещенным одной или более карбоксильными группами.
Термин «ацил» относится к одноатомному радикалу, оставшемуся после удаления гидроксильной группы из органической или неорганической оксикислоты, представленному общей формулой R-M(O)-, где М обычно представляет собой С.
Термин «карбонил» представляет собой органическую функциональную группу (С=0), образованную атомом углерода и атомом кислорода посредством двойной связи.
Термин «алканоил» или «алкилкарбонил» относится к карбонильной группе, дополнительно замещенной алкильной группой. Типичные алканоильные группы включают, но не ограничены перечисленными: ацетил, пропионил, бутирил, валерил, гексаноил и тому подобное.
Термин «сульфурил» или «сульфонил» относится к функциональной группе, оставшейся после утраты гидроксильной группы сульфоновой кислотой, и, в частности, относится к группе -S(=O)2-.
Термин «аминосульфурил» или «аминосульфонил» относится к группе -S(=O)2-NH2.
Термин «алкилсульфурил» или «алкилсульфонил» относится к -S(=O)2-R, где R представляет собой алкильную группу.
Термин «алкилсульфуриламидо» или «алкилсульфонамидо» и «циклоалкилсульфуриламидо» или «циклоалкилсульфонамидо» относятся к аминорадикалу в соответствии с определением в настоящем документе, замещенному алкилсульфурильной группой или циклоалкилсульфурильной группой в соответствии с определением в настоящем документе, то есть -NH-S(=O)2-R, где R представляет собой алкил или циклоалкил, соответственно.
Термины «циклоалкилсульфурил» и «циклоалкилсульфонил» относятся к -S(=O)2-R, где R представляет собой циклоалкильную группу.
Термин «необязательно» означает, что одно или более описанных далее событий могут иметь место или не иметь места, и включает как событие(я), которое(-ые) может(-гут) иметь место, так и событие(я), которое(-ые) может(-гут) не произойти. Термин «необязательно замещенный» или «замещенный» относится к тому, что упомянутая группа может быть замещена одной или более дополнительными группами, каждая из которых независимо выбрана из алкила, циклоалкила, арила, гетероарила, гетероциклила, гидрокси, алкокси, циано, галогена, амида, нитро, галогеналкила, амино, метилсульфонила, алкилкарбонила, алкоксикарбонила, гетероарилалкила, гетероциклоалкилалкилалкила, аминоацила, защитной группы для аминогруппы и т.д., где защитная группа для аминогруппы предпочтительно выбрана из группы, состоящей из пивалоила, трет-бутоксикарбонила, бензилоксикарбонила, 9-флуоренилметоксикарбонила, бензила, п-метоксибензила, аллилоксикарбонила, трифторацетила и тому подобного.
В настоящем описании термин «фармацевтически приемлемые соли» относится к солям, которые сохраняют желаемую биологическую активность рассматриваемого соединения и проявляют минимальные нежелательные токсикологические эффекты. Эти фармацевтически приемлемые соли могут быть получены in situ во время заключительно этапа выделения и очистки указанного соединения или путем раздельного осуществления реакции очищенного соединения в форме свободной кислоты или свободного основания с подходящим основанием или кислотой, соответственно.
«Сольват» означает формы присоединения растворителя, которые содержат либо стехиометрические, либо нестехиометрические количества растворителя. Некоторые соединения имеют тенденцию захватывать фиксированное молярное отношение молекул растворителя в кристаллическом твердом состоянии, образуя таким образом сольват.Если растворитель представляет собой воду, то образующийся сольват представляет собой гидрат; а если растворитель представляет собой спирт, то образующийся сольват представляет собой алкоголят.Гидраты образуются в результате объединения одной или более молекул воды с одной молекулой вещества, в котором вода сохраняет свое молекулярное состояние как H2O.
«Метаболит» соединения, описанного в настоящем документе, представляет собой производное указанного соединения, которое образуется при метаболизме указанного соединения. Термин «активный метаболит» относится к биологически активному производному соединения, которое образуется при метаболизме указанного соединения. В настоящем документе термин «метаболизированный» относится к совокупности процессов (включая, но не ограничиваясь перечисленными: реакции гидролиза и реакции, катализируемые ферментами, такие как реакции окисления), посредством которых конкретное вещество изменяется организмом. Таким образом, ферменты могут вызывать специфические структурные изменения соединения. Например, цитохром Р450 катализирует различные окислительные и восстановительные реакции, в то время как уридиндифосфатглюкуронилтрансферазы катализируют перенос активированной молекулы глюкуроновой кислоты на ароматический спирт, алифатический спирт, карбоновую кислоту, амин и свободную сульфгидрильную группу. Дополнительную информацию о метаболизме можно получить из The Pharmacological Basis of Therapeutics, 9th Edition, McGraw-Hill (1996). Метаболиты соединений, описанных в настоящем документе, могут быть идентифицированы либо путем введения соединений хозяину и анализа образцов ткани хозяина, либо путем инкубации соединений с клетками печени in vitro и анализа полученных соединений. Оба способа хорошо известны в данной области техники. В некоторых вариантах реализации метаболиты соединения образуются в результате окислительных процессов и соответствуют соответствующему гидроксисодержащему соединению. В некоторых вариантах реализации соединение метаболизируется до фармакологически активных метаболитов.
В настоящем документе термин «модулировать» означает взаимодействовать с мишенью либо напрямую, либо опосредованно с целью изменения активности мишени, в том числе, лишь в качестве примера, для усиления активности мишени, ингибирования активности мишени, ограничения активности мишени или продления активности мишени.
Термин «пролекарство» или «предшественник лекарственного средства» относится к производным, которые могут не обладать фармакологической активностью, но могут, в некоторых случаях, вводиться перорально или парентерально, а затем метаболизироваться в организме с образованием соединений в соответствии с настоящим изобретением, которые являются фармакологически активными. Неограничивающие примеры пролекарств включают сложные эфиры, сложные эфиры карбоновой кислоты, полуэфиры, фосфатные сложные эфиры, нитроэфиры, сульфатные сложные эфиры, сульфоксиды, амиды, карбаматы, азосоединения, фосфамиды, гликозиды, простые эфиры, ацетали и кетали и т.д.
«Эффективное количество» означает количество лекарственного средства или фармацевтического агента, которое будет вызывать биологический или медицинский ответ ткани, системы, животного или человека, которого добивается, например, исследователь или врач. Кроме того, термин «терапевтически эффективное количество» означает любое количество, которое, по сравнению с соответствующим субъектом, который не получал такое количество, приводит к более эффективному лечению, исцелению, предотвращению или облегчению заболевания, нарушения или побочного эффекта или снижению скорости прогрессирования заболевания или нарушения. В объем этого термина также входят количества, эффективные для улучшения нормальной физиологической функции.
Термин «лечение» в настоящем документе относится к облегчению по меньшей мере одного симптома заболевания, нарушения или состояния. Указанный термин включает введение и/или применение одного или более соединений, описанных в настоящем документе, субъекту с целью контролирования течения или предоставления лекарственного средства для лечения состояния. «Лечение» для целей настоящего изобретения может, но не обязательно должно приводить к излечению; скорее, «лечение» может иметь форму контроля течения состояния. Когда соединения, описанные в настоящем документе, применяют для лечения нежелательных пролиферирующих клеток, включая раки, «лечение» включает частичное или полное уничтожение нежелательных пролиферирующих клеток с минимальным разрушительным воздействием на нормальные клетки. Желательным механизмом лечения нежелательных быстро пролиферирующих клеток, включая раковые клетки, на клеточном уровне является апоптоз.
В объем термина «предотвращение» в настоящем документе входит либо предотвращение или замедление начала очевидного с клинической точки зрения прогрессирования заболевания в целом, либо предотвращение или замедление начала доклинически очевидной стадии заболевания у лиц, имеющих риск. Это включает профилактическое лечение субъектов, подверженных риску развития заболевания.
Термин «субъект» или «пациент» включает организмы, которые могут страдать клеточным пролиферативнымнарушением или нарушением, связанным с пониженной или недостаточной запрограммированной гибелью клеток (апоптозом), или которые могли бы иным образом получить пользу от введения соединения в соответствии с настоящим изобретением, такие как человек и животные, отличные от человека. Предпочтительные люди включают пациентов-людей, страдающих от или со склонностью к заболеваням или связанным ними состояниям, описанным в настоящей заявке. Термин «животное, отличное от человека» включает позвоночных, например, млекопитающих, таких как приматы, отличные от человека, овцы, крупный рогатый скот, собаки, кошки и грызуны, например, мыши, и не млекопитающих, таких как куры, амфибии, рептилии и т.д.
В настоящем документе термин GI50 относится к концентрации лекарственного средства, необходимой для ингибирования роста 50% клеток, то есть к концентрации лекарственного средства, при которой рост 50% клеток (таких как раковые клетки) ингибируется или контролируется.
В настоящем документе термин IC50 относится к количеству, концентрации или дозе конкретного исследуемого соединения, при которой достигается 50% ингибирование максимального ответа в анализе, посредством которого измеряют такой ответ.
В настоящем документе термин ЕС50 относится к дозе, концентрации или количеству исследуемого соединения, которое вызывает дозозависимый ответ на уровне 50% от максимального проявления конкретного ответа, который индуцируется, вызывается или усиливается конкретным исследуемым соединением.
Термин «заболевания, связанные с CDK9 и/или ее мутациями» или «заболевания, опосредованные CDK9 и/или ее мутациями», включает заболевания, ассоциированные с активностью CDK9 и/или ее мутациями или вызванные активностью CDK9 и/или ее мутациями (например, гиперактивностью CDK9 и/или ее мутациями), а также состояния, сопутствующие этим заболеваниям. Примеры «заболеваний, связанных с CDK9 и/или ее мутациями», или «заболеваний, опосредуемых CDK9 и/или ее мутациями», включают заболевания, возникающие в результате повышенной активности CDK9 и/или ее мутаций вследствие мутаций в генах, регулирующих активность CDK9 и/или ее мутации (таких как LARP7, HEXIM1/2 или 7SK мяРНК), заболевания, возникающие в результате повышенной активности CDK9 и/или ее мутаций вследствие активации комплекса CDK9/циклин Т/РНК-полимераза II вирусными белками (такими как HIVTAT или HTLV-TAX), или заболевания, возникающие в результате повышенной активности CDK9 и/или ее мутаций вследствие активации митогенных сигнальных путей.
Термин «гиперактивность CDK9» относится к повышенной ферментативной активности CDK9 и/или ее мутациям по сравнению с нормальными не вызывающими заболевание клетками или к повышенной активности CDK9, приводящей к нежелательной пролиферации клеток или к сниженной или недостаточной запрограммированной гибели клеток (апоптозу), или к мутациям, приводящим к конститутивной активации CDK9.
Термин «гиперпролиферативное нарушение» включает нарушения, вызванные нежелательной или неконтролируемой пролиферацией клеток, и включает нарушения, вызванные сниженной или недостаточной запрограммированной гибелью клеток (апоптозом).
Ингибитор киназы в соответствии с настоящим изобретением.
Настоящее изобретение относится к ингибитору киназы, содержащему соединение формулы (I) или его фармацевтически приемлемую соль, сольват, сложный эфир, кислоту, метаболит или пролекарство,
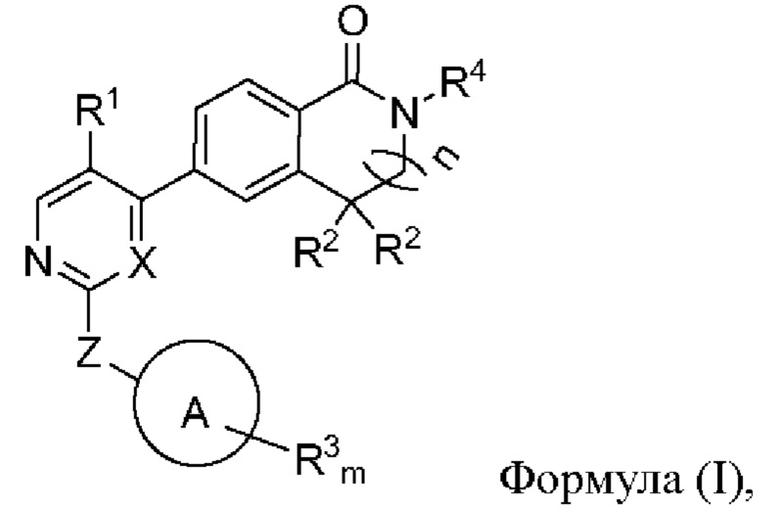
где А выбран из группы, состоящей из циклогексила, фенила, пиридинила и пиперидила;
n представляет собой 0 или 1;
X представляет собой СН или N;
Z представляет собой -NH- или -NH-C(=O)-;
R1 выбран из группы, состоящей из водорода, галогена, циано, (С1-С6)алкила и (С1-С6)галогеналкила;
R2 выбраны из группы, состоящей из водорода и (С1-С6)алкила, или два R2 вместе образуют (С3-С6)циклоалкил;
m выбран из целого числа 1-3, и каждый R3 независимо выбран из группы, состоящей из водорода, -NH-(С1-С3)алкил-(С1-С3)алкокси, галогена, (С1-С6)алкила, (С1-С6)алкокси, (С1-С6)галогеналкила, (С1-С6)алкилациламино, (С1-С6)алкилсульфонила, (С1-С6)алкилсульфонамидо, аминосульфонила, (С1-С6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, карбоксил(С1-С3)алкилом, аминосульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С3-С6)циклоалкилом, гетероциклиламиноацила в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, гетероциклилом, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, -S(=O)(=NH)(С1-С3)алкилом и -(С1-С3)алкил-S(=O))(=NH)(С1-С3)алкилом;
R4 выбран из группы, состоящей из водорода и (С1-С6)алкила.
В предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ia) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
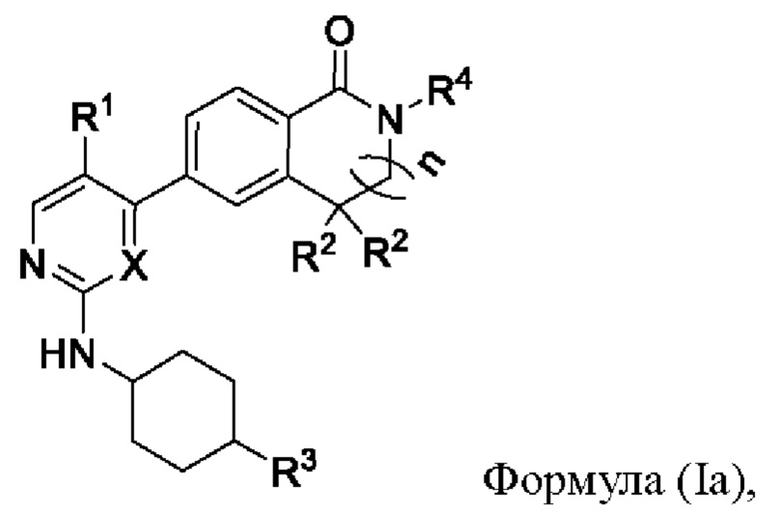
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В этом варианте реализации X предпочтительно представляет собой N; в другом варианте реализации R3 предпочтительно представляет собой -NH-(С1-С3)алкил-(С1-С3)алкокси или карбоксил(С1-С3)алкил.
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ib) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
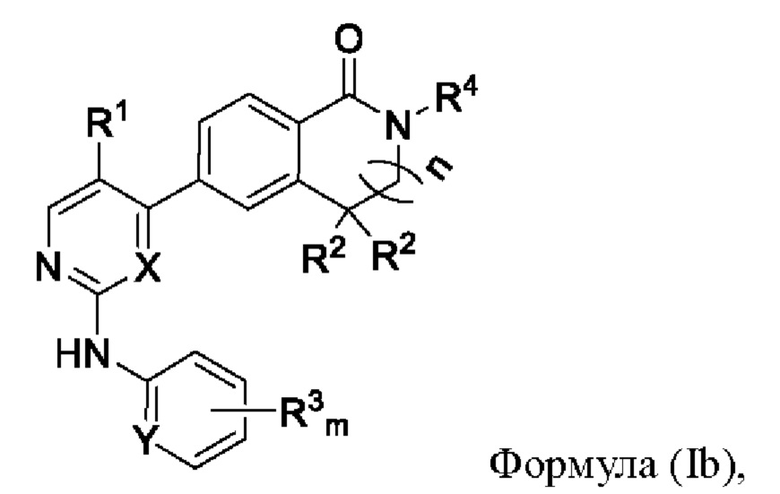
где Y представляет собой СН или N; X, m, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В более предпочтительном аспекте X представляет собой N; в другом предпочтительном аспекте Y представляет собой СН.
В другом предпочтительном аспекте каждый R3 независимо выбран из группы, состоящей из галогена, (С1-С6)алкила, (С1-С6)алкокси, (С1-С6)галогеналкила, (С1-С6)алкилсульфонила, (С1-С6)алкилсульфонамидо, аминосульфонила, (С1-С6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, аминосульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С1-С3)алкилом, (С1-С3)алкилсульфонил(С3-С6)циклоалкилом, гетероциклиламиноацила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, гетероциклила, в котором гетероатом(ы) необязательно замещен(ы) (С1-С6)алкилом, -S(=OX=NH)(C1-C3)алкилом и -(С1-С3)алкил-S(=O)(=NH)(С1-С3)алкилом.
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Ic) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В более предпочтительном аспекте R3 представляет собой (С1-С6)алкилациламино.
В другом предпочтительном варианте реализации настоящее изобретение относится к соединению формулы (Id) или его фармацевтически приемлемой соли, сольвату, сложному эфиру, кислоте, метаболиту или пролекарству,
где X, n, R1, R2, R3 и R4 имеют значения, определенные выше.
В этом варианте реализации X предпочтительно представляет собой N; в более предпочтительном аспекте R3 представляет собой (С1-С6)алкилсульфонил.
В иллюстративном варианте реализации настоящего изобретения R1 предпочтительно выбран из группы, состоящей из водорода, хлора, фтора, циано, (С1-С3)алкила (более предпочтительно метила) и (С1-С3)галогеналкила (более предпочтительно трифторметила).
В другом иллюстративном варианте реализации R2 предпочтительно выбран из группы, состоящей из водорода, (С1-С3)алкила (более предпочтительно метила), или два R2 вместе образуют циклопропил или циклобутил.
В других иллюстративных вариантах реализации каждый R3 независимо выбран из группы, состоящей из водорода, (2-метокси)этиламино, хлора, фтора, метила, метокси, трифторметила, ацетиламино, метансульфонила, метансульфониламино, сульфамоила, метилсульфамоила, диметилсульфамоила, морфолиносульфонила, карбоксиметила, сульфамоилметила,
метансульфонилметила, метансульфонилциклопропила (N-метилпиперидин-4-ил)аминоацила, N-метилпиперазин-1-ила,
N-этилпиперазин-1-ила, N-изопропилпиперазин- 1-ила, гомопиперазин- 1-ила, -S(=O)(=NH)метила и -метил-S(=O)(=ХН)метила.
В другом иллюстративном варианте реализации R4 предпочтительно выбран из группы, состоящей из водорода и (С1-С3)алкила (более предпочтительно метила).
В настоящем описании описан новый ингибитор киназы. Также описаны фармацевтически приемлемые соли, сольваты, сложные эфиры, кислоты, метаболиты и пролекарства указанных соединений.
Соединения в соответствии с настоящим изобретением могут существовать в свободной форме, например, в виде свободного основания, или в виде свободной кислоты, или в виде цвиттериона, или могут существовать в форме соли. Указанная соль может представлять собой любую соль, либо органическую, либо неорганическую соль присоединения, в частности, любую физиологически приемлемую органическую или неорганическую соль присоединения, обычно используемую в фармацевтике.
Соли, которые являются предпочтительными для целей настоящего изобретения, представляют собой физиологически приемлемые соли соединений в соответствии с настоящим изобретением. Тем не менее, в объем настоящего изобретения также входят соли, которые сами по себе не пригодны для фармацевтических применений, но которые, например, могут применяться для выделения или очистки соединений в соответствии с настоящим изобретением.
Термин «фармацевтически приемлемая соль» относится к относительно нетоксичной, неорганической или органической соли присоединения кислоты соединения в соответствии с настоящим изобретением, например, см. S. М. Berge, et al. «Pharmaceutical Salts», J. Pharm. Sci. 1977, 66, 1-19.
Фармацевтически приемлемые соли соединений в соответствии с настоящим изобретением включают соли присоединения кислоты, образованные с минеральными кислотами: карбоновыми кислотами и сульфоновыми кислотами, например, соли присоединения соляной кислоты, бромистоводородной кислоты, йодистоводородной кислоты, серной кислоты, дисерной кислоты, фосфорной кислоты, азотной кислоты; или образованные с органической кислотой, такой как муравьиная, уксусная, ацетоуксусная, пировиноградная, трифторуксусная, пропионовая, масляная, гексановая, гептановая, ундекановая, лауриновая, бензойная, салициловая, 2-(4-гидроксибензоил)-бензойная, камфорная, коричная, циклопентанпропионовая, диглюконовая, 3-гидрокси-2-нафтойная, никотиновая, памоевая, пектиновая, надсерная, 3-фенилпропионовая, пикриновая, пивалиновая, 2-гидроксиэтансульфоновая, итаконовая, сульфаминовая,
трифторметансульфоновая, додецилсерная, этансульфоновая, бензолсульфоновая, паратолуолсульфоновая, метансульфоновая, 2-нафталинсульфоновая,
нафталиндисульфоновая, камфорсульфоновая кислота, лимонная, винная, стеариновая, молочная, щавелевая, малоновая, янтарная, яблочная, адипиновая, альгиновая, малеиновая, фумаровая, D-глюконовая, миндальная, аскорбиновая, глюкогептановая, глицерофосфорная, аспарагиновая, сульфосалициловая, гемисерная или тиоциановая кислота, в качестве примера.
Фармацевтически приемлемые соли соединений в соответствии с настоящим изобретением также включают соли обычных оснований, такие как, в качестве примера и в качестве предпочтительного варианта, соли щелочных металлов (например, соли натрия и калия), соли щелочноземельных металлов (например, соли кальция и магния) и соли аммония, полученные из аммиака или органических аминов с 1 - 16 атомами С, таких как, в качестве примера и в качестве предпочтительного варианта, этиламин, диэтиламин, триэтиламин, этилдиизопропиламин, моноэтаноламин, диэтаноламин, триэтаноламин, дициклогексиламин, диметиламиноэтанол, прокаин, дибензиламин, N-метилморфолин, аргинин, лизин, этилендиамин, N-метилпиперидин, -метилглюкамин, диметилглюкамин, этилглюкамин, 1,6-гексадиамин, глюкозамин, саркозин, серинол, трис(гидроксиметил)аминометан, аминопропандиол, основание Совакаи 1-амино-2,3,4-бутантриол.
В объем настоящего изобретения входят все возможные соли соединений в соответствии с настоящим изобретением в виде отдельных солей или в виде любой смеси указанных солей в любом соотношении.
Сольваты - это термин, используемый для целей настоящего изобретения по отношению к тем формам соединений в соответствии с настоящим изобретением, которые в твердом или жидком состоянии образуют комплекс путем координации с молекулами растворителя. Гидраты представляют собой особую форму сольватов, в которой координация происходит с молекулами воды. В рамках настоящего изобретения гидраты являются предпочтительными сольватами.
Кроме того, в объем настоящего изобретения также входят пролекарства соединений в соответствии с настоящим изобретением. В объем термина «пролекарства» входят соединения, которые сами по себе могут быть биологически активными или неактивными, но преобразуются (например, путем метаболизма или гидролиза) в соединения в соответствии с настоящим изобретением во время их нахождения в организме.
Кроме того, в объем настоящего изобретения входят все возможные кристаллические формы, или полиморфы, соединений в соответствии с настоящим изобретением либо в виде отдельных полиморфов, либо в виде смеси более чем одного полиморфа в любом соотношении.
В настоящем описании, для удобства в некоторых случаях, формула соединения представляет собой конкретный изомер, но в объем настоящего изобретения входят все изомеры, такие как геометрические изомеры, оптические изомеры на основе асимметричных атомов углерода, стереоизомеры, таутомеры и т.д.
Хиральные соединения, используемые в настоящем изобретении, могут быть любой конфигурации или представлять собой рацемическую смесь. Если соединение, пригодное в соответствии с настоящим изобретением, содержит более одного хирального центра, оно может существовать в диастереоизомерных формах. Диастереоизомерные соединения могут быть разделены способами, известными специалистам в данной области техники (например, с помощью хроматографии или кристаллизации), а отдельные энантиомеры могут быть разделены, как описано выше. В объем настоящего изобретения входит применение различных диастереоизомеров соединений, пригодных в соответствии с настоящим изобретением, и их смесей. Соединения, пригодные для применения в соответствии с настоящим изобретением, могут существовать в различных таутомерных формах или в виде различных геометрических изомеров, и в объем настоящего изобретения входит применение каждого таутомера и/или геометрического изомера соединений, пригодных для применения в соответствии с настоящим изобретением, и их смесей. Соединения, пригодные в соответствии с настоящим изобретением, могут существовать в цвиттер-ионной форме. В объем настоящего изобретения входит применение каждой цвиттер-ионной формы соединений, пригодных для применения в соответствии с изобретением, и их смесей.
Скрининг и определение характеристик фармацевтически приемлемых солей, полиморфов и/или сольватов могут быть осуществлены с применением различных методов, включая, но не ограничиваясь перечисленными: термический анализ, рентгеновскую дифракцию, спектроскопию, микроскопию и элементный анализ. Различные применяемые спектроскопические методы включают, но не ограничены перечисленными: рамановскую спектроскопию, инфракрасную спектроскопию с преобразованием Фурье (ИКФС), спектроскопию в ультрафиолетовой и видимой области спектра (UVIS) и ЯМР (в жидком и твердом состоянии). Различные методы микроскопии включают, но не ограничены перечисленными: ИК-микроскопию и рамановскую микроскопию.
Соответственно, в объем настоящего изобретения входят все возможные соли, полиморфы, метаболиты, гидраты, сольваты или пролекарства (например, сложные эфиры) соединений в соответствии с настоящим изобретением в виде отдельной соли, полиморфа, метаболита, гидрата, сольвата или пролекарства (например, сложного эфира) или в виде смеси более чем одной соли, полиморфа, метаболита, гидрата, сольвата или пролекарства (например, сложного эфира) в любом соотношении.
Способ лечения и применение
Другим объектом настоящего изобретения являются способ и применение ингибитора киназы в соответствии с настоящим изобретением для лечения и/или предотвращения заболеваний, предпочтительно заболеваний, связанных с активностью CDK9 и ее мутациями или опосредованных ими, особенно гиперпролиферативных заболеваний, инфекционных заболеваний, вызванных вирусом, и/или сердечно-сосудистых заболеваний, более предпочтительно гиперпролиферативных заболеваний.
Соединение в соответствии с настоящим изобретением можно применять для ингибирования активности или экспрессии CDK9 и ее мутантов. Следовательно, соединения формул (I), (Ia), (Ib), (Ic) или (Id) пригодны для применения в качестве терапевтических агентов. В одном из вариантов реализации настоящего изобретения предложен способ лечения заболеваний, связанных с активностью CDK9 и ее мутациями или опосредованных ими, у пациента, которого необходимо лечить, который включает введение пациенту эффективного количества соединений формул (I), (Ia), (Ib), (Ic) или (Id), описанных выше. В некоторых вариантах реализации заболевания, связанные с активностью CDK9 и ее мутантами, представляют собой гиперпролиферативное заболевание, вызванные вирусом инфекционные заболевания и/или сердечно-сосудистые заболевания, более предпочтительно гиперпролиферативное заболевание, особенно рак, и более предпочтительно лейкоз, рак печени, рак яичников, рак шейки матки, колоректальный рак, желудочно-кишечную стромальную опухоль или лимфому.
Гиперпролиферативные нарушения в контексте настоящего изобретения включают, но не ограничены перечисленными: например, псориаз, келоидные и другие гиперплазии, поражающие кожу, эндометриоз, скелетные нарушения, ангиогенные нарушения или пролиферативные нарушения кровеносных сосудов, легочную гипертензию, фиброзные нарушения, нарушения пролиферации мезангиальных клеток, полипы толстой кишки, поликистоз почек, доброкачественную гиперплазию предстательной железы и солидные опухоли, такие как рак молочной железы, дыхательных путей, головного мозга, репродуктивных органов, пищеварительного тракта, мочевыводящих путей, глаза, печени, кожи, головы и шеи, щитовидной железы, паращитовидной железы, и их отдаленные метастазы, лимфомы, саркомы и лейкозы.
Примеры рака молочной железы включают, но не ограничены перечисленными: инвазивную протоковую карциному, инвазивную дольковую карциному, протоковую карциному in situ и дольковую карциному in situ, карциному молочной железы собак или кошек.
Примеры рака дыхательных путей включают, но не ограничены перечисленными: мелкоклеточную и не мелко клеточную карциному легкого, а также аденому бронха, плевролегочную бластому и мезотелиому.
Примеры рака головного мозга включают, но не ограничены перечисленными: глиому ствола мозга и гипоталамуса, астроцитому мозжечка и головного мозга, глиобластому медуллобластому эпендимому а также нейроэктодермальную опухоль и опухоль шишковидной железы.
Опухоли репродуктивных органов включают, но не ограничены перечисленными: рак предстательной железы, рак яичка, рак эндометрия, рак шейки матки, рак яичников, рак влагалища, рак вульвы, а также саркому матки.
Опухоли пищеварительного тракта включают, но не ограничены перечисленными: рак анального канала, толстой кишки, колоректальный рак, рак пищевода, желчного пузыря, желудка, поджелудочной железы, прямой кишки, тонкой кишки, слюнных желез и аденокарциномы анальных желез.
Опухоли мочевыводящих путей включают, но не ограничены перечисленными: рак мочевого пузыря, полового члена, почки, почечной лоханки, мочеточника, уретры, а также наследственный и спорадический папиллярный рак почки.
Рак глаза включает, но не ограничен перечисленными: внутриглазную меланому и ретинобластому.
Примеры рака печени включают, но не ограничены перечисленными: гепатоцеллюлярную карциному (карциномы клеток печени в фиброламеллярном варианте или не фиброламеллярном варианте), холангиокарциному (карциному внутрипеченочных желчных протоков) и смешанную гепатоцеллюлярную холангиокарциному.
Рак кожи включает, но не ограничен перечисленными: плоскоклеточную карциному, саркому Капоши, злокачественную меланому рак кожи из клеток Меркеля, немеланомный рак кожи и мастоцитомы.
Рак головы и шеи включает, но не ограничен перечисленными: рак гортани, гипофарингеальный рак, рак носоглотки, рак ротоглотки, рак губы, рак полости рта, плоскоклеточный рак и меланому полости рта.
Лимфомы включают, но не ограничены перечисленными: лимфому связанную со СПИД, неходжкинскую лимфому, кожную Т-клеточную лимфому, лимфому Беркитта, болезнь Ходжкина и лимфому центральной нервной системы.
Саркомы включают, но не ограничены перечисленными: саркому мягких тканей, остеосаркому, злокачественную фиброзную гистиоцитому лимфосаркому, рабдомиосаркому злокачественный гистиоцитоз, фибросаркому гемангиосаркому, гемангиоперицитому и лейомиосаркому.
Лейкозы включают, но не ограничены перечисленными: острый миелоидный лейкоз, острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, хронический миелоидный лейкоз и волосатоклеточный лейкоз.
Предпочтительным объектом настоящего изобретения является лечение и/или предотвращение рака легких (особенно немелкоклеточной карциномы легких), рака предстательной железы (особенно гормононезависимого рака предстательной железы человека), рака шейки матки (включая рак шейки матки человека с множественной лекарственной устойчивостью), колоректального рака, меланомы, рака яичников или лейкоза (особенно острого миелоидного лейкоза).
Фиброзные пролиферативные нарушения (т.е. аномальное образование внеклеточного матрикса), которые можно лечить соединениями и способами в соответствии с настоящим изобретением, включают фиброз легких, атеросклероз, рестеноз, цирроз печени и нарушения пролиферации мезангиальных клеток, включая заболевания почек, такие как гломерулонефрит, диабетическую нефропатию, злокачественный нефросклероз, синдромы тромботической микроангиопатии, отторжение трансплантата и гломерулопатии.
Другие состояния у людей или других млекопитающих, которые можно лечить путем введения соединения в соответствии с настоящим изобретением, включают рост опухоли, ретинопатию (включая диабетическую ретинопатию, ишемическую окклюзию вены сетчатки, ретинопатию недоношенных и возрастную макулярную дегенерацию), ревматоидный артрит, псориаз и буллезные нарушения, связанные с формированием субэпидермальных пузырей (включая буллезный пемфигоид, многоформную эритему и герпетиформный дерматит).
Соединения в соответствии с настоящим изобретением также можно применять для предотвращения и лечения заболеваний дыхательных путей и легкого, заболеваний желудочно-кишечного тракта, а также заболеваний мочевого пузыря и желчного протока.
Нарушения, упомянутые выше, были хорошо охарактеризованы у людей, но также существуют с аналогичной этиологией у других животных, включая млекопитающих, и их можно лечить путем введения фармацевтических композиций в соответствии с настоящим изобретением.
В дополнительном аспекте настоящего изобретения соединения в соответствии с настоящим изобретением применяют в способе предотвращения и/или лечения инфекционных заболеваний, в частности, вызванных вирусами инфекционных заболеваний. Указанные заболевания включают, но не ограничены перечисленными: вызванные вирусами инфекционные заболевания, включая оппортунистические заболевания, которые вызваны ретровирусами, гепаднавирусами, герпесвирусами, флавививирусами и/или аденовирусами. В дополнительном предпочтительном варианте реализации данного способа ретровирусы выбраны из лентивирусов или онкоретровирусов, где лентивирус выбран из группы, включающей: ВИЧ-1, ВИЧ-2, FIV, BIV, SIV, SHIV, CAEV, VMV или EIAV, предпочтительно ВИЧ-1 или ВИЧ-2; и где онкоретровирус выбран из группы: HTLV-I, HTLV-II или BLV. В дополнительном предпочтительном варианте реализации данного способа гепаднавирус выбран из HBV, GSHV или WHV, предпочтительно HBV; герпесвирус выбран из группы, включающей: HSV I, HSV II, ВЭБ, VZV, HCMV или HHV 8, предпочтительно HCMV; и флавививирусы выбраны из HCV, вируса Западного Нила или желтой лихорадки.
Соединения в соответствии с настоящим изобретением также пригодны для предотвращения и/или лечения сердечно-сосудистых заболеваний, таких как гипертрофия сердца, врожденный порок сердца у взрослых, аневризма, стабильная стенокардия, нестабильная стенокардия, стенокардия, ангионевротический отек, стеноз аортального клапана, аневризма аорты, аритмия, аритмогенная дисплазия правого желудочка, артериосклероз, артериовенозные мальформации, фибрилляция предсердий, синдром Бехчета, брадикардия, тампонада сердца, кардиомегалия, застойная кардиомиопатия, гипертрофическая кардиомиопатия, рестриктивная кардиомиопатия, предотвращен^ сердечно-сосудистых заболеваний, стеноз сонной артерии, кровоизлияние в мозг, синдром Чарга-Стросса, диабет, аномалия Эбштейна, комплекс Эйзенменгера, холестериновая эмболия, бактериальный эндокардит, фиброзно-мышечная дисплазия, врожденные пороки сердца, болезни сердца, застойная сердечная недостаточность, заболевания клапанов сердца, сердечный приступ, эпидуральная гематома, субдуральная гематома, болезнь Гиппеля-Линдау гиперемия, гипертензия, легочная гипертензия, гипертрофический рост, гипертрофия левого желудочка, гипертрофия правого желудочка, синдром гипоплазии левых отделов сердца, гипотензия, перемежающаяся хромота, ишемическая болезнь сердца, синдром Клиппеля-Треноне-Вебера, латеральный медуллярный синдром, синдром удлиненного интервала QT, пролапс митрального клапана, болезнь Мойя-мойя, слизисто-кожный лимфонодулярный синдром, инфаркт миокарда, ишемия миокарда, миокардит, перикардит, заболевания периферических сосудов, флебит, узелковый полиартериит, атрезия легкого, болезнь Рейно, рестеноз, синдром Снеддона, стеноз, синдром верхней полой вены, синдром X, тахикардия, артериит Такаясу наследственная геморрагическая телеангиэктазия, телеангиэктазия, височный артериит, тетрада Фалло, облитерирующий тромбоангиит, тромбоз, тромбоэмболия, атрезия трехстворчатого клапана, варикозное расширение вен, сосудистые заболевания, васкулит, спазм сосудов, фибрилляция желудочков, синдром Вильямса, заболевание периферических сосудов, варикозное расширение вен с язвами ног, тромбоз глубоких вен, синдром Вольфа-Паркинсона-Уайта.
Соединения в соответствии с настоящим изобретением предпочтительно применяют для предотвращения и/или лечения гипертрофии сердца, врожденного порока сердца у взрослых, аневризм, стенокардии (angina), стенокардии (angina pectoris), аритмий, предотвращения сердечно-сосудистых заболеваний, предотвращения и/или лечения кардиомиопатий, застойной сердечной недостаточности, инфаркта миокарда, легочной гипертензии, гипертрофического роста, рестеноза, стеноза, тромбоза и артериосклероза.
Другим объектом настоящего изобретения является применение ингибиторов киназ формул (I), (Ia), (Ib), (Ic) или (Id) в соответствии с настоящим изобретением для получения лекарственных средств.
Другим объектом настоящего изобретения является применение ингибиторов киназ формул (I), (Ia), (Ib), (Ic) или (Id) в соответствии с настоящим изобретением для получения лекарственного средства для лечения и/или предотвращения заболеваний, особенно упомянутых выше заболеваний.
Фармацевтическая композиция
Другой аспект настоящего изобретения относится к фармацевтической композиции, которая содержит ингибитор киназы в соответствии с настоящим изобретением и фармацевтически приемлемый разбавитель или носитель, а также необязательно один или более других активных ингредиентов.
Другой аспект настоящего изобретения относится к фармацевтической композиции, которая содержит комбинацию ингибитора киназы формул (I), (Ia), (Ib), (Ic) или (Id) в соответствии с настоящим изобретением с инертным нетоксичным фармацевтически приемлемым адъювантом.
Другой аспект изобретения относится к применению фармацевтической композиции в соответствии с настоящим изобретением для лечения и/или предотвращения заболеваний, в частности, упомянутых выше заболеваний.
Другой аспект изобретения относится к применению фармацевтической композиции в соответствии с настоящим изобретением для лечения и/или предотвращения карцином легких (особенно немелкоклеточных карцином легких), карцином предстательной железы (особенно гормононезависимых карцином предстательной железы человека), карцином шейки матки (включая карциномы шейки матки человека с множественной лекарственной устойчивостью), колоректальных карцином, меланом, карцином яичников или лейкозов (особенно острых миелоидных лейкозов).
Соединения в соответствии с настоящим изобретением можно вводить в качестве единственного фармацевтического агента или в комбинации с одним или более дополнительными терапевтическими агентами, если комбинация не вызывает неприемлемых побочных эффектов. Эта фармацевтическая комбинация включает введение одной фармацевтической лекарственной формы, которая содержит соединение в соответствии с настоящим изобретением и один или более дополнительных терапевтических агентов, а также введение соединения в соответствии с настоящим изобретением и каждого дополнительного терапевтического агента в его собственной отдельной фармацевтической лекарственной форме. Например, соединение формул (I), (Ia), (Ib), (Ic) или (Id) и терапевтический агент можно вводить пациенту совместно в виде единой лекарственной композиции для перорального применения, такой как таблетка или капсула, или каждый агент можно вводить в виде отдельных лекарственных форм.
В тех случаях, когда применяют отдельные лекарственные формы, соединение в соответствии с настоящим изобретением и один или более дополнительных терапевтических агентов можно вводить по существу в одно и то же время (например, одновременно) или с разнесением по времени (например, последовательно).
В частности, соединения в соответствии с настоящим изобретением можно применять в фиксированной или отдельной комбинации с другими противоопухолевыми агентами, такими как алкилирующие агенты, антиметаболиты, противоопухолевые агенты растительного происхождения, агенты для гормональной терапии, ингибиторы топоизомеразы, производные камптотецина, ингибиторы киназы, таргетные лекарственные средства, антитела, интерфероны и/или модификаторы биологического ответа, антиангиогенные соединения и другие противоопухолевые лекарственные средства. В этой связи ниже представлен неограничивающий перечень примеров вторичных агентов, которые можно применять в комбинации с соединениями в соответствии с настоящим изобретением: 1311-chTNT, абареликс, абиратерон, акларубицин, альдеслейкин, алемтузумаб, алитретиноин, альтретамин, аминоглутетимид, амрубицин, амсакрин, анастрозол, арглабин, триоксид мышьяка, аспарагиназа, азацитидин, базиликсимаб, BAY 80-6946, BAY 1000394, белотекан, бендамустин, бевацизумаб, бексаротен, бикалутамид, бисантрен, блеомицин, бортезомиб, бусерелин, бусульфан, кабазитаксел, фолинат кальция, левофолинат кальция, капецитабин, карбоплатин, кармофур, кармустин, катумаксомаб, целекоксиб, целмолейкин, цетуксимаб, хлорамбуцил, хлормадинон, хлорметин, цисплатин, кладрибин, клодроновая кислота, клофарабин, кризантаспаза, циклофосфамид, ципротерон, цитарабин, дакарбазин, дактиномицин, дарбэпоэтин альфа, дазатиниб, даунорубицин, децитабин, дегареликс, денилейкин дифтитокс, деносумаб, деслорелин, диброспидия хлорид, доцетаксел, доксифлуридин, доксорубицин, доксорубицин+эстрон, экулизумаб, эдреколомаб, эллиптиния ацетат, элтромбопаг, эндостатин, эноцитабин, эпирубицин, эпитиостанол, эпоэтин альфа, эпоэтин бета, эптаплатин, эрибулин, эрлотиниб, эстрадиол, эстрамустин, этопозид, эверолимус, эксеместан, фадрозол, филграстим, флударабин, фторурацил, флутамид, форместан, фотемустин, фулвестрант, нитрат галлия, ганиреликс, гефитиниб, гемцитабин, гемтузумаб, глутоксим, гозерелин, гистамина дигидрохлорид, гистрелин, гидроксикарбамид, зерна 1-125, ибандроновая кислота, ибритумомаб тиуксетан, идарубицин, ифосфамид, иматиниб, имиквимод, импросульфан, интерферон альфа, интерферон бета, интерферон гамма, ипилимумаб, иринотекан, иксабепилон, ланреотид, лапатиниб, леналидомид, ленограстим, лентинан, летрозол, лейпрорелин, левамизол, лизурид, лобаплатин, ломустин, лонидамин, мазопрокол, медроксипрогестерон, мегестрол, мелфалан, мепитиостан, меркаптопурин, метотрексат, метоксален, метиламинолевулинат, метилтестостерон, мифамуртид, милтефозин, мириплатин, митобронитол, митогуазон, митолактол, митомицин, митотан, митоксантрон, недаплатин, неларабин, нилотиниб, нилутамид, нимотузумаб, нимустин, нитракрин, офатумумаб, омепразол, опрелвекин, оксалиплатин, генотерапия р53, паклитаксел, палифермин, зерна палладия-103, памидроновая кислота, панитумумаб, пазопаниб, пэгаспаргаза, ПЭГ-эпоэтин бета (метокси-ПЭГ-эпоэтин бета), пэгфилграстим, пэгинтерферон альфа-2b, пеметрексед, пентазоцин, пентостатин, пепломицин, перфосфамид, пицибанил, пирарубицин, плериксафор, плакамицин, полиглусам, полиэстрадиолфосфат, полисахарид-К, порфимер натрия, пралатрексат, преднимустин, прокарбазин, хинаголид, хлорид радия-223, ралоксифен, ралтитрексед, ранимустин, разоксан, рефаметиниб, регорафениб, ризедроновая кислота, ритуксимаб, ромидепсин, ромиплостим, сарграмостим, сипулейцел-Т, сизофиран, собузоксан, глицидидазол натрия, сорафениб, стрептозоцин, сунитиниб, талапорфин, тамибаротен, тамоксифен, тазонермин, тецелейкин, тегафур, тегафур+гимерацил+отерацил, темопорфин, темозоломид, темсиролимус, тенипозид, тестостерон, тетрофосмин, талидомид, тиотепа, тимальфазин, тиогуанин, тоцилизумаб, топотекан, торемифен, тозитумомаб, трабектедин, трастузумаб, треосульфан, третиноин, трилостан, трипторелин, трофосфамид, триптофан, убенимекс, валрубицин, вандетаниб, вапреотид, вемурафениб, винбластин, винкристин, виндезин, винфлунин, винорелбин, вориностат, ворозол, стеклянные микросферы с иттрием-90, зиностатин, зиностатина стималамер, золедроновая кислота и зорубицин.
Соединения в соответствии с настоящим изобретением также можно применять для лечения рака в сочетании с лучевой терапией и/или хирургическим вмешательством.
Соединения в соответствии с настоящим изобретением могут действовать системно и/или местно. Для этой цели их можно вводить подходящим способом, таким как, например, пероральный, парентеральный, легочный, назальный, сублингвальный, лингвальный, буккальный, ректальный, дермальный, трансдермальный, конъюнктивальный или ушной путь, или в виде имплантата или стента.
Для этих путей введения можно вводить соединения в соответствии с настоящим изобретением в подходящих формах для применения.
Подходящими для перорального введения являются лекарственные формы для введения, которые действуют, как описано в известном уровне техники, и доставляют соединения в соответствии с настоящим изобретением быстро и/или в модифицированной форме, которая содержит соединения в соответствии с настоящим изобретением в кристаллической, и/или аморфной, и/или растворенной форме, такой как, например, таблетки (покрытые или не покрытые, например, таблетки с энтеросолюбильными покрытиями или покрытиями, растворение которых задерживается или которые являются нерастворимыми и которые контролируют высвобождение соединения в соответствии с настоящим изобретением), таблетки, которые быстро распадаются в полости рта, или пленки/облатки, пленки/лиофилизаты, капсулы (например, твердые или мягкие желатиновые капсулы), таблетки в сахарной оболочке, гранулы, пеллеты, порошки, эмульсии, суспензии, аэрозоли или растворы.
Парентеральное введение может осуществляться без этапа абсорбции (например, внутривенно, внутриартериально, внутрисердечно, внутрипозвоночно или интралюмбально) или с включением абсорбции (например, внутримышечно, подкожно, внутрикожно, чрескожно или интраперитонально). Лекарственные формы для введения, подходящие для парентерального введения, представляют собой, среди прочего, препараты для инъекций и инфузий в форме растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков.
Примерами лекарственных форм, подходящих для других путей введения, являются фармацевтические формы для ингаляций (среди прочего, порошковые ингаляторы, небулайзеры), назальные капли/растворы/спреи; таблетки для введения лингвально, сублингвально или буккально, пленки/облатки или капсулы, суппозитории, препараты для глаз или ушей, вагинальные капсулы, водные суспензии (лосьоны, болтушки), липофильные суспензии, мази, кремы, трансдермальные терапевтические системы (такие как пластыри), молочко, пасты, пены, присыпки, имплантаты или стенты.
Соединения в соответствии с настоящим изобретением могут быть преобразованы в указанные лекарственные формы для введения. Это можно осуществить хорошо известным способом путем смешивания с инертными нетоксичными фармацевтически подходящими адъювантами. Эти адъюванты включают, среди прочего, носители (например, микрокристаллическую целлюлозу, лактозу, маннит), растворители (например, жидкие полиэтиленгликоли), эмульгаторы и диспергирующие агенты или смачивающие агенты (например, додецилсульфат натрия, олеат полиоксисорбитана), связующие вещества (например, поливинилпирролидон), синтетические и природные полимеры (например, альбумин), стабилизаторы (например, антиоксиданты, такие как аскорбиновая кислота), красители (например, неорганические пигменты, такие как оксиды железа) и агенты для маскировки вкуса и/или запаха.
Кроме того, в соответствии с настоящим изобретением предложены лекарственные средства, содержащие по меньшей мере одно соединение в соответствии с настоящим изобретением, обычно вместе с одним или более инертными нетоксичными фармацевтически приемлемыми адъювантами, и их применение для целей, упомянутых выше.
Независимо от выбранного способа введения, ингибиторы киназы в соответствии с настоящим изобретением и/или фармацевтические композиции в соответствии с настоящим изобретением включают в состав фармацевтически приемлемых лекарственных форм обычными способами, известными специалистам в данной области техники.
Фактические уровни дозировки и продолжительность введения активных ингредиентов в фармацевтических композициях в соответствии с настоящим изобретением могут быть изменены таким образом, чтобы получить количество активного ингредиента, которое эффективно для достижения требуемого терапевтического ответа у конкретного пациента, и при этом не токсично для указанного пациента.
Получение соединений
Соединения в соответствии с настоящим изобретением могут быть синтезированы с применением стандартных способов синтеза, известных специалистам в данной области техники, или с применением способов, известных в данной области техники, в комбинации со способами, описанными в настоящем документе. Кроме того, растворители, температуры и другие условия реакций, представленные в настоящем документе, могут быть изменены по усмотрению специалистов в данной области техники. В качестве дополнительного руководства также могут быть применены следующие способы синтеза.
Указанные реакции можно использовать последовательно для получения соединений, описанных в настоящем документе; или их можно использовать для синтеза фрагментов, которые затем объединяют способами, описанными в настоящем документе, и/или способами, известными в данной области техники.
Исходные материалы, применяемые для синтеза соединений, описанных в настоящем документе, могут быть синтезированы или могут быть получены из коммерческих источников. Соединения, описанные в настоящем документе, и другие родственные соединения, имеющие отличающиеся заместители, могут быть синтезированы с применением методов и материалов, известных специалистам в данной области техники. Общие способы получения соединений, раскрытых в настоящем документе, могут быть получены на основе известных реакций в данной области, и реакции могут быть модифицированы с применением соответствующих реагентов и условий, которые будут очевидны специалисту в данной области техники, для введения различных фрагментов в молекулы, предложенные в настоящем изобретении.
Продукты реакций могут быть выделены и очищены при необходимости с применением обычных методов, включая, но не ограничиваясь перечисленными: фильтрацию, дистилляцию, кристаллизацию, хроматографию и тому подобное. Характеристики таких продуктов могут быть определены с применением обычных средств, включая физические константы и спектральные данные.
Неограничивающие примеры схемы синтеза для получения соединений формулы (I) описаны ниже.
Примеры
Следующие конкретные неограничивающие примеры следует рассматривать только как иллюстративные, но никоим образом не ограничивающие настоящее изобретение. Хотя дополнительное подробное описание не требуется, полагают, что специалисты в данной области техники могут в полной мере применять настоящее изобретение на основании приведенного здесь описания.
Пример 1: Синтез
6-(2-((4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,4-дигидро изохинолин-1 (2Н)-она
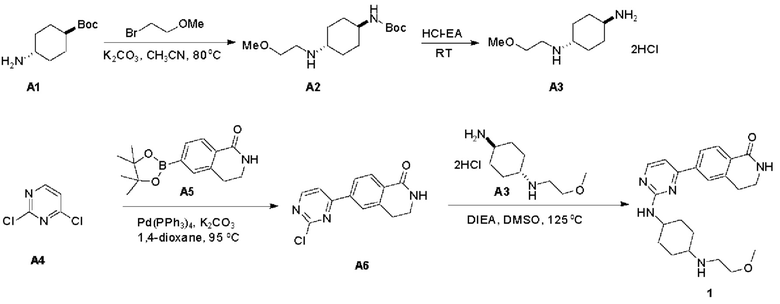
Трет-бутиловый эфир ((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)карбаминовой кислоты (А2): Соединение А1 (10,0 г, 46,7 ммоль), 2-бромэтилметиловый эфир (5,2 г, 37,4 ммоль) и карбонат калия (12,9 г, 93,4 ммоль) добавляли к ацетонитрилу (150 мл) и перемешивали при 80°С в течение 16 часов. Реакцию останавливали после того как мониторинг методом ТСХ показал, что осталось небольшое количество исходного материала. Реакционный раствор охлаждали до комнатной температуры, фильтровали и удаляли фильтрат путем ротационного выпаривания. Полученный продукт загружали на силикагель для колоночной хроматографии (система элюентов: ДХМ/МеОН=100:1→40:1→20:1), в результате чего получали 6,3 г твердого вещества желто-белого цвета А2 с выходом 50%.
(1r, 4r)-N1-(2-метоксиэтил)циклогексан-1,4-диамина гидрохлорид (A3): Соединение А2 (6 г, 22,0 ммоль) растворяли в HCl-ЭА (80 мл) и перемешивали при комнатной температуре в течение 2 часов. Было получено большое количество твердого осадка. Реакционный раствор фильтровали и осадок на фильтре сушили с получением 5,1 г твердого вещества белого цвета (дигидрохлорида) A3 с выходом 94,8%.
6-(2-хлорпиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он (А6): А4 (81 мг, 0,54 ммоль, 1,5 экв.) растворяли в 1,4-диоксане (10 мл), а затем добавляли А5 (100 мг, 0,36 ммоль, 1,0 экв.), карбонат калия (99 мг, 0,72 ммоль, 2 экв.) и Pd(PPh3)4 (41 мг, 0,036 ммоль, 0,1 экв.) и перемешивали реакционную смесь при 95°С в течение 4 часов. С помощью ТСХ показали, что реакция была завершена. Реакционную систему загружали на необработанный силикагель и разделяли с помощью колоночной хроматографии (система элюентов: ДХМ/ЭА=3:1), в результате чего получали соединение А6 (60 мг, 64%).
6-(2-((4-(2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1 (2Н)-он (1): Соединение А6 (50 мг, 0,19 ммоль, 1,0 экв.), A3 (56 мг, 0,22 ммоль, 1,2 экв.), диизопропилэтиламин (ДИЭА) (73 мг, 0,57 ммоль, 3,0 экв.) и диметилсульфоксид (ДМСО) (2 мл) добавляли в бутыль соответственно и перемешивали в течение ночи при 125°С. ЖХ/МС показала, что исходный материал был израсходован. В полученный продукт добавляли воду, экстрагировали дихлорметаном, сушили над безводным сульфатом натрия, а затем фильтровали и концентрировали. Полученный остаток разделяли с помощью колонки (система элюентов: ДХМ/МеОН=30:1), в результате чего получали целевое соединение 1 (твердое вещество белого цвета, 30 мг, 40%). МС: (М+1) 396,2. 1Н ЯМР (500 МГц, ДМСО-d6) 5 8,37 (s, Ш), 8,08 - 7,97 (m, 3Н), 7,94 (d, J=8,0 Гц, Ш), 7,15 (t, J=6,5 Гц, 2Н), 3,74 (s, Ш), 3,41 (s, 4Н), 3,26 (s, 3Н), 2,98 (t, J=6,6 Гц, 2Н), 2,75 (d, J=5,7 Гц, 2Н), 2,46 (s, Ш), 1,95 (s, 4Н), 1,35-1,27 (m, 2Н), 1,16 (s, 2Н).
Следующие примеры соединений 2-25 синтезировали аналогично примеру 1, если не указано иное.
Пример 2:
6-(5-хлор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин- 1(2Н)-он 2 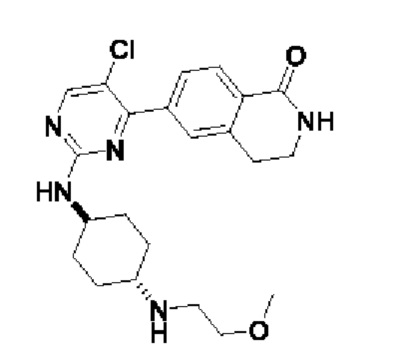
MC (ИЭР)m/z(M+1)+: 430,2.
Пример 3:
6-(5-фтор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-и л)-3,4-дигидроизохинолин-1(2Н)-он 3
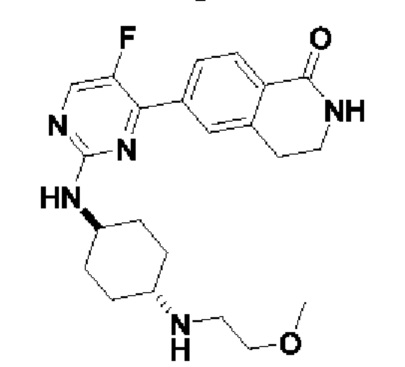
MC (ИЭР )m/z(M+1)+: 414,22.
Пример 4:
6-(2-(((1 г,4к)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2-мет ил-3,4-дигидроизохинолин-1(2Н)-он 4
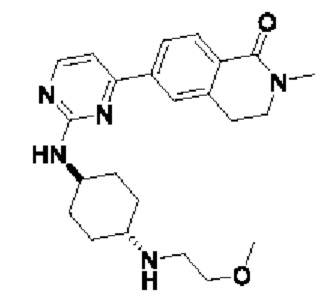
MC (ИЭР )m/z(M+1)+: 410,26.
Пример 5:
5- (2-(((1 г,4 г))-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)изоин долин-1-он 5
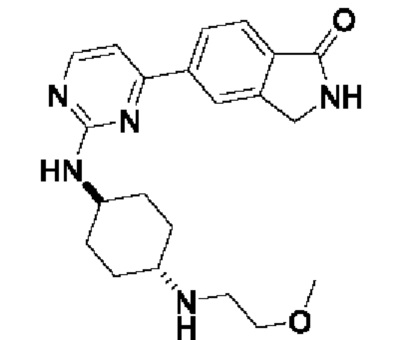
MC (ИЭР)m/z(M+1)+: 382,22.
Пример 6:
6- (2-((1 г,4 г)-4-(2-метоксиэтил)амино)циклогексил)амино)-5-метилпиридин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 6
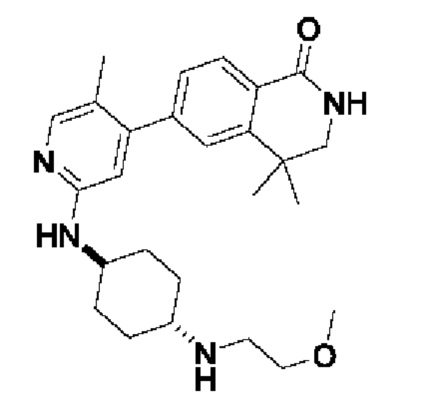
Синтез соединения 6 завершали с применением стадий, аналогичных описанным в примере 1, с заменой 2,4-дихлорпиримидина на 4-бром-2-фтор-5-метилпиридин. МС (ИЭР) m/z(M+1)+: 437,29.
Пример 7:
6-(2-((1r,4r)-4-(2-метоксиэтил)амино)циклогексил)амино)-5-метилпиримидин-4-ил)-3,4-дигидроизохинолин- 1(2Н)-он 7
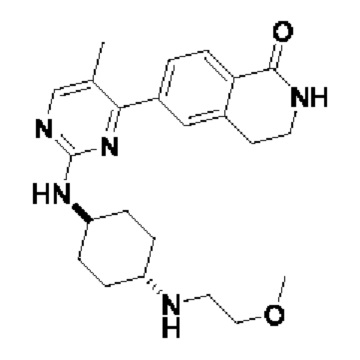
MC (ИЭР)n/z(М+1)+: 410,26.
Пример 8:
6-(5-хлор-2-((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиридин-4-ил)-3, 4-дигидроизохинолин-1(2Н)-он 8
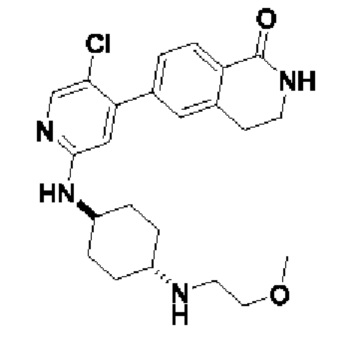
Соединение из примера 8 синтезировали с применением стадий, аналогичных описанным в примере 6. МС (ИЭР) m/z(M+1)+: 429,21.
Пример 9:
2-((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)-4-(1-оксо-1,2,3,4-тетрагид роизохинолин-6-ил)пиримидин-5-карбонитрил 9
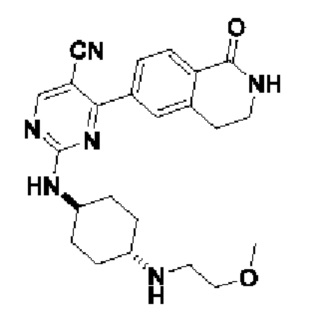
МС (ИЭР )m/z(M+1)+: 421,24.
Пример 10:
6-(5-хлор-2-((1 г,4 г)-4-((2-метоксиэтил)амино)циклогексил)амино)пиридин-4-ил)-4, 4-диметил-3,4-дигидроизохинолин-1(2Н)-он 10
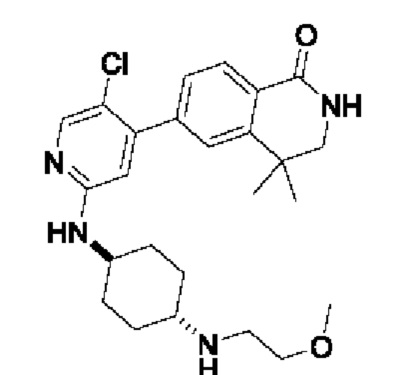
Соединение из примера 10 синтезировали с применением стадий, аналогичных описанным в примере 6. МС (ИЭР) m/z(M+1)+: 457,24.
Пример 11:
6-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-4,4-д иметил-3,4-дигидроизохинолин- 1(2Н)-он 11
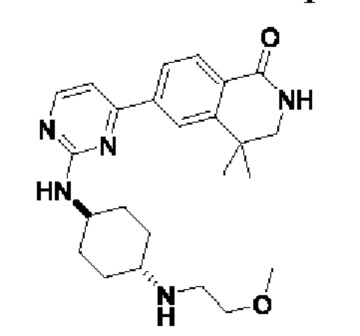
МС (ИЭР)m/z(M+1)+: 424,27.
Пример 12:
6'-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2',3'-дигидро-1'Н-спиро[циклопропан-1,4'-изохинолин]-1'-он 12
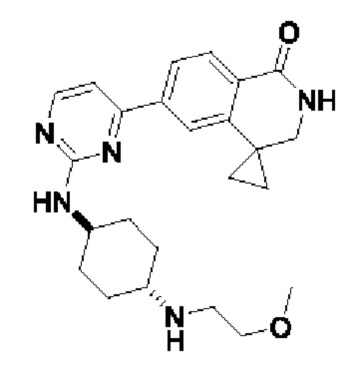
МС (ИЭР)m/z(M+1)+: 422,26.
Пример 13:
4,4-диэтил-6-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 13
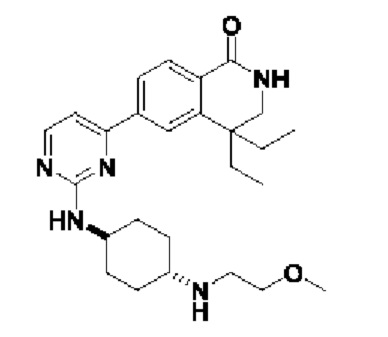
МС (ИЭР )m/z(M+1)+: 452,30.
Пример 14:
4,4-диизопропил-6-(2-(((1 г,4 г)-4-((2-метоксиэтил)амино)циютогексил)амино)пирим идин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 14
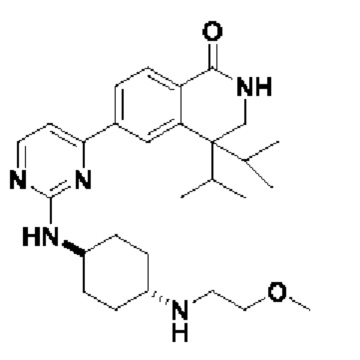
МС (ИЭР)m/z(M+1)+: 480,33.
Пример 15:
6-(5-хлор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 15
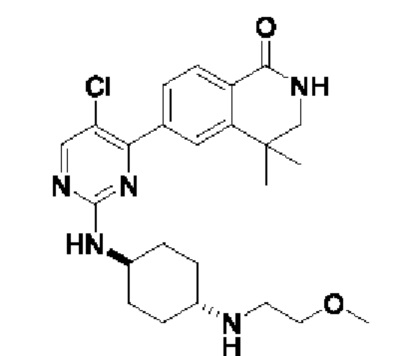
MC (ИЭР ИЭР)m/z(M+1)+: 458,23.
Пример 16:
6-(5-фтор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-и л)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 16
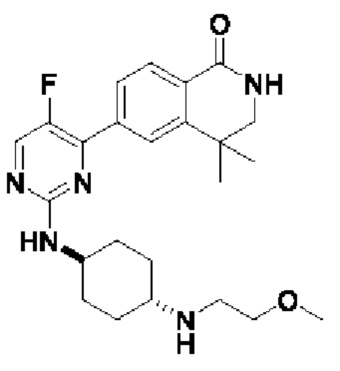
МС (ИЭР)m/z(M+1)+: 442,26.
Пример 17:
6-(2-((1r,4r)-4-(2-метоксиэтил)амино)циклогексил)амино)-5-метилпиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 17
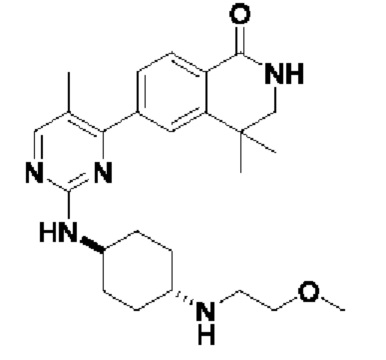
МС (ИЭР)m/z(M+1)+: 438,29.
Пример 18:
6-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2,4,4-триметил-3,4-дигидроизохинолин- 1(2Н)-он 18
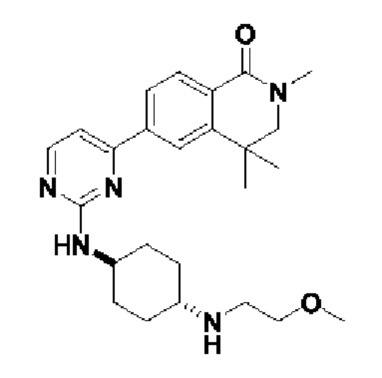
МС (ИЭР)m/z(M+1)+: 424,27.
Пример 19:
6-(5-хлор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2,4,4-триметил-3,4-дигидроизохинолин-1(2Н)-он 19
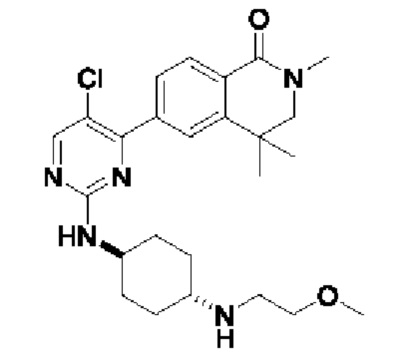
MC (ИЭР)m/z(M+1)+: 472,25.
Пример 20:
5-(5-фтор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-и л)-3,3-диметилизоиндолин-1-он 20
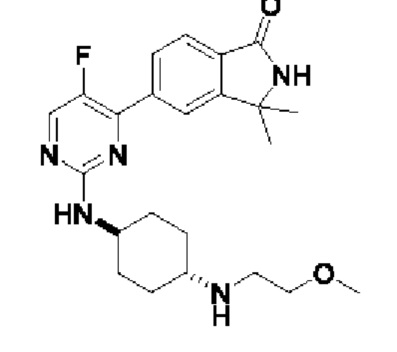
МС (ИЭР)m/z(M+1)+: 428,25.
Пример 21:
5-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,3-д иметилизоиндолин-1-он 21
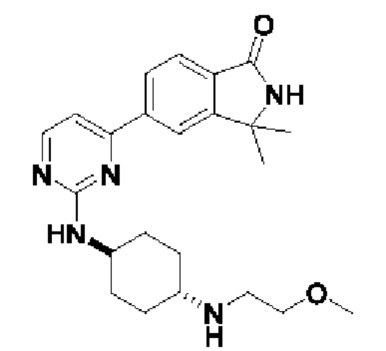
МС (ИЭР )m/z(M+1)+: 410,26.
Пример 22:
5-(5-хлор-2-(((1 г,4 г)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-3,3-диметилизоиндолин-1-он 22
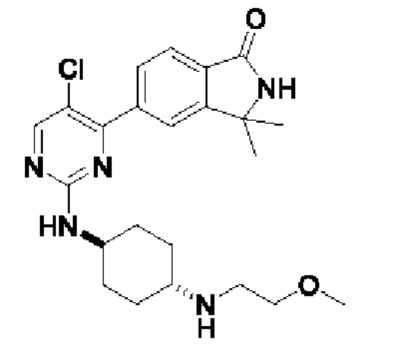
МС (ИЭР)m/z(M+1)+: 444,22.
Пример 23:
5-(2-(((1 г,4 г)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2,3,3-триметилизоиндолин-1-он 23
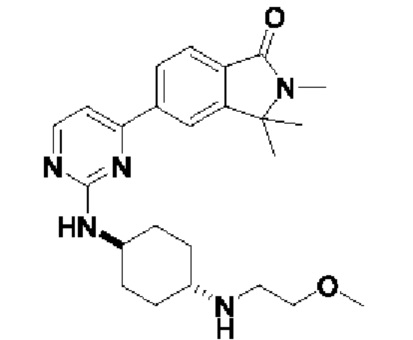
MC (ИЭР)m/z(M+1)+: 424,27.
Пример 24:
5-(5-хлор-2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2,3,3-триметилизоиндолин-1-он 24
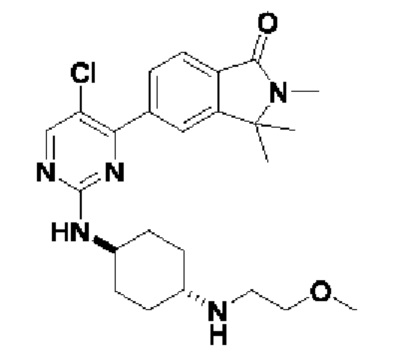
МС (ИЭР)m/z(M+1)+: 458,23.
Пример 25:
6'-(2-(((1r,4r)-4-((2-метоксиэтил)амино)циклогексил)амино)пиримидин-4-ил)-2',3'-дигидро- 1'Н-спиро[циклобутан- 1,4'-изохинолин]-1'-он 25
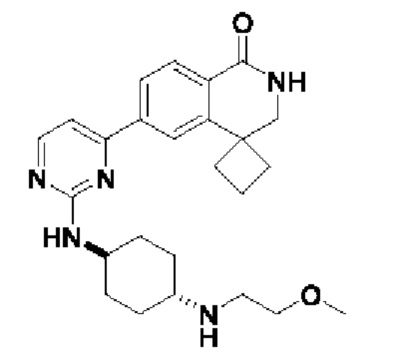
МС (ИЭР)m/z(M+1)+: 436,27.
Пример 26: Синтез
3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)ам ино)бензолсульфонамида 26
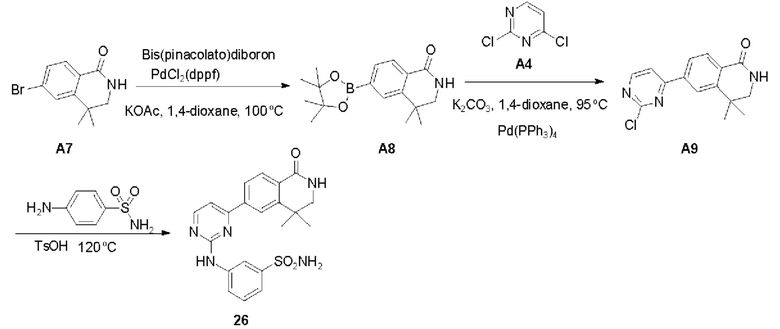
4,4-диметил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-3,4-дигидроизохинолин-1(2Н)-он (А8): К 1,4-диоксану (20 мл) добавляли соединение А7 (1,0 г, 3,93 ммоль), бис(пинаколато)дибор (1,2 г, 4,72 ммоль, 1,2 экв.), ацетат калия (0,77 г, 7,86 ммоль, 2 экв.) и PdCh(dppf) (0,32 г, 0,39 ммоль, 0,1 экв.) и перемешивали при 100°С в течение 5 часов. Реакцию останавливали после того, как мониторинг с помощью ТСХ показал отсутствие исходного материала. Реакционный раствор охлаждали до комнатной температуры и загружали на силикагель для колоночной хроматографии (система элюентов: ДХМ/ЭА=3:1), в результате чего получали твердое вещество красновато-коричневого цвета А8 (0,9 г, 76%).
6-(2-хлорпиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он (А9): А8 (300 мг, 0,99 ммоль, 1,0 экв.) растворяли в 1,4-диоксане (10 мл), в который затем добавляли А4 (178 мг, 1,19 ммоль, 1,2 экв.), карбонат калия (0,27 г, 1,98 ммоль, 2 экв.) и Pd(PPh3)4 (0,11 г, 0,099 ммоль, 0,1 экв.) и перемешивали при 95°С в течение 4 часов. ТСХ показала, что реакция была завершена. Систему загружали на необработанный силикагель для колоночной хроматографии (система элюентов: ДХМ/ЭА=3:1), в результате чего получали целевое соединение А9 (130 мг, 45%).
3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-и л)амино)бензолсульфонамид (26): Соединение А9 (50 мг, 0,17 ммоль, 1,0 экв.), 4-аминобензолсульфонамид (30 мг, 0,17 ммоль, 1,0 экв.), п-толуолсульфоновую кислоту (29 мг, 0,17 ммоль, 1,0 экв.) и втор-бутанол (2 мл) добавляли в бутыль соответственно и перемешивали в течение ночи при 120°С. После фильтрации осадок на фильтре промывали небольшим количеством метанола и метил-трет-бутилового эфира в результате чего получали твердое вещество светло-желтого цвета. Указанное твердое вещество переносили во флакон, добавляли насыщенный раствор бикарбоната натрия, перемешивали и последний раз фильтровали. Твердое вещество промывали метанолом и метил-трет-бутиловым эфиром, в результате чего получали целевое соединение 26 (твердое вещество белого цвета, 30 мг, 41%). МС: (М+1) 424,14. 1Н ЯМР (500 МГц, ДМСО-d6) δ 10,08 (s, 1H), 8,65 (d, J=5,2 Гц, 1H), 8,54 (s, 1H), 8,20-8,18 (m, 2Н), 8,10 (s, 1H), 8,01 (d, J=8,1 Гц, 1H), 7,97-7,94 (m, 1H), 7,59 (d, J=5,2 Гц, 1H), 7,52-7,44 (m, 2Н), 7,31 (s, 2Н), 3,23 (d, J=3,0 Гц, 2Н), 1,37 (s, 6Н).
Соединения из следующих примеров 27-95 и 99-101 синтезировали аналогично примеру 26, если не указано иное.
Пример 27:
(3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)ам ино)фенил)метансульфамид 27
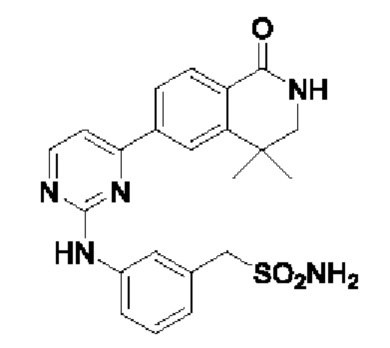
МС (ИЭР)m/z(M+1)+: 438,16.
Пример 28: 4,4-диметил-6-(2-((3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 28
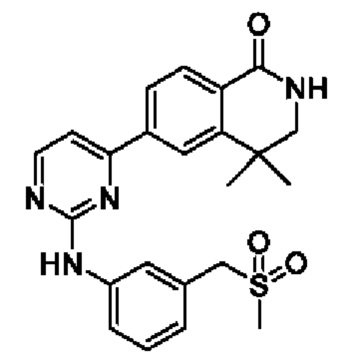
МС (ИЭР) m/z(M+1)+: 437,16.
Пример 29
3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)амино)-N,N-диметилбензолсульфонамид 29
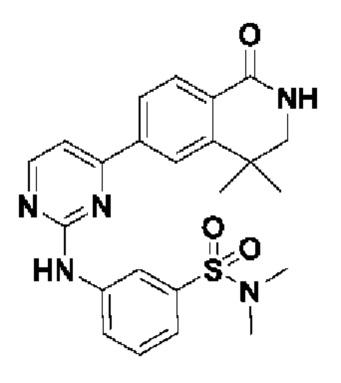
МС (ИЭР)m/z(M+1)+: 452,18.
Пример 30:
4,4-диметил-6-(2-((3-(морфолиносульфонил)фенил)амино)пиримидин-4-ил)-3,4-ди гидроизохинолин-1(2Н)-он 30
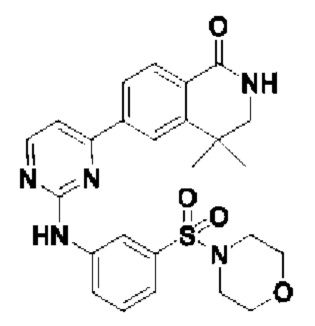
МС (ИЭР)m/z(М+1)+: 494,19.
Пример 31:
3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)ам ино)-N-метилбензолсульфонамид 31
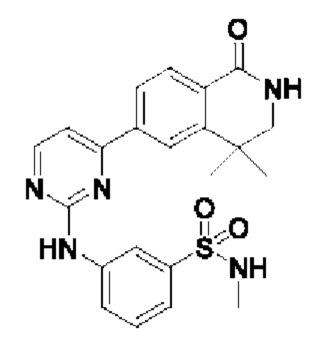
МС (ИЭР)m/z(М+1)+: 438,16.
Пример 32:
4,4-диметил-6-(2-((3-(метилсульфонил)фенил)амино)пиримидин-4-ил)-3,4-дигидр оизохинолин-1(2Н)-он 32
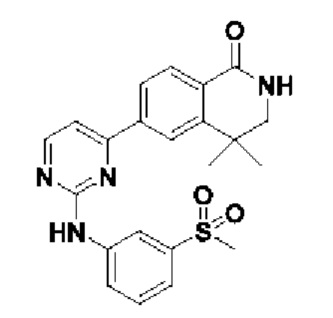
МС (ИЭР) m/z(M+1)+: 423,15.
Пример 33:
3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)амино)-N-(1-метилпиперидин-4-ил)бензамид 33
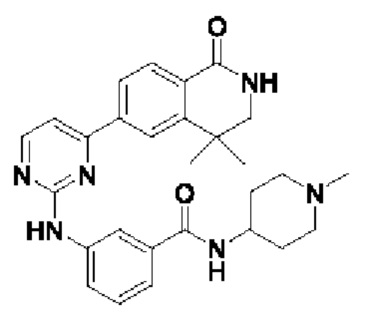
МС (ИЭР)m/z(M+1)+: 485,27.
Пример 34:
N-(5-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил) амино)-2-фторфенил)метансульфамид 34
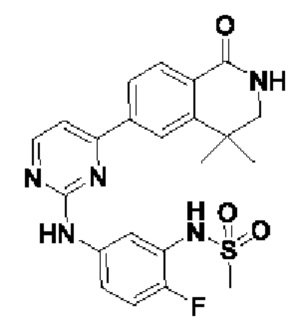
МС (ИЭР)m/z(M+1)+: 456,15.
Пример 35:
6-(2-((3-(1,4-гомопиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 35
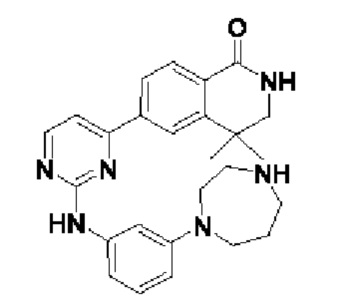
МС (ИЭР)m/z(M+1)+: 443,26.
Пример 36:
6-(2-((4-фтор-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 36

МС (ИЭР )m/z(M+1)+: 455,16.
Пример 37:
4,4-диметил-6-(2-((3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 37
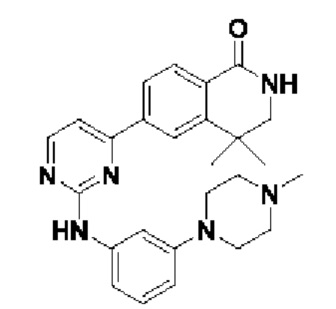
MC (ИЭР)m/z(M+1)+: 433,26.
Пример 38:
4,4-диметил-6-(2-((3-(S-метилсульфонимид)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 38
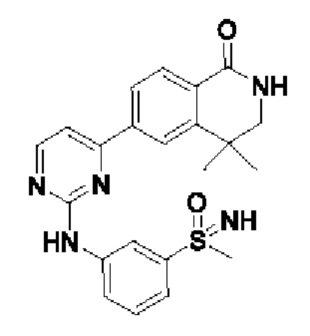
МС (ИЭР)m/z(M+1)+: 422,17.
Пример 39:
4,4-диметил-6-(2-((4-(метилсульфонил)фенил)амино)пиримидин-4-ил)-3,4-дигидр оизохинолин-1(2Н)-он 39
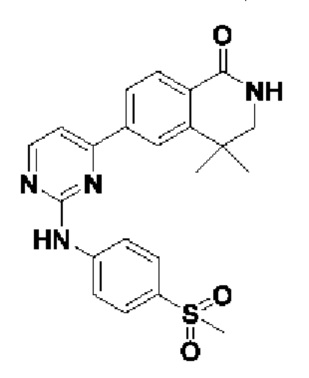
МС (ИЭР)m/z(M+1)+: 423,15.
Пример 40:
4,4-диметил-6-(2-((4-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 40
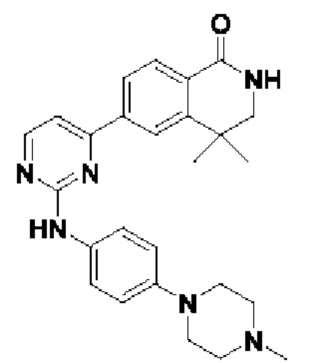
МС (ИЭР )m/z(M+1)+: 443,26.
Пример 41: 5-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)амино)-2-фтор-N-(1-метилпиперидин-4-ил)бензамид 41
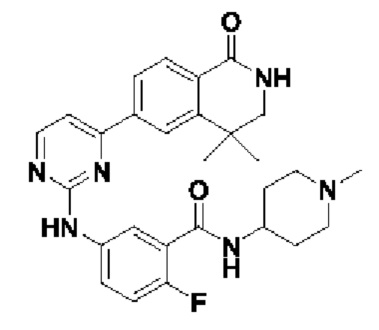
МС (ИЭР)m/z(M+1)+: 503,26.
Пример 42:
4,4-диметил-6-(2-((4-метил-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 42
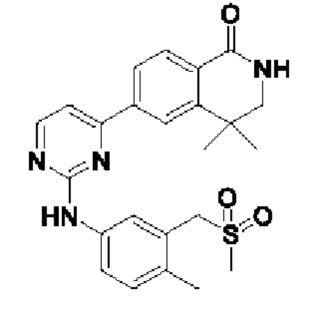
MC (ИЭР)m/z(M+1)+: 451,18.
Пример 43:
6-(2-((2,4-дифтор-5-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 43
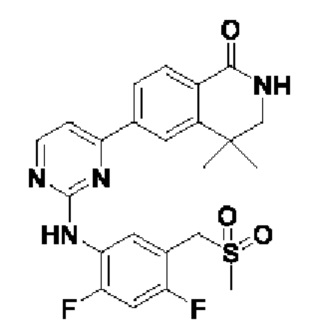
МС (ИЭР)m/z(M+1)+: 473,15.
Пример 44:
4,4-диметил-6-(2-((3-((метилсульфонил)метил)-4-(трифторметил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 44
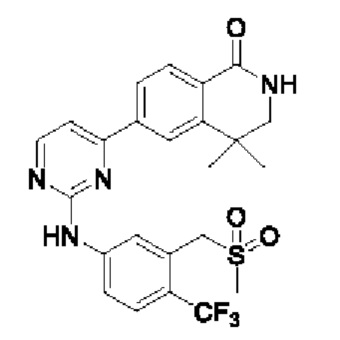
МС (ИЭР)m/z(M+1)+: 505,15.
Пример 45:
6-(2-((4-метокси-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-4,4-ди метил-3,4-дигидроизохинолин- 1(2Н)-он 45
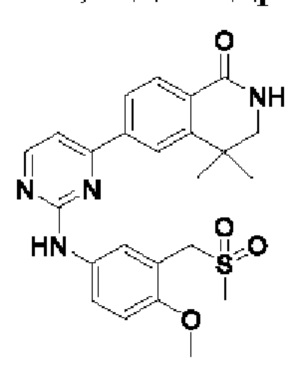
МС (ИЭР)m/z(M+1)+: 467,18.
Пример 46: 6-(2-((4-фтор-3-((метилсульфонил)метил)фенил)амино)пиридин-4-ил)-4,4-диметил -3,4-дигидроизохинолин- 1(2Н)-он 46
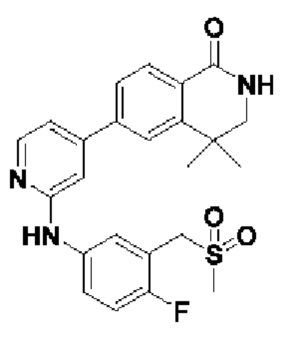
МС (ИЭР)m/z(M+1)+: 454,16.
Пример 47:
4,4-диметил-6-(2-((2-((метилсульфонил)метил)пиридин-4-ил)амино)пиридин-4-ил)-3,4-дигидроизохинолин- 1(2Н)-он 47

МС (ИЭР )m/z(M+1)+: 437,16.
Пример 48:
5-(2-((4-фтор-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,3-Диметилизоиндолин-1-он 48
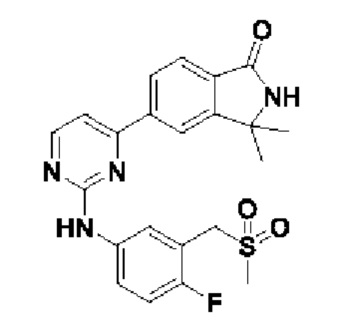
МС (ИЭР)m/z(M+1)+: 441,14.
Пример 49:
3,3-диметил-5-(2-((4-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)изоиндолин- 1-он 49
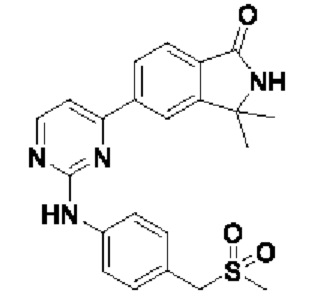
МС (ИЭР)m/z(M+1)+: 423,15.
Пример 50:
5-(5-фтор-2-((4-фтор-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,3-диметилизоиндолин-1-он 50
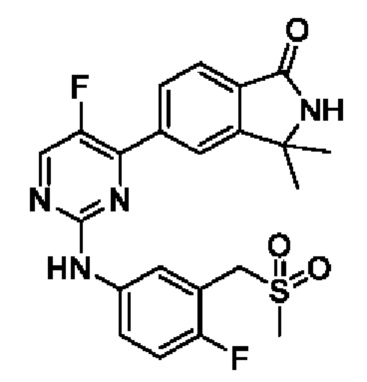
МС (ИЭР)m/z(M+1)+: 459,13.
Пример 51:
5-(5-хлор-2-((4-фтор-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,3-диметилизоиндолин-1-он 51
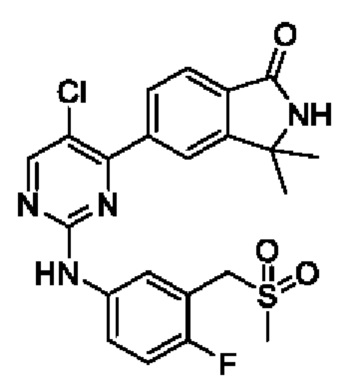
MC (ИЭР)m/z(M+1)+: 475,10.
Пример 52:
5-(5-хлор-2-((2,4-дифтор-5-((метилсульфонил)метил)фенил)амино)пиримидин-4-и л)-3,3-диметилизоиндолин-1-он 52
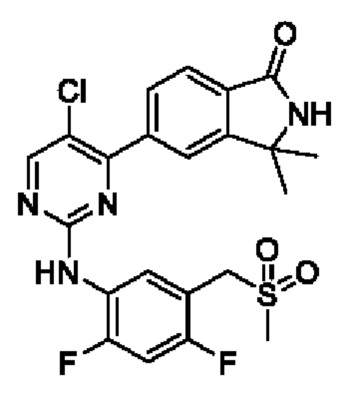
МС (ИЭР)m/z(M+1)+: 493,09.
Пример 53:
5-(2-((2,4-дифтор-5-((метилсульфонил)метил)фенил)амино)-5-фторпиримидин-4-ил)-3,3-диметилизоиндолин-1-он 53
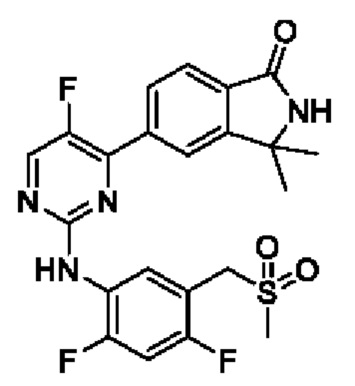
МС (ИЭР)m/z(M+1)+: 477,12.
Пример 54:
5-(5-хлор-2-((4-метил-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,3-диметилизоиндолин-1-он 54
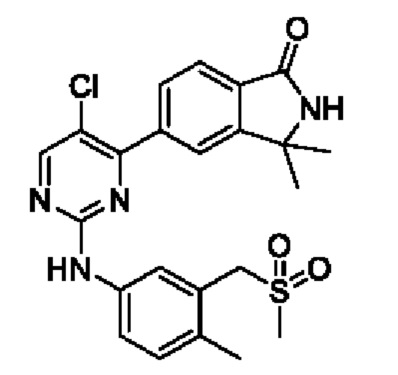
МС (ИЭР)m/z(M+1)+: 471,13.
Пример 55:
5-(5-фтор-2-((4-метил-3-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3.3-диметилизоиндолин-1-он 55
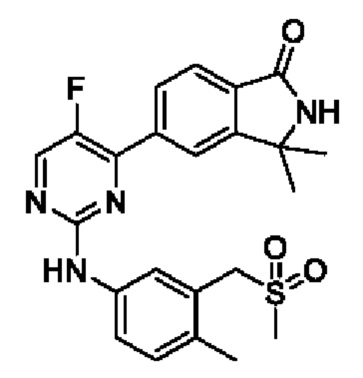
МС (ИЭР)m/z(M+1)+: 455,16.
Пример 56:
4.4-диметил-6-(2-((2-((метилсульфонил)метил)пиридин-4-ил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 56
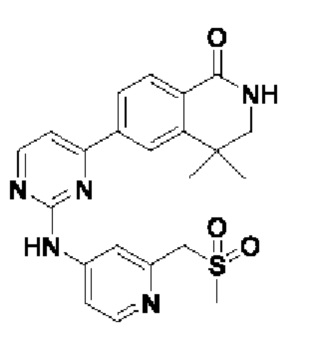
MC (ИЭР)m/z(M+1)+: 438,16.
Пример 57:
4,4-диметил-6-(2-((4-((метилсульфонил)метил)пиридин-2-ил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 57
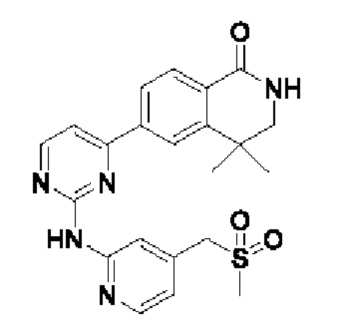
МС (ИЭР)m/z(M+1)+: 438,16.
Пример 58: 4,4-диметил-6-(2-((4-((S-метилсульфонимид)метил)пиридин-2-ил)амино)пиримид ин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 58

МС (ИЭР)m/z(M+1)+: 437,18.
Пример 59:
4,4-диметил-6-(2-((4-(1-(метилсульфонил)циклопропил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 59
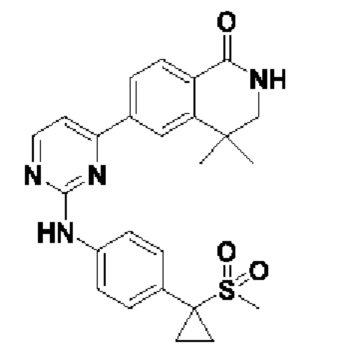
МС (ИЭР)m/z(M+1)+: 463,18.
Пример 60:
6-(5-хлор-2-((4-(1-(метилсульфонил)циклопропил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 60
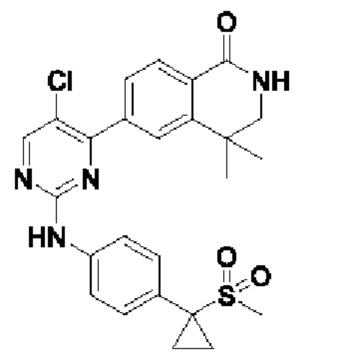
МС (ИЭР)m/z(M+1)+: 497,14.
Пример 61:
6-(5-фтор-2-((4-(1-(метилсульфонил)циклопропил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 61
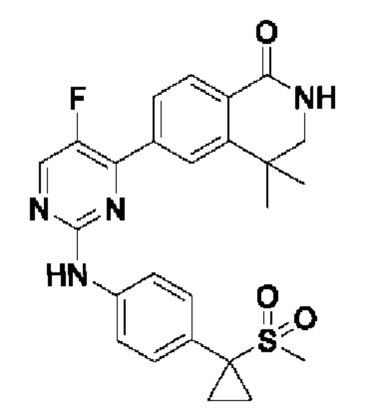
МС (ИЭР)m/z(M+1)+: 481,17.
Пример 62:
6-(5-хлор-2-((4-фтор-3-(1-(метилсульфонил)циклопропил)фенил)амино)пиримиди н-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 62
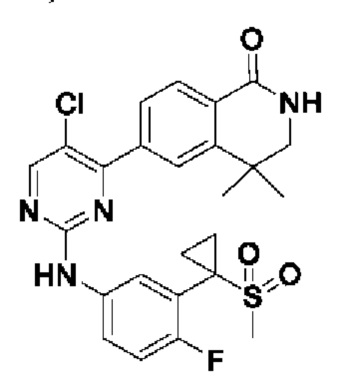
МС (ИЭР) m/z(M+1)+: 515,13.
Пример 63:
6-(5-фтор-2-((4-фтор-3-(1-(метилсульфонил)циклопропил)фенил)амино)пиримиди н-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 63
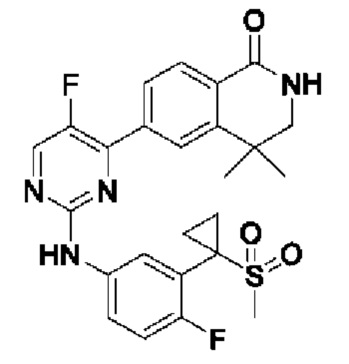
МС (ИЭР)m/z(М+1)+: 499,16.
Пример 64:
6-(5-хлор-2-((2,4-дифтор-5-((метилсульфонил)метил)фенил)амино)пиримидин-4-и л)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 64
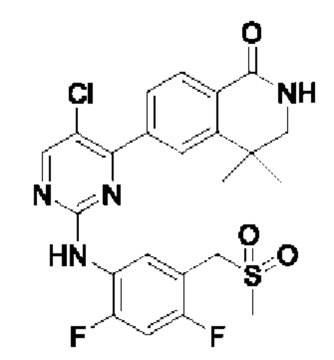
МС (ИЭР)m/z(M+1)+: 507,11.
Пример 65:
6-(2-((4-фтор-3-(1-(метилсульфонил)циклопропил)фенил)амино)пиримидин-4-ил)-2,4,4-триметил-3,4-дигидроизохинолин-1(2Н)-он 65
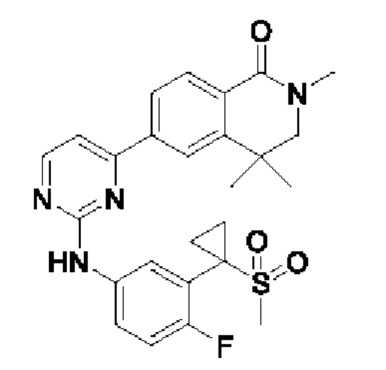
MC (ИЭР)m/z(M+1)+: 495,19.
Пример 66:
6-(5-хлор-2-((4-фтор-3-(1-(метилсульфонил)циклопропил)фенил)амино)пиримиди н-4-ил)-2,4,4-триметил-3,4-дигидроизохинолин-1(2Н)-он 66
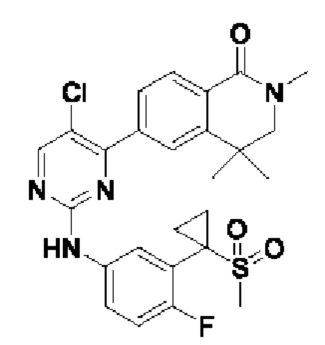
МС (ИЭР)m/z(M+1)+: 529,15.
Пример 67:
6-(5-фтор-2-((4-фтор-3-(1-(метилсульфонил)циклопропил)фенил)амино)пиримиди н-4-ил)-2,4,4-триметил-3,4-дигидроизохинолин-1(2Н)-он 67
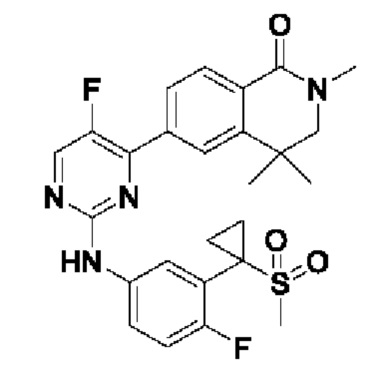
МС (ИЭР)m/z(M+1)+: 513,18.
Пример 68:
6-(5-хлор-2-((3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-димет ил-3,4-дигидроизохинолин-1(2Н)-он 68
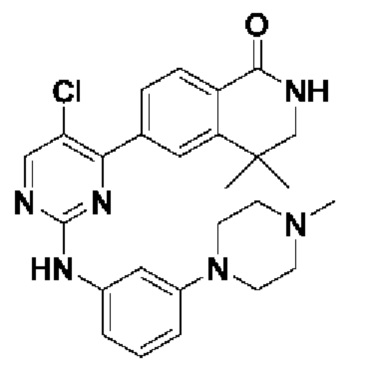
МС (ИЭР)m/z(M+1)+: 477,22.
Пример 69:
6-(5-фтор-2-((3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 69
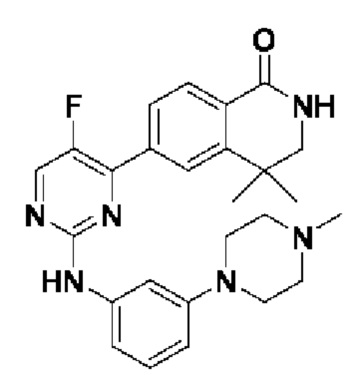
MC (ИЭР)m/z(M+1)+: 461,25.
Пример 70:
4,4-диметил-6-(5-метил-2-((3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 70
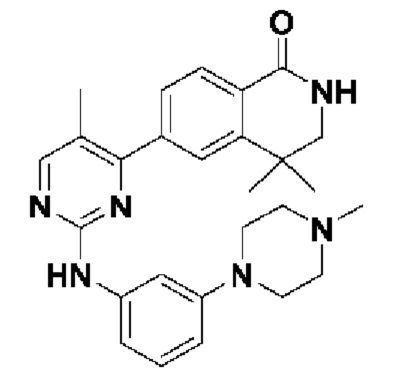
МС (ИЭР)m/z(M+1)+: 457,27.
Пример 71:
6-(5-фтор-2-((4-метил-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 71
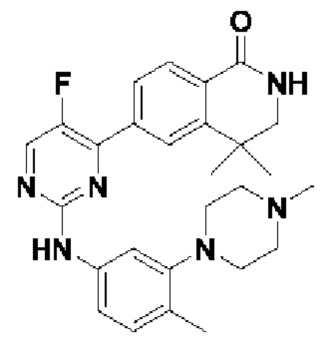
МС (ИЭР)m/z(M+1)+: 475,26.
Пример 72:
6-(5-фтор-2-((4-фтор-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 72
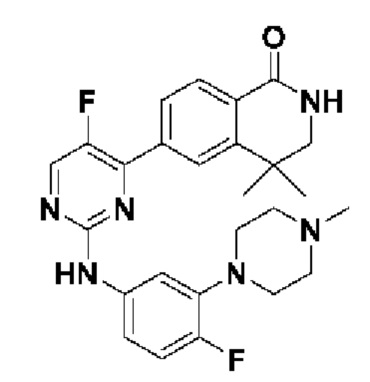
МС (ИЭР)m/z(M+1)+: 479,24.
Пример 73:
6-(5-фтор-2-((3-фтор-5-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 73
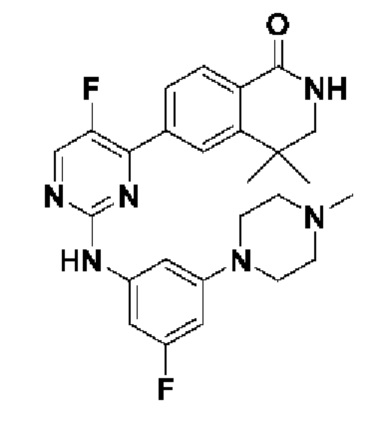
MC (ИЭР)m/z(M+1)+: 479,24.
Пример 74:
6-(5-хлор-2-((4-метил-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 74
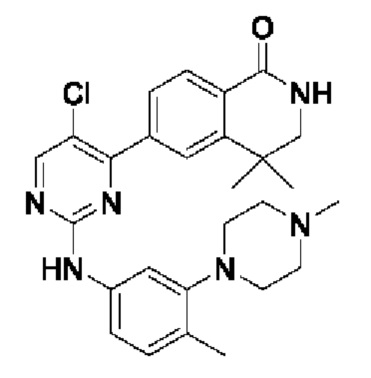
МС (ИЭР)m/z(M+1)+: 491,23.
Пример 75:
6-(5-хлор-2-((4-фтор-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 75
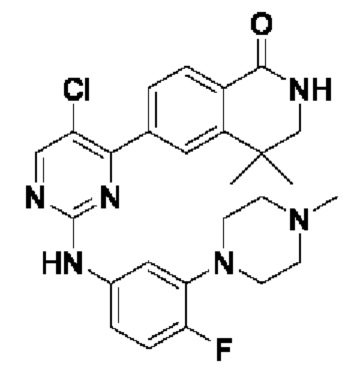
МС (ИЭР )m/z(M+1)+: 495,21.
Пример 76:
6-(5-хлор-2-((3-(4-этилпиперазин-1-ил)-4-фторфенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 76
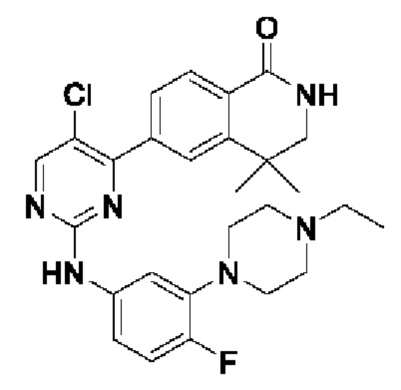
МС (ИЭР)m/z(M+1)+: 509,22.
Пример 77:
6-(5-хлор-2-(4-фтор-3-(4-изопропилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 77
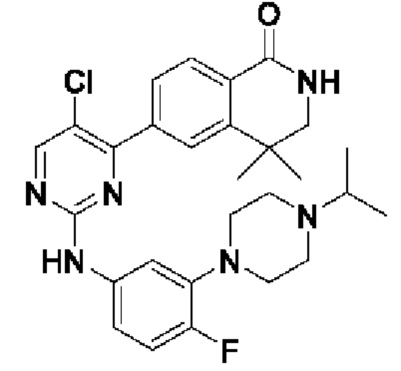
MC (ИЭР )m/z(M+1)+: 523,24.
Пример 78:
6-(5-хлор-2-((3-(4-изопропилпиперазин-1-ил)-4-метилфенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 78
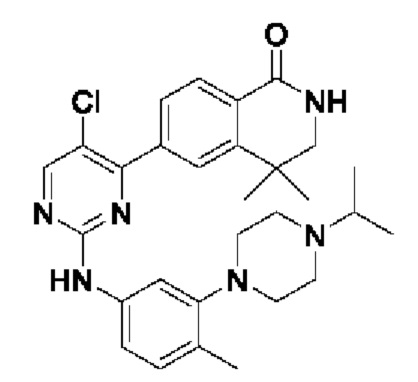
МС (ИЭР)m/z(M+1)+: 519,26.
Пример 79:
6-(2-((3-(4-этилпиперазин-1-ил)-4-фторфенил)амино)
5- фторпиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 79
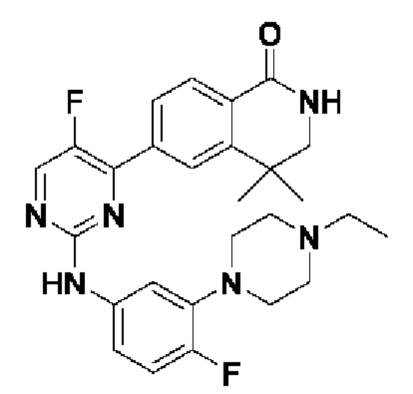
МС (ИЭР )m/z(M+1)+: 493,25.
Пример 80:
6- (5-фтор-2-((4-фтор-3-(4-изопропилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 80
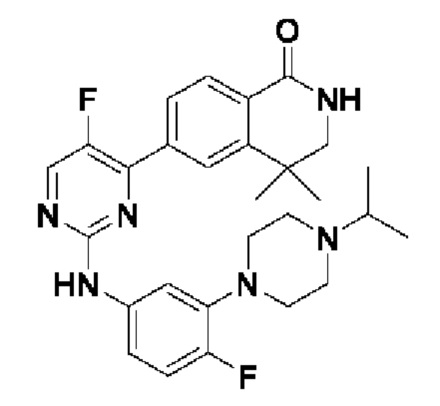
МС (ИЭР)m/z(M+1)+: 507,27.
Пример 81:
6-(2-((4-фтор-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 81
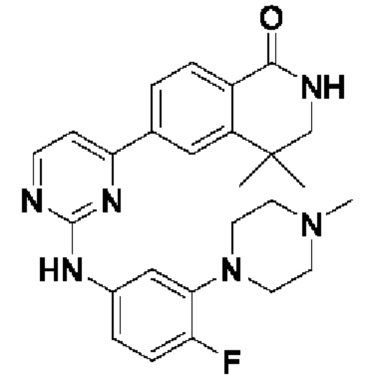
MC (ИЭР)m/z(M+1)+: 461,25.
Пример 82:
4,4-метил-6-(2-((4-метил-3-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-дигидроизохинолин-1(2Н)-он 82
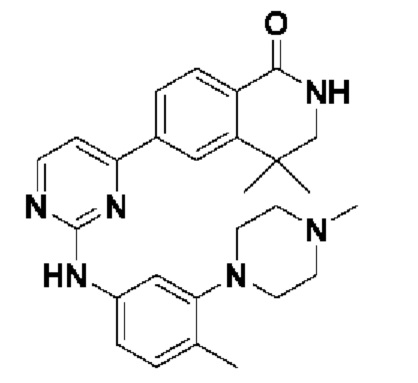
МС (ИЭР)m/z(M+1)+: 457,27.
Пример 83:
6-(5-фтор-2-((4-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 83
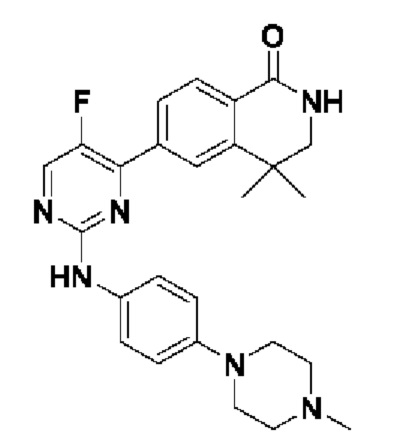
МС (ИЭР)m/z(M+1)+: 461,25.
Пример 84:
6-(2-((3-(4-этилпиперазин-1-ил)-4-фторфенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 84
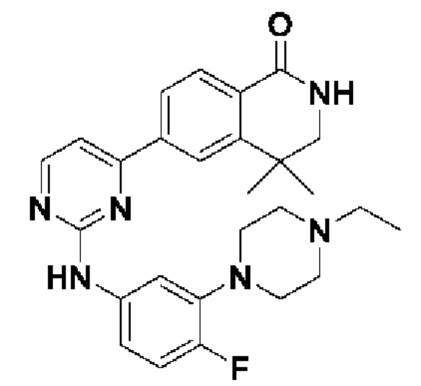
МС (ИЭР)m/z(M+1)+: 475,26.
Пример 85:
6-(2-((4-фтор-3-(4-изопропилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 85
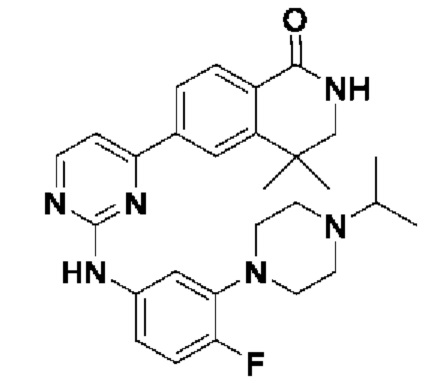
MC (ИЭР)m/z(M+1)+: 489,28.
Пример 86:
6-(2-((3-(4-этилпиперазин-1-ил)-4-метилфенил)амино)пиримидин-4-ил)-4,4-димет ил-3,4-дигидроизохинолин-1(2Н)-он 86

МС (ИЭР)m/z(M+1)+: 471,29.
Пример 87:
6-(2-((3-(4-изопропилпиперазин-1-ил)-4-метилфенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 87

МС (ИЭР )m/z(M+1)+: 485,30.
Пример 88:
6-(5-хлор-2-((4-(4-метилпиперазин-1-ил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 88

МС (ИЭР)m/z(M+1)+: 477,22.
Пример 89:
6-(5-фтор-2-((4-((метилсульфонил)метил)пиридин-2-ил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 89
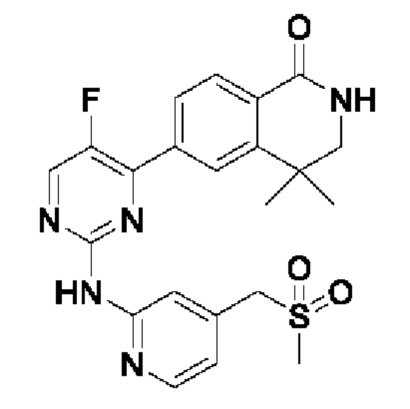
MC (ИЭР)m/z(M+1)+: 456,15.
Пример 90:
6-(5-хлор-2-((4-((метилсульфонил)метил)пиридин-2-ил)амино)пиримидин-4-ил)-4, 4-диметил-3,4-дигидроизохинолин-1(2Н)-он 90
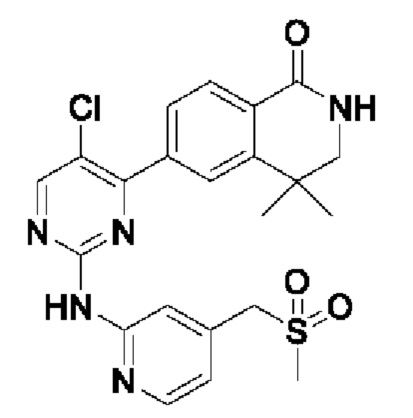
МС (ИЭР)m/z(M+1)+: 472,12.
Пример 91:
4,4-диметил-6-(5-метил-2-((4-((метилсульфонил)метил)пиридин-2-ил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 91
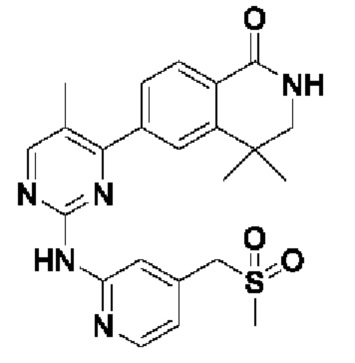
МС (ИЭР)m/z(M+1)+: 452,18.
Пример 92:
4,4-диметил-6-(2-((4-((метилсульфонил)метил)пиридин-2-ил)амино) -5-(трифторметил)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 92

МС (ИЭР )m/z(M+1)+: 506,15.
Пример 93:
6-(5-фтор-2-((4-((8-метилсульфонимид)метил)пиридин-2-ил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 93
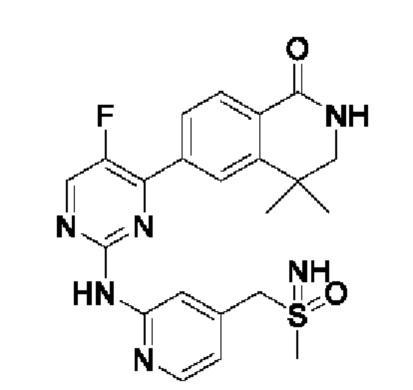
MC (ИЭР)m/z(M+1)+: 455,17.
Пример 94:
6-(5-хлор-2-((4-((S-метилсульфонимид)метил)пиридин-2-ил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 94
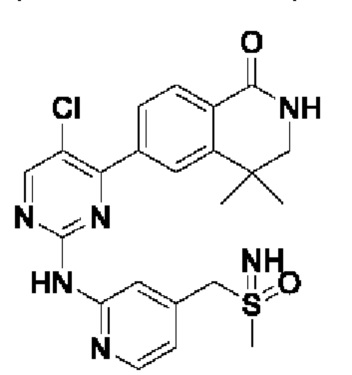
МС (ИЭР)m/z(M+1)+: 471,14.
Пример 95:
4,4-диметил-6-(5-метил-2-((4-((S-метилсульфонимид)метил)пиридин-2-ил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин- 1(2Н)-он 95
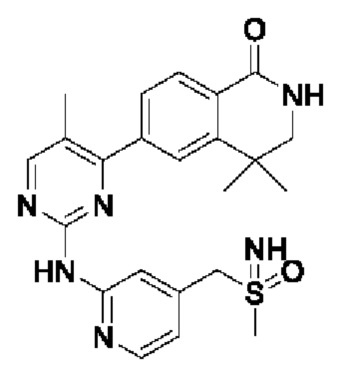
МС (ИЭР)m/z(M+1)+: 451,19.
Пример 96:
(18,ЗИ)-3-ацетиламино-К-(5-хлор-4-(4,4-диметил-1 -оксо-1,2,3,4-тетрагидроизохин олин-6-ил)пиридин-2-ил)циклогексил-1-формамид 96
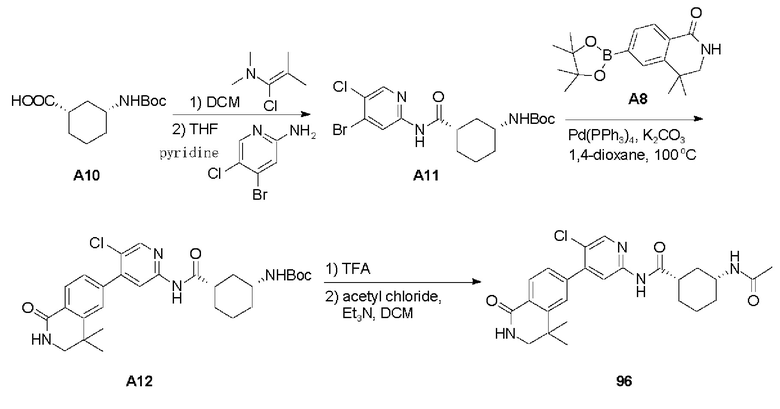
Трет-бутил-((1R,3S)-3-((4-бром-5-хлорпиридин-2-ил)карбамоил)циклогексил) карбамат (A11): соединение А10 (1,0 г, 4,11 ммоль) растворяли в дихлорметане, а затем добавляли по каплям 1-хлор-N,N,2-триметилпропениламин (0,82 г, 6,17 ммоль, 1,5 экв.) на ледяной бане. Реакционную смесь непрерывно перемешивали при 0°С в течение 30 минут. Затем добавляли 2-амино-4-бром-5-хлорпиридин (0,68 г, 3,28 ммоль, 0,8 эквив.) и пиридин (0,32 г, 4,11 ммоль, 1 эквив.) в растворе тетрагидрофурана, и полученный продукт перемешивали при комнатной температуре в течение 3 часов. Реакцию останавливали после того, как мониторинг с помощью ТСХ показал отсутствие исходного материала. Добавляли насыщенный раствор карбоната натрия, экстрагировали этилацетатом, сушили над безводным сульфатом натрия, фильтровали, концентрировали, а затем загружали на силикагель для колоночной хроматографии (система элюентов: ПЭ/ЭА=3:1), в результате чего получали твердое вещество белого цвета All (1,2 г, 68%).
Трет-бутил-((1R,3S)-3-((5-хлор-4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизох инолин-6-ил)пиридин-2-ил)карбамоил)циклогексил)карбамат (А12): А11 (800 мг, 1,85 ммоль, 1,0 экв.) растворяли в 1,4-диоксане (10 мл), затем добавляли А8 (613 мг, 2,03 ммоль, 1,1 экв.), карбонат калия (0,51 г, 3,7 ммоль, 2 экв.) и Pd(PPh3)4 (0,21 г, 0,185 ммоль, 0,1 экв.) и перемешивали при 100°С в течение 4 часов. ТСХ показала, что реакция была завершена. Реакционную систему загружали на необработанный силикагель и разделяли с помощью колоночной хроматографии (система элюентов: ДХМ/ЭА=3:1), в результате чего получали целевое соединение А12 (585 мг, 60%).
(18,3R)-3-ацетиламино-N-(5-хлор-4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроиз охинолин-6-ил)пиридин-2-ил)циклогексил-1-формамид (96): Соединение А12 (100 мг, 0,19 ммоль) растворяли в дихлорметане (2 мл), добавляли по каплям трифторуксусную кислоту (2 мл) и перемешивали при комнатной температуре в течение получаса. После концентрирования полученный продукт нейтрализовали насыщенным бикарбонатом натрия до рН=10, и экстрагировали дихлорметаном, сушили над безводным сульфатом натрия, фильтровали и концентрировали с получением масла светло-желтого цвета, которое непосредственно использовали на следующей стадии (60 мг). Продукт, полученный на предыдущей стадии, растворяли в дихлорметане, добавляли триэтиламин (21 мг, 0,21 ммоль), а затем добавляли по каплям ацетилхлорид (16 мг, 0,21 ммоль) на ледяной бане. Реакцию останавливали после того, как ТСХ показывала завершение реакции. Полученный продукт концентрировали для колоночной хроматографии (система элюентов: ДХМ/МеОН=30:1), в результате чего получали целевое соединение 96 (твердое вещество белого цвета, 30 мг, 46%). МС: (М+1) 469,20. 1Н ЯМР (500 МГц, ДМСО-d6) δ 10,74 (s, 1H), 8,49 (s, 1H), 8,18 (s, 1H), 8,08 (d, J=3,1 Гц, 1H), 7,98 (d, J=7,9 Гц, 1H), 7,78 (d, J=7,9 Гц, 1H), 7,50 (d, J=1,7 Гц, 1H), 7,44 (dd, J=7,9, 1,7 Гц, 1H), 3,60-3,51 (m, 1H), 3,23 (d, J=3,0 Гц, 2Н), 2,64-2,60 (m, 1H), 1,88 (d, J=12,4 Гц, 1H), 1,77 (s, 6Н), 1,31-1,24 (m, 9Н), 1,07 (q, J=11,3, 10,8 Гц, 1H).
Соединения из следующих примеров 97, 98, 102 и 107 синтезировали аналогично примеру 96, если не указано иное.
Пример 97:
(18,3R)-3-ацетиламино-N-(5-хлор-4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохин олин-6-ил)пиримидин-2-ил)циклогексил-1-формамид 97
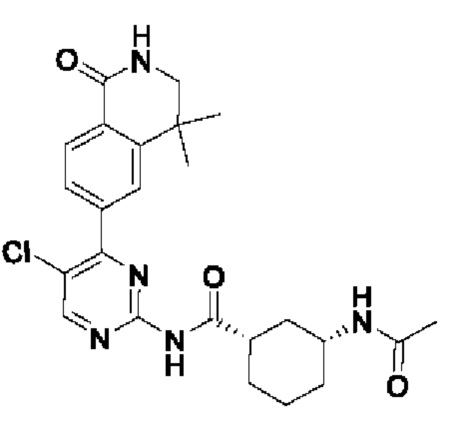
МС (ИЭР)m/z(М+1)+: 470,20.
Пример 98:
(18,3R)-3-ацетиламино-N-(4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)-5-метилпиримидин-2-ил)циклогексил-1-формамид 98
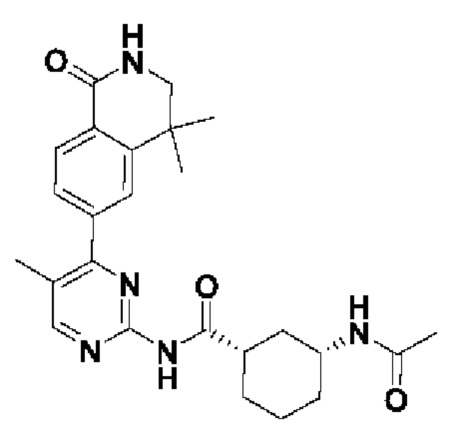
МС (ИЭР)m/z(M+1)+: 450,25.
Пример 99:
6-(5-хлор-2-((4-(метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 99
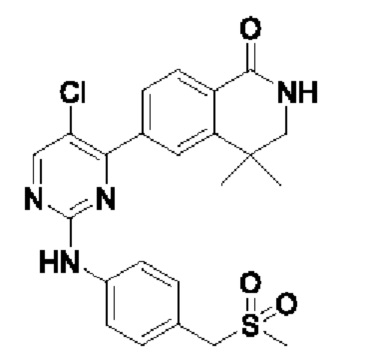
МС (ИЭР)m/z(М+1)+: 471,12.
Пример 100:
6-(5-фтор-2-((4-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-4,4-диметил-3,4-дигидроизохинолин-1(2Н)-он 100
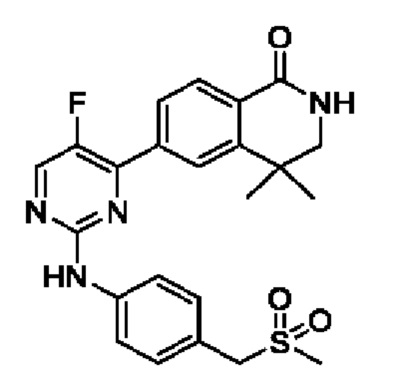
МС (ИЭР)m/z(M+1)+: 455,15.
Пример 101:
5-(2-((2,4-дифтор-5-((метилсульфонил)метил)фенил)амино)пиримидин-4-ил)-3,3-диметилизоиндол-1-он 101
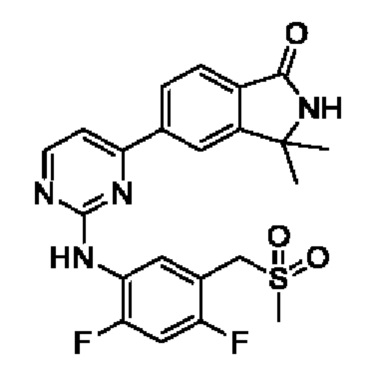
МС (ИЭР)m/z(M+1)+: 459,13.
Пример 102: (18,3R)-3-ацетиламино-N-(5-хлор-4-(3,3-диметил-1-оксоиндолин-5-ил)пиридин-2-ил)циклогексан-1-формамид 102
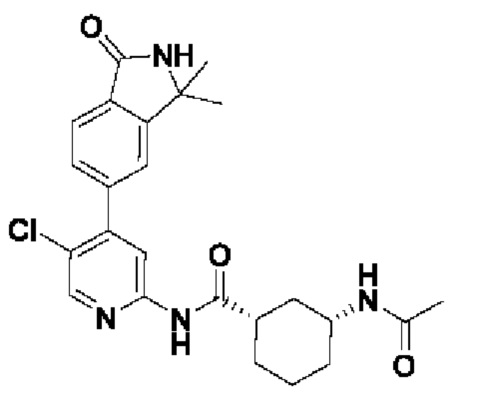
МС (ИЭР)m/z(М+1)+: 455,18.
Пример 103:
(S)-4,4-диметил-6-(2-((1-(метансульфонил)пиперидин-3-ил)амино)пиримидин-4-и л)-3,4-дигидроизохинолин-1(2Н)-он 103

(S)-3-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)амино)пиперидин-1-карбоновой кислоты трет-бутиловый эфир (А14): А9 (100 мг, 0,35 ммоль), А13 (105 мг, 0,52 ммоль) и ДИЭА (90 мг, 0,7 ммоль) растворяли в втор-бутаноле (2 мл), и смеси позволяли реагировать при 130°С в течение ночи. После завершения реакции, что показала ЖХ/МС, реакционную систему загружали на необработанный силикагель, и А14 (70 мг, 44%) разделяли с помощью колоночной хроматографии.
(S)-4,4-диметил-6-(2-(пиперидин-3-иламино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он (А15): А14 (70 мг) растворяли в ДХМ (3 мл), добавляли трифторуксусную кислоту (ТФУ) (1 мл) и перемешивали при комнатной температуре. После завершения реакции, что показала ЖХ/МС, полученный продукт нейтрализовали насыщенным бикарбонатом натрия до щелочного рН, а затем экстрагировали этилацетатом. Органическую фазу сушили, концентрировали, и остаток разделяли с помощью колоночной хроматографии, в результате чего получали А15 (38 мг, 73%).
(S)-4,4-диметил-6-(2-((1-(метансульфонил)пиперидин-3-ил)амино)пиримидин -4-ил)-3,4-дигидроизохинолин-1(2Н)-он (103): А15 (38 мг, 0,11 ммоль) растворяли в ДХМ (2 мл) и добавляли метансульфонилхлорид (18 мг, 0,16 ммоль) на ледяной бане. После завершения реакции, что показала ЖХ/МС, полученный продукт концентрировали, и остаток разделяли с помощью колоночной хроматографии с получением 103 (22 мг, 48%). 1Н ЯМР (500 МГц, ДМСО-d6) δ 8,43 (d, J=5,1 Гц, 1H), 8,11-7,94 (m, 4Н), 7,32 (d, J=7,3 Гц, 1H), 7,27 (d, J=5,2 Гц, 1H), 3,99-3,94 (m, 1H), 3,47 (s, 1H), 3,21-3,20 (m, 2Н), 2,87 (s, 3Н), 2,75 (td, J=11,3, 2,8 Гц, 1H), 2,56 (t, J=10,3 Гц, 1H), 1,97-1,85 (m, 2Н), 1,62-1,51 (m, 2Н), 1,34 (d, J=6,0 Гц, 6Н).
Соединения из следующих примеров 104 - 106 синтезировали аналогично примеру 103, если не указано иное.
Пример 104:
(R)-4,4-диметил-6-(2-(((1-(метилсульфонил)пиперидин-3-ил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 104
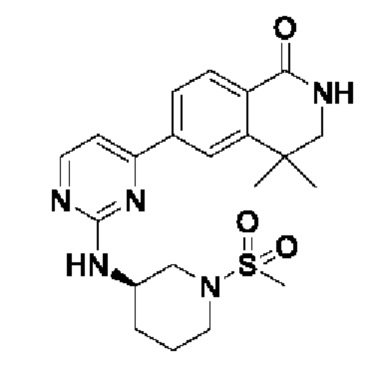
МС (ИЭР)m/z(M+1)+: 430,19.
Пример 105:
4,4-диметил-6-(2-((1-(метилсульфонил)пиперидин-4-ил)амино)пиримидин-4-ил)-3,4-дигидроизохинолин-1(2Н)-он 105
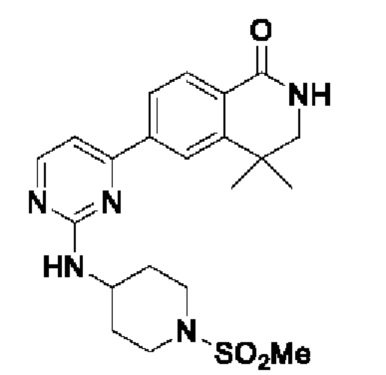
МС (ИЭР)m/z(М+1)+: 430,19.
Пример 106:
2-(1R,4R-4-((4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиримидин-2-ил)амино)циклогексил)уксусная кислота 106
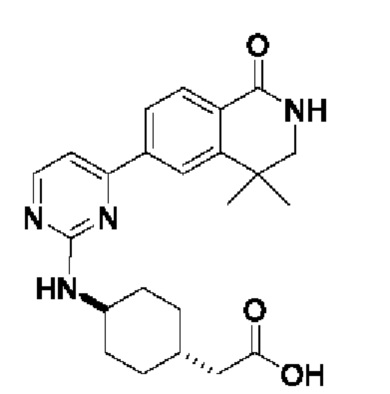
MC (ИЭР)m/z(M+1)+: 409,22.
Пример 107:
(R)-N-(5-хлор-4-(4,4-диметил-1-оксо-1,2,3,4-тетрагидроизохинолин-6-ил)пиридин-2-ил)пиперидин-3-формамид 107
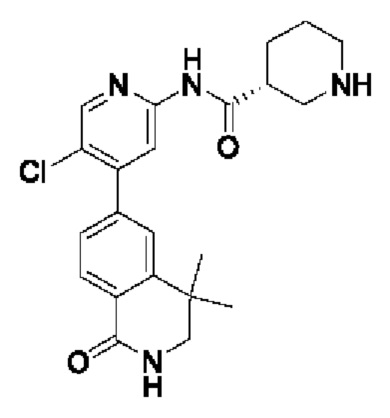
МС (ИЭР)m/z(M+1)+: 413,17.
Пример 108:
Влияние ингибитора CDK9 на рост раковых клеток
Посредством тестирования влияния ингибитора CDK9 на рост раковых клеток, авторы настоящего изобретения оценили селективность соединений в отношении ингибирования пролиферации раковых клеток.
В этом примере выбирали следующее: линии клеток острого миелоидного лейкоза OCI-AML-3, MV4-11, MOLM13, MOLM14, клетку гистиоцитарной лимфомы U-937, клетку хронического миелоидного лейкоза человека К562, клетку колоректального рака человека НСТ116, DLD1, клетку гранулезоклеточной опухоли яичника человека COV434, линию клеток рака печени человека HepG2, клетку лимфомы WSU-DLCL2, клетку рака шейки матки HeLa, клетку стромальной опухоли желудочно-кишечного тракта GIST-T1 (все вышеуказанные клетки были приобретены у Nanjing Cobioer), лекарственно-устойчивый штамм MOLM13 - MOLM13 BR1, полученный путем длительного лечения ингибитором CDK9 BAY1251152 (приобретен у МСЕ, Китай), и лекарственно-устойчивый штамм HepG2 - HepG2 KI С20-1, полученный путем нокина с помощью технологии CRISPR/Cas9 с применением следующего способа конструирования: Клетки HepG2 трансфицировали плазмидой направляющая РНК-РХ459, а затем получали клетки HepG2 CDK9 KI путем скрининга на пуриномицине и скрининга на BAY1251152, что затем позволило получить моноклональные клетки HepG2 KI С20-1 после скрининга на моноклональные клетки; мутации, придающие устойчивость к CDK9, детектировали путем секвенирования.
В указанном примере к вышеуказанным клеткам добавляли, соответственно, различные концентрации (0,000508 мкМ, 0,00152 мкМ, 0,00457 мкМ, 0,0137 мкМ, 0,0411 мкМ, 0,123 мкМ, 0,370 мкМ, 1,11 мкМ, 3,33 мкМ, 10 мкМ) соединений в соответствии с настоящим изобретением и контрольных соединений Динациклиба, JSH-009 и BAY1251152 (все приобретены у МСЕ, Китай) и инкубировали в течение 72 часов, а затем определяли количество живых клеток путем количественного определения АТФ в живых клетках с использованием набора для тестирования жизнеспособности клеток с помощью хемилюминесценции Cell Titer-Glo® (Promega, США), которое использовали в качестве основы для расчета GI50. Результаты показаны в таблицах 1-3.
В указанном тесте установили, что соединения в соответствии с настоящим изобретением оказывают значительное ингибирующее действие на различные линии раковых клеток. В таблице 1 и ее продолжении показано, что их ингибирующее действие сравнимо с таковым у контрольного соединения -пан-ингибитора CDK - динациклиба и селективного ингибитора CDK9 - JSH-009; антипролиферативная активность большинства соединений в отношении клеток сравнима или даже лучше таковой у селективного ингибитора CDK9 -BAY 1251152. Кроме того, в таблице 2 показаны значительные антипролиферативные действия в отношении лекарственно-устойчивого штамма, который был получен путем обработки BAY1251152 клеток острого миелоидного лейкоза MOLM13. Таким образом, соединения в соответствии с настоящим изобретением демонстрируют ингибирующие действия, которые преодолевают лекарственную устойчивость. В таблице 3 показано, что результаты анализа на лекарственно-устойчивом штамме клеток рака печени HepG2 показали, что соединения в соответствии с настоящим изобретением могут преодолевать лекарственную устойчивость, в то время как очевидна лекарственная устойчивость к BAY1251152.
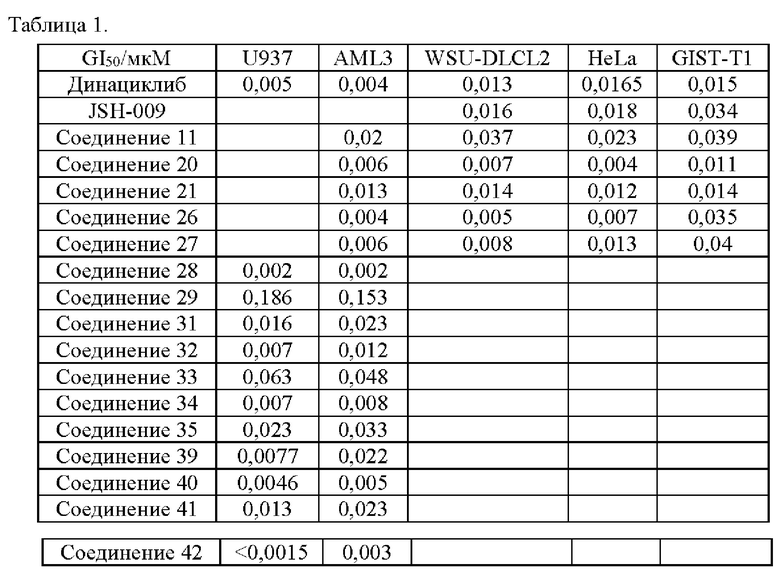
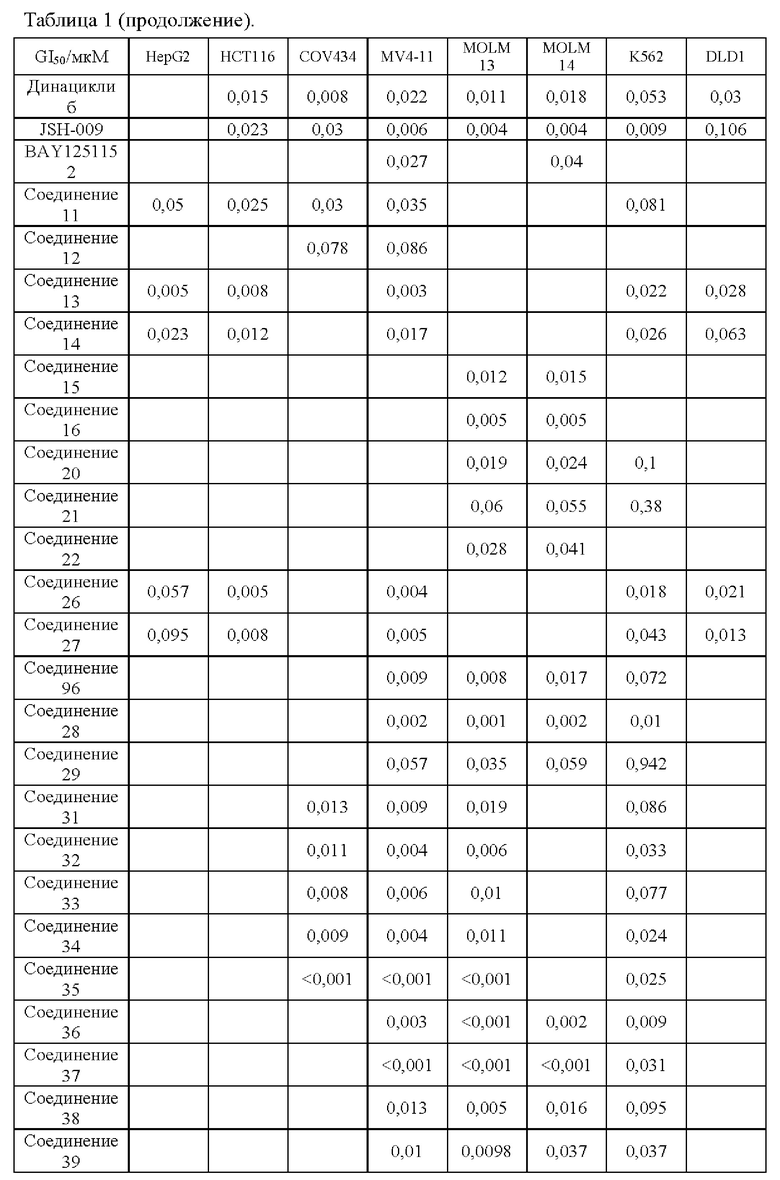
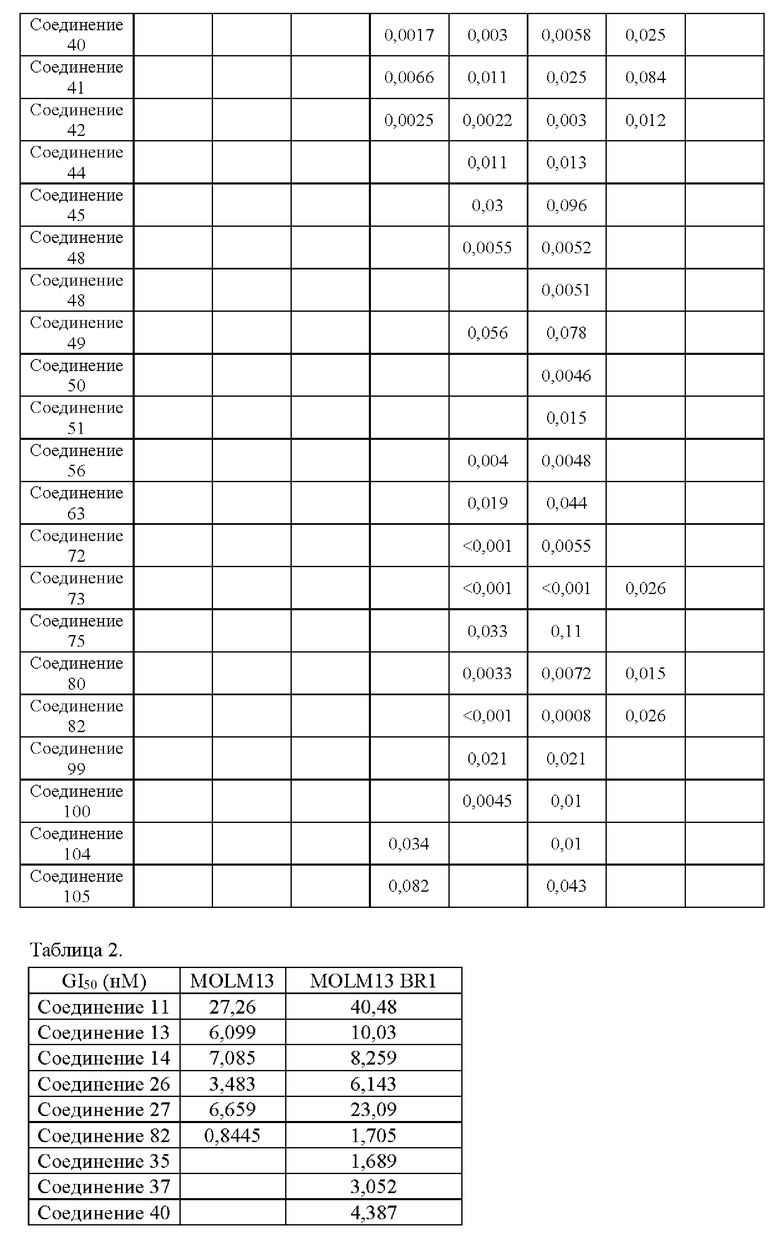
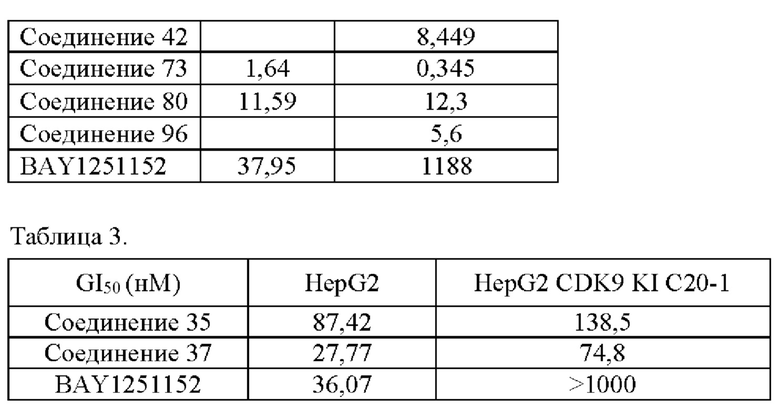
Пример 109. Детектирование активности связывания соединения и CDK9
Плазмиду системы разделенной люциферазы конструировали с помощью технологии молекулярного клонирования. N-концевой домен (NLuc) и С-концевой домен (CLuc) люциферазы, соответственно, клонировали и вставляли в вектор PCDNA3 для конструирования векторов NLuc-PCDNA3 и CLuc-PCDNA3, а сайты множественного клонирования были сохранены на обоих концах последовательности. Затем CDC37 и CDK9 клонировали в соответствующие векторы для конструирования векторов C37-CL и CDK9-NL. Последовательность плазмиды C37-CL представлена в SEQ ID NO: 1. Последовательность плазмиды CDK9-NL представлена в SEQ ID NO: 2.
НЕК-293Т (приобретены у АТСС, США) высевали в чашку для культивирования клеток диаметром 10 см и ждали, пока плотность клеток достигнет 70%, перед применением. 2 мкг плазмиды C37-CL (SEQ ID NO: 1) и 2 мкг плазмиды CDK9-NL (SEQ ID NO: 2) добавляли в 1 мл Opti-MEM (продукт №2120763, приобретали у Gibco, США), затем добавляли 6 мкл реагента для трансфекции (продукт №20200918, приобретали у HanBio, Китай), а затем смешивали для применения. Смешанный комплекс для трансфекции добавляли в чашку для культивирования клеток диаметром 10 см и культивировали при 37°С и 5% СО2 в течение 24 часов. Через 24 часа клетки НЕК-293Т расщепляли трипсином. После подсчета трансфицированные клетки помещали в 96-луночный белый планшет для культивирования клеток Corning (приобретенный у Corning, США) в объеме 100 мкл, 5000 клеток/лунку. Через 12 часов среду удаляли из 96-луночного планшета и добавляли 100 мкл культуральной среды, содержащей соответствующую концентрацию тестируемого соединения, и культивировали непрерывно в течение 12 часов. Через 12 часов в каждую лунку добавляли 20 мкл реагента для определения активности люциферазы Luciferase-Glo (приобретенного у Promega, США). После смешивания детектировали значение флуоресценции с помощью устройства для прочтения микропланшетов. Значение относительной активности IC50 вычисляли по следующей формуле: относительная активность=(значение флуоресценции исследуемого лекарственного средства - оновое значение)/(значение флуоресценции группы ДМСО - фоновое значение) х 100%. Результаты исследования показали, что соединения в соответствии с настоящим изобретением обладают сильной активностью связывания с CDK9.
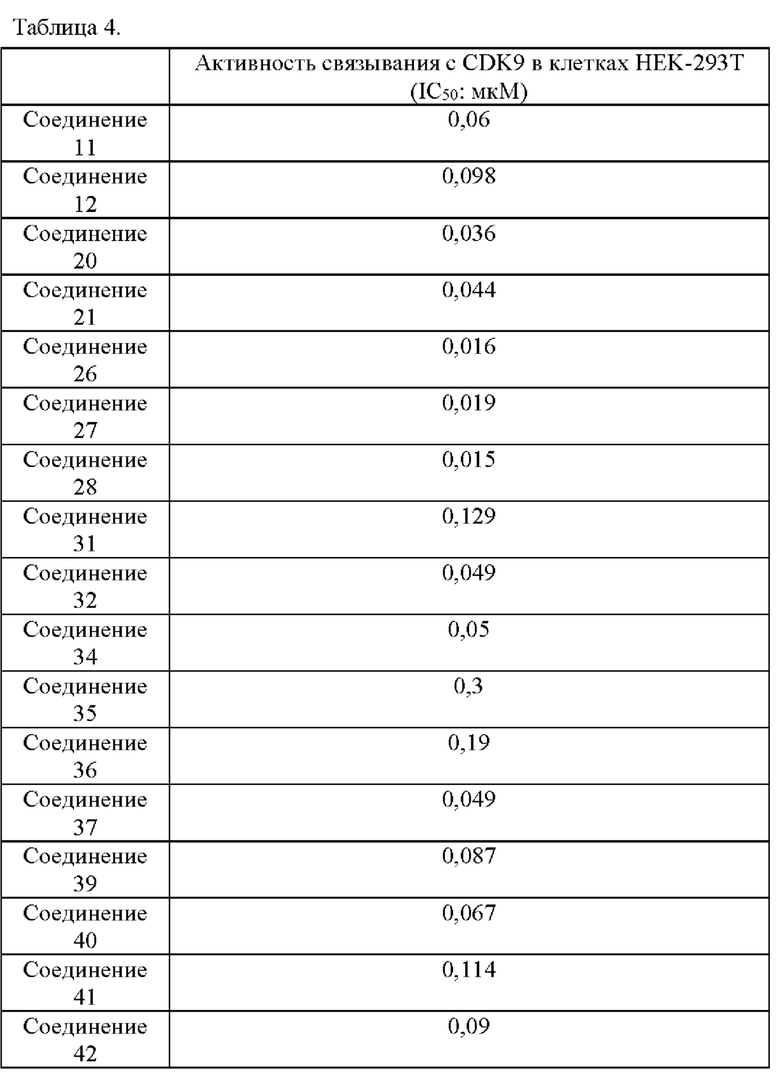
Пример ПО. Анализ ферментативной активности ингибирования белка CDK9 in vitro
Разведенные в ДМСО соединения и контрольные соединения Динациклиб, JSH-009, BAY-1211152, AZD4573 (все приобретены у МСЕ, Китай) смешивали с детектируемым белком CDK9/циклин T1 (Invitrogen, США), мутантным белком CDK9-L156F мут/циклин Т1 (эта мутация соответствует мутации в HepG2 KI С20-1, которые были сконструированы, как описано в примере 108) и инкубировали при комнатной температуре в течение 30 минут.Добавляли смесь пептидных субстратов для киназ (Invitrogen, США) и 4 х АТФ для смешивания, и смешанную систему переносили в 384-луночный непрозрачный белый планшет для ведения реакции при комнатной температуре в течение 1 часа. Добавляли 5 мкл проявляющего раствора (Invitrogen, США) и проводили реакцию при комнатной температуре в течение 1 часа, и, наконец, к реакционной смеси добавляли стоп-реагент (Invitrogen, США), чтобы остановить реакцию; значение флуоресценции считывали с использованием спектрофотометра для прочтения микропланшетов MD SpectraMax I3X (Molecular Devices, США). Значения IC50 для соединений в соответствии с настоящим изобретением для тестируемого белка СОК9/циклин Т1 и мутантного белка CDK9 - CDK9-L156F мут/циклин Т1 -рассчитывали путем построения графика с использованием Prism 5.0 (GraphPad Software, Сан-Диего, Калифорния) на основании считанного значения флуоресценции, и они представлены в таблице 5 и таблице 6 ниже. Результаты показали, что соединения в соответствии с настоящим изобретением оказывают значительное ингибирующее действие на CDK9 и ее мутированную форму: для белка СОК9/циклин Т1 дикого типа они продемонстрировали превосходящее или сопоставимое действие по сравнению с контрольными соединениями, в то время как для мутантного белка CDK9 - CDK9-L156F мут/циклин Т1 - их ингибирующее действие значительно превосходило ингибирующее действие контрольного соединения BAY1251152.
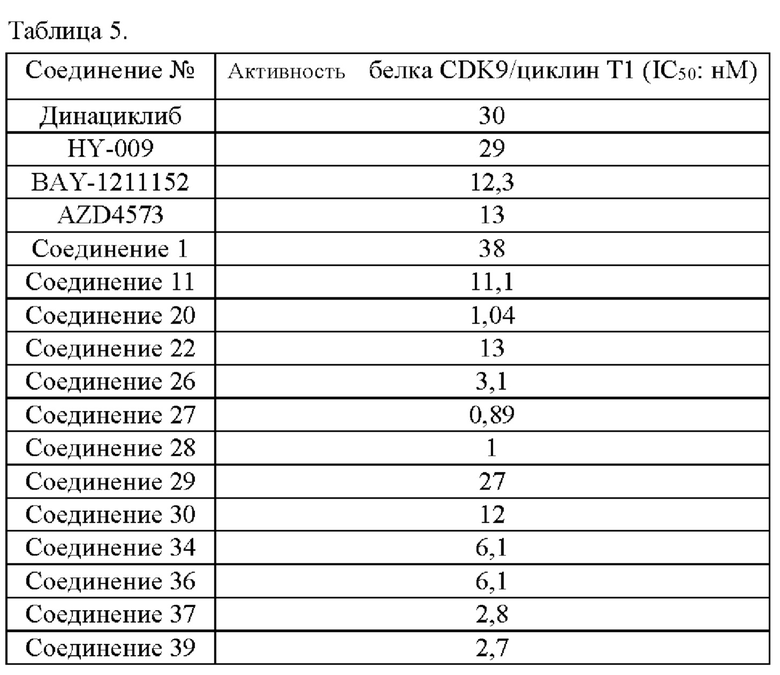
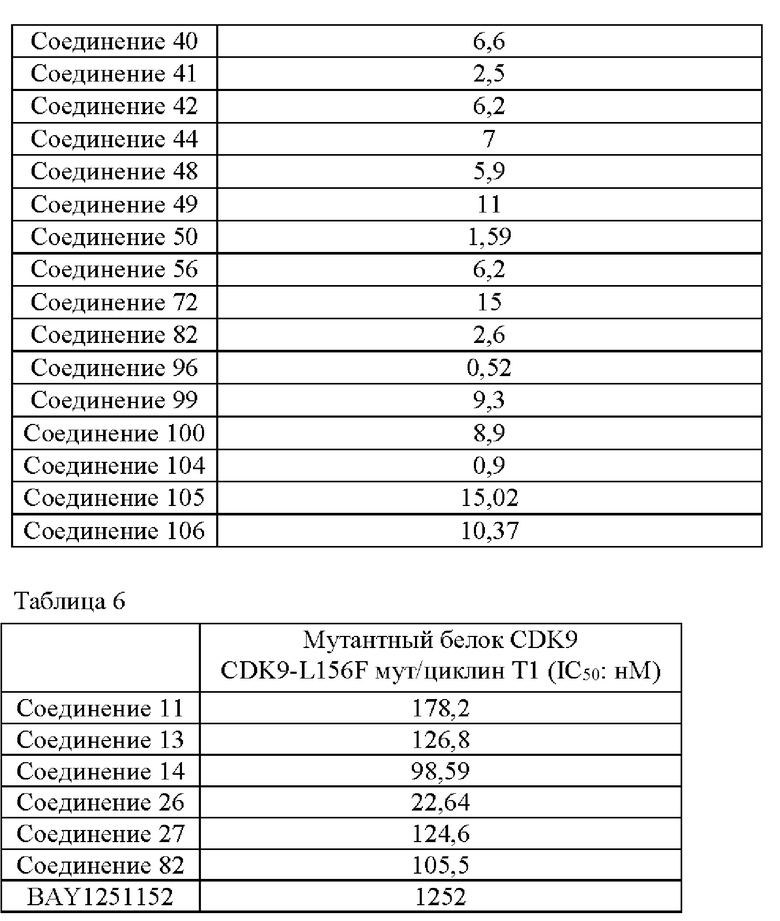
Промышленная применимость
В соответствии с настоящим изобретением предложен ингибитор киназы CDK9, который можно применять для ингибирования активности CDK9 и/или его мутированной киназы и для лечения или предотвращения заболеваний, связанных с активностью CDK9 и/или ее мутациями или опосредованных ими. Таким образом, можно получить соответствующие лекарственные средства, пригодные для промышленного применения.
Хотя изобретение подробно описано в настоящем документе, оно не ограничивается настоящим описанием. Специалисты в данной области техники могут вносить модификации в соответствии с принципом настоящего изобретения. Следовательно, следует понимать, что все модификации, внесенные в соответствии с принципом настоящего изобретения, входят в объем охраны настоящего изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> HEFEI INSTITUTES OF PHYSICAL SCIENCE, CHINESE ACADEMY OF SCIENCES
<120> Производные дигидроизохинолинона и изоиндолинона и их применение
<130> CPL212071
<150> CN202011308146.4
<151> 2020-11-20
<160> 2
<170> SIPOSequenceListing 1.0
<210> 1
<211> 6856
<212> ДНК
<213> Искусственная последовательность
<400> 1
gacggatcgg gagatctccc gatcccctat ggtgcactct cagtacaatc tgctctgatg 60
ccgcatagtt aagccagtat ctgctccctg cttgtgtgtt ggaggtcgct gagtagtgcg 120
cgagcaaaat ttaagctaca acaaggcaag gcttgaccga caattgcatg aagaatctgc 180
ttagggttag gcgttttgcg ctgcttcgcg atgtacgggc cagatatacg cgttgacatt 240
gattattgac tagttattaa tagtaatcaa ttacggggtc attagttcat agcccatata 300
tggagttccg cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc 360
cccgcccatt gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc 420
attgacgtca atgggtggag tatttacggt aaactgccca cttggcagta catcaagtgt 480
atcatatgcc aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt 540
atgcccagta catgacctta tgggactttc ctacttggca gtacatctac gtattagtca 600
tcgctattac catggtgatg cggttttggc agtacatcaa tgggcgtgga tagcggtttg 660
actcacgggg atttccaagt ctccacccca ttgacgtcaa tgggagtttg ttttggcacc 720
aaaatcaacg ggactttcca aaatgtcgta acaactccgc cccattgacg caaatgggcg 780
gtaggcgtgt acggtgggag gtctatataa gcagagctct ctggctaact agagaaccca 840
ctgcttactg gcttatcgaa attaatacga ctcactatag ggagacccaa gctggctagc 900
gccaccatgg tggactacag cgtgtgggac cacattgagg tgtctgatga tgaagacgag 960
acgcacccca acatcgacac ggccagtctc ttccgctggc ggcatcaggc ccgggtggaa 1020
cgcatggagc agttccagaa ggagaaggag gaactggaca ggggctgccg cgagtgcaag 1080
cgcaaggtgg ccgagtgcca gaggaaactg aaggagctgg aggtggccga gggcggcaag 1140
gcagagctgg agcgcctgca ggccgaggca cagcagctgc gcaaggagga gcggagctgg 1200
gagcagaagc tggaggagat gcgcaagaag gagaagagca tgccctggaa cgtggacacg 1260
ctcagcaaag acggcttcag caagagcatg gtaaatacca agcccgagaa gacggaggag 1320
gactcagagg aggtgaggga gcagaaacac aagaccttcg tggaaaaata cgagaaacag 1380
atcaagcact ttggcatgct tcgccgctgg gatgacagcc aaaagtacct gtcagacaac 1440
gtccacctgg tgtgcgagga gacagccaat tacctggtca tttggtgcat tgacctagag 1500
gtggaggaga aatgtgcact catggagcag gtggcccacc agacaatcgt catgcaattt 1560
atcctggagc tggccaagag cctaaaggtg gacccccggg cctgcttccg gcagttcttc 1620
actaagatta agacagccga tcgccagtac atggagggct tcaacgacga gctggaagcc 1680
ttcaaggagc gtgtgcgggg ccgtgccaag ctgcgcatcg agaaggccat gaaggagtac 1740
gaggaggagg agcgcaagaa gcggctcggc cccggcggcc tggaccccgt cgaggtctac 1800
gagtccctcc ctgaggaact ccagaagtgc ttcgatgtga aggacgtgca gatgctgcag 1860
gacgccatca gcaagatgga ccccaccgac gcaaagtacc acatgcagcg ctgcattgac 1920
tctggcctct gggtccccaa ctctaaggcc agcgaggcca aggagggaga ggaggcaggt 1980
cctggggacc cattactgga agctgttccc aagacgggcg atgagaagga tgtcagtgtg 2040
aagcttggta ccgagctcgg atccggtggc ggagggagcg gtggcggagg gagcggcggc 2100
cgcaagcccg acgtcgtcca gattgtccgc aactacaacg cctaccttcg ggccagcgac 2160
gatctgccta agatgttcat cgagtccgac cctgggttct tttccaacgc tattgtcgag 2220
ggagctaaga agttccctaa caccgagttc gtgaaggtga agggcctcca cttcagccag 2280
gaggacgctc cagatgaaat gggtaagtac atcaagagct tcgtggagcg cgtgctgaag 2340
aacgagcaga gtctagaggc tgactacaaa gaccatgacg gtgattataa agatcatgac 2400
atcgactaca aggatgacga tgacaagtga gtttaaaccc gctgatcagc ctcgactgtg 2460
ccttctagtt gccagccatc tgttgtttgc ccctcccccg tgccttcctt gaccctggaa 2520
ggtgccactc ccactgtcct ttcctaataa aatgaggaaa ttgcatcgca ttgtctgagt 2580
aggtgtcatt ctattctggg gggtggggtg gggcaggaca gcaaggggga ggattgggaa 2640
gacaatagca ggcatgctgg ggatgcggtg ggctctatgg cttctgaggc ggaaagaacc 2700
agctggggct ctagggggta tccccacgcg ccctgtagcg gcgcattaag cgcggcgggt 2760
gtggtggtta cgcgcagcgt gaccgctaca cttgccagcg ccctagcgcc cgctcctttc 2820
gctttcttcc cttcctttct cgccacgttc gccggctttc cccgtcaagc tctaaatcgg 2880
gggctccctt tagggttccg atttagtgct ttacggcacc tcgaccccaa aaaacttgat 2940
tagggtgatg gttcacgtag tgggccatcg ccctgataga cggtttttcg ccctttgacg 3000
ttggagtcca cgttctttaa tagtggactc ttgttccaaa ctggaacaac actcaaccct 3060
atctcggtct attcttttga tttataaggg attttgccga tttcggccta ttggttaaaa 3120
aatgagctga tttaacaaaa atttaacgcg aattaattct gtggaatgtg tgtcagttag 3180
ggtgtggaaa gtccccaggc tccccagcag gcagaagtat gcaaagcatg catctcaatt 3240
agtcagcaac caggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca 3300
tgcatctcaa ttagtcagca accatagtcc cgcccctaac tccgcccatc ccgcccctaa 3360
ctccgcccag ttccgcccat tctccgcccc atggctgact aatttttttt atttatgcag 3420
aggccgaggc cgcctctgcc tctgagctat tccagaagta gtgaggaggc ttttttggag 3480
gcctaggctt ttgcaaaaag ctcccgggag cttgtatatc cattttcgga tctgatcaag 3540
agacaggatg aggatcgttt cgcatgattg aacaagatgg attgcacgca ggttctccgg 3600
ccgcttgggt ggagaggcta ttcggctatg actgggcaca acagacaatc ggctgctctg 3660
atgccgccgt gttccggctg tcagcgcagg ggcgcccggt tctttttgtc aagaccgacc 3720
tgtccggtgc cctgaatgaa ctgcaggacg aggcagcgcg gctatcgtgg ctggccacga 3780
cgggcgttcc ttgcgcagct gtgctcgacg ttgtcactga agcgggaagg gactggctgc 3840
tattgggcga agtgccgggg caggatctcc tgtcatctca ccttgctcct gccgagaaag 3900
tatccatcat ggctgatgca atgcggcggc tgcatacgct tgatccggct acctgcccat 3960
tcgaccacca agcgaaacat cgcatcgagc gagcacgtac tcggatggaa gccggtcttg 4020
tcgatcagga tgatctggac gaagagcatc aggggctcgc gccagccgaa ctgttcgcca 4080
ggctcaaggc gcgcatgccc gacggcgagg atctcgtcgt gacccatggc gatgcctgct 4140
tgccgaatat catggtggaa aatggccgct tttctggatt catcgactgt ggccggctgg 4200
gtgtggcgga ccgctatcag gacatagcgt tggctacccg tgatattgct gaagagcttg 4260
gcggcgaatg ggctgaccgc ttcctcgtgc tttacggtat cgccgctccc gattcgcagc 4320
gcatcgcctt ctatcgcctt cttgacgagt tcttctgagc gggactctgg ggttcgaaat 4380
gaccgaccaa gcgacgccca acctgccatc acgagatttc gattccaccg ccgccttcta 4440
tgaaaggttg ggcttcggaa tcgttttccg ggacgccggc tggatgatcc tccagcgcgg 4500
ggatctcatg ctggagttct tcgcccaccc caacttgttt attgcagctt ataatggtta 4560
caaataaagc aatagcatca caaatttcac aaataaagca tttttttcac tgcattctag 4620
ttgtggtttg tccaaactca tcaatgtatc ttatcatgtc tgtataccgt cgacctctag 4680
ctagagcttg gcgtaatcat ggtcatagct gtttcctgtg tgaaattgtt atccgctcac 4740
aattccacac aacatacgag ccggaagcat aaagtgtaaa gcctggggtg cctaatgagt 4800
gagctaactc acattaattg cgttgcgctc actgcccgct ttccagtcgg gaaacctgtc 4860
gtgccagctg cattaatgaa tcggccaacg cgcggggaga ggcggtttgc gtattgggcg 4920
ctcttccgct tcctcgctca ctgactcgct gcgctcggtc gttcggctgc ggcgagcggt 4980
atcagctcac tcaaaggcgg taatacggtt atccacagaa tcaggggata acgcaggaaa 5040
gaacatgtga gcaaaaggcc agcaaaaggc caggaaccgt aaaaaggccg cgttgctggc 5100
gtttttccat aggctccgcc cccctgacga gcatcacaaa aatcgacgct caagtcagag 5160
gtggcgaaac ccgacaggac tataaagata ccaggcgttt ccccctggaa gctccctcgt 5220
gcgctctcct gttccgaccc tgccgcttac cggatacctg tccgcctttc tcccttcggg 5280
aagcgtggcg ctttctcata gctcacgctg taggtatctc agttcggtgt aggtcgttcg 5340
ctccaagctg ggctgtgtgc acgaaccccc cgttcagccc gaccgctgcg ccttatccgg 5400
taactatcgt cttgagtcca acccggtaag acacgactta tcgccactgg cagcagccac 5460
tggtaacagg attagcagag cgaggtatgt aggcggtgct acagagttct tgaagtggtg 5520
gcctaactac ggctacacta gaagaacagt atttggtatc tgcgctctgc tgaagccagt 5580
taccttcgga aaaagagttg gtagctcttg atccggcaaa caaaccaccg ctggtagcgg 5640
tttttttgtt tgcaagcagc agattacgcg cagaaaaaaa ggatctcaag aagatccttt 5700
gatcttttct acggggtctg acgctcagtg gaacgaaaac tcacgttaag ggattttggt 5760
catgagatta tcaaaaagga tcttcaccta gatcctttta aattaaaaat gaagttttaa 5820
atcaatctaa agtatatatg agtaaacttg gtctgacagt taccaatgct taatcagtga 5880
ggcacctatc tcagcgatct gtctatttcg ttcatccata gttgcctgac tccccgtcgt 5940
gtagataact acgatacggg agggcttacc atctggcccc agtgctgcaa tgataccgcg 6000
agacccacgc tcaccggctc cagatttatc agcaataaac cagccagccg gaagggccga 6060
gcgcagaagt ggtcctgcaa ctttatccgc ctccatccag tctattaatt gttgccggga 6120
agctagagta agtagttcgc cagttaatag tttgcgcaac gttgttgcca ttgctacagg 6180
catcgtggtg tcacgctcgt cgtttggtat ggcttcattc agctccggtt cccaacgatc 6240
aaggcgagtt acatgatccc ccatgttgtg caaaaaagcg gttagctcct tcggtcctcc 6300
gatcgttgtc agaagtaagt tggccgcagt gttatcactc atggttatgg cagcactgca 6360
taattctctt actgtcatgc catccgtaag atgcttttct gtgactggtg agtactcaac 6420
caagtcattc tgagaatagt gtatgcggcg accgagttgc tcttgcccgg cgtcaatacg 6480
ggataatacc gcgccacata gcagaacttt aaaagtgctc atcattggaa aacgttcttc 6540
ggggcgaaaa ctctcaagga tcttaccgct gttgagatcc agttcgatgt aacccactcg 6600
tgcacccaac tgatcttcag catcttttac tttcaccagc gtttctgggt gagcaaaaac 6660
aggaaggcaa aatgccgcaa aaaagggaat aagggcgaca cggaaatgtt gaatactcat 6720
actcttcctt tttcaatatt attgaagcat ttatcagggt tattgtctca tgagcggata 6780
catatttgaa tgtatttaga aaaataaaca aataggggtt ccgcgcacat ttccccgaaa 6840
agtgccacct gacgtc 6856
<210> 2
<211> 7338
<212> ДНК
<213> Искусственная последовательность
<400> 2
gacggatcgg gagatctccc gatcccctat ggtgcactct cagtacaatc tgctctgatg 60
ccgcatagtt aagccagtat ctgctccctg cttgtgtgtt ggaggtcgct gagtagtgcg 120
cgagcaaaat ttaagctaca acaaggcaag gcttgaccga caattgcatg aagaatctgc 180
ttagggttag gcgttttgcg ctgcttcgcg atgtacgggc cagatatacg cgttgacatt 240
gattattgac tagttattaa tagtaatcaa ttacggggtc attagttcat agcccatata 300
tggagttccg cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc 360
cccgcccatt gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc 420
attgacgtca atgggtggag tatttacggt aaactgccca cttggcagta catcaagtgt 480
atcatatgcc aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt 540
atgcccagta catgacctta tgggactttc ctacttggca gtacatctac gtattagtca 600
tcgctattac catggtgatg cggttttggc agtacatcaa tgggcgtgga tagcggtttg 660
actcacgggg atttccaagt ctccacccca ttgacgtcaa tgggagtttg ttttggcacc 720
aaaatcaacg ggactttcca aaatgtcgta acaactccgc cccattgacg caaatgggcg 780
gtaggcgtgt acggtgggag gtctatataa gcagagctct ctggctaact agagaaccca 840
ctgcttactg gcttatcgaa attaatacga ctcactatag ggagacccaa gctggctagc 900
gccaccatgg cttccaaggt gtacgacccc gagcaacgca aacgcatgat cactgggcct 960
cagtggtggg ctcgctgcaa gcaaatgaac gtgctggact ccttcatcaa ctactatgat 1020
tccgagaagc acgccgagaa cgccgtgatt tttctgcatg gtaacgctgc ctccagctac 1080
ctgtggaggc acgtcgtgcc tcacatcgag cccgtggcta gatgcatcat ccctgatctg 1140
atcggaatgg gtaagtccgg caagagcggg aatggctcat atcgcctcct ggatcactac 1200
aagtacctca ccgcttggtt cgagctgctg aaccttccaa agaaaatcat ctttgtgggc 1260
cacgactggg gggcttgtct ggcctttcac tactcctacg agcaccaaga caagatcaag 1320
gccatcgtcc atgctgagag tgtcgtggac gtgatcgagt cctgggacga gtggcctgac 1380
atcgaggagg atatcgccct gatcaagagc gaagagggcg agaaaatggt gcttgagaat 1440
aacttcttcg tcgagaccat gctcccaagc aagatcatgc ggaaactgga gcctgaggag 1500
ttcgctgcct acctggagcc attcaaggag aagggcgagg ttagacggcc taccctctcc 1560
tggcctcgcg agatccctct cgttaaggga ggcggtggcg gagggagcgg tggcggaggg 1620
agcaagcttg gtaccgagct cggatccact agatctgtta acgtgtggtg gaattctatg 1680
gcaaagcagt acgactcggt ggagtgccct ttttgtgatg aagtttccaa atacgagaag 1740
ctcgccaaga tcggccaagg caccttcggg gaggtgttca aggccaggca ccgcaagacc 1800
ggccagaagg tggctctgaa gaaggtgctg atggaaaacg agaaggaggg gttccccatt 1860
acagccttgc gggagatcaa gatccttagc ttctaaaaca cgagaatgtg gtcaacttga 1920
ttgagatttg tcgaaccaaa gcttccccct ataaccgctg caagggtagt atatacctgg 1980
tgttcgactt ctgcgagcat gaccttgctg ggctgttgag caatgttttg gtcaagttca 2040
cgctgtctga gatcaagagg gtgatgcaga tgctgcttaa cggcctctac tacatccaca 2100
gaaacaagat cctgcatagg gacatgaagg ctgctaatgt gcttatcact cgtgatgggg 2160
tcctgaagct ggcagacttt gggctggccc gggccttcag cctggccaag aacagccagc 2220
ccaaccgcta caccaaccgt gtggtgacac tctggtaccg gcccccggag ctgttgctcg 2280
gggagcggga ctacggcccc cccattgacc tgtggggtgc tgggtgcatc atggcagaga 2340
tgtggacccg cagccccatc atgcagggca acacggagca gcaccaactc gccctcatca 2400
gtcagctctg cggctccatc acccctgagg tgtggccaaa cgtggacaac tatgagctgt 2460
acgaaaagct ggagctggtc aagggccaga agcggaaggt gaaggacagg ctgaaggcct 2520
atgtgcgtga cccatacgca ctggacctca tcgacaagct gctggtgctg gaccctgccc 2580
agcgcatcga cagcgatgac gccctcaacc acgacttctt ctggtccgac cccatgccct 2640
ccgacctcaa gggcatgctc tccacccacc tgacgtccat gttcgagtac ttggcaccac 2700
cgcgccggaa gggcagccag atcacccagc agtccaccaa ccagagtcgc aatcccgcca 2760
ccaccaacca gacggagttt gagcgcgtct tctggaattc tgcagatatc cagcacagtg 2820
gcggccgctc gagtctagag gctgactaca aagaccatga cggtgattat aaagatcatg 2880
acatcgacta caaggatgac gatgacaagt gagtttaaac ccgctgatca gcctcgactg 2940
tgccttctag ttgccagcca tctgttgttt gcccctcccc cgtgccttcc ttgaccctgg 3000
aaggtgccac tcccactgtc ctttcctaat aaaatgagga aattgcatcg cattgtctga 3060
gtaggtgtca ttctattctg gggggtgggg tggggcagga cagcaagggg gaggattggg 3120
aagacaatag caggcatgct ggggatgcgg tgggctctat ggcttctgag gcggaaagaa 3180
ccagctgggg ctctaggggg tatccccacg cgccctgtag cggcgcatta agcgcggcgg 3240
gtgtggtggt tacgcgcagc gtgaccgcta cacttgccag cgccctagcg cccgctcctt 3300
tcgctttctt cccttccttt ctcgccacgt tcgccggctt tccccgtcaa gctctaaatc 3360
gggggctccc tttagggttc cgatttagtg ctttacggca cctcgacccc aaaaaacttg 3420
attagggtga tggttcacgt agtgggccat cgccctgata gacggttttt cgccctttga 3480
cgttggagtc cacgttcttt aatagtggac tcttgttcca aactggaaca acactcaacc 3540
ctatctcggt ctattctttt gatttataag ggattttgcc gatttcggcc tattggttaa 3600
aaaatgagct gatttaacaa aaatttaacg cgaattaatt ctgtggaatg tgtgtcagtt 3660
agggtgtgga aagtccccag gctccccagc aggcagaagt atgcaaagca tgcatctcaa 3720
ttagtcagca accaggtgtg gaaagtcccc aggctcccca gcaggcagaa gtatgcaaag 3780
catgcatctc aattagtcag caaccatagt cccgccccta actccgccca tcccgcccct 3840
aactccgccc agttccgccc attctccgcc ccatggctga ctaatttttt ttatttatgc 3900
agaggccgag gccgcctctg cctctgagct attccagaag tagtgaggag gcttttttgg 3960
aggcctaggc ttttgcaaaa agctcccggg agcttgtata tccattttcg gatctgatca 4020
agagacagga tgaggatcgt ttcgcatgat tgaacaagat ggattgcacg caggttctcc 4080
ggccgcttgg gtggagaggc tattcggcta tgactgggca caacagacaa tcggctgctc 4140
tgatgccgcc gtgttccggc tgtcagcgca ggggcgcccg gttctttttg tcaagaccga 4200
cctgtccggt gccctgaatg aactgcagga cgaggcagcg cggctatcgt ggctggccac 4260
gacgggcgtt ccttgcgcag ctgtgctcga cgttgtcact gaagcgggaa gggactggct 4320
gctattgggc gaagtgccgg ggcaggatct cctgtcatct caccttgctc ctgccgagaa 4380
agtatccatc atggctgatg caatgcggcg gctgcatacg cttgatccgg ctacctgccc 4440
attcgaccac caagcgaaac atcgcatcga gcgagcacgt actcggatgg aagccggtct 4500
tgtcgatcag gatgatctgg acgaagagca tcaggggctc gcgccagccg aactgttcgc 4560
caggctcaag gcgcgcatgc ccgacggcga ggatctcgtc gtgacccatg gcgatgcctg 4620
cttgccgaat atcatggtgg aaaatggccg cttttctgga ttcatcgact gtggccggct 4680
gggtgtggcg gaccgctatc aggacatagc gttggctacc cgtgatattg ctgaagagct 4740
tggcggcgaa tgggctgacc gcttcctcgt gctttacggt atcgccgctc ccgattcgca 4800
gcgcatcgcc ttctatcgcc ttcttgacga gttcttctga gcgggactct ggggttcgaa 4860
atgaccgacc aagcgacgcc caacctgcca tcacgagatt tcgattccac cgccgccttc 4920
tatgaaaggt tgggcttcgg aatcgttttc cgggacgccg gctggatgat cctccagcgc 4980
ggggatctca tgctggagtt cttcgcccac cccaacttgt ttattgcagc ttataatggt 5040
tacaaataaa gcaatagcat cacaaatttc acaaataaag catttttttc actgcattct 5100
agttgtggtt tgtccaaact catcaatgta tcttatcatg tctgtatacc gtcgacctct 5160
agctagagct tggcgtaatc atggtcatag ctgtttcctg tgtgaaattg ttatccgctc 5220
acaattccac acaacatacg agccggaagc ataaagtgta aagcctgggg tgcctaatga 5280
gtgagctaac tcacattaat tgcgttgcgc tcactgcccg ctttccagtc gggaaacctg 5340
tcgtgccagc tgcattaatg aatcggccaa cgcgcgggga gaggcggttt gcgtattggg 5400
cgctcttccg cttcctcgct cactgactcg ctgcgctcgg tcgttcggct gcggcgagcg 5460
gtatcagctc actcaaaggc ggtaatacgg ttatccacag aatcagggga taacgcagga 5520
aagaacatgt gagcaaaagg ccagcaaaag gccaggaacc gtaaaaaggc cgcgttgctg 5580
gcgtttttcc ataggctccg cccccctgac gagcatcaca aaaatcgacg ctcaagtcag 5640
aggtggcgaa acccgacagg actataaaga taccaggcgt ttccccctgg aagctccctc 5700
gtgcgctctc ctgttccgac cctgccgctt accggatacc tgtccgcctt tctcccttcg 5760
ggaagcgtgg cgctttctca tagctcacgc tgtaggtatc tcagttcggt gtaggtcgtt 5820
cgctccaagc tgggctgtgt gcacgaaccc cccgttcagc ccgaccgctg cgccttatcc 5880
ggtaactatc gtcttgagtc caacccggta agacacgact tatcgccact ggcagcagcc 5940
actggtaaca ggattagcag agcgaggtat gtaggcggtg ctacagagtt cttgaagtgg 6000
tggcctaact acggctacac tagaagaaca gtatttggta tctgcgctct gctgaagcca 6060
gttaccttcg gaaaaagagt tggtagctct tgatccggca aacaaaccac cgctggtagc 6120
ggtttttttg tttgcaagca gcagattacg cgcagaaaaa aaggatctca agaagatcct 6180
ttgatctttt ctacggggtc tgacgctcag tggaacgaaa actcacgtta agggattttg 6240
gtcatgagat tatcaaaaag gatcttcacc tagatccttt taaattaaaa atgaagtttt 6300
aaatcaatct aaagtatata tgagtaaact tggtctgaca gttaccaatg cttaatcagt 6360
gaggcaccta tctcagcgat ctgtctattt cgttcatcca tagttgcctg actccccgtc 6420
gtgtagataa ctacgatacg ggagggctta ccatctggcc ccagtgctgc aatgataccg 6480
cgagacccac gctcaccggc tccagattta tcagcaataa accagccagc cggaagggcc 6540
gagcgcagaa gtggtcctgc aactttatcc gcctccatcc agtctattaa ttgttgccgg 6600
gaagctagag taagtagttc gccagttaat agtttgcgca acgttgttgc cattgctaca 6660
ggcatcgtgg tgtcacgctc gtcgtttggt atggcttcat tcagctccgg ttcccaacga 6720
tcaaggcgag ttacatgatc ccccatgttg tgcaaaaaag cggttagctc cttcggtcct 6780
ccgatcgttg tcagaagtaa gttggccgca gtgttatcac tcatggttat ggcagcactg 6840
cataattctc ttactgtcat gccatccgta agatgctttt ctgtgactgg tgagtactca 6900
accaagtcat tctgagaata gtgtatgcgg cgaccgagtt gctcttgccc ggcgtcaata 6960
cgggataata ccgcgccaca tagcagaact ttaaaagtgc tcatcattgg aaaacgttct 7020
tcggggcgaa aactctcaag gatcttaccg ctgttgagat ccagttcgat gtaacccact 7080
cgtgcaccca actgatcttc agcatctttt actttcacca gcgtttctgg gtgagcaaaa 7140
acaggaaggc aaaatgccgc aaaaaaggga ataagggcga cacggaaatg ttgaatactc 7200
atactcttcc tttttcaata ttattgaagc atttatcagg gttattgtct catgagcgga 7260
tacatatttg aatgtattta gaaaaataaa caaatagggg ttccgcgcac atttccccga 7320
aaagtgccac ctgacgtc 7338
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ ИНГИБИТОР КИНАЗЫ PAN-RAF И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2792626C1 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ И ЗАМЕЩЕННЫЕ ПУРИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОЦЕССИРУЮЩЕЙ ПРОТЕАЗЫ 1 (USP1) | 2019 |
|
RU2833222C2 |
| ПИРИДОПИРИМИДИНОВОЕ СОЕДИНЕНИЕ, СПОСОБ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ УКАЗАННЫХ СОЕДИНЕНИЙ | 2014 |
|
RU2662713C2 |
| ИНГИБИТОРЫ АРГИНАЗЫ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2011 |
|
RU2586219C2 |
| ПРОИЗВОДНОЕ ПИРИМИДИН-4,6-ДИАМИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2834353C2 |
| ПРОИЗВОДНЫЕ ОКСОТИОИМИДАЗОЛИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ В КАЧЕСТВЕ ИНГИБИТОРОВ АНДРОГЕННОГО РЕЦЕПТОРА | 2013 |
|
RU2639145C2 |
| ИНГИБИТОР КИНАЗЫ PAN-KIT, ИМЕЮЩИЙ СТРУКТУРУ ХИНОЛИНА, И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2789405C2 |
| ИМИДНЫЕ МОДУЛЯТОРЫ ПРОТЕОЛИЗА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2738833C2 |
| ИНДАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ FGFR, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2719428C2 |
| СОЕДИНЕНИЕ, ИМЕЮЩЕЕ ИНГИБИРУЮЩУЮ АКТИВНОСТЬ В ОТНОШЕНИИ КИНАЗ | 2021 |
|
RU2831403C1 |
Изобретение относится к ингибитору киназы CDK9, содержащему соединение формулы (I) или его фармацевтически приемлемую соль, которые могут найти применение для лечения заболеваний, связанных с ингибированием CDK9 и/или с ее активностью, вызванной мутациями. В формуле (I) А выбран из группы, состоящей из циклогексила, фенила и пиридинила; X представляет собой CH или N; Z представляет собой -NH- или -NH-C(=O)-; n представляет собой 0 или 1; R1 выбран из группы, состоящей из водорода, галогена, циано, (C1-C6)алкила и (C1-C6)галогеналкила; R2 выбраны из группы, состоящей из водорода и (C1-C6)алкила, или два R2 вместе образуют (C3-C6)циклоалкил; m выбран из целого числа 1-3 и каждый R3 независимо выбран из группы, состоящей из -NH-(C1-C3)алкил(C1-C3)алкокси, галогена, (C1-C6)алкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)алкилациламино, (C1-C6)алкилсульфонила, (C1-C6)алкилсульфонамидо, аминосульфонила, (C1-C6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, аминосульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C3-C6)циклоалкила, гетероциклиламиноацила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, гетероциклила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, -S(=O)(=NH)(C1-C3)алкила и -(C1-C3)алкил-S(=O)(=NH)(C1-C3)алкила, где гетероциклил независимо представляет собой моноциклическое неароматическое кольцо, образованное шестью или семью атомами, где один или два указанных атомов кольца представляют собой гетероатом, выбранный из группы, состоящей из азота и кислорода; R4 выбран из группы, состоящей из водорода и (C1-C6)алкила. Изобретение относится также к фармацевтической композиции, содержащей указанный ингибитор, и его применению для лечения заболеваний, которые несут CDK9 и/или мутации CDK9, в частности гиперпролиферативных заболеваний, инфекционных заболеваний, вызванных вирусом, и сердечно-сосудистых заболеваний. 4 н. и 6 з.п. ф-лы, 6 табл., 110 пр.
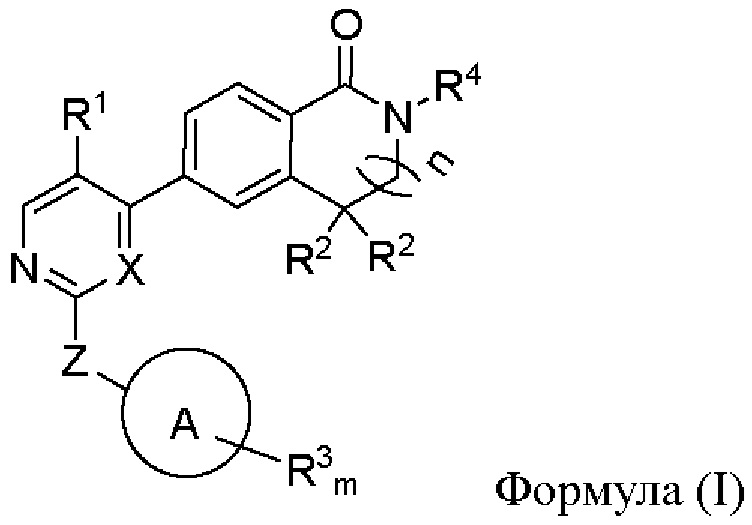
1. Ингибитор киназы CDK9, содержащий соединение формулы (I) или его фармацевтически приемлемую соль
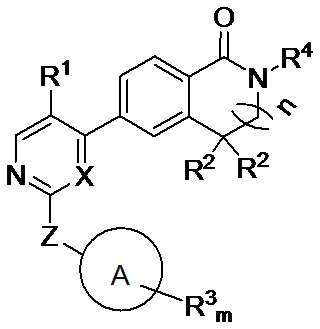 формула (I),
формула (I),
где А выбран из группы, состоящей из циклогексила, фенила и пиридинила;
X представляет собой CH или N;
Z представляет собой -NH- или -NH-C(=O)-;
n представляет собой 0 или 1;
R1 выбран из группы, состоящей из водорода, галогена, циано, (C1-C6)алкила и (C1-C6)галогеналкила;
R2 выбраны из группы, состоящей из водорода и (C1-C6)алкила, или два R2 вместе образуют (C3-C6)циклоалкил;
m выбран из целого числа 1-3 и каждый R3 независимо выбран из группы, состоящей из -NH-(C1-C3)алкил(C1-C3)алкокси, галогена, (C1-C6)алкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)алкилациламино, (C1-C6)алкилсульфонила, (C1-C6)алкилсульфонамидо, аминосульфонила, (C1-C6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, аминосульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C3-C6)циклоалкила, гетероциклиламиноацила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, гетероциклила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, -S(=O)(=NH)(C1-C3)алкила и -(C1-C3)алкил-S(=O)(=NH)(C1-C3)алкила, где гетероциклил независимо представляет собой моноциклическое неароматическое кольцо, образованное шестью или семью атомами, где один или два указанных атомов кольца представляют собой гетероатом, выбранный из группы, состоящей из азота и кислорода;
R4 выбран из группы, состоящей из водорода и (C1-C6)алкила.
2. Ингибитор киназы CDK9 по п. 1, содержащий соединение формулы (Ia) или его фармацевтически приемлемую соль
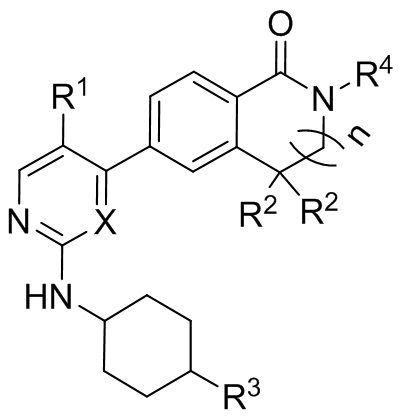 формула (Ia),
формула (Ia),
где R3 представляет собой -NH-(C1-C3)алкил(C1-C3)алкокси.
3. Ингибитор киназы CDK9 по п. 1, содержащий соединение формулы (Ib) или его фармацевтически приемлемую соль
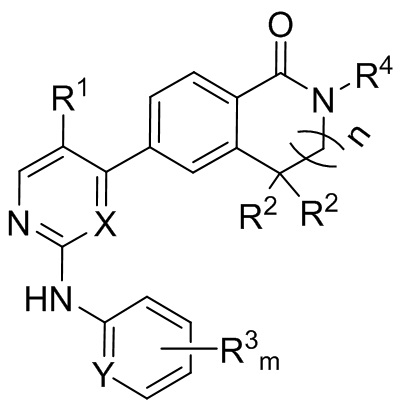 формула (Ib),
формула (Ib),
где Y представляет собой CH или N;
m выбран из целого числа 1-3 и каждый R3 независимо выбран из группы, состоящей из галогена, (C1-C6)алкила, (C1-C6)алкокси, (C1-C6)галогеналкила, (C1-C6)алкилсульфонила, (C1-C6)алкилсульфонамидо, аминосульфонила, (C1-C6)алкиламиносульфонила, гетероциклилсульфонила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, аминосульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C1-C3)алкила, (C1-C3)алкилсульфонил(C3-C6)циклоалкила, гетероциклиламиноацила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, гетероциклила, в котором гетероатом(ы) необязательно замещен(ы) (C1-C6)алкилом, -S(=O)(=NH)(C1-C3)алкила и -(C1-C3)алкил-S(=O)(=NH)(C1-C3)алкила.
4. Ингибитор киназы CDK9 по п. 1, содержащий соединение формулы (Ic) или его фармацевтически приемлемую соль
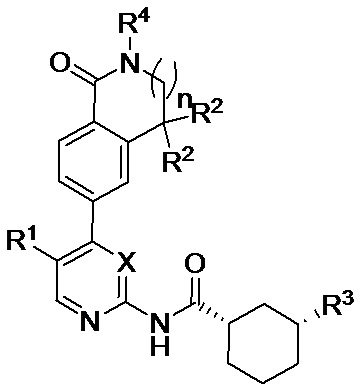 формула (Ic),
формула (Ic),
где R3 представляет собой (C1-C6)алкилациламино.
5. Ингибитор киназы CDK9 по любому из пп. 1-4, отличающийся тем, что X представляет собой N.
6. Ингибитор киназы CDK9 по п. 1, содержащий следующее соединение или его фармацевтически приемлемую соль:
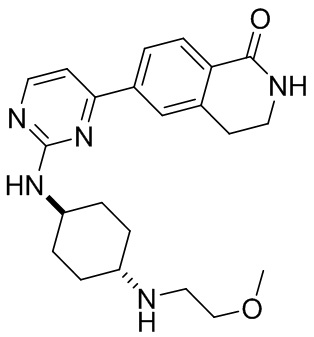
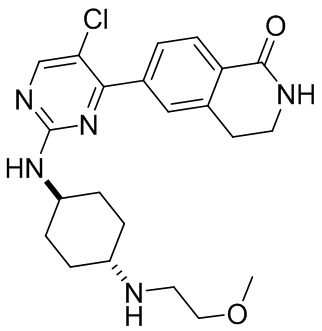
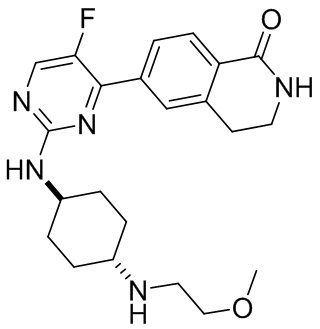
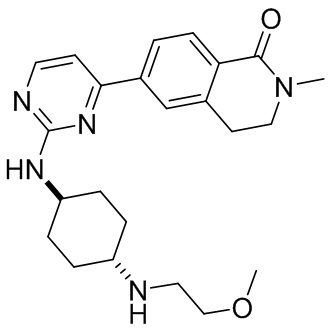
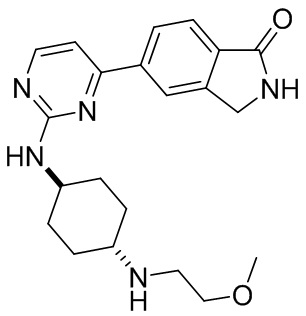
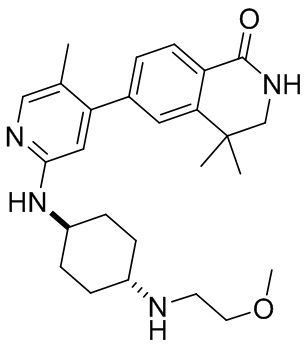
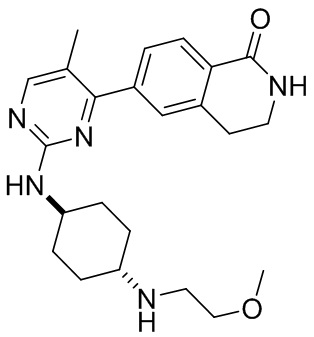
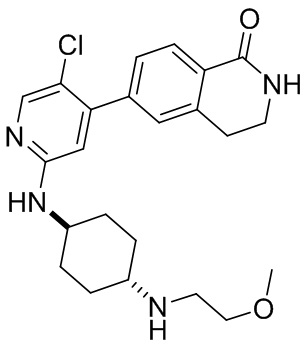
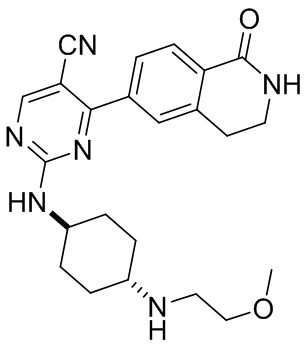
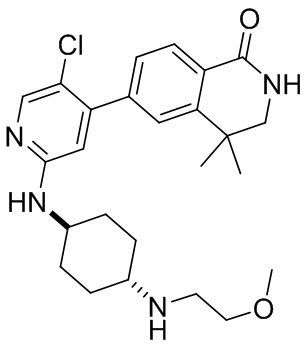
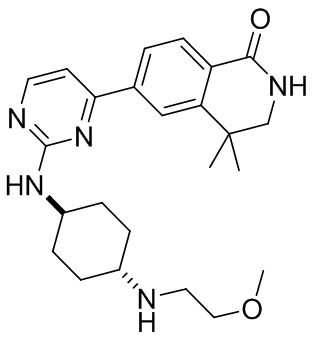
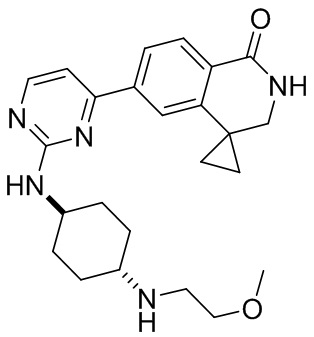
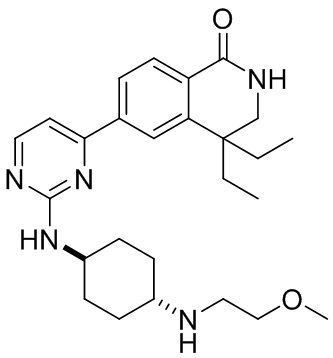
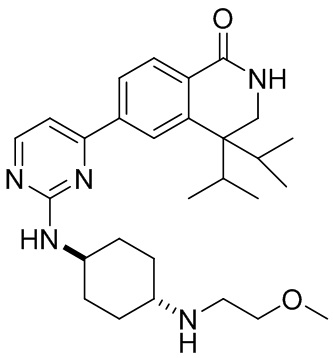
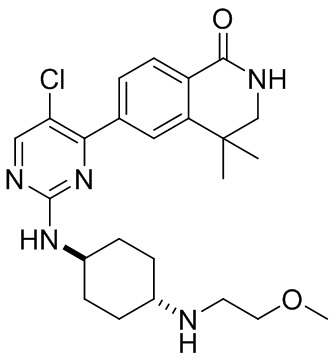
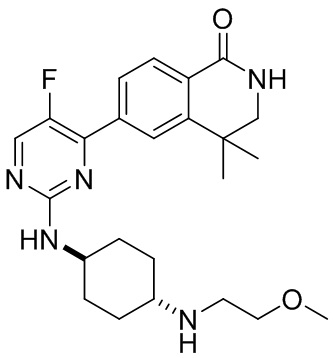
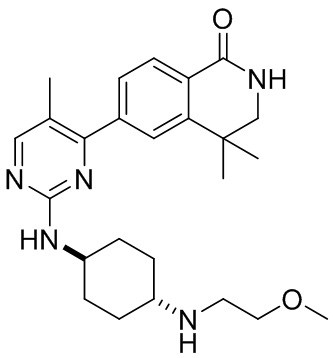
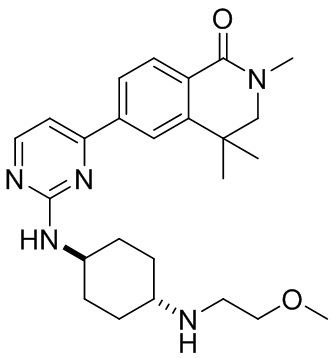
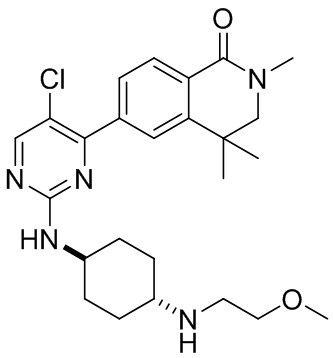
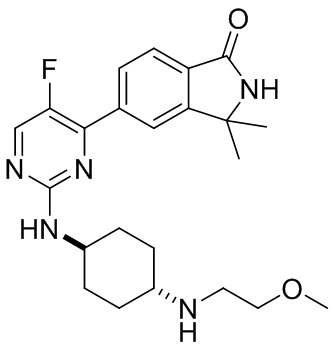
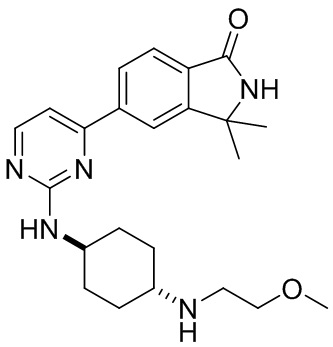
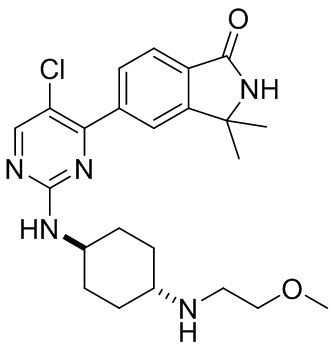
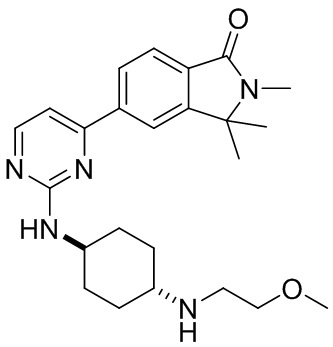
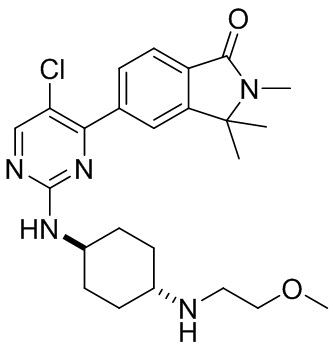

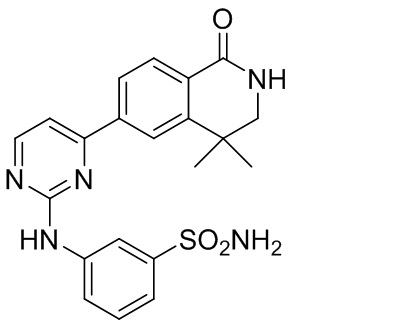
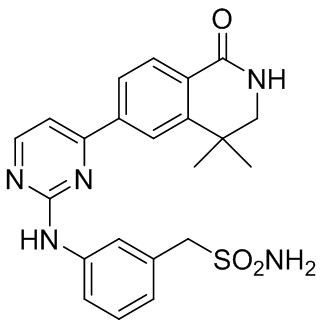
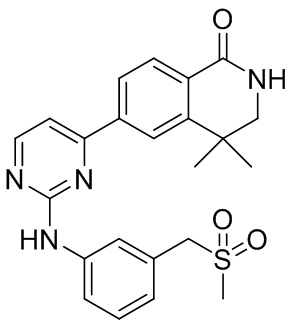
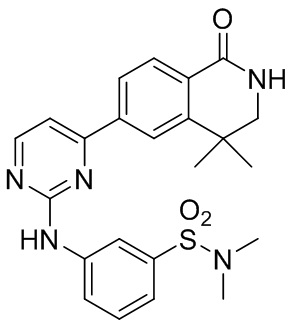
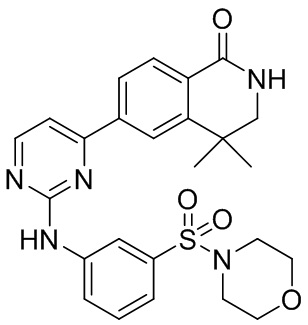
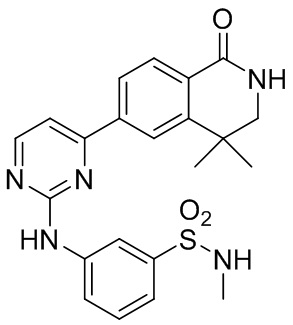
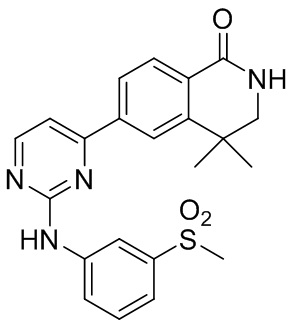
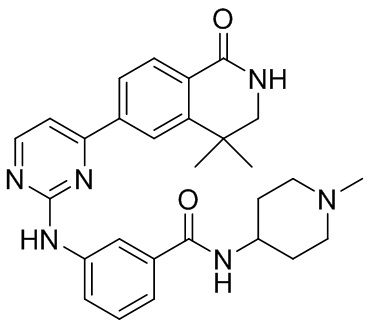
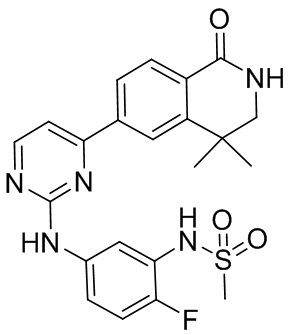
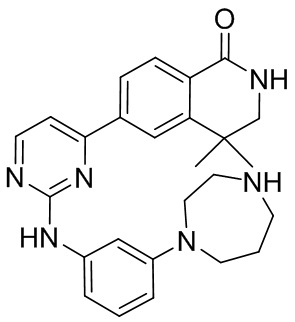
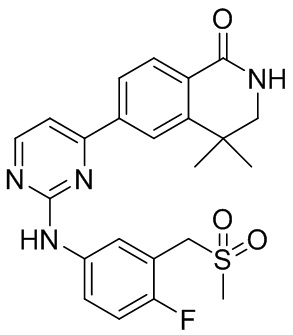

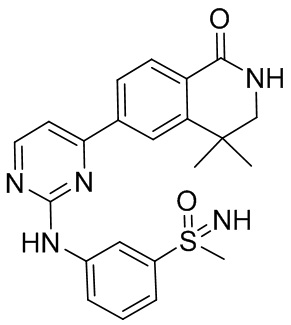
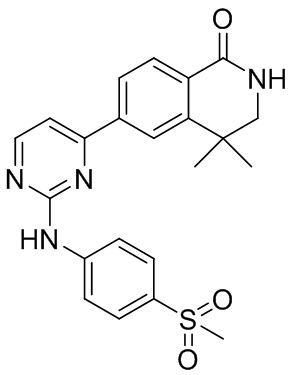
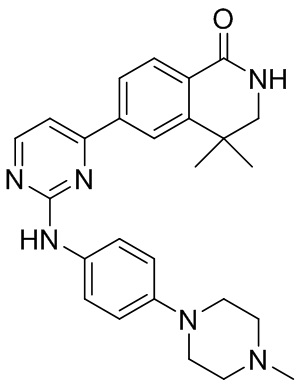
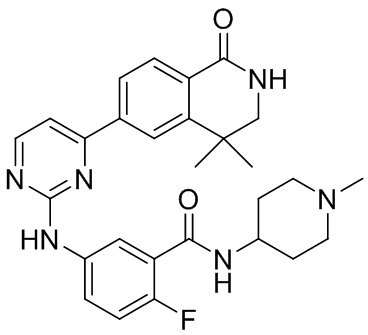
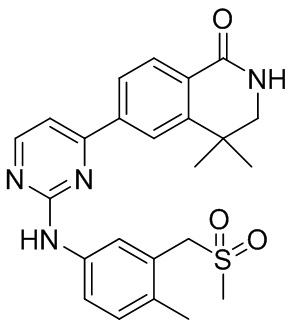
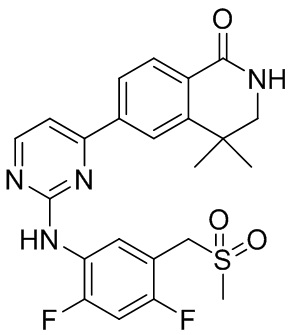
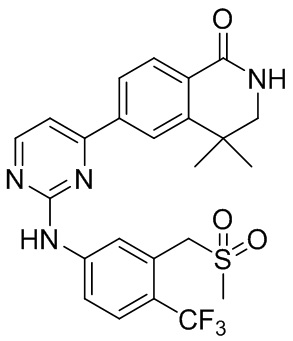
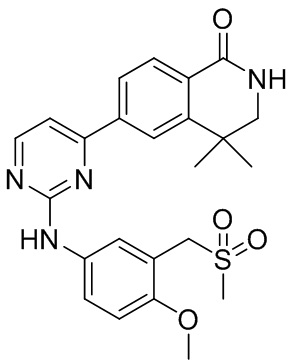
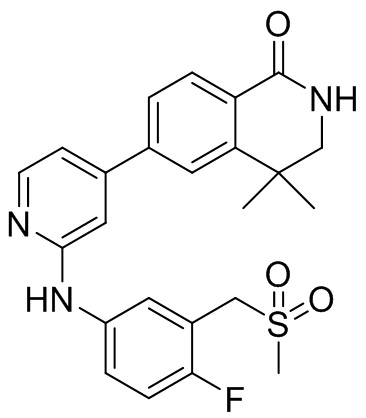
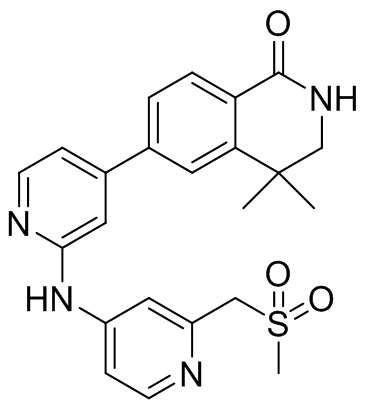
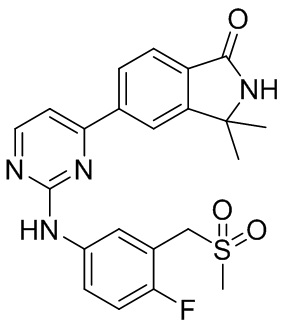
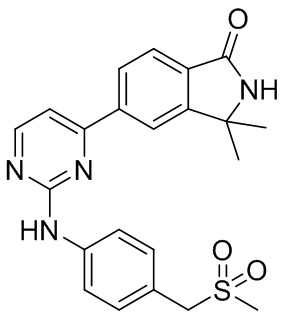
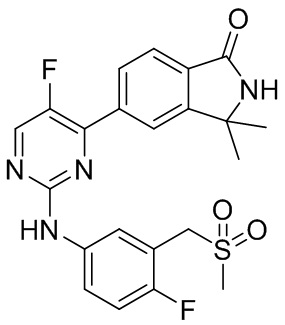
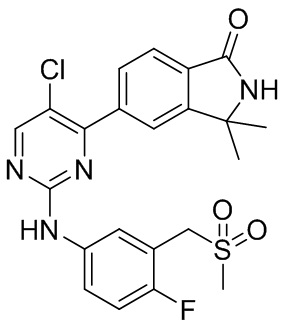
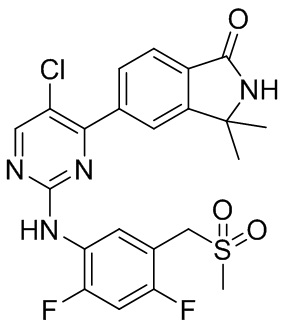
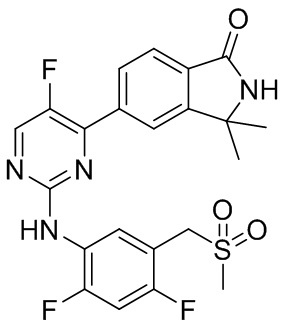

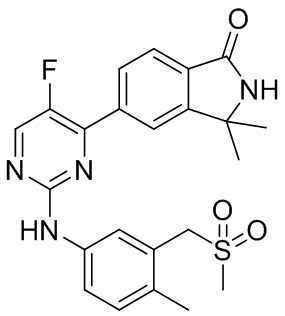
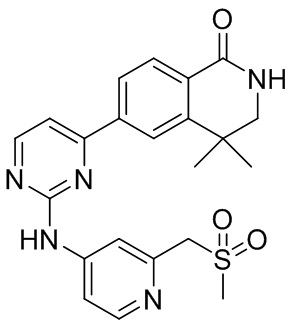
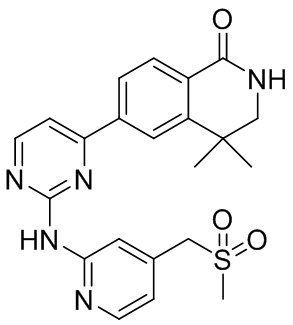
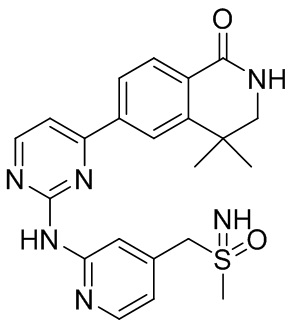
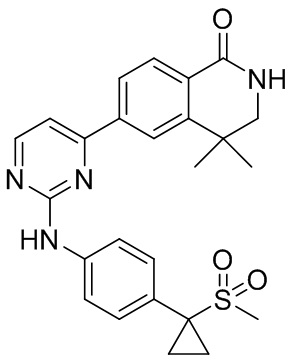
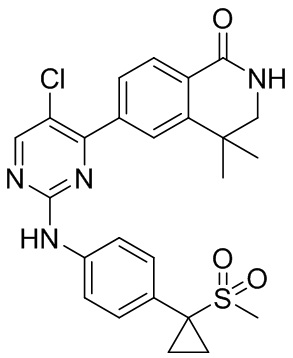
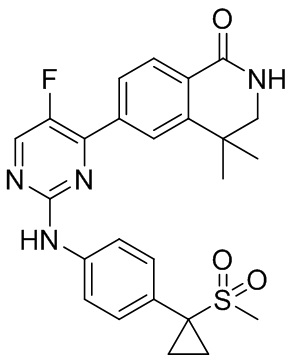
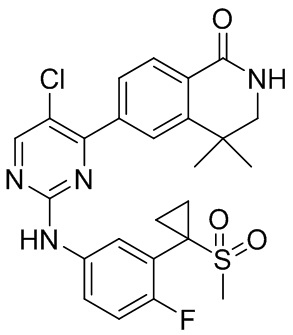

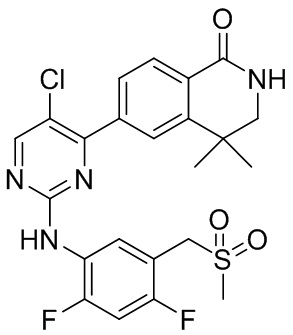
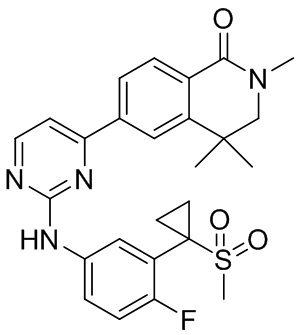
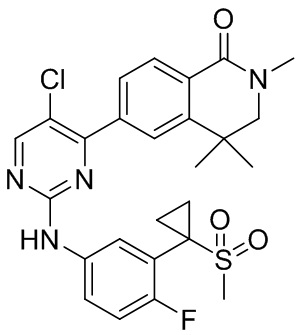
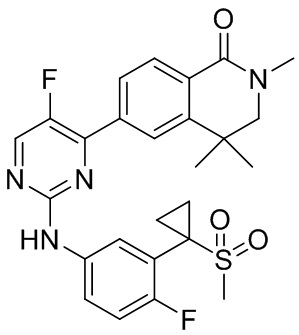
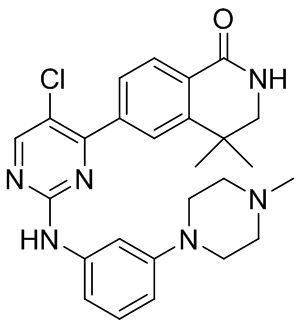
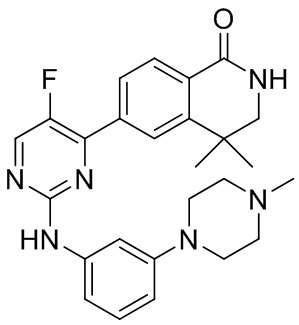
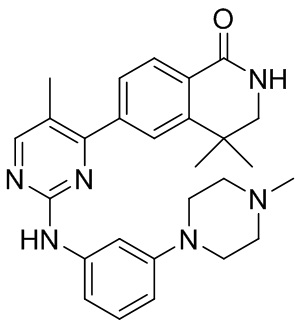
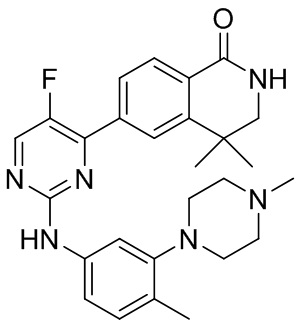
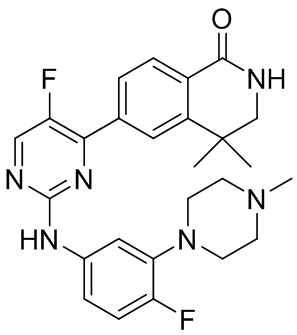
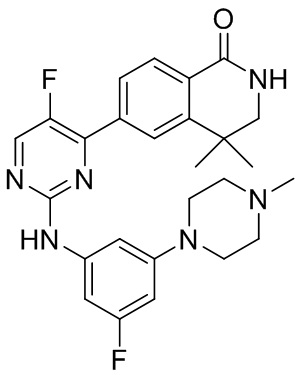
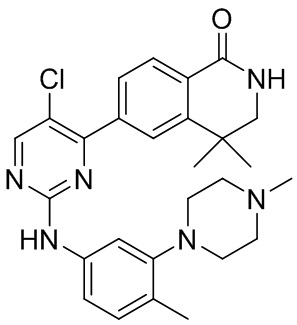
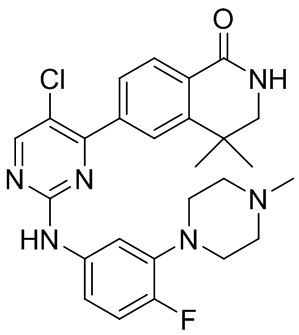
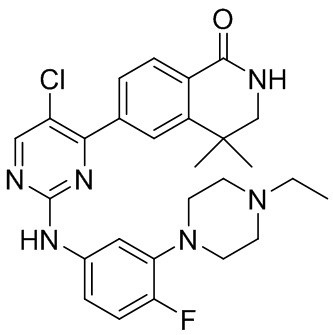
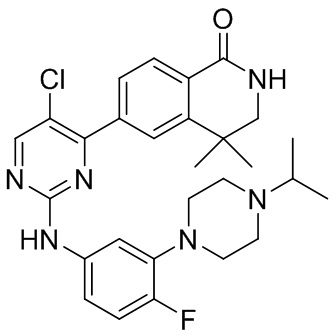
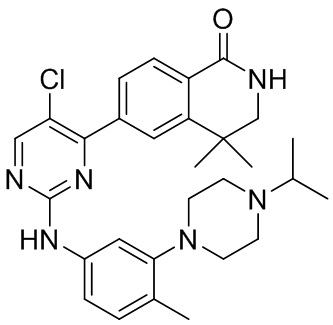
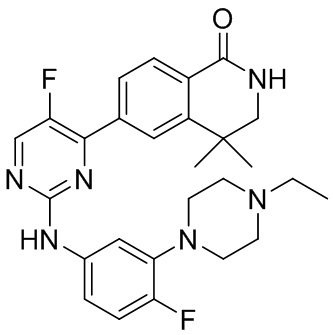
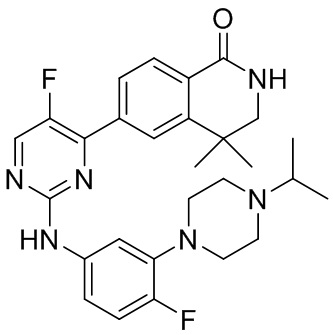
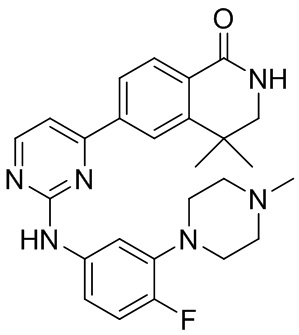
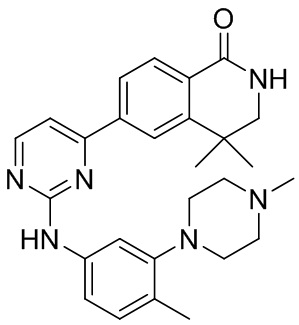
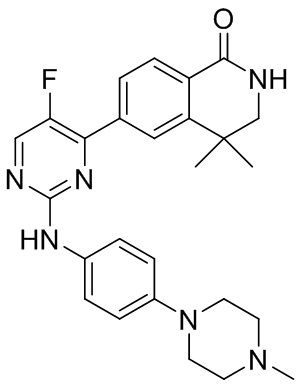
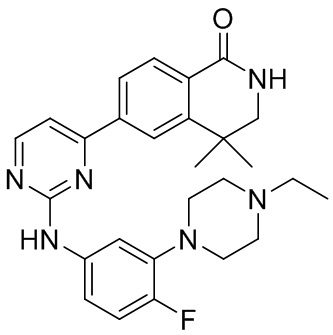
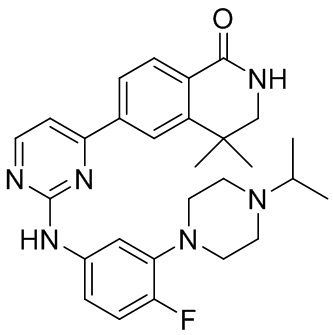
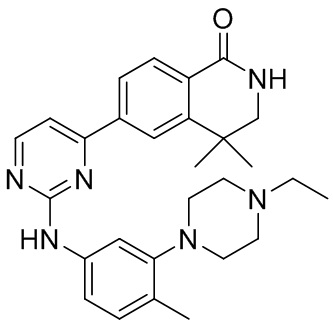
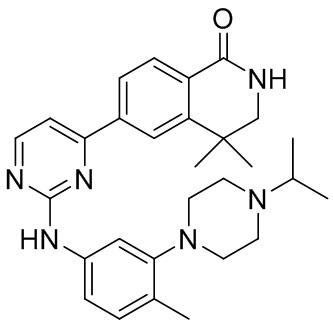
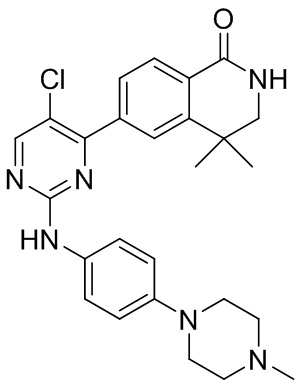
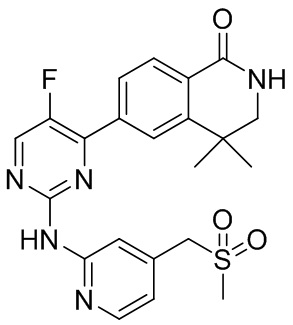
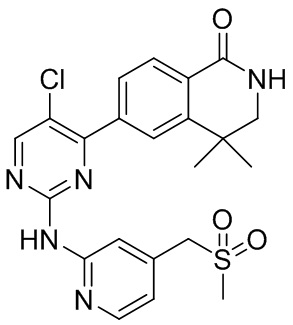
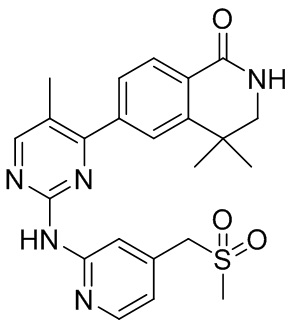
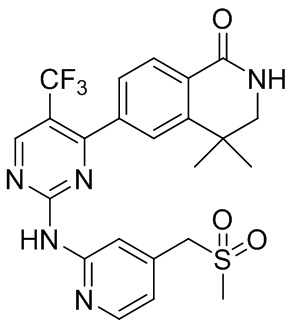
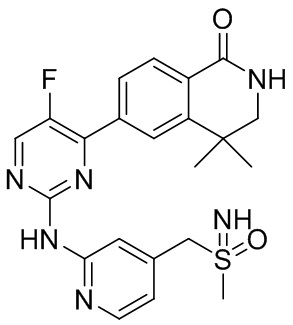
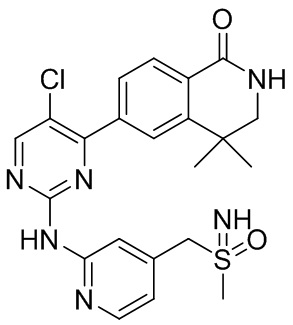
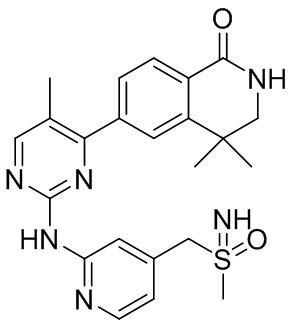
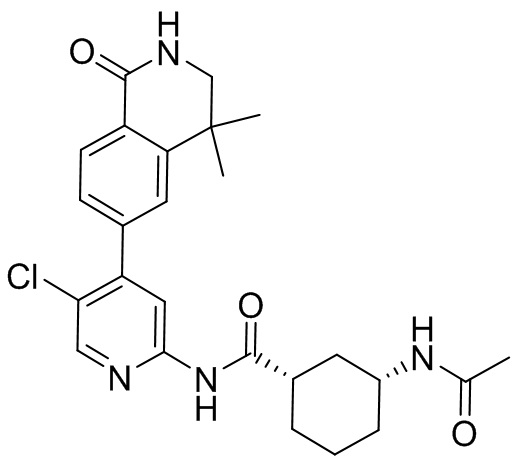
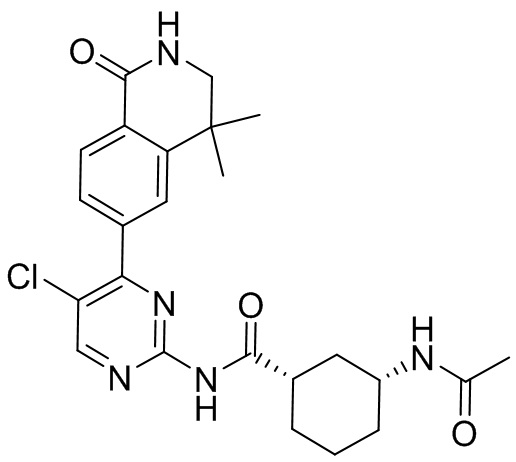
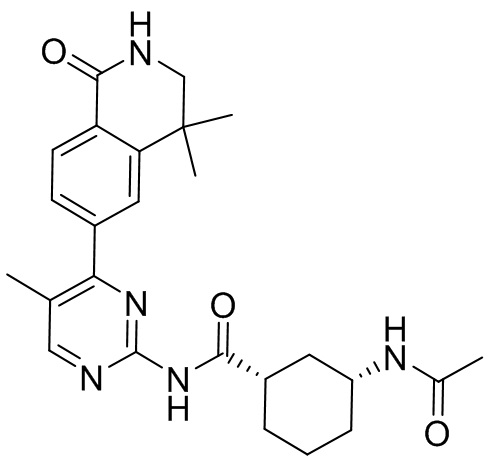
7. Фармацевтическая композиция для ингибирования киназы CDK9, содержащая ингибитор киназы по любому из пп. 1-6 и фармацевтически приемлемый разбавитель или носитель.
8. Ингибитор киназы CDK9 по любому из пп. 1-6 для применения для лечения заболеваний, выбранных из заболеваний, которые несут CDK9 и/или мутации CDK9.
9. Ингибитор киназы CDK9 по любому из пп. 1-6 для применения для лечения гиперпролиферативных заболеваний, инфекционных заболеваний, вызванных вирусом, и сердечно-сосудистых заболеваний, ассоциированных с или опосредуемых активностью CDK9 и/или ее мутациями.
10. Ингибитор киназы CDK9 для применения по п. 9, отличающийся тем, что указанное гиперпролиферативное заболевание представляет собой рак и предпочтительно выбрано из группы, состоящей из лейкоза, рака печени, рака яичников, рака шейки матки, колоректального рака, стромальной опухоли желудочно-кишечного тракта и лимфомы.
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ИНГИБИТОРЫ ФОСФАТИДИЛИНОЗИТОЛ-3-КИНАЗЫ НА ОСНОВЕ ИЗОИНДОЛИНОНА | 2010 |
|
RU2573569C2 |
Авторы
Даты
2025-01-21—Публикация
2021-10-21—Подача