Настоящее изобретение относится к способу получения диосмина. Диосмин представляет собой соединение формулы (I):
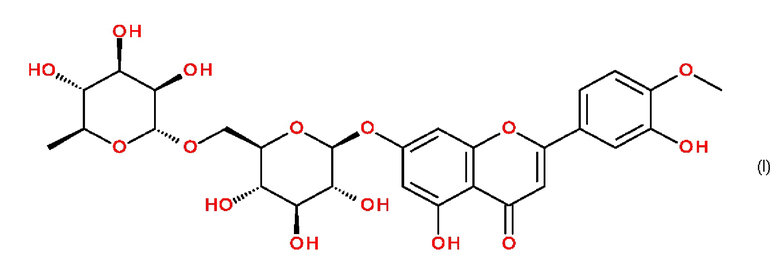
Диосмин используют при лечении венозных заболеваний, таких как хроническая венозная недостаточность или геморроидальные заболевания.
Он также является основным компонентом микронизированной очищенной фракции флавоноидов или FFPM (Daflon®).
Диосмин синтезируют путем окисления гесперидина. Гесперидин представляет собой соединение формулы (II):
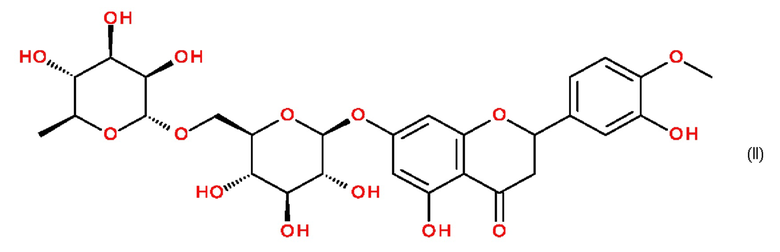
Гесперидин получают из природных веществ (недозревших апельсинов). Разнообразие используемых апельсинов приводит к гесперидинам неодинаковой чистоты, содержащим другие флавоноиды с переменным содержанием. В частности, гесперидин может содержать до 4% изонарингина, который при окислении превращается в изороифолин.
Поэтому диосмин обычно содержит другие флавоноиды, некоторые из которых образуются в результате окисления флавоноидов, присутствующих в исходном гесперидине, а другие являются вторичными продуктами реакции.
Учитывая фармацевтический интерес диосмина, важно получать его с отличным выходом и требуемой чистотой, независимо от источника гесперидина.
Технические требования, установленные Европейской фармакопеей, являются следующими:
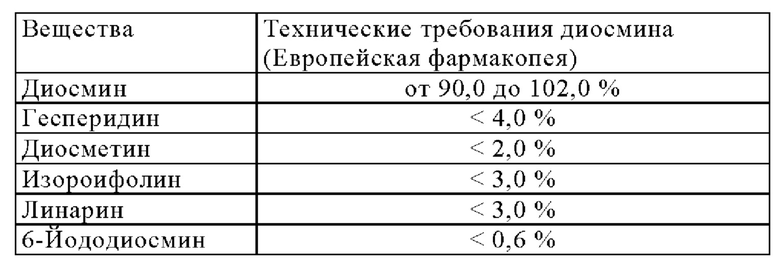
В частности, существенно, чтобы полученный диосмин содержал менее 0,6% 6-йододиосмина и менее 3,0% изороифолина.
В литературных источниках описаны способы получения диосмина из гесперидина.
В FR 2311028 описан способ получения диосмина ацетилированием гесперидина, затем окислением ацетилированного гесперидина бромированием, щелочным гидролизом и выделением. Полученный таким образом неочищенный диосмин очищают на стадии повторной обработки с использованием пиридина.
Этот способ не идеален, потому что выход составляет всего 65%. Кроме того, в нем используют пиридин, канцерогенный растворитель класса 3.
Патентная заявка WO 2016/124585 имеет то преимущество, что не используют органические растворители, такие как пиридин. Однако описанный там способ не позволяет получить диосмин требуемой чистоты, когда используемый гесперидин содержит большое количество изонарингина.
Одна из задач настоящего изобретения состояла в том, чтобы минимизировать содержание 6-йододиосмина в полученном диосмине, избегая при этом использования растворителей класса 3, таких как пиридин.
Другая задача настоящего изобретения заключалась в том, чтобы свести к минимуму содержание изороифолина в полученном диосмине, избегая при этом использования растворителей класса 3, таких как пиридин, из гесперидина, содержащего до 4% изонарингина.
Более конкретно, настоящее изобретение относится к способу получения диосмина путем
а) ацетилирования гесперидина,
б) окисления ацетилированного гесперидина до ацетилированного диосмина донором йода при температуре от 90 до 120°С,
в) нагревания ацетилированного диосмина в автоклаве при давлении от 5 до 8 бар при кипячении с обратным холодильником со спиртом, таким как метанол, этанол или изопропанол, в присутствии основания, выбранного из ацетата натрия или калия, гидроксида натрия, калия или лития, карбоната калия, метилата натрия или этилата натрия, отдельно или в смеси с другим из этих оснований,затем
г) снятия защиты с ацетилированного диосмина до диосмина путем нагревания в присутствии основания, выбранного из гидроксида натрия, калия или лития, карбоната калия, метилата натрия или этилата натрия, отдельно или в смеси с ацетатом натрия или калия,
д) очистки обработкой основанием/кислотой.
Согласно одному варианту осуществления настоящего изобретения полученный диосмин содержит другие флавоноиды, такие как гесперидин, изороифолин, линарин или диосметин.
В соответствии с одним вариантом осуществления настоящего изобретения стадию ацетилирования (а) проводят путем взаимодействия гесперидина с уксусным ангидридом и ацетатом калия или натрия.
Реакцию ацетилирования предпочтительно проводят при температуре от 40°С до 135°С.
Количество уксусного ангидрида предпочтительно составляет от 8 до 10 молярных эквивалентов по отношению к используемому гесперидину.
Донор йода, используемый на стадии окисления (б), предпочтительно выбирают из NaI/H2O2, KI/H2O2, TBAI/H2O2 и NaI/I2 (предпочтительно 9/1)/H2O2.
Количество NaI предпочтительно составляет от 0,05 до 0,20 молярных эквивалентов по отношению к используемому гесперидину.
Количество пероксида водорода предпочтительно составляет от 1,0 до 1,2 молярных эквивалентов по отношению к используемому гесперидину.
В соответствии с одним из вариантов осуществления настоящего изобретения ацетилированный диосмин, полученный в конце стадии окисления (б), выделяют, предпочтительно путем осаждения в воде, перед тем как использовать на стадии в).
В соответствии с одним вариантом осуществления настоящего изобретения основание, используемое на стадии в), представляет собой водный раствор гидроксида натрия или калия, водный раствор ацетата натрия или калия или смесь гидроксида натрия или калия и ацетата натрия или калия в водном растворе.
Ацетат натрия или калия, используемый на стадии в), может быть получен in situ путем нейтрализации остаточной уксусной кислоты, присутствующей в ацетилированном диосмине, гидроксидом натрия или калия.
Количество основания, используемого на стадии (в), предпочтительно составляет от 0,5 до 2,5 молярных эквивалентов по отношению к используемому гесперидину.
В соответствии с одним вариантом осуществления настоящего изобретения основание, добавляемое на стадии деацетилирования (г), представляет собой гидроксид натрия или калия.
Количество основания, добавляемого на стадии деацетилирования (г), предпочтительно составляет от 2 до 4,5 молярных эквивалентов по отношению к используемому гесперидину.
В соответствии с одним вариантом осуществления настоящего изобретения обработку основанием/кислотой (стадия д) проводят путем растворения в воде в присутствии основания, такого как гидроксид натрия, с последующим осаждением путем солеобразования с кислотой, такой как серная кислота.
Следующие примеры иллюстрируют изобретение.
Сокращения:
мол. экв. - молярные эквиваленты (относительно гесперидина)
ВЭЖХ - высокоэффективная жидкостная хроматография
мас./мас. - соотношение, выраженное в массе/массе
TBAI - йодид тетра-н-бутиламмония
об. - объемные эквиваленты (в пересчете на гесперидин)
Пример 1: Диосмин
Стадия А: Ацетилированный диосмин
В реактор при температуре 20-25°С загружают ацетат калия (98,6 ммоль) и уксусный ангидрид (2996,2 ммоль).
Суспензию нагревают при перемешивании до 40°С, затем загружают гесперидин (2 х 163,8 ммоль; титр ВЭЖХ: 91,3%, изонарингин 3,8%). Перемешивание продолжают при нагревании до 40°С, затем нагревают до 132°С в течение 45 мин. при перемешивании. В конце нагревания смесь становится прозрачным раствором. Раствор оставляют перемешиваться в течение 60 мин. до 132°С, затем охлаждают до 105°С.
Загружают водный раствор йодида натрия (33 ммоль в 20 г воды). Вливают при 105°С в 35% перекись водорода (341,5 ммоль), стабилизированную 0,1% серной кислотой.
Оставляют перемешиваться в течение 30 мин. при 105°С, затем охлаждают до 100°С при перемешивании и осаждают в химическом стакане, содержащем воду (около 7 об.), при механическом перемешивании при 20-40°С.
После перемешивания в течение 30 мин. при 20-40°С фильтруют в вакууме, осадок промывают водой (9 об.; затем 2 x 2 об.). Выпаривают в течение 16 ч. в вакууме при 20-25°С.
Стадия В: Диосмин
В автоклав загружают ацетилированный диосмин, полученный на стадии А, и метанол (3,5 об.). Перемешивают, затем нагревают до температуры кипения с обратным холодильником при давлении 5 бар. Через 15 мин при кипячении с обратным холодильником вводят 30%-й водный раствор гидроксида натрия (1,2 мол. экв.). Нагревают при кипячении с обратным холодильником в течение 30 мин., затем охлаждают до 50°С при нормальном давлении и вводят 30%-й водный раствор гидроксида натрия (2,4 мол. экв.). Через 2 ч при 50°С, охлаждают до 20°С, затем фильтруют и осадок промывают метанолом (2 x 3 об.).
Неочищенный диосмин растворяют в 2,5 мол. экв. гидроксида натрия и воды (2,5 об.) при 20°С.
Добавляют серную кислоту, чтобы отрегулировать рН от 2 до 4. Выдерживают в течение 30 мин. при 20°С, фильтруют, промывают 2 раза водой (2 x 5 об.) и сушат.
Выход в пересчете на гесперидин: 83,8%
Чистота (ВЭЖХ): 90,6%
Содержание 6-йододиосмина: 0,3%
Содержание изороифолина: 2,0%.
Пример 2: Диосмин
Стадия А: Ацетилированный диосмин
В реактор при температуре 20-25°С загружают ацетат калия (207,1 ммоль) и уксусный ангидрид (6291,9 ммоль).
Суспензию нагревают при перемешивании до 100°С, затем загружают гесперидин (5 х 137,6 ммоль; титр ВЭЖХ: 91,7% и изонарингин 3,6%). Перемешивание продолжают при нагревании до 100°С, затем нагревают до 132°С в течение 15 мин. при перемешивании. В конце нагревания смесь становится прозрачным раствором. Раствор оставляют перемешиваться в течение 120 мин. при 132°С, затем охлаждают до 105°С.
Загружают водный раствор йодида натрия (68,8 ммоль в 40 г воды). Вливают при 105°С в 35% перекись водорода (717,1 ммоль), стабилизированную 0,1% серной кислотой.
Оставляют перемешиваться в течение 30 мин. при 105°С, затем охлаждают до 100°С при перемешивании и осаждают в химическом стакане, содержащем воду (около 7 об.), при механическом перемешивании при 20-40°С.
После перемешивания в течение 30 мин. при 20-40°С фильтруют в вакууме, осадок промывают водой (9 об.; затем 2 х 2 об.). Выпаривают в течение 16 ч. в вакууме при 20-25°С.
Стадия Б: Диосмин
В автоклав загружают ацетилированный диосмин, полученный на стадии А, и метанол (3,5 об.). Перемешивают, затем нагревают до температуры кипения с обратным холодильником при давлении 5 бар. Через 15 мин при кипячении с обратным холодильником вводят 30%-й водный раствор гидроксида натрия (1,2 мол. экв.). Нагревают при кипячении с обратным холодильником в течение 30 мин., затем охлаждают до 50°С при нормальном давлении и вводят 30%-й водный раствор гидроксида натрия (2,4 мол. экв.). Через 2 ч. при 50°С охлаждают до 20°С, затем фильтруют и осадок промывают метанолом (2 x 3 об.).
Неочищенный диосмин растворяют в 2,5 мол. экв. гидроксида натрия и воды (2,5 об.) при 20°С.
Добавляют серную кислоту, чтобы отрегулировать рН от 2 до 4. Выдерживают в течение 30 мин. при 20°С, фильтруют, промывают 2 раза водой (2 x 5 об.) и сушат.
Выход в пересчете на гесперидин: 81,2%
Чистота (ВЭЖХ): 90,4%
Содержание 6-йододиосмина: 0,29%
Содержание изороифолина: 2,2%.
Пример 3: Диосмин
В автоклав загружают ацетилированный диосмин, полученный на стадии А примера 1 и метанол (3,5 об.), добавляют 2 мол. экв. водного раствора ацетата калия, затем нагревают до температуры кипения с обратным холодильником при давлении от 7 до 8 бар. После этого охлаждают до 50°С и вводят водный раствор калия (4,2 мол. экв.). После контакта при 50°С охлаждают до 20°С, затем фильтруют и промывают метанолом (2 х 1,5 об.).
Неочищенный диосмин растворяют в 2,5 мол. экв. гидроксида натрия и воды (2,5 об.) при 20°С. Добавляют серную кислоту, чтобы отрегулировать рН от 2 до 4. Выдерживают в течение 30 мин. при 20°С, затем фильтруют, промывают 2 раза водой (2 x 5 об.) и сушат.
Выход в пересчете на гесперидин: 87,7%
Чистота (ВЭЖХ): 90,1%
Содержание 6-йододиосмин: не обнаружено (<0,10%)
Пример 4: Ацетилирование диосмина различными донорами йода В трехгорлую колбу объемом 25 мл, снабженную яйцевидной мешалкой и шприцевым насосом, загружают 10 г гесперидина, 0,5 г ацетата калия и 14 мл/15,6 г уксусного ангидрида. Постепенно доводят температуру до 132°С и оставляют на 1 ч. при 130°С.
Охлаждают примерно до 90°С, затем загружают 0,322 г йодида натрия или эквивалентного донора йода и 2,258 г воды. Нагревают до 105°С, затем добавляют 35% перекись водорода (1,1835 мл/1,645 г) и 5,161 г воды.
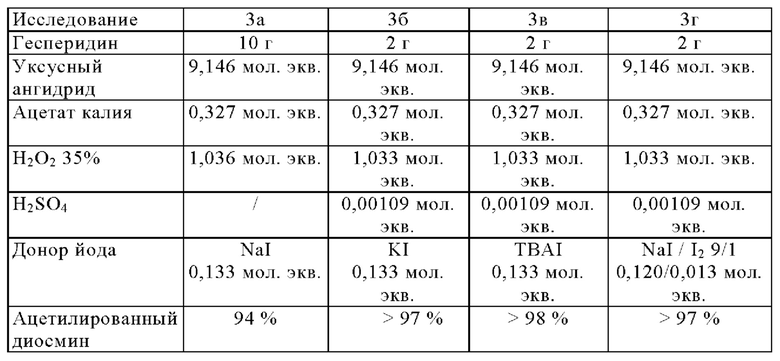
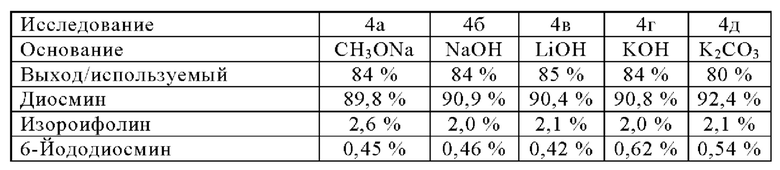
Пример 5: Диосмин с разными основаниями
В автоклав загружают ацетилированный диосмин, полученный на стадии А примера 2 и метанол (3,5 об.). Перемешивают, затем нагревают до температуры кипения с обратным холодильником при давлении 7 бар. Через 15 мин. при кипячении с обратным холодильником вводят 30%-й водный раствор основания (1,2 мол. экв.). Нагревают при кипячении с обратным холодильником в течение 30 мин., затем охлаждают до 50°С при нормальном давлении и вводят 30%-й водный раствор основания (2,4 мол. экв.). Через 2 ч. при 50°С охлаждают до 20°С, затем фильтруют и осадок промывают метанолом (2 x 3 об.).
Пример 6: (сравнительный): Воспроизведение способа из WO 2016/124585 В реактор загружают 40 г уксусного ангидрида, 0,75 г ацетата калия и 30 г гесперидина (чистота 91,3%; изонарингина 3,8%). Затем реакционную смесь нагревают до 115-120°С, поддерживая эту температуру примерно в течение часа, затем смесь охлаждают до 60-70°С.
Добавляют раствор йодида натрия (0,9 г) в воде (6 мл) и реакционную смесь нагревают до температуры кипения с обратным холодильником. Затем к реакционной смеси добавляют 35 мл раствора перекиси водорода с концентрацией 5,4% (мас.), стабилизированной серной кислотой, поддерживая кипячение с обратным холодильником. После этого реакционную смесь охлаждают до 40-50°С и к реакционной смеси добавляют гидроксид калия (10 г); затем рН составляет 4. После этого смесь нагревают до 115-120°С в течение 3 часов, затем охлаждают до 30°С.
Реакционную смесь добавляют в реактор, содержащий водный раствор 2 н. гидроксида натрия (300 мл). Через 1 ч. 30 мин. добавляют серную кислоту до тех пор, пока рН не достигнет 7,5. Затем осадок фильтруют и промывают водой, чтобы получить влажный неочищенный диосмин.
Полученный таким образом неочищенный диосмин кристаллизуют, растворяя его в водном растворе гидроксида натрия, затем подкисляя его серной кислотой до осаждения продукта.
Твердое вещество фильтруют, промывают водой и сушат.
Анализ (ВЭЖХ):

Настоящее изобретение относится к области органической химии, конкретно к технологии получения диосмина, который используют при лечении хронической венозной недостаточности и геморроя. Способ получения диосмина включает ацетилирование гесперидина, окисление ацетилированного гесперидина до ацетилированного диосмина донором йода при температуре от 90 до 120°С, кипячение ацетилированного диосмина со спиртом в присутствии основания в автоклаве с обратным холодильником при давлении от 5 до 8 бар. Затем снимают защиту с ацетилированного диосмина для получения диосмина путем нагревания в присутствии основания, выбранного из гидроксида натрия, калия или лития, карбоната калия, метилата натрия или этилата натрия, отдельно или в смеси с ацетатом натрия или калия. На последнем этапе проводят последовательную очистку диосмина обработкой основанием и кислотой. Техническим результатом изобретения является уменьшение содержания примесей 6-йододиосмина и изороифолина в полученном целевом соединении и предоставление технологии синтеза диосмина без использования токсичного пиридина. 12 з.п. ф-лы, 4 табл., 14 пр.
1. Способ получения диосмина путем
а) ацетилирования гесперидина,
б) окисления ацетилированного гесперидина до ацетилированного диосмина донором йода при температуре от 90 до 120°С,
в) нагревания ацетилированного диосмина в автоклаве при давлении от 5 до 8 бар при кипячении с обратным холодильником со спиртом, в присутствии основания, выбранного из ацетата натрия или калия, гидроксида натрия, калия или лития, карбоната калия, метилата натрия или этилата натрия, отдельно или в смеси с другим из этих оснований, затем
г) снятия защиты с ацетилированного диосмина до диосмина путем нагревания в присутствии основания, выбранного из гидроксида натрия, калия или лития, карбоната калия, метилата натрия или этилата натрия, отдельно или в смеси с ацетатом натрия или калия,
д) очистки обработкой основанием/кислотой.
2. Способ по п. 1, в котором полученный диосмин содержит другие флавоноиды.
3. Способ по любому из пп. 1 или 2, в котором полученный диосмин содержит менее 0,6% 6-иододиосмина и менее 3,0% изороифолина.
4. Способ по любому из пп. 1-3, в котором количество уксусного ангидрида составляет от 8 до 10 молярных эквивалентов по отношению к используемому гесперидину.
5. Способ по любому из пп. 1-4, в котором реакцию ацетилирования (а) проводят при температуре от 40°С до 135°С.
6. Способ по любому из пп. 1-5, в котором донор йода выбирают из NaI/H2O2, KI/H2O2, TBAI/H2O2 и NaI/I2/H2O2.
7. Способ по п. 6, в котором донор йода представляет собой NaI в количестве от 0,05 до 0,2 молярных эквивалентов по отношению к используемому гесперидину.
8. Способ по любому из пп. 1-7, в котором количество перекиси водорода равно от 1,0 до 1,2 молярных эквивалентов по отношению к используемому гесперидину.
9. Способ по любому из пп. 1-8, в котором ацетилированный диосмин, полученный в конце стадии окисления (б), выделяют путем осаждения в воде перед использованием на стадии в).
10. Способ по любому из пп. 1-9, в котором основание, используемое на стадии в), представляет собой водный раствор гидроксида натрия или калия, водный раствор ацетата натрия или калия или смесь гидроксида натрия или калия и ацетата натрия или калия в водном растворе.
11. Способ по любому из пп. 1-10, в котором спирт, используемый на стадии в), представляет собой метанол, этанол или изопропанол.
12. Способ по любому из пп. 1-11, в котором количество основания, используемого на стадии (в), составляет от 0,5 до 2,5 молярных эквивалентов по отношению к используемому гесперидину.
13. Способ по любому из пп. 1-12, в котором количество основания, добавляемого на стадии деацетилирования (г), составляет от 2 до 4,5 молярных эквивалентов по отношению к используемому гесперидину.
| ПРИСПОСОБЛЕНИЕ К БЕСЧЕЛНОЧНЫМ ТКАЦКИМ СТАНКАМ ДЛЯ ОБРЕЗАНИЯ УТОЧНОЙ НИТИ | 1932 |
|
SU32402A1 |
| ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ ФАРМАКОПЕЙНОГО ДИОСМИНА И ЕГО КРИСТАЛЛИЧЕСКАЯ ФОРМА (ВАРИАНТЫ) | 2011 |
|
RU2481353C1 |
| CN 102070689 B, 28.11.2012 | |||
| Способ оценки риска преждевременного разрыва плодных оболочек у беременных | 2020 |
|
RU2740950C1 |
| WO 2010092592 A2, 19.08.2010 | |||
| Способ получения термопластичного полимерно-керамического филамента для 3-D печати методом послойного наплавления | 2020 |
|
RU2760015C1 |
| Устройство для реверсирования направления вращения двигателей постоянного тока | 1926 |
|
SU11009A1 |
Авторы
Даты
2025-03-03—Публикация
2021-07-08—Подача