ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет по предварительной заявке на патент США №62/976,386, поданной 14 февраля 2020 г., озаглавленной «NEOANTIGENS EXPRESSED IN MULTIPLE MYELOMA AND THEIR USES», которая полностью включена в настоящий документ путем ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка содержит перечень последовательностей, представленный в электронном виде в формате ASCII и настоящим включенный в данный документ посредством ссылки во всей своей полноте. Копия перечня в формате ASCII, созданная 22 января 2021 г., называется JBI6239WOPCT1_SL.txt и имеет размер 154 445 байт.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к неоантигенам множественной миеломы, кодирующим их полинуклеотидам, векторам, клеткам-хозяевам, вакцинам, содержащим неоантигены, белковым молекулам, связывающим неоантигены множественной миеломы, а также способам их получения и применения.
УРОВЕНЬ ТЕХНИКИ
Множественная миелома приводит к значительному уровню заболеваемости и смертности. Она составляет приблизительно 1% всех злокачественных новообразований и 13% гематологических раковых заболеваний во всем мире. В ЕС и США множественную миелому диагностируют примерно у 50000 пациентов в год, и 30000 пациентов в год умирают от множественной миеломы.
У большинства пациентов с множественной миеломой вырабатывается моноклональный белок (парапротеин, М-белок или М-компонент), который представляет собой иммуноглобулин (Ig) или его фрагмент, который утратил свою функцию (Kyle and Rajkumar, Leukemia 23: 3-9, 2009; Palumbo and Anderson, N Engl J Med 364: 1046-1060, 2011). У пациентов нарушается нормальный уровень иммуноглобулина, что приводит к восприимчивости к инфекциям. Пролиферирующие клетки множественной миеломы вытесняют нормальный костный мозг, что приводит к дисфункции нормальной кроветворной ткани и разрушению нормальной архитектуры костного мозга, что отражается клиническими проявлениями, такими как анемия, парапротеин в сыворотке или моче и резорбция костной ткани в виде диффузного остеопороза или литических поражений на рентгеновских снимках (Kyle et al., Mayo ClinProc 78: 21-33, 2003). Кроме того, часто наблюдается гиперкальциемия, почечная недостаточность или отказ почек, а также неврологические осложнения. У очень небольшого числа пациентов диагностируют несекретирующую множественную миелому.
Варианты лечения множественной миеломы варьируют в зависимости от возраста, сопутствующих патологий, агрессивности заболевания и родственных прогностических факторов (Palumbo and Anderson, N Engl J Med 364: 1046-1060, 2011). Вновь выявленные пациенты с множественной миеломой, как правило, делятся на 2 субпопуляции, как правило, определяемые их возрастом и соответствием последующему подходу к лечению. Молодым пациентам, как правило, назначают индукционную схему лечения с последующей консолидирующей терапией с использованием высокодозной химиотерапии (ВДХТ) и аутологичной трансплантации стволовых клеток (АТСК). Для тех, кто не подходит для ВДХТ и АТСК, в качестве стандарта лечения в настоящее время рассматривается более длительная терапия с использованием многоагентных комбинаций, включающих алкиляторы, стероиды в высоких дозах и новые агенты. Как правило, пациенты в возрасте от 65 лет или со значительными сопутствующими патологиями обычно не считаются соответствующими условиям ВДХТ и АТСК. В течение многих лет пероральная комбинация мелфалан-преднизон (MP) считалась стандартом лечения пациентов со множественной миеломой, которым не подходит АТСК (Gay and Palumbo, Blood Reviews 25: 65-73, 2011). Появление иммуномодулирующих препаратов (IMiD) и ингибиторов протеасом (PI) привело к появлению множества новых вариантов лечения для вновь диагностированных пациентов, которые не считаются соответствующими условиям терапии на основе трансплантации.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем описании предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагменты.
В настоящем описании также предложен выделенный гетерологичный полипептид, содержащий два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагменты.
В настоящем описании также предложен выделенный полинуклеотид, содержащий последовательность SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422 или их фрагменты.
В настоящем описании также предложены векторы, содержащие полинуклеотиды, кодирующие полипептиды, представленные в настоящем документе.
В настоящем описании также предложены вирусы или рекомбинантные вирусы, содержащие векторы в соответствии с настоящим описанием.
В настоящем описании также предложены клетки, содержащие векторы в соответствии с настоящим описанием или рекомбинантные вирусы в соответствии с настоящим описанием или трансдуцированные ими.
В настоящем описании также предложена вакцина, содержащая полинуклеотиды в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая полипептиды в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая векторы в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая рекомбинантные вирусы в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая самореплицирующуюся молекулу РНК в соответствии с настоящим описанием.
В настоящем описании также предложен способ предотвращения или лечения множественной миеломы у субъекта, включающий введение субъекту терапевтически эффективного количества одной или более вакцин в соответствии с настоящим описанием, или одного или более вирусов или рекомбинантных вирусов в соответствии с настоящим описанием, или одной или более фармацевтических композиций в соответствии с настоящим описанием.
В настоящем описании также предложен способ индукции иммунного ответа против одной или более аминокислотных последовательностей SEQ ID NO: 1,3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 у субъекта, включающий введение субъекту одной или более вакцин в соответствии с настоящим описанием или одного или более рекомбинантных вирусов в соответствии с настоящим описанием, содержащих полинуклеотиды в соответствии с настоящим описанием, и при этом рекомбинантный вирус представляет собой Ad26, GAd20, MVA, и/или введение самореплицирующейся молекулы РНК, кодирующей полипептиды в соответствии с настоящим описанием.
В настоящем описании также предложен способ лечения или предотвращения множественной миеломы у субъекта, включающий
введение субъекту терапевтически эффективного количества композиции, содержащей рекомбинантный вирус, и/или композиции, содержащей самореплицирующуюся молекулу РНК, кодирующую гетерологичный полипептид, содержащий два, три, четыре, пять, шесть, семь, восемь, девять, десять, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203 или 204 полипептида, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов. В некоторых вариантах осуществления рекомбинантный вирус представляет собой вирус Ad26, GAd20 или MVA. В некоторых вариантах осуществления введение включает одно или более введений композиции.
В настоящем описании также предложен способ лечения или предотвращения множественной миеломы у субъекта, включающий введение субъекту
первой композиции, содержащей первый гетерологичный полинуклеотид, кодирующий первый гетерологичный полипептид, причем первый гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов; и
второй композиции, содержащей второй гетерологичный полинуклеотид, кодирующий второй гетерологичный полипептид, причем второй гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов; при этом первый гетерологичный полипептид и второй гетерологичный полипептид имеют разные аминокислотные последовательности.
В настоящем описании также предложен способ лечения или предотвращения множественной миеломы у субъекта, включающий введение субъекту терапевтически эффективного количества композиции, содержащей рекомбинантный вирус, и/или композиции, содержащей самореплицирующуюся молекулу РНК, кодирующую гетерологичный полипептид, выбранный SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421
В настоящем описании также предложен способ индукции иммунного ответа у субъекта, включающий введение субъекту композиции, содержащей гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов; и при этом введение включает одно или более введений композиции, и причем гетерологичные полипептиды имеют различные аминокислотные последовательности.
В настоящем описании также представляет способ индукции иммунного ответа у субъекта, включающий введение субъекту композиции, содержащей гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377,379, 381, 383, 385 и 421
В настоящем описании также предложена выделенная белковая молекула, которая специфически связывается с полипептидом в соответствии с настоящим описанием.
В настоящем описании также предложен способ предотвращения или лечения множественной миеломы у субъекта, включающий введение субъекту белковой молекулы в соответствии с настоящим описанием.
В настоящем описании также предусмотрено введение антитела к CTLA-4, антитела к PD-1 или антитела к PD-L1 в комбинации с любой из композиций, содержащих полинуклеотиды, полипептиды, векторы или вирусы, раскрытые в настоящем документе.
Следует понимать, что вышеописанные варианты осуществления изобретения охватывают полипептиды, содержащие также, в дополнение к конкретно перечисленным полипептидам и их фрагментам, дополнительные полипептидные последовательности, включая один или более полипептидов, отличных от конкретно перечисленных. Аналогичным образом приведенные выше варианты осуществления настоящего изобретения также охватывают полинуклеотиды, содержащие также, в дополнение к конкретно перечисленным полинуклеотидам и их фрагментам, дополнительные полинуклеотидные последовательности, включая один или более полинуклеотидов, отличных от конкретно перечисленных полинуклеотидов.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На ФИГ. 1 показаны в виде рисунка химерные сквозные слияния между геном А и геном В. Неоантигенные пептидные последовательности возникают на участке соединения точек разрыва.
На ФИГ. 2 показаны в виде рисунка слияния генов в результате хромосомного изменения, такого как транслокации ДНК.
На ФИГ. 3 показаны в виде рисунка варианты сплайсинга с 5' и 3'-концевыми сайтами альтернативного сплайсинга, сохраненными нитронами, исключенными экзонами или альтернативными терминациями или вставками.
На ФИГ. 4 в виде рисунка представлен подход к идентификации вариантов сплайсинга.
На ФИГ. 5А, ФИГ. 5В, ФИГ. 5С и ФИГ. 5D показана тепловая карта, представляющая ограниченную опухолью экспрессию неоантигенов множественной миеломы (ММ). Экспрессия этих антигенов не поддается выявлению ни в здоровых тканях или ни в иммунных клетках, полученных от здоровых доноров. Типы иммунных клеток (первые 15 рядов) были получены от трех здоровых доноров (ID донора: D001003103, D001000682 и D001004622). Образцы CD138+ ММ маркированы префиксом «ММ». Исходные значения Ct нормализовали по отношению к экспрессии эндогенного контрольного гена, RPL13A. Черные клетки представляют высокую экспрессию (ΔCt ниже 15) в каждом образце. Четыре неоантигена (FUS7, FUS20, AS43 и AS76), демонстрирующие экспрессию в нормальных В-клетках и плазмоцитах, полученных от донора, сохраняли в этой группе.
На ФИГ. 6А, ФИГ. 6В, ФИГ. 6С и ФИГ. 6D показана тепловая карта, представляющая кандидатов неоантигенов множественной миеломы с экспрессией в обоих контролях (тканях и иммунных клетках, полученных от здоровых доноров) и образцах опухоли. Типы иммунных клеток (первые 15 рядов) были получены от трех здоровых доноров (ID донора: D001003103, D001000682 и D001004622). Образцы CD138+ ММ маркированы префиксом «ММ». Исходные значения Ct нормализовали по отношению к экспрессии эндогенного контрольного гена, RPL13A. Черные клетки представляют высокую экспрессию (ΔCt ниже 15) в каждом образце.
На ФИГ. 7А и ФИГ. 7В показаны репрезентативные точечные графики, изображающие положительные иммуногенные ответы неоантигенов с использованием анализа рестимуляции экзогенного аутологичного здорового донора. Ответы иммуногенности измеряли путем оценки двойных положительных клеток TNFα IFNγ в популяциях CD4+ и/или CD8+ Т-клеток. Считается, что ответ является положительным, если двойная положительная фракция TNFα IFNγ была больше или равна трехкратному превышению над нестимулированными клетками (отрицательный контроль ДМСО) с минимальной частотой >=0,01%.
На ФИГ. 8А и ФИГ. 8В показано количество доноров с положительными иммуногенными ответами (CD8+ и/или CD4+ Т-клетки) для неоантигенов, связанных со слиянием генов.
На ФИГ. 9А и ФИГ. 9В показано количество доноров с положительными иммуногенными ответами (CD8+ и/или CD4+ Т-клетки) для неоантигенов, связанных с альтернативным сплайсингом.
ПОДРОБНОЕ ОПИСАНИЕ
Определения
Все публикации, включая, без ограничений, патенты и заявки на патенты, цитируемые в данном описании, включены в настоящий документ путем ссылки, как если бы они были полностью изложены в данном документе.
Следует понимать, что применяемые в настоящем документе термины предназначены только для описания конкретных вариантов осуществления и не имеют ограничительного характера. Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют общепринятое значение, понятное любому специалисту в области, к которой относится изобретение.
В настоящем документе описаны иллюстративные способы и материалы, хотя при практическом осуществлении для проверки настоящего изобретения могут быть использованы любые способы и материалы, подобные или эквивалентные тем, которые описаны в настоящем документе. При описании и изложении формулы настоящего изобретения будут применяться следующие термины.
При использовании в этом описании и в прилагаемой формуле изобретения формы единственного числа включают и множественное число, если содержание текста ясно не указывает на иное. Так, например, ссылка на «клетку» включает комбинацию двух или более клеток и т.п.
Переходные термины «содержащий», «состоящий по существу из» и «состоящий из» предназначены для обозначения их по существу общепринятых патентных значений; т.е. (i) термин «содержащий», который является синонимом терминам «включающий», «содержащий» или «характеризующийся», является включающим или неограниченным и не исключает дополнительные, неуказанные элементы или стадии способа; (ii) термин «состоящий из» исключает любые элемент, стадию или ингредиент, не указанные в пункте формулы изобретения; и (iii) «состоящий по существу из» ограничивает объем формулы изобретения конкретными материалами или стадиями «и теми, которые не оказывают существенного влияния на основные и новые характеристики» заявленного изобретения. Варианты осуществления, описанные в отношении фразы «содержащий» (или его эквивалентов), обеспечивают такое же значение, как варианты осуществления, описанные независимо друг от друга в отношении фразы «состоящий из» и «состоящий по существу из».
В контексте настоящего описания и прилагаемой формулы изобретения фраза «а также их фрагменты» при добавлении к списку включает в себя все члены соответствующего списка. Список может содержать группу Маркуша, так что, например, фраза «группа, состоящая из пептидов А, В и С и их фрагментов» указывает или перечисляет группу Маркуша, включая А, В, С, фрагменты А, фрагменты В и фрагменты С.
Термин «выделенный» относится к однородной популяции молекул (таких как синтетические полинуклеотиды или полипептиды), которые были по существу отделены и/или очищены от других компонентов той системы, в которой данные молекулы формировались, такой как рекомбинантная клетка, а также к белку, который был подвергнут по меньшей мере одной стадии очистки или выделения. Термин «выделенное» относится к антителу, которое по существу не содержит иных клеточных материалов и/или химических веществ, и охватывает молекулы, которые выделены с большей чистотой, такой как 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% чистотой.
Термин «полинуклеотид» относится к синтетической молекуле, содержащей цепь нуклеотидов, ковалентно связанных через сахарофосфатную основную цепь или другую эквивалентную ковалентную химическую структуру. кДНК является типичным примером полинуклеотида.
Термин «полипептид» или «белок» относится к молекуле, которая содержит по меньшей мере два аминокислотных остатка, связанных пептидной связью с образованием полипептида. Малые полипептиды, содержащие менее 50 аминокислотных остатков, могут называться «пептидами».
Термин «иммуногенный фрагмент» относится к полипептиду, который распознается цитотоксическими Т-лимфоцитами, хелперными Т-лимфоцитами или В-клетками, когда фрагмент находится вместе с молекулами МНС класса I или МНС класса II.
Термин «внутри рамки считывания» относится к рамке считывания кодонов в первом полинуклеотиде, которая совпадает с рамкой считывания кодонов во втором полинуклеотиде, которые связаны вместе с образованием гетерологичного полинуклеотида. Гетерологичный полинуклеотид внутри рамки считывания кодирует гетерологичный полипептид, кодируемый как первым полинуклеотидом, так и вторым полинуклеотидом.
Термин «иммуногенный» относится к полипептиду, который содержит один или более иммуногенных фрагментов.
Термин «гетерологичный» относится к двум или более полинуклеотидам или двум или более полипептидам, не находящимся в одинаковых отношениях друг к другу в природе.
Термин «гетерологичный полинуклеотид» относится к не встречающемуся в природе полинуклеотиду, который кодирует два или более неоантигенов, как описано в настоящем документе.
Термин «гетерологичный полипептид» относится к не встречающемуся в природе полипептиду, содержащему два или более неоантигенных полипептида, как описано в настоящем документе.
Термин «не встречающийся в природе» относится к молекуле, которая не существует - в природе.
Термин «вектор» относится к полинуклеотиду, который способен к удвоению внутри биологической системы, или может быть перемещен между такими системами. Полинуклеотиды-векторы, как правило, содержат элементы, такие как точки начала репликации, сигнал полиаденилирования или селективные маркеры, функция которых состоит в том, чтобы способствовать удвоению или сохранению таких полинуклеотидов в биологической системе. Примеры таких биологических систем могут включать клетку, вирус, животное, растение и реконструированные биологические системы, использующие биологические компоненты, способные к удвоению вектора. Содержащий вектор полинуклеотид может представлять собой молекулы ДНК или РНК или их гибрид.
Термин «экспрессионный вектор» относится к вектору, который можно использовать в биологической системе или реконструированной биологической системе для управления трансляцией полипептида, кодируемого полинуклеотидной последовательностью, присутствующей в экспрессионном векторе.
Термин «вирусный вектор» относится к конструкции вектора, которая включает по меньшей мере один полинуклеотидный элемент вирусного происхождения и может быть упакована в частицу вирусного вектора.
Термин «неоантиген» относится к полипептиду, присутствующему в CD138+клетках+клетках, выделенных из аспиратов костного мозга от пациентов с множественной миеломой, и имеющему по меньшей мере одно изменение, которое отличает его от соответствующего полипептида дикого типа, присутствующего в незлокачественной ткани, например, посредством мутации в опухолевой клетке или посттрансляционной модификации, специфической для опухолевой клетки. Мутация может включать вставку или делецию со сдвигом рамки считывания или без сдвига рамки считывания, миссенс-замену или нонсенс-замену, изменение сайта сплайсинга, варианты аберрантного сплайсинга, геномную перестройку или слияние генов или любое геномное или экспрессионное изменение, приводящее к образованию неоантигена.
Термин «распространенность» относится к процентной доле исследуемой популяции, имеющей неоантиген множественной миеломы.
Термин «рекомбинантный» относится к полинуклеотидам, полипептидам, векторам, вирусам и другим макромолекулам, которые получены, экспрессированы, созданы или выделены рекомбинантными средствами.
Термин «вакцина» относится к композиции, которая содержит один или более иммуногенных полипептидов, иммуногенных полинуклеотидов или фрагментов или любую их комбинацию, намеренно введенную для индуцирования приобретенного иммунитета у реципиента (например, у субъекта).
Термины «лечить», «лечение» или «терапия» заболевания или расстройства, такого как рак, относятся к достижению одной или более следующих целей: уменьшение тяжести и/или продолжительности расстройства, замедление нарастания выраженности симптомов, характерных для этого расстройства, ограничение или предотвращение рецидива расстройства у субъектов, которые ранее страдали расстройством, либо ограничение или предотвращение рецидива симптомов у субъектов с ранее проявлявшимися симптомами расстройства.
Термины «предотвращать», «предотвращающий», «предотвращение» или «профилактика» заболевания или расстройства означают предотвращение возникновения у субъекта расстройства.
Термин «терапевтически эффективное количество» относится к некоторому количеству, эффективному в дозах и в течение периодов времени, необходимых для достижения желаемого терапевтического результата. Терапевтически эффективное количество может изменяться в зависимости от таких факторов, как течение заболевания, возраст, пол и масса тела субъекта, а также от способности терапевтического средства или комбинации терапевтических средств вызывать у субъекта желаемый ответ. Примеры показателей эффективного терапевтического средства или комбинации терапевтических средств, которые включают, например, улучшенное самочувствие пациента.
Термин «рецидивирующий» относится к повторному возникновению заболевания или признаков и симптомов заболевания после периода улучшения после предшествующего лечения терапевтическим средством.
Термин «рефрактерный» относится к заболеванию, которое не реагирует на лечение. Рефрактерное заболевание может быть устойчивым к лечению до или в начале лечения или рефрактерное заболевание может стать устойчивым во время лечения.
Термин «репликон» относится к вирусной нуклеиновой кислоте, которая способна направлять генерацию собственных копий и включает РНК, а также ДНК. Например, для получения одноцепочечного РНК-транскрипта, составляющего репликон артеривируса, можно использовать версии двухцепочечной ДНК геномов артеривируса. Как правило, репликон вируса содержит весь геном вируса. Термин «субгеномный репликон» относится к вирусной нуклеиновой кислоте, которая содержит что-либо меньшее, чем полный комплемент генов и других признаков вирусного генома, но все же способна направлять создание самих копий. Например, субгеномные репликоны артеривируса могут содержать большинство генов неструктурных белков вируса, но в них отсутствует большинство генов, кодирующих структурные белки. Субгеномные репликоны способны направлять экспрессию всех вирусных генов, необходимых для репликации вирусного субгенома (репликация субгеномного репликона), без продукции вирусных частиц.
Термин «РНК-репликон» (или «самореплицирующаяся молекула РНК») относится к РНК, содержащей всю генетическую информацию, необходимую для направления ее собственной амплификации или саморепликации в пределах пермиссивной клетки. Чтобы направлять свою собственную репликацию, молекула РНК 1) кодирует полимеразу, репликазу или другие белки, которые могут взаимодействовать с белками вируса или клетки-хозяина, нуклеиновыми кислотами или рибонуклеотидными белками для катализирования процесса амплификации РНК; и 2) содержат цис-действующие последовательности РНК, необходимые для репликации и транскрипции кодируемой репликоном РНК. Самореплицирующуюся РНК, как правило, получают из геномов РНК-вирусов с положительной цепью и ее можно использовать в качестве основы для введения инородных последовательностей в клетки-хозяева путем замены вирусных последовательностей, кодирующих структурные или неструктурные гены, или вставки инородных последовательностей, кодирующих структурные или неструктурные гены, на 5'-конце или 3'-конце. Инородные последовательности также могут быть введены в субгеномные области альфавирусов. Самореплицирующаяся РНК может быть упакована в рекомбинантные вирусные частицы, такие как рекомбинантные альфавирусные частицы, или альтернативно доставлена хозяину с помощью липидных наночастиц (LNP).
Самореплицирующаяся РНК может составлять по меньшей мере 1 т.п.н., или по меньшей мере 2 т.п.н., или по меньшей мере 3 т.п.н., или по меньшей мере 4 т.п.н., или по меньшей мере 5 т.п.н., или по меньшей мере 6 т.п.н., или по меньшей мере 7 т.п.н., или по меньшей мере 8 т.п.н., или по меньшей мере 10 т.п.н., или по меньшей мере 12 т.п.н., или по меньшей мере 15 т.п.н., или по меньшей мере 17 т.п.н., или по меньшей мере 19 т.п.н., или по меньшей мере 20 т.п.н., или может составлять 100 п.о. - 8 т.п.н. или 500 п.о. - 8 т.п.н. или 500 п.о. - 7 т.п.н. или 1-7 т.п.н. или 1-8 т.п.н. или 2-15 т.п.н. или 2-20 т.п.н. или 5-15 т.п.н. или 5-20 т.п.н. или 7-15 т.п.н. или 7-18 т.п.н. или 7-20 т.п.н. по размеру. Самореплицирующиеся РНК описаны, например, в WO 2017/180770, WO 2018/075235, WO 2019143949 A2,
«Вновь диагностированный» относится к субъекту-человеку, у которого было диагностировано заболевание, такое как множественная миелома, но лечение еще не начато.
Термин «пациент» включает в себя любого человека или не относящееся к человеку животное. Термин «не относящееся к человеку животное» включает в себя всех позвоночных, например млекопитающих и немлекопитающих, таких как приматы, овцы, собаки, кошки, лошади, коровы, куры, амфибии, рептилии и т.д. Термины «индивид» и «пациент» в настоящем документе могут применяться взаимозаменяемо.
Выражение «в комбинации с» означает, что два или более терапевтических средства вводят субъекту вместе в смеси, одновременно в виде отдельных средств или последовательно в виде отдельных средств в любом порядке.
Термины «усиливать» или «индуцировать» в отношении иммунного ответа относятся к повышению масштаба и/или эффективности иммунного ответа или увеличению длительности иммунного ответа. Термины используются взаимозаменяемо с термином «усиливаться».
Термин «иммунный ответ» относится к любому ответу на иммуногенный полипептид, или полинуклеотид, или фрагмент иммунной системы субъекта, относящегося к позвоночным. Примеры иммунных ответов включают местные и системные клеточные ответы, а также гуморальный иммунитет, такой как ответы цитотоксических Т-лимфоцитов (CTL), включая антиген-специфическую индукцию CTL CD8+, ответы хелперных Т-клеток, включая пролиферативные Т-клеточные ответы и высвобождение цитокинов, и В-клеточные ответы, включая выделение антител.
Термины «специфически связывается», «специфическое связывание», «специфически связывает» или «связывает» относятся к связыванию белковой молекулы с антигеном или эпитопом в пределах антигена (например, с неоантигеном множественной миеломы) с большей аффинностью, чем у других антигенов. Как правило, белковая молекула связывается с антигеном или эпитопом в пределах антигена с равновесной константой диссоциации (KD) около 1×10-7 М или менее, например около 5×10-8 М или менее, около 1×10-8 М или менее, около 1×10-9 М или менее, около 1×10-10 М или менее, около 1×10-11 М или менее или около 1×10-12 М или менее, как правило, со значением KD, которое по меньшей мере в сто раз ниже его значения KD связывания с неспецифическим антигеном (например, BSA, казеином). В контексте неоантигенов множественной миеломы, описанных в настоящем документе, термин «специфическое связывание» относится к связыванию белковой молекулы с неоантигеном множественной миеломы без обнаружимого связывания с белком дикого типа, вариантом которого является неоантиген.
Термины «вариант», «мутант» или «измененный» относятся к полипептиду или полинуклеотиду, который отличается от эталонного полипептида или эталонного полинуклеотида одной или более модификациями, например одной или более заменами, вставками или делециями.
Термин «антитело» относится к молекуле иммуноглобулина, включая моноклональные антитела, в том числе мышиные, человеческие, гуманизированные и химерные моноклональные антитела, антигенсвязывающие фрагменты, биспецифические или мультиспецифические антитела, димерные, тетрамерные или мультимерные антитела, одноцепочечные антитела, доменные антитела и любую другую модифицированную конфигурацию молекулы иммуноглобулина, которая содержит антигенсвязывающий сайт требуемой специфичности.
Термин «альтернативные каркас» относится к одноцепочечному белковому каркасу, который содержит структурированную сердцевину, связанную с вариабельными доменами с высокой конформационной толерантностью. Вариабельные домены допускают изменение, внесенное без ущерба для целостности каркаса, и, следовательно, вариабельные домены можно конструировать и выбирать для связывания со специфическим антигеном.
Термин «химерный антигенный рецептор» или «CAR», относится к сконструированным Т-клеточным рецепторам, которые прививают лиганд или антигенную специфичность на Т-клетки (например, наивные Т-клетки, центральные Т-клетки памяти, эффекторные Т-клетки памяти или их комбинации). CAR также известны как искусственные Т-клеточные рецепторы, химерные Т-клеточные рецепторы или химерные иммунорецепторы. CAR содержат внеклеточный домен, способный связываться с антигеном, трансмембранный домен и по меньшей мере один внутриклеточный домен. Внутриклеточный домен CAR содержит полипептид, который, как известно, выполняет функцию домена, передающего сигнал для активации или ингибирования биологического процесса в клетке. Трансмембранный домен содержит любой пептид или полипептид, который, как известно, охватывает клеточную мембрану и может выполнять функцию связывания внеклеточного и сигнального доменов. Химерный антигенный рецептор может дополнительно содержать шарнирный домен, который служит в качестве линкера между внеклеточным и трансмембранным доменами.
Термины «Т-клеточный рецептор» или «TCR» относятся к молекуле, способной распознавать пептид, если он представлен молекулой МНС. Гетеродимер TCR природного происхождения состоит из альфа (α) и бета (β) цепи в около 95% Т-клеток, тогда как приблизительно 5% Т-клеток имеют TCR, состоящий из гамма (γ) и дельта (δ) цепей. Каждая цепь природного TCR является членом суперсемейства иммуноглобулинов и имеет один N-концевой вариабельный (V) домен иммуноглобулина (Ig), один Ig-константный (С) домен, трансмембранную область и короткий цитоплазматический хвост на С-конце. Вариабельный домен как α-цепи, так и β-цепи TCR имеет три гипервариабельных или определяющих комплементарность участка (CDR) - CDR1, CDR2 и CDR3, которые отвечают за распознавание обработанных антигенов, представленных на МНС.
TCR может представлять собой полноразмерный гетеродимер α/β или γ/δ или растворимую молекулу, содержащую часть внеклеточного домена TCR, которая сохраняет связывание комплекса пептид/МНС. TCR может быть сконструирован в виде одноцепочечного TCR.
Термин «комплекс Т-клеточного рецептора» или «комплекс TCR» относится к известному комплексу TCR, состоящему из цепей TCRα и TCRβ, молекул CD3ε, CD3γ, CD3δ и CD3ζ. В некоторых случаях цепи TCRα и TCRβ замещены цепями TCRγ и TCRδ. аминокислотные последовательности различных белков, образующих TCR-комплекс, хорошо известны.
Термины «Т-клетка» и «Т-лимфоцит» являются взаимозаменяемыми и используются в настоящем документе как синонимы. Т-клетка включает тимоциты, наивные Т-лимфоциты, Т-клетки памяти, незрелые Т-лимфоциты, зрелые Т-лимфоциты, покоящиеся Т-лимфоциты или активированные Т-лимфоциты. Т-клетка может представлять собой клетку Т-хелпер (Th), например Т-хелпер 1 (Th1) или Т-хелпер 2 (Th2). Т-клетка может представлять собой хелперную Т-клетку (HTL; CD4+ Т-клетка) CD4+ Т-клетку, цитотоксическую Т-клетку (CTL; CD8+ Т-клетка), инфильтрирующую опухоль цитотоксическую Т-клетку (TIL; CD8+ Т-клетка), CD4+CD8+ Т-клетку или любую другую подгруппу Т-клеток. Также включены «NKT-клетки», относящиеся к специализированной популяции Т-клеток, которые экспрессируют полуинвариантный αβ Т-клеточный рецептор, но также экспрессируют различные молекулярные маркеры, которые, как правило, ассоциированы с Nk-клетками, такими как NK1.1. NKT-клетки включают NK1.1+ и NK1.1-, а также клетки CD4+, CD4-, CD8+ и CD8-. TCR на NKT-клетках уникален тем, что он распознает гликолипидные антигены, презентированные подобной ГКГС I молекулой CD Id. NKT-клетки могут иметь как защитные, так и вредные эффекты из-за их способности продуцировать цитокины, которые способствуют воспалению или иммунной толерантности. Также включены «гамма-дельта-Т-клетки (γδ Т-клетки)», которые относятся к специализированной популяции, а именно к небольшой подгруппе Т-клеток, имеющей на своей поверхности отдельный TCR, и в отличие от большинства Т-клеток, в которых TCR состоит из двух гликопротеиновых цепей, обозначенных как α- и β-цепи TCR, Т-клеточный рецептор в Т-клетках γδ состоит из γ-цепи и δ-цепи. Т-клетки γδ могут играть роль в иммунонадзоре и иммунорегуляции, и было обнаружено, что они являются важным источником IL-17 и индуцируют устойчивый цитотоксический CD8+ Т-клеточный ответ. Также включены «регуляторные Т-клетки» или «Трег», которые относятся к Т-клеткам, которые подавляют аномальный или избыточный иммунный ответ и играют роль в иммунной толерантности. Treg обычно представляют собой Foxp3-положительные CD4+ Т-клетки и могут также включать Foxp3-отрицательные регуляторные Т-клетки, которые представляют собой IL-10-продуцирующие CD4+ Т-клетки.
Термины «естественный киллер» или «NK-клетка» относятся к дифференцированному лимфоциту с CD16+, CD56+ и/или CD57+ TCR-фенотипом. NK-клетки характеризуются способностью связываться с клетками, которые не экспрессируют «собственные» антигены MHC/HLA, и уничтожать их путем активации специфических цитолитических ферментов, способностью уничтожать опухолевые клетки или другие пораженные клетки, которые экспрессируют лиганд для рецепторов, активирующих NK-клетки, а также способностью высвобождать молекулы белка, называемые цитокинами, которые стимулируют или ингибируют иммунный ответ.
Термин «около» означает «в пределах приемлемого диапазона ошибки» для конкретного значения, определенного обычным специалистом в данной области, причем ошибка отчасти зависит от того, каким образом измерено или определено это значение, т.е. от ограничений системы измерения. Если в примерах или в других разделах настоящего описания в контексте конкретного анализа, результата или варианта осуществления явным образом не указано иное, термин «около» означает «в пределах одного среднеквадратичного отклонения» в соответствии с практикой, принятой в данной области, или «в диапазоне до 5%», в зависимости от того, что больше.
Термин «антигенпрезентирующая клетка» (АПК) относится к любой клетке, которая представляет на своей поверхности антиген в сочетании с молекулой главного комплекса гистосовместимости (МНС) - либо с МНС класса I, либо с МНС класса II, либо с обеими молекулами.
Термины «примирование/стимулирование» или «режим примирования/стимулирования» относятся к способу лечения субъекта, включающему примирование Т-клеточного ответа первой вакциной с последующей стимуляцией иммунного ответа второй вакциной. Первая вакцина и вторая вакцина, как правило, различаются. Такие иммунизации с использованием режима праймирования-бустирования вызывают иммунные ответы большей интенсивности и охвата, чем это возможно при праймировании и бустировании одной и той же вакциной. На этапе праймирования инициируются клеточная память, а на этапе бустирования происходит расширение вторичного иммунного ответа. Бустирование может происходить один или несколько раз.
Термин «вспомогательный элемент» относится к любому полинуклеотидному или полипептидному элементу, функционально связанному с полинуклеотидом или полипептидом, и включает промоторы, энхансеры, сигналы полиаденилирования, стоп-кодоны, белковые метки, такие как гистидиновая метка, и т.п. В настоящем документе вспомогательные элементы включают в себя регуляторные элементы.
Термин «различный» в контексте полипептидных или полинуклеотидных последовательностей означает неидентичные полипептидные или полинуклеотидные последовательности.
Композиции изобретения
Настоящее описание относится к неоантигенам множественной миеломы, кодирующим их полинуклеотидам, векторам, клеткам-хозяевам, вакцинам, содержащим неоантигены или полинуклеотиды, кодирующие неоантигены, белковым молекулам, связывающим неоантигены множественной миеломы, а также способам их получения и применения. В настоящем описании также предложены вакцины, содержащие неоантигены множественной миеломы в соответствии с настоящим описанием, которые преобладают в популяции пациентов с множественной миеломой, таким образом обеспечивая пан-вакцину, которая может использоваться для лечения широкой популяции пациентов с диагностированными различными стадиями множественной миеломы, такими как тлеющая множественная миелома или прогрессирующая множественная миелома.
Раковые клетки продуцируют неоантигены, возникающие в результате геномных изменений и аберрантных транскрипционных программ. Неоантигенная нагрузка у пациентов ассоциировалась с ответом на иммунотерапию (Snyder et al., N Engl J Med. 2014 Dec 4; 371 (23): 2189-2199; Le et al., N Engl J Med. 2015 Jun 25; 372 (26): 2509-20; Rizvi et al., Science. 2015 Apr 3; 348 (6230): 124-8; Van Allen et al., Science. 2015 Oct 9; 350 (6257): 207-211). Изобретение основано по меньшей мере частично на выявлении неоантигенов множественной миеломы, которые часто встречаются у пациентов с множественной миеломой и, следовательно, могут использоваться для разработки терапии, пригодной для лечения спектра пациентов с множественной миеломой. Один или более неоантигенов или полинуклеотидов, кодирующих неоантигены в соответствии с настоящим описанием, также можно использовать для диагностических или прогностических целей.
Полипептиды
В настоящем документе описаны полипептиды, содержащие последовательности неоантигенов множественной миеломы, которые могут вызывать иммунный ответ у субъекта.
В настоящем описании предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагменты. В некоторых вариантах осуществления полипептид кодируется полинуклеотидной последовательностью SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422 или их фрагментами.
В некоторых вариантах осуществления выделенный полипептид может содержать по меньшей мере две или более последовательностей неоантигенов множественной миеломы.
В настоящем описании также предложен выделенный гетерологичный полипептид, содержащий два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов. В некоторых вариантах осуществления два или более полипептидов, представленных в настоящем документе, могут присутствовать в тандемных повторах в любом порядке.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 3 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 5 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 7 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 9 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 11 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 13 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 15 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 17 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 19 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 21 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 23 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 25 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 27 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 29 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 31 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 33 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 35 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 37 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 39 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 41 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 43 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 45 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 47 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 49 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 51 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 53 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 55 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 57 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 59 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 61 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 63 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 65 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 67 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 69 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 71 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 73 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 75 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 77 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 79 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 81 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 83 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 85 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 87 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 89 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 91 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 93 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 95 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 97 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 99 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 101 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 103 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 105 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 107 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 109 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 111 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 113 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 115 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 117 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 119 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 121 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 123 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 125 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 127 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 129 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 131 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 133 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 135 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 137 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 139 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 141 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 143 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 145 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 147 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 149 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 151 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 153 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 155 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 157 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 159 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 161 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 163 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 165 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 167 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 169 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 171 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 173 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 175 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 177 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 179 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 181 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 183 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 185 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 187 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 189 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 191 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 193 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 195 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 197 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 199 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 201 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 203 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 205 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 207 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 209 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 211 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 213 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 215 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 217 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 219 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 221 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 223 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 225 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 227 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 229 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 231 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 233 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 235 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 237 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 239 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 241 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 243 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 245 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 247 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 249 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 251 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 253 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 255 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 257 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 259 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 261 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 263 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 265 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 267 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 269 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 271 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 273 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 275 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 277 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 279 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 281 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 283 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 285 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 287 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 289 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 291 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 293 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 295 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 297 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 299 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 301 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 303 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 305 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 307 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 309 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 311 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 313 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 315 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 317 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 319 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 321 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 323 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 325 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 327 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 329 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 331 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 333 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 335 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 337 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 339 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 341 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 343 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 345 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 347 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 349 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 351 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 353 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 355 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 357 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 359 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 361 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 363 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 365 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 367 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 369 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 371 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 373 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 375 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 377 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 379 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 381 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 383 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 385 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 387 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 389 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 391 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 393 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 395 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 397 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 399 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 401 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 403 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 405 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 407 или ее фрагменты.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 421 или ее фрагменты.
В некоторых вариантах осуществления длина фрагментов составляет около 6-25 аминокислот.
В некоторых вариантах осуществления фрагменты содержат по меньшей мере 6 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 7 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 8 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 9 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 10 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 11 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 12 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 13 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 14 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 15 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 16 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 17 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 18 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 19 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 20 аминокислот. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 21 аминокислоту. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 22 аминокислоты. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 23 аминокислоты. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 24 аминокислоты. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 25 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 6 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 7 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 10 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 11 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 12 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 13 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 14 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 15 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 16 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 17 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 18 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 19 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 20 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 21 аминокислоты. В некоторых вариантах осуществления фрагменты содержат около 22 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 23 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 24 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 25 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 6-25 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 7-25 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-25 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-24 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-23 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-22 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-21 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-20 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-19 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-18 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-17 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-16 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-15 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 8-14 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9-14 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9-13 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9-12 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9-11 аминокислот. В некоторых вариантах осуществления фрагменты содержат около 9-10 аминокислот.
В некоторых вариантах осуществления фрагменты представляют собой иммуногенные фрагменты.
Иммуногенные фрагменты по существу представляют собой пептиды, которые активируют Т-клетки, например те, которые индуцируют цитотоксические Т-клетки при презентации на молекуле МНС. Способы оценки активации Т-клеток и/или индукции цитотоксических Т-лимфоцитов хорошо известны. В примере анализа МКПК, выделенные у пациента с множественной миеломой, культивируют in vitro в присутствии исследуемого неоантигена или его фрагментов и IL-25. Культуры можно периодически пополнять IL-15 и IL-2 и культивировать в течение дополнительных 12 дней. Надень 12 культуры повторно стимулируют исследуемым неоантигеном или его фрагментами, и на следующий день активацию Т-клеток можно оценить путем измерения процента IFNγ+TNAα+CD8+ клеток по сравнению с контрольной культурой.
Полипептиды и гетерологичные полипептиды в соответствии с настоящим описанием содержат один или более неоантигенов множественной миеломы, описанных в настоящем документе. Полипептиды и гетерологичные полипептиды в соответствии с настоящим описанием целесообразно использовать для получения рекомбинантных вирусов, клеток и вакцин в соответствии с настоящим описанием, а также белковых молекул, которые специфически связывают один или более неоантигенов множественной миеломы в соответствии с настоящим описанием или могут использоваться непосредственно в качестве терапевтических агентов путем их доставки субъекту с множественной миеломой с использованием различных технологий. Два или более неоантигенов (например, полипептиды) могут быть включены в вакцину в любом порядке с применением стандартных способов клонирования.
В процессе валидации 115 полипептидов неоантигена SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421 были идентифицированы как особенно полезные для включения в вакцину против множественной миеломы на основании их профиля экспрессии, распространенности и иммуногенности in vitro. Ожидается, что любую комбинацию двух или более из 115 неоантигенов можно использовать для создания вакцины от множественной миеломы, которую можно доставлять субъекту с использованием любых доступных носителей и любой доступной формы, такой как пептиды, ДНК, РНК, репликоны, или с использованием вирусной доставки. Два или более неоантигенов (например, полипептиды) могут быть включены в вакцину в любом порядке с применением стандартных способов клонирования.
Два или более полипептидов могут быть собраны в гетерологичные полинуклеотиды, кодирующие гетерологичные полипептиды, в любом порядке, и порядок полипептидов может отличаться для различных вариантов доставки. Как правило, сборка полипептидов в конкретный порядок может быть основана на генерировании минимального количества соединительных эпитопов с использованием известных алгоритмов.
В некоторых вариантах осуществления в настоящем описании предложен полипептид, содержащий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
В настоящем описании также предложен полипептид, содержащий два или более тандемных повторов SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов. В некоторых вариантах осуществления полипептид содержит 2, 3, 4, 5 или более 5 повторов полипептидов в соответствии с настоящим описанием.
В некоторых вариантах осуществления полипептиды соединяются головка к хвосту.
В некоторых вариантах осуществления полипептиды могут быть разделены линкером.
Иллюстративные линкерные последовательности включают AAY, RR, DPP, ННАА, ННА, HHL, RKSYL, RKSY, SSL или REKR. В некоторых вариантах осуществления линкеры, представленные в настоящем документе, могут содержать сайт расщепления протеазой, так что гетерологичные полипептиды могут расщепляться in vivo у субъекта на пептидные фрагменты, содержащие последовательности неоантигенов, что приводит к усилению иммунного ответа.
В некоторых вариантах осуществления полипептиды соединены друг с другом непосредственно без линкера.
В некоторых вариантах осуществления полипептиды по настоящему изобретению могут дополнительно содержать лидерную последовательность или последовательность энхансера Т-клеток (ТСЕ) на N-конце. Лидерные последовательности могут увеличивать экспрессию и/или увеличивать иммунологический ответ. Примеры лидерных последовательностей включают сщепь рецептора TCR лимфоцитов Т2 (HAVT20) (MACPGFLWALVISTC LEFSMA; SEQ ID NO: 423), сигнальную последовательность убиквитина (Ubiq) (MQIFVKTLTGKTITLEVEP SDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRG VR; SEQ ID NO: 424) или последовательность Т-клеточного энхансера (ТСЕ), такую как пептидный фрагмент длиной 28аа, из инвариантной цепи рыбы мандаринки (MGQKEQIHTLQKNSERMSKQLTRSSQAV; SEQ ID NO: 425). Считается, что лидерные последовательности могут способствовать усилению иммунного ответа на описанные в данном документе эпитопы.
Полинуклеотиды
В настоящем изобретении также предложены полинуклеотиды, которые кодируют любой из полипептидов, описанных в данном документе.
В некоторых вариантах осуществления в настоящем описании предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагменты.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид, который по меньшей мере на 90% идентичен полипептиду SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33,35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагментам;
В настоящем описании также предложен выделенный полинуклеотид, содержащий полинуклеотидную последовательность SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422 или их фрагменты.
В настоящем описании также представлен выделенный полинуклеотид, содержащий полинуклеотидную последовательность, по меньшей мере на 90% идентичную полинуклеотид ной последовательности SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422 или их фрагментам.
В настоящем описании также предложен выделенный гетерологичный полинуклеотид, содержащий два или более полинуклеотидов, выбранных из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 и 422, а также их фрагментов.
В настоящем описании также предложен выделенный гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, содержащий два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов.
В некоторых вариантах осуществления фрагменты содержат по меньшей мере 18 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 21 нуклеотид. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 24 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 27 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 30 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 33 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 36 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 39 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 42 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 45 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 48 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 51 нуклеотид. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 54 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 57 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 60 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 63 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 66 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 69 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 72 нуклеотида. В некоторых вариантах осуществления фрагменты содержат по меньшей мере 75 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 18 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 21 нуклеотида. В некоторых вариантах осуществления фрагменты содержат около 24 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 30 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 33 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 36 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 39 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 42 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 45 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 48 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 51 нуклеотида. В некоторых вариантах осуществления фрагменты содержат около 54 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 57 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 60 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 63 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 66 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 69 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 72 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 75 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 18-75 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 21-75 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-75 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-72 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-69 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-66 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-63 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-60 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-57 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-54 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-51 нуклеотида. В некоторых вариантах осуществления фрагменты содержат около 24-48 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-45 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 24-42 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27-42 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27-39 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27-36 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27-33 нуклеотидов. В некоторых вариантах осуществления фрагменты содержат около 27-30 нуклеотидов.
Полинуклеотиды и гетерологичные полинуклеотиды в соответствии с настоящим описанием кодируют неоантигены множественной миеломы и гетерологичные полипептиды, содержащие два или более неоантигенов множественной миеломы, описанных в настоящем документе. Полинуклеотиды и гетерологичные полинуклеотиды в соответствии с настоящим описанием можно использовать для получения полипептидов, гетерологичных полипептидов, векторов, рекомбинантных вирусов, клеток и вакцин в соответствии с настоящим описанием. Полинуклеотиды и гетерологичные полинуклеотиды в соответствии с настоящим описанием можно использовать в качестве терапевтических средств путем их доставки субъекту, имеющему множественную миелому, с использованием различных технологий, включая вирусные векторы, описанные в настоящем документе, или другие технологии доставки, также описанные в настоящем документе.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 1 или ее фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 1 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 2 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 3 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 3 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 4 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 5 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 5 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 6 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 7 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 7 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 8 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 9 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 9 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 10 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 11 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 11 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 12 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 13 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 13 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 14 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 15 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 15 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 16 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 17 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 17 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 18 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 19 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 19 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 20 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 21 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 21 или его фрагмент кодируется полинуклеотид ом SEQ ID NO: 22 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 23 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 23 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 24 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 25 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 25 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 26 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 27 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 27 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 28 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 29 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 29 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 30 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 31 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 31 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 32 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 33 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 33 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 34 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 35 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 35 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 36 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 37 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 37 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 38 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 39 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 39 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 40 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 41 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 41 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 42 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 43 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 43 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 44 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 45 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 45 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 46 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 47 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 47 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 48 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 49 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 49 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 50 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 51 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 51 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 52 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 53 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 53 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 54 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 55 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 55 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 56 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 57 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 57 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 58 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 59 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 59 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 60 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 61 или ее фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 61 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 62 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 63 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 63 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 64 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 65 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 65 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 66 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 67 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 67 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 68 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 69 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 69 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 70 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 71 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 71 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 72 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 73 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 73 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 74 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 75 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 75 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 76 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 77 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 77 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 78 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 79 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 79 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 80 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 81 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 81 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 82 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 83 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 83 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 84 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 85 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 85 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 86 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 87 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 87 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 88 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 89 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 89 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 90 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 91 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 91 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 92 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 93 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 93 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 94 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 95 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 95 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 96 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 97 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 97 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 98 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 99 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 99 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 100 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 101 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 101 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 102 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 103 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 103 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 104 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 105 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 105 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 106 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 107 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 107 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 108 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 109 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 109 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 110 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 111 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 111 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 112 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 113 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 113 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 114 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 115 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 115 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 116 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 117 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 117 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 118 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 119 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 119 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 120 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 121 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 121 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 122 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 123 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 123 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 124 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 125 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 125 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 126 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 127 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 127 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 128 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 129 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 129 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 130 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 131 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 131 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 132 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 133 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 133 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 134 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 135 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 135 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 136 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 137 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 137 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 138 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 139 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 139 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 140 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 141 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 141 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 142 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 143 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 143 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 144 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 145 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 145 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 146 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 147 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 147 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 148 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 149 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 149 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 150 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 151 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 151 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 152 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 153 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 153 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 154 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 155 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 155 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 156 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 157 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 157 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 158 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 159 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 159 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 160 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 161 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 161 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 162 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 163 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 163 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 164 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 165 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 165 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 166 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 167 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 167 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 168 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 169 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 169 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 170 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 171 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 171 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 172 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 173 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 173 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 174 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 175 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 175 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 176 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 177 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 177 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 178 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 179 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 179 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 180 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 181 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 181 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 182 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 183 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 183 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 184 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 185 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 185 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 186 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 187 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 187 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 188 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 189 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 189 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 190 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 191 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 191 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 192 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 193 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 193 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 194 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 195 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 195 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 196 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 197 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 197 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 198 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 199 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 199 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 200 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 201 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 201 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 202 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 203 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 203 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 204 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 205 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 205 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 206 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 207 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 207 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 208 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 209 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 209 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 210 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 211 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 211 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 212 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 213 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 213 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 214 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 215 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 215 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 216 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 217 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 217 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 218 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 219 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 219 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 220 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 221 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 221 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 222 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 223 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 223 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 224 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 225 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 225 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 226 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 227 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 227 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 228 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 229 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 229 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 230 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 231 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 231 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 232 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 233 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 233 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 234 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 235 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 235 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 236 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 237 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 237 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 238 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 239 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 239 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 240 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 241 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 241 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 242 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 243 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 243 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 244 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 245 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 245 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 246 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 247 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 247 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 248 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 249 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 249 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 250 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 251 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 251 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 252 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 253 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 253 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 254 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 255 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 255 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 256 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 257 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 257 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 258 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 259 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 259 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 260 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 261 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 261 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 262 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 263 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 263 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 264 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 265 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 265 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 266 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 267 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 267 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 268 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 269 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 269 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 270 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 271 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 271 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 272 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 273 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 273 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 274 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 275 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 275 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 276 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 277 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 277 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 278 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 279 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 279 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 280 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 281 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 281 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 282 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 283 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 283 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 284 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 285 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 285 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 286 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 287 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 287 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 288 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 289 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 289 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 290 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 291 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 291 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 292 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 293 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 293 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 294 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 295 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 295 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 296 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 297 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 297 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 298 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 299 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 299 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 300 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 301 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 301 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 302 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 303 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 303 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 304 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 305 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 305 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 306 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 307 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 307 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 308 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 309 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 309 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 310 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 311 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 311 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 312 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 313 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 313 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 314 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 315 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 315 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 316 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 317 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 317 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 318 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 319 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 319 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 320 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 321 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 321 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 322 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 323 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 323 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 324 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 325 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 325 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 326 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 327 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 327 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 328 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 329 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 329 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 330 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 331 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 331 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 332 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 333 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 333 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 334 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 335 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 335 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 336 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 337 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 337 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 338 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 339 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 339 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 340 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 341 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 341 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 342 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 343 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 343 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 344 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 345 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 345 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 346 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 347 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 347 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 348 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 349 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 349 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 350 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 351 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 351 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 352 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 353 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 353 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 354 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 355 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 355 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 356 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 357 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 357 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 358 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 359 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 359 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 360 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 361 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 361 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 362 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 363 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 363 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 364 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 365 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 365 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 366 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 367 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 367 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 368 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 369 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 369 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 370 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 371 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 371 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 372 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 373 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 373 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 374 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 375 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 375 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 376 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 377 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 377 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 378 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 379 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 379 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 380 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 381 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 381 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 382 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 383 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 383 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 384 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 385 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 385 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 386 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 387 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 387 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 388 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 389 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 389 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 390 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 391 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 391 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 392 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 393 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 393 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 394 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 395 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 395 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 396 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 397 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 397 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 398 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 399 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 399 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 400 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 401 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 401 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 402 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 403 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 403 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 404 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 405 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 405 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 406 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 407 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 407 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 408 или его фрагментами.
В настоящем описании также предложен выделенный полинуклеотид, кодирующий полипептид SEQ ID NO: 387 или его фрагменты. В некоторых вариантах осуществления полипептид SEQ ID NO: 421 или его фрагмент кодируется полинуклеотидом SEQ ID NO: 422 или его фрагментами.
В некоторых вариантах осуществления гетерологичный полинуклеотид представляет собой гетерологичный полинуклеотид внутри рамки считывания.
Для экспрессии в различных хозяевах полинуклеотиды могут быть кодон-оптимизированы с использованием известных способов.
В некоторых вариантах осуществления выделенный гетерологичный полинуклеотид представляет собой гетерологичный полинуклеотид внутри рамки считывания.
В некоторых вариантах осуществления полинуклеотид содержит ДНК или РНК.
В некоторых вариантах осуществления полинуклеотид содержит РНК. В некоторых вариантах осуществления РНК представляет собой мРНК.
Варианты сконструированных полинуклеотидов, полипептидов, гетерологичных полинуклеотидов и гетерологичных полипептидов в соответствии с настоящим описанием
Варианты полинуклеотидов, полипептидов, гетерологичных полинуклеотидов и гетерологичных полипептидов или их фрагментов входят в объем настоящего описания. Например, варианты могут содержать одну или более замен, делеций или вставок при условии, что варианты сохраняют или имеют улучшенные характеристики (такие как иммуногенность или стабильность) по сравнению с исходным соединением. В некоторых вариантах осуществления идентичность последовательностей может составлять около 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% между исходным соединением и вариантом. В некоторых вариантах осуществления варианты формируются путем консервативных замен.
В некоторых вариантах осуществления идентичность составляет около 80%. В некоторых вариантах осуществления идентичность составляет около 85%. В некоторых вариантах осуществления идентичность составляет около 90%. В некоторых вариантах осуществления идентичность составляет около 91%. В некоторых вариантах осуществления идентичность составляет около 91%. В некоторых вариантах осуществления идентичность составляет около 92%. В некоторых вариантах осуществления идентичность составляет около 93%. В некоторых вариантах осуществления идентичность составляет около 94%. В некоторых вариантах осуществления идентичность составляет 94%. В некоторых вариантах осуществления идентичность составляет около 95%. В некоторых вариантах осуществления идентичность составляет около 96%. В некоторых вариантах осуществления идентичность составляет около 97%. В некоторых вариантах осуществления идентичность составляет около 98%. В некоторых вариантах осуществления идентичность составляет около 99%.
Процент идентичности между двумя последовательностями зависит от числа идентичных положений, общих для последовательностей (т.е. % идентичности=число идентичных положений / общее число положений х 100), с учетом числа гэпов и длины каждого гэпа, который необходимо встроить для оптимального выравнивания двух последовательностей. Процент идентичности между двумя аминокислотным последовательностями можно определить с помощью алгоритма Е. Meyers and W. Miller (Comput Appl Biosci 4:11-17 (1988)), который встроен в программу ALIGN (версия 2.0), используя таблицы массы остатков РАМ 120, штрафа на длину гэпа 12 и штрафа гэпа 4. Кроме того, процент идентичности между двумя аминокислотными последовательностями можно определить с помощью алгоритма Needleman and Wunsch (JMolBiol 48:444-453 (1970)), который встроен в программу GAP в пакете программ GCG (доступен на сайте http_//_www_gcg_com), используя либо матрицы Blossum 62, либо матрицы РАМ250, а также веса гэпов 16, 14, 12, 10, 8, 6 или 4 и веса длины гэпов 1, 2, 3, 4, 5 или 6.
Варианты полипептидов или гетер о логичных полипептидов или их фрагментов, содержащих одно изменение аминокислотного состава, обычно сохраняют аналогичную третичную структуру и антигенность по сравнению с исходным соединением. В некоторых случаях вариант также может содержать по меньшей мере одно изменение аминокислотного состава, которое приводит к повышенной антигенности варианта, повышенной аффинности связывания с TCR, или с антителом, или и с тем, и с другим. Варианты полипептидов или гетерологичных полипептидов также могут иметь улучшенную способность связываться с молекулой HLA.
Варианты в соответствии с настоящим описанием можно сконструировать так, чтобы они содержали консервативные замены. Консервативные замены в настоящем документе определяются как замены в пределах одной из следующих пяти групп: группа 1 - малые алифатические неполярные или слабополярные остатки (Ala, Ser, Thr, Pro, Gly); группа 2 - полярные отрицательно заряженные остатки и их амиды (Asp, Asn, Glu, Gin); группа 3 - полярные положительно заряженные остатки (His, Arg, Lys); группа 4 - большие алифатические неполярные остатки (Met, Leu, lie, Val, Cys); и группа 5 - большие ароматические остатки (Phe, Tyr, Trp).
Варианты в соответствии с настоящим описанием можно сконструировать так, чтобы они содержали менее консервативные замены, такие как замена одной аминокислоты на другую, имеющую аналогичные характеристики, но несколько отличающуюся по размеру, например, замена аланина на остаток изолейцина. Варианты в соответствии с настоящим описанием также можно сконструировать так, чтобы они содержали сильно неконсервативные замены, которые могут включать замещение кислой аминокислоты полярной или даже щелочной по своему характеру.
Дополнительные замены, которые можно выполнять для получения вариантов в соответствии с настоящим описанием, включают в себя замены, которые могут включать структуры, отличные от обычных L-аминокислот. Таким образом, D-аминокислоты и нестандартные аминокислоты (т.е. отличные от обычных протеиногенных аминокислот природного происхождения) также можно использовать для целей замены для получения вариантов с повышенной иммуногенностью по сравнению с исходным соединением.
Если обнаружено, что замены в более чем одном положении приводят к получению полипептидов или гетерологичных полипептидов с по существу эквивалентной или большей иммуногенностью, то можно протестировать комбинации этих замен, чтобы определить, оказывают ли комбинированные замены аддитивное или синергетическое воздействие на иммуногенность варианта.
Аминокислотные остатки, которые по существу не участвуют во взаимодействии с TCR, могут быть модифицированы путем замены другой аминокислотой, встраивание которой по существу не влияет на реактивность Т-клеток и не исключает связывание с соответствующим МНС аминокислотные остатки, которые по существу не участвуют во взаимодействии с TCR, также могут быть удалены, если такая делеция не оказывает существенного влияния на реактивность Т-клеток и не исключает связывание с соответствующим МНС.
Кроме того, полипептиды, или гетерологичные полипептиды, или их фрагменты, или варианты могут быть дополнительно модифицированы для повышения стабильности и/или связывания с молекулами МНС, чтобы вызвать более сильный иммунный ответ. Способы такой оптимизации пептидной последовательности хорошо известны в данной области и включают, например, введение обратных пептидных связей или непептидных связей. При обратной пептидной связи аминокислотные остатки не соединены пептидными (-СО- NH-) связями, а пептидная связь является обратной. Такие ретро-инверсные пептид о миметики могут быть получены с использованием методов, известных в данной области, например, таких, как описано в Meziere et al. (1997) (Meziere et al., 1997). Данный подход включает получение псевдопептидов, содержащих изменения, затрагивающие основную цепь, а не ориентацию боковых цепей. Работа Meziere et al. (Meziere et al., 1997) показывает, что эти псевдопептиды являются полезными для связывания МНС и Т-хелперных клеток. Ретро-инверсные пептиды, содержащие NH-СО связи вместо СО-NH пептидных связей, гораздо более устойчивы к протеолизу. Дополнительными непептидными связями, которые можно использовать, являются, например, -СН2-NH, -CH2S-, -СН2СН2-, СН=СН, СОСН2, СН(ОН)СН2 и CH2SO-.
Полипептиды, или гетерологичные полипептиды, или их фрагменты, или варианты в соответствии с настоящим описанием могут быть синтезированы с помощью дополнительных химических групп, присутствующих на их амино- и/или карбокси-концах, для повышения стабильности, биодоступности и/или аффинности пептидов. Например, к амино-концу могут быть добавлены гидрофобные группы, такие как карбобензоксильная, данзильная или трет-бутилоксикарбонильная группа. Аналогичным образом ацетильная группа или 9-фторенилметоксикарбонильная группа может быть размещена на амино-концах. Кроме того, к карбокси-концам можно добавлять гидрофобную группу, трет-бутилоксикарбонильную группу или амидную группу.
Кроме того, полипептиды, или гетерологичные полипептиды, или их фрагменты, или варианты в соответствии с настоящим описанием могут быть синтезированы для изменения их стерической конфигурации. Например, вместо обычного L-изомера может использоваться D-изомер одного или более аминокислотных остатков пептида.
Аналогичным образом полипептиды, или гетерологичные полипептиды, или их фрагменты, или варианты в соответствии с настоящим описанием могут быть модифицированы химически путем посредством взаимодействия конкретных аминокислот либо до, либо после синтеза полипептидов, или гетерологичных полипептидов, или их фрагментов, или вариантов в соответствии с настоящим описанием. Примеры таких модификаций хорошо известны в данной области и обобщены, например, в публикации R. Lundblad, Chemical Reagents for Protein Modification, 3rd ed. CRC Press, 2004 (Lundblad, 2004), которая включена в настоящий документ путем ссылки. Химическая модификация аминокислот включает без ограничений модификацию путем ацилирования, амидирования, пиридоксилирования лизина, восстановительного алкилирования, тринитробензилирования аминогрупп 2,4,6-тринитробензолсульфоновой кислотой (TNBS), амидной модификации карбоксильных групп и сульфгидрильной модификации путем окисления цистеина надмуравьиной кислотой до цистеиновой кислоты, образования производных ртути, образования смешанных дисульфидов с другими тиольными соединениями, реакции с малеимидом, карбоксиметилирования йодуксусной кислотой или йодацетамидом и карбамоилирования цианатом при щелочном рН, не ограничиваясь вышеупомянутым. В этом отношении специалист в данной области может обратиться к главе 15 публикации Current Protocols In Protein Science, Eds. Coligan et al. (John Wiley and Sons NY 1995-2000) (Coligan et a 1., 1995) для ознакомления с более широкой методологией, связанной с химической модификацией белков.
Вкратце, модификация, например, аргининильных остатков в белках часто основана на реакции соседних дикарбонильных соединений, таких как фенилглиоксаль, 2,3-бутандион и 1,2-циклогександион с образованием аддукта. Другим примером является реакция метилглиоксаля с остатками аргинина. Цистеин можно модифицировать без сопутствующей модификации других нуклеофильных сайтов, таких как лизин и гистидин. В результате большое количество реагентов доступно для модификации цистеина. Веб-сайты таких компаний, как Sigma-Aldrich (http://www.sigma-aldrich.com), предоставляют информацию о конкретных реагентах. Селективное восстановление дисульфидных связей в белках также является распространенным. Дисульфидные связи могут образовываться и окисляться в процессе термической обработки биофармацевтических препаратов. Реагент Woodward's Reagent K можно использовать для модификации конкретных остатков глутаминовой кислоты. N-(3-(диметиламино)пропил)-N'-этилкарбодиимид можно применять для образования внутримолекулярных сшивок между остатком лизина и остатком глутаминовой кислоты. Например, диэтилпирокарбонат является реагентом для модификации гистидильных остатков в белках. Гистидин также можно модифицировать, используя 4-гидрокси-2-ноненаль. Реакция лизиновых остатков и других α-аминогрупп может использоваться, например, для связывания пептидов с поверхностями или сшивок белки/пептиды. Лизин представляет собой сайт присоединения поли(этилен)гликоля и основной сайт модификации в гликозилировании белков. Остатки метионина в белках могут быть модифицированы, например, иодоацетамидом, бромэтиламином и хлорамином Т. Тетранитрометан и N-ацетилимидазол могут быть использованы для модификации тирозильных остатков. Сшивка посредством образования дитирозина может быть достигнута с помощью ионов перекиси водорода/меди. В недавних исследованиях по модификации триптофана использовали N-бромсукцинимид, 2-гидрокси-5-нитробензилбромид или 3-бром-3-метил-2-(2-нитрофенилмеркапто)-3Н-индол (BPNS-скатол). Успешная модификация терапевтических белков и пептидов с помощью ПЭГ часто связана с увеличением периода полужизни в кровотоке при сшивании белков с глутаральдегидом, диакрилатом полиэтиленгликоля и формальдегидом для получения гидрогелей. Химическую модификацию аллергенов для иммунотерапии часто проводят путем карбамилирования с использованием цианата калия.
В настоящем описании предложен выделенный полипептид, который на около 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичен полипептиду SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421.
В настоящем описании также предложен выделенный полинуклеотид, который на около 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичен полинуклеотиду SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, ПО, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421, а также их фрагменты, причем полипептид содержит одну или более обратных пептидных связей.
В некоторых вариантах осуществления обратная пептидная связь содержит связь NH СО.
В некоторых вариантах осуществления обратная пептидная связь содержит связь СН2-NH, -CH2S-,
-СН2СН2-, -СН=СН-, -СОСН2-, -СН(ОН)СН2- или -CH2SO-.
В настоящем описании также предложен выделенный полипептид, содержащий аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421, а также их фрагменты, причем полипептид содержит одну или более химических модификаций.
В некоторых вариантах осуществления одна или более химических модификаций содержат модификацию карбобензоксилом, данзилом, трет-бутилоксикарбонилом, 9-фторенилметоксикарбонилом или D-изомером аминокислоты.
Способы получения полинуклеотидов и полипептидов в соответствии с настоящим описанием
Полинуклеотиды в соответствии с настоящим описанием или варианты могут быть в форме РНК или в форме ДНК, полученной путем клонирования или синтеза. ДНК может быть двухцепочечной или одноцепочечной.
Способы создания полинуклеотидов и гетерологичных полинуклеотидов в соответствии с настоящим описанием или вариантами известны в данной области и включают в себя химический синтез, ферментативный синтез (например, транскрипцию in vitro), ферментативное или химическое расщепление более длинного предшественника, химический синтез более мелких фрагментов полинуклеотидов с последующим лигированием фрагментов или использованием известных способов ПЦР. Синтезированная полинуклеотидная последовательность может быть сконструирована с помощью соответствующих кодонов для желаемой аминокислотной последовательности. Как правило, предпочтительные кодоны могут быть выбраны для предполагаемого хозяина, в котором для экспрессии будет применяться последовательность.
Способы получения полипептидов и гетерологичных полипептидов в соответствии с настоящим описанием известны в данной области и включают стандартные методы молекулярной биологии для клонирования и экспрессии полипептидов, а также химического синтеза полипептидов.
Пептиды можно синтезировать с помощью режима Fmoc-полиамида твердофазного синтеза пептидов, как описано в публикации Lukas et al. (Lukas et al., 1981) и в приведенных в ней ссылках. Временная защита N-аминогруппы обеспечивается группой 9-фторенилметилоксикарбонила (Fmoc). Повторяющееся расщепление этой высоколабильной защитной группы проводят с использованием 20% пиперидина в N, N-диметилформамиде. Функциональные группы боковой цепи могут быть защищены в виде их бутиловых эфиров (в случае серинтреонина и тирозина), бутиловых сложных эфиров (в случае глутаминовой кислоты и аспарагиновой кислоты), бутилоксикарбонильного производного (в случае лизина и гистидина), тритилового производного (в случае цистеина) и 4-метокси-2,3,6-триметилбензолсульфонильного производного (в случае аргинина). Если глутамин или аспарагин являются С-концевыми остатками, применяют 4,4'-диметоксибензгидрильную группу для защиты амидных функциональных групп боковой цепи. Твердофазная подложка основана на полидиметилакриламидном полимере, состоящем из трех мономеров диметилакриламида (мономер главной цепи), бисакрилоилэтилен диамина (кросс-линкер) и метилового сложного эфира акрилоилсаркозина (функционализирующий агент). В качестве расщепляемого агента, связывающего пептид с резиной, используется кислотно-лабильное производное 4-гидроксиметил-феноксиуксусной кислоты. Все аминокислотные производные добавляют в виде предварительно подготовленных симметричных производных ангидрида, за исключением аспарагина и глутамина, которые добавляют в ходе обратной процедуры связывания, опосредованной N, N-дициклогексилкарбодиимид/! гидроксибензотриазолом. Все реакции связывания и снятия защиты отслеживают с помощью процедур тестирования нингидрина, тринитробензолсульфоновой кислоты или изотина. После завершения синтеза пептиды отщепляют от смоляной подложки с одновременным удалением защитных групп боковых цепей путем обработки 95% трифторуксусной кислотой, содержащей 50% смеси поглотителей. Обычно используемые поглотители включают в себя этандитиол, фенол, анизол и воду, точный выбор которых зависит от составляющих аминокислот синтезированного пептида. Также возможно сочетание методик синтеза пептидов в твердой фазе и фазе раствора (см., например, публикацию Bruckdorfer et al., 2004 г.) и приведенные в ней ссылки).
В патенте США №4,897,445 представлен способ твердофазного синтеза непептидных связей (-СН2-NH) в полипептидных цепях, который включает полипептиды, синтезированные в ходе стандартных процедур, и непептидную связь, синтезированную путем взаимодействия аминоальдегида с аминокислотой в присутствии NaCNBH3.
Векторы и рекомбинантные вирусы в соответствии с настоящим описанием
В настоящем описании также предложен вектор, содержащий полинуклеотид или гетерологичный полинуклеотид в соответствии с настоящим описанием. В настоящем изобретении также преложены векторы, содержащие полинуклеотид, кодирующий один или более полипептидов, представленных в настоящем документе.
В настоящем описании также предложен вектор, содержащий полинуклеотид, кодирующий один или более полипептидов SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагменты.
В настоящем описании также предложен вектор, содержащий один или более полинуклеотидов SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 или 422 или их фрагментами.
В настоящем описании также предложен вектор, содержащий полинуклеотид, кодирующий один или более полипептидов SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагменты.
В настоящем описании также предложен вектор, содержащий один или более полинуклеотидов SEQ ID NO: 8, 10, 12, 14, 18, 22, 24, 26, 28, 32, 34, 36, 38, 40, 42, 44, 46, 48, 52, 54, 56, 60, 62, 64, 66, 70, 72, 76, 80, 82, 84, 86, 90, 92, 102, 104, 106, 108, ПО, 112, 114, 120, 122, 124, 126, 132, 134, 136, 144, 146, 148, 150, 152, 158, 162, 164, 166, 172, 174, 180, 186, 188, 198, 200, 208, 243, 218, 222, 224, 226, 242, 248, 250, 260, 266, 268, 270, 282, 286, 288, 290, 294, 298, 300, 302, 304, 306, 308, 330, 332, 334, 336, 338, 340, 342, 344, 346, 350, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 376, 378, 380, 382, 384, 386, или 422 или их фрагменты.
В настоящем описании также предложен вектор, содержащий гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, содержащий два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов.
В настоящем описании также предложен вектор, содержащий гетерологичный полинуклеотид, содержащий два или более полинуклеотидов, выбранных из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 и 422, а также их фрагментов.
В настоящем описании также предложен вектор, содержащий гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, содержащий 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203 или 204 полипептида, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89,91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов.
В настоящем описании также предложен вектор, содержащий гетерологичный полинуклеотид, содержащий 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, ПО, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142, 143, 144, 145, 146, 147, 148, 149, 150, 151, 152, 153, 154, 155, 156, 157, 158, 159, 160, 161, 162, 163, 164, 165, 166, 167, 168, 169, 170, 171, 172, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186, 187, 188, 189, 190, 191, 192, 193, 194, 195, 196, 197, 198, 199, 200, 201, 202, 203 или 204 полинуклеотида, выбранных из группы состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, 406, 408 и 422, а также их фрагментов.
В некоторых вариантах осуществления вектор представляет собой вектор экспрессии. Вектор может представлять собой вектор, предназначенный для экспрессии полинуклеотида или гетерологичного полинуклеотида в соответствии с настоящим описанием в любом хозяине, таком как бактерия, дрожжи или млекопитающее. Как правило, приемлемые экспрессионные векторы могут реплицироваться в организмах-хозяевах либо в виде эписом, либо в виде неотъемлемой части хромосомной ДНК хозяина. Обычно экспрессионные векторы содержат селективные маркеры, такие как вызывающие резистентность к ампициллину, резистентность к гигромицину, резистентность к тетрациклину, резистентность к канамицину или резистентность к неомицину, чтобы обеспечивать обнаружение таких клеток, трансформированных или трансдуцированных желаемыми последовательностями ДНК. Примерами векторов являются плазмиды, космиды, фаги, вирусные векторы, транспозоны или искусственные хромосомы.
Известны подходящие векторы; многие из них коммерчески доступны для создания рекомбинантных конструктов. Следующие векторы представлены в качестве примера. Бактериальные: pBs, phagescript, PsiX174, pBluescript SK, pBs KS, pNH8a, pNH16a, pNHlSa, pNH46a (Stratagene, Ла-Холья, г. Сан-Диего, штат Калифорния, США); РТгс99А, рКК223-3, pKK233-3, pDR540 и pRIT5 (Pharmacia, г. Уппсала, Швеция). Эукариотические: pWLneo, pSV2cat, pOG44, PXR1, pSG (Stratagene), pSVK3, pBPV, pMSG и pSVL (Pharmacia). Транспозоновые векторы: Транспозон «Спящая красавица» сна и транспозон PiggyBac.
В некоторых вариантах осуществления вектор представляет собой вирусный вектор. Векторы в соответствии с настоящим описанием можно использовать для получения рекомбинантных вирусов, содержащих векторы в соответствии с настоящим описанием, или для экспрессии полипептидов в соответствии с настоящим описанием. Вирусные векторы получают из вирусных геномов природного происхождения, которые, как правило, модифицируют так, чтобы они были не способны к репликации, т.е. не реплицировались. Нереплицирующимся вирусам необходимо предоставление белков в транс-конфигурации для репликации. Как правило, эти белки стабильно или временно экспрессируются в линии вирусных продуцирующих клеток, тем самым допуская репликацию вируса. Таким образом, вирусные векторы являются, как правило, инфекционными и нереплицирующимися. Вирусные векторы могут представлять собой аденовирусные векторы, векторы на основе адено-ассоциированного вируса (AAV) (например, AAV 5-го типа и 2-го типа), альфавирусные векторы (например, вирус венесуэльского лошадиного энцефалита (VEE), вирус Синдбис (SIN), вирус леса Семлики (SFV) и химеры VEE-SIN), векторы на основе вируса герпеса (например, векторы, полученные из цитомегаловирусов, таких как цитомегаловирус резуса (RhCMV)), векторы на основе аренавируса (например, векторы на основе вируса лимфоцитарного хориоменингита (LCMV)), векторы на основе вируса кори, векторы на основе поксвируса (например, вирус осповакцины, модифицированный вирус осповакцины Анкара (MVA), NYVAC (производное от штамма осповакцины Копенгаген) и векторы на основе авипоксмвируса: векторы на основе каннарипокса (ALVAC) и вируса оспы кур (FPV)), векторы на основе вируса везикулярного стоматита, ретровирусные векторы, лентивирусные векторы, вирусоподобные частицы, бакуловирусные векторы и бактериальные споры.
Векторы в соответствии с настоящим описанием могут быть получены с использованием известных методик.
Аденовирусные векторы
В некоторых вариантах осуществления вирусный вектор получен из аденовируса. В некоторых вариантах осуществления рекомбинантный вирус, содержащий вектор, получен из аденовируса.
Аденовирусные векторы могут быть получены из аденовируса человека (Ad), а также из аденовирусов, которые инфицируют другие виды, такие как бычий аденовирус (например, бычий аденовирус 3, BAdV3), аденовирус собаки (например, CAdV2), аденовирус свиньи (например, PAdV3 или 5) или аденовирус человекообразных обезьян, таких как шимпанзе (Pan), горилла (Gorilla), орангутан (Pongo), бонобо (Pan paniscus) и обычный шимпанзе (Pan troglodytes). Как правило, аденовирусы человекообразных обезьян природного происхождения выделяют из образцов кала соответствующих человекообразных обезьян.
Векторы на основе аденовируса человека могут быть получены из различных аденовирусных серотипов, например, из серотипов аденовируса человека hAd5, hAd7, hAd11, hAd26, hAd34, hAd35, hAd48, hAd49 или hAd50 (серотипы также обозначены как Ad5, Ad7, Ad11, Ad26, Ad34, Ad35, Ad48, Ad49 или Ad50).
Векторы на основе аденовирусов человекообразных обезьян могут быть получены из различных аденовирусных серотипов, например из серотипов аденовируса человекообразных обезьян GAd20, Gad19, GAd21, GAd25, GAd26, GAd27, GAd28, GAd29, GAd30, GAd31, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAd146, ChAd147, PanAd1, PanAd2 или PanAd3.
Аденовирусные векторы известны в данной области. Последовательности большинства человеческих и не относящихся к человеку аденовирусов известны, а другие могут быть получены с помощью стандартных процедур. Пример геномной последовательности Ad26 представлен в каталоге GenBank Accession под №EF153474 и под SEQ ID NO: 1 в международной патентной публикации №WO 2007/104792. Пример геномной последовательности Ad35 представлен на ФИГ. 6 в международной патентной публикации №WO 2000/70071. Векторы на основе Ad26 описаны, например, в международной патентной публикации №WO 2007/104792. Векторы на основе Ad35 описаны, например, в патенте США №7,270,811 и международной патентной публикации №WO 2000/70071. Векторы на основе ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAdS, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd82 описаны в WO 2005/071093. Векторы на основе PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAdl46 и ChAd147 описаны в международной патентной публикации №WO 2010/086189.
Аденовирусные векторы конструируют так, чтобы они включали по меньшей мере одну функциональную делецию или полное удаление продукта гена, необходимого для репликации вируса, такого как одна или более аденовирусных областей E1, Е2 и Е4, тем самым делая аденовирус неспособным к репликации. Делеция области Е1 может содержать делеции EIA, EIB 55K, EIB 21K или любой их комбинации. Аденовирусы с недостаточной репликацией размножают путем получения белков, кодируемых удаленной(-ыми) областью(-ями), транс-продуцирующими клетками с использованием плазмид хелперов или конструирования продуцирующей клетки для экспрессии необходимых белков. Аденовирусные векторы также могут иметь делецию в области Е3, которая является несущественной для репликации, и, следовательно, такая делеция не обязательно должна быть дополненной. Аденовирусный вектор в соответствии с настоящим описанием может содержать функциональную делецию или полное удаление области Е1 и по меньшей мере части области Е3. Аденовирусный вектор в соответствии с настоящим описанием может дополнительно содержать функциональную делецию или полное удаление области Е4 и/или области Е2. Подходящими для использования продуцирующими клетками являются клетки сетчатки человека иммортализованные Е1, например, клетки 911 или PER.C6 (см., например, патент США №5,994,128), преобразованные Е1 амниоциты (см., например, ЕР 1230354), Е1-преобразованные клетки А549 (см., например, международную патентную публикацию №WO 1998/39411, патент США №5,891,690); Примерами векторов, которые могут быть использованы, являются Ad26, содержащие функциональную кодирующую область Е1, достаточную для репликации вируса, делецию в кодирующей области Е3 и делецию в кодирующей области Е4, при условии, что открытая рамка считывания 6/7 Е4 не удалена (см., например, патент США№9,750,801)
В некоторых вариантах осуществления аденовирусный вектор представляет собой вектор аденовируса человека (Ad). В некоторых вариантах осуществления вектор Ad получают из Ad5. В некоторых вариантах осуществления вектор Ad получают из Adl 1. В некоторых вариантах осуществления вектор Ad получают из Ad26. В некоторых вариантах осуществления вектор Ad получают из Ad34. В некоторых вариантах осуществления вектор Ad получают из Ad35. В некоторых вариантах осуществления вектор Ad получают из Ad48. В некоторых вариантах осуществления вектор Ad получают из Ad49. В некоторых вариантах осуществления вектор Ad получают из Ad50.
В некоторых вариантах осуществления аденовирусный вектор представляет собой вектор аденовируса человекообразных обезьян (GAd). В некоторых вариантах осуществления вектор GAd получают из GAd20. В некоторых вариантах осуществления вектор GAd получают из GAd19. В некоторых вариантах осуществления вектор GAd получают из GAd21. В некоторых вариантах осуществления вектор GAd получают из GAd25. В некоторых вариантах осуществления вектор GAd получают из GAd26. В некоторых вариантах осуществления вектор GAd получают из GAd27. В некоторых вариантах осуществления вектор GAd получают из GAd28. В некоторых вариантах осуществления вектор GAd получают из GAd29. В некоторых вариантах осуществления вектор GAd получают из GAd30. В некоторых вариантах осуществления вектор GAd получают из GAd31. В некоторых вариантах осуществления вектор GAd получают из ChAd4. В некоторых вариантах осуществления вектор GAd получают из ChAd5. В некоторых вариантах осуществления вектор GAd получают из ChAd6. В некоторых вариантах осуществления вектор GAd получают из ChAd7. В некоторых вариантах осуществления вектор GAd получают из ChAd8. В некоторых вариантах осуществления вектор GAd получают из ChAd9. В некоторых вариантах осуществления вектор GAd получают из ChAd20. В некоторых вариантах осуществления вектор GAd получают из ChAd22. В некоторых вариантах осуществления вектор GAd получают из ChAd24. В некоторых вариантах осуществления вектор GAd получают из ChAd26. В некоторых вариантах осуществления вектор GAd получают из ChAd30. В некоторых вариантах осуществления вектор GAd получают из ChAd31. В некоторых вариантах осуществления вектор GAd получают из ChAd32. В некоторых вариантах осуществления вектор GAd получают из ChAd33. В некоторых вариантах осуществления вектор GAd получают из ChAd37. В некоторых вариантах осуществления вектор GAd получают из ChAd38. В некоторых вариантах осуществления вектор GAd получают из ChAd44. В некоторых вариантах осуществления вектор GAd получают из ChAd55. В некоторых вариантах осуществления вектор GAd получают из ChAd63. В некоторых вариантах осуществления вектор GAd получают из ChAd68. В некоторых вариантах осуществления вектор GAd получают из ChAd73. В некоторых вариантах осуществления вектор GAd получают из ChAd82. В некоторых вариантах осуществления вектор GAd получают из ChAd83.
Полипептид или гетерологичный полипептид в соответствии с настоящим описанием может быть вставлен в сайт или область (область вставки) вектора, которые не влияют на вирусную жизнеспособность полученного рекомбинантного вируса. Полипептид или гетерологичный полипептид в соответствии с настоящим описанием может быть вставлен в удаленную область Е1 в параллельной (транскрибированной от 5' к 3') или антипараллельной (транскрибированной в направлении от 3' к 5' относительно основной цепи вектора) ориентации. Кроме того, соответствующие регуляторные элементы транскрипции, которые способны направлять экспрессию полипептида или гетерологичного полипептида в соответствии с настоящим описанием в клетках-хозяевах млекопитающих, для применения которых получен вектор, могут быть функционально связаны с полипептидом или гетерологичным полипептидом настоящего описания. «Оперативно связанные» последовательности включают в себя как последовательности управления экспрессией, которые примыкают к нуклеотидным последовательностям, которые они регулируют, так и регуляторные последовательности, которые действуют в транс-конфигурации или на расстоянии, позволяющем управлять регулируемой нуклеотидной последовательностью.
Рекомбинантные аденовирусные частицы могут быть получены и размножены в соответствии с любой общепринятой методикой в данной области техники (например, международная патентная публикация №WO 1996/17070) с использованием комплементарной клеточной линии или вируса хелперов, который поставляет в транс-конфигурации отсутствующие вирусные гены, необходимые для репликации вируса. Клеточные линии 293 (Graham et al., 1977, J. Gen. Virol. 36: 59-72), PER.C6 (см., например, патент США №5,994,128), E1 А549 и 911 обычно применяют для дополнения делеций Е1. Были созданы другие клеточные линии, комплементарные дефектным векторам (Yeh, et al., 1996, J. Virol. 70: 559-565; Kroughak and Graham, 1995, Human Gene Ther. 6: 1575-1586; Wang, et al., 1995, Gene Ther. 2: 775-783; Lusky, et al., 1998, J. Virol. 72: 2022-203; EP 919627 и международная патентная публикация №WO 1997/04119). Аденовирусные частицы могут быть выделены из супернатанта культуры, а также из клеток после лизиса и при необходимости дополнительно очищены в соответствии со стандартными методиками (например, хроматография, ультрацентрифугирование, как описано в международной патентной публикации №WO 1996/27677, международной патентной публикации №WO 1998/00524, международной патентной публикации №WO 1998/26048 и в международной патентной публикации №WO 2000/50573). Конструирование и способы размножения аденовирусных векторов также описаны, например, в патенте США №5,559,099, 5,837,511, 5,846,782, 5,851,806, 5,994,106, 5,994,128, 5,965,541, 5,981,225, 6,040,174, 6,020,191 и 6,113,913.
В настоящем описании предложен рекомбинантный аденовирус, содержащий вектор в соответствии с настоящим описанием. В настоящем описании также предложен рекомбинантный аденовирус человека (rAd), содержащий вектор в соответствии с настоящим описанием. В настоящем описании также предложен рекомбинантный аденовирус человека, полученный из серотипа 26 (rAd26), содержащий вектор в соответствии с настоящим описанием.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 1 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 1.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 3.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 5 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 5.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 7 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 7.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 9 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 9.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 11 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 11.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 13 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 13.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 15 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 15.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 17 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 17.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид SEQ ID NO: 19 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 19, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 19.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид SEQ ID NO: 21 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 21.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид SEQ ID NO: 23 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 23.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид, кодирующий аминокислотную последовательность SEQ ID NO: 25 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 25.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид, кодирующий аминокислотную последовательность SEQ ID NO: 27 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 27.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид, кодирующий аминокислотную последовательность SEQ ID NO: 29 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 29.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий полипептид, кодирующий аминокислотную последовательность SEQ ID NO: 31 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 31.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 33 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 33.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 35 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 35.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 37 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 37.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 39 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 39.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 41 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 41.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 43 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 43.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 45 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 45.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 47 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 47.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 49 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 49.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 51 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 51.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 53 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 53.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 55 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 55.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 57 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 57.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 59 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 59.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 61 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 61.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 63.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 65 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 65.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 67 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 67.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 69 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 69.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 71 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 71.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 73 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 73.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 75 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 75.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 77 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 77.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 79 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 79.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 81 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 81.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 83 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 83.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 85 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 85.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 87 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 87.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 89 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 89.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 91 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 91.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 93 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 93.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 95 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 95.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 97 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 97.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 99 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 99.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 101 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 101.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 103 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 103.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 105 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 105.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 107 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 107.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 109 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 109.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 111 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 111.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 113 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 113.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 115 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 115.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 117 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 117.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 119 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 119.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 121 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 121.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 123 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 123.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 125 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 125.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 127 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 127.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 129 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 129.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность последовательность SEQ ID NO: 131 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 131.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 133 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 133.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 135 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 135.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 137 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 137.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 139 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 139.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 141 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 141.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 143 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 143.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 145 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 145.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 147 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 147.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 149 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 149.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 151 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 151.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 153 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 153.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 155 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 155.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 157 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 157.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 159 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 159.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 161 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 161.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 163 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 163.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 165 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 165.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 167 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 167.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 169 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 169.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 171 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 171.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 173 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 173.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 175 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 175.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 177 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 177.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 179 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 179.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 181 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 181.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 183 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 183.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 185 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 185.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 187 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 187.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 189 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 189.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 191 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 191.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 193 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 193.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 195 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 195.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 197 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 197.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 199 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 199.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 201 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 201.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 203 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 203.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 205 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 205.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 207 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 207.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 209 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 209.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 211 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 211.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 213 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 213.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 215 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 215.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 217 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 217.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 219 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 219.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 221 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 221.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 223 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 223.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 225 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 225.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 227 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 227.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 229 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 229.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 231 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 231.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 233 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 233.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 235 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 235.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 237 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 237.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 239 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 239.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 241 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 241.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 243 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 243.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 245 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 245.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 247 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 247.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 249 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 249.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 251 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 251.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 253 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 253.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 255 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 255.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 257 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 257.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 259 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 259.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 261 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 261.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 263 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 263.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 265 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 265.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 267 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 267.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 269 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 269.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 271 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 271.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 273 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 273.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 275 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 275.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 277 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 277.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 279 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 279.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 281 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 281.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 283 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 283.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 285 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 285.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 287 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 287.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 289 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 289.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 291 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 291.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 293 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 293.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 295 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 295.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 297 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 297.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 299 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 299.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 301 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 301.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 303 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 303.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 305 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 305.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 307 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 307.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 309 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 309.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 311 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 311.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 313 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 313.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 315 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 315.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 317 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 317.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 319 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 319.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 321 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 321.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 323 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 323.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 325 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 325.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 327 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 327.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 329 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 329.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 331 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 331.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 333 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 333.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 335 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 335.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 337 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 337.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 339 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 339.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 341 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 341.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 343 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 343.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 345 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 345.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 347 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 347.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 349 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 349.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 351 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 351.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 353 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 353.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 355 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 355.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 357 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 357.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 359 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 359.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 361 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 361.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 363 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 363.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 365 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 365.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 367 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 367.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 369 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 369.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 371 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 371.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 373 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 373.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 375 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 375.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 377 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 377.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 379 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 379.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 381 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 381.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 383 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 383.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 385.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 387 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 387.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 389 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 389.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 391 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 391.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 393 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 393.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 395 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 395.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 397 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 397.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 399 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 399.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 401 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 401.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 403 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 403.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 405.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 407 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 407.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 421 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 421.
В некоторых вариантах осуществления вектор Ad26 содержит полинуклеотид, кодирующий аминокислотную последовательность двух или более полипептидов, выбранных из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
В настоящем описании также предложен рекомбинантный аденовирус человекообразных обезьян (rGAd), содержащий вектор в соответствии с настоящим описанием. В некоторых вариантах осуществления rGAd получают из GAd20. В некоторых вариантах осуществления rGAd получают из GAdl9. В некоторых вариантах осуществления rGAd получают из GAd21. В некоторых вариантах осуществления rGAd получают из GAd25. В некоторых вариантах осуществления rGAd получают из GAd26. В некоторых вариантах осуществления rGAd получают из GAd27. В некоторых вариантах осуществления rGAd получают из GAd28. В некоторых вариантах осуществления rGAd получают из GAd29. В некоторых вариантах осуществления rGAd получают из GAd30. В некоторых вариантах осуществления rGAd получают из GAd31. GAd19-21 и GAd25-31 описаны в международной патентной публикации №WO2019/008111 и представляют собой линии с высокой иммуногенностью, не имеющие ранее существовавшего иммунитета в общей популяции людей. Полинуклеотидная последовательность генома GAd20 описана в WO 2019/008111.
В настоящем описании также предложен рекомбинантный аденовирус шимпанзе, полученный из серотипа 20 (rChAd20), содержащий вектор в соответствии с настоящим описанием. В некоторых вариантах осуществления вирусный вектор содержит любой из полинуклеотидов в соответствии с настоящим изобретением, причем вектор получен из GAd20.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 1 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 1.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 3.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 5 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 5.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 7 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 7.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 9 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 9.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 11 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 11.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 13 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 13.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 15 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 15.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 17 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 17.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 19 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 19, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 19.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 21 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 21.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 23 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 23.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 25 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 25.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 27 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 27.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 29 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 29.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 31 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 31.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 33 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 33.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 35 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 35.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 37 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 37.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 39 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 39.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 41 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 41.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 43 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 43.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 45 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 45.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 47 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 47.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 49 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 49.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 51 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 51.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 53 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 53.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 55 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 55.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 57 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 57.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 59 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 59.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 61 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 61.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 63.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 65 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 65.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 67 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 67.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 69 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 69.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 71 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 71.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 73 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 73.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 75 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 75.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 77 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 77.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 79 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 79.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 81 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 81.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 83 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 83.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 85 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 85.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 87 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 87.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 89 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 89.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 91 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 91.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 93 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 93.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 95 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 95.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 97 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 97.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 99 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 99.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 101 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 101.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 103 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 103.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 105 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 105.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 107 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 107.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 109 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 109.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 111 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 111.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 113 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 113.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 115 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 115.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 117 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 117.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 119 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 119.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 121 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 121.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 123 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 123.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 125 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 125.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 127 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 127.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 129 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 129.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 131 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 131.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 133 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 133.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 135 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 135.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 137 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 137.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 139 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 139.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 141 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 141.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 143 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 143.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 145 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 145.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 147 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 147.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 149 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 149.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 151 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 151.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 153 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 153.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 155 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 155.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 157 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 157.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 159 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 159.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 161 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 161.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 163 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 163.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 165 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 165.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 167 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 167.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 169 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 169.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 171 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 171.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 173 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 173.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 175 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 175.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 177 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 177.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 179 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 179.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 181 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 181.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 183 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 183.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 185 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 185.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 187 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 187.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 189 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 189.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 191 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 191.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 193 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 193.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 195 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 195.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 197 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 197.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 199 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 199.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 201 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 201.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 203 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 203.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 205 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 205.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 207 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 207.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 209 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 209.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 211 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 211.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 213 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 213.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 215 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 215.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 217 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 217.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид; кодирующий аминокислотную последовательность SEQ ID NO: 219 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 219.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 221 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 221.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 223 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 223.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 225 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 225.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 227 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 227.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 229 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 229.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 231 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 231.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 233 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 233.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 235 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 235.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 237 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 237.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 239 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 239.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 241 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 241.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 243 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 243.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 245 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 245.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 247 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 247.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 249 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 249.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 251 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 251.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 253 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 253.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 255 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 255.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 257 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 257.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 259 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 259.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 261 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 261.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 263 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 263.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 265 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 265.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 267 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 267.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 269 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 269.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 271 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 271.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 273 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 273.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 275 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 275.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 277 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 277.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 279 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 279.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 281 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 281.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 283 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 283.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 285 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 285.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 287 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 287.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 289 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 289.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 291 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 291.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 293 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 293.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 295 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 295.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 297 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 297.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 299 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 299.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 301 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 301.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 303 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 303.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 305 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 305.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 307 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 307.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 309 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 309.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 311 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 311.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 313 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 313.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 315 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 315.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 317 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 317.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 319 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 319.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 321 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 321.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 323 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 323.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 325 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 325.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 327 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 327.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 329 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 329.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 331 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 331.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 333 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 333.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 335 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 335.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 337 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 337.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 339 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 339.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 341 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 341.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 343 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 343.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 345 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 345.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 347 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 347.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 349 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 349.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 351 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 351.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 353 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 353.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 355 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 355.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 357 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 357.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 359 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 359.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 361 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 361.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 363 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 363.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 365 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 365.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 367 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 367.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 369 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 369.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 371 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 371.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 373 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 373.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 375 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 375.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 377 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 377.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 379 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 379.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 381 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 381.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 383 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 383.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 385.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 387 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 387.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 389 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 389.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 391 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 391.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 393 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 393.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 395 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 395.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 397 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 397.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 399 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 399.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 401 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 401.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 403 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 403.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 405.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 407.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 421.
В некоторых вариантах осуществления вектор GAd20 содержит полинуклеотид, кодирующий аминокислотную последовательность двух или более полипептидов, выбранных из SEQ IDNO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
Поксвирусные векторы
В некоторых вариантах осуществления вирусный вектор получен из поксвируса. В некоторых вариантах осуществления рекомбинантный вирус, содержащий вектор, получен из поксвируса.
Поксвирусные (Poxviridae) векторы могут быть получены из вируса натуральной оспы (вариолы), вируса осповакцины, вируса коровьей оспы или вируса оспы обезьян. Примерами вирусов осповакцины являются вирус осповакцины Копенгаген (W), аттенуированный вирус осповакцины Нью-Йорк (NYVAC), ALVAC, TROVAC и модифицированный вирус осповакцины Анкара (MVA).
MVA происходит из кожного штамма осповакцины Анкара (вирус хориоалантоисной осповакцины Анкара (CVA)), который сохранялся в Институте вакцинации, Анкара, Турция многие годы и использовался в качестве основы для вакцинации людей. Однако в связи с часто серьезными поствакцинальными осложнениями, связанными с вирусами осповакцины (VACV), предпринималось несколько попыток получить более ослабленную, более безопасную вакцину против вируса натуральной оспы.
MVA получали с помощью 516 последовательных пассажей на фибробластах куриного эмбриона вируса CVA (см. Meyer et al., J. Gen. Virol., 72: 1031-1038 (1991) и патент США №10,035,832). Вследствие этих длительных пассажей полученный вирус MVA удалил около 31 т.п.н. из геномной последовательности и, следовательно, описывался как высоко рестриктированный к птичьим клеткам (Meyer, Н. et al., Mapping of deletions in the genome of the highly attenuated vaccinia virus MVA and their influence on virulence, J. Gen. Virol. 72, 1031-1038, 1991; Meisinger-Henschel etal., Genomic sequence of chorioallantois vaccinia virus Ankara, the ancestor of modified vaccinia virus Ankara, J. Gen. Virol. 88, 3249-3259, 2007). Сравнение генома MVA с его родительским геномом (CVA) позволило выявить 6 основных делеций геномной ДНК (делеции I, II, III, IV, V и VI) с полным количеством пар оснований 31,000. (Meyer et al., J. Gen. Virol. 72:1031-8 (1991)). В различных моделях на животных было показано, что полученный в результате MVA был в значительной степени невирулентный (Mayr, A. & Danner, K. Vaccination against pox diseases under immunosuppressive conditions, Dev. Biol. Stand. 41: 225-34, 1978). Поскольку для ослабления MVA использовали множество пассажей, существует ряд различных штаммов или изолятов в зависимости от числа пассажей в клетках CEF, таких как MVA 476 MG/14/78, MVA-571, MVA-572, MVA-574, MVA-575 и MVA-BN. MVA 476 MG/14/78 описан, например, в международной патентной публикации № WO 2019/115816 A1. Штамм MVA-572 депонирован в Европейской коллекции культур клеток животных («ЕСАСС»), Агентство по защите здоровья, Отдел микробиологии, Porton Down, Salisbury SP4 OJG, United Kingdom (Великобритания), под номером депонирования ЕСАСС 94012707 от 27 января 1994 г. Штамм MVA-575 депонирован в ЕСАСС под номером депонирования ЕСАСС 00120707 от 7 декабря 2000 года; Штамм MVA-Bavarian Nordic (MVA-BN) депонирован в ЕСАСС под номером депонирования V00080038 от 30 августа 2000 г. Геномные последовательности MVA-BN и MVA-572 доступны в GenBank (учетные номера DQ983238 и DQ983237 соответственно). Геномные последовательности других штаммов MVA могут быть получены с использованием стандартных способов секвенирования.
Векторы и вирусы согласно настоящему изобретению могут быть получены из любого штамма MVA или дополнительных производных штамма MVA. Дополнительным примером штамма MVA является депонированный VR-1508, депонированный в Американской коллекции типовых культур (АТСС), г. Манассас, штат Вирджиния. 20108, США.
Термин «производные» MVA относится к вирусам, показывающим по существу такие же характеристики, как и у исходного MVA, но показывающим различия в одной или более частях их геномов.
В некоторых вариантах осуществления вектор MVA получают из MVA 476 MG/14/78. В некоторых вариантах осуществления вектор MVA получают из MVA-571. В некоторых вариантах осуществления вектор MVA получают из MVA-572. В некоторых вариантах осуществления вектор MVA получают из MVA-574. В некоторых вариантах осуществления вектор MVA получают из MVA-575. В некоторых вариантах осуществления вектор MVA получают из MVA-BN.
Полинуклеотид или гетерологичный полинуклеотид в соответствии с настоящим описанием может быть вставлен в сайт или область (область вставки) вектора MVA, которые не влияют на вирусную жизнеспособность полученного рекомбинантного вируса. Такие области можно легко идентифицировать путем тестирования сегментов вирусной ДНК на области, которые обеспечивают рекомбинантное образование, не оказывая существенного влияния на вирусную жизнеспособность рекомбинантного вируса. Ген тимидинкиназы (ТК) представляет собой область вставки, которая может применяться и присутствовать во многих вирусах, например во всех исследованных геномах поксвирусов. Кроме того, MVA содержит 6 сайтов естественной делеции, каждый из которых может быть использован в качестве мест вставки (например, делеция I, II, III, IV, V и VI; см., например, патент США №5,185,146 и патент США №6.440,442. В качестве места вставки можно также использовать одну или более межгенных областей (IGR) MVA, таких как IGR IGR07/08, IGR 44/45, IGR 64/65, IGR 88/89, IGR 136/137 и IGR 148/149 (см., например, патентные публикации США №2018/0064803). Дополнительные подходящие места вставки описаны в международной патентной публикации № WO 2005/048957.
Рекомбинантные поксвирусные частицы, такие как rMVA, получают, как описано в данной области (Piccini, et al., 1987, Methods of Enzymology 153: 545-563; патент США №4,769,330; патент США №4,772,848; патент США №4,603,112; патент США №5,100,587 и патент США №5,179,993). В примере способа последовательность ДНК для вставки в вирус может быть помещена в конструкт плазмиды Е. coli, в который была вставлена ДНК, гомологичная участку ДНК MVA. Отдельно вставляемую последовательность ДНК может быть лигирована с промотором. Связь промотор-ген может быть расположена в конструкте плазмиды так, чтобы связь промотор-ген фланкировалась с обоих концов ДНК, гомологичной последовательности ДНК, фланкирующей область ДНК MVA, содержащую несущественный локус. Полученный в результате конструкт плазмиды может быть амплифицирован путем размножения внутри бактерий Е. coli и выделен. Выделенная плазмида, содержащая вставляемую последовательность гена ДНК, может быть трансфицирована в клеточную культуру, например фибробластов куриного эмбриона (CEF), одновременно с инфицированием культуры MVA. Рекомбинация между гомологичной ДНК MVA в плазмиде и вирусным геномом соответственно может генерировать MVA, модифицированный посредством присутствия чужеродных последовательностей ДНК. частицы rMVA могут быть выделены из супернатанта культуры или из культивированных клеток после этапа лизиса (например, химический лизис, замораживание/размораживание, осмотический шок, обработка ультразвуком и т.п.). Для удаления загрязняющего вируса дикого типа можно использовать последовательные циклы очистки бляшкообразования. Затем вирусные частицы могут быть очищены с помощью методик, известных специалистам в данной области (например, хроматографические способы или ультрацентрифугирование на хлориде цезия или градиенте сахарозы).
В данном документе предусмотрен вирусный вектор, содержащий любой из полинуклеотидов по настоящему изобретению, причем вектор получен из MVA. В настоящем описании также предложена рекомбинантная модифицированная осповакцина Анкара (rMVA), содержащая вектор в соответствии с настоящим описанием.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 1 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 1.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 3.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 5 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 5.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 7 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 7.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 9 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 9.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 11 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 11.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 13 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 13.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 15 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 15.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 17 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 17.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 19 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 19, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 19.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 21 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 21.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 23 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 23.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 25 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 25.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 27 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 27.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 29 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 29.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 31 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 31.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 33 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 33.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 35 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 35.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 37 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 37.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 39 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 39.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 41 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 41.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 43 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 43.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 45 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 45.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 47 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 47.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 49 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 49.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 51 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 51.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 53 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 53.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 55 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 55.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 57 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 57.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 59 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 59.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 61 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 61.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 63.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 65 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 65.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 67 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 67.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 69 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 69.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 71 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 71.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 73 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 73.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 75 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 75.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 77 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 77.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 79 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 79.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 81 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 81.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 83 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 83.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 85 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 85.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 87 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 87.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 89 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 89.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ IDNO: 91 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 91.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 93 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 93.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 95 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 95.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 97 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 97.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 99 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 99.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 101 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 101.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 103 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 103.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 105 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 105.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 107 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 107.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 109 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 109.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 111 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 111.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 113 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 113.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 115 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 115.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 117 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 117.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 119 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 119.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 121 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 121.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 123 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 123.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 125 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 125.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 127 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 127.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 129 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 129.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 131 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 131.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 133 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 133.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 135 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 135.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 137 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 137.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 139 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 139.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 141 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 141.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 143 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 143.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 145 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 145.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 147 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 147.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 149 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 149.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 151 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 151.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 153 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 153.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 155 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 155.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 157 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 157.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 159 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 159.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 161 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 161.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 163 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 163.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 165 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 165.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 167 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 167.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 169 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 169.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 171 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 171.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 173 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 173.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 175 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 175.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 177 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 177.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 179 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 179.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 181 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 181.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 183 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 183.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 185 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 185.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 187 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 187.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 189 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 189.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 191 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 191.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 193 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 193.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 195 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 195.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 197 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 197.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 199 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 199.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 201 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 201.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 203 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 203.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 205 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 205.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 207 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 207.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 209 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 209.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 211 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 211.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 213 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 213.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 215 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 215.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 217 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 217.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 219 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 219.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 221 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 221.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 223 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 223.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 225 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 225.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 227 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 227.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 229 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 229.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 231 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 231.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 233 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 233.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 235 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 235.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 237 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 237.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 239 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 239.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 241 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 241.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 243 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 243.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 245 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 245.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 247 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 247.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 249 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 249.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 251 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 251.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 253 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 253.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 255 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 255.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 257 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 257.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 259 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 259.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 261 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 261.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 263 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 263.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 265 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 265.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 267 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 267.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 269 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 269.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 271 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 271.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 273 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 273.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 275 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 275.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 277 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 277.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 279 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 279.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 281 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 281.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 283 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 283.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 285 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 285.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 287 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 287.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 289 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 289.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 291 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 291.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 293 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 293.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 295 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 295.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 297 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 297.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 299 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 299.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 301 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 301.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 303 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 303.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 305 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 305.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 307 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 307.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 309 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 309.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 311 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 311.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 313 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 313.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 315 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 315.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 317 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 317.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 319 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 319.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 321 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 321.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 323 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 323.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 325 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 325.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 327 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 327.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 329 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 329.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 331 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 331.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 333 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 333.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 335 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 335.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 337 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 337.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 339 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 339.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 341 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 341.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 343 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 343.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 345 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 345.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 347 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 347.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 349 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 349.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 351 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 351.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 353 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 353.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 355 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 355.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 357 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 357.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 359 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 359.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 361 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 361.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид; кодирующий аминокислотную последовательность SEQ ID NO: 363 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 363.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 365 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 365.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 367 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 367.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 369 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 369.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 371 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 371.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 373 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 373.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 375 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 375.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 377 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 377.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 379 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 379.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 381 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 381.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 383 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 383.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 385.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 387 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 387.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 389 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 389.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 391 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 391.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 393 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 393.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 395 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 395.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 397 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 397.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 399 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 399.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 401 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 401.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 403 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 403.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 405.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 407.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 421.
В некоторых вариантах осуществления вектор MVA содержит полинуклеотид, кодирующий аминокислотную последовательность двух или более полипептидов, выбранных из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
Самореплицирующиеся молекулы РНК
В некоторых вариантах осуществления вирусный вектор представляет собой самореплицирующуюся молекулу РНК, полученную из альфавируса.
Самореплицирующаяся молекула РНК может быть получена из альфавируса. Альфавирусы могут принадлежать к группе VEEV/EEEV, группе SF или группе SIN. Неограничивающие примеры альфавирусов группы SF включают вирус леса Семлики, вирус О'Ньонг-Ньонг, вирус Росс-Ривер, вирус Мидделбурга, вирус Чикунгунья, вирус леса Барма, вирус Гета, вирус Маяро, вирус Сагияма, вирус Бебару и вирус Уна. Неограничивающие примеры альфавирусов группы SIN включают вирус Синдбис, вирус Гирдвуд С.А., южноафриканский арбовирус №86, вирус Окельбо, вирус Aura, вирус Бабанки, вирус Whataroa и вирус Кызылагач. Неограничивающие примеры альфавирусов группы VEEV/EEEV включают вирус восточного энцефалита лошадей (EEEV), вирус венесуэльского энцефалита лошадей (VEEV), вирус эверглейд (EVEV), вирус Мукамбо (MUCV), вирус Пиксуна (PIXV), вирус Мидделбурга (MIDV), вирус Чикунгунья (CHIKV), вирус О'Ньонг-Ньонг (ONNV), вирус Росс-Ривер (RRV), вирус леса Бармах (BF), вирус Гета (GET), вирус Сагияма (SAGV), вирус Бебару (BEBV), вирус Маяро (MAYV) и вирус Уна (UNAV).
Самореплицирующиеся молекулы РНК могут быть получены из геномов альфавирусов, что означает, что они имеют некоторые структурные характеристики геномов альфавирусов или сходны с ними. Самореплицирующиеся молекулы РНК могут быть получены из модифицированных геномов альфавируса.
Самореплицирующиеся молекулы РНК могут быть получены из вируса восточного энцефалита лошадей (EEEV), вируса венесуэльского энцефалита лошадей (VEEV), вируса эверглейда (EVEV), вируса Мукамбо (MUCV), вируса леса Семлики (SFV), вируса Пиксуна (PIXV), вируса Мидделбурга (MIDV), вируса Чикунгунья (CHIKV), вируса О'Ньонг-Ньонг (ONNV), вируса Росс-Ривер (RRV), вируса леса Барма (BF), вируса Гета (GET), вируса Сагияма (SAGV), вируса Бебару (BEBV), вируса Майаро (MAYV), вируса Уна (UNAV), вируса Синдбис (SINV), вируса Аура (AURAV), вируса Ватароа (WHAV), вируса Бабанки (BABV), вируса Кызылагач (KYZV), вируса западного энцефалита лошадей (WEEV), вируса Highland J (HJV), вируса Форт-Моргана (FMV), вируса Ндуму (NDUV) и вируса Багги-Крик. Подходят как вирулентные, так и авирулентные штаммы альфавируса. В некоторых вариантах осуществления репликон РНК альфавируса относится к вирусу Синдбис (SIN), вирусу леса Семлики (SFV), вирусу Росс-Ривер (RRV), вирусу венесуэльского энцефалита лошадей (VEEV) или вирусу восточного энцефалита лошадей (EEEV).
В некоторых вариантах осуществления самореплицирующаяся молекула РНК, полученная из альфавируса, представляет собой вирус венесуэльского лошадиного энцефалита (VEEV).
Самореплицирующиеся молекулы РНК могут содержать последовательности РНК (или кодируемые аминокислотные последовательности) генома альфавируса дикого типа Нового Света или Старого Света. Любая из самореплицирующихся молекул РНК, описанных в данном документе, может содержать последовательности РНК, «полученные из» или «на основе» последовательностей генома альфавируса дикого типа, что означает, что они имеют по меньшей мере 60%, или по меньшей мере 65%, или по меньшей мере 68%, или по меньшей мере 70%, или по меньшей мере 80%, или по меньшей мере 85%, или по меньшей мере 90%, или по меньшей мере 95%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100%, или 80-99%, или 90-100%, или 95-99%, или 95-100%, или 97-99%, или 98-99% идентичность последовательности с последовательностью РНК (которая может быть соответствующей последовательностью РНК) из генома РНК альфавируса дикого типа, который может быть геномом альфавируса Нового Света или Старого Света.
Самореплицирующиеся молекулы РНК содержат всю генетическую информацию, необходимую для управления собственной амплификацией или саморепликацией в пермиссивной клетке. Для управления собственной репликацией Самореплицирующиеся молекулы РНК кодируют полимеразу, репликазу или другие белки, которые могут взаимодействовать с белками, происходящими из вируса или клетки-хозяина, нуклеиновыми кислотами или рибонуклеопротеинами, чтобы катализировать процесс амплификации РНК; и содержат цис-действующие последовательности РНК, необходимые для репликации и транскрипции РНК, кодируемой репликоном. Таким образом, репликация РНК приводит к образованию множества дочерних РНК. Эти дочерние РНК, а также коллинеарные субгеномные транскрипты могут быть транслированы для обеспечения экспрессии интересующего гена in situ или могут быть транскрибированы для получения дополнительных транскриптов с тем же смыслом, что и доставленная РНК, которые транслируются для обеспечения экспрессии in situ интересующего гена. Общими результатами этой последовательности транскрипций является огромное увеличение количества введенных репликонов РНК, и поэтому интересующий кодируемый ген становится основным полипептидным продуктом клеток.
В геноме альфавирусов есть две открытые рамки считывания (ORF), неструктурные (ns) и структурные гены. ns ORF кодирует белки (nsP1-nsP4), необходимые для транскрипции и репликации вирусной РНК, продуцируются в виде полипротеина и являются механизмом репликации вируса. Структурная ORF кодирует три структурных белка: основной нуклеокапсидный белок С и оболочечные белки Р62 и Е1, которые связываются в виде гетеродимера. Поверхностные гликопротеины вируса, закрепленные на мембране, отвечают за распознавание рецепторов и проникновение в клетки-мишени посредством слияния мембран. Четыре гена ns-белка кодируются генами в 5'-двух третях генома, в то время как три структурных белка транслируются с субгеномной мРНК, коллинеарной 3'-трети генома.
Самореплицирующиеся молекулы РНК можно использовать в качестве основы для введения чужеродных последовательностей в клетки-хозяева путем замены вирусных последовательностей, кодирующих структурные гены, или путем вставки чужеродных последовательностей 5' или У последовательностей, кодирующих структурные гены. Их можно сконструировать для замены вирусных структурных генов ниже репликазы, которые находятся под контролем субгеномного промотора, генами, представляющими интерес, например, любой из полинуклеотидов, кодирующий любой из полипептидов в соответствии с настоящим описанием. При трансфекции репликаза, которая транслируется немедленно, взаимодействует с 5'- и 3'-концами геномной РНК и синтезирует комплементарные копии геномной РНК. Они действуют как матрицы для синтеза новых положительноцепочечных, кэпированных и полиаденилированных геномных копий и субгеномных транскриптов. Амплификация в конечном итоге приводит к очень высокому количеству копий РНК, до 2×105 копий на клетку. Результатом является равномерная и/или повышенная экспрессия генов, представляющих интерес (например, полинуклеотида, кодирующего один или более полипептидов в соответствии с настоящим изобретением), которые могут повлиять на эффективность вакцины или терапевтическое воздействие лечения.
Таким образом, вакцины на основе самореплицирующихся молекул РНК могут иметь очень низкую дозировку из-за очень большого количества генерируемых копий РНК по сравнению с обычным вирусным вектором.
Самореплицирующиеся молекулы РНК по настоящему изобретению, содержащие РНК, кодирующую один или более полипептидов неоантигена множественной миеломы в соответствии с настоящим изобретением, можно использовать в качестве терапевтических средств путем их доставки субъекту, страдающему множественной миеломой или с риском развития множественной миеломы, с использованием различных технологий, включая вирусные векторы, как описано в данном документе или другие технологии доставки, также описанные в данном документе.
Полинуклеотиды неоантигенов множественной миеломы в соответствии с настоящим описанием могут экспрессироваться под контролем субгеномного промотора. В некоторых вариантах осуществления вместо нативного субгеномного промотора субгеномная РНК может быть помещена под контроль внутреннего участка посадки рибосомы (IRES), полученного из вирусов энцефаломиокардита (EMCV), вирусов вирусной диареи крупного рогатого скота (BVDV), полиовирусов, вирусов ящура (FMD), энтеровируса 71 или вирусов гепатита С.Субгеномные промоторы имеют длину от 24 нуклеотидов (вирус Синдбис) до более 100 нуклеотидов (вирус некротического пожелтения жилок свеклы) и обычно находятся выше начала транскрипции.
В изобретении предусмотрена самореплицирующаяся молекула РНК, содержащая всю генетическую информацию, необходимую для управления собственной амплификацией или саморепликацией в пермиссивной клетке.
В настоящем описании также предложена самореплицирующаяся молекула РНК, которую можно использовать в качестве основы для введения чужеродных последовательностей в клетки-хозяева (например, полипептиды неоантигенов множественной миеломы в соответствии с настоящим описанием) путем замены вирусных последовательностей, кодирующих структурные гены.
В данном документе предусмотрен вирусный вектор, содержащий любой из полинуклеотидов по настоящему изобретению, где вектор представляет собой самореплицирующуюся молекулу РНК.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит последовательность РНК, кодирующую аминокислотную последовательность SEQ ID NO: 1 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 1.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 3 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 3.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 5 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 5.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 7 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 7.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 9 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 9.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 11 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 11.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 13 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 13.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 15 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 15.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 17 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 17.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 19 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 19.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 21 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 21.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 23 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 23.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 25 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 25.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 27 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 27.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 29 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 29.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 31 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 31.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 33 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 33.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 35 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 35.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 37 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 37.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 39 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 39.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 41 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 41.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 43 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 43.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 45 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 45.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 47 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 47.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 49 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 49.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 51 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 51.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 53 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 53.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 55 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 55.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 57 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 57.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 59 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 59.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 61 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 61.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 63 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 63.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 65 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 65.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 67 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 67.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 69 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 69.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 71 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 71.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 73 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 73.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 75 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 75.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 77 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 77.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 79 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 79.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 81 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 81.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 83 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 83.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 85 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 85.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 87 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 87.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 89 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 89.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 91 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 91.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 93 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 93.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 95 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 95.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 97 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 97.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 99 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 99.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 101 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 101.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 103 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 103.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 105 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 105.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 107 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 107.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 109 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 109.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 111 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 111.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 113 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 113.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 115 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 115.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 117 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 117.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 119 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 119.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 121 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 121.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 123 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 123.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 125 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 125.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 127 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 127.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 129 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 129.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 131 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 131.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 133 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 133.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 135 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 135.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 137 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 137.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 139 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 139.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 141 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 141.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 143 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 143.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 145 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 145.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 147 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 147.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 149 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 149.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 151 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 151.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 153 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 153.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 155 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 155.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 157 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 157.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 159 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 159.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 161 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 161.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 163 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 163.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 165 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 165.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 167 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 167.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 169 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 169.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 171 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 171.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 173 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 173.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 175 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 175.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 177 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 177.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 179 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 179.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 181 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 181.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 183 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 183.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 185 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 185.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 187 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 187.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 189 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 189.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 191 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 191.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 193 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 193.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 195 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 195.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 197 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 197.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 199 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 199.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 201 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 201.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 203 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 203.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 205 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 205.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 207 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 207.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 209 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 209.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 211 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 211.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 213 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 213.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 215 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 215.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 217 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 217.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 219 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 219.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 221 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 221.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 223 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 223.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 225 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 225.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 227 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 227.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 229 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 229.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 231 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 231.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 233 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 233.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 235 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 235.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 237 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 237.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 239 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 239.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 241 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 241.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 243 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 243.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 245 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 245.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 247 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 247.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 249 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 249.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 251 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 251.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 253 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 253.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 255 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 255.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 257 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 257.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 259 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 259.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 261 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 261.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 263 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 263.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 265 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 265.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 267 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 267.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 269 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 269.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 271 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 271.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 273 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 273.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 275 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 275.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 277 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 277.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 279 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 279.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 281 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 281.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 283 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 283.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 285 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 285.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 287 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 287.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 289 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 289.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 291 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 291.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 293 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 293.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 295 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 295.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 297 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 297.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 299 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 299.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 301 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 301.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 303 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 303.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 305 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 305.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 307 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 307.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 309 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 309.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 311 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 311.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 313 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 313.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 315 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 315.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 317 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 317.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 319 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 319.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 321 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 321.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 323 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 323.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 325 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 325.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 327 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 327.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 329 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 329.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 331 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 331.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 333 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 333.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 335 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 335.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 337 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 337.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 339 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 339.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 341 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 341.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 343 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 343.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 345 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 345.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 347 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 347.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 349 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 349.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 351 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 351.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 353 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 353.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 355 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 355.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 357 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 357.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 359 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 359.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 361 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 361.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 363 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 363.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 365 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 365.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 367 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 367.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 369 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 369.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 371 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 371.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 373 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 373.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 375 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 375.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 377 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 377.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 379 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 379.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 381 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 381.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 383 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 383.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 385.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 387 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 387.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 389 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 389.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 391 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 391.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 393 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 393.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 395 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 395.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 397 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 397.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 399 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 399.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 401 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 401.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 403 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 403.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность SEQ ID NO: 405 или имеющий по меньшей мере 90% идентичность последовательности, или по меньшей мере 95% идентичность последовательности, или по меньшей мере 99% идентичность последовательности с SEQ ID NO: 405.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий аминокислотную последовательность двух или более полипептидов, выбранных из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
Любая из вышеуказанных самореплицирующихся молекул РНК может дополнительно содержать одно или более из следующего:
• один или более неструктурных генов nsP1, nsP2, nsP3 и nsP4;
• по меньшей мере одно из мотива DLP, 5' UTR, 3'UTR и поли-А; и
• субгеномный промотор.
В некоторых вариантах осуществления, например, самореплицирующаяся молекула РНК может содержать одно или более из следующего:
• один или более неструктурных генов nsP1, nsP2, nsP3 и nsP4;
• по меньшей мере одно из мотива DLP, 5' UTR, 3'UTR и поли-А; и
• субгеномный промотор; и
• РНК, кодирующая любой из полипептидов в соответствии с настоящим описанием, и функционально связанная с субгеномным промотором.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит последовательность РНК, кодирующую белок или пептид; 5'-и 3'-нетранслируемые области альфавируса; Последовательности РНК, кодирующие аминокислотные последовательности, полученные из неструктурных белков nsP1, nsP2, nsP3 и nsP4 альфавируса Нового Света VEEV; субгеномного промотора, функционально связанного с трансляцией последовательности РНК, кодирующей белок, и регулирующего ее; 5'-кэпа и 3'-поли-А-хвоста; положительной смысловой одноцепочечной РНК; DLP из вируса Синдбис выше неструктурного белка 1 (nsP1); элемент пропуска рибосомы 2А и нуклеотидного повтора nsp1 ниже от 5'-UTR и выше DLP.
В некоторых вариантах осуществления молекулы самореплицирующейся РНК могут составлять по меньшей мере 1 т.п.н., или по меньшей мере 2 т.п.н., или по меньшей мере 3 т.п.н., или по меньшей мере 4 т.п.н., или по меньшей мере 5 т.п.н., или по меньшей мере 6 т.п.н., или по меньшей мере 7 т.п.н., или по меньшей мере 8 т.п.н., или по меньшей мере 10 т.п.н., или по меньшей мере 12 т.п.п., или по меньшей мере 15 т.п.н., или по меньшей мере 17 т.п.н., или по меньшей мере 19 т.п.н., или по меньшей мере 20 т.п.н., или могут составлять 100 п.о.-8 т.п.н. или 500 п.о.-8 т.п.н. или 500 п.о.-7 т.п.н. или 1-7 т.п.н. или 1-8 т.п.н. или 2-15 т.п.н. или 2-20 т.п.н. или 5-15 т.п.н. или 5-20 т.п.н. или 7-15 т.п.н. или 7-18 т.п.н. или 7-20 т.п.н. по размеру.
Любая из описанных выше самореплицирующихся молекул РНК может дополнительно включать последовательность, кодирующую пептид аутопротеазы (например, аутокаталитический саморасщепляющийся пептид), где последовательность, кодирующая аутопротеазу, необязательно функционально связана выше со второй последовательностью нуклеиновой кислоты.
Как правило, любой сайт протеолитического расщепления, известный в данной области техники, может быть включен в молекулы нуклеиновой кислоты по настоящему изобретению и может представлять собой, например, последовательности протеолитического расщепления, которые расщепляются протеазой после выработки. Другие подходящие сайты протеолитического расщепления также включают последовательности протеолитического расщепления, которые могут быть расщеплены после добавления внешней протеазы. Используемый в данном документе термин «аутопротеаза» относится к «саморасщепляющемуся» пептиду, который обладает аутопротеолитической активностью и способен отщеплять себя от большего полипептидного фрагмента. Аутопротеаза была первые идентифицирована в вирусе ящура (FMDV), члене группы пикорнавирусов; впоследствии было идентифицировано несколько аутопротеаз, таких как, например, «2А-подобные» пептиды из вируса ринита лошадей А (Е2А), тешовируса-1 свиней (Р2А) и вируса Thosea asigna (Т2А), и их активность в протеолитическом расщеплении была показана также в различных эукариотических системах ex vitro и in vivo. Таким образом, понятие аутопротеаз доступно специалистам в данной области техники, поскольку было идентифицировано множество встречающихся в природе систем аутопротеаз. Хорошо изученными системами аутопротеаз являются, например, вирусные протеазы, белки развития (например, HetR, белки хеджехог), домен аутопротеазы RumA, UmuD и т.д.). Неограничивающие примеры аутопротеазных пептидов, подходящих для композиций и способов по настоящему изобретению, включают пептидные последовательности свиного тешовируса-1 2А (Р2А), вируса ящура 2А (F2A), вируса ринита А лошадей (ERAV) 2А (Е2А), вируса Thesa asigna 2А (Т2А), вирус цитоплазматического полиэдроза 2А (BmCPV2A), вирус Флашерия 2А (BmIFV2A) или их комбинация.
В некоторых вариантах осуществления кодирующая последовательность аутопротеазного пептида функционально связана ниже мотива DLP и выше первого и второго полинуклеотидов.
В некоторых вариантах осуществления аутопротеазный пептид содержит или состоит из пептидной последовательности, выбранной из группы, состоящей из свиного тешовируса-1 2А (Р2А), вируса ящура 2А (F2A), вируса ринита А лошадей (ERAV) 2А (Е2А), вируса Thesa asigna 2А (Т2А), вирус цитоплазматического полиэдроза 2А (BmCPV2A), вирус Флашерия 2А (BmIFV2A) или их комбинации. В некоторых вариантах осуществления аутопротеазный пептид включает пептидную последовательность свиного тешовируса-1 2А (Р2А).
В некоторых вариантах осуществления аутопротеазный пептид представляет собой свиной тешовирус-1 2А (Р2А).
Включение пептида Р2А в репликоны модифицированной вирусной РНК в соответствии с настоящим описанием позволяет высвобождать белок, кодируемый генами, представляющими интерес (например, полипептиды неоантигенов множественной миеломы в соответствии с настоящим описанием), из слияния капсид-ген, представляющий интерес.
В некоторых вариантах осуществления, раскрытых в данном документе, пептидная последовательность 2А (Р2А) свиного тешовируса-1 сконструирована в рамке считывания сразу после последовательности DLP и в рамке считывания непосредственно перед всеми GOI.
Любая из описанных выше самореплицирующихся молекул РНК может дополнительно включать мотив нисходящей петли (DLP) кодирующей последовательности.
Некоторые вирусы имеют последовательности, способные образовывать одну или несколько структур «петля-на-стебле», которые регулируют, например, увеличение экспрессии капсидных генов. Энхансер вирусного капсида, используемый в данном документе, относится к регуляторному элементу, содержащему последовательности, способные образовывать такие структуры «петля-на-стебле». В некоторых примерах структуры «петля-на-стебле» образованы последовательностями внутри кодирующей последовательности капсидного белка и называются последовательностями нисходящей петли (DLP). Как раскрыто в данном документе, эти структуры «петля-на-стебле» или их варианты можно использовать для регуляции, например, повышения уровня экспрессии представляющих интерес генов. Например, эти структуры «петля-на-стебле» или их варианты можно использовать в рекомбинантном векторе (например, в гетерологичном вирусном геноме) для усиления транскрипции и/или трансляции кодирующей последовательности, функционально связанной с ним ниже.
Известно, что репликация альфавируса в клетках-хозяевах индуцирует двухцепочечную РНК-зависимую протеинкиназу (PKR). PKR фосфорилирует эукариотический фактор инициации трансляции 2α (eIF2α). Фосфорилирование eIF2α блокирует инициацию трансляции мРНК и тем самым препятствует завершению продуктивного цикла репликации вирусов. Представители рода альфавирусов могут сопротивляться активации противовирусной РНК-активируемой протеинкиназы (PKR) за счет нисходящей петли (DLP), присутствующей внутри вирусных транскриптов 26S, что позволяет инициировать трансляцию этих мРНК независимо от eIF2. Структура DLP может задерживать рибосому на AUG дикого типа, и это поддерживает трансляцию субгеномной мРНК без потребности в функциональном eIF2α. Структура DLP была впервые охарактеризована в мРНК вируса Синдбис 26S (SINV), а также обнаружена в вирусе леса Семлики (SFV). Сообщается, что аналогичные структуры DLP присутствуют у по меньшей мере 14 других представителей рода альфавирусов, включая Новый Свет (например, MAYV, UNAV, EEEV (NA), EEEV (SA), AURAV) и Старый Свет (SV, SFV, BEBV, RRV, SAG, GETV, MIDV, CHIKV и ONNV). DLP расположена ниже AUG в мРНК SINV 26S и у других представителей рода альфавирусов.
В некоторых вариантах осуществления молекулы нуклеиновой кислоты по настоящему изобретению могут включать последовательность, кодирующую интересующий ген (GOI), функционально связанную с мотивом(-ами) DLP, и/или последовательность, кодирующую мотивы DLP.
В некоторых вариантах осуществления DLP самореплицирующейся молекулы РНК получают из вируса Синдбис.
В некоторых вариантах осуществления нисходящая петля (DLP) содержит по меньшей мере одну структуру РНК-стебель-петля.
В некоторых случаях активность DLP зависит от расстояния между мотивом DLP и инициирующим кодоном AUG (AUGi). Расстояние AUG-DLP в мРНК альфавируса 26S настроено на топологию ES6S-области рибосомной 18S рРНК таким образом, что позволяет разместить AUGi в Р-сайте 40S-субъединицы, задержанной DLP, что позволяет включать Met-tRNA без участия eIF2. В случае вируса Синдбис мотив DLP обнаруживается в первых ~150 нуклеотидах субгеномной РНК Синдбис. Шпилька расположена ниже инициирующего кодона AUG капсида Синдбис (AUG в нуклеотиде 50 субгеномной РНК Синдбис) и приводит к остановке рибосомы, так что для инициации трансляции используется правильный капсидный ген AUG.
Не привязываясь к какой-либо конкретной теории, считается, что размещение мотива DLP выше кодирующей последовательности для любого GOI обычно приводит к слитому белку N-концевых капсидных аминокислот, которые кодируются в области шпильки с белком, кодируемым GOI, поскольку инициация происходит на AUG капсида, а не на AUG GOI.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит нисходящую петлю, расположенную выше неструктурного белка 1 (nsP1).
В некоторых вариантах осуществления нисходящая петля расположена перед неструктурным белком 1 (nsP1) и соединена с nsP1 с помощью элемента пропуска рибосомы 2А (Р2А) тешовируса-1 свиньи.
Содержащая DLP самореплицирующаяся РНК в соответствии с настоящим описанием также может быть подходящей для придания устойчивости врожденной иммунной системе у субъекта. Немодифицированные репликоны РНК чувствительны к исходному состоянию врожденной иммунной системы клеток, в которые они вводятся. Если клетки/индивидуумы находятся в высокоактивном состоянии врожденной иммунной системы, это может отрицательно сказаться на характеристиках репликона РНК (например, на репликацию и экспрессию GOI). Путем разработки DLP для контроля инициации трансляции белка, особенно неструктурных белков, влияние существовавшего ранее состояния активации врожденной иммунной системы на влияние эффективной репликации репликона РНК устраняется или уменьшается. Результатом является более однородная и/или усиленная экспрессия GOI, которая может повлиять на эффективность вакцины или терапевтическое воздействие лечения.
Мотив DLP самореплицирующейся РНК по настоящему изобретению может обеспечивать эффективную трансляцию мРНК в клеточной среде, где трансляция клеточной мРНК ингибируется. Когда DLP связан с трансляцией генов неструктурных белков вектора репликона, белки репликазы и транскриптазы способны инициировать функциональную репликацию в PKR-активированной клеточной среде. Когда DLP связан с трансляцией субгеномных мРНК, возможна устойчивая экспрессия GOI, даже если клеточная мРНК ограничена активацией врожденного иммунитета. Соответственно, разработка самореплицирующихся РНК, содержащих структуры DLP, которые помогают управлять трансляцией как генов неструктурных белков, так и субгеномных мРНК, обеспечивает мощный способ преодоления активации врожденного иммунитета.
Примеры вектора самореплицирующейся РНК, содержащего мотив DLP, описаны в публикации заявки на патент США 2018/0171340 и публикации международной заявки на патент WO 2018106615, содержание которых полностью включено в данный документ посредством ссылки.
Любая из описанных выше самореплицирующихся молекул РНК может дополнительно содержать неструктурные гены nsP1, nsP2, nsP3 и/или nsP4.
Геномы альфавирусов кодируют неструктурные белки nsP1, nsP2, nsP3 и nsP4, которые продуцируются как единый полипротеиновый предшественник, иногда обозначаемый Р1234 (или nsP1-4, или nsP1234), и который расщепляется на зрелые белки посредством протеолитического процессия. nsP1 может иметь размер около 60 кДа, может обладать метилтрансферазной активностью и участвовать в реакции кэпирования вируса. nsP2 имеет размер около 90 кДа и может обладать хеликазной и протеазной активностью, в то время как nsP3 имеет размер около 60 кДа и содержит три домена: макродомен, центральный (или уникальный для альфавируса) домен и гипервариабельный домен (HVD). nsP4 имеет размер около 70 кДа и содержит основной каталитический домен РНК-зависимой РНК-полимеразы (RdRp). После инфицирования геномная РНК альфавируса транслируется с образованием полипротеина Р1234, который расщепляется на отдельные белки.
Геномы альфавирусов также кодируют три структурных белка: основной нуклеокапсидный белок С и оболочечные белки Р62 и Е1, которые связываются в виде гетеродимера. Структурные белки находятся под контролем субгеномного промотора и могут быть заменены представляющим интерес геном (GIO).
В некоторых вариантах осуществления самореплицирующаяся молекула РНК не кодирует функциональный вирусный структурный белок.
В некоторых вариантах осуществления настоящего изобретения в самореплицирующейся РНК может отсутствовать (или не содержаться) последовательность(-и) по меньшей мере одного (или всех) структурных белков вируса (например, нуклеокапсидного белка С и оболочечных белков Р62, 6К и Е1). В этих вариантах осуществления последовательности, кодирующие один или более структурных генов, могут быть заменены одной или более последовательностями, такими как, например, кодирующая последовательность по меньшей мере одного белка или пептида (или другого представляющего интерес гена), такого как полипептиды неоантигенов множественной миеломы в соответствии с настоящим описанием.
В некоторых вариантах осуществления в самореплицирующейся РНК отсутствуют последовательности, кодирующие структурные белки альфавируса; или не кодируют (или, необязательно, любые другие) структурные белки альфавируса. В некоторых вариантах осуществления самореплицирующиеся молекулы РНК дополнительно лишены части или всей кодирующей области одного или нескольких структурных белков вируса. Например, в системе экспрессии альфавируса может отсутствовать часть или вся кодирующая последовательность для одного или нескольких белков вирусного капсида С, гликопротеина E1; гликопротеина Е2, белка Е3 и белка 6К.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК не содержит кодирующих последовательностей по меньшей мере одного из структурных белков вируса. В этих случаях последовательности, кодирующие структурные гены, могут быть заменены одной или несколькими последовательностями, такими как, например, кодирующая последовательность для полинуклеотидов неоантигенов множественной миеломы в соответствии с настоящим описанием.
В изобретении также предусмотрена самореплицирующаяся молекула РНК, содержащая неструктурные гены nsP1, nsP2, nsP3 и nsP4, при этом самореплицирующаяся молекула РНК не кодирует функциональный вирусный структурный белок.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК может включать один или более неструктурных вирусных белков. В определенных вариантах осуществления один или более неструктурных вирусных белков получают из того же вируса. В других вариантах осуществления один или более неструктурных белков получают из различных вирусов.
В некоторых вариантах осуществления в настоящем изобретении предусмотрена самореплицирующаяся молекула РНК, содержащая последовательность, кодирующую по меньшей мере один, по меньшей мере два, по меньшей мере три или по меньшей мере четыре неструктурных вирусных белка (например, nsP1, nsP2, nsP3, nsP4). Белки nsP1, nsP2, nsP3 и nsP4, кодируемые репликоном, являются функциональными или биологически активными белками.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит последовательность, кодирующую часть по меньшей мере одного неструктурного вирусного белка. Например, самореплицирующиеся молекулы РНК могут включать около 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 100% или диапазон между любыми двумя из этих значений кодирующей последовательности для по меньшей мере одного неструктурного вирусного белка. В некоторых вариантах осуществления самореплицирующаяся молекула РНК может включать последовательность, кодирующую значительную часть по меньшей мере одного неструктурного вирусного белка. Используемый в данном документе термин «существенная часть» последовательности нуклеиновой кислоты, кодирующей неструктурный вирусный белок, содержит достаточное количество последовательности нуклеиновой кислоты, кодирующей неструктурный вирусный белок, чтобы обеспечить предполагаемую идентификацию этого белка либо путем ручной оценки последовательности специалистом в данной области техники или компьютерным автоматическим сравнением и идентификацией последовательностей с использованием таких алгоритмов, как BLAST (см., например, в «Basic Local Alignment Search Tool»; Altschul S F et al., J. Mol. Biol. 215:403-410, 1993).
В некоторых вариантах осуществления самореплицирующаяся молекула РНК может включать всю кодирующую последовательность для по меньшей мере одного неструктурного белка. В некоторых вариантах осуществления самореплицирующаяся молекула РНК включает по существу всю кодирующую последовательность для нативных вирусных неструктурных белков.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит последовательности nsP1, nsP2, nsP3 и nsP4, полученные из венесуэльского вируса энцефалита лошадей (VEEV), и мотив DLP, полученный из вируса Синдбис (SIN).
В некоторых вариантах осуществления самореплицирующиеся молекулы РНК также имеют субпоследовательность РНК, кодирующую аминокислотную последовательность, полученную из макродомена альфавируса nsP3, и субпоследовательность РНК, кодирующую аминокислотную последовательность, полученную из центрального домена альфавируса nsP3. В различных вариантах осуществления макро- и центральный домен(-ы) могут быть получены из альфавируса дикого типа nsP3 Нового Света или могут быть получены из белка альфавируса nsP3 дикого типа Старого Света. В других вариантах осуществления макродомен может быть получен из макродомена альфавируса дикого типа Нового Света и центральный домен может быть получен из центрального домена альфавируса дикого типа Старого Света или наоборот. Различные домены могут иметь любую последовательность, описанную в данном документе. Самореплицирующиеся молекулы РНК также могут иметь субпоследовательность РНК, кодирующую аминокислотную последовательность, которая полностью получена из гипервариабельного домена альфавируса nsP3 Старого Света; или могут иметь аминокислотную последовательность, имеющую часть, полученную из гипервариабельного домена альфавируса nsP3 Нового Света, и часть, полученную из гипервариабельного домена альфавируса nsP3 Старого Света, т.е. гипервариабельный домен (HVD) может представлять собой гибридную или химерную последовательность Нового Света/Старого Света.
В некоторых вариантах осуществления самореплицирующиеся молекулы РНК могут иметь последовательность РНК; кодирующую аминокислотные последовательности, полученные из белковых последовательностей nsP1, nsP2, nsP3 и nsP4 альфавируса дикого типа Нового Света.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит неструктурные белки VEEV nsP1, nsP2, nsP3 и nsP4.
Накопленные экспериментальные данные продемонстрировали, что репликация/амплификация VEEV и других геномов альфавируса и их дефектная интерферирующая (DI) РНК определяются тремя промоторными элементами: (i) консервативный элемент 3'-концевой последовательности (3' CSE) и следующий поли(А)-хвост; (ii) 5'-UTR, которая функционирует как ключевой промотор для синтеза РНК как с отрицательной, так и с положительной цепью; и (iii) элемент из 51 нуклеотида консервативной последовательности (51-nt CSE), который расположен в последовательности, кодирующей nsP1, и функционирует как энхансер репликации генома альфавируса (Kim et al., PNAS, 2014, 111: 10708-10713.).
5'- и 3'-нетранслируемые области могут быть функционально связаны с любой другой последовательностью, кодируемой репликоном. UTR могут быть функционально связаны с промотором и/или последовательностью, кодирующей белок или пептид, путем предоставления последовательностей и интервалов, необходимых для распознавания и транскрипции других кодируемых последовательностей.
Любая из описанных выше самореплицирующихся молекул РНК может дополнительно включать немодифицированную 5'-нетранслируемую область (5'UTR).
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит модифицированную 5'-нетранслируемую область (5'-UTR). Например, модифицированная 5'-UTR может содержать одну или несколько нуклеотидных замен в положениях 1, 2, 4 или их комбинацию.
Предпочтительно модифицированная 5'-UTR содержит нуклеотидную замену в положении 2, более предпочтительно модифицированная 5'-UTR имеет замену U->G в положении 2. Примеры таких самореплицирующихся молекул РНК описаны в публикации заявки на патент США 2018/0104359 и публикации международной заявки на патент WO 2018075235, содержание которых полностью включено в данный документ посредством ссылки.
В некоторых вариантах осуществления UTR могут представлять собой последовательности UTR альфавируса дикого типа Нового Света или Старого Света или последовательность, полученную из любой из них. 5'-UTR может иметь любую подходящую длину, например около 60 нуклеотидов, или 50-70 нуклеотидов, или 40-80 нуклеотидов. В некоторых вариантах осуществления 5'-UTR также может иметь консервативные первичные или вторичные структуры (например, одну или несколько структур петля-на-стебле) и может участвовать в репликации альфавируса или репликона РНК. 3'-UTR может составлять до нескольких сотен нуклеотидов, например, это может быть 50-900, или 100-900, или 50-800, или 100-700, или 200-700 нуклеотидов. '3-UTR также может иметь вторичные структуры, например, ступенчатая петля, за которой может следовать полиаденилатный путь или поли-А-хвост.
В некоторых вариантах осуществления самореплицирующиеся молекулы РНК могут иметь 3'-поли-А-хвост. Он также может включать последовательность распознавания поли-А-полимеразы (например, AAUAAA) вблизи своего 3'-конца.
В тех случаях, когда самореплицирующаяся молекула РНК должна быть упакована в рекомбинантную альфавирусную частицу, она может содержать одну или несколько последовательностей, так называемых сигналов упаковки, которые служат для инициации взаимодействий со структурными белками альфавируса, что приводит к образованию частиц. В некоторых вариантах осуществления альфавирусные частицы содержат РНК, полученную из одного или нескольких альфавирусов; и структурные белки, где по меньшей мере один из указанных структурных белков получен из двух или более альфавирусов.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК содержит вектор, полученный из VEEV, в котором структурные вирусные белки (например, нуклеокапсидный белок С и оболочечные белки Р62, 6К и Е1) удалены и заменены кодирующей последовательностью полинуклеотидов неоантигенов множественной миеломы в соответствии с настоящим описанием.
Предыдущие исследования показали, что во время инфекций, вызванных вирусами VEEV и Синдбис, только небольшая часть вирусных неструктурных белков (nsPs) локализуется совместно с промежуточными продуктами репликации dsRNA. Таким образом, оказывается, что большая часть nsP не участвует в репликации РНК (Gorchakov R, et al. (2008) A new role for ns polyprotein cleavage in Sindbis virus replication. J Virol 82(13):6218-6231). Это дало возможность использовать недостаточно используемые ns-белки для амплификации субгеномных РНК, кодирующих представляющие интерес белки, которые обычно транскрибируются из субгеномного промотора и далее не амплифицируются.
В некоторых вариантах осуществления фрагмент nsP1 самореплицирующейся молекулы РНК по настоящему изобретению дуплицируется ниже 5'-UTR и выше DLP. В некоторых вариантах осуществления первые 193 нуклеотида nsP1 дунлицированы ниже 5'-UTRH выше DLP.
Другие вирусные векторы и рекомбинантные вирусы
Вирусный вектор, содержащий полинуклеотид в соответствии с настоящим описанием, может быть получен из других вирусных векторов, включая векторы, полученные из человеческих аденоассоциированных вирусов, таких как AAV-2 (аденоассоциированный вирус типа 2). Привлекательной особенностью AAV векторов является то, что они не экспрессируют каких-либо вирусных генов. Единственными вирусными последовательностями ДНК, включенными в AAV векторы, являются инвертированные концевые повторы (ITR) длиной 145 п.н. Таким образом, как и при иммунизации депротеинизированной ДНК, единственным экспрессируемым геном является ген антигена или химерного антигена. Кроме того, известно, что AAV векторы трансдуцируют как делящиеся, так и не делящиеся клетки, такие как дендритные клетки, полученные из моноцитов периферической крови человека, со стойкой экспрессией трансгена, а также с возможностью перорального и интраназального введения для создания иммунитета слизистых оболочек. Более того, количество необходимой ДНК оказывается гораздо меньше на несколько порядков с максимальными ответами при дозах от 1010 до 1011 частиц или копий ДНК в отличие от доз в 50 мкг или около 1015 копий депротеинизированной ДНК. AAV векторы упаковывают путем совместной трансфекции подходящей клеточной линии (например, человеческие клетки 293) ДНК, содержащейся в конструктах, кодирующих химерный белок AAV ITR, и хелперной плазмиды AAV ACG2, содержащей кодирующую область AAV (гены AAV rep и cap) без ITR. Затем клетки инфицируют аденовирусом Ad5. Векторы могут быть очищены от клеточных лизатов с помощью способов, известных в данной области (например, такого как ультрацентрифугирование в градиенте плотности хлористого цезия), и проверены на отсутствие выявляемых репликационно-компетентных AAV или аденовирусов (например, с помощью биоанализа цитопатического эффекта).
Также можно применять ретровирусные векторы. Ретровирусы представляют собой класс интегративных вирусов, которые реплицируются с использованием кодируемой вирусом обратной транскриптазы для репликации вирусного РНК-генома в двухцепочечную ДНК, интегрированную в хромосомную ДНК инфицированных клеток (например, клетки-мишени). Такие векторы включают векторы, полученные из вирусов мышиного лейкоза, особенно Moloney (Gilboa, et al., 1988, Adv. Exp.Med. Biol. 241: 29) или штаммы Friend FB29 (международная патентная публикация № WO 1995/01447). Как правило, ретровирусный вектор лишен всех или части вирусных генов gag, pol и env и сохраняет 5' и 3' LTR и последовательность капсидирования. Эти элементы могут быть модифицированы для повышения уровня экспрессии или стабильности ретро вирусного вектора. Такие модификации включают замену ретровирусной последовательности капсидирования одним из ретротранспозонов, таких как VL30 (см., например, патент США№5,747,323). Полинуклеотиды в соответствии с настоящим описанием могут быть вставлены ближе к 3 '-концу от последовательности капсидирования, например, в противоположном направлении относительно ретровирусного генома. Ретровирусные частицы получают в присутствии вируса хелпера или в соответствующей дополнительной (упаковочной) клеточной линии, которая содержит интегрированные в ее геном ретровирусные гены, для которых ретровирусный вектор является дефектным (например, gag/pol и env). Такие клеточные линии описаны в известном уровне техники (Miller and Rosman, 1989, BioTechniques 7: 980: Danos and Mulligan, 1988, Proc. Natl. Acad. Sci. USA 85: 6460: Marowitz, et al., 1988, Virol. 167: 400). Продукт гена env отвечает за связывание вирусной частицы с вирусными рецепторами, присутствующими на поверхности клетки-мишени, и, таким образом, определяет диапазон хозяев ретровирусной частицы. Таким образом, упаковочную линию клеток, такую как клетки РА317 (АТСС CRL 9078) или 293EI6 (WO 97/35996), содержащие амфотропный белок оболочки, можно использовать для инфицирования человеческих и других видов клеток-мишеней. Ретровирусные частицы выделяют из супернатанта культуры и могут необязательно дополнительно очищать в соответствии со стандартными методиками (например, хроматография, ультрацентрифугирование).
Регуляторные элементы
Полинуклеотид или гетерологичный полинуклеотид в соответствии с настоящим описанием может быть функционально связан с одним или более регуляторными элементами в векторе. Регуляторные элементы могут содержать промоторы, энхансеры, сигналы полиаденилирования, репрессоры и т.п. Используемый в данном документе термин «функционально связанный» следует понимать в его самом широком приемлемом контексте и он относится к соединению полинуклеотидных элементов в функциональной взаимосвязи. Полинуклеотид является «функционально связанным», когда он находится в функциональной взаимосвязи с другим полинуклеотидом. Например, промотор функционально связан с кодирующей последовательностью, если он влияет на транскрипцию кодирующей последовательности.
Некоторые из широко используемых энхансерных и промоторных последовательностей в экспрессионных векторах и вирусных векторах представляют собой, например, промоторы человеческого цитомегаловируса (hCMV), ранний/поздний промотор осповакцины Р7.5, CAG, SV40, мышиного CMV (mCMV), EF-1 и hPGK. Благодаря своей высокой эффективности и умеренному размеру приблизительно 0,8 т.п.н. промотор hCMV представляет собой один из наиболее часто используемых промоторов. Промотор hPGK характеризуется малым размером (прибл. 0,4 т.п.н.), но он менее эффективен, чем промотор hCMV. С другой стороны, промотор CAG, состоящий из элемента раннего энхансера цитомегаловируса, промотора, первого экзона и интрона гена бета-актина курицы и акцептора сплайсинга гена бета-глобулина кролика, может направлять очень сильную экспрессию гена, сопоставимую с промотором hCMV, но его большой размер делает его менее подходящим для вирусных векторов, где ограничения пространства могут быть важными проблемами, например, для аденовирусных векторов (AdV), аденоассоциированных вирусных векторов (AAV) или лентивирусных векторов (LV).
Дополнительными промоторами, которые могут быть использовны, являются основной немедленно-ранний промотор Aotine Herpesvirus 1 (промотор AoHV-1), описанный в международной патентной публикации № WO 2018/146205. Промотор может быть функционально связан с последовательностью репрессорного оператора, с которой может связываться репрессорный белок, чтобы подавлять экспрессию промотора в присутствии репрессорного белка. В некоторых вариантах осуществления последовательность репрессорного оператора представляет собой последовательность TetO или последовательность CuO (см., например, US 9790256).
В некоторых случаях может быть желательно экспрессировать по меньшей мере два отдельных полипептида из одного вектора. В данном случае каждый полинуклеотид может быть функционально связан с одной и той же или разными промоторными и/или энхансерными последовательностями, или можно использовать хорошо известные бицистронные экспрессионные системы, например, с использованием внутреннего сайта посадки рибосом (IRES) из вируса энцефаломиокардита. Альтернативно можно использовать двунаправленные синтетические промоторы, такие как промотор hCMV-rhCMV и другие промоторы, описанные в международной патентной публикации № WO 2017/220499.
Сигналы полиаденилирования могут быть получены из SV40 или бычьего гормона роста (BGH).
Полинуклеотид или гетерологичный полинуклеотид векторов самореплицирующейся РНК в соответствии с настоящим описанием может быть функционально связан с одним или более регуляторными элементами в векторе. Векторы самореплицирующейся РНК, содержащие полинуклеотид, кодирующий полипептид по настоящему изобретению, могут дополнительно содержать любые регуляторные элементы для установления обычной(-ых) функции(-й) вектора, включая, но не ограничиваясь этим, репликацию и экспрессию полипептида по настоящему изобретению, кодируемого полинуклеотидной последовательностью вектора. Регуляторные элементы включают, но не ограничиваются ими, промотор, энхансер, сигнал полиаденилирования, стоп-кодон трансляции, элемент связывания рибосомы, терминатор транскрипции, маркеры селекции, начало репликации и т.д. Вектор может содержать один или несколько кассет экспрессии. «Кассета экспрессии» является частью вектора, который управляет клеточным механизмом для получения РНК и белка. Кассета экспрессии обычно содержит три компонента: промоторную последовательность, открытую рамку считывания и 3'-нетранслируемую область (UTR), необязательно содержащую сигнал полиаденилирования. Открытая рамка считывания (ORF) представляет собой рамку считывания, которая содержит кодирующую последовательность представляющего интерес белка (например, полипептидов по настоящему изобретению) от стартового кодона до стоп-кодона. Регуляторные элементы кассеты экспрессии могут быть функционально связаны с полинуклеотидной последовательностью, кодирующей представляющие интерес полипептиды. Любые компоненты, подходящие для использования в описанной в данном документе кассете экспрессии, можно использовать в любой комбинации и в любом порядке для получения векторов применения.
Вектор может содержать промоторную последовательность, предпочтительно в кассете экспрессии, для контроля экспрессии полипептидов согласно настоящему изобретению.
В самореплицирующейся РНК вектор может дополнительно содержать дополнительные полинуклеотидные последовательности, которые стабилизируют экспрессируемый транскрипт, усиливают ядерный экспорт транскрипта РНК и/или улучшают транскрипционно-трансляционное сочетание. Примеры таких последовательностей включают сигналы полиаденилирования и энхансерные последовательности. Сигнал полиаденилирования обычно расположен ниже кодирующей последовательности представляющего интерес белка (например, полипептидов по настоящему изобретению) в кассете экспрессии вектора. Энхансерные последовательности представляют собой регуляторные последовательности ДНК, которые при связывании с факторами транскрипции усиливают транскрипцию ассоциированного гена. Энхансерная последовательность предпочтительно расположена выше последовательности полинуклеотидов, кодирующей полипептиды по настоящему изобретению, но ниже последовательности промотора внутри кассеты экспрессии вектора.
Можно использовать любую энхансерную последовательность, известную специалистам в данной области техники в связи с настоящим изобретением.
Любой из компонентов или последовательностей самореплицирующегося вектора РНК по настоящему изобретению может быть функционально связан с любыми другими компонентами или последовательностями.
Промотор или UTR, функционально связанные с кодирующей последовательностью, способны влиять на транскрипцию и экспрессию кодирующей последовательности, когда присутствуют соответствующие ферменты. Промотор не обязательно должен быть смежным с кодирующей последовательностью, пока он функционирует, чтобы направлять ее экспрессию. Таким образом, функциональная связь между последовательностью РНК, кодирующей белок или пептид, и регуляторной последовательностью (например, промотором или UTR) представляет собой функциональную связь, которая обеспечивает экспрессию представляющего интерес полинуклеотида. «Функционально связанные» могут также относиться к последовательностям, таким как последовательности, кодирующие RdRp (например, nsP4), nsP1-4, UTR, промоторы и другие последовательности, кодирующие репликон РНК, которые связаны таким образом, что они обеспечивают транскрипцию и трансляцию полипептида и/или репликацию репликона. UTR могут быть функционально связаны путем предоставления последовательностей и интервалов, необходимых для распознавания и трансляции рибосомой других кодируемых последовательностей.
Молекула является функциональной или биологически активной, если она проявляет по меньшей мере 50% той же активности, что и ее природная (или дикого типа) соответствующая молекула, но функциональная молекула также может проявлять по меньшей мере 60%, или по меньшей мере 70%, или по меньшей мере 90%, или по меньшей мере 95%, или 100% той же активности, что и у ее природной (или дикого типа) соответствующей молекулы. Самореплицирующиеся молекулы РНК также могут кодировать аминокислотную последовательность, полученную из аминокислотной последовательности альфавируса дикого типа или основанную на ней, что означает, что они имеют по меньшей мере 60%, или по меньшей мере 65%, или по меньшей мере 68%, или по меньшей мере 70%, или по меньшей мере 80%, или по меньшей мере 70%, или по меньшей мере 80%, или по меньшей мере 90%, или по меньшей мере 95%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100%, или 80-99%, или 90-100%, или 95-99%, или 95-100%, или 97-99%, или 98-99% идентичность последовательности с аминокислотной последовательностью (которая может быть соответствующей последовательностью), кодируемой геномом РНК альфавируса дикого типа, который может быть геномом альфавируса Нового Света или Старого Света. Последовательности, полученные из других последовательностей, могут быть до 5%, или до 10%, или до 20%, или до 30% длиннее или короче исходной последовательности. В любом из вариантов осуществления идентичность последовательности может составлять по меньшей мере 95%, или по меньшей мере 97%, или по меньшей мере 98%, или по меньшей мере 99%, или 100% для любой нуклеотидной последовательности, кодирующей (или содержащей аминокислотную последовательность) сайт связывания G3BP или FXR на ней. Эти последовательности также могут быть до 5%, или до 10%, или до 20%, или до 30% длиннее или короче исходной последовательности.
Клетки в соответствии с настоящим описанием
В настоящем описании также предложена клетка, содержащая или трансдуцированная одним или более векторами в соответствии с настоящим описанием или одним или более рекомбинантными вирусами в соответствии с настоящим описанием.
Подходящие клетки включают прокариотические и эукариотические клетки, например клетки млекопитающих, дрожжи, грибы и бактерии (такие как Е. coli), такие как Hek293, СНО, PER.C6 или эмбриональные фибробласты курицы (CEF). Клетка может быть использована in vitro, например, для исследований или для получения полипептидов или вирусов, или клетка может быть использована in vivo. В некоторых вариантах осуществления клетка представляет собой мышечную клетку. В некоторых вариантах осуществления клетка представляет собой антигенпредставляющую клетку (АПК). Подходящие антигенпредставляющие клетки включают дендритные клетки, В-лимфоциты, моноциты и макрофаги.
Клетки, трансфицированные полинуклеотидами или векторами в соответствии с настоящим описанием, как правило, могут быть получены из хранилищ клеточных культур, таких как АТСС. АПК могут быть получены из периферической крови при помощи лейкафереза и центрифугирования в градиенте плотности «FICOLL/HYPAQUE» (поэтапное центрифугирование при помощи Ficoll и дисперсных градиентов плотности Percoll). АПК могут быть выделены, культивированы и сконструированы с использованием известных способов. Например, незрелые и зрелые дендритные клетки можно получить из мононуклеарных клеток периферической крови (РВМС) с использованием известных способов. В примере способа выделенные РВМС предварительно обрабатывают для истощения Т- и В-клеток с помощью иммуномагнитной методики. Обедненные лимфоцитами РВМС затем культивируют в среде RPMI 9 например, приблизительно 7 дней) с добавлением человеческой плазмы (предпочтительно аутологичной плазмы) и GM-CSF/IL-4 с получением дендритных клеток. Дендритные клетки являются неадгезивными по сравнению с их моноцитарными клетками-предшественниками. Таким образом, примерно на 7 день неприкрепившиеся клетки собираются для дальнейшей обработки. Дендритные клетки, полученные из ПКМК в присутствии GM-CSF и IL-4, являются незрелыми, поскольку они могут утратить неадгезивное свойство и вернуться к судьбе макрофагов клеток при удалении стимулов цитокинов из культуры. Дендритные клетки в незрелом состоянии эффективны в процесинге нативных белковых антигенов для ограниченного пути МНС класса II (Romani, et al., J. Exp. Med. 169: 1169, 1989). Дальнейшее созревание культивированных дендритных клеток достигается путем культивирования в течение 3 дней в кондиционированной макрофагами среде (СМ), которая содержит необходимые факторы созревания. Зрелые дендритные клетки менее способны захватывать новые белки для представления, но гораздо лучше стимулируют рост и дифференциацию покоящихся Т-клеток (как CD4, так и CD8). Зрелые дендритные клетки могут быть выявлены по их изменению морфологии, такому как образование более подвижных цитоплазматических отростков; благодаря отсутствию их адгезии; благодаря присутствию по крайней мере одного из последующих маркеров: CD83, CD68, HLA-DR или CD86; или в результате потери Fc-рецепторов, таких как CD115 (обзор в публикации Steinman, Annu. Rev. hnmunol. 9: 271, 1991). Зрелые дендритные клетки могут быть собраны и проанализированы с использованием типичных методов и приборов цитофлюорографии и сортировки клеток, таких как FACScan и FACStar. Первичные антитела, используемые для проточной цитометрии, являются специфичными к антигенам клеточной поверхности зрелых дендритных клеток и доступны в продаже. Вторичные антитела могут представлять собой биотинилированные Ig с последующим добавлением стрептавидина, конъюгированного с FITC или РЕ. Векторы и рекомбинантные вирусы в соответствии с настоящим описанием можно вводить в клетки, включая АПК, с использованием способов, известных в данной области, включая, без ограничений, трансфекцию, электропорацию, слияние, микроинъекцию, доставку на основе вируса или доставку на основе клеток.
Вакцины и фармацевтические композиции в соответствии с настоящим описанием
В изобретении также предусмотрены композиции, содержащие любой из полинуклеотидов, любой из полипептидов и любой из векторов, описанных в данном документе. В некоторых вариантах осуществления композиции могут содержать вектор, содержащий любой из нуклеотидов, раскрытых в данном документе, причем вектор выбран из Ad26, GAd20, MVA или самореплицирующейся молекулы РНК. В некоторых вариантах осуществления композиции могут содержать рекомбинантный вирус или самореплицирующуюся молекулу РНК, экспрессирующую любой из полипептидов или неоантигенов, описанных в данном документе. В некоторых вариантах осуществления рекомбинантный вирус может представлять собой вирус Ad26, вирус GAd20 или вирус MVA.
Любая из описанных выше композиций может включать или может быть включена в состав фармацевтической композиции, содержащей композицию и фармацевтически приемлемое вспомогательное вещество.
Полипептиды или гетерологичные полипептиды, или их фрагменты, или кодирующие их полинуклеотиды могут быть доставлены субъекту с использованием любого известного средства доставки, подходящего для введения субъекту. Ожидается, что полипептиды, гетерологичные полипептиды или их фрагменты будут иммуногенными у субъекта независимо от используемого средства доставки. Полинуклеотид может представлять собой ДНК, или РНК, или их производные. РНК может быть представлена в виде олигонуклеотидной РНК, тРНК (транспортной РНК), мяРНК (малой ядерной РНК), рРНК (рибосомальной РНК), мРНК (матричной РНК), антисмысловой РНК, миРНК (малая интерферирующая РНК), самореплицирующейся РНК, рибозимов, химерных последовательностей или производных этих групп.
В настоящем описании также предложена вакцина, содержащая полинуклеотид в соответствии с настоящим описанием.
В некоторых вариантах осуществления полинуклеотид представляет собой ДНК.
В некоторых вариантах осуществления полинуклеотид представляет собой РНК.
В некоторых вариантах осуществления РНК представляет собой мРНК.
В настоящем описании также предложена вакцина, содержащая вектор в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая rAd26 в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая rMVA в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая rGAd в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая rGAd20 в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая ChAd20 в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая самореплицирующуюся молекулу РНК в соответствии с настоящим описанием.
В настоящем описании также предложена вакцина, содержащая клетку в соответствии с настоящим описанием.
Получение вакцинных композиций хорошо известно. Вакцины могут содержать или могут входить в состав фармацевтической композиции, содержащей вакцину и фармацевтически приемлемый эксципиент.
«Фармацевтически приемлемый» относится к вспомогательному веществу, которое в применяемых дозировках и концентрациях не вызывает нежелательных или вредных эффектов у субъектов, которым его вводят, и включает носитель, буферы, стабилизаторы или другие материалы, хорошо известные специалистам в данной области техники. Определенные свойства носителя или другого материала могут зависеть от пути введения, например, внутримышечным, подкожным, пероральным, внутривенным, кожным, интрамукозальным (например, в слизистую кишечника), интраназальным или внутрибрюшинным путем. Могут быть включены жидкие носители, такие как вода, керосин, животные или растительные масла, минеральное масло или синтетическое масло. Также могут быть включены физиологический солевой раствор, раствор декстрозы или другого сахарида, или гликоли, такие как этиленгликоль, пропиленгликоль или полиэтиленгликоль. В качестве примера вирусного состава представлен мировой стандарт аденовируса (Hoganson et al, 2002): 20 мМ трис рН 8, 25 мМ NaCl, 2.5% глицерина; или 20 мМ трис, 2 мМ MgCl2, 25 мМ NaCl, сахарозы 10% масс./об., полисорбата-80 0,02% масс./об.; или 10-25 мМ цитратного буфера с рН 5,9-6,2, 4-6% (масс./масс.) гидроксипропил-бета-циклодекстрина (HBCD), 70-100 мМ NaCl, 0,018-0,035% (масс./масс.) полисорбата-80 и необязательно 0,3-0,45% (масс./масс.) этанола. Можно использовать множество других буферных растворов, и известны примеры подходящих составов для хранения и фармацевтического введения очищенных фармацевтических препаратов.
Адъюванты
Вакцина или фармацевтическая композиция может содержать один или несколько адъювантов. Примеры таких адъювантов включают, но не ограничиваются ими, неорганические адъюванты (например, неорганические соли металлов, такие как фосфат алюминия или гидроксид алюминия), органические адъюванты (например, сапонины или сквален), адъюванты на масляной основе (например, полный адъювант Фрейнда и неполный адъювант Фрейнда), липосомы или биоразлагаемые микросферы), виросомы, бактериальные адъюванты (например, монофосфориллипид А или мурамиловые пептиды), синтетические адъюванты (например, неионогенные блок-сополимеры, аналоги мурамиловых пептидов или синтетический липид А) или синтетические полинуклеотидные адъюванты (например, полиаргинин или полилизин). Приемлемые адъюванты включают QS-21, Detox-PC, MPL- SE, MoGM-CSF, TiterMax-G, CRL-1005, GERBU, TERamide, PSC97B, Adjumer, PG-026, GSK-I, GcMAF, B-alethine, MPC-026, Adjuvax, CpG ODN, Betafectm, Alum и MF59. Другие адъюванты, которые можно использовать, включают лектины, факторы роста, цитокины и лимфокины, такие как альфа-интерферон, гамма-интерферон, тромбоцитарный фактор роста (PDGF), гранулоцитарно-колониестимулирующий фактор (gCSF), гранулоцитарно-макрофагальный колониестимулирующий фактор (gMCSF), фактор некроза опухоли (TNF), эпидермальный фактор роста (EGF), IL-1, IL-2, IL-4, IL-6, IL-8, IL-10, IL-12 или агонисты TLR.
Термины «адъювант» и «иммуностимулятор» используются в данном документе взаимозаменяемо и определяются как одно или более веществ, вызывающих стимуляцию иммунной системы. В данном контексте адъювант используется для усиления иммунного ответа на вакцины или вирусные векторы, описанные в настоящем документе.
В определенных вариантах осуществления фармацевтическая композиция в соответствии с настоящим изобретением может представлять собой вакцину в соответствии с настоящим описанием.
Аналогичным образом, полинуклеотиды, гетерологичные полинуклеотиды, полипептиды и гетерологичные полипептиды в соответствии с настоящим описанием могут быть приготовлены в виде фармацевтических композиций, содержащих полинуклеотиды, гетерологичные полинуклеотиды, полипептиды и гетерологичные полипептиды, а также фармацевтически приемлемые эксципиенты.
В некоторых вариантах осуществления фармацевтические композиции не содержат адъювантов.
Нано частицы
В некоторых вариантах осуществления композиции могут содержать наночастицы. Любой из полипептидов или гетерологичных полипептидов или их фрагментов, кодирующих их полинуклеотидов или векторов, содержащих полинуклеотиды в соответствии с настоящим описанием, может быть присоединен к наночастицам или контактировать с ними для доставки субъекту. Доставка полипептидов или гетерологичных полипептидов или их фрагментов, кодирующих их полинуклеотидов или векторов, содержащих полинуклеотиды, с использованием наночастиц может устранить необходимость включения вируса или адъюванта в состав композиции вакцины. Наночастицы могут содержать сигналы иммунной опасности, которые способствуют эффективной индукции иммунного ответа на пептиды. Наночастицы могут индуцировать активацию и созревание дендритных клеток (DC), необходимых для устойчивого иммунного ответа. Наночастицы могут содержать не собственные компоненты, которые улучшают поглощение наночастиц и, следовательно, пептидов клетками, такими как антигенпрезентирующие клетки.
Диаметр наночастиц обычно составляет от около 1 нм до около 100 нм, например от около 20 нм до около 40 нм. Наночастицы со средним диаметром от 20 до 40 нм могут облегчать поглощение наночастицы цитозолем (см., например, WO 2019/135086). Примерами наночастиц являются полимерные наночастицы, неорганические наночастицы, липосомы, липидные наночастицы (LNP), иммунностимулирующий комплекс (ISCOM), вирусоподобные частицы (VLP) или самособирающийся белок.
Наночастицы могут представлять собой наночастицы фосфата кальция, наночастицы кремния или наночастицы золота. Полимерные наночастицы могут содержать один или более синтетических полимеров, таких как поли(d,l-лактида-ко-гликолид) (PLG), поли(d,l-лактид-ко-гликолевая кислота) (PLGA), поли(G-глутаминовая кислота) (g-PGA)m поли(этиленгликоль) (PEG), или полистирол, или один или более природных полимеров, таких как полисахарид, например пуллулан, альгинат, инулин и хитозан. Применение полимерных наночастиц может быть выгодным благодаря свойствам полимеров, которые могут быть включены в наночастицу. Например, перечисленные выше натуральные и синтетические полимеры могут обладать хорошей биосовместимостью и биоразлагаемостью, нетоксичностью и/или способностью к переработке с получением желаемых форм и размеров. Полимерная наночастица может также образовывать гидрогелевые наночастицы, гидрофильные трехмерные полимерные сети с благоприятными свойствами, включая гибкий размер ячейки, большую площадь поверхности для мультивалентной конъюгации, высокое содержание воды и высокую сорбционную емкость для антигенов. Полимеры, такие как поли-L-молочная кислота (PLA), PLGA, PEG, и полисахариды подходят для формирования гидрогелевых наночастиц. Неорганические наночастицы, как правило, имеют жесткую структуру и содержат оболочку, в которой инкапсулирован антиген, или ядро, к которому может быть ковалентно присоединен антиген. Ядро может содержать один или более атомов, таких как золото (Au), серебро (Ag), атомы меди (Cu), Au/Ag, Au/Cu, Au/Ag/Cu, Au/Pt, Au/Pd или Au/Ag/Cu/Pd или фосфат кальция (СаР).
В некоторых вариантах осуществления наночастицы могут быть липосомами Липосомы, как правило, образуются из биоразлагаемых нетоксичных фосфолипидов и содержат самособирающуюся фосфолипидную бислойную оболочку с водным ядром. Липосомы могут представлять собой однослойную везикулу, содержащую один фосфолипидный бислой, или многослойную везикулу, содержащую несколько концентрических фосфолипидных оболочек, разделенных слоями воды. Как следствие, липосомы можно оптимизировать для включения либо гидрофильных молекул в водное ядро, либо гидрофобных молекул в фосфолипидные бислой. Липосомы могут инкапсулировать полинуклеотиды или полипептиды или их фрагменты согласно настоящему изобретению внутри ядра для доставки. Липосомы и липосомные составы можно приготовить стандартными способами и хорошо известными в данной области, см., например. Remington's; Akimani, 1995, Cytokines Mol. Ther. 1: 197-210; Alving, 1995, Immunol. Rev. 145: 5-31; Szoka, 1980, Ann. Rev. Biophys. Bioeng. 9: 467: патент США №4,235,871; патент США №4,501,728; и патент США №4,837,028. Липосомы могут содержать нацеливающую молекулу для нацеливания комплексов липосомы на определенный тип клеток. Нацеливающая молекула может содержать партнера по связыванию (например, лиганд или рецептор) для биомолекулы (например, рецептор или лиганд) на поверхности кровеносного сосуда или клетки, обнаруживаемой в ткани-мишени. Заряд липосом является важным фактором, определяющим выведение липосом из крови, при этом отрицательно заряженные липосомы быстрее захватываются ретикулоэндотелиальной системой (Juliano, 1975, Biochem. Biophys. Res. Commun. 63: 651) и, таким образом, имеют более короткий период полужизни в кровотоке. Включение производных фосфатидилэтаноламина увеличивает время циркуляции за счет предотвращения агрегации липосомы. Например, встраивание N-(омега-карбокси)ациламидофосфатидилэтаноламинов в большие однослойные везикулы L-альфа-дистеароилфосфатидилхолина резко увеличивает продолжительность жизни липосомальной циркуляции in vivo (см., например, Ahl, 1997, Biochim. Biophys. Acta 1329: 370-382). Как правило, липосомы получают с содержанием от около 5 до 15 молярных процентов отрицательно заряженных фосфолипидов, таких как фосфатидилглицерин, фосфатидилсерин или фосфатидилинозитол. Добавленные отрицательно заряженные фосфолипиды, такие как фосфатидилглицерин, также служат для предотвращения спонтанной агрегации липосом и, таким образом, сведения к минимуму риска образования недостаточных по размеру липосомальных агрегатов. Упрочняющие мембрану агенты, такие как сфингомиелин или насыщенный нейтральный фосфолипид, в концентрации по меньшей мере около 50 мольных процентов, и от 5 до 15 мольных процентов моносиалилганглиозида также могут придавать желательные липосомные свойства, такие как жесткость (см., например, патент США No 4,837,028). Кроме того, суспензия липосом может содержать липид-защитные агенты, которые защищают липиды от свободнорадикальных и липид-пероксидазных повреждений при хранении. Предпочтительными являются липофильные гасители свободных радикалов, такие как альфа-токоферол, и водорастворимые железоспецифические хелаторы, такие как ферриоксианин.
В некоторых вариантах осуществления наночастицы могут включать мультиламеллярные везикулы разного размера. Например, образующие везикулу липиды можно растворить в подходящем органическом растворителе или системе растворителей и высушить под вакуумом или в инертном газе с образованием тонкой липидной пленки. При желании пленку можно повторно растворить в подходящем растворителе, таком как третичный бутанол, а затем лиофилизировать с образованием более однородной липидной смеси, которая находится в более легко гидратированной порошковой форме. Данную пленку покрывают водным раствором полипептида или полинуклеотида и позволяют ей гидратироваться, как правило, в течение периода времени от 15 до 60 минут, перемешивая.
Распределение по размерам полученных многослойных везикул можно сдвинуть в сторону меньших размеров путем гидратации липидов при более энергичном перемешивании или путем добавления солюбилизирующих детергентов, таких как дезоксихолат. Среда для гидратации может содержать нуклеиновую кислоту в концентрации, необходимой во внутреннем объеме липосом в конечной суспензии липосом. Подходящие липиды, которые можно применять для образования многослойных везикул, включают DOTMA DOGS или Transfectain™, DNERIE или DOME, DC-CHOL, DOTAP™, Lipofectamine™ и глицеролипидные соединения.
В некоторых вариантах осуществления наночастица может представлять собой иммуностимулирующий комплекс (ISCOM). ISCOM представляют собой каркасные частицы, которые обычно образуются из коллоидных сапонин-содержащих мицелл. ISCOM могут содержать холестерин, фосфолипид (такой как фосфатидилэтаноламин или фосфатидилхолин) и сапонин (такой как Quil А из дерева Quillaia saponaria).
В некоторых вариантах осуществления наночастица может представлять собой вирусе подобную частицу (VLP). VLP представляют собой самособирающиеся наночастицы, не содержащие инфекционной нуклеиновой кислоты, которые образуются в результате самосборки биосовместимого капсидного белка. Как правило, диаметр VLP составляет от около 20 до около 150 нм, например от около 20 до около 40 нм, от около 30 до около 140 нм, от около 40 до около 130 нм, от около 50 до около 120 нм, от около 60 до около 110 нм, от около 70 до около 100 нм или от около 80 до около 90 нм. Преимуществом VLP является то, что они используют возможности развитой вирусной структуры, которая естественным образом оптимизирована для взаимодействия с иммунной системой. Оптимизированный естественным образом размер наночастиц и повторяющийся структурный порядок означают, что VLP индуцируют мощные иммунные ответы даже в отсутствие адъюванта.
Инкапсулированные самореплицирующиеся молекулы РНК
Самореплицирующиеся молекулы РНК и/или содержащие их композиции также могут быть составлены в виде наночастиц с использованием комбинации полимеров, липидов и/или других биоразлагаемых средств, таких как, но не ограничиваясь ими, фосфат кальция, полимеры. Компоненты могут быть объединены в ядро-оболочку, гибридную и/или послойную архитектуру, чтобы обеспечить точную настройку наночастиц, чтобы можно было улучшить доставку молекул и/или композиций согласно настоящему изобретению.
Раскрытые самореплицирующиеся молекулы РНК и/или композиции, содержащие самореплицирующиеся молекулы РНК, кодирующие любой из полипептидов по настоящему изобретению, могут быть инкапсулированы с использованием одной или нескольких липосом, липоплексов и/или липидных наночастиц. Липосомы представляют собой искусственно полученные везикулы, которые в основном могут состоять из двойного липидного слоя и могут использоваться в качестве средства доставки для введения полинуклеотидов и самореплицирующихся молекул РНК. Липосомы могут быть разных размеров, например, многослойная везикула (MLV), которая может иметь диаметр в сотни нанометров и может содержать ряд концентрических двойных слоев, разделенных узкими водными отсеками, небольшая одноклеточная везикула (SUV), которая может быть меньше 50 нм в диаметре, и большая однослойная везикула (LUV), которая может иметь диаметр от 50 до 500 нм. Конструкция липосом может включать, но не ограничиваться ими, опсонины или лиганды для улучшения прикрепления липосом к нездоровой ткани или для активации таких явлений, как, но не ограничиваясь ими, эндоцитоз. Липосомы могут иметь низкий или высокий рН для улучшения доставки полинуклеотидов и самореплицирующихся молекул РНК, описанных в данном документе.
Образование липосом может зависеть от физико-химических характеристик, таких как, помимо прочего, захваченная фармацевтическая композиция и липосомальные ингредиенты, характер среды, в которой диспергированы липидные везикулы, эффективная концентрация захваченного вещества и его потенциальная токсичность, любые дополнительные процессы, связанные с применением и/или доставкой везикул, оптимизация размера, полидисперсность и срок годности везикул для предполагаемого применения, а также воспроизводимость от партии к партии и возможность крупномасштабного производства безопасных и эффективных липосомальных продуктов.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК инкапсулирована, связана или адсорбирована на липосоме, липоплексе, липидной наночастице или их комбинациях, предпочтительно, самореплицирующаяся молекула РНК инкапсулирована в липидную наночастицу.
В некоторых вариантах осуществления молекула самореплицирующейся РНК, кодирующая любой из полипептидов по настоящему изобретению, может быть полностью инкапсулирована в липидную часть частицы, тем самым защищая РНК от расщепления нуклеазой. «Полностью инкапсулированная» означает, что РНК существенно не расщепляется после воздействия сыворотки или нуклеазного анализа, который значительно расщепляет свободную РНК. При полной инкапсуляции предпочтительно менее 25% нуклеиновой кислоты в частице подвергается расщеплению при обработке, которая обычно разрушает 100% свободной нуклеиновой кислоты, более предпочтительно менее 10% и наиболее предпочтительно менее 5% нуклеиновой кислоты в частице разрушается. «Полностью инкапсулированный» также означает, что частицы нуклеиновой кислоты-липида не распадаются быстро на составные части при введении in vivo.
В некоторых вариантах осуществления самореплицирующиеся молекулы РНК и/или композиции по настоящему изобретению, содержащие их, могут быть включены в состав липидной везикулы, которая может иметь поперечные связи между функционализированными липидными двойными слоями. В некоторых вариантах осуществления самореплицирующиеся молекулы РНК и/или композиции по настоящему изобретению могут быть включены в состав комплекса липид-поликатион. Образование комплекса липид-поликатион можно осуществить способами, известными в данной области техники. В качестве неограничивающего примера поликатион может включать катионный пептид или полипептид, такой как, но не ограничиваясь ими, полилизин, полиорнитин и/или полиаргинин и катионные пептиды. В некоторых вариантах осуществления самореплицирующиеся молекулы РНК и/или композиции, раскрытые в данном документе, могут быть включены в состав комплекса липид-поликатион, который может дополнительно включать нейтральный липид, такой как, помимо прочего, холестерин или диолеоилфосфатидилэтаноламин (DOPE). На состав липидных наночастиц может влиять, помимо прочего, выбор катионного липидного компонента, степень насыщения катионного липида, природа пегилирования, соотношение всех компонентов и биофизические параметры, такие как размер.
В некоторых вариантах осуществления описанная в данном документе самореплицирующаяся молекула РНК инкапсулирована в липидной наночастице (LNP). Липидные наночастицы обычно содержат четыре различных липида: ионизируемый липид, нейтральный вспомогательный липид, холестерин и диффундирующий липид полиэтиленгликоля (ПЭГ). LNP аналогичны липосомам, но имеют немного отличающиеся функции и состав. LNP разработаны для инкапсулирования полинуклеотидов, таких как ДНК, мРНК, миРНК и кРНК. Традиционные липосомы содержат водное ядро, окруженное одним или более липидными бислоями. LNP могут иметь мицеллообразную структуру, инкапсулируя полинуклеотиды в неводном ядре. LNP, как правило, содержат катионный липид, некатионный липид и липид, который предотвращает агрегацию частицы (например, PEG-липидный конъюгат). LNP подходят для системного применения, поскольку они демонстрируют увеличенную продолжительность жизни циркуляции после внутривенной инъекции и накапливаются в дистальных участках (например, участках, физически отделенных от места введения). LNP могут иметь средний диаметр от около 50 нм до около 150 нм, например от около 60 нм до около 130 нм, или от около 70 нм до около 110 нм, или от около 70 нм до около 90 нм, и являются по существу нетоксичными. Получение загруженных полинуклеотидами LNP описано в патенте США №5,976,567; 5,981,501; 6,534,484; 6,586,410; 6,815,432; патентной публикации № WO 96/40964. Полинуклеотид, содержащий LNP, описан, например, в WO 2019/191780.
В некоторых вариантах осуществления липидные наночастицы содержат катионный липид (например, один или несколько катионных липидов или их солей, описанных в данном документе), фосфолипид и конъюгированный липид, который ингибирует агрегацию частиц (например, один или несколько конъюгатов ПЭГ-липид). Липидные частицы могут также содержать холестерин. Липидные частицы могут инкапсулировать по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более самореплицирующихся молекул РНК, которые кодируют один или несколько полипептидов.
В некоторых вариантах осуществления составы LNP, содержащие поликатионную композицию, можно использовать для доставки описанных в данном документе самореплицирующихся молекул РНК in vivo и/или ex vitro. В изобретении дополнительно предусмотрены составы LNP; содержащие катионный липид.
Термины «катионный липид» и «аминолипид» используются в данном документе взаимозаменяемо и включают те липиды и их соли, которые имеют одну, две, три или более жирных кислот или жирных алкильных цепей и концевую аминогруппу, рН-титруемую (например, алкиламиногруппу или концевую диалкиламиногруппу). Катионный липид обычно протонирован (т.е. положительно заряжен) при рН ниже рКа катионного липид а и является по существу нейтральным при рН выше рКа. Катионные липиды можно также назвать титруемыми катионными липидами. В некоторых вариантах осуществления катионные липиды содержат: протонируемую концевую группу третичного амина (например, рН-титруемую); С 18-алкильные цепи, где каждая алкильная цепь независимо содержит от 0 до 3 (например, 0, 1, 2 или 3) двойных связей; и эфирные, сложноэфирные или кетальные связи между концевой группой и алкильными цепями. Такие катионные липиды включают, но не ограничиваются ими, DSDMA, DODMA, DLinDMA, DLenDMA, у-DLenDMA, DLin-K-DMA, DLin-K-C2-DMA (также известный как DLin-C2K-DMA, XTC2 и C2K), DLin-K-C3-DM A, DLin-K-C4-DMA, DLen-C2K-DMA, y-DLen-C2K-DMA, DLin-M-C2-DMA (также известный как МС2), DLin-M-C3-DMA (также известный как МС3) и (DLin-МР-DMA)(также известный как 1-В1 1).
В изобретении также предусмотрена инкапсулированная самореплицирующаяся молекула РНК, в которой катионный липид содержит протонируемый третичный амин. В некоторых вариантах осуществления катионный липид представляет собой ди((Z)-нон-2-ен-1-ил)-8,8'-((((2-(диметиламино)этил)тио)карбонил)азандиил)диоктаноат.
В некоторых вариантах осуществления катионные липидные соединения относительно нецитотоксичны. Катионные липидные соединения могут быть биосовместимыми и биоразлагаемыми. Катионный липид может иметь рКа в диапазоне от приблизительно 5,5 до приблизительно 7,5, более предпочтительно от приблизительно 6,0 до приблизительно 7,0.
Катионные липидные соединения, описанные в данном документе, особенно привлекательны для доставки лекарственных средств по нескольким причинам: они содержат аминогруппы для взаимодействия с ДНК, РНК, другими полинуклеотидами и другими отрицательно заряженными средствами, для буферизации рН, для вызова эндоосмолиза, для защиты доставляемых самореплицирующихся молекул РНК, могут быть синтезированы из коммерчески доступных исходных материалов; и/или они чувствительны к рН и могут быть сконструированы с желаемым рКа.
Составы липидных наночастиц можно улучшить, заменив катионный липид биоразлагаемым катионным липидом, который известен как быстро выводимая липидная наночастица (reLNP). Было показано, что ионизируемые катионные липиды, такие как, помимо прочего, DLinDMA, DLin-KC2-DMA и DLin-МС3-DMA, со временем накапливаются в плазме крови и тканях и могут быть потенциальным источником токсичности. Быстрый метаболизм быстро выводимых липидов может улучшить переносимость и терапевтический индекс липидных наночастиц на порядок величины от дозы 1 мг/кг до дозы 10 мг/кг у крыс. Включение ферментативно разлагаемой сложноэфирной связи может улучшить профиль распада и метаболизма катионного компонента, сохраняя при этом активность состава reLNP. Сложноэфирная связь может быть расположена внутри липидной цепи или может быть расположена на терминальном конце липидной цепи. Внутренняя сложноэфирная связь может заменить любой углерод в липидной цепи.
В некоторых вариантах осуществления самореплицирующаяся молекула РНК может быть упакована или инкапсулирована в катионных молекулах, таких как полиамидоамин, дендритный полилизин, полиэтилениринин или полипропилен h-нин, полилизин, хитозан, коацерваты ДНК-желатина или декстран DEAE, дендримеры или полиэтиленимин (PEI).
В некоторых вариантах осуществления липидные частицы могут содержать липидный конъюгат. Конъюгированный липид полезен тем, что он предотвращает агрегацию частиц. Подходящие конъюгированные липиды включают, но не ограничиваются ими, конъюгаты ПЭГ-липид, конъюгаты катионный полимер-липид и их смеси.
ПЭГ представляет собой линейный водорастворимый полимер повторяющихся звеньев этилена ПЭГ с двумя концевыми гидроксильными группами. ПЭГ классифицируются по их молекулярной массе; и включают следующее: монометоксиполиэтиленгликоль (MePEG-OH), монометоксиполиэтиленгликоль-сукцинат (MePEG-S), монометоксиполиэтиленгликоль-сукцинимидилсукцинат (MePEG-8-NHS), монометоксиполиэтиленгликоль-амин (MePEG-NH2), монометоксиполиэтиленгликоль-трезилат (MePEG-TRES), монометоксиполиэтиленгликоль-имидазолил-карбонил (MePEG-IM), а также такие соединения, содержащие концевую гидроксильную группу вместо концевой метоксигруппы (например. HO-PEG-S, HO-PEG-S-NHS, HO-PEG-NH2).
Фрагмент ПЭГ описанных в данном документе конъюгатов ПЭГ-липид может иметь среднюю молекулярную массу в диапазоне от 550 дальтон до 10000 дальтон. Примеры ПЭГ-липидов включают, но не ограничиваются ими, ПЭГ, связанный с диалкилоксипропилами (ПЭГ-DAA), ПЭГ, связанный с диацилглицерином (ПЭГ-DAG), ПЭГ, связанный с фосфолипидами, такими как фосфатидилэтаноламин (ПЭГ-РЕ), ПЭГ, связанный с церамидами, ПЭГ, конъюгированный с холестерином или его производным, и их смеси. В некоторых вариантах осуществления конъюгат ПЭГ-липид представляет собой DMG-PEG-2000.
Самореплицирующиеся молекулы РНК также могут быть составлены в частице, содержащей некатионные липиды. Подходящие некатионные липиды включают, например, нейтральные незаряженные, цвиттерионные или анионные липиды, способные образовывать стабильный комплекс. Неограничивающие примеры некатионных липидов включают фосфолипиды, такие как лецитин, фосфатидилэтаноламин, лизолецитин, лизофосфатидилэтаноламин, фосфатидилсерин, фосфатидилинозитол, сфингомиелин, яичный сфингомиелин (ESM), цефалин, кардиолипин, фосфатидная кислота, цереброзиды, дицетилфосфат, дистеароилфосфатидилхолин (DSPC), диолеоилфосфатидилхолин (DOPC), дипальмитоилфосфатидилхолин (DPPC), диолеоилфосфатидилглицерин (DOPG), дипальмитоилфосфатидилглицерин (DPPG), диолеоилфосфатидилэтаноламин (DOPE), пальмитоилолеоилфосфатидилхолин (РОРС), пальмитоилолеоилфосфатидилэтаноламин (POPE), пальмитоилолеоилфосфатидилглицерин (POPG), диолеоилфосфатидилэтаноламин-4-(N-малеимидометил)циклогексан-1-карбоксилат (DOPE-mal), фосфатидилэтаноламин фосфатидилэтаноламин фосфатидилэтаноламин фосфатидилэтаноламин, фосфатидилэтаноламин, фосфатидилэтаноламиндипальмитоилдимиристоилдистеароилмонометилдиметилдиел аидоилстеароилолеоилфосфатидилэтаноламин (SOPE), лизофосфатидилхолин, дилинолеоилфосфатидилхолин и их смеси. Также можно использовать другие диацилфосфатидилхолин- и диацилфосфатидилэтаноламинфосфолипиды. Ацильные группы в этих липидах предпочтительно представляют собой ацильные группы, полученные из жирных кислот, имеющих углеродные цепи С10-С24, например, лауроил, миристоил, пальмитоил, стеароил или олеоил.
Дополнительные примеры некатионных липидов включают стеролы, такие как холестерин и его производные. Неограничивающие примеры производных холестерина включают полярные аналоги, такие как 5а-холестанол, 5а-копростанол, холестерил-(2'-гидрокси)этиловый эфир, холестерил-(4'-гидрокси)бутиловый эфир и 6-кетохолестанол; неполярные аналоги, такие как 5а-холестан, холестенон, 5а-холестанон, 5а-холестанон и холестерилдеканоат; и их смеси. В предпочтительных вариантах осуществления производное холестерина представляет собой полярный аналог, такой как холестерил-(4'-гидрокси)-бутиловый эфир. В некоторых вариантах осуществления фосфолипид представляет собой DSPC. В некоторых вариантах осуществления некатионный липид, присутствующий в липидных частицах, содержит или состоит из смеси одного или нескольких фосфолипидов и холестерина или его производного. В некоторых вариантах осуществления, где липидные частицы содержат смесь фосфолипида и холестерина или производного холестерина, смесь может составлять до 40 мол. %, 45 мол. %, 50 мол. %, 55 мол. % или 60 мол. % от общего количества присутствующих липидов в частице.
В некоторых вариантах осуществления LNP могут содержать 30-70% катионного липидного соединения, 0-60% холестерина, 0-30% фосфолипида и 1-10% полиэтиленгликоля (ПЭГ).
В некоторых вариантах осуществления катионный липид, цвиттерионный липид, холестерин и конъюгированный липид объединяют в молярном соотношении 50:7:40:3 соответственно в липидной наночастице.
В некоторых вариантах осуществления составы LNP, описанные в данном документе, могут дополнительно содержать молекулу, усиливающую проницаемость.
В некоторых вариантах осуществления составы наночастиц могут представлять собой углеводную наночастицу, содержащую углеводный носитель и самореплицирующуюся молекулу РНК. В качестве неограничивающего примера углеводный носитель может включать, но не ограничиваться ими, модифицированный ангидридом фитогликоген или материал типа гликогена, октенилсукцинат фитогликогена, бета-декстрин фитогликогена и бета-декстрин фитогликогена, модифицированный ангидридом.
Наборы
В настоящем изобретении также предусмотрен набор, содержащий одну или несколько композиций, один или несколько полинуклеотидов, один или несколько полипептидов или один или несколько векторов по настоящему изобретению. В настоящем описании также предложен набор, содержащий один или более рекомбинантных вирусов в соответствии с настоящим описанием. Наборы можно использовать для облегчения выполнения способов, описанных в настоящем документе. В некоторых вариантах осуществления набор дополнительно содержит реагенты для облегчения введения вакцин в соответствии с настоящим описанием в клетку, такие как составы на основе липидов или вирусные упаковочные материалы.
В некоторых вариантах осуществления набор содержит один или несколько векторов Ad26, содержащих любой из полинуклеотидов по настоящему изобретению. В некоторых вариантах осуществления набор содержит один или несколько векторов MVA, содержащих любой из полинуклеотидов по настоящему изобретению. В некоторых вариантах осуществления набор содержит один или несколько векторов GAd20, содержащих любой из полинуклеотидов по настоящему изобретению. В некоторых вариантах осуществления набор содержит одну или несколько самореплицирующихся молекул РНК, содержащих любой из полинуклеотидов по настоящему изобретению.
В некоторых вариантах осуществления набор содержит вектор Ad26 по изобретению и вектор MVA по изобретению. В некоторых вариантах осуществления набор содержит вектор Gad20 по изобретению и вектор MVA по изобретению. В некоторых вариантах осуществления набор содержит вектор Ad26 по изобретению и вектор Gad20 по изобретению. В некоторых вариантах осуществления набор содержит самореплицирующуюся молекулу РНК по изобретению и вектор GAd20 по изобретению. В некоторых вариантах осуществления набор содержит самореплицирующуюся молекулу РНК по изобретению и вектор MVA по изобретению. В некоторых вариантах осуществления набор содержит самореплицирующуюся молекулу РНК по изобретению и вектор Ad26 по изобретению. В некоторых вариантах осуществления набор содержит один или более полинуклеотидов в соответствии с настоящим описанием. В некоторых вариантах осуществления набор содержит один или более полипептидов в соответствии с настоящим описанием. В некоторых вариантах осуществления набор содержит одну или более клеток в соответствии с настоящим описанием.
В некоторых вариантах осуществления набор содержит:
первую вакцину, содержащую рекомбинантный вирус, полученный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов; и
вторую вакцину, содержащую рекомбинантный вирус, полученный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 и 421, а также их фрагментов.
В некоторых вариантах осуществления набор содержит:
первую вакцину, содержащую рекомбинантный вирус, полученный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов; и
вторую вакцину, содержащую рекомбинантный вирус, полученный из Ad26, Gad20 или MVA, или самореплицирующуюся молекулу РНК, содержащую гетерологичный полинуклеотид, кодирующий гетерологичный полипептид, причем гетерологичный полипептид содержит два или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их фрагментов.
Другие молекулы
Комплексы неоантиген множественной миеломы / HLA
В настоящем описании также предложен белковый комплекс, содержащий неоантиген множественной миеломы и HLA. В настоящем описании также предложен белковый комплекс, содержащий фрагмент неоантигена множественной миеломы и HLA. В настоящем описании также предложен белковый комплекс, содержащий вариант неоантигена множественной миеломы и HLA. В настоящем описании также предложен белковый комплекс, содержащий вариант фрагмента неоантигена множественной миеломы и HLA.
В некоторых вариантах осуществления неоантиген множественной миеломы содержит полипептидную последовательность, выбранную из группы SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115,117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405 407 и 421, а также их фрагментов.
В некоторых вариантах осуществления HLA представляет собой HLA класса I. В некоторых вариантах осуществления HLA представляет собой HLA класса II. В некоторых вариантах осуществления HLA представляет собой HLA-A. В некоторых вариантах осуществления HLA представляет собой HLA-B. В некоторых вариантах осуществления HLA представляет собой HLA-C. В некоторых вариантах осуществления HLA представляет собой HLA-DP. В некоторых вариантах осуществления HLA представляет собой HLA-DQ. В некоторых вариантах осуществления HLA представляет собой HLA-DR. В некоторых вариантах осуществления HLA представляет собой HLA-A*01:01, А*02:01, А*03:01, А*24:02, В*07:02 или В*08:01.
Комплекс неоантигена множественной миеломы и HLA можно использовать, например, для выделения когнатных Т-клеток in vitro или in vivo. Комплекс неоантигена множественной миеломы и HLA также может быть конъюгирован с обнаруживаемой меткой и использован в качестве агента обнаружения для обнаружения, визуализации или выделения когнатных TCR или Т-клеток, экспрессирующих когнатный TCR. Комплекс неоантигена множественной миеломы и HLA также может быть конъюгирован с цитотоксическим агентом и использован для истощения или уменьшения числа клеток, экспрессирующих когнатный TCR. Комплекс может находиться в своей нативной конфигурации, или в альтернативном варианте осуществления может быть создан неоантиген множественной миеломы и/или HLA. В некоторых вариантах осуществления белковый комплекс в соответствии с настоящим описанием конъюгирован с агентом обнаружения или цитотоксическим агентом.
Концепции конструирования включают ковалентное связывание пептида с HLA, например, путем применения ковалентных линкеров, которые могут быть расщепляемыми. Комплекс неоантигена множественной миеломы и HLA может представлять собой мономер или мультимер. Комплекс неоантигена множественной миеломы и HLA может связываться с токсином или агентом обнаружения. Различные инженерные концепции включают в себя экспрессию комплекса в виде ковалентной цепи неоантигена-β2-α2-α1-β1 множественной миеломы или цепи неоантигена-β множественной миеломы, например, в виде растворимого комплекса. Между неоантигеном множественной миеломы и HLA можно использовать линкеры длиной по меньшей мере 15 аминокислот. В альтернативном варианте осуществления комплекс может быть экспрессирован как ковалентно связанный одноцепочечный неоантиген-β1-α1 множественной миеломы. Комплекс неоантиген множественной миеломы/HLA может также экспрессироваться в виде полноразмерных цепей HLAαβ, с которыми неоантиген множественной миеломы ковалентно связан с N-концом α-цепи, или в альтернативном варианте осуществления неоантиген множественной миеломы связан с αβ-цепью посредством нековалентных взаимодействий. Различные форматы экспрессии описаны в US 5976551, US 5734023, US 5820866, US 7141656 B2, US 6270772 B1 и US 7074905 B2. Кроме того, HLA можно экспрессировать в виде одноцепочечного конструкта, который мутирован в цепи αl или стабилизирован дисульфидными связями посредством доменов α2 и β2, как описано в US 8377447 B2 и US 8828379 B2. Неоантиген множественной миеломы или его фрагмент можно связывать с HLA посредством чувствительных к свету или чувствительных к периодату расщепляемых линкеров, как описано в US 9079941 B2. Комплексы неоантиген множественной миеломы и HLA могут быть сконструированы в мультимерном формате. Мультимерные форматы могут быть получены путем присоединения реакционноспособной боковой цепи к С-концу а или β-цепи HLA для облегчения перекрестного сшивания двух или более комплексов неоантигена множественной миеломы и HLA, как описано в US 7074904 B2. В альтернативном варианте осуществления последовательность распознавания биотинилирования BirA может быть встроена в С-конец α- или β-цепи HLA, который затем биотинилировали, а мультимер образуется путем связывания с авидином/стрептавидином, как описано в US 563536. Мультимерные комплексы неоантигена множественной миеломы и HLA могут быть дополнительно получены с использованием fc-слияний, связывания комплексов неоантигена множественной миеломы и HLA в декстрановых носителях, олигомеризации посредством полых спиральных доменов, использования дополнительных биотинилированных пептидов или конъюгации комплексов неоантигена множественной миеломы и HLA с наночастицами или хелатирующим носителем, как описано в US 6197302 B1, US 6268411 B1, US 20150329617 A1, ЕР 1670823 В1, ЕР1882700 В1, ЕР 2061807 В1, US 20120093934 A1, US 20130289253 A1, US 20170095544 A1, US 20170003288 A1 и WO 2017015064 A1.
В настоящем описании предложен белковый комплекс, содержащий человеческий лейкоцитарный антиген (HLA) и полипептид в соответствии с настоящим описанием, содержащий аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагмент.
В некоторых вариантах осуществления HLA может включать класс I или класс II.
В некоторых вариантах осуществления HLA может содержать HLA-A, HLA-B или HLA-C.
В некоторых вариантах осуществления HLA может содержать HLA-DP, HLA-DQ или HLA-DR.
В некоторых вариантах осуществления HLA может содержать аллели класса I HLA-A*01:01, А*02:01, А*03:01, А*24:02, В*07:02 или В*08:01.
Белковые молекулы
В изобретении также предусмотрена выделенная белковая молекула, которая специфически связывается с полипептидом согласно изобретению или комплексом HLA и полипептида.
В некоторых вариантах осуществления белковая молекула представляет собой антитело, альтернативный каркас, химерный антигенный рецептор (CAR) или Т-клеточный рецептор (TCR).
В некоторых вариантах осуществления в настоящем описании также предложены белковые молекулы, которые связывают полипептид SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421. Белковые молекулы незначительно связываются с белком дикого типа, вариантом которого является неоантиген.
В настоящем описании также предложены белковые молекулы, которые связывают комплекс неоантигена множественной миеломы и HLA, причем неоантиген множественной миеломы содержит полипептид SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, 405, 407 или 421 или их фрагменты.
В некоторых вариантах осуществления белковая молекула представляет собой антигенсвязывающий фрагмент антитела.
В некоторых вариантах осуществления белковая молекула представляет собой мультиспецифическую молекулу. В некоторых вариантах осуществления белковая молекула представляет собой биспецифическую молекулу. В некоторых вариантах осуществления белковая молекула представляет собой триспецифическую молекулу. В некоторых вариантах осуществления мультиспецифическая молекула связывает два или более разных неоантигенов множественной миеломы. В некоторых вариантах осуществления мультиспецифическая молекула связывает неоантиген множественной миеломы и комплекс Т-клеточного рецептора (TCR). В некоторых вариантах осуществления мультиспецифическая молекула связывает два или более различных неоантигена множественной миеломы и комплекс Т-клеточного рецептора (TCR).
В некоторых вариантах осуществления белковая молекула представляет собой антитело.
В некоторых вариантах осуществления белковая молекула представляет собой мультиспецифическое антитело. В некоторых вариантах осуществления белковая молекула представляет собой биспецифическое антитело. В некоторых вариантах осуществления белковая молекула представляет собой триспецифическое антитело. В некоторых вариантах осуществления белковая молекула представляет собой перенаправляющую Т-клетки молекулу.
В случаях, когда неоантиген множественной миеломы в соответствии с настоящим описанием является частью внеклеточного домена белка, неоантиген множественной миеломы может использоваться в качестве опухоль-ассоциированного антигена для привлечения Т-клеток к опухолям или нацеливания CAR-T и других клеточных терапий на опухоль с помощью антигенсвязывающих доменов, которые селективно связывают неоантиген множественной миеломы на опухолевых клетках.
В случаях, когда неоантиген множественной миеломы является частью внутриклеточного домена, в качестве терапевтических средств могут использоваться антигенсвязывающие домены, имеющие возможность доставки во внутриклеточные компартменты, конъюгированные с цитотоксическим агентом или терапевтическим агентом. В альтернативном варианте осуществления в качестве терапевтических средств можно использовать клетки, сконструированные с возможностью экспрессировать когнатный TCR, который связывает комплекс неоантигена множественной миеломы и HLA.
В некоторых вариантах осуществления белковая молекула представляет собой альтернативный каркас.
В некоторых вариантах осуществления белковая молекула представляет собой химерный антигенный рецептор (CAR).
В некоторых вариантах осуществления белковая молекула представляет собой Т-клеточный рецептор (TCR).
Связывание белковой молекулы с неоантигеном множественной миеломы или комплексом неоантигена множественной миеломы и HLA в соответствии с настоящим описанием можно определить экспериментально с использованием любого приемлемого способа. Такие способы могут включать применение оборудования ProteOn XPR36, Biacore 3000 или KinExA, ИФА или анализы конкурентного связывания, известные специалистам в данной области. Измеренное значение асвязывания может изменяться при измерении в различных условиях (например, осмолярности, рН). Таким образом, измерения аффинности и других параметров связывания (например, KD, Kon, Koff), как правило, проводятся в стандартизированных условиях и с использованием стандартизированного буферного раствора, такого как буферный раствор, описанный в настоящем документе. Специалистам в данной области будет понятно, что внутренняя ошибка измерений аффинности, например, с применением оборудования Biacore 3000 или ProteOn (измеряемая как среднеквадратичное отклонение (СО)), как правило, может составлять 5-33% для измерений, проводимых в границах типичных пределов обнаружения. Термин «несущественный» относится к связыванию, которое в 100 раз меньше по сравнению с измеренным связыванием белковой молекулы с неоантигеном множественной миеломы в соответствии с настоящим описанием. Белковую молекулу в соответствии с настоящим описанием можно дополнительно охарактеризовать в зависимости от ее активности и функции с применением известных способов и описанных в настоящем документе, таких как способность белковых молекул уничтожать клетки, экспрессирующие неоантигены множественной миеломы или комплексы неоантигена множественной миеломы и HLA.
Антитела и антигенсвязывающие домены
Антитела и антигенсвязывающие домены, которые специфически связывают неоантигены множественной миеломы или комплексы неоантигена множественной миеломы и HLA, можно создавать с помощью известных способов. Такие антитела могут включать в себя молекулы иммуноглобулина любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса.
Например, для создания моноклональных антител можно применять способ гибридом по Kohler and Milstein, Nature 256:495, 1975. В способе гибридомы мышь или другое животное-хозяина, например хомяка, крысу или обезьяну, иммунизируют одним или более неоантигенами множественной миеломы или комплексами неоантигена множественной миеломы и HLA с последующим слиянием спленоцитов от иммунизированных животных с клетками миеломы с использованием стандартных способов с получением клеток гибридомы (Goding, Monoclonal Antibodies: Principles and Practice, pp. 59-103 (Academic Press, 1986)). Колонии, возникающие из одиночных иммортализованных клеток гибридомы, подвергают скринингу для определения продукции антител с желательными свойствами, такими как специфичность связывания и аффинности для неоантигена множественной миеломы в соответствии с настоящим описанием.
Для получения антител можно использовать различных животных-хозяев. Например, можно использовать мышей Balb/c, крыс или цыплят для получения антител, содержащих пару VH/VL, а лам и альпак можно использовать для создания антител только с тяжелой цепью (VHH) с помощью стандартных протоколов иммунизации. Антитела, полученные от нечеловекоподобных животных, могут быть гуманизированы с применением разнообразных методик для создания последовательностей, имеющих большее сходство с человеческими последовательностями.
Примеры методик гуманизации, включающих в себя отбор человеческих акцепторных каркасов, известны и включают в себя прививание CDR (патент США №5,225,539), прививание SDR (патент США №6,818,749), изменение поверхности (Padlan, (1991) Mol Immunol 28:489-499), изменение поверхности определяющих специфичность остатков (патентная публикация США №2010/0261620), адаптацию человеческого каркаса (патент США №8,748,356) и супергуманизацию (патент США №7,709, 226). В этих способах CDR исходных антител переносят на человеческие каркасы, которые можно выбирать на основании их общей гомологии с исходными каркасами, на основании сходства длины CDR или идентичности канонической структуры либо их комбинации.
Гуманизированные антитела могут быть дополнительно оптимизированы для улучшения их селективности или аффинности к требуемому антигену посредством включения измененных остатков, поддерживающих каркас, с сохранением аффинности связывания (обратных мутаций) такими методиками, которые описаны в международных патентных публикациях № WO 1090/007861 и WO 1992/22653, или посредством встраивания вариации в любую из CDR, например, для улучшения аффинности антитела.
Для получения человеческих антител против неоантигенов множественной миеломы иди комплексов неоантигена множественной миеломы и HLA можно применять трансгенных животных, таких как мыши или крысы, несущих в своем геноме локусы иммуноглобулинов (Ig) человека, которые описаны, например, в патенте США №6,150,584, международной патентной публикации № WO 99/45962, международных патентных публикациях № WO 2002/066630, WO 2002/43478, WO 2002/043478 и WO 1990/04036, Lonberg et al. (1994) Nature 368:856-9; Green et al. (1994) Nature Genet. 7:13-21; Green & Jakobovits (1998) Exp. Med. 188:483-95; Lonberg and Huszar (1995) Int Rev Immunol 13:65-93; Bruggemann et al., (1991) Eur J Immunol 21:1323-1326; Fishwild et al., (1996) Nat Biotechnol 14:845-851; Mendez et al., (1997) Nat Genet 15:146-156; Green (1999) J Immunol Methods 231:11-23; Yang et al., (1999) Cancer Res 59:1236-1243; Brüggemann and Taussig (1997) Curr Opin Biotechnol 8:455-458. Эндогенные локусы иммуноглобулинов у таких животных можно разрывать или удалять, и в геном животного можно встраивать по меньшей мере один полный или частичный локус иммуноглобулина человека посредством гомологичной или негомологичной рекомбинации, с применением трансхромосом или с применением минигенов. Для получения человеческих антител, направленных против выбранного антигена, с применением описанной выше технологии можно обратиться к таким компаниям, как Regeneron (http://_www_regeneron_com), Harbour Antibodies (http://_www_harbourantibodies_com), Open Monoclonal Technology, Inc. (OMT) (http://_www_omtinc_net), KyMab (http://_www_kymab_com), Trianni (http://_www.trianni_com) и Ablexis (http://_www_ablexis_com).
Человеческие антитела можно выбирать из библиотеки фагового дисплея, причем фаг сконструирован с возможностью экспрессии человеческих иммуноглобулинов или их участков, таких как Fab, одноцепочечные антитела (scFv), домены антител или неспаренные либо спаренные вариабельные области антител (Knappik et al., (2000) J Mol Biol 296:57-86; Krebs et al., (2001) J Immunol Meth 254:67-84; Vaughan et al., (1996) Nature Biotechnology 14:309-314; Sheets et al., (1998) PITAS (USA) 95:6157-6162; Hoogenboom and Winter (1991) J Mol Biol 227:381; Marks et al., (1991) J Mol Biol 222:581). Антитела в соответствии с настоящим описанием могут быть выделены, например, из библиотеки фагового дисплея, экспрессирующей вариабельные области тяжелой и легкой цепей антитела в виде гетерологичных полипептидов с белком оболочки бактериофага pIX, как описано в публикации Shi et al., (2010) J Mol Biol 397:385-96 и в международной патентной публикации № WO 09/085462). В библиотеках можно проводить скрининг на связывание фагов с неоантигеном множественной миеломы или комплексом неоантигена множественной миеломы и HLA, и полученные положительные клоны могут быть дополнительно охарактеризованы, из лизатов клонов могут быть выделены Fab и экспрессированы в виде полноразмерных IgG. Такие способы использования фагового дисплея для выделения человеческих антител описаны, например, в патенты США №5,223,409, 5,403,484, 5,571,698, 5,427,908, 5, 580,717, 5,969,108, 6,172,197, 5,885,793; 6,521,404; 6,544,731; 6,555,313; 6,582,915 и 6,593,081. Антитела можно дополнительно тестировать на предмет их связывания с комплексом HLA/неоантиген или только с неоантигеном.
Получение иммуногенных антигенов и продукция моноклональных антител могут быть выполнены с применением любой приемлемой методики, такой как продукция рекомбинантного белка или химический синтез пептидов. Иммуногенные антигены можно вводить животным в форме очищенного белка или белковых смесей, включающих в себя целые клетки или клеточные либо тканевые экстракты, или антиген может быть образован de novo в организме животного из нуклеиновых кислот, кодирующих указанный антиген или его часть.
Антигенсвязывающие домены, которые специфически связываются с неоантигеном множественной миеломы или комплексами неоантигена множественной миеломы и HLA, также могут быть получены из антител, описанных в настоящем документе. Антигенсвязывающие домены включают одноцепочечные антитела, Fab-фрагменты, Fv-фрагменты, одноцепочечные Fv-фрагменты (scFv), домены VHH, VH, VL, альтернативные каркасы (например, антигенсвязывающие домены, не относящиеся к антителам), двухвалентный фрагмент антитела, например (Fab)2'-фрагмент, F(ab')-фрагменты, дисульфид-связанные Fv (sdFv), интратритела, минитела, диатела, триатела и декатела.
Биспецифические и мультиспецифические антитела, которые специфически связывают неоантиген множественной миеломы или комплексы неоантигена множественной миеломы и HLA и второй антиген, можно создавать с использованием известных способов. Второй антиген может представлять собой комплекс Т-клеточного рецептора (комплекс TCR). Второй антиген может представлять собой CD3 в пределах комплекса TCR. Биспецифические и мультиспецифические антитела, которые специфически связывают неоантиген множественной миеломы или комплексы неоантиген множественной миеломы/HLA в соответствии с настоящим описанием и второй антиген, могут быть сконструированы в любом мультивалентном формате с использованием любого известного формата антигенсвязывающих доменов, который специфически связывает неоантигены множественной миеломы или комплексы неоантиген множественной миеломы/HLA и второй антиген. Антигенсвязывающий домен, который специфически связывает неоантиген множественной миеломы или комплекс неоантиген множественной миеломы/HLA, может быть конъюгирован с одним или более Fc-доменами или их фрагментом или необязательно с другими каркасами, такими как фрагменты, увеличивающие период полужизни, включая альбумин, ПЭГ или трансферрин.
Мультиспецифические антитела, которые специфически связывают два или более неоантигенов множественной миеломы, могут обеспечивать преимущество в отношении улучшенной специфичности нацеливания на опухолевые клетки, экспрессирующие неоантигены множественной миеломы.
Антигенсвязывающие домены, которые специфически связывают неоантиген множественной миеломы или комплексы неоантиген множественной миеломы/HLA, можно конструировать в полноразмерные мультиспецифические антитела, которые созданы с помощью обмена Fab-фрагментами, в которых замены вводят в два моноспецифических двухвалентных антитела в пределах константного участка Ig домена СН3, который способствует обмену Fab-фрагментами in vitro. В этих способах два моноспецифических бивалентных антитела конструируют так, чтобы они имели определенные замены в домене СН3, способствующие стабильности гетеродимера; антитела инкубируют вместе в восстановительных условиях, достаточных для обеспечения подверженности цистеинов в шарнирной области изомеризации дисульфидной связи; получая таким образом биспецифическое антитело в результате обмена Fab-фрагментами. Условия инкубации можно оптимально возвращать к невосстанавливающим. Примерами восстанавливающих агентов, которые можно использовать, являются 2-меркаптоэтиламин (2-МЕА), дитиотреитол (DTT), дитиоэритрит (DTE), глутатион, трис(2-карбоксиэтил)фосфин (ТСЕР), L-цистеин и бета-меркаптоэтанол, предпочтительно восстанавливающий агент выбирают из группы, состоящей из: 2-меркаптоэтиламина, дитиотреитола и трис(2-карбоксиэтил)фосфина. Например, можно использовать инкубирование в течение по меньшей мере 90 мин при температуре по меньшей мере 20°С в присутствии по меньшей мере 25 мМ 2-МЕА или в присутствии по меньшей мере 0,5 мМ дитиотреитола при уровне рН 5-8, например при рН = 7,0 или при рН = 7,4.
Мутации СН3, которые можно использовать, включают в себя такие технологии, как мутации «выступ во впадину» (Genentech), электростатически спариваемые мутации (Chugai, Amgen, NovoNordisk, Oncomed), сконструированное посредством обмена цепей доменное тело (SEEDbody) (EMD Serono) и другие асимметричные мутации (например, Zymeworks).
Мутации типа «выступ во впадину» описаны, например, в WO 1996/027011 и включают мутации на границе раздела области СН3, в которой аминокислоту с небольшой боковой цепью (впадина) вносят в первую область СН3, а аминокислоту с большой боковой цепью (выступ) вносят во вторую область СН3, что приводит к предпочтительному взаимодействию между первой областью СН3 и второй областью СН3. Примерами мутаций в области СН3, образующих выступ и впадину, являются T366Y/F405A, T366W/F405W, F405W/Y407A, T394W/Y407T, T394S/Y407A, T366W/T394S, F405W/T394S и T366W/T366S_L368A_Y407V.
Образование гетеродимера тяжелой цепи можно стимулировать путем использования электростатических взаимодействий посредством замены положительно заряженных остатков в первой области СН3 и отрицательно заряженных остатков во второй области СН3, как описано в US 2010/0015133, US 2009/0182127, US 2010/028637 или US 2011/0123532.
Другими асимметричными мутациями, которые можно применять для стимуляции гетеродимеризации тяжелых цепей, являются L351Y_F405A_Y407V/T394W, T366I_K392M_T394W/F405A_Y407V, T366L_K392M_T394W/F405A_Y407V, L351Y_Y407A/T366A_K409F, L351Y_Y407A/T366V_K409F, Y407A/T366A_K409F, or T350V_L351Y_F405A_Y407V/T350V_T366L_K392L_T394W, как описано в US 2012/0149876 or US 2013/0195849 (Zymeworks).
Мутации SEEDbody включают замещение выбранных остатков IgG остатками IgA для стимуляции гетеродимеризации тяжелых цепей, как описано в US 20070287170.
Другими примерами мутаций, которые можно использовать, являются R409D_K370E/D399K_E357K, S354C_T366W/Y349C_T366S_L368A_Y407V, Y349C_T366W/S354C_T366S_L368A_Y407V, T366K/L351D, L351K/Y349E, L351K/Y349D, L351K/L368E, L351Y_Y407A/T366A_K409F, L351Y_Y407A/T366V_K409F, K392D/D399K, K392D/E356K, K253E_D282K_K322D/D239K_E240K_K292D, K392D_K409D/D356K_D399K, описанные в WO 2007/147901, WO 2011/143545, WO 2013157954, WO 2013096291 и US 2018/0118849.
Мутации Duobody® (Genmab) описаны, например, в US 9150663 и US 2014/0303356 и включают в себя мутации F405L/K409R, дикий тип/F405L_R409K, T350I_K370T_F405L/K409R, K370W/K409R, D399AFGHILMNRSTVWY/K409R, T366ADEFGHILMQVY/K409R, L368ADEGHNRSTVQ/K409AGRH, D399FHKRQ/K409AGRH, F405IKLSTVW/K409AGRH и Y407LWQ/K409AGRH.
Дополнительные биспецифические или мультиспецифические структуры, в которые могут быть встроены антигенсвязывающие домены, которые специфически связываются с неоантигеном множественной миеломы или комплексами неоантиген множественной миеломы/HLA, включают иммуноглобулины с двойным вариабельным доменом (DVD) (международная патентная публикация № WO 2009/134776; DVD представляют собой полноразмерные антитела, содержащие тяжелую цепь, имеющую структуру VH1-линкер-VH2-CH, и легкую цепь, имеющую структуру VL1-линкер-VL2-CL где линкер необязателен), структуры, включающие различные димеризационные домены для соединения двух плеч антител с разной специфичностью, такие как «лейциновая застежка» или коллагеновые димеризационные домены (международная патентная публикация № WO 2012/022811, патент США №5,932,448; патент США №6,833,441), два или более доменных антитела (dAb), конъюгированных вместе, диатела, антитела, имеющие только тяжелую цепь, такие как антитела верблюжьего типа и сконструированные антитела верблюжьего типа, антитела с двойным нацеливанием (DT)-Ig (GSK/Domantis), антитело «два в одном» (Genentech), поперечно сшитые Mab (Karmanos Cancer Center), mAb2 (F-Star) и CovX-тело (CovX/Pfizer), IgG-подобные биспецифические антитела (InnClone/Eli Lilly), Ts2Ab (MedImmune/AZ) и BsAb (Zymogenetics), HERCULES (Biogen Idec) и TvAb (Roche), слитые белки ScFv/Fc (Academic Institution), SCORPION (Emergent BioSolutions/Trubion, Zymogenetics/BMS), перенацеливающиеся антитела с двойной аффинностью (Fc-DART) (MacroGenics) и Dual(ScFv)2-Fab (National Research Center for Antibody Medicine, Китай), антитела «двойного действия» или Bis-Fab (Genentech), Dock-and-Lock (DNL) (ImmunoMedics), двухвалентное биспецифическое антитело (Biotecnol) и Fab-Fv (UCB-Celltech). Антитела на основе ScFv, диател и доменные антитела включают в себя, без ограничений, биспецифический Т-клеточный активатор (BiTE) (Micromet), тандемное диатело (Tandab) (Affimed), перенацеливающиеся антитела с двойной аффинностью (DART) (MacroGenics), одноцепочечное диатело (Academic), TCR-подобные антитела (AIT, ReceptorLogics), слитый белок ScFv и человеческого сывороточного альбумина (Merrimack), COMBODY (Epigen Biotech), нанотела с двойным нацеливанием (Ablynx), доменные антитела с двойным нацеливанием, имеющие только тяжелую цепь.
Альтернативные каркасы
Альтернативные каркасы (также называемые миметиками антител), которые специфически связывают неоантиген множественной миеломы или комплексы неоантигена множественной миеломы и HLA, могут быть получены с использованием различных каркасов, известных в данной области и описанных в настоящем документе. Альтернативными каркасами могут быть монотела, выполненные с возможностью включения фибронектинового домена типа III (Fn3) фибронектина или тенасцина в качестве белкового каркаса (патент США No 6,673,901; Патент США №. 6,348,584) или синтетические домены FN3, такие как тенкон, как описано в патентной публикации США №. 2010/0216708 и патентной публикации №2010/0255056. Дополнительные альтернативные каркасы включают Adnectin™, an iMab, an Anticalin®, an EETI-II/AGRP, домен Куница, тиоредоксин-пептидный аптамер, Affibody®, a DARPin, Affilin, Tetranectin, Fynomer и Avimer. Альтернативными каркасами являются одноцепочечные полипептидные каркасы, которые содержат высокоструктурное ядро, связанное с вариабельными доменами с высокой конформационной толерантностью, позволяющее вставлять, удалять или производить другие замены в пределах вариабельных доменов. Библиотеки, внедряющие разнообразие в один или более вариабельных доменов, а в некоторых случаях в структурированную сердцевину, могут быть созданы с использованием известных протоколов, и полученные библиотеки могут быть подвергнуты скринингу на предмет связывания с неоантигеном настоящего описания, а идентифицированные связывающие вещества могут быть дополнительно охарактеризованы на предмет их специфичности с использованием известных способов. Альтернативный каркас может быть получен из белка А, в частности, его Z-домена (аффитела), ImmE7 (иммунные белки), BPTI/APPI (домены Куница), RAS-связывающего белка AF-6 (PDZ-домены), хариботоксина (токсин скорпиона), CTLA-4, Min-23 (ноттинсы), липокалина (антикалины), неокарзиностатина, фибронектинового домена, консенсусного домена с анкириновыми повторами или тиоредоксина (Skerra, A., "Alternative Non-Antibody Scaffolds for Molecular Recognition" Curr. Opin. Biotechnol. 18:295-304 (2005); Hosse et al., "A New Generation of Protein Display Scaffolds for Molecular Recognition," Protein Sci. 15:14-27 (2006); Nicaise et al., "Affinity Transfer by CDR Grafting on a Nonimmunoglobulin Scaffold," Protein Sci. 13:1882-1891 (2004); Nygren and Uhlen, "Scaffolds for Engineering Novel Binding Sites in Proteins," Curr. Opin. Struc. Biol. 7:463-469 (1997).
Химерные антигенные рецепторы (CAR)
Могут быть получены CAR, которые связываются с неоантигенами множественной миеломы или комплексом неоантигена множественной миеломы и HLA, путем включения антигенсвязывающего домена, который специфически связывает неоантигены множественной миеломы или комплекс неоантигена множественной миеломы и HLA с внеклеточным доменом CAR. Car представляют собой генно-инженерные рецепторы. Эти сконструированные рецепторы могут быть легко вставлены в иммунные клетки, включая Т-клетки, и экспрессированы ими в соответствии с методиками, известными в данной области. С помощью CAR один рецептор может быть запрограммирован как на распознавание специфического антигена, так и на активацию иммунной клетки для атаки и разрушения клетки, несущей этот антиген, при связывании с этим антигеном. Если эти антигены существуют на опухолевых клетках, иммунная клетка, которая экспрессирует CAR, может нацеливаться на опухолевую клетку и уничтожать ее.
CAR, как правило, содержит внеклеточный домен, который связывает антиген (например, неоантиген множественной миеломы или комплекс неоантиген множественной миеломы/HLA), необязательный линкер, трансмембранный домен и цитозольный домен, содержащий костимулирующий домен и/или сигнальный домен.
Внеклеточный домен в составе CAR может содержать любой полипептид, который специфично связывает нужный антиген (например, неоантиген множественной миеломы). Внеклеточный домен может содержать scFv, часть антитела или альтернативную каркасную молекулу. CAR также могут быть сконструированы с возможностью связывания с двумя или более нужными антигенами, которые могут быть расположены в тандеме и разделены линкерными последовательностями. Например, одно или более доменных антител, антител scFv, 1lama VHH или других фрагментов антител, содержащих только VH, могут быть расположены в тандеме посредством линкера для обеспечения биспецифичности или мультиспецифичности к CAR.
Трансмембранный домен CAR может быть получен из трансмембранного домена CD8, альфа-, бета- или дзета-цепи Т-клеточного рецептора, CD28, CD3-эпсилон, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, CD154, KIRDS2, ОХ40, CD2, CD27, LFA-1 (CDI la, CD18), ICOS (CD278), 4-1 ВВ (CD 137), 4-1 BBL, GITR, CD40, BAFFR, HVEM (LIGHTR), SLAMF7, NKp80 (KLRFI), CD160, CD1 9, IL2R-6eTa, IL2R-гамма, IL7R a, ITGA1, VLA1, CD49a, ITGA4, IA4, CD49D, ITGA6, VLA-6, CD49f, ITGAD, CDI Id, ITGAE, CD103, ITGAL, CDI la, LFA-1, ITGAM, CDI lb, ITGAX, CDI lc, ITGB1, CD29, ITGB2, CD1 8, LFA-1, ITGB7, TNFR2, DNAM1 (CD226), SLAMF4 (CD244, 2B4), CD84, CD96 (Tactile), CEACAM1, CRT AM, Ly9 (CD229), CD160 (BY55), PSGL1, CD100 (SEMA4D), SLAMF6 (NTB-A, Lyl08), SLAM (SLAMF1, CD150, IPO-3), BLAME (SLAMF8), SELPLG (CD162), LTBR, PAG/Cbp, NKp44, NKp30, NKp46, NKG2D и/или NKG2C.
Внутриклеточный костимулирующий домен CAR может быть получен из внутриклеточных доменов одной или более костимулирующих молекул. Ко стимулирующие молекулы хорошо известны как молекулы клеточной поверхности, отличные от антигенных рецепторов или Fc-рецепторов, которые обеспечивают второй сигнал, необходимый для эффективной активации и функционирования Т-лимфоцитов при связывании с антигеном. Примерами костимулирующих доменов, которые можно использовать в CAR, являются внутриклеточные домены 4-1ВВ, CD2, CD7, CD27, CD28, CD30, CD40, CD54 (ICAM), CD83, CD134 (ОХ40), CD150 (SLAMF1), CD152 (CTLA4), CD223 (LAG3), CD270 (HVEM), CD278 (ICOS), DAP10, LAT, NKD2C SLP76, TRIM, BTLA, GITR, CD226, HVEM и ZAP70.
Внутриклеточный сигнальный домен CAR может быть получен из сигнальных доменов, например CD3ζ, CD3ε, CD22, CD79a, CD66d, CD39 DAP10, DAP12, гамма-цепи Fc-епсилон-рецептора I (FCER1G), FcR β, CD3δ, CD3γ, CD5, CD226 или CD79B. «Внутриклеточный сигнальный домен» относится к части полипептида CAR, которая участвует в передаче сообщения об эффективном связывании CAR с целевым антигеном во внутреннюю часть иммунной эффекторной клетки для запуска функции эффекторной клетки, например активации, выработки цитокинов, пролиферации и цитотоксической активности, включая высвобождение цитотоксических факторов в клетку-мишень, связанную с CAR, или других клеточных ответов, запускаемых после связывания антигена с внеклеточным доменом CAR.
Необязательный линкер CAR, расположенный между внеклеточным доменом и трансмембранным доменом, может представлять собой полипептид длиной от около 2 до около 100 аминокислот. Линкер может включать в себя гибкие остатки, такие как глицин и серин, или состоять из них, так что смежные домены белка могут свободно перемещаться относительно друг друга. Можно применять более длинные линкеры, если желательно обеспечить, чтобы два смежных домена не создавали стерических помех друг для друга. Линкеры могут быть расщепляемыми или нерасщепляемыми. Примеры расщепляемых линкеров включают линкеры 2А (например, Т2А), 2А-подобные линкеры или их функциональные эквиваленты, а также их комбинации. Линкер также может быть получен из шарнирной области или части шарнирной области любого иммуноглобулина. Не имеющие ограничительного характера примеры линкеров включают часть человеческой цепи CD8a, частичный внеклеточный домен CD28, рецептор FcyRllla, IgG, IgM, IgA, IgD, IgE, шарнир Ig или его функциональный фрагмент.
Примерами CAR, которые могут быть использованы, являются, например, CAR, содержащий внеклеточный домен, который связывает неоантиген множественной миеломы в соответствии с настоящим описанием, трансмембранный домен CD8 и сигнальный домен CD3ζ. Другие примеры CAR содержат внеклеточный домен, который связывает неоантиген множественной миеломы в соответствии с настоящим описанием, трансмембранный домен CD8 или CD28, костимулирующий домен CD28, 41ВВ или ОХ40 и сигнальный домен CD3ζ.
CAR получают с помощью стандартных методов молекулярной биологии. Внеклеточный домен, который связывается с нужным антигеном, может быть получен из антител или их антигенсвязывающих фрагментов, полученных с использованием технологий, описанных в настоящем документе.
Секвенирование Т-клеточных рецепторов (TCR)
Могут быть получены TCR, которые связываются с комплексами неоантиген множественной миеломы/HLA. TCR могут быть идентифицированы на основе связывания Т-клеток с комплексом неоантиген множественной миеломы/HLA in vivo или как система in-vitro, например, в виде мультимерного комплекса неоантигенсвязанных HLA-молекул, выделения Т-клетки и секвенирования TCR, экспрессируемого в Т-клетках. Идентифицированные TCR могут быть идентифицированы из αβ Т-клеток или γδ Т-клеток. Идентифицированные TCR могут быть дополнительно сконструированы для улучшения их аффинности, стабильности, растворимости и т.п. Аффинность TCR может созревать использованием тех же технологий, что и для аффинного созревания иммуноглобулинов. TCR могут экспрессироваться в виде растворимых TCR, которые были стабилизированы цистеином, и они могут быть стабилизированы с помощью инженерных мутаций на поверхности взаимодействия α/β, например G192R в α-цепи и R208G в β-цепи. TCR также можно стабилизировать путем конструирования цистеиновых остатков, которые образуют дисульфидные связи в константный домен TCR, путем введения мутаций в гидрофобное ядро, например, в положениях 11, 13,19, 21, 53, 76, 89, 91 или 94 α-цепи, использования перестановки доменов, включая перестановки между V-доменами α- и β-цепи, транс мембранными доменами или константными доменами, как описано в US 7329731, US 7871817 B2, US 7569664, US 9133264, US 9624292, US 20120252742 A1, US 2016/0130319, ЕР 3215164 А1, ЕР 3286210 А1, WO 2017091905 A1 или US 9884075.
Клетки, экспрессирующие CAR или TCR в соответствии с настоящим описанием
Клетки, экспрессирующие CAR или TCR, которые специфически связывают неоантигены множественной миеломы в соответствии с настоящим описанием комплексов неоантиген множественной миеломы/HLA в соответствии с настоящим описанием, входят в объем настоящего описания. В настоящем описании также предложены выделенные клетки, содержащие CAR по настоящему описанию или TCR по настоящему описанию. В некоторых вариантах осуществления выделенные клетки трансдуцируют CAR или TCR по настоящему описанию, что приводит к конститутивной экспрессии CAR или TCR по настоящему описанию на поверхности клетки. Клетки, экспрессирующие CAR или TCR по настоящему описанию, могут быть дополнительно сконструированы с возможностью экспрессии одной или более костимулирующих молекул. Примерами костимулирующих молекул являются CD28, ICOS, СВЕТ, GITR, 4-1ВВ и ОХ40. Клетки, экспрессирующие CAR или TCR в соответствии с настоящим описанием могут быть дополнительно сконструированы с возможностью продуцировать один или более цитокинов, или хемокинов, или провоспалительных медиаторов, таких как TNFα, IFNγ, IL-2, IL-3, IL-6, IL-7, IL-11, IL-12, IL-15, IL-17 или IL-21. Клетки могут иметь свой эндогенный локус TCR и/или инактивированный локус HLA с использованием известных технологий редактирования генов. В некоторых вариантах осуществления клетка, содержащая CAR или TCR в соответствии с настоящим описанием, представляет собой Т-клетку, естественную киллерную (NK) клетку, цитотоксический Т-лимфоцит (CTL), регуляторную Т-клетку (Treg), эмбриональную стволовую клетку человека, лимфоидную клетку-предшественника, клетку-предшественника Т-клеток, плюрипотентную стволовую клетку или индуцированную плюрипотентную стволовую клетку (iPSC), из которых могут быть дифференцированы лимфоидные клетки.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR или TCR по настоящему описанию, представляет собой Т-клетку. Т-клетка может представлять собой любую Т-клетку, такую как культивированная Т-клетка, например первичная Т-клетка или Т-клетка из культивированной Т-клеточной линии, например, Jurkat, SupT1 и т.д., или Т-клетку, полученную от млекопитающего. При получении от млекопитающего Т-клетку можно получить из любого источника, включая костный мозг, кровь, лимфатический узел, тимус или другие ткани или жидкости. Т-клетки также могут быть обогащенными или очищенными. Т-клетка может представлять собой Т-клетку человека. Т-клетка может представлять собой Т-клетку, выделенную из человека. Т-клетка может относиться к любому типу Т-клеток и может относиться к любому этапу развития, включая двойные положительные CD4+CD8+ Т-клетки, CD8+ Т-клетки (например, цитотоксические Т-клетки), хелперные CD4+ Т-клети, например Th1 и Th2, мононуклеарные клетки периферической крови (МКПК), лейкоциты периферической крови (PBL), инфильтрирующие опухоль клетки, Т-клетки памяти, интактные Т-клетки и т.п. Т-клетка может представлять собой CD8+ Т-клетку или CD4+ Т-клетку. Т-клетка может представлять собой αβ Т-клетку или γδ Т-клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой NK-клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой αβ Т-клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой γδ Т-клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой CTL-клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой человеческую эмбриональную стволовую клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой лимфоидную клетку-предшественник.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой плюрипотентную стволовую клетку.
В некоторых вариантах осуществления выделенная клетка, содержащая CAR в соответствии с настоящим описанием или TCR в соответствии с настоящим описанием, представляет собой индуцированную плюрипотентную стволовую клетку (iPSC).
Клетки по настоящему описанию могут быть получены путем введения лентивирусного вектора, содержащего необходимый CAR или TCR, в клетки с использованием известных способов. Клетки по настоящему описанию способны реплицироваться in vivo, что приводит к длительной персистенции, которая может приводить к устойчивому контролю опухоли.
Конъюгаты с цитотоксическими агентами, лекарственными препаратами, выявляемыми метками и т.п.
Полипептиды, гетерологичный полипептид и связывающие их белковые молекулы могут быть конъюгированы с цитотоксическим агентом, терапевтическими средствами, обнаруживаемыми метками и т.п. В данном документе эти молекулы называются иммуноконъюгатами. Иммуноконъюгаты, содержащие неоантигены множественной миеломы, можно использовать для обнаружения, доставки полезной нагрузки или уничтожения клеток, экспрессирующих молекулу HLA, которая связывает неоантиген множественной миеломы. Иммуноконъюгаты, содержащие антитела, антигенсвязывающие фрагменты или альтернативные каркасы, которые специфически связывают неоантиген множественной миеломы или комплекс неоантиген множественной миеломы/HLA, можно использовать для обнаружения, доставки полезной нагрузки или уничтожения клеток, которые экспрессируют неоантиген множественной миеломы на своей поверхности в контексте, или на более крупном белке, или в комплексе с HLA, или обнаружения внутриклеточных неоантигенов множественной миеломы после лизиса клеток.
В некоторых вариантах осуществления иммуноконъюгат содержит выявляемую метку.
В некоторых вариантах осуществления иммуноконъюгат дополнительно содержит цитотоксический агент.
В некоторых вариантах осуществления иммуноконъюгат содержит терапевтическое средство.
Обнаруживаемые метки включают в себя композиции, которые можно визуализировать с помощью спектроскопических, фотохимических, биохимических, иммунохимических или химических средств. Обнаруживаемые метки могут также включать цитотоксические агенты, цитотоксические агенты могут включать обнаруживаемые метки.
Примеры выявляемых меток включают радиоактивные изотопы, магнитные гранулы, металлические гранулы, коллоидные частицы, флуоресцентные красители, электроноплотные реагенты, ферменты (например, широко используемые в иммуноферментном анализе (ИФА)), биотин, дигоксигенин, гаптены, люминисцентные молекулы, хемилюминесцентные молекулы, флуорохромы, флуорофоры, гасящие флуоресценцию агенты, цветные молекулы, радиоактивные изотопы, сцинтиллирующие средства, авидин, стрептавидин, протеин А, протеин G, антитела или их фрагменты, полигистидин, Ni2+, Flag-теги, myc-теги, тяжелые металлы, ферменты, щелочную фосфатазу, пероксидазу, люциферазу, доноры/акцепторы электронов, сложные эфиры акридиния и колориметрические субстраты.
Выявляемая метка может испускать сигнал спонтанно, например, когда выявляемая метка представляет собой радиоактивный изотоп. В других случаях выявляемая метка испускает сигнал в результате стимуляции внешним полем.
Примерами радиоактивных изотопов могут быть γ-излучающие, Оже-электрон-излучающие, β-излучающие, альфа-излучающие или позитрон-излучающие радиоактивные изотопы. К примерам радиоактивных изотопов относятся 3Н, 11С, 13С, 15N, 18F, 19F, 55Со, 57Со, 60Со, 61Cu, 62Cu, 64Cu, 67Cu, 68Ga, 72As, 75Br, 86Y, 89Zr, 90Sr, 94mTc, 99mTc, 115In, 1231, 1241, 125I, 1311, 211At, 212Bi, 213Bi, 223Ra, 226Ra, 225Ac и 227Ac.
К примерам атомов металлов относятся металлы с атомным номером более 20, например атомы кальция, атомы скандия, атомы титана, атомы ванадия, атомы хрома, атомы марганца, атомы железа, атомы кобальта, атомы никеля, атомы меди, атомы цинка, атомы галлия, атомы германия, атомы мышьяка, атомы селена, атомы брома, атомы криптона, атомы рубидия, атомы стронция, атомы иттрия, атомы циркония, атомы ниобия, атомы молибдена, атомы технеция, атомы рутения, атомы родия, атомы палладия, атомы серебра, атомы кадмия, атомы индия, атомы олова, атомы сурьмы, атомы теллура, атомы йода, атомы ксенона, атомы цезия, атомы бария, атомы лантана, атомы гафния, атомы тантала, атомы вольфрама, атомы рения, атомы осмия, атомы иридия, атомы платины, атомы золота, атомы ртути, атомы таллия, атомы свинца, атомы висмута, атомы франция, атомы радия, атомы актиния, атомы церия, атомы празеодима, атомы неодима, атомы прометия, атомы самария, атомы европия, атомы гадолиния, атомы тербия, атомы диспрозия, атомы гольмия, атомы эрбия, атомы туллия, атомы иттербия, атомы лютеция, атомы тория, атомы протактиния, атомы урана, атомы нептуния, атомы плутония, атомы америция, атомы кюрия, атомы берклия, атомы калифорния, атомы эйнштейния, атомы фермия, атомы менделевия, атомы нобелия или атомы лоуренсия.
В некоторых вариантах осуществления атомы металла могут представлять собой щелочноземельные металлы с атомным номером более двадцати.
В некоторых вариантах осуществления атомы металлов могут представлять собой лантаниды.
В некоторых вариантах осуществления атомы металлов могут представлять собой актиниды.
В некоторых вариантах осуществления атомы металла могут представлять собой переходные металлы.
В некоторых вариантах осуществления атомы металла могут представлять собой постпереходные металлы.
В некоторых вариантах осуществления атомы металла могут представлять собой атомы золота, атомы висмута, атомы тантала и атомы гадолиния.
В некоторых вариантах осуществления атомы металла могут представлять собой металлы с атомным номером от 53 (т.е. йод) до 83 (т.е. висмут).
В некоторых вариантах осуществления атомы металла могут представлять собой атомы, приемлемые для магнитно-резонансной томографии.
Атомы металлов могут представлять собой ионы металлов со степенью окисления +1, +2, +3, например Ва2+, Bi3+, Cs+, Са2+, Cr2+, Cr3+, Cr6+, Со2+, Со3+, Cu+, Cu2+, Cu3+, Ga3+, Gd3+, Au+, Au3+, Fe2+, Fe3+, F3+, Pb2+, Mn2+, Mn3+, Mn4+, Mn7+, Hg2+, Ni2+, Ni3+, Ag+, Sr2+, Sn2+, Sn4+ и Zn2+. Атомы металлов могут включать оксид металла, такой как оксид железа, оксид марганца или оксид гадолиния.
Приемлемые красители включают любые коммерчески доступные красители, такие как, например, 5(6)-карбоксифлуоресцеин, малеимид IRDye 680RD или IRDye 800CW, красители на основе комплекса рутений/полипиридил и т.п.
К приемлемым флуорофорам относятся флуоресцеин изотиоцианат (FITC), флуоресцеин тиосемикарбазид, родамин, Texas Red, красители CyDye (например, Су3, Су5, Су5.5), красители Alexa Fluor (например, Alexa488, Alexa555, Alexa594; Alexa647), флуоресцентные красители ближнего ИК-диапазона (NIR) (700-900 нм) и карбоцианиновые и аминостирильные красители.
Иммуноконъюгаты, содержащие выявляемую метку, можно использовать в качестве агента для визуализации.
В некоторых вариантах осуществления цитотоксический агент представляет собой химиотерапевтический препарат, лекарственное средство, ингибирующий рост агент, токсин (например, токсин бактериального, грибкового, растительного или животного происхождения, обладающий ферментативной активностью, или его фрагменты) или радиоактивный изотоп (т.е. радиоактивный конъюгат).
В некоторых вариантах осуществления цитотоксический агент представляет собой дауномицин, доксорубицин, метотрексат, виндезин, бактериальные токсины, такие как дифтерийный токсин, рицин, гелданамицин, мейтансиноиды или калихеамицин. Цитотоксический агент может индуцировать цитотоксический и цитостатический эффекты посредством механизмов, включающих связывание с тубулином, связывание с ДНК или ингибирование топоизомеразы.
В некоторых вариантах осуществления цитотоксический агент представляет собой токсин с ферментативной активностью, такой как A-цепь дифтерийного токсина, несвязывающие активные фрагменты дифтерийного токсина, А-цепь экзотоксина (из Pseudomonas aeruginosa), A-цепь рицина, A-цепь абрина, А-цепь модецина, альфа-сарцин, белки Aleurites fordii, диантиновые белки, белки Phytolaca americana (PAPI, PAPII и PAP-S), ингибитор momordica charantia, курцин, кротин, ингибитор sapaonaria officinali, гелонин, митогеллин, рестриктоцин, феномицин, эномицин и трикотецены.
В некоторых вариантах осуществления цитотоксический агент представляет собой радионуклид, такой как 212Bi, 131I, 131In, 90Y и 186Re.
В некоторых вариантах осуществления цитотоксический агент представляет собой долостатины или пептидные аналоги и производные долостатина, ауристатин или монометилауристатин фенилаланин. Примеры молекул описаны в патентах США №5635483 и 5780588. Показано, что долостатины и ауристатины блокируют динамику микротрубочек, гидролиз ГТФ и деление ядра и клетки (Woyke et al (2001) Antimicrob Agents and Chemother. 45(12):3580-3584) и обладают противораковой и противогрибковой активностью. Функциональная группа лекарственного препарата долостатина или ауристатина может быть присоединена к антителу по изобретению, посредством N (амино) конца или С (карбоксильного) конца функциональной группы пептидного лекарственного средства (WO 02/088172) или посредством любого цистеина, искусственно внедренного в антитело.
Иммуноконъюгаты можно получать, используя известные методы.
В некоторых вариантах осуществления выявляемая метка находится в комплексе с хелатирующим агентом.
Выявляемая метка, цитотоксический агент или терапевтическое средство могут быть связаны непосредственно или опосредованно через линкер с полипептидами, гетерологичными полипептидами или белковыми молекулами, которые связываются с полипептидами или гетерологичными полипептидами. Подходящие линкеры известны в данной области техники и включают, например, простетические группы, нефенольные линкеры (производные N-сукцинимидилбензоатов; додекарборат), хелатирующие группы как макролитических, так и ациклических хелаторов, например производные 1,4,7,10-тетраазациклододекан-1,4,7,10,-тетрауксусной кислоты (DOTA), производные диэтилентриаминпентауксусной кислоты (DTPA), производные S-2-(4-изотиоцианатобензил)-1,4,7-триазациклононан-1,4,7-триуксусной кислоты (NOTA) и производные 1,4,8,11-тетраазациклододекан-1,4,8,11-тетрауксусной кислоты (ТЕТА), N-сукцинимидил-3-(2-пиридилдитиол) пропионат (SPDP), иминотиолан (IT), дифункциональные производные сложных имидоэфиров (такие как диметиладипимидат HCl), активные сложные эфиры (такие как дисукцинимидил суберат), альдегиды (такие как глутаральдегид), бис-азидные соединения (такие как бис-(п-азидобензоил)гександиамин), производные бис-диазония (такие как бис-(п-диазонийбензоил)этилендиамин), диизоцианаты (такие как толуол 2,6-диизоцианат) и бис-активные фтористые соединения (такие как 1,5-дифтор-2,4-динитробензол) и другие хелатирующие группы. Подходящие пептидные линкеры хорошо известны.
Способы лечения, применения и введения любой из композиций, описанных в настоящем документе
В данном документе предусмотрены способы лечения субъекта композициями, раскрытыми в данном документе. Предложенные в данном документе способы включают введение композиции, включающей любые полинуклеотиды, полипептиды, векторы и рекомбинантные вирусы в соответствии с настоящим описанием. Композиция, включающая полинуклеотиды, полипептиды, векторы, рекомбинантные вирусы, а также режимы введения в соответствии с настоящим описанием могут быть использованы для лечения, предотвращения или снижения риска клинического состояния.
В некоторых вариантах осуществления клиническое состояние представляет собой множественную миелому.
«Множественная миелома» относится к злокачественному заболеванию плазмоцитов, характеризующемуся неконтролируемой и прогрессирующей пролиферацией одного или более злокачественных плазмоцитов. Нормальная пролиферация клеток плазмы (миеломы) вызывает вытеснение нормального костного мозга, что приводит к дисфункции в гематопоэтических тканях и разрушении архитектуры костного мозга, что приводит к прогрессирующей заболеваемости и возможной смертности.
У большинства пациентов множественная миелома развивается из предзлокачественных, бессимптомных нарушений плазмоцитов, таких как моноклональная гаммопатия неясного генеза (MGUS) не IgM типа или тлеющая множественная миелома (SMM), которые характеризуются пролиферацией моноклональных плазмоцитов в костном мозге и отсутствием поражения конечных органов, таких как почечная недостаточность, анемия и литические поражения костной ткани. Тлеющая множественная миелома составляет от 13% до 15% всех пациентов с миеломами и прогрессирует до симптоматической множественной миеломы со скоростью 10% в год в течение первых 5 лет, снижаясь до 3% в год в течение следующих 5 лет.
В некоторых вариантах осуществления множественная миелома представляет собой моноклональную гаммопатию неясного генеза (MGUS) не IgM типа или тлеющую множественную миелому (SMM).
В некоторых вариантах осуществления множественная миелома представляет собой вновь выявленную множественную миелому.
В некоторых вариантах осуществления множественная миелома является рецидивирующей, рефрактерной или как рецидивирующей, так и рефрактерной.
В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению антителом к CD38, производным глутаминовой кислоты, ингибитором протеасом, алкилирующим агентом, ингибитором микротрубочек, леналидомидом, бортезомибом, помалидомидом, карфилзомибом, элотузумабом, иксазомибом, мелфаланом или талидомидом или любой их комбинацией.
В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению антителом к CD38. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению производным глутаминовой кислоты. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению ингибитором протеасом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению алкилирующим агентом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению агентом микротрубочек. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению леналиномидом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению бортезомибом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению помалидомидом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению карфилзомибом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению элотозумабом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению иксазомибом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению мелфаланом. В некоторых вариантах осуществления множественная миелома является рецидивирующей или рефрактерной к лечению талидомидом.
В некоторых вариантах осуществления у субъекта наблюдается множественная миелома высокого риска. Субъектов можно классифицировать как имеющих «высокий риск», если они имеют одну или более из следующих цитогенетических аномалий: t(4;14)(p16;q32), t(14;16)(q32;Q23) или del17p. В некоторых вариантах осуществления субъект с множественной миеломой высокого риска имеет одну или более хромосомных аномалий, включающих:
a. t(4;14)(p16;q32);
b. t(14;16)(q32;q23);
c. del17p;
d. t(4;14)(p16;q32) и t(14;16)(q32;q23);
e. t(4;14)(p16;q32) и del17p;
f. t(14;16)(q32;q23) и del17p; или
g. t(4;14)(p16;q32), t(14;16)(q32;q23) и del17p.
Цитогенетические аномалии можно обнаружить, например, с помощью флуоресцентной гибридизации in situ (FISH). При хромосомных транслокациях онкоген перемещается в область IgH на хромосоме 14q32, что приводит к дисрегуляции этих генов. Аномалия t(4;14)(P16;q32) включает транслокацию рецептора фактора роста фибробластов 3 (FGFR3) и белка, содержащего домен множественной миеломы SET (MMSET) (также называемого WHSC1/NSD2), а t(14;16)(q32;q23) включает транслокацию фактора транскрипции MAF C-MAF. Делеция 17р (del17p) включает утрату локуса гена р53.
В некоторых вариантах осуществления субъект ранее не проходил лечение.
В некоторых вариантах осуществления субъект получал высокодозную химиотерапию (ВДХТ) и трансплантацию стволовых клеток (ТСК).
В некоторых вариантах осуществления субъект имеет повышенный уровень моноклонального парапротеина (М-белка). Уровни М-белка также можно сравнивать с уровнями после приема высокодозной химиотерапии (ВДХТ) и трансплантации стволовых клеток (ТСК). Субъекты, страдающие множественной миеломой, соответствуют критериям CRAB (повышение уровня кальция, почечная недостаточность, анемия и костные аномалии), имеют клональные плазматические клетки костного мозга ≥10% или подтвержденную биопсией костную или экстрамедуллярную плазмоцитому, а также измеримое заболевание. Измеримое заболевание определяется как любое из следующего:
Миелома IgG: Уровень моноклонального парапротеина (М-белка) в сыворотке ≥1,0 г/дл или уровень М-белка в моче ≥200 мг/24 часа; или
Множественная миелома IgA, IgM, IgD или IgE: уровень М-белка в сыворотке ≥0,5 г/дл или уровень М-белка в моче ≥200 мг/24 ч; или
Множественная миелома легкой цепи без измеримого заболевания в сыворотке или моче: Концентрация свободных легких цепей иммуноглобулина в сыворотке ≥10 мг/дл и ненормальное соотношение свободных легких цепей иммуноглобулина каппа и лямбда.
Критерии CRAB определяют следующим образом:
• Гиперкальциемия: кальций в сыворотке >0,25 мМ/л (> 1 мг/дл) выше верхнего предела нормального диапазона [ULN] или >2,75 мМ/л (>11 мг/дл)
• Почечная недостаточность: клиренс креатинина <40 мл/мин или креатинин в сыворотке >177 мкМ/л ( >2 мг/дл)
• Анемия: гемоглобин >2 г/дл ниже нижнего предела нормального значения или гемоглобин <10 г/дл
• Очаги нарушений в костной ткани: один или более остеолитических очагов на рентгенографии скелета, КТ или ПЭТ-КТ.
Ответ на лечение может быть оценен с использованием рекомендаций по единым критериям ответа (International Uniform Response Criteria Consensus Recommendations), составленных рабочей группой по изучению миеломы International Myeloma Working Group (IMWG), как показано в таблице 1.

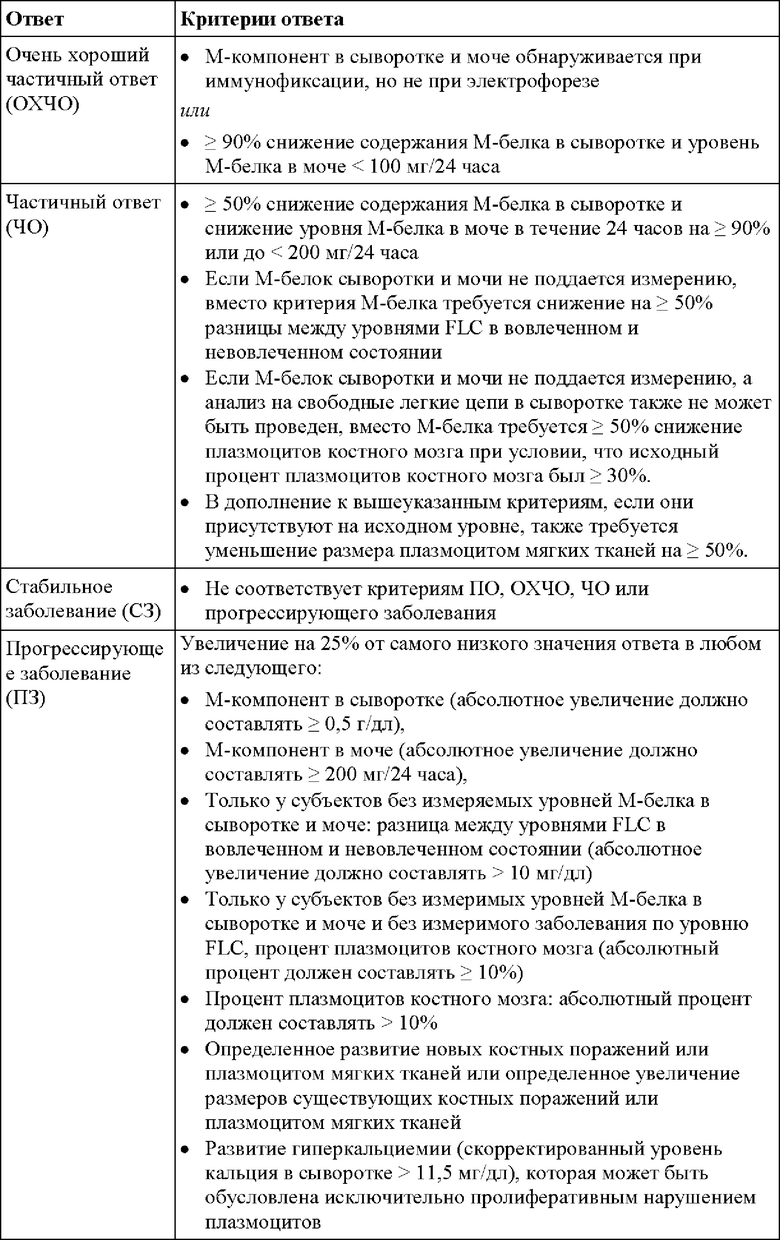

В настоящем описании предложены методы лечения, предотвращения или снижения риска возникновения множественной миеломы у субъекта, включающие введение различных композиций в соответствии с настоящим описанием, которые можно применять для введения неоантигенов множественной миеломы в соответствии с настоящим описанием субъекту, например, полинуклеотиды, гетерологичные полинуклеотиды, полипептиды, гетерологичные полипептиды, векторы, рекомбинантные вирусы и вакцины в соответствии с настоящим описанием могут применяться для лечения множественной миеломы у субъекта. Кроме того, белковые молекулы, которые связывают неоантигены множественной миеломы в соответствии с настоящим описанием, можно использовать в способах в соответствии с настоящим описанием.
В настоящем описании также предложены методы индукции иммунного ответа у субъекта, включающие введение различных композиций в соответствии с настоящим описание которые можно применять для введения раковых неоантигенов множественной миеломы в соответствии с настоящим описанием субъекту, например полинуклеотидов, гетерологичных полинуклеотидов, полипептидов, гетерологичных полипептидов, векторов, рекомбинантных вирусов и вакцин в соответствии с настоящим описанием.
В некоторых вариантах осуществления неоантигены множественной миеломы, определенные в настоящем документе, присутствуют с частотой по меньшей мере около 1% или более, около 2% или более, около 3% или более, около 4% или более, около 5% или более, около 6% или более, около 7% или более, около 8% или более, около 9% или более, около 10% или более, около 11% или более, около 12% или более, около 13% или более, около 14% или более, около 15% или более, около 16% или более, около 17% или более, около 18% или более, около 19% или более, около 20% или более, около 21% или более, около 22% или более, около 23% или более, около 24% или более, около 25% или более, около 26% или более, около 27% или более, около 28% или более, около 29% или более, около 30% или более, около 35% или более, около 40% или более, около 45% или более, около 50% или более, около 55% или более, около 60% или более, около 65% или более или около 70% или более у популяции субъектов с множественной миеломой.
В некоторых вариантах осуществления способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта, включает введение субъекту, нуждающемуся в этом, любой из композиций, представленных в настоящем документе, и при этом введение включает одно или более введений композиции.
В некоторых вариантах осуществления способ индукции иммунного ответа включает введение субъекту, нуждающемуся в этом, любой из композиций, представленных в настоящем документе, и при этом введение включает одно или более введений композиции.
В любом из описанных в данном документе способов композиция, которую вводят субъекту, может содержать рекомбинантный вирус, выбранный из аденовируса, альфавируса, поксвируса, аденоассоциированного вируса, ретровируса, или может содержать самореплицирующуюся РНК, или их комбинации.
В некоторых вариантах осуществления рекомбинантный вирус содержит раковые неоантигены множественной миеломы в соответствии с настоящим описанием, например полинуклеотиды, гетерологичные полинуклеотиды, полипептиды, гетерологичные полипептиды и векторы в соответствии с настоящим описанием.
В некоторых вариантах осуществления вирус или рекомбинантный вирус выбирают из Ad26, MVA, GAd20 и их комбинаций.
В некоторых вариантах осуществления вакцина содержит rAd26 в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rMVA в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rGAd в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rGAd20 в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rCh20 в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rAd26 в соответствии с настоящим описанием и rMVA в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит rGAd20 в соответствии с настоящим описанием и rMVA в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит самореплицирующуюся молекулу РНК в соответствии с настоящим описанием и rMVA в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит гетерологичный полипептид в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит гетерологичный полинуклеотид в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит полинуклеотид в соответствии с настоящим описанием.
В некоторых вариантах осуществления композиция содержит полипептид в соответствии с настоящим описанием.
Второе введение
В некоторых вариантах осуществления раскрытые в данном документе способы включают одно или несколько введений композиций, представленных в изобретении. Например, способ включает первое введение, за которым следует второе введение, с периодом времени между двумя введениями.
В некоторых вариантах осуществления первое введение и второе введение могут включать одинаковые или разные композиции. Например, первое введение может включать композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов в соответствии с настоящим описанием, или их комбинацию. В некоторых вариантах осуществления второе введение может содержать композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов в соответствии с настоящим описанием, или их комбинацию.
В некоторых вариантах осуществления первое введение и второе введение осуществляют один раз в жизни субъекта. В некоторых вариантах осуществления первое введение и второе введение осуществляют два или более раз в течение жизни субъекта.
В некоторых вариантах осуществления период времени между первым введением и вторым введением составляет от около 1 недели до около 2 недель, от около 1 недели до около 4 недель, от около 1 недели до около 6 недель, от около 1 недели до около 8 недель, от около 1 недели до около 12 недель, от около 1 недели до около 20 недель, от около 1 недели до около 24 недель или от около 1 недели до около 52 недель.
В некоторых вариантах осуществления период времени между первым введением и вторым введением составляет около 2 недель, около 3 недель, около 4 недель, около 5 недель, около 6 недель, около 7 недель, около 8 недель, около 9 недель, около 10 недель, около 11 недель, около 12 недель, около 13 недель, около 14 недель, около 15 недель, около 16 недель, около 17 недель, около 18 недель, около 19 недель, около 20 недель, около 21 недель, около 22 недель, около 23 недель, около 24 недель, около 25 недель, около 26 недель, около 27 недель, около 28 недель, около 29 недель, около 30 недель, около 31 недель, около 32 недель, около 33 недель, около 34 недель, около 35 недели, около 36 недель, около 37 недель, около 38 недель, около 39 недель, около 40 недель, около 41 недели, около 42 недель, около 43 недель, около 44 недель, около 45 недель, около 46 недель, около 47 недель, около 48 недель, около 49 недель, около 50 недель, около 51 недели или около 52 недель.
В некоторых вариантах осуществления период времени между первым введением и вторым введением составляет около 2 недель.
В некоторых вариантах осуществления период времени между первым введением и вторым введением составляет около 4 недель.
В некоторых вариантах осуществления первое введение и второе введение составляют цикл, и схема лечения может включать два или более циклов, причем каждый цикл разнесен на около 1 месяц, на около 2 месяца, на около 3 месяца, на около 4 месяца, на около 5 месяцев, на около 6 месяцев, на около 7 месяцев, на около 8 месяцев, на около 9 месяцев, на около 10 месяцев, на около 11 месяцев или на около 12 месяцев.
Представленные ниже примеры приведены для дополнительного описания некоторых из описанных в данном документе вариантов осуществления данного изобретения. Целью примеров является иллюстрация, а не ограничение описанных вариантов осуществления. В некоторых вариантах осуществления первое введение и второе введение могут включать любую комбинацию рекомбинантного вируса или самореплицирующейся молекулы РНК, представленной в таблице 2, включающей полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, или любую их комбинацию.
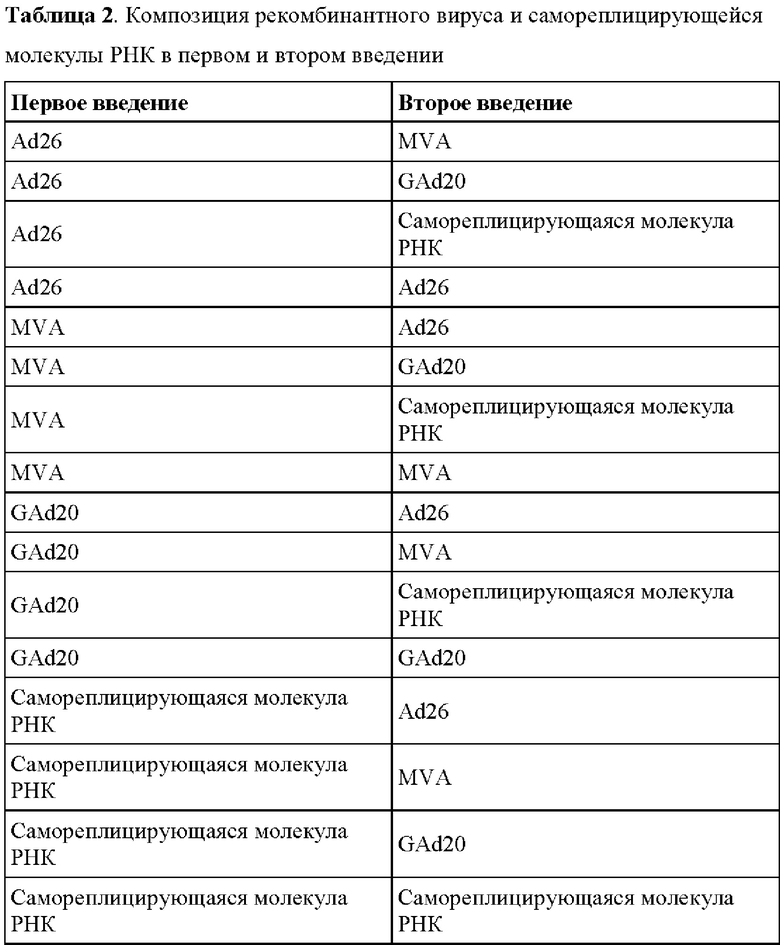
В некоторых вариантах осуществления первое введение и второе введение могут включать полинуклеотид, кодирующий любой полипептид в соответствии с настоящим описанием или их комбинацию. В некоторых вариантах осуществления первое введение и второе введение могут включать полинуклеотид, кодирующий любой полипептид, выбранный из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их комбинаций. В некоторых вариантах осуществления первое введение и второе введение могут включать полинуклеотид, кодирующий два или более тандемных повторов любых полипептидов в соответствии с настоящим описанием.
В некоторых вариантах осуществления первое введение и второе введение могут включать различные рекомбинантные вирусы.
В некоторых вариантах осуществления первое и второе введение включают рекомбинантный вирус, содержащий полинуклеотид, кодирующий полипептид с различной аминокислотной последовательностью.
В некоторых вариантах осуществления способ индукции иммунного ответа или способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения множественной миеломы у субъекта включает цикл лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, или их комбинацию, причем вирус или рекомбинантный вирус выбирают из Ad26, MVA, GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой полипептид в соответствии с настоящим описанием, или их комбинацию, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20.
Третье введение
В некоторых вариантах осуществления любой из способов, раскрытых в данном документе, может дополнительно включать третье введение. Например, способ может включать первое введение, второе введение, за которым следует третье введение, с периодом времени между каждым введением.
В некоторых вариантах осуществления первое введение, второе введение и третье введение могут содержать одинаковые или разные композиции. Например, первое введение может включать композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов композиции или их комбинацию. В некоторых вариантах осуществления второе введение может включать рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов композиции или их комбинацию. В некоторых вариантах осуществления третье введение может включать композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов композиции или их комбинацию.
В некоторых вариантах осуществления первое введение, второе введение и третье введение включают композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20, MVA или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их комбинаций.
В некоторых вариантах осуществления первое, второе или третье введение включают полинуклеотид, кодирующий два или более тандемных повторов любых полипептидов в соответствии с настоящим описанием.
В некоторых вариантах осуществления первое, второе или третье введение могут включать различный рекомбинантный вирус.
В некоторых вариантах осуществления первое, второе или третье введение могут включать рекомбинантный вирус, содержащий полинуклеотид, кодирующий полипептид с различной аминокислотной последовательностью.
Например, первое введение может включать полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их комбинаций. В некоторых вариантах осуществления второе введение может включать полинуклеотид, содержащий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их комбинации. В некоторых вариантах осуществления третье введение может включать полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, а также их комбинаций.
В некоторых вариантах осуществления первое введение, второе введение и третье введение вводят один раз в течение жизни субъекта. В некоторых вариантах осуществления первое, второе и третье введение вводят два или более раз в течение жизни субъекта.
В некоторых вариантах осуществления период времени между вторым введением и третьим введением составляет от около 1 недели до около 2 недель, от около 1 недели до около 4 недель, от около 1 недели до около 6 недель, от около 1 недели до около 8 недель, от около 1 недели до около 12 недель, от около 1 недели до около 20 недель, от около 1 недели до около 24 недель или от около 1 недели до около 52 недель.
В некоторых вариантах осуществления период времени между вторым введением и третьим введением составляет около 2 недель, около 3 недель, около 4 недель, около 5 недель, около 6 недель, около 7 недель, около 8 недель, около 9 недель, около 10 недель, около 11 недель, около 12 недель, около 13 недель, около 14 недель, около 15 недель, около 16 недель, около 17 недель, около 18 недель, около 19 недель, около 20 недель, около 21 недель, около 22 недель, около 23 недель, около 24 недель, около 25 недель, около 26 недель, около 27 недель, около 28 недель, около 29 недель, около 30 недель, около 31 недель, около 32 недель, около 33 недель, около 34 недель, около 35 недели, около 36 недель, около 37 недель, около 38 недель, около 39 недель, около 40 недель, около 41 недели, около 42 недель, около 43 недель, около 44 недель, около 45 недель, около 46 недель, около 47 недель, около 48 недель, около 49 недель, около 50 недель, около 51 недели или около 52 недель.
В некоторых вариантах осуществления период времени между вторым введением и третьим введением составляет около 6 недель.
В некоторых вариантах осуществления период времени между вторым введением и третьим введением составляет около 8 недель.
В некоторых вариантах осуществления первое введение, второе введение и третье введение вместе составляют цикл, и схема лечения может включать два или более циклов, причем каждый цикл разнесен на около 1 месяц, на около 2 месяца, на около 3 месяца, на около 4 месяца, на около 5 месяцев, на около 6 месяцев, на около 7 месяцев, на около 8 месяцев, на около 9 месяцев, на около 10 месяцев, на около 11 месяцев или на около 12 месяцев.
Представленные ниже примеры приведены для дополнительного описания некоторых из описанных в данном документе вариантов осуществления. Первое, второе и третье введение, используемые в способах, описанных в данном документе, могут включать любую комбинацию эпитопов и композиций, представленных в таблице 3.
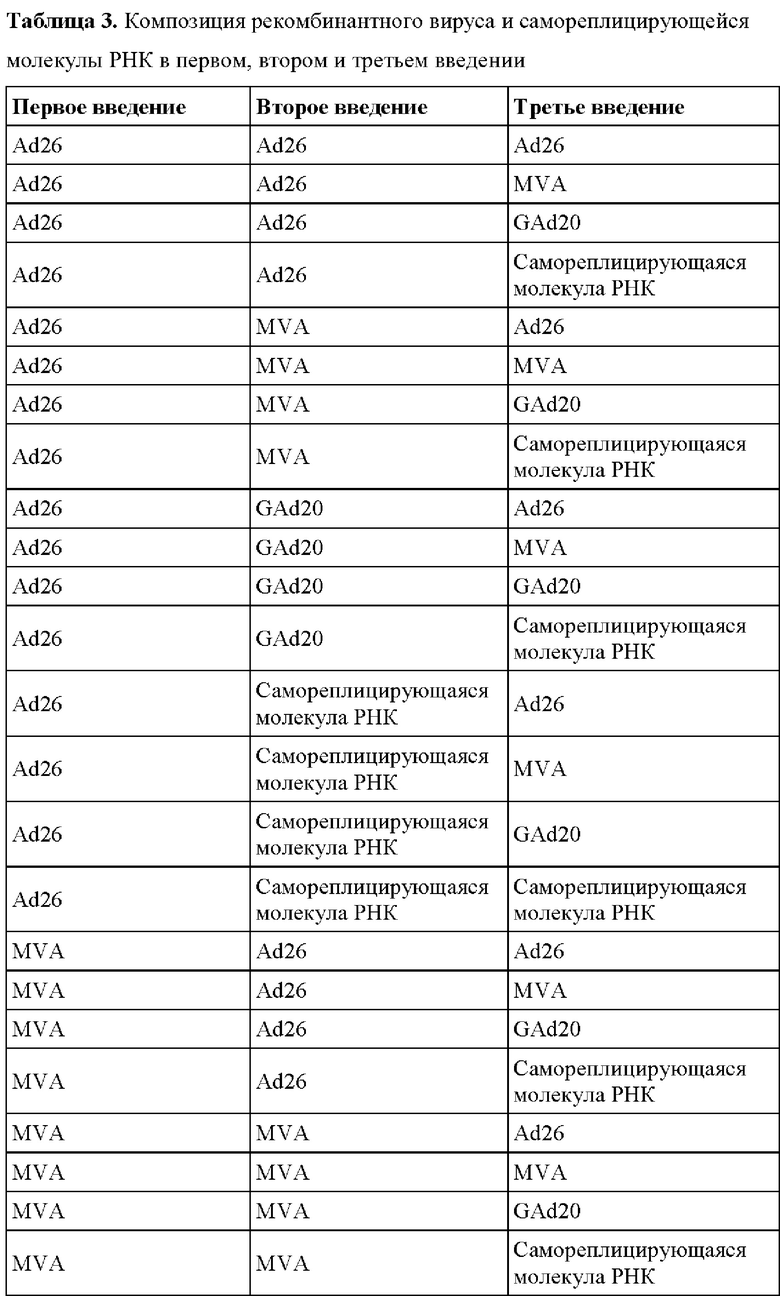
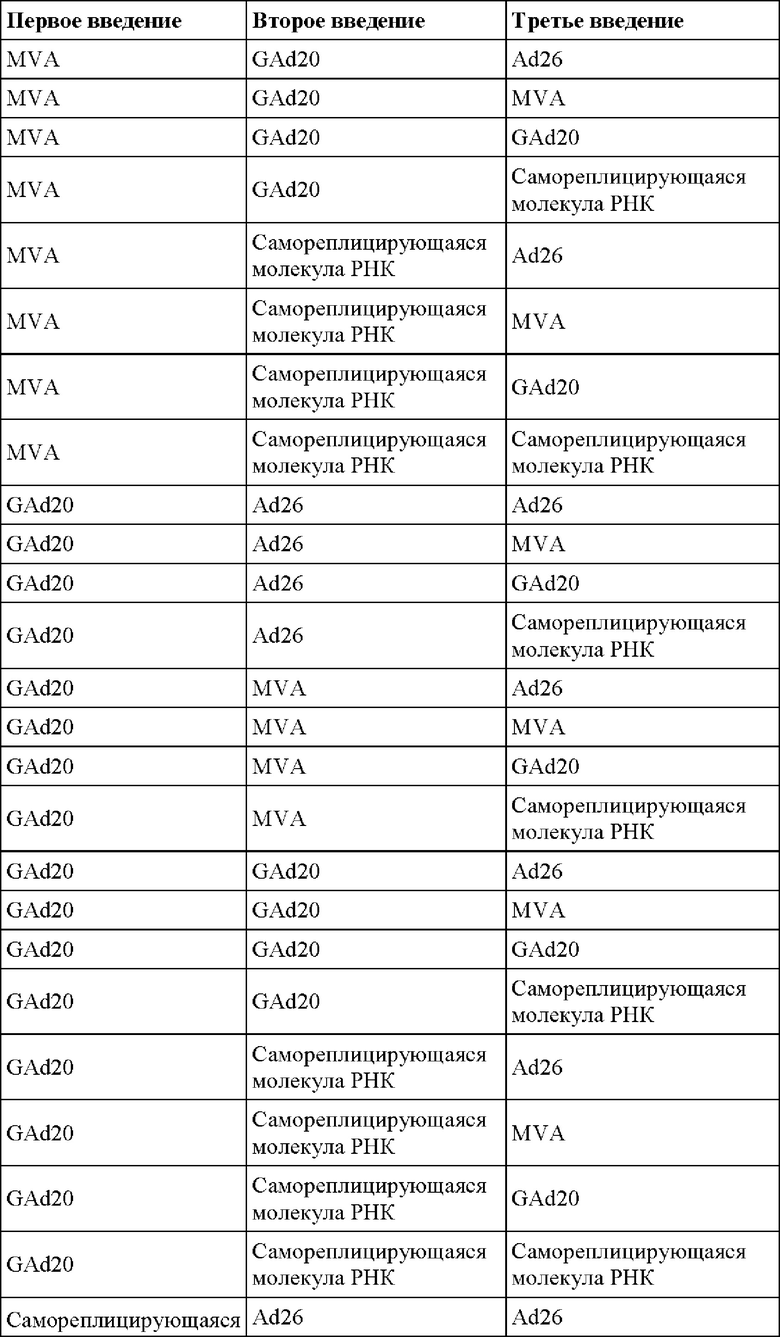
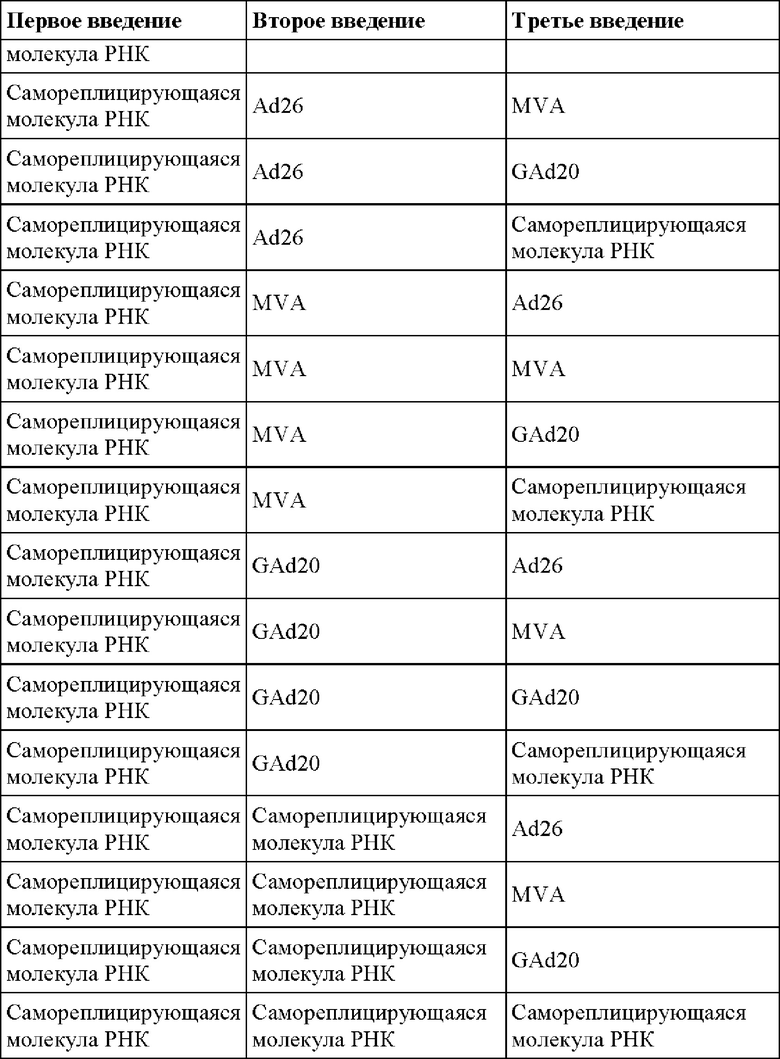
В некоторых вариантах осуществления способ индукции иммунного ответа или способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения множественной миеломы у субъекта включает цикл лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20; и
третье введение, включающее третью композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20.
Четвертое введение
В некоторых вариантах осуществления любой из способов, раскрытых в данном документе, может дополнительно включать четвертое введение. Например, способ может включать первое введение, второе введение, третье введение и четвертое введение с периодом времени между каждым введением. В некоторых вариантах осуществления первое введение, второе введение, третье введение и четвертое введение могут включать одинаковые или разные композиции.
Например, четвертое введение может включать композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, кодирующую один или более полипептидов в соответствии с настоящим описанием.
В некоторых вариантах осуществления первое введение, второе введение, третье введение и четвертое введение включают композицию, содержащую рекомбинантный вирус, выбранный из Ad26, GAd20 или MVA, или самореплицирующуюся молекулу РНК, кодирующую один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385, и 421, а также их комбинаций.
В некоторых вариантах осуществления первое, второе, третье или четвертое введение включают полинуклеотид, кодирующий два или более тандемных повторов любых полипептидов в соответствии с настоящим описанием.
В некоторых вариантах осуществления первое, второе, третье или четвертое введение могут включать различный рекомбинантный вирус.
В некоторых вариантах осуществления первое, второе, третье или четвертое введение могут включать рекомбинантный вирус, содержащий полинуклеотид, кодирующий полипептид с различной аминокислотной последовательностью.
В некоторых вариантах осуществления первое введение, второе введение, третье введение и четвертое введение осуществляют один раз в течение жизни субъекта. В некоторых вариантах осуществления первое, второе, третье и четвертое введение вводят два или более раз в течение жизни субъекта.
В некоторых вариантах осуществления период времени между третьем введением и четвертым введением составляет от около 1 недели до около 2 недель, от около 1 недели до около 4 недель, от около 1 недели до около 6 недель, от около 1 недели до около 8 недель, от около 1 недели до около 12 недель, от около 1 недели до около 20 недель, от около 1 недели до около 24 недель или от около 1 недели до около 52 недель.
В некоторых вариантах осуществления период времени между третьим введением и четвертым введением составляет около 2 недель, около 3 недель, около 4 недель, около 5 недель, около 6 недель, около 7 недель, около 8 недель, около 9 недель, около 10 недель, около 11 недель, около 12 недель, около 13 недель, около 14 недель, около 15 недель, около 16 недель, около 17 недель, около 18 недель, около 19 недель, около 20 недель, около 21 недель, около 22 недель, около 23 недель, около 24 недель, около 25 недель, около 26 недель, около 27 недель, около 28 недель, около 29 недель, около 30 недель, около 31 недель, около 32 недель, около 33 недель, около 34 недель, около 35 недели, около 36 недель, около 37 недель, около 38 недель, около 39 недель, около 40 недель, около 41 недели, около 42 недель, около 43 недель, около 44 недель, около 45 недель, около 46 недель, около 47 недель, около 48 недель, около 49 недель, около 50 недель, около 51 недели или около 52 недель.
В некоторых вариантах осуществления период времени между третьим введением и четвертым введением составляет около 4 недель.
В некоторых вариантах осуществления период времени между третьим введением и четвертым введением составляет около 8 недель.
В некоторых вариантах осуществления первое введение, второе введение, третье введение и четвертое введение вместе составляют цикл, и схема лечения может включать два или более циклов, причем каждый цикл разнесен на около 1 месяц, на около 2 месяца, на около 3 месяца, на около 4 месяца, на около 5 месяцев, на около 6 месяцев, на около 7 месяцев, на около 8 месяцев, на около 9 месяцев, на около 10 месяцев, на около 11 месяцев или на около 12 месяцев.
В некоторых вариантах осуществления способ индукции иммунного ответа или способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения множественной миеломы у субъекта включает цикл лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20; и
третье введение, включающее третью композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20, или самореплицирующейся молекулы РНК; и
четвертое введение, включающее четвертую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов в соответствии с настоящим описанием, причем рекомбинантный вирус выбирают из Ad26, MVA, GAd20.
Введение поддерживающей терапии
В некоторых вариантах осуществления способ дополнительно включает введение субъекту композиции через равные промежутки времени в течение циклов лечения и может продолжаться даже после окончания циклов лечения. Например, композицию можно вводить субъекту каждый месяц в течение схемы лечения и можно продолжать в течение дополнительных 6 месяцев. В некоторых вариантах осуществления композицию можно вводить между двумя циклами лечения. В некоторых вариантах осуществления композиция может представлять собой любую из композиций, раскрытых в данном документе, например, композицию, содержащую вектор, выбранный из вектора Ad26, вектора GAd20, вектора MVA или самореплицирующейся молекулы РНК, кодирующей последовательности эпитопа.
Доза и способ введения
Композиции в соответствии с настоящим описанием можно вводить субъекту различными способами, такими как подкожный, местный, пероральный и внутримышечный. Введение композиций можно осуществлять перорально или парентерально. Способы парентеральной доставки включают местное, внутриартериальное (непосредственно в ткани), внутримышечное, внутридермальное, подкожное, интрамедуллярное, подоболочечное, внутрижелудочковое, внутривенное, внутрибрюшинное или интраназальное введение. Настоящее изобретение также имеет целью обеспечение подходящих местных, пероральных, системных и парентеральных составов для применения в способах профилактики и лечения.
В некоторых вариантах осуществления внутримышечное введение вакцины может быть выполнено с помощью иглы. Альтернативным вариантом является применение инъекционного устройства без иглы для введения композиции (с использованием, например, BiojectorTM) или сублимированного порошка композиции агента.
Для внутривенной, кожной или подкожной инъекции или инъекции в пораженное место композиция вакцины может находиться в форме приемлемого для парентерального введения водного раствора, который не содержит пирогенов и имеет приемлемый рН, изотоничность и стабильность. Специалисты в данной области легко могут получить приемлемые растворы, используя, например, изотонические несущие среды, такие как инъекция хлорида натрия, инъекция раствора Рингера, инъекция раствора Рингера с лактатом. При необходимости можно включить консерванты, стабилизаторы, буферы, антиоксиданты и/или другие добавки. Можно также использовать состав с медленным высвобождением.
Как правило, введение будет иметь профилактическую цель формирования иммунного ответа против неоантигенов множественной миеломы до развития симптомов множественной миеломы.
Композиции по настоящему описанию вводят субъекту, что приводит к иммунному ответу у субъекта. Количество вакцины, способное вызывать обнаруживаемый иммунный ответ, определяется как «иммунологически эффективная доза». Композиции по настоящему описанию могут индуцировать гуморальный, а также клеточно-опосредованный иммунный ответ. В типичном варианте осуществления иммунный ответ представляет собой защитный иммунный ответ.
В некоторых вариантах осуществления способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта, включает введение субъекту терапевтически эффективного количества одной или более вакцин в соответствии с настоящим описанием.
В некоторых вариантах осуществления способы лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта включают введение субъекту терапевтически эффективного количества одной или более композиций в соответствии с настоящим описанием.
В некоторых вариантах осуществления способ формирования иммунного ответа у субъекта включает введение субъекту иммунологически терапевтически эффективного количества одной или более композиций в соответствии с настоящим описанием.
В некоторых вариантах осуществления способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта включает введение субъекту терапевтически эффективного количества вакцины или композиции, содержащей полинуклеотид, кодирующий один или более полипептидов SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, тем самым обеспечивая лечение, предотвращение, снижение риска возникновения или отсрочку возникновения клинического состояния множественной миеломы у субъекта, при этом введение включает одно или несколько введений композиции.
В любом из описанных в данном документе способов композиция, которую вводят субъекту, может содержать рекомбинантный вирус, выбранный из аденовируса, альфавируса, поксвируса, аденоассоциированного вируса, ретровируса, или может содержать самореплицирующуюся РНК, или их комбинации.
В некоторых вариантах осуществления субъект предположительно имеет или предположительно у субъекта может развиться множественная миелома.
Фактическое вводимое количество, а также скорость и динамика введения будут зависеть от характера и тяжести объекта лечения. Назначения лечения, например, решение о дозировке и т.д., находятся в пределах ответственности врачей общей практики и других медицинских специалистов и, как правило, учитывают расстройство, подлежащее лечению, состояние конкретного пациента, место доставки, способ введения и другие известные медработникам факторы.
В некоторых вариантах осуществления композиции, содержащие рекомбинантный аденовирус, вводят в дозе от около 1×104 IFU (инфекционных единиц) до около 1×1012 IFU на дозу, от около 1×104 IFU до около 1×1011 IFU на дозу, от около 1×104 IFU до около 1×1010 IFU на дозу, от около 1×104 IFU до около 1×109 IFU на дозу, от около 1×104 IFU до около 1×108 IFU на дозу или от около 1×104 IFU до около 1×106 IFU на дозу.
В некоторых вариантах осуществления композиции, содержащие рекомбинантный аденовирус, вводят в дозе от около 1×106 VP (вирусных частиц) до около 1×1014 VP на дозу, от около 1×106 VP до около 1×1012 VP на дозу, от около 1×106 VP до около 1×1010 VP на дозу, от около 1×106 VP до около 1×108 VP на дозу или от около 1×106 VP до около 1×107 VP на дозу.
В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус Ad26, вводят в дозе около 1×1010IFU. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус Ad26, вводят в дозе около 1×1011 IFU. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус Ad26, вводят в дозе около 1×1010 VP. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус Ad26, вводят в дозе около 1×1011 VP.
В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус GAd20, вводят в дозе около 1×108 IFU. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус GAd20, вводят в дозе около 1×1010 IFU. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус GAd20, вводят в дозе около 1×1010 VP. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус GAd20, вводят в дозе около 1×1011 VP.
В некоторых вариантах осуществления композиции, содержащие рекомбинантный поксвирус, вводят в дозе от около 1×104 IFU (инфекционных единиц) до около 1×1012 IFU на дозу, от около 1×104 IFU до около 1×1011 IFU на дозу, от около 1×104 IFU до около 1×1010 IFU на дозу, от около 1×104 IFU до около 1×109 IFU на дозу, от около 1×104 IFU до около 1×108 IFU на дозу или от около 1×104 IFU до около 1×106 IFU на дозу.
В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус MVA, вводят в дозе около 1×10 IFU. В некоторых вариантах осуществления композицию, содержащую рекомбинантный вирус MVA, вводят в дозе около 1×1010 IFU.
В некоторых вариантах осуществления композиции, содержащие самореплицирующуюся молекулу РНК, вводят в дозе от около 1 микрограмма до около 100 микрограмм, от около 1 микрограмма до около 90 микрограмм, от около 1 микрограмма до около 80 микрограмм, от около 1 микрограмма до около 70 микрограмм, от около 1 микрограмма до около 60 микрограмм, от около 1 микрограмма до около 50 микрограмм, от около 1 микрограмма до около 40 микрограмм, от около 1 микрограмма до около 30 микрограмм, от около 1 микрограмма до около 20 микрограмм, от около 1 микрограмма до около 10 микрограмм или от около 1 микрограмма до около 5 микрограмм самореплицирующейся молекулы РНК.
В одном примере схемы лечения композицию, содержащую аденовирус, вводят (например, внутримышечно) в объеме от около 100 мкл до около 10 мл, содержащем концентрации от около 104 до 1012 вирусных частиц/мл. Аденовирусный вектор может вводиться в объеме от 0,25 до 1,0 мл, например, в объеме 0,5 мл.
Аденовирус можно вводить человеческому индивиду в количестве от около 109 до около 1012 вирусных частиц (VP) во время одного введения, более типично в количестве от около 1010 до около 1012 VP.
В одном примере схемы лечения композицию, содержащую вирус rMVA в соответствии с настоящим описанием, вводят (например, внутримышечно) в объеме, варьирующемся в диапазоне от около 100 мкл до около 10 мл физиологического раствора, содержащего дозу от около 1×107 TCID50 до 1×109 TCID50 (50%-ная инфекционная доза в тканевой культуре) или Inf.U. (Инфекционная единица). Вирус rMVA можно вводить в объеме в диапазоне от 0,25 до 1,0 мл. Композиции можно вводить два или более раз, через недели или месяцы после введения праймирующей композиции, например через от около 1, или 2 недель, или 3 недель, или 4 недель, или 6 недель, или 8 недель, или 12 недель, или 16 недель, или 20 недель, или 24 недель, или 28 недель, или 32 недель, или от одного до двух лет после первого введения первой композиции. Дополнительные введения композиций можно вводить в диапазоне от через 6 недель до 5 лет после стадии бустирования (b), например через 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 недель, или 7, 8, 9, 10, 11 или 12 месяцев, или 2, 3, 4 или 5 лет после первоначальной бустирующей инокуляции. Необязательно дополнительный этап введения (с) можно повторять один или более раз по мере необходимости.
Комбинированные терапии
Вакцины и композиции в соответствии с настоящим описанием можно использовать в комбинации с по меньшей мере одним дополнительным противораковым терапевтическим агентом для лечения множественной миеломы.
Дополнительный противораковый терапевтический агент может представлять собой химиотерапевтический агент, иммуномодулирующий агент, кортикостероид, лучевую терапию, таргетную терапию, высокодозную химиотерапию (ВДХТ) и трансплантацию стволовых клеток (ТСК), ингибитор контрольных точек, антибиотик, иммуностимулирующий агент, или клеточную терапию, или хирургическое вмешательство, или любую их комбинацию.
Примерами химиотерапевтических агентов являются ингибиторы протеасом; алкилирующие агенты; ингибиторы микротрубочек; нитрозомочевины; противоопухолевые антиметаболиты; противоопухолевые антибиотики; растительные алкилоиды; таксаны; гормональные агенты; и различные агенты, такие как бусульфан, соединение платина (например, карбоплатин, цисплатин), хлорамбуцил, циклофосфамид, дакарбазин, ифосфамид, мехлоретамина гидрохлорид, мелфалан, прокарбазин, тиотепа, урациловый иприт, 5-фторурацил, 6-меркаптопурин, капецитабин, цитозина арабинозид, флоксуридин, флударабин, гемцитабин, метотрексат, тиогуанин, дактиномицин, даунорубицин, доксорубицин, идарубицин, митомицин-С и митоксантрон, винбластин, винкристин, виндезин, винорелбин, паклитаксел, а также доцетаксел.
В некоторых вариантах осуществления химиотерапевтический агент представляет собой ингибитор протеосом.
В некоторых вариантах осуществления ингибитор протеосом представляет собой бортезомиб, карфилзомиб, маризомиб или иксазомиб или любую их комбинацию.
В некоторых вариантах осуществления химиотерапевтический агент представляет собой алкилирующий агент.
Термин «алкилирующий агент» относится к семейству алкилирующих ДНК агентов, включая циклофосфамид, ифосфамид, мелфалан или нитрозомочевины. Циклофосфамид доступен на рынке под торговым названием Cyclostin™. Ифосфамид доступен на рынке под торговым наименованием Holoxan™. Мелфалан доступен на рынке под торговым названием ALKERAN®. Нитросахары включают кармустин, ломустин и семустин. Кармустин доступен на рынке под торговым названием BiCNU. Ломустин доступен на рынке под торговым названием GLEOSTINE®.
В некоторых вариантах осуществления алкилирующий агент представляет собой мелфалан, циклофосфамид, ифосфамид или нитрозомочевину или любую их комбинацию.
В некоторых вариантах осуществления химиотерапевтический агент представляет собой ингибитор микротрубочек.
«Ингибитор микротрубочек» (MTI) относится к дестабилизирующим микротрубочки соединениям и ингибиторам полимеризации микротрубочек, включая таксаны, такие как паклитаксел и доцетаксел, алкалоиды винка, такие как винбластин или сульфат винбластина, винкристин или сульфат винкристина и винорелбин. Паклитаксел доступен на рынке под торговым названием TAXOL®. Доцетаксел доступен на рынке под торговым названием TAXOTERE. Сульфат винбластина доступен на рынке под торговым названием Vinblastin R.P™. Сульфат винкристина доступен на рынке под торговым названием Farmistin™. Дексаметазон доступен на рынке под торговым названием NAVELBINE®.
В некоторых вариантах осуществления ингибитор микротрубочек представляет собой таксан или алкалоид винка или любую их комбинацию.
В некоторых вариантах осуществления алкалоид винка представляет собой винкристин.
В некоторых вариантах осуществления химиотерапевтический агент представляет собой противоопухолевый антиметаболит.
Термин «противоопухолевый антиметаболит» включает без ограничений 5-фторурацил или 5-FU, капецитабин, гемцитабин, соединения, деметилирующие ДНК, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат, а также антагонисты фолиевой кислоты, такие как пеметрексед. Капецитабин доступен на рынке под торговым названием XELODA®. Гемцитабин доступен на рынке под торговым наименованием GEMZAR®.
Примеры иммуномодулирующих агентов включают производные глутаминовой кислоты,
Термин «производное глутаминовой кислоты» относится к иммуномодулирующим лекарственным средствам, которые являются производными глутаминовой кислоты, такие как линалидомид, талидомид и помалидомид. Леналидомид доступен на рынке под торговым названием REVLIMID®. Талидомид доступен на рынке под торговым названием THALOMID®. Помалидомид доступен на рынке под торговым названием POMALYST®.
В некоторых вариантах осуществления производное глутаминовой кислоты представляет собой леналидомид, помлидомид или талидомид или любую их комбинацию.
Примеры кортикостероидов включают дексаметазон или преднизон или любую их комбинацию.
Радиационную терапию можно проводить с помощью различных способов, включая дистанционную радиационную терапию, внутреннюю радиационную терапию, облучение с имплантатом, стереотаксическую радиохирургию, системную радиационную терапию, радиотерапию и постоянную или временную интерстициальную брахитерапию. К дистанционной радиационной терапии относятся трехмерная, конформная радиационная терапия, в которой формируется поле облучения, местное облучение (например, облучение, направленное на выбранную мишень или орган) или сфокусированное облучение. Сфокусированное облучение можно выбирать из стереотаксической радиохирургии, фракционированной стереотаксической радиохирургии или радиационной терапии с модуляцией интенсивности. В качестве источника радиации при сфокусированном облучении может использоваться пучок частиц (протоны), кобальт-60 (фотоны), линейный ускоритель (рентгеновские лучи) (например, см. WO 2012/177624). Термин «брахитерапия» относится к радиационной терапии с источником в пространственно-ограниченном радиоактивном материале, введенном в организм в или рядом с опухолью или другим местом пролиферативного заболевания ткани, и включает в себя воздействие радиоактивных изотопов (например, At-211, I-131, I-125, Y-90, Re-186, Re-188, Sm-153, Bi-212, P-32 и радиоактивных изотопов Lu). Приемлемые источники излучения для применения при кондиционировании клеток включают в себя как твердые вещества, так и жидкости. Источник излучения может представлять собой радионуклид, такой как твердые источники I-125, I-131, Yb-169, Ir-192, твердый источник I-125 или другие радионуклиды, которые испускают фотоны, бета-частицы, гамма-излучение или другие терапевтические лучи. Радиоактивный материал также может представлять собой жидкость из любого раствора радионуклида (-ов), например, раствора I-125 или I-131, или радиоактивную жидкость, которую можно получить из взвеси малых частиц приемлемых твердых радионуклидов, таких как Au-198, Y-90, в жидкости. Радионуклид (-ы) можно заключать в гель или в радиоактивные микросферы.
Таргетная терапия включает, в частности, антитела к CD38 (например, даратумумаб и элотузумаб), антитела или CAR-T к ВСМА, антитела или CAR-T к GPRC5D и антитела к SLAMF7 (например, элотузумаб).
Трансплантация стволовых клеток (ТСК) может быть аутологичной (АТСК), аллогенной или сингенной. В некоторых вариантах осуществления ТСК представляет собой АТСК.
В некоторых вариантах осуществления дополнительные терапевтические средства включают бортезомиб и дексаметазон.
В некоторых вариантах осуществления бортезомиб вводят в дозе около 1,3 мг/м2, а дексаметазон вводят в дозе около 20 мг.
В некоторых вариантах осуществления дополнительные терапевтические средства включают линалидомид и дексаметазон.
В некоторых вариантах осуществления линалидомид вводят в дозе около 25 мг, а дексаметазон вводят в дозе от около 20 мг до около 40 мг.
В некоторых вариантах осуществления дополнительные терапевтические средства включают помалидомид и дексаметазон.
В некоторых вариантах осуществления помалидомид вводят в дозе около 25 мг, а дексаметазон вводят в дозе от около 20 мг до около 40 мг.
В некоторых вариантах осуществления дополнительные терапевтические средства включают бортезомиб, мелфалан и преднизон.
В некоторых вариантах осуществления бортезомиб вводят в дозе около 1,3 мг/м2, мелфалан вводят в дозе около 9 мг/м2, а преднизон вводят в дозе около 60 мг/м2.
В некоторых вариантах осуществления дополнительные терапевтические средства включают бортезомиб, талидомид и дексаметазон.
В некоторых вариантах осуществления бортезомиб вводят в дозе около 1,3 мг/м2, талидомид вводят в дозе около 25 мг, а дексаметазон вводят в дозе от около 20 мг до около 40 мг.
В некоторых вариантах осуществления субъект подходит для высокодозной химиотерапии (ВДХТ) и трансплантации стволовых клеток (ТСК).
«Высокодозная химиотерапия» (ВДХТ) и «трансплантация аутологичных стволовых клеток» (АТСК) относятся к лечению субъектов с вновь диагностированной множественной миеломой, которые считаются подходящими для таких видов терапии (например, субъекты являются «подходящими»). Субъекты в возрасте до 65 лет, имеющие один или несколько сопутствующих заболеваний, которые могут негативно повлиять на переносимость ВДХТ и АТСК, или субъекты старше 65 лет обычно не считаются подходящими для ВДХТ и АТСК из-за их слабого физического статуса, который повышает риск смертности и осложнений, связанных с трансплантацией (например, субъекты являются «неподходящими»). Примером сопутствующего заболевания является дисфункция почек. Примерами схем ВДХТ являются мелфалан в дозе 200 мг/м площади поверхности тела со снижением дозы в зависимости от возраста и функции почек, циклофосфамид и мелфалан, кармустин, этопозид, цитарабин и мелфалан (BEAM), идарубицин в высокой дозе, циклофосфамид, тиотепа, бусульфан и циклофосфамид, бусульфан и мелфалан, а также леналидомид в высоких дозах (Mahajan et at, Ther AdvHematol 9:123-133, 2018). Циклофосфамид доступен на рынке под торговым названием Cyclostin™. Мелфалан доступен на рынке под торговым названием ALKERAN®. Кармустин доступен на рынке под торговым названием BiCNU. Этопозид доступен на рынке под торговым названием VEPESID®. Цитарабин доступен на рынке под торговым названием CYTOSAR-U®. Идарубицин доступен на рынке под торговым названием IDAMYCIN. Тиотепа доступна на рынке под торговым названием THIOPLEX®. Леналидомид доступен на рынке под торговым названием REVLIMID.
В некоторых вариантах осуществления ТСК представляет собой аутологичную ТСК (АТСК), аллогенную ТСК или сингенную ТСК.
В некоторых вариантах осуществления ТСК представляет собой АТСК.
В некоторых вариантах осуществления ВДХТ представляет собой мелфалан.
Примерами ингибиторов контрольных точек являются антагонисты PD-1, PD-L1, PD-L2, VISTA, BTNL2, В7-Н3, В7-Н4, HVEM, HHLA2, CTLA-4, LAG-3, TIM-3, BTLA, CD160, СЕАСАМ-1, LAIR1, TGFβ, IL-10, белок семейства Siglec, KIR, CD96, TIGIT, NKG2A, CD112, CD47, SIRPA или CD244. Термин «антагонист» относится к молекуле, которая при связывании с клеточным белком подавляет по меньшей мере одну реакцию или тип активности, индуцируемые естественным лигандом белка. Молекула является антагонистом, если происходит подавление по меньшей мере одной реакции или типа активности на по меньшей мере около 30%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% или 100% по сравнению с подавлением по меньшей мере одной реакции или типа активности в отсутствие антагониста (например, отрицательный контроль) или когда подавление является статистически значимым по сравнению с подавлением в отсутствие антагониста. Антагонистом может быть антитело, растворимый лиганд, малая молекула, ДНК или РНК, такая как миРНК. Примеры антагонистов ингибиторов контрольных точек описаны в патентной публикации США №2017/0121409.
В некоторых вариантах осуществления одну или более вакцин или композиций в соответствии с настоящим описанием вводят в комбинации с антителом к CTLA-4, лигандом CTLA4, ингибитором оси PD-1, ингибитором оси PD-L1, агонистом TLR, агонистом CD40, агонистом ОХ40, гидроксимочевиной, руксолитинибом, федратинибом, агонистом 41 ВВ, агонистом CD28, агонистом STING, агонистом RIG-I, терапией TCR-T, терапией CAR-T, лигандом FLT3, сульфатом алюминия, ингибитором ВТК, антителом к CD38, ингибитором CDK, антителом к CD33, антителом к CD37, антителом к CD25, ингибитором GM-CSF, IL-2, IL-15, IL-7, молекулами перенаправления CD3, помалимибом, IFNγ, IFNα, TNFα, антителом к VEGF, антителом к CD70, антителом к CD27, антителом к ВСМА, антителом к GPRC5D или любой их комбинацией.
В некоторых вариантах осуществления ингибитор контрольной точки представляет собой ипилимумаб, цетрелимаб, пембролизумаб, ниволумаб, синтилимаб, цемиплимаб, торипалимаб, камрелизумаб, тислелизумаб, достралимаб, спартализумаб, пролголимаб, AK-105, HLX-10, балстилимаб, MEDI-0680, НХ-008, GLS-010, BI-754091, генолимзумаб, АК-104, MGA-012, F-520, 609А, LY-3434172, AMG-404, SL-279252, ТСК-I10A, RO-7121661, ICTCAR-014, MEDI-5752, CS-1003, XmAb-23104, Sym-021, LZM-009, hAB21, BAT-1306, MGD-019, JTX-4014, будигалимаб, XmAb-20717, AK-103, MGD-013, IBI-318, сасанлимаб, CC-90006, авелумаб, атезолизумаб, дурвалумаб, CS-1001, бинтрафусп альфа, энвафолимаб, СХ-072, GEN-1046, GS-4224, KL-A167, BGB-A333, SHR-1316, СВТ-502, IL-103, KN-046, ZKAB-001, СА-170, TG1501, LP-002, INCB-86550, ADG-104, SHR-1701, BCD-135, IMC-001, MSB-2311, FPT-155, FAZ-053, HLX-20, йодаполимаб, FS-118, BMS-986189, АК-106, MCLA-145, IBI-318 или СК-301 или любую их комбинацию.
В некоторых вариантах осуществления одну или более вакцин или композиций в соответствии с настоящим описанием вводят в комбинации со следующими средствами: ипилимумаб, цетрелимаб, пембролизумаб, ниволумаб, синтилимаб, цемиплимаб, торипалимаб, камрелизумаб, тислелизумаб, достралимаб, спартализумаб, пролголимаб, балстилимаб, будиглимаб, сасанлимаб, авелумаб, атезолизумаб, дурвалумаб, энвафолимаб, йодаполимаб или любой их комбинацией.
В некоторых вариантах осуществления одну или более вакцин или композиций в соответствии с настоящим описанием вводят в комбинации с антителом к CTLA-4, лигандом CTLA4, ингибитором оси PD-1, ингибитором оси PD-L1, агонистом TLR, агонистом CD40, агонистом ОХ40, гидроксимочевиной, руксолитинибом, федратинибом, агонистом 41ВВ, агонистом CD28, агонистом STING, агонистом RIG-I, терапией TCR-T, терапией CAR-T, лигандом FLT3, сульфатом алюминия, ингибитором ВТК, антителом к CD38, ингибитором CDK, антителом к CD33, антителом к CD37, антителом к CD25, ингибитором GM-CSF, IL-2, IL-15, IL-7, молекулами перенаправления CD3, помалимибом, IFNγ, IFNα, TNFα, антителом к VEGF, антителом к CD70, антителом к CD27, антителом к ВСМА или антителом к GPRC5D или любой их комбинацией.
В некоторых вариантах осуществления второй терапевтический агент может вводиться в комбинации с первой композицией первого введения, или второй композицией второго введения, или третьей композицией третьего введения, или четвертой композицией четвертого введения.
В некоторых вариантах осуществления антитело к CTLA-4 комбинируют с любым из первого, или второго, или третьего, или четвертого введения композиции согласно настоящему изобретению.
В некоторых вариантах осуществления антитело к PD-1 или антитело к PD-L1 комбинируют с любым из первого, или второго, или третьего, или четвертого введения композиции согласно настоящему изобретению.
В некоторых вариантах осуществления ингибиторы контрольных точек вводят в виде дозы от около 0,5 до около 5 мг/кг, от около 5 до около 10 мг/кг, от около 10 до около 15 мг/кг, от около 15 мг/кг до около 20 мг/кг, от около 20 мг/кг до около 25 мг/кг, от 20 мг/кг до около 50 мг/кг, от около 25 мг/кг до около 50 мг/кг, от около 50 мг/кг до около 75 мг/кг, от около 50 до около 100 мг/кг, от около 75 мг/кг до около 100 мг/кг, от около 100 мг/кг до около 125 мг/кг, от около 125 до около 150 мг/кг, от около 150 до около 175 мг/кг, от около 175 мг/кг до около 200 мг/кг, от около 200 мг/кг до около 225 мг/кг, от около 225 до около 250 мг/кг или от около 250 до около 300 мг/кг.
ПРИМЕРЫ
Представленные ниже примеры приведены для дополнительного описания некоторых из описанных в данном документе вариантов осуществления. Целью примеров является иллюстрация, а не ограничение описанных вариантов осуществления.
Пример 1: Идентификация неоантигенов путем биоинформатики
Была разработана вычислительная структура для анализа различных наборов данных РНК-секвенирования множественной миеломы средствами биоинформатики с целью выявления общих неоантигенов множественной миеломы, возникающих в результате событий слияния генов, которые привели к образованию новых пептидных последовательностей, сохранению интронов, альтернативно сплайсированным вариантам, аберрантной экспрессии заглушенных развитием генов или точечным мутациям. Запрашиваемые наборы данных:
• Genotype-Tissue Expression (GTEx) Consortium. Этот набор данных включает 6137 наборов данных РНК-секвенирования из 49 нормальных тканей, которые использовали для оценки частоты кандидатов неоантигенов множественной миеломы в нормальной ткани.
• Набор данных РНК-секвенирования, специфичный для иммунных клеток. Это внутреннее исследование включало 110 наборов данных РНК-секвенирования, полученных из 20 типов иммунных клеток (Т-клеток, В-клеток, NK-клеток и миелоидных клеток), полученных от пяти здоровых доноров.
• Исследование MMRF CoMMpass (https://themmrf.org/we-are-curing-multiple-myeloma/mmrf-commpass-study/). Данное исследование охватывает 807 наборов данных РНК-секвенирования, полученных от вновь диагностированных пациентов с множественной миеломой.
• Исследование SMM 2001. Данное исследование включало 130 наборов данных РНК-секвенирования, полученных от пациентов с тлеющей множественной миеломой.
• Исследование MMY3007. Данное исследование охватывает 586 наборов данных РНК-секвенирования, полученных от пациентов, включенных в клиническое исследование даратумумаба.
• Исследование MMY3003-3004. Данное исследование охватывает 861 набор данных РНК-секвенирования, полученных от пациентов, включенных в клиническое исследование даратумумаба.
Все образцы, включенные в базу данных РНК-секвенирования (описанные выше исследования MMRF и клинические испытания), представляют собой CD138+ клетки, обогащенные из аспиратов костного мозга пациентов.
Перед анализом проводили контроль качества (КК) необработанных данных. Прочтения секвенирования сначала обрезали для удаления адаптерных последовательностей Illumina и прочтения, картированные с человеческой тРНК и рРНК, удаляли из дальнейшего анализа. Из прочтений также были отсечены распознанные основания низкого качества(<10 показатель качества Phred; обозначает основание с 1 из 10 вероятностей того, что оно будет неправильным) с обоих концов. Из наборов данных удаляли обрезанные прочтения с менее 25 пар оснований (п.о.). Кроме того, для удаления прочтений низкого качества использовали следующие этапы: удаление прочтений с максимальным базовым показателем качества менее 15, удаление прочтений со средним базовым показателем качества менее 10, удаление прочтений, имеющих степень полиАТСG >80%, удаление последовательностей РНК, в которых одно из двух прочтений не прошло испытание.
Прочтения позже было картировано по Human Genome Build 38 с использованием платформы ArrayStudio ((https_//www_omicsoft_com/array-studio/). Модель гена Refseq NCBI (дата выпуска 6 июня 2017 г.) была использована для сопоставления прочтений с известными экзонными областями генома человека.
Выявление событий слияния генов
Алгоритм FusionMap (Ge Н et al., Bioinformatics. 2011 Jul 15; 27(14):1922-8.) использовали для идентификации событий слияния генов в описанных выше наборах данных раковых клеток. FusionMap определяет места соединения слияния на основании прочтений, которые содержат положение слияния в средней области прочтений последовательностей. Затем проводили поиск возможных положений соединений слияния из консенсуса затравочных прочтений. FusionMap построил эталонный индекс на основе библиотеки псевдослияний и выровнял несопоставленные потенциальные прочтения слияний с этим псевдоэталоном. Прочтения, сопоставленные на этой стадии, рассматривали как сохраненные прочтения.
Этот алгоритм идентифицировал как химерные сквозные слияния, как показано на ФИГ. 1, так и события слияния генов, полученные в результате хромосомных транслокаций, как показано на ФИГ. 2. Событие слияния генов вызывалось в наборе данных РНК-секвенирования, когда выполнялись следующие критерии: по меньшей мере два затравочных прочтения с разной позицией картирования в геноме, по меньшей мере четыре затравочных и сохраненных прочтения, поддерживающих соединение слияния, и по меньшей мере одна пара прочтений, перекрывающих соединение. События слияния генов, происходящие из пар генов, имеющих высокое сходство последовательностей (ортологи и семейства белков), не учитывались при последующем анализе.
Общие неоантигены, происходящие из событий слияния генов, были идентифицированы с использованием следующих критериев: частота событий слияния генов в когорте больных должна была превышать 5%, встречаемость события слияния генов должна была составлять менее 1% во всем наборе данных GTEx с использованием более мягкого критерия (по крайней мере 2 затравочных прочтения и одно перекрывающее соединение прочтение) и встречаемость события слияния генов должна была составлять <=2 наборам данных РНК-секвенирования, полученным из нормальных типов иммунных клеток. Открытую рамку считывания гена А (ФИГ. 1 и ФИГ. 2) использовали для получения белковой последовательности, исходящей из выявленного нового соединения.
Идентификация вариантов сплайсинга
Для анализа данных РНК-секвенирования на спаренных концах для идентификации потенциальных неоантигенов, возникающих в результате альтернативных событий сплайсинга, был разработан специальный биоинформатический процесс.С помощью разработанного процесса были идентифицированы варианты сплайсинга с сайтами альтернативного сплайсинга на 5' или 3'-концах, сохраненные интроны, исключенные экзоны, альтернативные концы или вставка(-и) новых кассет, как показано на ФИГ. 3. В ходе процесса идентифицировали варианты сплайсинга, которые отсутствовали в модели гена RefSeq NCBI через две основные функции: 1) Идентификация новых соединений на основе прочтения секвенирования с гэпами выравнивания > 5 пары оснований и > 15 пары оснований, выровненными с каждой стороны гэпа, в дальнейшем их называют прочтения с раздельным картированием. Для каждого набора данных РНК-секвенирования были названы новые соединения, если они были поддержаны по меньшей мере 5 прочтениями с раздельным картированием, а одна пара перекрывающих соединение прочтений 2) Идентификация островков выровненных прочтений, далее называемых островками покрытия. На ФИГ. 4 показан в виде рисунка подход.
Для оценки соотношения сигнал/шум в каждом образце, где геномная ДНК и пре-мРНК являются потенциальными источниками шума, два параметра были рассчитаны на основе набора из 200 высокоэкспрессируемых генов жизненно важных функций:
1. Глубина интрона покрытия (IDC): Глубина покрытия из 90-го процентиля для всех конститутивных интронных оснований. Если покрытие конкретной зоны попадало ниже этого значения, первое основание, на котором это произошло, определяли как границу зоны покрытия.
2. Отношение покрытия интрона/экзона (IECR): 90-й процентиль соотношения между медианным покрытием интрона и медианным покрытием ближайшего к 5'-концу экзона всех генов жизненно важных функций
Для классификации различных вариантов сплайсинга использовали следующие критерии:
Идентификация сайта альтернативного сплайсинга на 3'/5'-концах:
- Границу нового сайта сплайсинга определяли с помощью прочтений с раздельным картированием
- Интронная область, образующаяся при использовании сайта сплайсинга (если применимо), превышала IECR и вся область превышала IDC
Идентификация новой кассеты:
- Два новых сайта сплайсинга в интронной области, определенных прочтениями с раздельным картированием
- Область между двумя сайтами сплайсинга превышала IECR, а вся область превышала IDC
Идентификация сохранения интрона:
- Интронная область превышала IECR, а вся область превышала IDC
- По меньшей мере 5 прочтений перекрывающих обе границы интрона-экзона, при этом по меньшей мере 15 п. о. выровнены с каждой стороны от этих границ
Идентификация альтернативной терминации:
- 3'-граница, определяемая как край островка покрытия, не лежащей в пределах 60 п.о. от 3'-конца канонического экзона
- Любые интронные области между 5'-концом канонического экзона и 3'-концом границы превышали IECR, а вся область превышала IDC
-Идентификация исключения экзона:
- Новое соединение, определенное прочтениями с раздельным картированием, где один или более канонических экзонов были пропущены
Общие неоантигены, происходящие из событий аберрантного сплайсинга, были идентифицированы с использованием следующих критериев: частота событий сплайсинга в когорте больных должна была превышать 5%, встречаемость события сплайсинга должна была составлять менее 1% во всем наборе данных GTEx с использованием более мягкого критерия (по меньшей мере 2 прочтения с раздельным картированием) и событие сплайсинга должно было присутствовать в ≤ 2 наборах данных РНК-секвенирования, полученных из нормальных типов иммунных клеток. Для новой кассеты с исключением экзона и альтернативных 3'/5' сайтов сплайсинга события должны были иметь медианное прочтение с раздельным картированием на миллион картированных прочтений (СРМ) ≥ 0,05 и медианный процент сплайсинга (PSI) ≥ 0,1, рассчитанный по следующей формуле:

События с медианным значением 0,05 ≥ PSI ≥ 0,1 выбирали, если было обнаружено, что аберрантно сплайсированный ген был повышен в 2 раза в когорте больных по сравнению с дифференциальным анализом экспрессии генов в здоровых тканях. Для альтернативного прекращения и удерживания интронов события должны были иметь медианное количество СРМ с раздельным картированием ≥ 0,1 и медианный PSI > 0,5. Они также должны были быть обнаружены в ≥ 1% по меньшей мере в двух когортах заболеваний.
Прогнозирование и трансляция изоформ:
Для сборки изоформ, содержащих альтернативно сплайсированные неоантигены, канонические экзоны соседствующие с новыми сплайсированными элементами были идентифицированы с использованием прочтений с раздельным картированием. Наиболее экспрессируемая изоформа, которая потенциально может содержать прогнозируемый неоэпитоп, была выбрана для трансляции в соответствующий белок путем выбора подходящей открытой рамки считывания.
Неоантигенную часть белковой последовательности экстрагировали и последовательно соединяли с дополнительными 8 аминокислотными остатками перед первой измененной аминокислотой. Эту белковую последовательность затем использовали для последующих исследований валидации.
Идентификация мутаций ДНК / неоантигенов
Были исследованы наборы данных, созданные Broad Institute, содержащие данные секвенирования экзомов от пациентов с множественной миеломой (Lohr, J.G. et. al Cancer Cell 2014, Jan 13; 25(1) 91-101). Были загружены определения мутаций, опубликованные консорциумами, которые генерировали этот набор данных, и были выявлены мутации генов, которые присутствовали в > 5% популяции пациентов или в генах, которые, как известно, являются критическими факторами рака. Для этих генов для дальнейшего исследования были выбраны наиболее повторяющиеся точечные мутации, а гены, которые не имели повторяющихся точечных мутаций в той или иной позиции, были исключены из рассмотрения. Для каждой выбранной одиночной точечной мутации идентифицировали 17-мерный пептид с мутированной аминокислотой в его центре для дополнительных подтверждающих исследований.
Прогнозирование изоформы сплайсинга
В некоторых случаях перед идентифицированными событиями сплайсинга имелось несколько рамок считывания и экзонов, которые могли повлиять на последовательность канонического пептида, предшествующую последовательности неоэпитопа. В этих генах было определено, какие канонические экзоны расположены рядом с каждой особенностью неоэпитопа, на основании прочтений с раздельным картированием, присутствующих на границах экзона. Наиболее высоко экспрессируемая изоформа с самой высокой средней экспрессией в когорте заболеваний с наибольшей распространенностью события, которая может содержать предсказанный неоэпитоп, была выбрана для трансляции в соответствующий белок путем выбора открытой рамки считывания, связанной с этой изоформой. Неоэпитопную часть белковой последовательности экстрагировали, причем дополнительные 8 аминокислотных остатков перед первой измененной аминокислотой были включены и использованы для последующих подтверждающих исследований. Аналогичная процедура была проведена для выявления предполагаемых иммуногенных антигенов из изменений в ДНК со сдвигом рамки. Для делеций и вставок со сдвигом рамки считывания полученную последовательность ДНК транслировали в соответствующий белок путем выбора соответствующей открытой рамки считывания и извлекали измененную со сдвигом рамки считывания часть белковой последовательности, включая дополнительные 8 аминокислотных остатков перед первой измененной аминокислоты.
В таблице 5 представлено происхождение генов и аминокислотные последовательности выявленных неоантигенов, возникающие в результате событий слияния генов (FUS). В таблице 5 выделенными буквами обозначены канонические аминокислоты из гена 1. Буквы курсивом указывают на канонические аминокислоты из гена 2 для событий слияния генов в рамке. Буквы без выделения указывают на новые аминокислотные последовательности, сгенерированные из событий слияния генов вне рамки. В таблице 6 представлены полные названия слитых генов. В таблице 7 представлены соответствующие им полинуклеотидные последовательности.
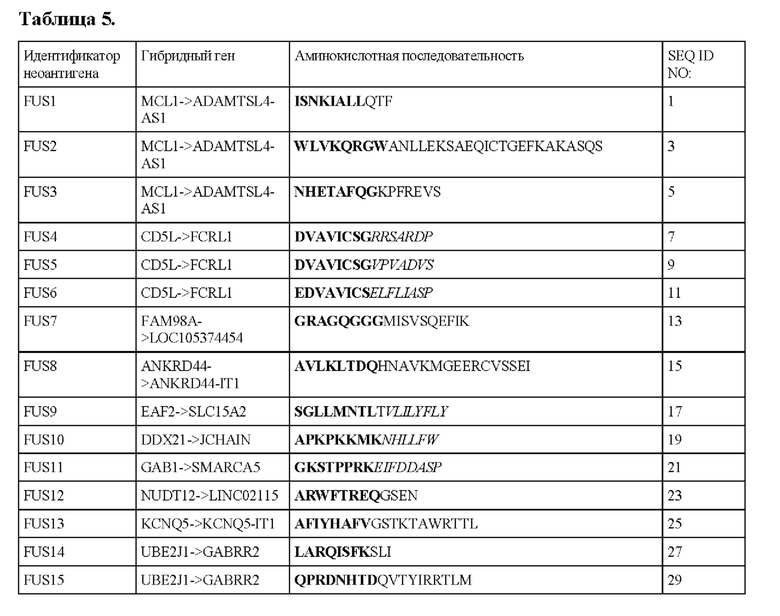
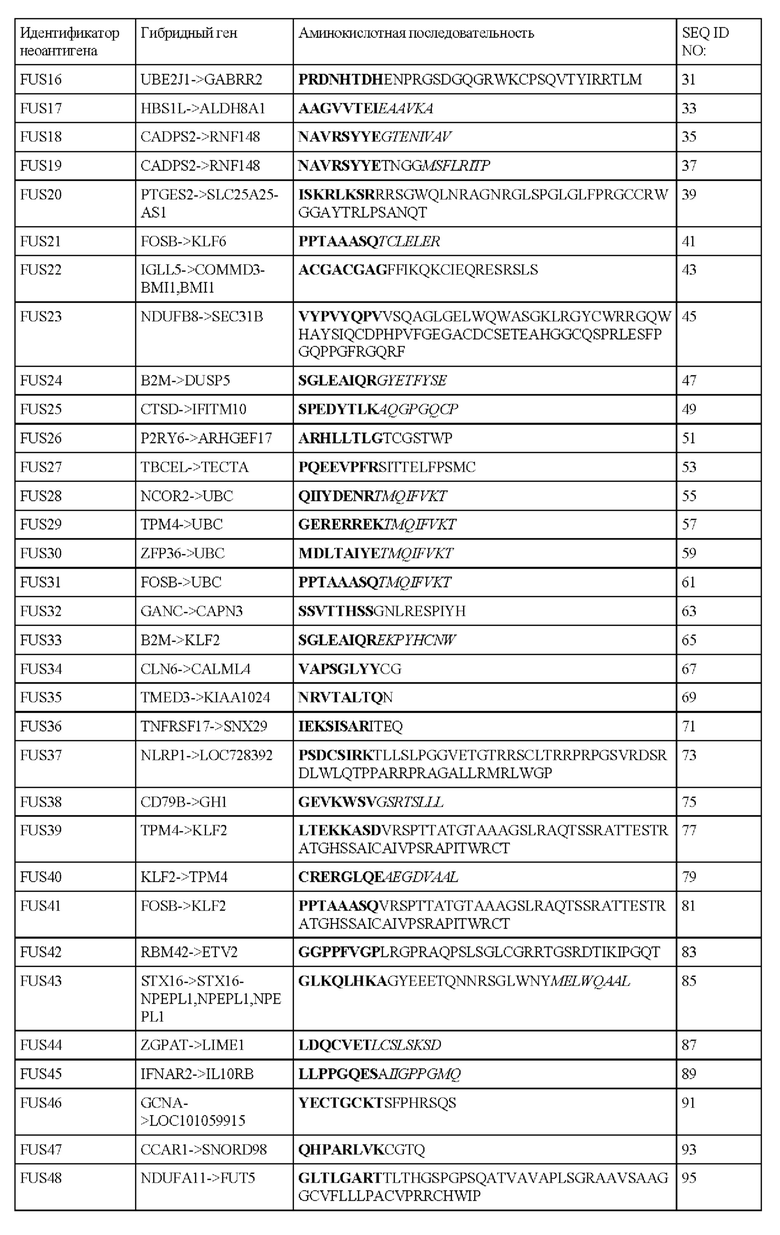

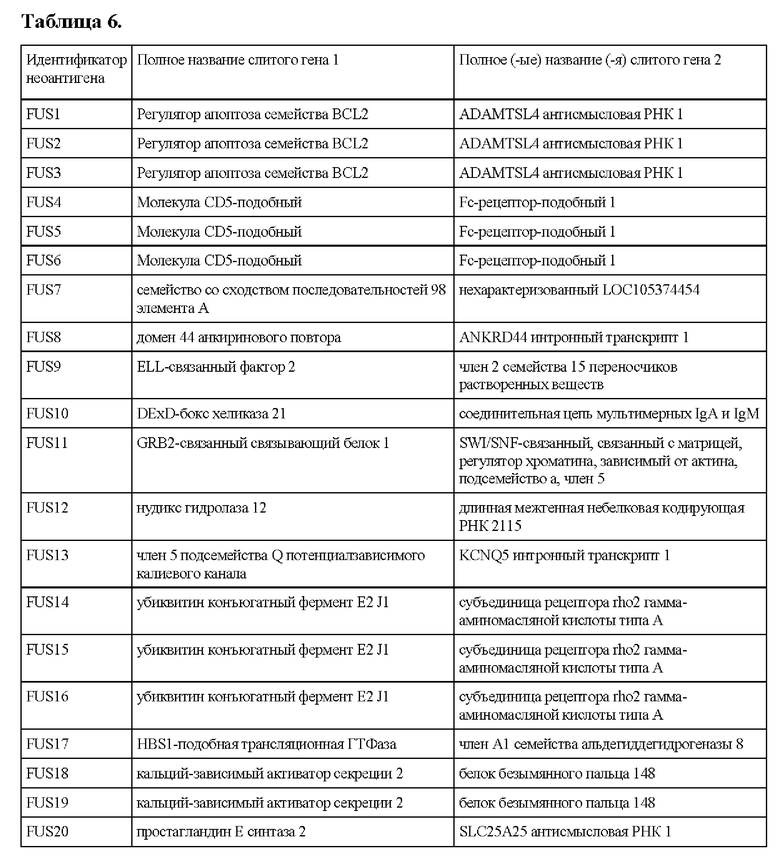
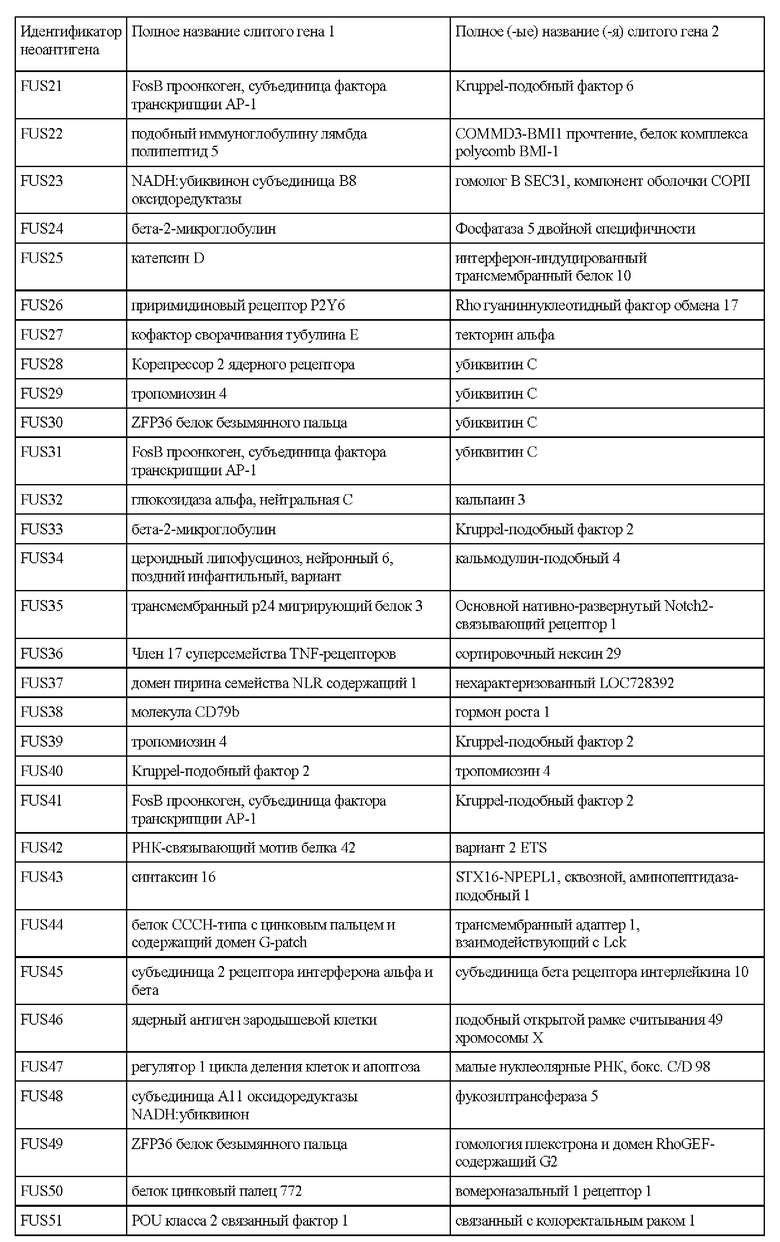
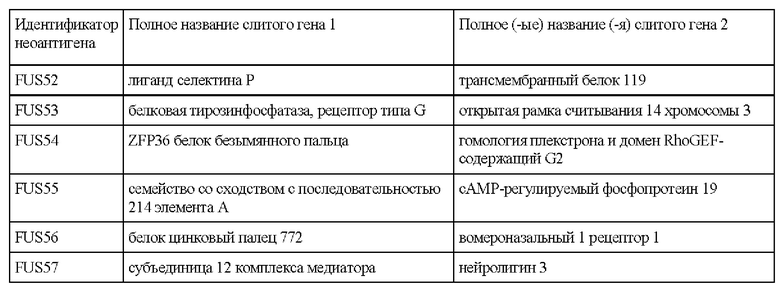
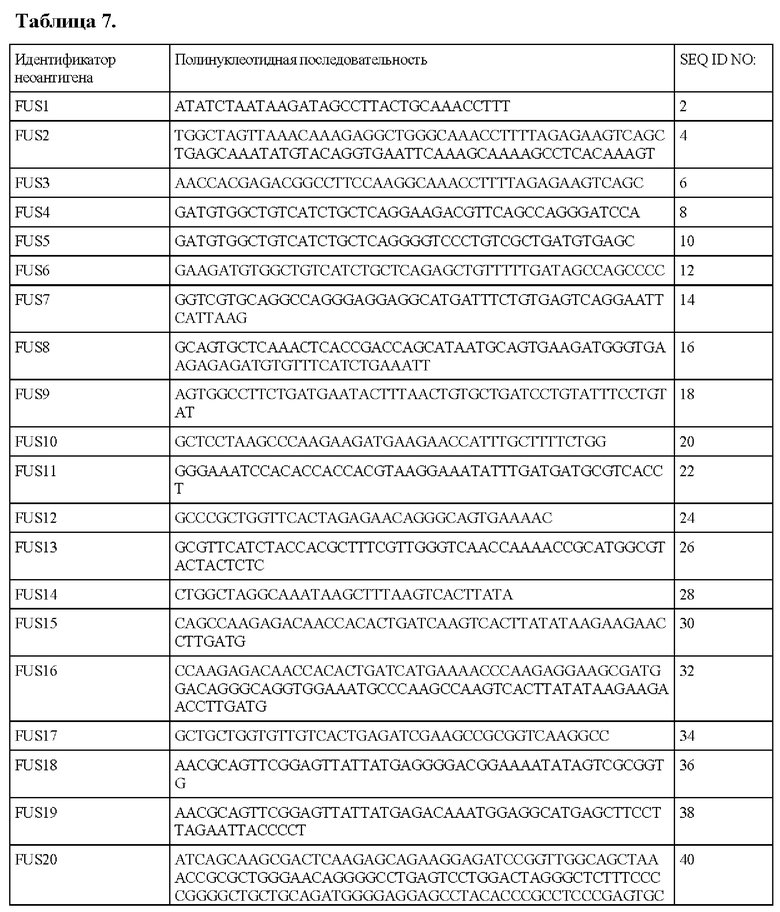
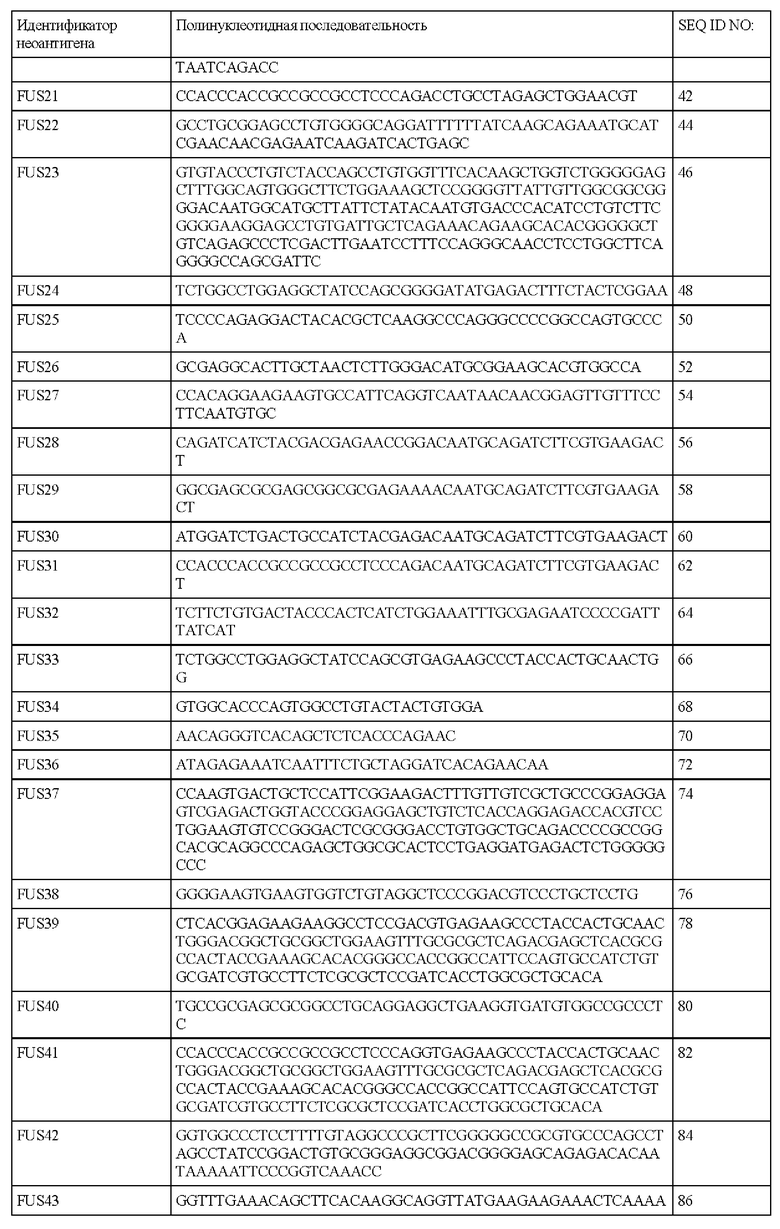
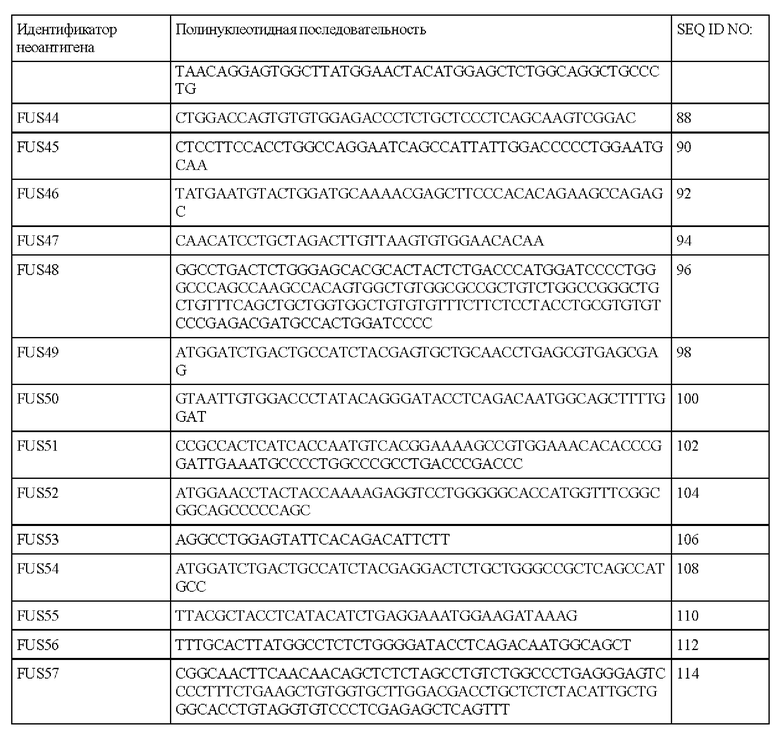
В таблице 8 представлено происхождение генов и аминокислотные последовательности выявленных неоантигенов, возникающие в результате событий альтернативного сплайсинга (AS). Выделенные буквы представляют последовательности из белка дикого типа, тогда как обычные буквы представляют мутантную последовательность, возникшую в результате событий альтернативного сплайсинга. В таблице 9 представлены геномные координаты событий альтернативного сплайсинга и полные названия генов. В таблице 10 представлены соответствующие им полинуклеотидные последовательности.

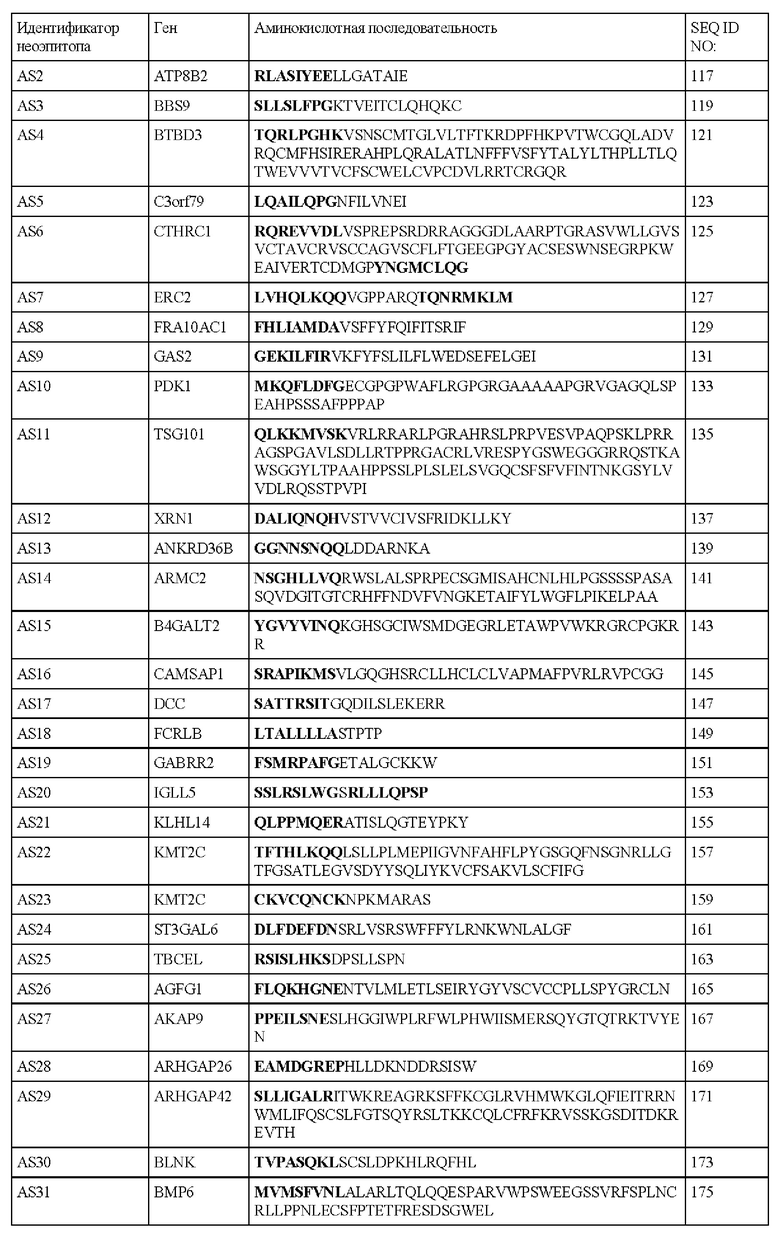
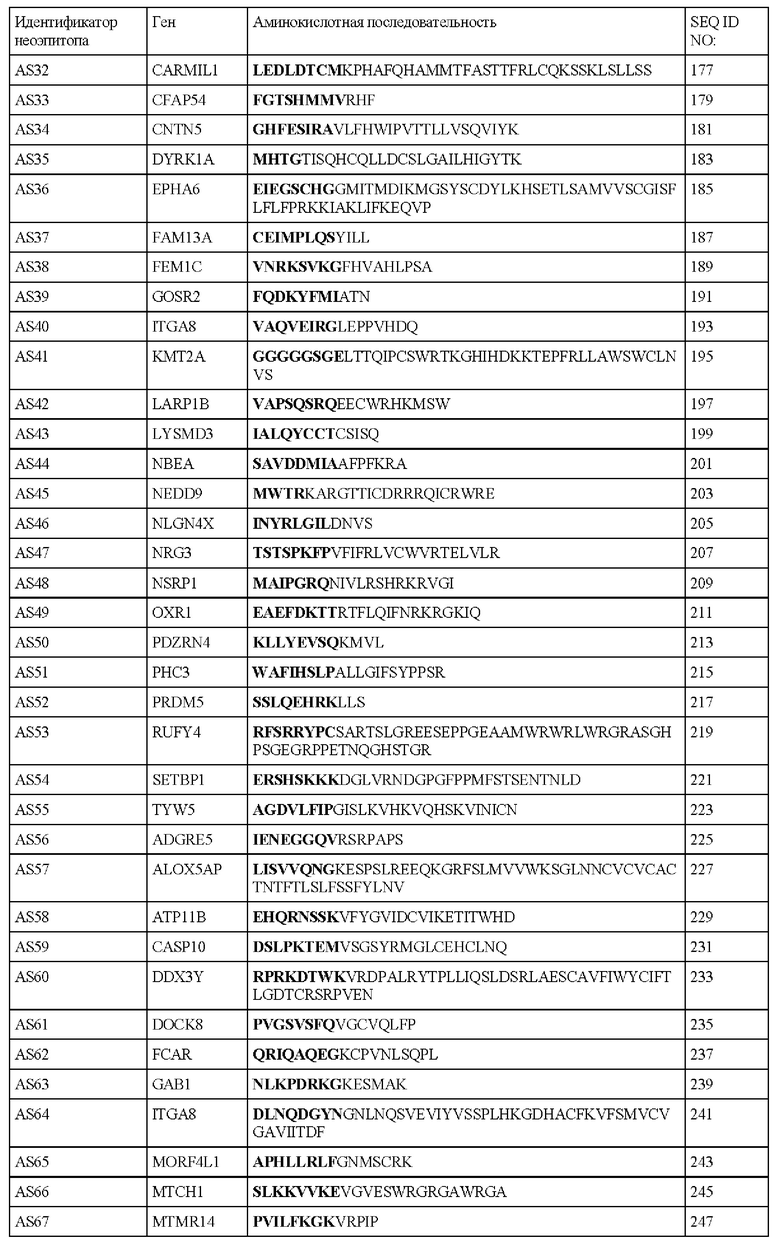
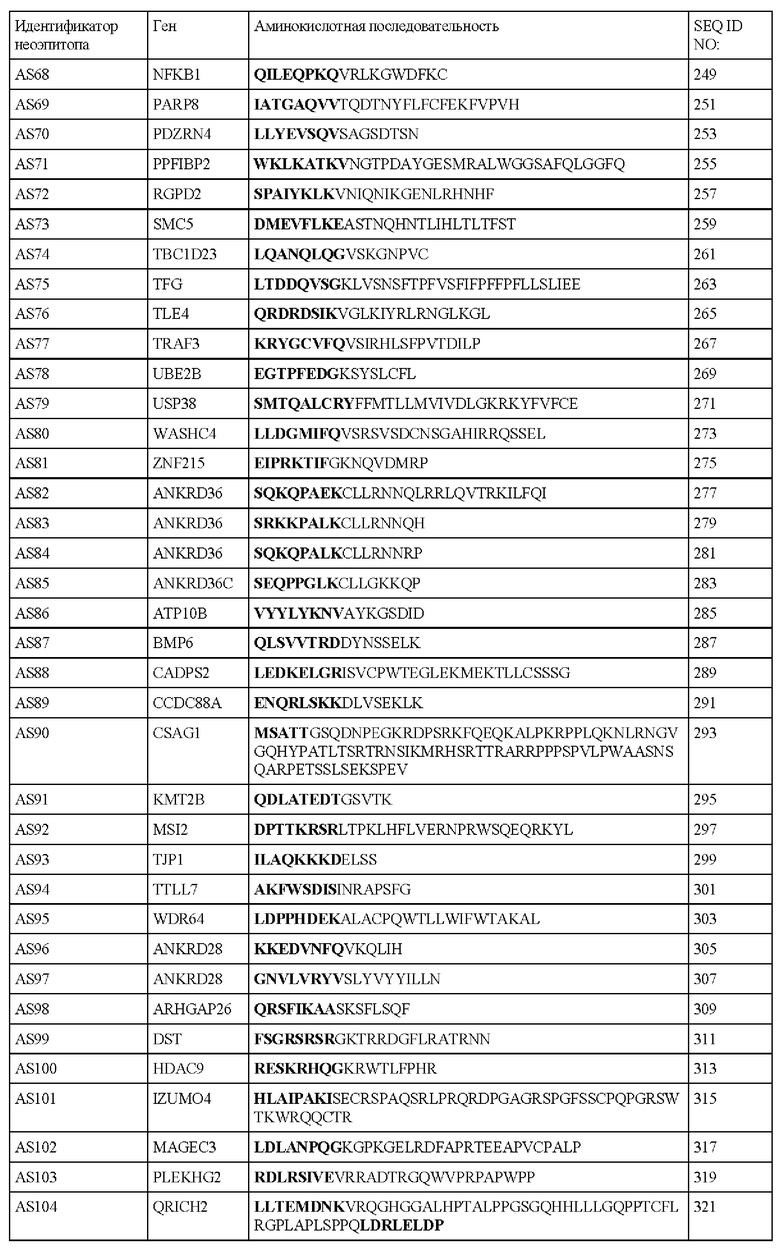
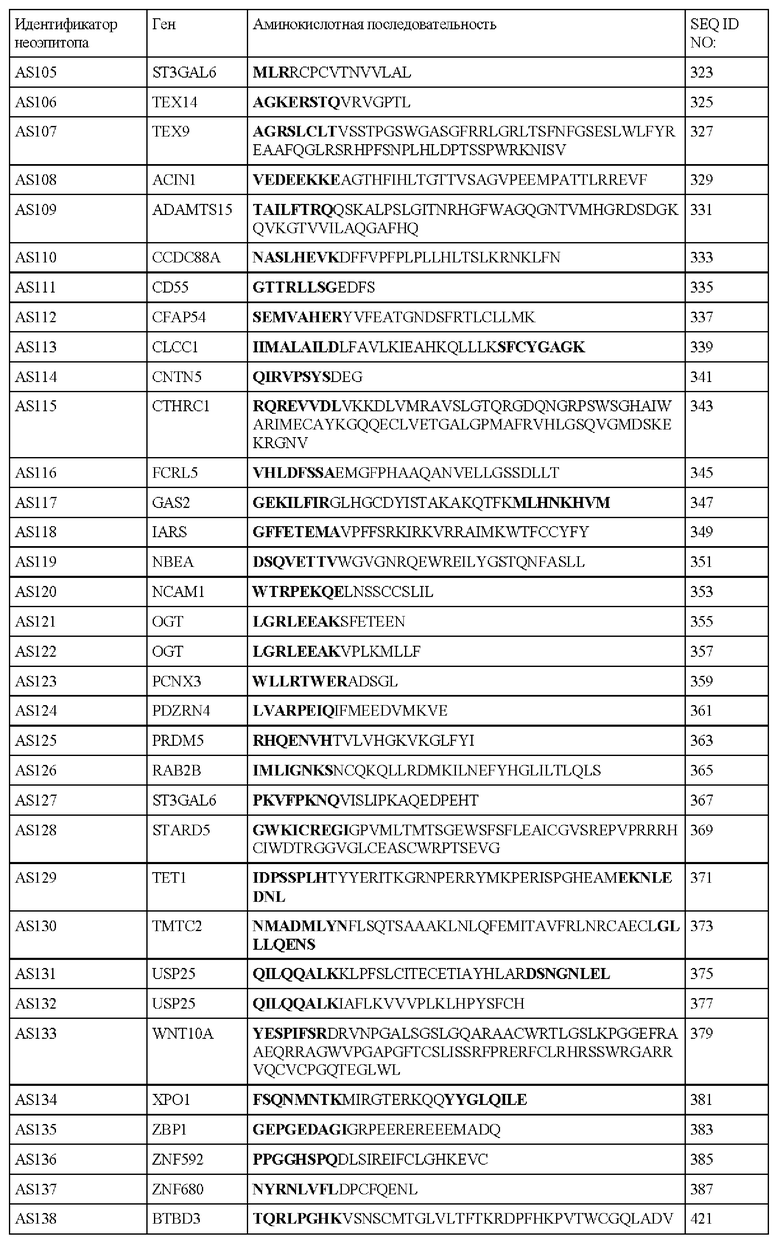

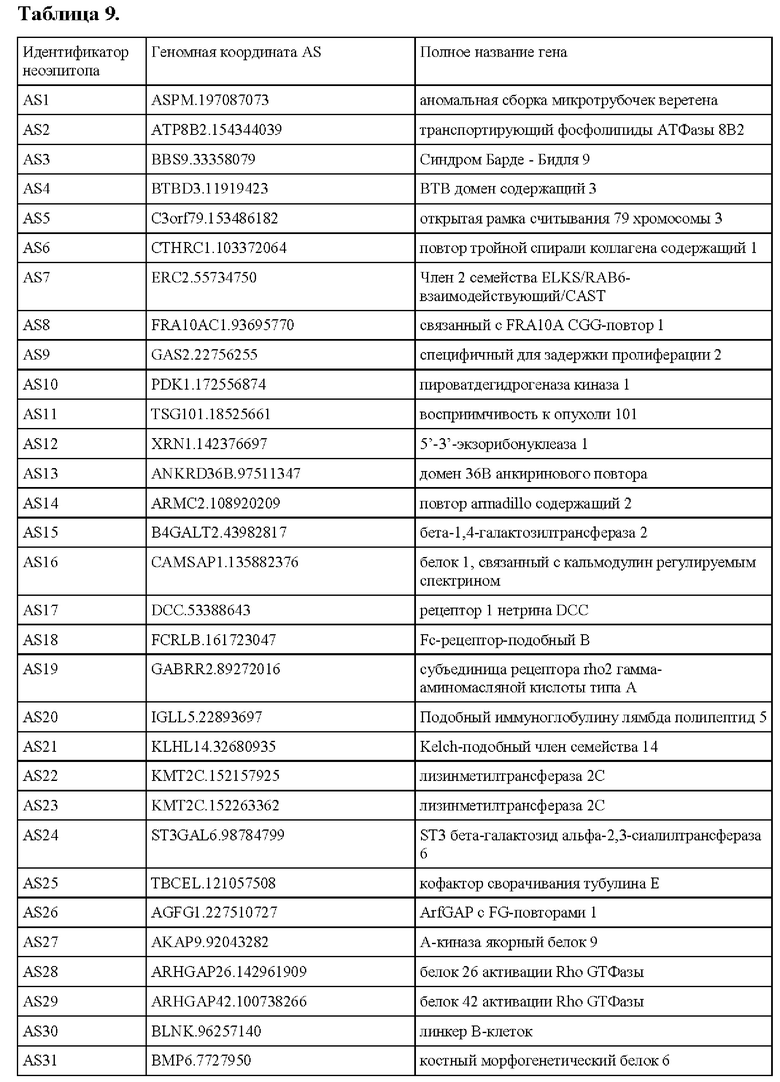
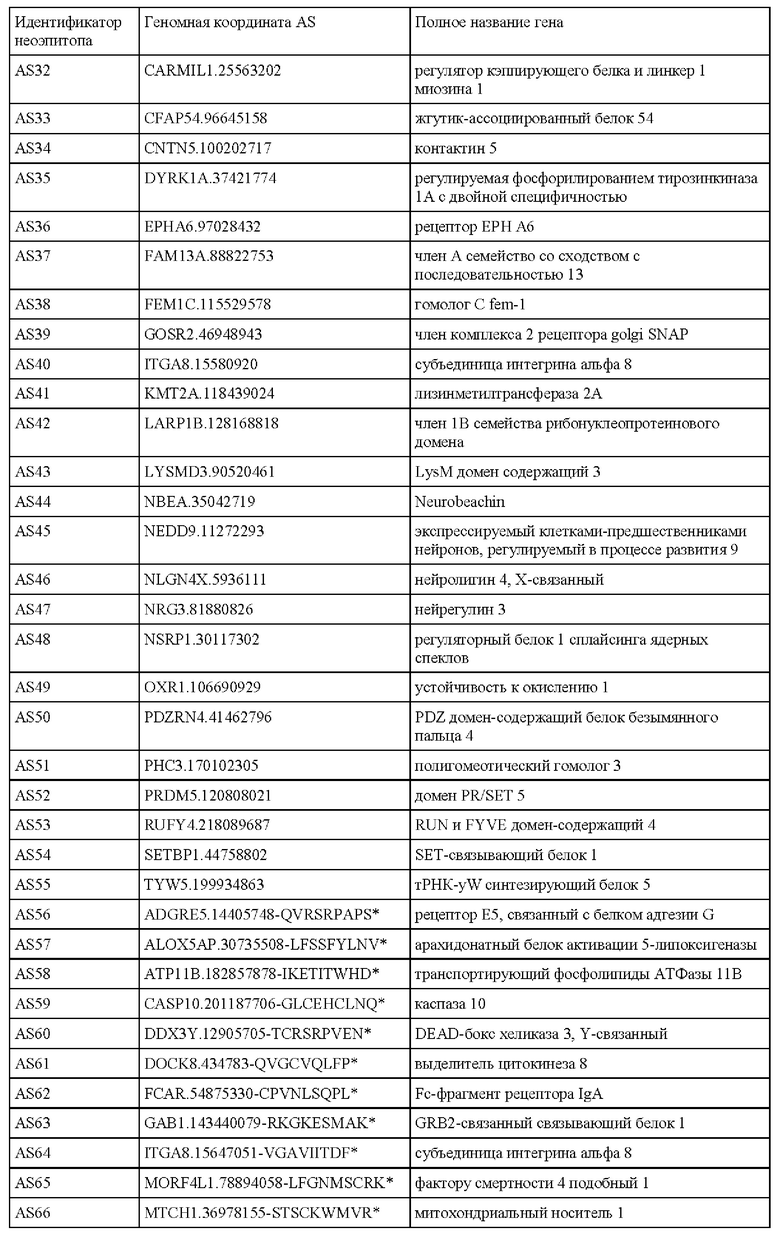
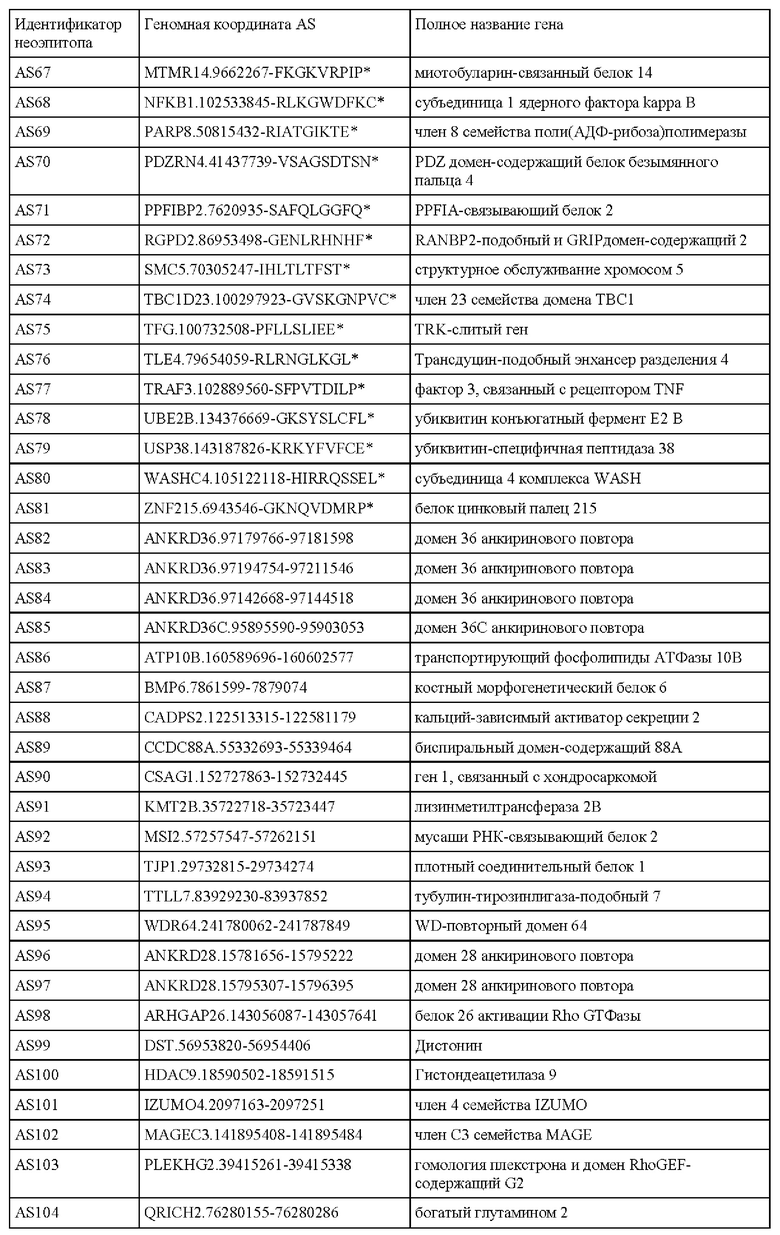
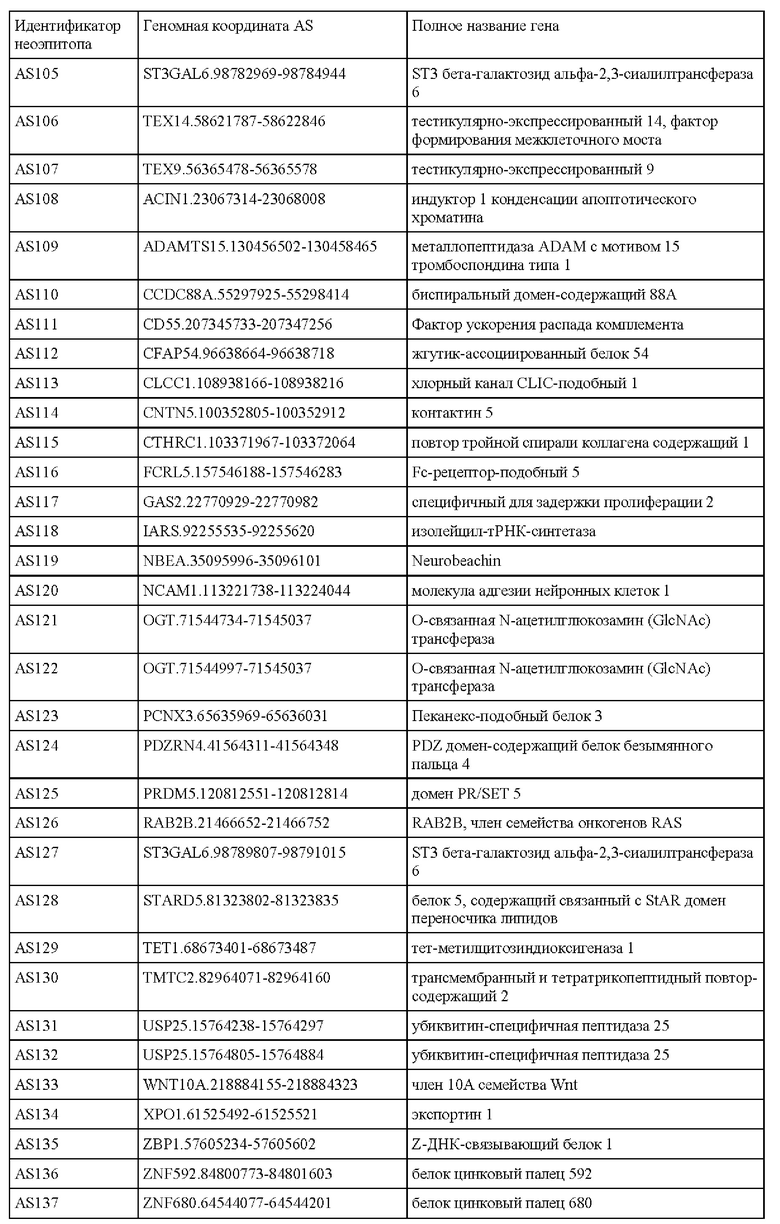
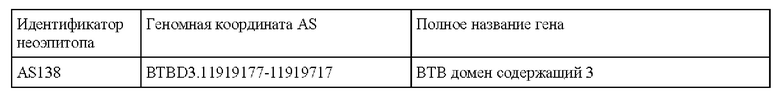
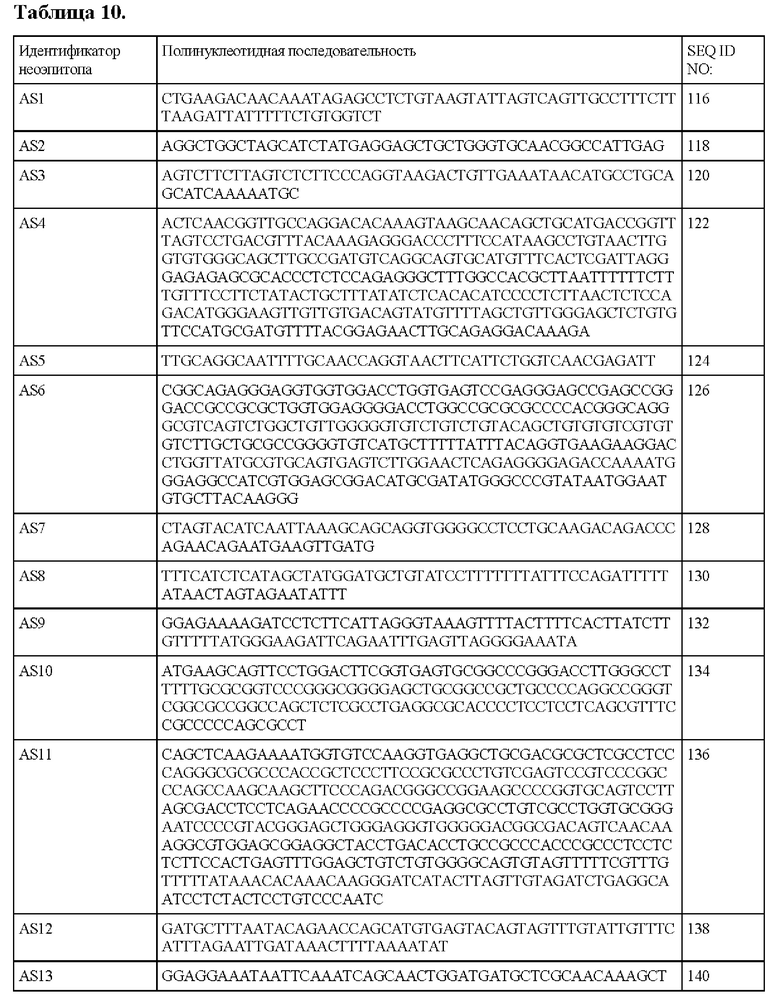
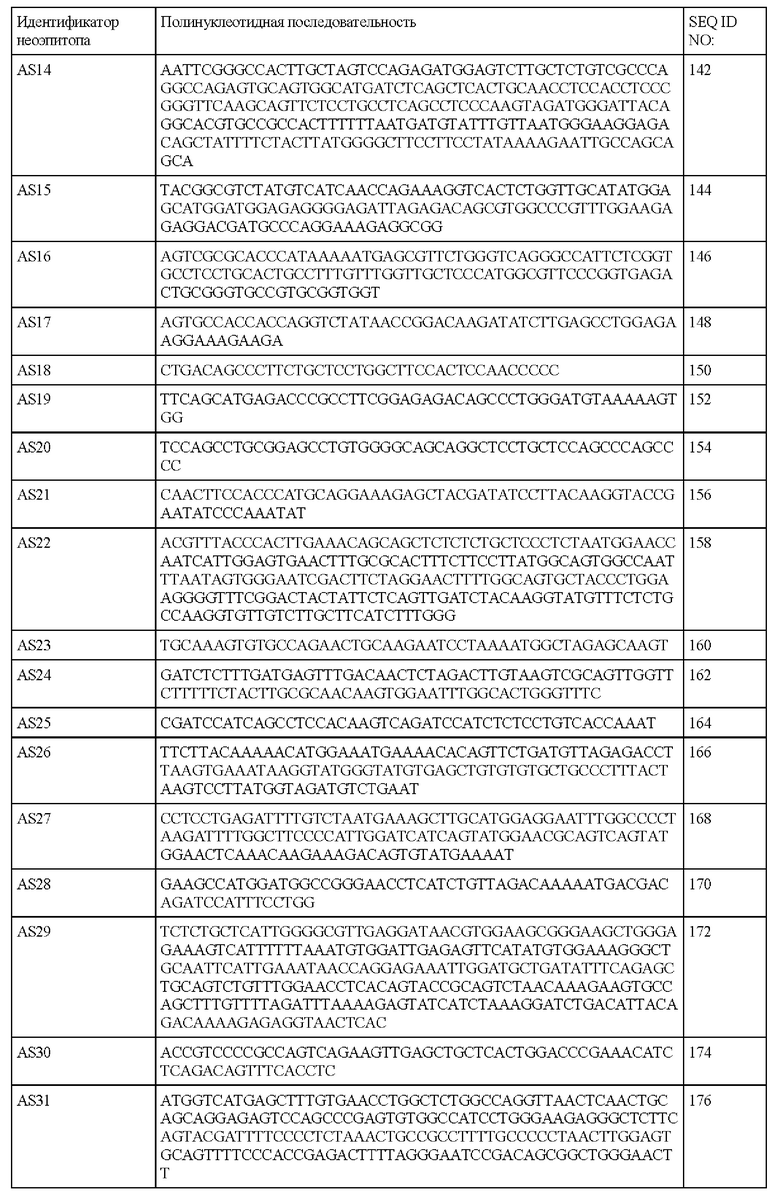
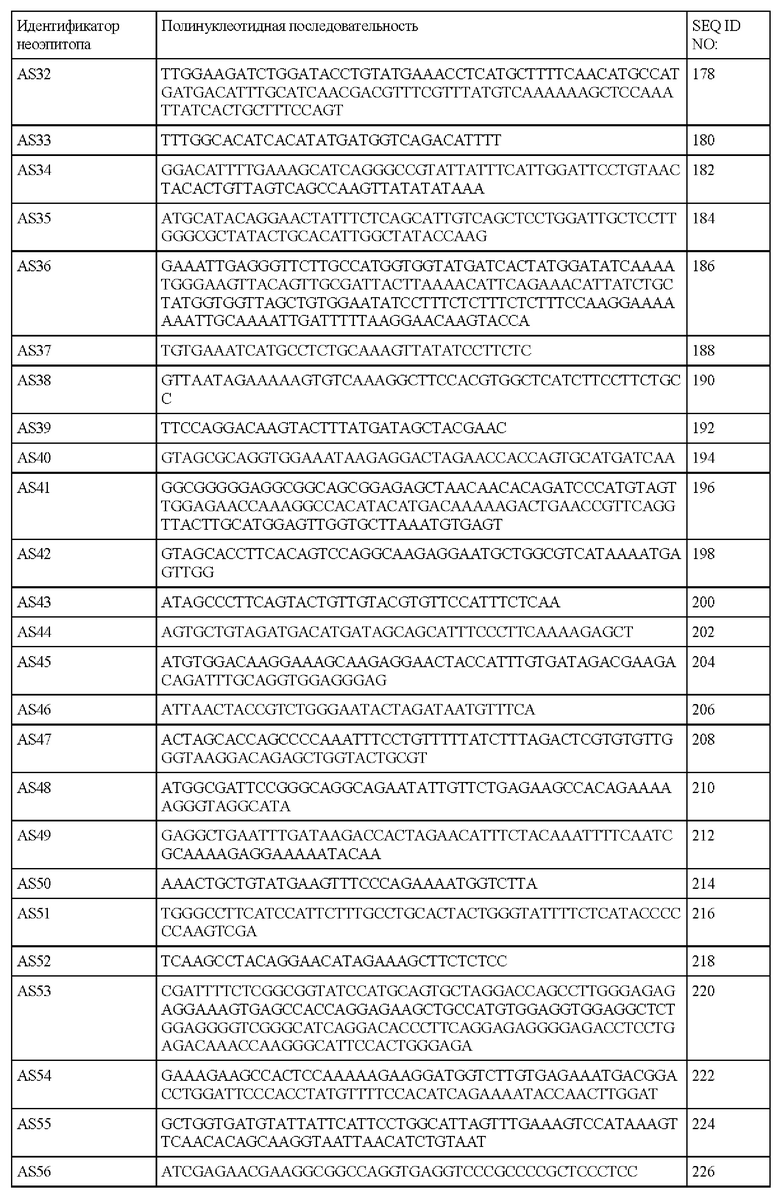
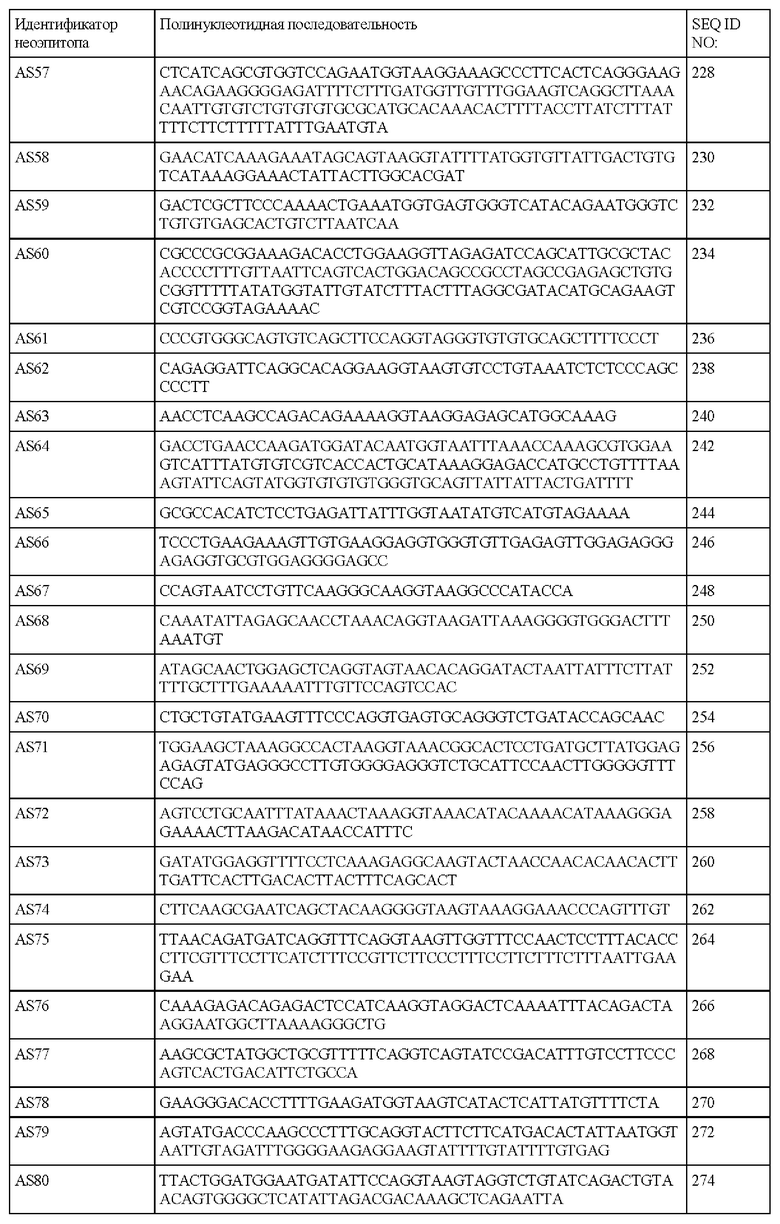
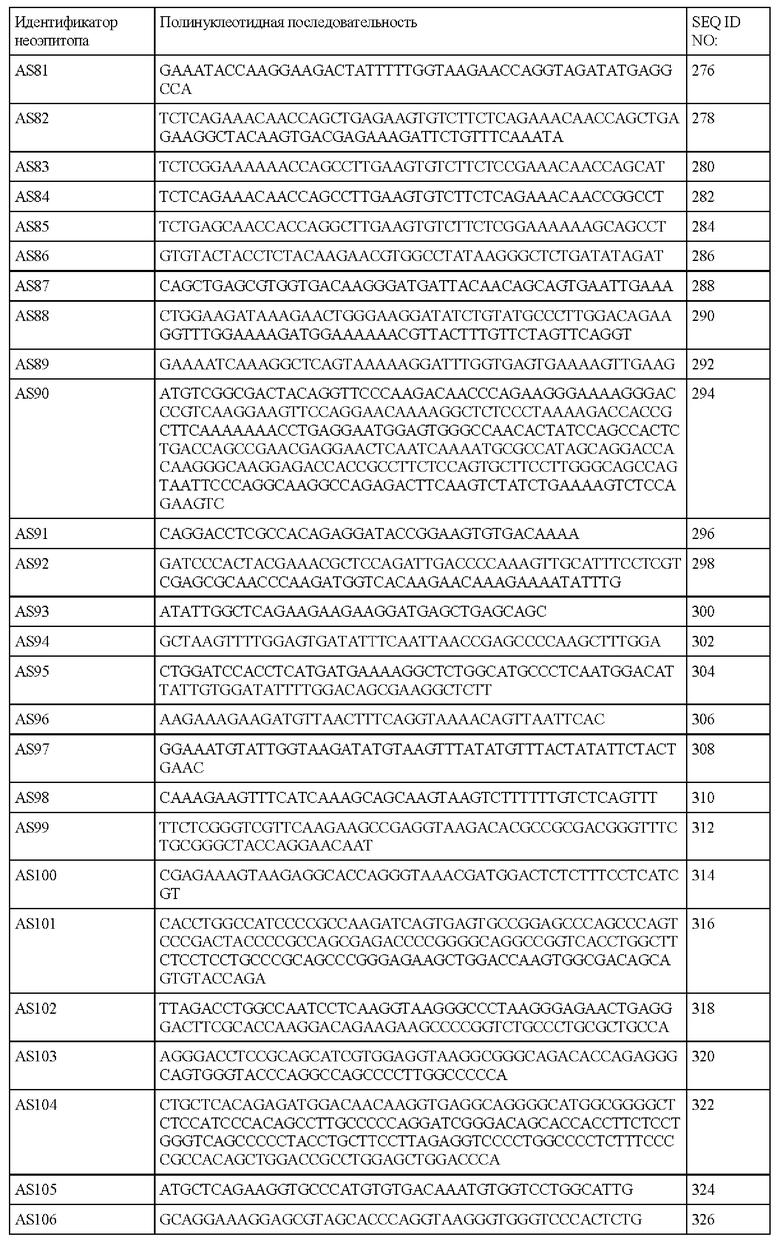
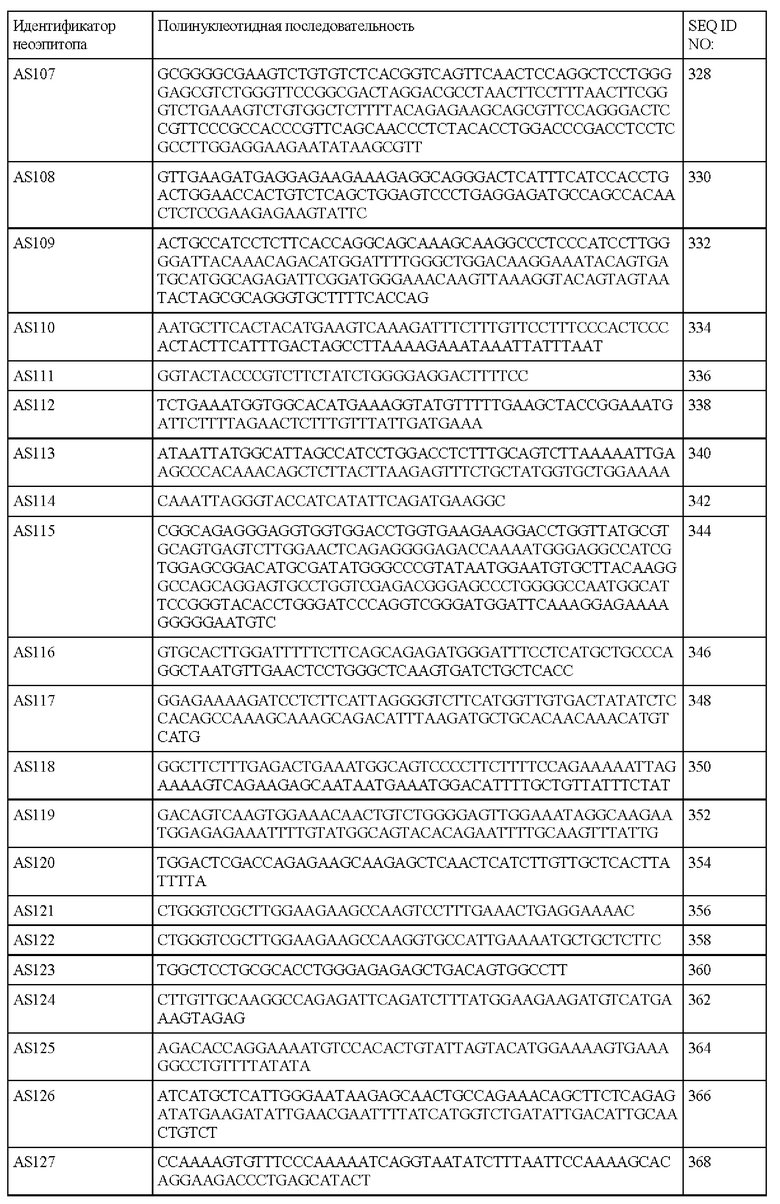
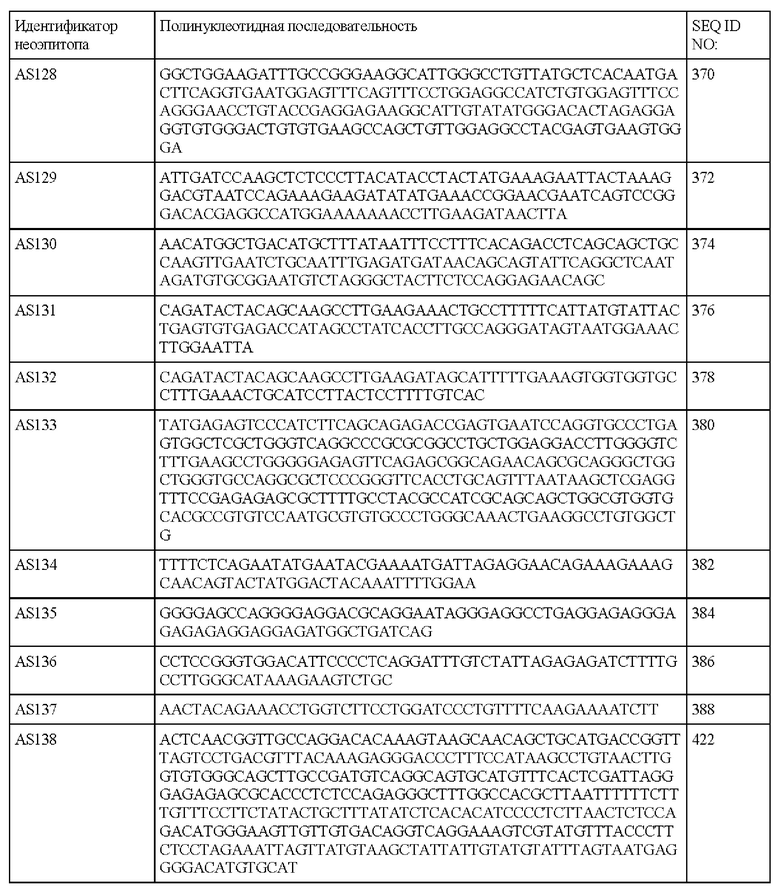
В таблице 11 представлено происхождение гена, полное название гена, мутация и аминокислотная последовательность идентифицированных неоантигенов, которые возникали из точечных мутаций. Точечные мутации указаны с помощью выделенных букв. В таблице 9 представлены соответствующие им полинуклеотидные последовательности.

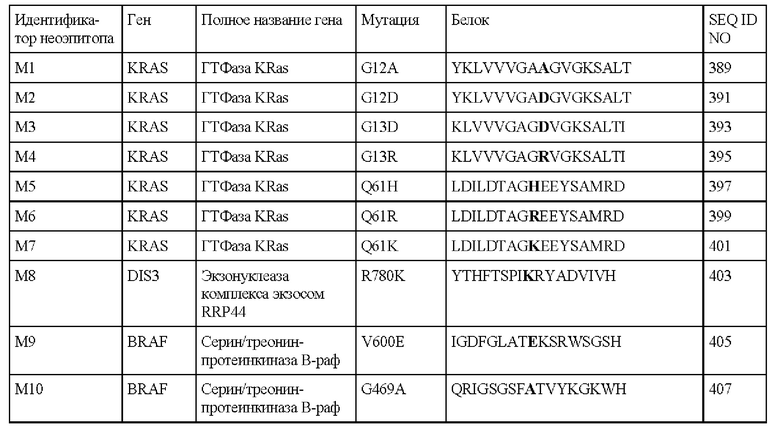

Пример 2: Количественный анализ ПЦР неоантигенов множественной миеломы в опухолевых и нормальных тканях
Кандидаты в неоантигены множественной миеломы (ММ) были протестированы на предмет их экспрессии в следующих образцах:
• 20 CD138+ плазмоцитов, полученных от пациентов с ММ
• 20 клеточных линий ММ и лимфомы (NALM6, Daudi, MM1R, MOLP8, JIM3, ELM, Н929, ОРМ2, RPMI8226, MM.1S, KMS11, ARH77, IM9, JIM1, KMS12-ВМ, МОР2, HUNS1, U266B1 и HTK)
• 11 МКПК, полученных от здоровых доноров, 5 - от молодых (<30 лет) и 6 - от пожилых доноров (>60 лет)
• Отсортированные иммунные клетки от 3 здоровых доноров (В-клетки, плазмоциты, Т-клетки, МКПК and моноциты) и
• 18 тканей от здоровых доноров (печень, почки, поджелудочная железа, предстательная железа, молочная железа, толстая кишка, желудок, скелетные мышцы, легкие, яичники, плацента, тонкий кишечник, спинной мозг, матка, селезенка, головной мозг, сердце и мочевой пузырь)
Праймеры для количественной ПЦР были разработаны для охвата последовательностей соединения точек разрыва, используя программное обеспечения Primer Express (версия 3.0.1). Для анализа экспрессии отбирали праймеры с Tm 60°С, содержанием GC от 30 до 80% и низкой вероятностью образования стабильных вторичных структур.
РНК из этих образцов выделяли с использованием набора для выделения РНК Qiagen (№430098094) согласно протоколу производителя. Библиотеки комплементарных ДНК готовили с использованием праймеров Oligo dT, входящих в набор для обратной транскрипции кДНК большой емкости (Invitrogen-part №11904018) из 200 нг общей РНК. Затем 3-10 нг кДНК предварительно амплифицировали в течение 10 циклов ПЦР в 15 мкл смеси для предварительной амплификации с использованием набора для предварительной амплификации TaqMan (ThermoFisher Scientific, №4384267). Для каждого образца оценивали входную кДНК для сохранения значений Ct эндогенных контролей (RPL13A, GAPDH, HPRT1, В2М) в диапазоне значений 13-15 Ct. Среди тестируемых контрольных генов RPL1 ЗА демонстрировали наиболее стабильную экспрессию среди здоровых тканей. Наконец, предварительно амплифицированную кДНК разбавляли в 5 раз и загружали в Fluidigm Biomark™ HD на 40 циклов амплификации ПЦР.
Экспрессию кандидатов в неоантигены (значения Ct) нормализовали по отношению к эндогенному контролю, RPL13A. Для определения экспрессии кандидатов в неоантигены в биологическом образце использовали значение отсечки Δct < 15 (кратное изменение ~ 32000). Результаты профиля экспрессии для всех опухолевоограниченных кандидатов в неоантигенны показаны на ФИГ. 5А, ФИГ. 5В, ФИГ. 5С и ФИГ. 5D. Антигены с экспрессией как в контрольных, так и в опухолевых образцах показаны на ФИГ. 6А, ФИГ. 6В, ФИГ. 6С и ФИГ. 6D.
Пример 3: Оценка иммуногенности неоантигенов in vitro
Иммуногенность неоантигенов оценивали с использованием известных способов. 9-мерные фрагменты, выбранные в примере 2, оценивали в отношении их способности активировать Т-клетки с использованием известных способов анализа с использованием продукции TNFα и IFNγ CD8+ и CD4+ Т-клетками в качестве показателей. Пептиды синтезировали с помощью GenScript с чистотой > 80%. Лиофилизированные пептиды растворяли в 100% ДМСО.
Анализ экзогенной аутологичной рестимуляции здорового донора
Перекрывающиеся 15-мерные пептиды были сконструированы таким образом, чтобы охватывать каждый указанный неоантиген. Их способность активировать Т-клетки оценивали с использованием известных способов, таких как анализ, определенный как анализ экзогенной аутологичной рестимуляции нормального донора. Пептиды использовали в качестве пулов с использованием продукции TNFα и IFNγ CD8+ и CD4+ Т-клетками, в качестве показателей. Для каждого пула пептидов анализировали максимальную частоту CD8+TNFα+IFNγ+ and CD4+TNFα+IFNγ+ Т-клеток, а также максимальное кратное изменение фона для каждого пула пептидов, что было рассчитано как самая высокая частота CD8+TNFα+IFNγ+ and CD4+TNFα+IFNγ+ Т-клеток, а полученное кратное изменение оценивали в отношении пептида для нормальных доноров.
CD1c+ дендритные клетки (CD1c+DC), выделенные из здоровых человеческих ПКМК, размораживали с использованием среды (IMDM (Gibco), обогащенной глутамином, HEPES, 5% человеческой сыворотки (Sigma) и 1X Pen-Strep). Дендритные клетки ресуспендировали в среде, обогащенной IL-4 (Peprotech, 20 нг/мл) и GM-CSF (Gibco, 20 нг/мл), высевали в 6-луночные микропланшеты и оставляли в инкубаторе на ночь при 37°С и 5% CO2. На следующий день подсчитывали DC-клетки и высевали в кругло донный микропланшет с 96 лунками в концентрации 30,000 жизнеспособных клеток на лунку. Пулы лиофилизированных неоантигенных пептидов (15-мерные пептиды с 8-мерными перекрывающимися пептидными последовательностями) солюбилизировали в 100% ДМСО с маточной концентрацией 20 мг/мл. Пулы неоантигенных пептидов добавляли в дендритные клетки для конечной концентрации 10 мкг/мл и выдерживали в течение 2 часов при 37°С и 5% CO2 в инкубаторе. CEF Peptide Pool "Plus" (Cellular Technologies, Ltd.) использовали в качестве положительного контроля (каждый вирусный пептид в конечной концентрации 4 мкг/мл), а ДМСО в той же конечной концентрации (0,05%), что и экспериментальные пептиды, использовали в качестве отрицательного контроля. Через 2 часа DC-клетки облучали ионизирующим излучением мощностью 50 грей. Аутологичные CD3+ пан-Т-клетки, выделенные из нормальных человеческих ПКМК, размораживали с использованием среды. После облучения к облученным DC добавляли аутологичные пан-Т-клетки в количестве 300,000 жизнеспособных клеток на лунку. Во все лунки добавляли человеческий IL-15 (Peprotech) в конечной концентрации 10 нг/мл. Планшеты инкубировали при 37°С и 5% CO2 в инкубаторе в общей сложности в течение 12 дней. Среду обновляли каждые 2-3 дня с использованием IL-15 (R&D System, конечная концентрация 10 нг/мл) и IL-2 (R&D System, конечная концентрация 10 IU/мл).
На 11 день клетки повторно стимулировали идентичными экспериментальными пулами пептидов или контролями в той же концентрации, что и стимуляция пептидом в 1 день. В каждую лунку добавляли коктейль белковых ингибиторов (eBioscience) и планшет инкубировали в течение ночи 14-16 часов при 37°С и 5% CO2 в инкубаторе. На 12 день клетки окрашивали для анализа поверхностной и внутриклеточной проточной цитометрии. Клетки промывали с использованием PBS и окрашивали красителем с использованием набора для определения мертвых клеток Live/Dead Fixable Aqua (Thermo-Fisher). После окрашивания блокировали с помощью не содержащего биотина ингибитора Fc-рецептора Biotin-Free Fc Receptor Blocker (Accurate Chemical & Scientific Corp). Панель внеклеточного потока (1 мкл/антитело на лунку в 50 мкл) состояла из CD3 PerCP-Cy5.5 (Biolegend), CD4 BV421 (Biolegend) и CD8 АРС-Су7 (Biolegend). После внеклеточного окрашивания клетки фиксировали и пермеабилизировали, используя буферный набор Foxp3/Transcription Factor Staining Buffer (eBioscience) и окрашивали на внутриклеточные белки (разведение 1:50) с использованием TNFα FITC (R&D Systems) и IFNγ BV785 (Biolegend). Клетки промывали, ресуспендировали в буфере для окрашивания, анализировали и записывали с помощью проточного цитометра BD Celesta.
Анализ проточной цитометрии проводили на ПО FlowJo v10. 6. Клетки гейтировали по живым синглетным CD3+, CD4+ и CD8+ Т-клеткам. CD8+ и CD4+ Т-клетки анализировали на экспрессию TNFα и IFNγ.
Ответы иммуногенности считали положительным для пула пептида, если были соблюдены следующие критерии:
• Частота дважды положительных TNFα/IFNγ CD8+ и/или TNFα/IFNγ CD4+ Т-клеток при стимуляции экспериментальным пулом пептидов была больше или равна 3-кратному превышению над контролем ДМСО
• Частота дважды положительных TNFα/IFNγ CD8+ и/или дважды положительных TNFα/IFNγ CD4+ Т-клеток была не менее 0,01%
Иммуногенность неоантигенов была впервые исследована у 5-7 здоровых доноров. Нереакционноспособные неоантигены дополнительно тестировали на новой когорте из 22 здоровых доноров. Данные об иммуногенности для неоантигенов обобщены в таблице 13. На ФИГ. 7А и ФИГ. 7В показан репрезентативный точечный график, показывающий стратегию гейтирования и иммуногенные ответы, достигаемые для нескольких неоантигенов. Интересно, что большинство неоантигенов демонстрировали иммуногенные ответы у нескольких доноров (ФИГ. 8А, ФИГ. 8В, ФИГ. 9А и ФИГ. 9В).
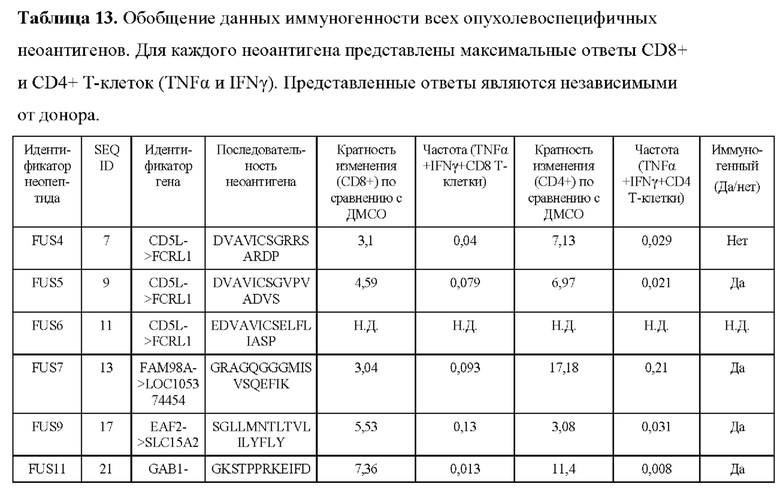
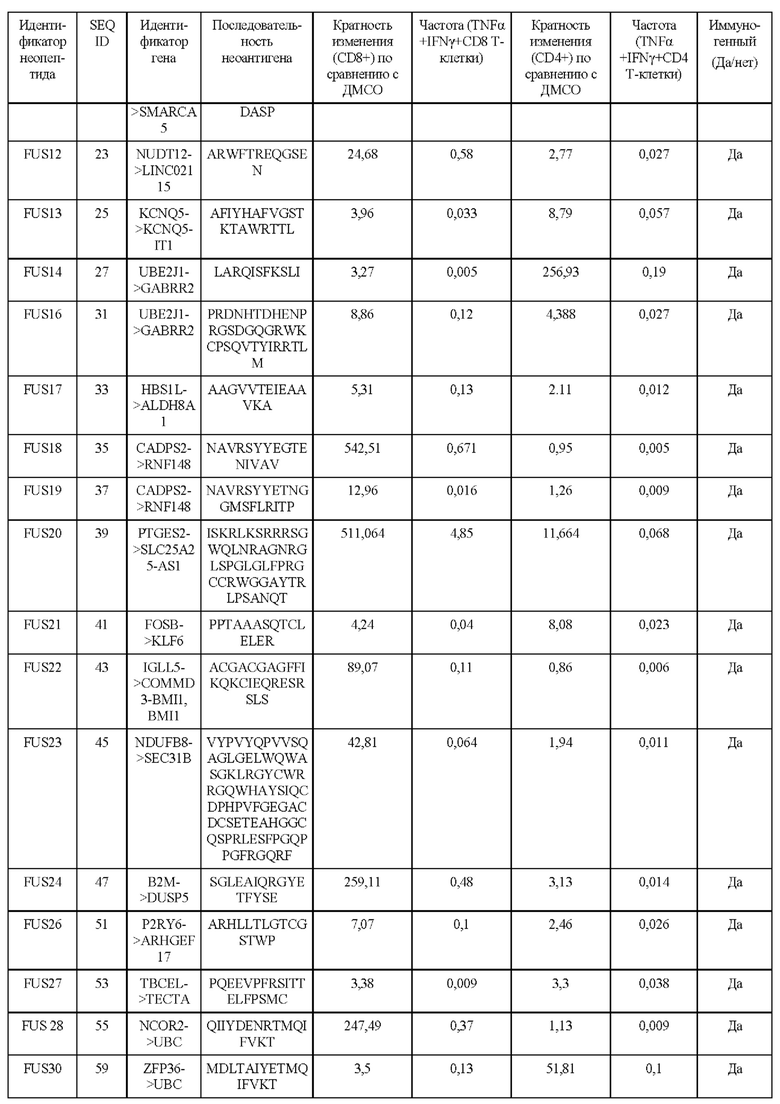
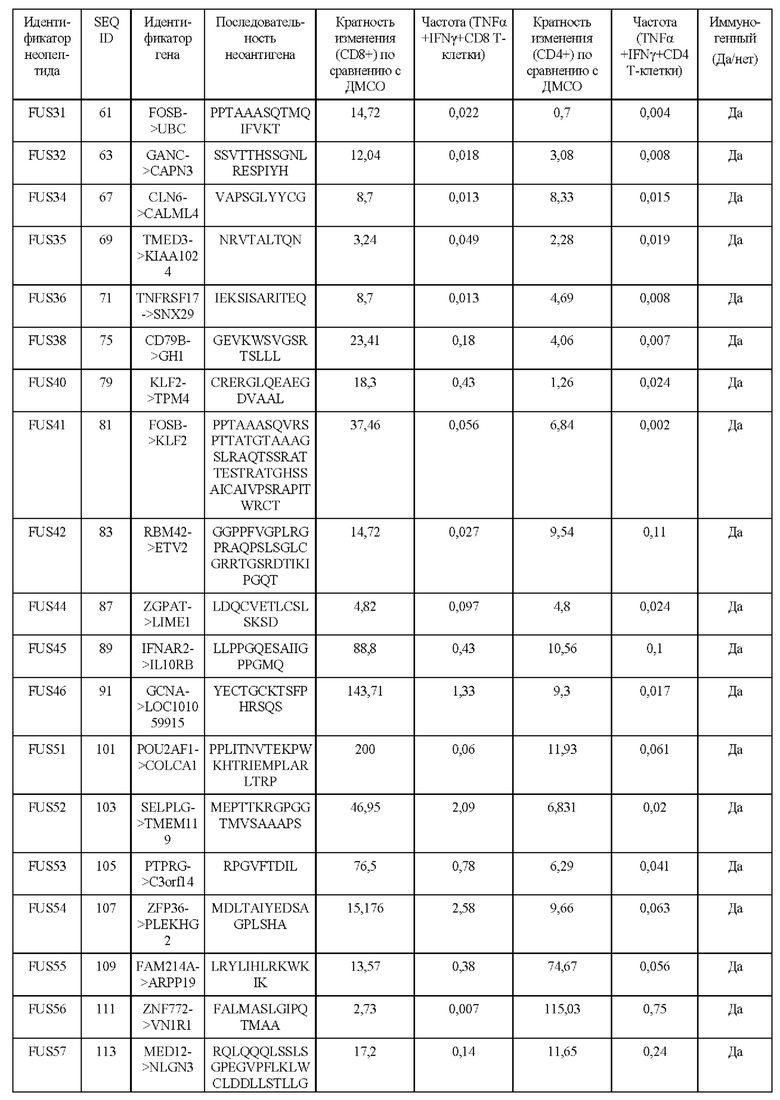
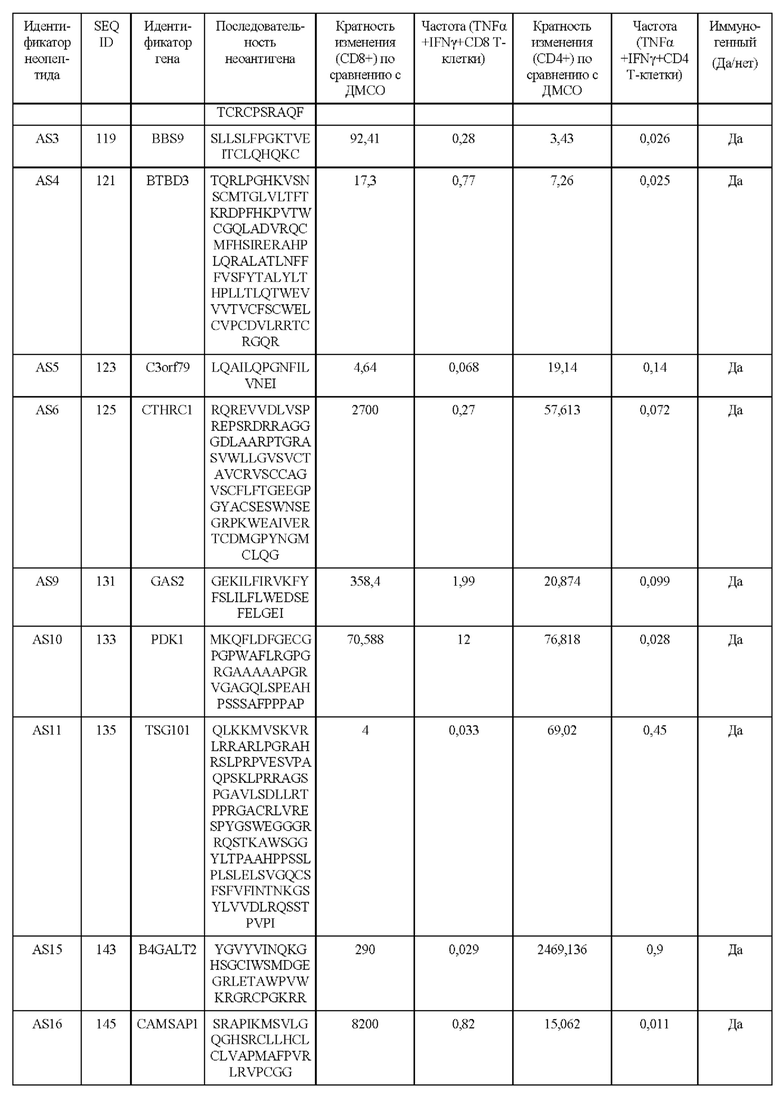
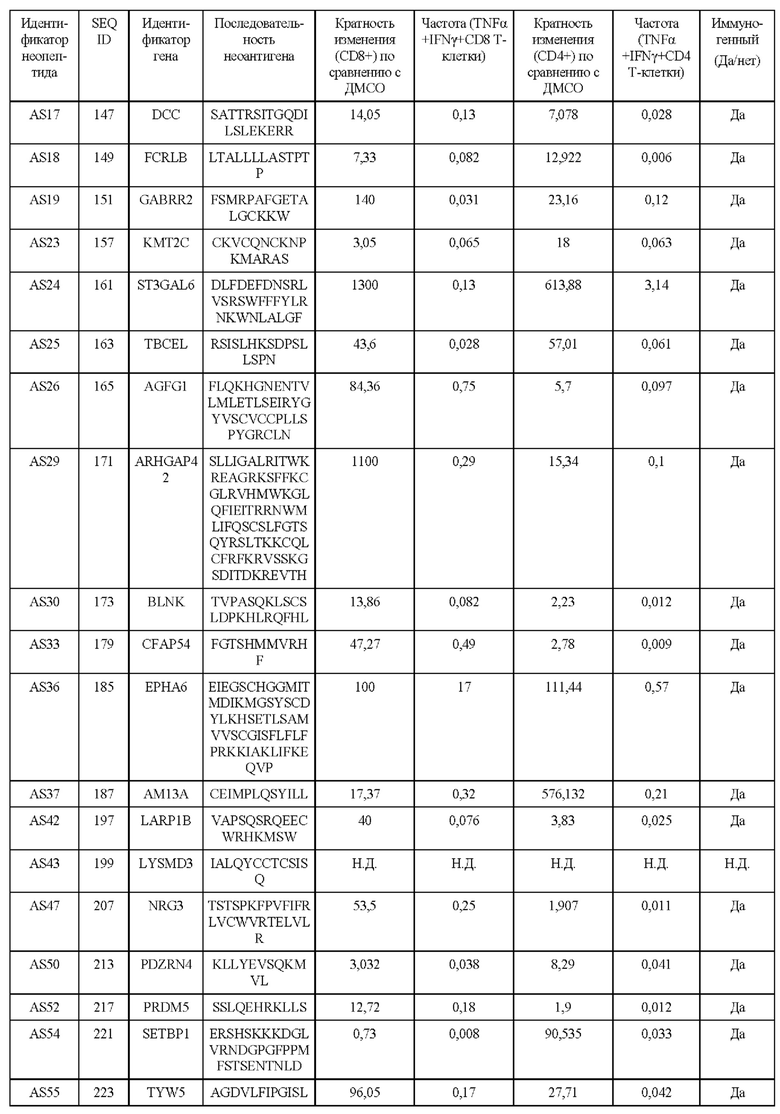
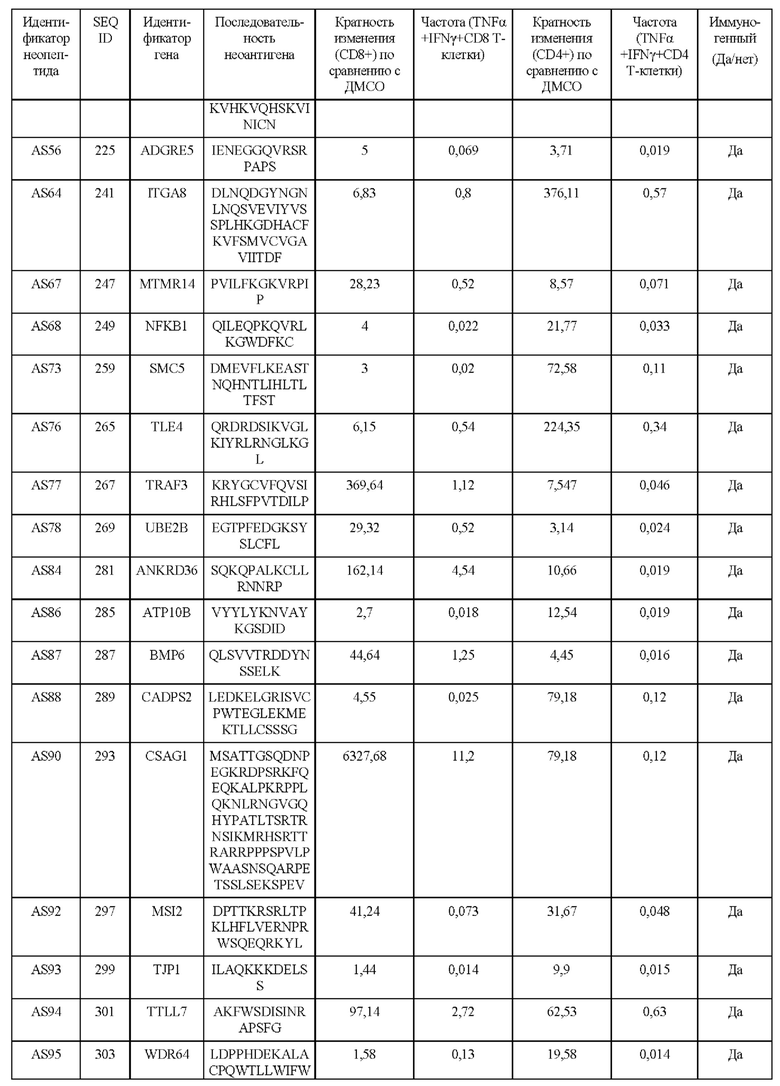
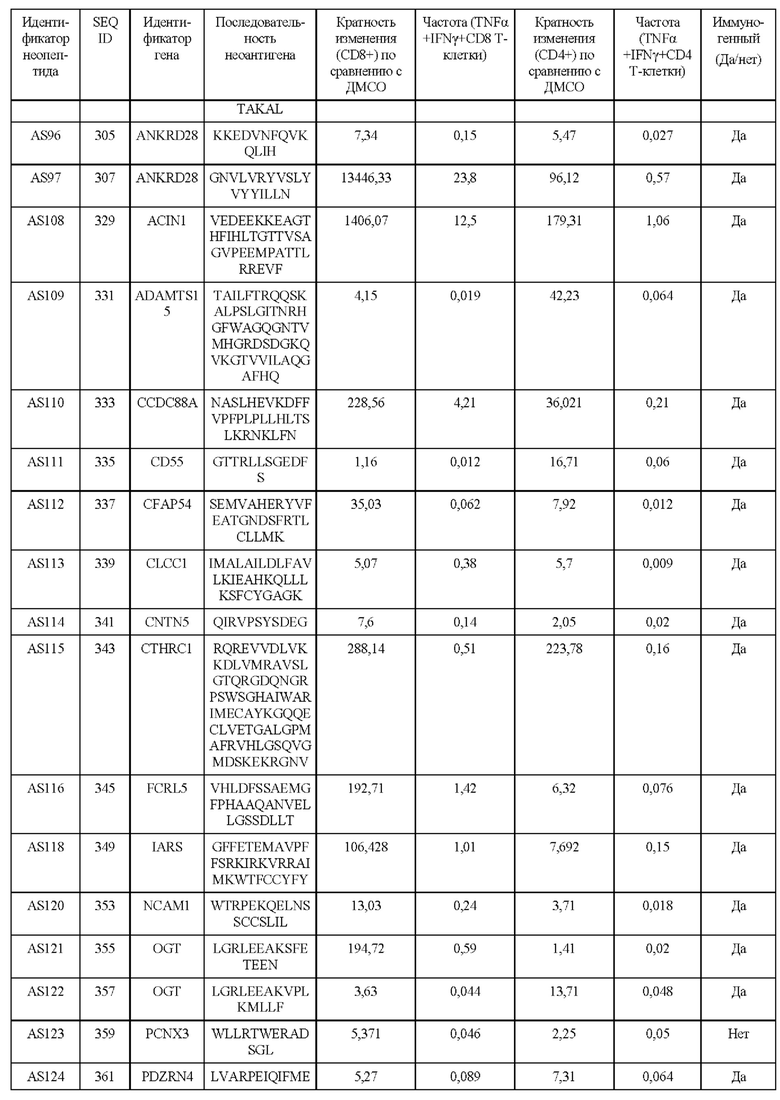
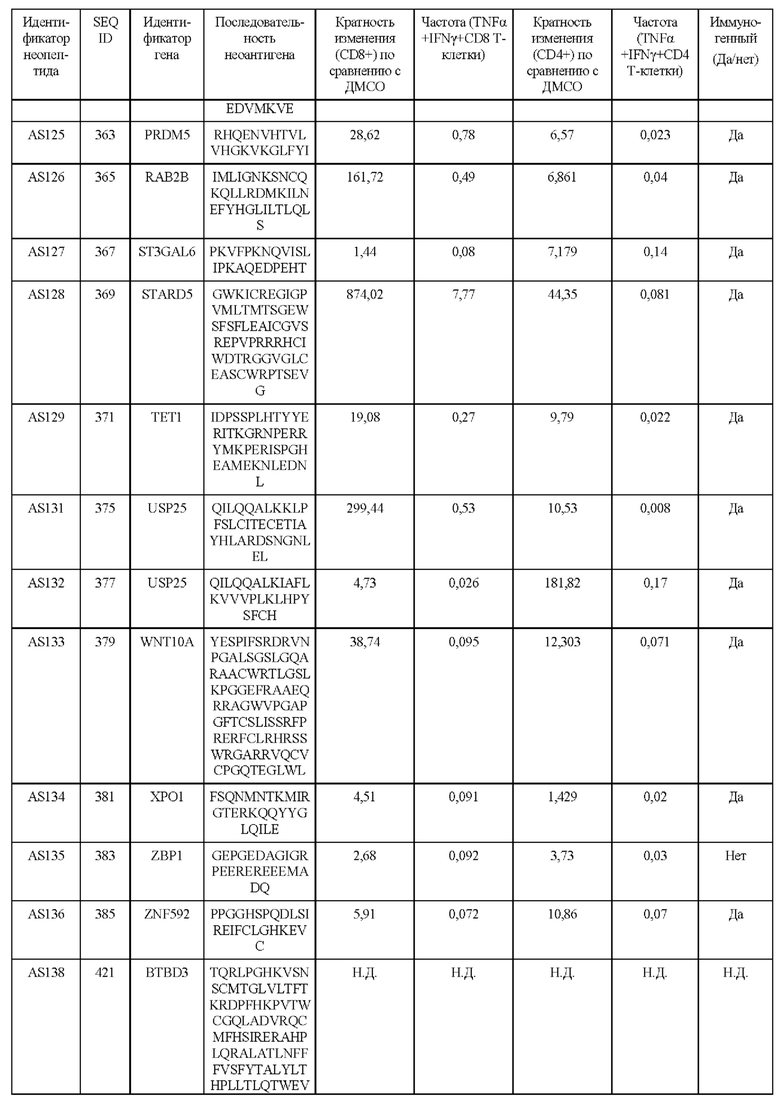
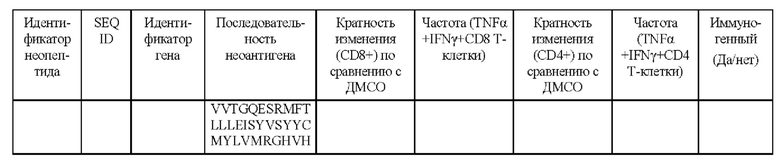
Пример 4: Прогнозирования связывания IILA
Аминокислотные последовательности неоантигенов, выявленных с использованием различных подходов, описанных в примере 1, разделяют на все возможные уникальные непрерывные 9-мерные аминокислотные фрагменты и выполняют прогнозирования связывания HLA с шестью обычными аллелями HLA (HLA-A*01:01, HLA-A*02:01, HLA-A*03:01, HLA-A*24:02, HLA-B*07:02, HLA-B*08:01) для каждого из этих 9-меров с использованием netMHCpan4.0. Для дополнительного анализа выбирают несколько 9-мерных фрагментов на основании ранжирования по вероятности связывания с одним или более из исследуемых аллелей HLA и их распространенности у пациентов с множественной миеломой.
Пример 5: Связывание неоантигенов с HLA in vitro
Связывание выбранных неоантигенов или их фрагментов с HLA-A*01:01, HLA-A*02:01, HLA-A*03:01, HLA-A*24:02, HLA-B*07:02 и HLA-B*08:01 или любыми другими HLA оценивают с использованием известных способов. Принцип способа кратко описан ниже и состоит из двух частей, одна из которых включает обмен пептида на положительный контроль под действием ультрафиолетового (УФ) излучения, а вторая представляет собой ферментативный иммуноанализ для обнаружения стабильного HLA-пептида и пустых комплексов HLA.
Связанные с HLA-клетками пептиды имеют решающее значение для стабильности комплекса HLA. Условный комплекс HLA класса I стабилизируют УФ-лабильным пептидом с использованием разного пептида (Pos) для каждого ULA(Pos: HLA-A*01:01: CTELKLSDY(SEQ ID NO: 409), HLA-A*02:01: NLVPMVATV (SEQ ID NO: 410), HLA-A*03:01: LIYRRRLMK (SEQ ID NO: 411), HLA-A*24:02: LYSACFWWL (SEQ ID NO: 412), HLA-B*07:02: NPKASLLSL (SEQ ID NO: 413), HLA-B*08:01: ELRSRYWAI (SEQ ID NO: 414)), который мог бы быть расщеплен Уф-излучением при связывании с молекулой HLA. После расщепления полученные в результате пептидные фрагменты диссоциируют от комплекса HLA класса I, поскольку их длина недостаточна для стабильного связывания с HLA. В условиях, в которых выполняют расщепление пептида (нейтральный рН на тающем льду), не содержащий пептид комплекс HLA остается стабильным. Таким образом, при выполнении расщепления в присутствии другого выбранного пептида HLA класса I эта реакция приводит к чистому обмену расщепленного УФ-лабильного пептида Pos на выбранный пептид (Rodenko, В et al. (2006) Nature Protocols 1: 1120-32, Toebes, M et al. (2006) Nat Med 12: 246-51, Bakker, AH et al. (2008) Proc Natl Acad Sci USA 105: 3825-30).
Эффективность обмена между интересующим пептидом и Pos анализируют с помощью ИФА HLA класса I. Комбинированные технологии позволяют идентифицировать лиганды для интересующей молекулы HLA, которые потенциально являются иммуногенными.
Обмен контрольным пептидом Pos показывает высокоаффинное связывание с соответствующим аллелем HLA класса I, тогда как обмен контрольным пептидом Neg является несвязывающим. УФ-контроль представляет собой УФ-излучение условного комплекса HLA класса I в отсутствие восстанавливающего пептида. Связывание обменного контрольного пептида Neg (HLA-A* 01: 01: NPKASLLSL (SEQ ID NO: 415), HLA-A*02-01: IVTDFSVIK (SEQ ID NO: 416), HLA-A*03:01: NPKASLLSL (SEQ ID NO: 417), HLA-A*24:02: NLVPMVATV (SEQ ID NO: 418), HLA-B*07:02: LIYRRRLMK (SEQ ID NO: 419), HLA-B*08:01: NLVPMVATV (SEQ ID NO: 420)) и все экспериментальные пептиды оценивают относительно таковых при замене контрольного пептида Pos. Абсорбцию последнего пептида устанавливают на уровне 100%. Эта процедура приводит к диапазону различных процентных долей обмена, которые отражают аффинности разных экспериментальных пептидов к используемому аллелю HLA.
ИФА HLA класса I представляет собой ферментный иммуноанализ, основанный на обнаружении бета-2-микроглобулина (В2М) (стабилизированного пептидом) комплексов HLA класса I. С этой целью стрептавидин связывают на полистирольных лунках для микротитрования. После промывки и блокирования комплекс HLA, присутствующий в реакционных смесях для обмена или контрольных смесях для ИФА, захватывают стрептавидином на титрационном микропланшете посредством его биотинилированной тяжелой цепи. Несвязанный материал удаляют промывкой. Впоследствии добавляют конъюгированное с пероксидазой хрена (HRP) антитело к человеческому В2М. Конъюгированное с HRP антитело связывается только с интактным комплексом HLA, присутствующим в лунке микротитрования, поскольку неудачный обмен пептидов приводит к разрушению исходного УФ-чувствительного комплекса HLA при УФ-освещении. В последнем случае на этапе промывки удаляют В2М. После удаления несвязанного HRP-конъюгата путем промывки в лунки добавляют раствор субстрата. Окрашенный продукт образовывается пропорционально количеству интактного комплекса HLA, присутствующего в образцах. После завершения реакции путем добавления стоп-раствора измеряют поглощение на считывающем устройстве для считывания титрационного микропланшета. Поглощение нормализуют до уровня поглощения заменяемого контрольного пептида (соответствует 100%). Субоптимальное связывание HLA пептидов с умеренной или низкой аффинностью к молекулам HLA класса I также можно обнаружить с помощью этого метода ИФА (Rodenko, В et al. (2006) Nature Protocols 1: 1120-32).
В соответствии с описанным в настоящем документе протоколом исследуемый аллель HLA имеет соответствующий пептид положительного (Pos) и отрицательного (Neg) контроля, на которые заменяют интересующий пептид. Таким образом, скорость обмена с Pos-пептидом, равная 100% означает, что интересующий пептид имеет такую же аффинность связывания с аллелем HLA, что и пептид положительного контроля. Пептиды со скоростью обмена по меньшей мере 10% с соответствующим Pes-пептидом для по меньшей мере одного из 6 аллелей HLA рассматриваются для дальнейшей оценки. Более высокие процентные значения соответствуют более сильному связыванию с аллелем HLA.
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
Следующий список вариантов осуществления предназначен для дополнения, а не замены или аннулирования предшествующих описаний.
Вариант осуществления 1.
Полипептид, содержащий по меньшей мере одну или более полипептидных последовательностей, выбранных из группы, состоящей из: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 393, 395, 397, 399, 401, 403, или 405, 407, или 421 или их фрагментов.
Вариант осуществления 2.
Полипептид, содержащий по меньшей мере одну или более полипептидных последовательностей, выбранных из группы, состоящей из: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 3.
Полипептид, содержащий два или более тандемных повторов SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 4.
Полипептид по любому из вариантов осуществления 1-3, в котором полипептидные последовательности соединены друг с другом в любом порядке.
Вариант осуществления 5.
Полипептид по варианту осуществления 2, который выбирают из:
аминокислотной последовательности SEQ ID NO: 7 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 7;
аминокислотной последовательности SEQ ID NO: 9 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 9;
аминокислотной последовательности SEQ ID NO: 11 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 11;
аминокислотной последовательности SEQ ID NO: 13 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 13;
аминокислотной последовательности SEQ ID NO: 17 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 17;
аминокислотной последовательности SEQ ID NO: 21 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 21;
аминокислотной последовательности SEQ ID NO: 23 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 23;
аминокислотной последовательности SEQ ID NO: 25 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 25;
аминокислотной последовательности SEQ ID NO: 27 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 27;
аминокислотной последовательности SEQ ID NO: 31 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 31;
аминокислотной последовательности SEQ ID NO: 33 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 33;
аминокислотной последовательности SEQ ID NO: 35 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 35;
аминокислотной последовательности SEQ ID NO: 37 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 37;
аминокислотной последовательности SEQ ID NO: 39 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 39;
аминокислотной последовательности SEQ ID NO: 41 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 41;
аминокислотной последовательности SEQ ID NO: 43 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 43;
аминокислотной последовательности SEQ ID NO: 45 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 45;
аминокислотной последовательности SEQ ID NO: 89 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 89;
аминокислотной последовательности SEQ ID NO: 47 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 47;
аминокислотной последовательности SEQ ID NO: 51 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 51;
аминокислотной последовательности SEQ ID NO: 53 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 53;
аминокислотной последовательности SEQ ID NO: 55 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 55;
аминокислотной последовательности SEQ ID NO: 59 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 59;
аминокислотной последовательности SEQ ID NO: 61 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 61;
аминокислотной последовательности SEQ ID NO: 63 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 63;
аминокислотной последовательности SEQ ID NO: 67 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 67;
аминокислотной последовательности SEQ ID NO: 69 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 69;
аминокислотной последовательности SEQ ID NO: 71 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 71;
аминокислотной последовательности SEQ ID NO: 75 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 75;
аминокислотной последовательности SEQ ID NO: 79 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 79;
аминокислотной последовательности SEQ ID NO: 81 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 81;
аминокислотной последовательности SEQ ID NO: 83 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 83;
аминокислотной последовательности SEQ ID NO: 87 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 87;
аминокислотной последовательности SEQ ID NO: 91 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 91;
аминокислотной последовательности SEQ ID NO: 147 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 147;
аминокислотной последовательности SEQ ID NO: 101 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 101;
аминокислотной последовательности SEQ ID NO: 103 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 103;
аминокислотной последовательности SEQ ID NO: 105 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 105;
аминокислотной последовательности SEQ ID NO: 109 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 109;
аминокислотной последовательности SEQ ID NO: 111 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 111;
аминокислотной последовательности SEQ ID NO: 113 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 113;
аминокислотной последовательности SEQ ID NO: 119 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 119;
аминокислотной последовательности SEQ ID NO: 121 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 121;
аминокислотной последовательности SEQ ID NO: 123 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 123;
аминокислотной последовательности SEQ ID NO: 125 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 125;
аминокислотной последовательности SEQ ID NO: 131 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 131;
аминокислотной последовательности SEQ ID NO: 133 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 133;
аминокислотной последовательности SEQ ID NO: 135 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 135;
аминокислотной последовательности SEQ ID NO: 143 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 143;
аминокислотной последовательности SEQ ID NO: 145 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 145;
аминокислотной последовательности SEQ ID NO: 149 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 149;
аминокислотной последовательности SEQ ID NO: 221 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 221;
аминокислотной последовательности SEQ ID NO: 151 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 151;
аминокислотной последовательности SEQ ID NO: 157 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 157;
аминокислотной последовательности SEQ ID NO: 161 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 161;
аминокислотной последовательности SEQ ID NO: 163 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 163;
аминокислотной последовательности SEQ ID NO: 165 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 165;
аминокислотной последовательности SEQ ID NO: 171 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 171;
аминокислотной последовательности SEQ ID NO: 173 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 173;
аминокислотной последовательности SEQ ID NO: 179 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 179;
аминокислотной последовательности SEQ ID NO: 185 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 185;
аминокислотной последовательности SEQ ID NO: 187 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 187;
аминокислотной последовательности SEQ ID NO: 197 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 197;
аминокислотной последовательности SEQ ID NO: 199 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 199;
аминокислотной последовательности SEQ ID NO: 207 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 207;
аминокислотной последовательности SEQ ID NO: 213 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 213;
аминокислотной последовательности SEQ ID NO: 217 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 217;
аминокислотной последовательности SEQ ID NO: 223 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 223;
аминокислотной последовательности SEQ ID NO: 301 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 301;
аминокислотной последовательности SEQ ID NO: 225 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 225;
аминокислотной последовательности SEQ ID NO: 241 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 241;
аминокислотной последовательности SEQ ID NO: 247 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 247;
аминокислотной последовательности SEQ ID NO: 249 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 249;
аминокислотной последовательности SEQ ID NO: 259 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 259;
аминокислотной последовательности SEQ ID NO: 265 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 265;
аминокислотной последовательности SEQ ID NO: 267 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 267;
аминокислотной последовательности SEQ ID NO: 269 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 269;
аминокислотной последовательности SEQ ID NO: 281 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 281;
аминокислотной последовательности SEQ ID NO: 285 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 285;
аминокислотной последовательности SEQ ID NO: 287 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 287;
аминокислотной последовательности SEQ ID NO: 289 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 289;
аминокислотной последовательности SEQ ID NO: 293 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 293;
аминокислотной последовательности SEQ ID NO: 297 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 297;
аминокислотной последовательности SEQ ID NO: 299 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 299;
аминокислотной последовательности SEQ ID NO: 303 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 303;
аминокислотной последовательности SEQ ID NO: 365 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 365;
аминокислотной последовательности SEQ ID NO: 305 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 305;
аминокислотной последовательности SEQ ID NO: 307 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 307;
аминокислотной последовательности SEQ ID NO: 329 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 329;
аминокислотной последовательности SEQ ID NO: 331 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 331;
аминокислотной последовательности SEQ ID NO: 333 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 333;
аминокислотной последовательности SEQ ID NO: 335 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 335;
аминокислотной последовательности SEQ ID NO: 337 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 337;
аминокислотной последовательности SEQ ID NO: 339 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 339;
аминокислотной последовательности SEQ ID NO: 341 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 341;
аминокислотной последовательности SEQ ID NO: 343 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 343;
аминокислотной последовательности SEQ ID NO: 345 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 345;
аминокислотной последовательности SEQ ID NO: 349 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 349;
аминокислотной последовательности SEQ ID NO: 359 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 359;
аминокислотной последовательности SEQ ID NO: 361 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 361;
аминокислотной последовательности SEQ ID NO: 363 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 363;
аминокислотной последовательности SEQ ID NO: 367 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 367;
аминокислотной последовательности SEQ ID NO: 369 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 369;
аминокислотной последовательности SEQ ID NO: 371 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 371;
аминокислотной последовательности SEQ ID NO: 375 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 375;
аминокислотной последовательности SEQ ID NO: 377 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 377;
аминокислотной последовательности SEQ ID NO: 379 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 379;
аминокислотной последовательности SEQ ID NO: 381 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 381;
аминокислотной последовательности SEQ ID NO: 383 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 383;
аминокислотной последовательности SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 385;
аминокислотной последовательности SEQ ID NO: 385 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 385;
аминокислотной последовательности SEQ ID NO: 421 или имеющий по меньшей мере 90% идентичность последовательности SEQ ID NO: 421;
и их комбинации.
Вариант осуществления 6.
Полинуклеотид, кодирующий полипептид по любому из вариантов осуществления 1-5.
Вариант осуществления 7.
Полинуклеотид по варианту осуществления 6, который выбирают из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 394, 396, 398, 400, 402, 404, или 406, 408, или 422 или их фрагментов.
Вариант осуществления 8.
Вектор, содержащий полинуклеотид по варианту осуществления 6 или варианту осуществления 7.
Вариант осуществления 9.
Вектор по варианту осуществления 8, который выбран из аденовирусного вектора, альфавирусного вектора, вектора на основе поксвируса, аденоассоциированного вирусного вектора, ретровирусного вектора, самореплицирующейся молекулы РНК и их комбинации.
Вариант осуществления 10.
Вектор по варианту осуществления 9, в котором аденовирусный вектор выбран из hAd5, hAd7, hAd11, hAd26, hAd34, hAd35, hAd48, hAd49, hAd50, GAd20, Gadl9, GAd21, GAd25, GAd26, GAd27, GAd28, GAd29, GAd30, GAd31, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAdl6, ChAdI7, ChAdl9, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAdl46, ChAdl47, PanAd1, PanAd2 и PanAd3.
Вариант осуществления 11.
Вектор по варианту осуществления 9, в котором вектор на основе поксвируса выбран из вектора вируса оспы, вектора вируса осповакцины, вектора вируса коровьей оспы, вектора вируса оспы обезьян, вектора вируса осповакцины Копенгаген (W), вектора вируса осповакцины Нью-Йорк (NYVAC) и вектора модифицированного вируса осповакцины Анкара (MVA).
Вариант осуществления 12.
Вектор по варианту осуществления 9, который представляет собой аденовирусный вектор, содержащий полинуклеотид, кодирующий любой из полипептидов одного из вариантов осуществления 1-5.
Вариант осуществления 13.
Вектор по варианту осуществления 9, который представляет собой поксвирусный вектор, содержащий полинуклеотид, кодирующий любой из полипептидов одного из вариантов осуществления 1-5.
Вариант осуществления 14.
Вектор по варианту осуществления 9, который представляет собой самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий любой из полипептидов любого из вариантов осуществления 1-5.
Вариант осуществления 15.
Фармацевтическая композиция, содержащая полипептид по любому из вариантов осуществления 1-5.
Вариант осуществления 16.
Фармацевтическая композиция, содержащая полинуклеотид по любому из вариантов осуществления 6 и 7.
Вариант осуществления 17.
Фармацевтическая композиция, содержащая вектор по любому из вариантов осуществления 8-14.
Вариант осуществления 18.
Фармацевтическая композиция по варианту осуществления 17, в которой вектор выбран из вектора Ad26, вектора MVA, вектора GAd20, самореплицирующейся молекулы РНК и их комбинаций.
Вариант осуществления 19.
Фармацевтическая композиция по варианту осуществления 18, в которой вектор представляет собой вектор Ad26, содержащий
полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, или
полинуклеотид, кодирующий один или более полипептидов, имеющих по меньшей мере 90% идентичность последовательности с SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 20.
Фармацевтическая композиция по варианту осуществления 18, в которой вектор представляет собой вектор GAd20, содержащий
Полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, или
полинуклеотид, кодирующий один или более полипептидов, имеющих по меньшей мере 90% идентичность последовательности с SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 21.
Фармацевтическая композиция по варианту осуществления 18, в которой вектор представляет собой вектор MVA, содержащий
полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, или
полинуклеотид, кодирующий один или более полипептидов, имеющих по меньшей мере 90% идентичность последовательности SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментам.
Вариант осуществления 22.
Фармацевтическая композиция по варианту осуществления 18, в которой вектор представляет собой самореплицирующуюся молекулу РНК, содержащую
полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, или
полинуклеотид, кодирующий один или более полипептидов, имеющих по меньшей мере 90% идентичность последовательности с SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 23.
Способ индукции иммунного ответа у субъекта, включающий введение субъекту, нуждающемуся в этом, фармацевтической композиции по любому из вариантов осуществления 15-22.
Вариант осуществления 24.
Способ индукции иммунного ответа у субъекта, включающий введение субъекту, нуждающемуся в этом, композиции, содержащей рекомбинантный вирус, и/или композиции, содержащей самореплицирующуюся молекулу РНК, причем рекомбинантный вирус или самореплицирующаяся молекула РНК содержат полинуклеотид, кодирующий по меньшей мере один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 25.
Способ по варианту осуществления 23 или 24, в котором субъект экспрессирует или предположительно экспрессирует один или более полипептидов по п. 1.
Вариант осуществления 26.
Способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта, включающий введение субъекту, нуждающемуся в этом, фармацевтической композиции по любому из вариантов осуществления 15-22.
Вариант осуществления 27.
Способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта, включающий введение нуждающемуся в этом субъекту композиции, содержащей рекомбинантный вирус, и/или композиции, содержащей самореплицирующуюся молекулу РНК, причем рекомбинантный вирус или самореплицирующаяся молекула РНК содержат полинуклеотид, кодирующий по меньшей мере один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69,71,75, 79,81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 28.
Способ лечения, предотвращения, снижения риска возникновения или отсрочки возникновения клинического состояния множественной миеломы у субъекта, включающий введение нуждающемуся в этом субъекту композиции, содержащей рекомбинантный вирус, и/или композиции, содержащей самореплицирующуюся молекулу РНК, причем рекомбинантный вирус или самореплицирующаяся молекула РНК содержат полинуклеотид, кодирующий по меньшей мере один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и при этом введение включает одно или более введений композиции.
Вариант осуществления 29.
Способ по любому из вариантов осуществления 23-28, в котором вирус или рекомбинантный вирус выбран из Ad26, MVA, GAd20 и их комбинаций.
Вариант осуществления 30.
Способ по варианту осуществления 29, в котором рекомбинантный вирус представляет собой вирус Ad26, содержащий полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 31.
Способ по варианту осуществления 29, в котором рекомбинантный вирус представляет собой вирус GAd20, содержащий полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 32.
Способ по варианту осуществления 29, в котором рекомбинантный вирус представляет собой вирус MVA, содержащий полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 33.
Способ по варианту осуществления 29, в котором самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов.
Вариант осуществления 34.
Способ по любому из вариантов осуществления 23-33, включающий один или более циклов лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20.
Вариант осуществления 35.
Способ по любому из вариантов осуществления 23-33, включающий один или более циклов лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
третье введение, включающее вторую композицию, содержащую рекомбинантный вирус, содержащий полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20.
Вариант осуществления 36.
Способ по любому из вариантов осуществления 23-33, включающий один или более циклов лечения, причем каждый цикл включает:
первое введение, включающее первую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
второе введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69,71,75, 79,81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
третье введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61,63, 67, 69,71,75, 79,81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20; и
четвертое введение, включающее вторую композицию, содержащую рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий один или более полипептидов из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 или 421 или их фрагментов, и причем рекомбинантный вирус выбирают из Ad26, MVA или GAd20.
Вариант осуществления 37.
Способ по вариантам осуществления 34-36, в котором первое, второе, третье или четвертое введение включают различный рекомбинантный вирус.
Вариант осуществления 38.
Способ по вариантам осуществления 34-37, в котором первое, второе, третье или четвертое введение включают рекомбинантный вирус, содержащий полинуклеотид, кодирующий полипептид с различной аминокислотной последовательностью.
Вариант осуществления 39.
Способ по любому из вариантов осуществления 26-38, дополнительно включающий введение второго терапевтического агента, выбранного из антитела к CTLA-4, антитела к PD-1, антитела к PD-L1, агониста TLR, агониста CD40, агониста ОХ40, гидроксимочевины, руксолитиниба, федратиниба, агониста 41 ВВ, агониста CD28, лиганда FLT3, сульфата алюминия, ингибитора ВТК, ингибитора JAK, антитела к CD38, ингибитора CDK, антитела к CD33, антитела к CD37, антитела к CD25, ингибитора GM-CSF, IL-2, IL-15, IL-7, IFNγ, IFNα, TNFα, антитела к VEGF, антитела к CD70, антитела к CD27, антитела к ВСМА, антитела к GPRC5D и их комбинаций.
Вариант осуществления 40.
Способ по варианту осуществления 25-39, в котором множественная миелома представляет собой моноклональную гаммапатию неясного генеза (MGUS) не IgM типа или тлеющую множественную миелому (SMM) или их комбинацию.
Вариант осуществления 41.
Способ по варианту осуществления 23-40, в котором один или более полипептидов по п. 1 присутствуют с частотой по меньшей мере около 1% или более, около 2% или более, около 3% или более, около 4% или более, около 5% или более, около 6% или более, около 7% или более, около 8% или более, около 9% или более, около 10% или более, около 11% или более, около 12% или более, около 13% или более, около 14% или более, около 15% или более, около 16% или более, около 17% или более, около 18% или более, около 19% или более, около 20% или более, около 21% или более, около 22% или более, около 23% или более, около 24% или более, около 25% или более, около 26% или более, около 27% или более, около 28% или более, около 29% или более, около 30% или более, около 35% или более, около 40% или более, около 45% или более, около 50% или более, около 55% или более, около 60% или более, около 65% или более или около 70% или более у популяции субъектов, страдающих множественной миеломой.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ЯНССЕН БАЙОТЕК, ИНК.
<120> НЕОАНТИГЕНЫ, ЭКСПРЕССИРУЕМЫЕ ПРИ МНОЖЕСТВЕННОЙ МИЕЛОМЕ, И ИХ
ПРИМЕНЕНИЕ
<130> JBI6239WOPCT1
<140>
<141>
<150> 62/976,386
<151> 2020-02-14
<160> 425
<170> PatentIn, версия 3.5
<210> 1
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 1
Ile Ser Asn Lys Ile Ala Leu Leu Gln Thr Phe
1 5 10
<210> 2
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 2
atatctaata agatagcctt actgcaaacc ttt 33
<210> 3
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 3
Trp Leu Val Lys Gln Arg Gly Trp Ala Asn Leu Leu Glu Lys Ser Ala
1 5 10 15
Glu Gln Ile Cys Thr Gly Glu Phe Lys Ala Lys Ala Ser Gln Ser
20 25 30
<210> 4
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 4
tggctagtta aacaaagagg ctgggcaaac cttttagaga agtcagctga gcaaatatgt 60
acaggtgaat tcaaagcaaa agcctcacaa agt 93
<210> 5
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 5
Asn His Glu Thr Ala Phe Gln Gly Lys Pro Phe Arg Glu Val Ser
1 5 10 15
<210> 6
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 6
aaccacgaga cggccttcca aggcaaacct tttagagaag tcagc 45
<210> 7
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 7
Asp Val Ala Val Ile Cys Ser Gly Arg Arg Ser Ala Arg Asp Pro
1 5 10 15
<210> 8
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 8
gatgtggctg tcatctgctc aggaagacgt tcagccaggg atcca 45
<210> 9
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 9
Asp Val Ala Val Ile Cys Ser Gly Val Pro Val Ala Asp Val Ser
1 5 10 15
<210> 10
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 10
gatgtggctg tcatctgctc aggggtccct gtcgctgatg tgagc 45
<210> 11
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 11
Glu Asp Val Ala Val Ile Cys Ser Glu Leu Phe Leu Ile Ala Ser Pro
1 5 10 15
<210> 12
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 12
gaagatgtgg ctgtcatctg ctcagagctg tttttgatag ccagcccc 48
<210> 13
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 13
Gly Arg Ala Gly Gln Gly Gly Gly Met Ile Ser Val Ser Gln Glu Phe
1 5 10 15
Ile Lys
<210> 14
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 14
ggtcgtgcag gccagggagg aggcatgatt tctgtgagtc aggaattcat taag 54
<210> 15
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 15
Ala Val Leu Lys Leu Thr Asp Gln His Asn Ala Val Lys Met Gly Glu
1 5 10 15
Glu Arg Cys Val Ser Ser Glu Ile
20
<210> 16
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 16
gcagtgctca aactcaccga ccagcataat gcagtgaaga tgggtgaaga gagatgtgtt 60
tcatctgaaa tt 72
<210> 17
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 17
Ser Gly Leu Leu Met Asn Thr Leu Thr Val Leu Ile Leu Tyr Phe Leu
1 5 10 15
Tyr
<210> 18
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 18
agtggccttc tgatgaatac tttaactgtg ctgatcctgt atttcctgta t 51
<210> 19
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 19
Ala Pro Lys Pro Lys Lys Met Lys Asn His Leu Leu Phe Trp
1 5 10
<210> 20
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 20
gctcctaagc ccaagaagat gaagaaccat ttgcttttct gg 42
<210> 21
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 21
Gly Lys Ser Thr Pro Pro Arg Lys Glu Ile Phe Asp Asp Ala Ser Pro
1 5 10 15
<210> 22
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 22
gggaaatcca caccaccacg taaggaaata tttgatgatg cgtcacct 48
<210> 23
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 23
Ala Arg Trp Phe Thr Arg Glu Gln Gly Ser Glu Asn
1 5 10
<210> 24
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 24
gcccgctggt tcactagaga acagggcagt gaaaac 36
<210> 25
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 25
Ala Phe Ile Tyr His Ala Phe Val Gly Ser Thr Lys Thr Ala Trp Arg
1 5 10 15
Thr Thr Leu
<210> 26
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 26
gcgttcatct accacgcttt cgttgggtca accaaaaccg catggcgtac tactctc 57
<210> 27
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 27
Leu Ala Arg Gln Ile Ser Phe Lys Ser Leu Ile
1 5 10
<210> 28
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 28
ctggctaggc aaataagctt taagtcactt ata 33
<210> 29
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 29
Gln Pro Arg Asp Asn His Thr Asp Gln Val Thr Tyr Ile Arg Arg Thr
1 5 10 15
Leu Met
<210> 30
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 30
cagccaagag acaaccacac tgatcaagtc acttatataa gaagaacctt gatg 54
<210> 31
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 31
Pro Arg Asp Asn His Thr Asp His Glu Asn Pro Arg Gly Ser Asp Gly
1 5 10 15
Gln Gly Arg Trp Lys Cys Pro Ser Gln Val Thr Tyr Ile Arg Arg Thr
20 25 30
Leu Met
<210> 32
<211> 102
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 32
ccaagagaca accacactga tcatgaaaac ccaagaggaa gcgatggaca gggcaggtgg 60
aaatgcccaa gccaagtcac ttatataaga agaaccttga tg 102
<210> 33
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 33
Ala Ala Gly Val Val Thr Glu Ile Glu Ala Ala Val Lys Ala
1 5 10
<210> 34
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 34
gctgctggtg ttgtcactga gatcgaagcc gcggtcaagg cc 42
<210> 35
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 35
Asn Ala Val Arg Ser Tyr Tyr Glu Gly Thr Glu Asn Ile Val Ala Val
1 5 10 15
<210> 36
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 36
aacgcagttc ggagttatta tgaggggacg gaaaatatag tcgcggtg 48
<210> 37
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 37
Asn Ala Val Arg Ser Tyr Tyr Glu Thr Asn Gly Gly Met Ser Phe Leu
1 5 10 15
Arg Ile Thr Pro
20
<210> 38
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 38
aacgcagttc ggagttatta tgagacaaat ggaggcatga gcttccttag aattacccct 60
<210> 39
<211> 50
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 39
Ile Ser Lys Arg Leu Lys Ser Arg Arg Arg Ser Gly Trp Gln Leu Asn
1 5 10 15
Arg Ala Gly Asn Arg Gly Leu Ser Pro Gly Leu Gly Leu Phe Pro Arg
20 25 30
Gly Cys Cys Arg Trp Gly Gly Ala Tyr Thr Arg Leu Pro Ser Ala Asn
35 40 45
Gln Thr
50
<210> 40
<211> 150
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 40
atcagcaagc gactcaagag cagaaggaga tccggttggc agctaaaccg cgctgggaac 60
aggggcctga gtcctggact agggctcttt ccccggggct gctgcagatg gggaggagcc 120
tacacccgcc tcccgagtgc taatcagacc 150
<210> 41
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 41
Pro Pro Thr Ala Ala Ala Ser Gln Thr Cys Leu Glu Leu Glu Arg
1 5 10 15
<210> 42
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 42
ccacccaccg ccgccgcctc ccagacctgc ctagagctgg aacgt 45
<210> 43
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 43
Ala Cys Gly Ala Cys Gly Ala Gly Phe Phe Ile Lys Gln Lys Cys Ile
1 5 10 15
Glu Gln Arg Glu Ser Arg Ser Leu Ser
20 25
<210> 44
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 44
gcctgcggag cctgtggggc aggatttttt atcaagcaga aatgcatcga acaacgagaa 60
tcaagatcac tgagc 75
<210> 45
<211> 84
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 45
Val Tyr Pro Val Tyr Gln Pro Val Val Ser Gln Ala Gly Leu Gly Glu
1 5 10 15
Leu Trp Gln Trp Ala Ser Gly Lys Leu Arg Gly Tyr Cys Trp Arg Arg
20 25 30
Gly Gln Trp His Ala Tyr Ser Ile Gln Cys Asp Pro His Pro Val Phe
35 40 45
Gly Glu Gly Ala Cys Asp Cys Ser Glu Thr Glu Ala His Gly Gly Cys
50 55 60
Gln Ser Pro Arg Leu Glu Ser Phe Pro Gly Gln Pro Pro Gly Phe Arg
65 70 75 80
Gly Gln Arg Phe
<210> 46
<211> 252
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 46
gtgtaccctg tctaccagcc tgtggtttca caagctggtc tgggggagct ttggcagtgg 60
gcttctggaa agctccgggg ttattgttgg cggcggggac aatggcatgc ttattctata 120
caatgtgacc cacatcctgt cttcggggaa ggagcctgtg attgctcaga aacagaagca 180
cacgggggct gtcagagccc tcgacttgaa tcctttccag ggcaacctcc tggcttcagg 240
ggccagcgat tc 252
<210> 47
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 47
Ser Gly Leu Glu Ala Ile Gln Arg Gly Tyr Glu Thr Phe Tyr Ser Glu
1 5 10 15
<210> 48
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 48
tctggcctgg aggctatcca gcggggatat gagactttct actcggaa 48
<210> 49
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 49
Ser Pro Glu Asp Tyr Thr Leu Lys Ala Gln Gly Pro Gly Gln Cys Pro
1 5 10 15
<210> 50
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 50
tccccagagg actacacgct caaggcccag ggccccggcc agtgccca 48
<210> 51
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 51
Ala Arg His Leu Leu Thr Leu Gly Thr Cys Gly Ser Thr Trp Pro
1 5 10 15
<210> 52
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 52
gcgaggcact tgctaactct tgggacatgc ggaagcacgt ggcca 45
<210> 53
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 53
Pro Gln Glu Glu Val Pro Phe Arg Ser Ile Thr Thr Glu Leu Phe Pro
1 5 10 15
Ser Met Cys
<210> 54
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 54
ccacaggaag aagtgccatt caggtcaata acaacggagt tgtttccttc aatgtgc 57
<210> 55
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 55
Gln Ile Ile Tyr Asp Glu Asn Arg Thr Met Gln Ile Phe Val Lys Thr
1 5 10 15
<210> 56
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 56
cagatcatct acgacgagaa ccggacaatg cagatcttcg tgaagact 48
<210> 57
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 57
Gly Glu Arg Glu Arg Arg Glu Lys Thr Met Gln Ile Phe Val Lys Thr
1 5 10 15
<210> 58
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 58
ggcgagcgcg agcggcgcga gaaaacaatg cagatcttcg tgaagact 48
<210> 59
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 59
Met Asp Leu Thr Ala Ile Tyr Glu Thr Met Gln Ile Phe Val Lys Thr
1 5 10 15
<210> 60
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 60
atggatctga ctgccatcta cgagacaatg cagatcttcg tgaagact 48
<210> 61
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 61
Pro Pro Thr Ala Ala Ala Ser Gln Thr Met Gln Ile Phe Val Lys Thr
1 5 10 15
<210> 62
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 62
ccacccaccg ccgccgcctc ccagacaatg cagatcttcg tgaagact 48
<210> 63
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 63
Ser Ser Val Thr Thr His Ser Ser Gly Asn Leu Arg Glu Ser Pro Ile
1 5 10 15
Tyr His
<210> 64
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 64
tcttctgtga ctacccactc atctggaaat ttgcgagaat ccccgattta tcat 54
<210> 65
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 65
Ser Gly Leu Glu Ala Ile Gln Arg Glu Lys Pro Tyr His Cys Asn Trp
1 5 10 15
<210> 66
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 66
tctggcctgg aggctatcca gcgtgagaag ccctaccact gcaactgg 48
<210> 67
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 67
Val Ala Pro Ser Gly Leu Tyr Tyr Cys Gly
1 5 10
<210> 68
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 68
gtggcaccca gtggcctgta ctactgtgga 30
<210> 69
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 69
Asn Arg Val Thr Ala Leu Thr Gln Asn
1 5
<210> 70
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 70
aacagggtca cagctctcac ccagaac 27
<210> 71
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 71
Ile Glu Lys Ser Ile Ser Ala Arg Ile Thr Glu Gln
1 5 10
<210> 72
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 72
atagagaaat caatttctgc taggatcaca gaacaa 36
<210> 73
<211> 64
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 73
Pro Ser Asp Cys Ser Ile Arg Lys Thr Leu Leu Ser Leu Pro Gly Gly
1 5 10 15
Val Glu Thr Gly Thr Arg Arg Ser Cys Leu Thr Arg Arg Pro Arg Pro
20 25 30
Gly Ser Val Arg Asp Ser Arg Asp Leu Trp Leu Gln Thr Pro Pro Ala
35 40 45
Arg Arg Pro Arg Ala Gly Ala Leu Leu Arg Met Arg Leu Trp Gly Pro
50 55 60
<210> 74
<211> 192
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 74
ccaagtgact gctccattcg gaagactttg ttgtcgctgc ccggaggagt cgagactggt 60
acccggagga gctgtctcac caggagacca cgtcctggaa gtgtccggga ctcgcgggac 120
ctgtggctgc agaccccgcc ggcacgcagg cccagagctg gcgcactcct gaggatgaga 180
ctctgggggc cc 192
<210> 75
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 75
Gly Glu Val Lys Trp Ser Val Gly Ser Arg Thr Ser Leu Leu Leu
1 5 10 15
<210> 76
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 76
ggggaagtga agtggtctgt aggctcccgg acgtccctgc tcctg 45
<210> 77
<211> 61
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 77
Leu Thr Glu Lys Lys Ala Ser Asp Val Arg Ser Pro Thr Thr Ala Thr
1 5 10 15
Gly Thr Ala Ala Ala Gly Ser Leu Arg Ala Gln Thr Ser Ser Arg Ala
20 25 30
Thr Thr Glu Ser Thr Arg Ala Thr Gly His Ser Ser Ala Ile Cys Ala
35 40 45
Ile Val Pro Ser Arg Ala Pro Ile Thr Trp Arg Cys Thr
50 55 60
<210> 78
<211> 183
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 78
ctcacggaga agaaggcctc cgacgtgaga agccctacca ctgcaactgg gacggctgcg 60
gctggaagtt tgcgcgctca gacgagctca cgcgccacta ccgaaagcac acgggccacc 120
ggccattcca gtgccatctg tgcgatcgtg ccttctcgcg ctccgatcac ctggcgctgc 180
aca 183
<210> 79
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 79
Cys Arg Glu Arg Gly Leu Gln Glu Ala Glu Gly Asp Val Ala Ala Leu
1 5 10 15
<210> 80
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 80
tgccgcgagc gcggcctgca ggaggctgaa ggtgatgtgg ccgccctc 48
<210> 81
<211> 61
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 81
Pro Pro Thr Ala Ala Ala Ser Gln Val Arg Ser Pro Thr Thr Ala Thr
1 5 10 15
Gly Thr Ala Ala Ala Gly Ser Leu Arg Ala Gln Thr Ser Ser Arg Ala
20 25 30
Thr Thr Glu Ser Thr Arg Ala Thr Gly His Ser Ser Ala Ile Cys Ala
35 40 45
Ile Val Pro Ser Arg Ala Pro Ile Thr Trp Arg Cys Thr
50 55 60
<210> 82
<211> 183
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 82
ccacccaccg ccgccgcctc ccaggtgaga agccctacca ctgcaactgg gacggctgcg 60
gctggaagtt tgcgcgctca gacgagctca cgcgccacta ccgaaagcac acgggccacc 120
ggccattcca gtgccatctg tgcgatcgtg ccttctcgcg ctccgatcac ctggcgctgc 180
aca 183
<210> 83
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 83
Gly Gly Pro Pro Phe Val Gly Pro Leu Arg Gly Pro Arg Ala Gln Pro
1 5 10 15
Ser Leu Ser Gly Leu Cys Gly Arg Arg Thr Gly Ser Arg Asp Thr Ile
20 25 30
Lys Ile Pro Gly Gln Thr
35
<210> 84
<211> 114
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 84
ggtggccctc cttttgtagg cccgcttcgg gggccgcgtg cccagcctag cctatccgga 60
ctgtgcggga ggcggacggg gagcagagac acaataaaaa ttcccggtca aacc 114
<210> 85
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 85
Gly Leu Lys Gln Leu His Lys Ala Gly Tyr Glu Glu Glu Thr Gln Asn
1 5 10 15
Asn Arg Ser Gly Leu Trp Asn Tyr Met Glu Leu Trp Gln Ala Ala Leu
20 25 30
<210> 86
<211> 96
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 86
ggtttgaaac agcttcacaa ggcaggttat gaagaagaaa ctcaaaataa caggagtggc 60
ttatggaact acatggagct ctggcaggct gccctg 96
<210> 87
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 87
Leu Asp Gln Cys Val Glu Thr Leu Cys Ser Leu Ser Lys Ser Asp
1 5 10 15
<210> 88
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 88
ctggaccagt gtgtggagac cctctgctcc ctcagcaagt cggac 45
<210> 89
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 89
Leu Leu Pro Pro Gly Gln Glu Ser Ala Ile Ile Gly Pro Pro Gly Met
1 5 10 15
Gln
<210> 90
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 90
ctccttccac ctggccagga atcagccatt attggacccc ctggaatgca a 51
<210> 91
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 91
Tyr Glu Cys Thr Gly Cys Lys Thr Ser Phe Pro His Arg Ser Gln Ser
1 5 10 15
<210> 92
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 92
tatgaatgta ctggatgcaa aacgagcttc ccacacagaa gccagagc 48
<210> 93
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 93
Gln His Pro Ala Arg Leu Val Lys Cys Gly Thr Gln
1 5 10
<210> 94
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 94
caacatcctg ctagacttgt taagtgtgga acacaa 36
<210> 95
<211> 56
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 95
Gly Leu Thr Leu Gly Ala Arg Thr Thr Leu Thr His Gly Ser Pro Gly
1 5 10 15
Pro Ser Gln Ala Thr Val Ala Val Ala Pro Leu Ser Gly Arg Ala Ala
20 25 30
Val Ser Ala Ala Gly Gly Cys Val Phe Leu Leu Leu Pro Ala Cys Val
35 40 45
Pro Arg Arg Cys His Trp Ile Pro
50 55
<210> 96
<211> 168
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 96
ggcctgactc tgggagcacg cactactctg acccatggat cccctgggcc cagccaagcc 60
acagtggctg tggcgccgct gtctggccgg gctgctgttt cagctgctgg tggctgtgtg 120
tttcttctcc tacctgcgtg tgtcccgaga cgatgccact ggatcccc 168
<210> 97
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 97
Met Asp Leu Thr Ala Ile Tyr Glu Cys Cys Asn Leu Ser Val Ser Glu
1 5 10 15
<210> 98
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 98
atggatctga ctgccatcta cgagtgctgc aacctgagcg tgagcgag 48
<210> 99
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 99
Val Ile Val Asp Pro Ile Gln Gly Tyr Leu Arg Gln Trp Gln Leu Leu
1 5 10 15
Asp
<210> 100
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 100
gtaattgtgg accctataca gggatacctc agacaatggc agcttttgga t 51
<210> 101
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 101
Pro Pro Leu Ile Thr Asn Val Thr Glu Lys Pro Trp Lys His Thr Arg
1 5 10 15
Ile Glu Met Pro Leu Ala Arg Leu Thr Arg Pro
20 25
<210> 102
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 102
ccgccactca tcaccaatgt cacggaaaag ccgtggaaac acacccggat tgaaatgccc 60
ctggcccgcc tgacccgacc c 81
<210> 103
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 103
Met Glu Pro Thr Thr Lys Arg Gly Pro Gly Gly Thr Met Val Ser Ala
1 5 10 15
Ala Ala Pro Ser
20
<210> 104
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 104
atggaaccta ctaccaaaag aggtcctggg ggcaccatgg tttcggcggc agcccccagc 60
<210> 105
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 105
Arg Pro Gly Val Phe Thr Asp Ile Leu
1 5
<210> 106
<211> 27
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 106
aggcctggag tattcacaga cattctt 27
<210> 107
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 107
Met Asp Leu Thr Ala Ile Tyr Glu Asp Ser Ala Gly Pro Leu Ser His
1 5 10 15
Ala
<210> 108
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 108
atggatctga ctgccatcta cgaggactct gctgggccgc tcagccatgc c 51
<210> 109
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 109
Leu Arg Tyr Leu Ile His Leu Arg Lys Trp Lys Ile Lys
1 5 10
<210> 110
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 110
ttacgctacc tcatacatct gaggaaatgg aagataaag 39
<210> 111
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 111
Phe Ala Leu Met Ala Ser Leu Gly Ile Pro Gln Thr Met Ala Ala
1 5 10 15
<210> 112
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 112
tttgcactta tggcctctct ggggatacct cagacaatgg cagct 45
<210> 113
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 113
Arg Gln Leu Gln Gln Gln Leu Ser Ser Leu Ser Gly Pro Glu Gly Val
1 5 10 15
Pro Phe Leu Lys Leu Trp Cys Leu Asp Asp Leu Leu Ser Thr Leu Leu
20 25 30
Gly Thr Cys Arg Cys Pro Ser Arg Ala Gln Phe
35 40
<210> 114
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 114
cggcaacttc aacaacagct ctctagcctg tctggccctg agggagtccc ctttctgaag 60
ctgtggtgct tggacgacct gctctctaca ttgctgggca cctgtaggtg tccctcgaga 120
gctcagttt 129
<210> 115
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 115
Leu Lys Thr Thr Asn Arg Ala Ser Val Ser Ile Ser Gln Leu Pro Phe
1 5 10 15
Phe Lys Ile Ile Phe Leu Trp Ser
20
<210> 116
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 116
ctgaagacaa caaatagagc ctctgtaagt attagtcagt tgcctttctt taagattatt 60
tttctgtggt ct 72
<210> 117
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 117
Arg Leu Ala Ser Ile Tyr Glu Glu Leu Leu Gly Ala Thr Ala Ile Glu
1 5 10 15
<210> 118
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 118
aggctggcta gcatctatga ggagctgctg ggtgcaacgg ccattgag 48
<210> 119
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 119
Ser Leu Leu Ser Leu Phe Pro Gly Lys Thr Val Glu Ile Thr Cys Leu
1 5 10 15
Gln His Gln Lys Cys
20
<210> 120
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 120
agtcttctta gtctcttccc aggtaagact gttgaaataa catgcctgca gcatcaaaaa 60
tgc 63
<210> 121
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 121
Thr Gln Arg Leu Pro Gly His Lys Val Ser Asn Ser Cys Met Thr Gly
1 5 10 15
Leu Val Leu Thr Phe Thr Lys Arg Asp Pro Phe His Lys Pro Val Thr
20 25 30
Trp Cys Gly Gln Leu Ala Asp Val Arg Gln Cys Met Phe His Ser Ile
35 40 45
Arg Glu Arg Ala His Pro Leu Gln Arg Ala Leu Ala Thr Leu Asn Phe
50 55 60
Phe Phe Val Ser Phe Tyr Thr Ala Leu Tyr Leu Thr His Pro Leu Leu
65 70 75 80
Thr Leu Gln Thr Trp Glu Val Val Val Thr Val Cys Phe Ser Cys Trp
85 90 95
Glu Leu Cys Val Pro Cys Asp Val Leu Arg Arg Thr Cys Arg Gly Gln
100 105 110
Arg
<210> 122
<211> 339
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 122
actcaacggt tgccaggaca caaagtaagc aacagctgca tgaccggttt agtcctgacg 60
tttacaaaga gggacccttt ccataagcct gtaacttggt gtgggcagct tgccgatgtc 120
aggcagtgca tgtttcactc gattagggag agagcgcacc ctctccagag ggctttggcc 180
acgcttaatt ttttctttgt ttccttctat actgctttat atctcacaca tcccctctta 240
actctccaga catgggaagt tgttgtgaca gtatgtttta gctgttggga gctctgtgtt 300
ccatgcgatg ttttacggag aacttgcaga ggacaaaga 339
<210> 123
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 123
Leu Gln Ala Ile Leu Gln Pro Gly Asn Phe Ile Leu Val Asn Glu Ile
1 5 10 15
<210> 124
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 124
ttgcaggcaa ttttgcaacc aggtaacttc attctggtca acgagatt 48
<210> 125
<211> 102
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 125
Arg Gln Arg Glu Val Val Asp Leu Val Ser Pro Arg Glu Pro Ser Arg
1 5 10 15
Asp Arg Arg Ala Gly Gly Gly Asp Leu Ala Ala Arg Pro Thr Gly Arg
20 25 30
Ala Ser Val Trp Leu Leu Gly Val Ser Val Cys Thr Ala Val Cys Arg
35 40 45
Val Ser Cys Cys Ala Gly Val Ser Cys Phe Leu Phe Thr Gly Glu Glu
50 55 60
Gly Pro Gly Tyr Ala Cys Ser Glu Ser Trp Asn Ser Glu Gly Arg Pro
65 70 75 80
Lys Trp Glu Ala Ile Val Glu Arg Thr Cys Asp Met Gly Pro Tyr Asn
85 90 95
Gly Met Cys Leu Gln Gly
100
<210> 126
<211> 306
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 126
cggcagaggg aggtggtgga cctggtgagt ccgagggagc cgagccggga ccgccgcgct 60
ggtggagggg acctggccgc gcgccccacg ggcagggcgt cagtctggct gttgggggtg 120
tctgtctgta cagctgtgtg tcgtgtgtct tgctgcgccg gggtgtcatg ctttttattt 180
acaggtgaag aaggacctgg ttatgcgtgc agtgagtctt ggaactcaga ggggagacca 240
aaatgggagg ccatcgtgga gcggacatgc gatatgggcc cgtataatgg aatgtgctta 300
caaggg 306
<210> 127
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 127
Leu Val His Gln Leu Lys Gln Gln Val Gly Pro Pro Ala Arg Gln Thr
1 5 10 15
Gln Asn Arg Met Lys Leu Met
20
<210> 128
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 128
ctagtacatc aattaaagca gcaggtgggg cctcctgcaa gacagaccca gaacagaatg 60
aagttgatg 69
<210> 129
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 129
Phe His Leu Ile Ala Met Asp Ala Val Ser Phe Phe Tyr Phe Gln Ile
1 5 10 15
Phe Ile Thr Ser Arg Ile Phe
20
<210> 130
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 130
tttcatctca tagctatgga tgctgtatcc tttttttatt tccagatttt tataactagt 60
agaatattt 69
<210> 131
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 131
Gly Glu Lys Ile Leu Phe Ile Arg Val Lys Phe Tyr Phe Ser Leu Ile
1 5 10 15
Leu Phe Leu Trp Glu Asp Ser Glu Phe Glu Leu Gly Glu Ile
20 25 30
<210> 132
<211> 90
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 132
ggagaaaaga tcctcttcat tagggtaaag ttttactttt cacttatctt gtttttatgg 60
gaagattcag aatttgagtt aggggaaata 90
<210> 133
<211> 54
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 133
Met Lys Gln Phe Leu Asp Phe Gly Glu Cys Gly Pro Gly Pro Trp Ala
1 5 10 15
Phe Leu Arg Gly Pro Gly Arg Gly Ala Ala Ala Ala Ala Pro Gly Arg
20 25 30
Val Gly Ala Gly Gln Leu Ser Pro Glu Ala His Pro Ser Ser Ser Ala
35 40 45
Phe Pro Pro Pro Ala Pro
50
<210> 134
<211> 162
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 134
atgaagcagt tcctggactt cggtgagtgc ggcccgggac cttgggcctt tttgcgcggt 60
cccgggcggg gagctgcggc cgctgcccca ggccgggtcg gcgccggcca gctctcgcct 120
gaggcgcacc cctcctcctc agcgtttccg cccccagcgc ct 162
<210> 135
<211> 138
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 135
Gln Leu Lys Lys Met Val Ser Lys Val Arg Leu Arg Arg Ala Arg Leu
1 5 10 15
Pro Gly Arg Ala His Arg Ser Leu Pro Arg Pro Val Glu Ser Val Pro
20 25 30
Ala Gln Pro Ser Lys Leu Pro Arg Arg Ala Gly Ser Pro Gly Ala Val
35 40 45
Leu Ser Asp Leu Leu Arg Thr Pro Pro Arg Gly Ala Cys Arg Leu Val
50 55 60
Arg Glu Ser Pro Tyr Gly Ser Trp Glu Gly Gly Gly Arg Arg Gln Ser
65 70 75 80
Thr Lys Ala Trp Ser Gly Gly Tyr Leu Thr Pro Ala Ala His Pro Pro
85 90 95
Ser Ser Leu Pro Leu Ser Leu Glu Leu Ser Val Gly Gln Cys Ser Phe
100 105 110
Ser Phe Val Phe Ile Asn Thr Asn Lys Gly Ser Tyr Leu Val Val Asp
115 120 125
Leu Arg Gln Ser Ser Thr Pro Val Pro Ile
130 135
<210> 136
<211> 414
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 136
cagctcaaga aaatggtgtc caaggtgagg ctgcgacgcg ctcgcctccc agggcgcgcc 60
caccgctccc ttccgcgccc tgtcgagtcc gtcccggccc agccaagcaa gcttcccaga 120
cgggccggaa gccccggtgc agtccttagc gacctcctca gaaccccgcc ccgaggcgcc 180
tgtcgcctgg tgcgggaatc cccgtacggg agctgggagg gtgggggacg gcgacagtca 240
acaaaggcgt ggagcggagg ctacctgaca cctgccgccc acccgccctc ctctcttcca 300
ctgagtttgg agctgtctgt ggggcagtgt agtttttcgt ttgtttttat aaacacaaac 360
aagggatcat acttagttgt agatctgagg caatcctcta ctcctgtccc aatc 414
<210> 137
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 137
Asp Ala Leu Ile Gln Asn Gln His Val Ser Thr Val Val Cys Ile Val
1 5 10 15
Ser Phe Arg Ile Asp Lys Leu Leu Lys Tyr
20 25
<210> 138
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 138
gatgctttaa tacagaacca gcatgtgagt acagtagttt gtattgtttc atttagaatt 60
gataaacttt taaaatat 78
<210> 139
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 139
Gly Gly Asn Asn Ser Asn Gln Gln Leu Asp Asp Ala Arg Asn Lys Ala
1 5 10 15
<210> 140
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 140
ggaggaaata attcaaatca gcaactggat gatgctcgca acaaagct 48
<210> 141
<211> 83
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 141
Asn Ser Gly His Leu Leu Val Gln Arg Trp Ser Leu Ala Leu Ser Pro
1 5 10 15
Arg Pro Glu Cys Ser Gly Met Ile Ser Ala His Cys Asn Leu His Leu
20 25 30
Pro Gly Ser Ser Ser Ser Pro Ala Ser Ala Ser Gln Val Asp Gly Ile
35 40 45
Thr Gly Thr Cys Arg His Phe Phe Asn Asp Val Phe Val Asn Gly Lys
50 55 60
Glu Thr Ala Ile Phe Tyr Leu Trp Gly Phe Leu Pro Ile Lys Glu Leu
65 70 75 80
Pro Ala Ala
<210> 142
<211> 249
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 142
aattcgggcc acttgctagt ccagagatgg agtcttgctc tgtcgcccag gccagagtgc 60
agtggcatga tctcagctca ctgcaacctc cacctcccgg gttcaagcag ttctcctgcc 120
tcagcctccc aagtagatgg gattacaggc acgtgccgcc acttttttaa tgatgtattt 180
gttaatggga aggagacagc tattttctac ttatggggct tccttcctat aaaagaattg 240
ccagcagca 249
<210> 143
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 143
Tyr Gly Val Tyr Val Ile Asn Gln Lys Gly His Ser Gly Cys Ile Trp
1 5 10 15
Ser Met Asp Gly Glu Gly Arg Leu Glu Thr Ala Trp Pro Val Trp Lys
20 25 30
Arg Gly Arg Cys Pro Gly Lys Arg Arg
35 40
<210> 144
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 144
tacggcgtct atgtcatcaa ccagaaaggt cactctggtt gcatatggag catggatgga 60
gaggggagat tagagacagc gtggcccgtt tggaagagag gacgatgccc aggaaagagg 120
cgg 123
<210> 145
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 145
Ser Arg Ala Pro Ile Lys Met Ser Val Leu Gly Gln Gly His Ser Arg
1 5 10 15
Cys Leu Leu His Cys Leu Cys Leu Val Ala Pro Met Ala Phe Pro Val
20 25 30
Arg Leu Arg Val Pro Cys Gly Gly
35 40
<210> 146
<211> 120
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 146
agtcgcgcac ccataaaaat gagcgttctg ggtcagggcc attctcggtg cctcctgcac 60
tgcctttgtt tggttgctcc catggcgttc ccggtgagac tgcgggtgcc gtgcggtggt 120
<210> 147
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 147
Ser Ala Thr Thr Arg Ser Ile Thr Gly Gln Asp Ile Leu Ser Leu Glu
1 5 10 15
Lys Glu Arg Arg
20
<210> 148
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 148
agtgccacca ccaggtctat aaccggacaa gatatcttga gcctggagaa ggaaagaaga 60
<210> 149
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 149
Leu Thr Ala Leu Leu Leu Leu Ala Ser Thr Pro Thr Pro
1 5 10
<210> 150
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 150
ctgacagccc ttctgctcct ggcttccact ccaaccccc 39
<210> 151
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 151
Phe Ser Met Arg Pro Ala Phe Gly Glu Thr Ala Leu Gly Cys Lys Lys
1 5 10 15
Trp
<210> 152
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 152
ttcagcatga gacccgcctt cggagagaca gccctgggat gtaaaaagtg g 51
<210> 153
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 153
Ser Ser Leu Arg Ser Leu Trp Gly Ser Arg Leu Leu Leu Gln Pro Ser
1 5 10 15
Pro
<210> 154
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 154
tccagcctgc ggagcctgtg gggcagcagg ctcctgctcc agcccagccc c 51
<210> 155
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 155
Gln Leu Pro Pro Met Gln Glu Arg Ala Thr Ile Ser Leu Gln Gly Thr
1 5 10 15
Glu Tyr Pro Lys Tyr
20
<210> 156
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 156
caacttccac ccatgcagga aagagctacg atatccttac aaggtaccga atatcccaaa 60
tat 63
<210> 157
<211> 76
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 157
Thr Phe Thr His Leu Lys Gln Gln Leu Ser Leu Leu Pro Leu Met Glu
1 5 10 15
Pro Ile Ile Gly Val Asn Phe Ala His Phe Leu Pro Tyr Gly Ser Gly
20 25 30
Gln Phe Asn Ser Gly Asn Arg Leu Leu Gly Thr Phe Gly Ser Ala Thr
35 40 45
Leu Glu Gly Val Ser Asp Tyr Tyr Ser Gln Leu Ile Tyr Lys Val Cys
50 55 60
Phe Ser Ala Lys Val Leu Ser Cys Phe Ile Phe Gly
65 70 75
<210> 158
<211> 228
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 158
acgtttaccc acttgaaaca gcagctctct ctgctccctc taatggaacc aatcattgga 60
gtgaactttg cgcactttct tccttatggc agtggccaat ttaatagtgg gaatcgactt 120
ctaggaactt ttggcagtgc taccctggaa ggggtttcgg actactattc tcagttgatc 180
tacaaggtat gtttctctgc caaggtgttg tcttgcttca tctttggg 228
<210> 159
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 159
Cys Lys Val Cys Gln Asn Cys Lys Asn Pro Lys Met Ala Arg Ala Ser
1 5 10 15
<210> 160
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 160
tgcaaagtgt gccagaactg caagaatcct aaaatggcta gagcaagt 48
<210> 161
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 161
Asp Leu Phe Asp Glu Phe Asp Asn Ser Arg Leu Val Ser Arg Ser Trp
1 5 10 15
Phe Phe Phe Tyr Leu Arg Asn Lys Trp Asn Leu Ala Leu Gly Phe
20 25 30
<210> 162
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 162
gatctctttg atgagtttga caactctaga cttgtaagtc gcagttggtt ctttttctac 60
ttgcgcaaca agtggaattt ggcactgggt ttc 93
<210> 163
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 163
Arg Ser Ile Ser Leu His Lys Ser Asp Pro Ser Leu Leu Ser Pro Asn
1 5 10 15
<210> 164
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 164
cgatccatca gcctccacaa gtcagatcca tctctcctgt caccaaat 48
<210> 165
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 165
Phe Leu Gln Lys His Gly Asn Glu Asn Thr Val Leu Met Leu Glu Thr
1 5 10 15
Leu Ser Glu Ile Arg Tyr Gly Tyr Val Ser Cys Val Cys Cys Pro Leu
20 25 30
Leu Ser Pro Tyr Gly Arg Cys Leu Asn
35 40
<210> 166
<211> 123
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 166
ttcttacaaa aacatggaaa tgaaaacaca gttctgatgt tagagacctt aagtgaaata 60
aggtatgggt atgtgagctg tgtgtgctgc cctttactaa gtccttatgg tagatgtctg 120
aat 123
<210> 167
<211> 44
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 167
Pro Pro Glu Ile Leu Ser Asn Glu Ser Leu His Gly Gly Ile Trp Pro
1 5 10 15
Leu Arg Phe Trp Leu Pro His Trp Ile Ile Ser Met Glu Arg Ser Gln
20 25 30
Tyr Gly Thr Gln Thr Arg Lys Thr Val Tyr Glu Asn
35 40
<210> 168
<211> 132
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 168
cctcctgaga ttttgtctaa tgaaagcttg catggaggaa tttggcccct aagattttgg 60
cttccccatt ggatcatcag tatggaacgc agtcagtatg gaactcaaac aagaaagaca 120
gtgtatgaaa at 132
<210> 169
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 169
Glu Ala Met Asp Gly Arg Glu Pro His Leu Leu Asp Lys Asn Asp Asp
1 5 10 15
Arg Ser Ile Ser Trp
20
<210> 170
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 170
gaagccatgg atggccggga acctcatctg ttagacaaaa atgacgacag atccatttcc 60
tgg 63
<210> 171
<211> 89
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 171
Ser Leu Leu Ile Gly Ala Leu Arg Ile Thr Trp Lys Arg Glu Ala Gly
1 5 10 15
Arg Lys Ser Phe Phe Lys Cys Gly Leu Arg Val His Met Trp Lys Gly
20 25 30
Leu Gln Phe Ile Glu Ile Thr Arg Arg Asn Trp Met Leu Ile Phe Gln
35 40 45
Ser Cys Ser Leu Phe Gly Thr Ser Gln Tyr Arg Ser Leu Thr Lys Lys
50 55 60
Cys Gln Leu Cys Phe Arg Phe Lys Arg Val Ser Ser Lys Gly Ser Asp
65 70 75 80
Ile Thr Asp Lys Arg Glu Val Thr His
85
<210> 172
<211> 267
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 172
tctctgctca ttggggcgtt gaggataacg tggaagcggg aagctgggag aaagtcattt 60
tttaaatgtg gattgagagt tcatatgtgg aaagggctgc aattcattga aataaccagg 120
agaaattgga tgctgatatt tcagagctgc agtctgtttg gaacctcaca gtaccgcagt 180
ctaacaaaga agtgccagct ttgttttaga tttaaaagag tatcatctaa aggatctgac 240
attacagaca aaagagaggt aactcac 267
<210> 173
<211> 22
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 173
Thr Val Pro Ala Ser Gln Lys Leu Ser Cys Ser Leu Asp Pro Lys His
1 5 10 15
Leu Arg Gln Phe His Leu
20
<210> 174
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 174
accgtccccg ccagtcagaa gttgagctgc tcactggacc cgaaacatct cagacagttt 60
cacctc 66
<210> 175
<211> 66
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 175
Met Val Met Ser Phe Val Asn Leu Ala Leu Ala Arg Leu Thr Gln Leu
1 5 10 15
Gln Gln Glu Ser Pro Ala Arg Val Trp Pro Ser Trp Glu Glu Gly Ser
20 25 30
Ser Val Arg Phe Ser Pro Leu Asn Cys Arg Leu Leu Pro Pro Asn Leu
35 40 45
Glu Cys Ser Phe Pro Thr Glu Thr Phe Arg Glu Ser Asp Ser Gly Trp
50 55 60
Glu Leu
65
<210> 176
<211> 198
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 176
atggtcatga gctttgtgaa cctggctctg gccaggttaa ctcaactgca gcaggagagt 60
ccagcccgag tgtggccatc ctgggaagag ggctcttcag tacgattttc ccctctaaac 120
tgccgccttt tgccccctaa cttggagtgc agttttccca ccgagacttt tagggaatcc 180
gacagcggct gggaactt 198
<210> 177
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 177
Leu Glu Asp Leu Asp Thr Cys Met Lys Pro His Ala Phe Gln His Ala
1 5 10 15
Met Met Thr Phe Ala Ser Thr Thr Phe Arg Leu Cys Gln Lys Ser Ser
20 25 30
Lys Leu Ser Leu Leu Ser Ser
35
<210> 178
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 178
ttggaagatc tggatacctg tatgaaacct catgcttttc aacatgccat gatgacattt 60
gcatcaacga cgtttcgttt atgtcaaaaa agctccaaat tatcactgct ttccagt 117
<210> 179
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 179
Phe Gly Thr Ser His Met Met Val Arg His Phe
1 5 10
<210> 180
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 180
tttggcacat cacatatgat ggtcagacat ttt 33
<210> 181
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 181
Gly His Phe Glu Ser Ile Arg Ala Val Leu Phe His Trp Ile Pro Val
1 5 10 15
Thr Thr Leu Leu Val Ser Gln Val Ile Tyr Lys
20 25
<210> 182
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 182
ggacattttg aaagcatcag ggccgtatta tttcattgga ttcctgtaac tacactgtta 60
gtcagccaag ttatatataa a 81
<210> 183
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 183
Met His Thr Gly Thr Ile Ser Gln His Cys Gln Leu Leu Asp Cys Ser
1 5 10 15
Leu Gly Ala Ile Leu His Ile Gly Tyr Thr Lys
20 25
<210> 184
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 184
atgcatacag gaactatttc tcagcattgt cagctcctgg attgctcctt gggcgctata 60
ctgcacattg gctataccaa g 81
<210> 185
<211> 61
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 185
Glu Ile Glu Gly Ser Cys His Gly Gly Met Ile Thr Met Asp Ile Lys
1 5 10 15
Met Gly Ser Tyr Ser Cys Asp Tyr Leu Lys His Ser Glu Thr Leu Ser
20 25 30
Ala Met Val Val Ser Cys Gly Ile Ser Phe Leu Phe Leu Phe Pro Arg
35 40 45
Lys Lys Ile Ala Lys Leu Ile Phe Lys Glu Gln Val Pro
50 55 60
<210> 186
<211> 183
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 186
gaaattgagg gttcttgcca tggtggtatg atcactatgg atatcaaaat gggaagttac 60
agttgcgatt acttaaaaca ttcagaaaca ttatctgcta tggtggttag ctgtggaata 120
tcctttctct ttctctttcc aaggaaaaaa attgcaaaat tgatttttaa ggaacaagta 180
cca 183
<210> 187
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 187
Cys Glu Ile Met Pro Leu Gln Ser Tyr Ile Leu Leu
1 5 10
<210> 188
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 188
tgtgaaatca tgcctctgca aagttatatc cttctc 36
<210> 189
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 189
Val Asn Arg Lys Ser Val Lys Gly Phe His Val Ala His Leu Pro Ser
1 5 10 15
Ala
<210> 190
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 190
gttaatagaa aaagtgtcaa aggcttccac gtggctcatc ttccttctgc c 51
<210> 191
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 191
Phe Gln Asp Lys Tyr Phe Met Ile Ala Thr Asn
1 5 10
<210> 192
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 192
ttccaggaca agtactttat gatagctacg aac 33
<210> 193
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 193
Val Ala Gln Val Glu Ile Arg Gly Leu Glu Pro Pro Val His Asp Gln
1 5 10 15
<210> 194
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 194
gtagcgcagg tggaaataag aggactagaa ccaccagtgc atgatcaa 48
<210> 195
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 195
Gly Gly Gly Gly Gly Ser Gly Glu Leu Thr Thr Gln Ile Pro Cys Ser
1 5 10 15
Trp Arg Thr Lys Gly His Ile His Asp Lys Lys Thr Glu Pro Phe Arg
20 25 30
Leu Leu Ala Trp Ser Trp Cys Leu Asn Val Ser
35 40
<210> 196
<211> 129
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 196
ggcgggggag gcggcagcgg agagctaaca acacagatcc catgtagttg gagaaccaaa 60
ggccacatac atgacaaaaa gactgaaccg ttcaggttac ttgcatggag ttggtgctta 120
aatgtgagt 129
<210> 197
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 197
Val Ala Pro Ser Gln Ser Arg Gln Glu Glu Cys Trp Arg His Lys Met
1 5 10 15
Ser Trp
<210> 198
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 198
gtagcacctt cacagtccag gcaagaggaa tgctggcgtc ataaaatgag ttgg 54
<210> 199
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 199
Ile Ala Leu Gln Tyr Cys Cys Thr Cys Ser Ile Ser Gln
1 5 10
<210> 200
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 200
atagcccttc agtactgttg tacgtgttcc atttctcaa 39
<210> 201
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 201
Ser Ala Val Asp Asp Met Ile Ala Ala Phe Pro Phe Lys Arg Ala
1 5 10 15
<210> 202
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 202
agtgctgtag atgacatgat agcagcattt cccttcaaaa gagct 45
<210> 203
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 203
Met Trp Thr Arg Lys Ala Arg Gly Thr Thr Ile Cys Asp Arg Arg Arg
1 5 10 15
Gln Ile Cys Arg Trp Arg Glu
20
<210> 204
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 204
atgtggacaa ggaaagcaag aggaactacc atttgtgata gacgaagaca gatttgcagg 60
tggagggag 69
<210> 205
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 205
Ile Asn Tyr Arg Leu Gly Ile Leu Asp Asn Val Ser
1 5 10
<210> 206
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 206
attaactacc gtctgggaat actagataat gtttca 36
<210> 207
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 207
Thr Ser Thr Ser Pro Lys Phe Pro Val Phe Ile Phe Arg Leu Val Cys
1 5 10 15
Trp Val Arg Thr Glu Leu Val Leu Arg
20 25
<210> 208
<211> 75
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 208
actagcacca gccccaaatt tcctgttttt atctttagac tcgtgtgttg ggtaaggaca 60
gagctggtac tgcgt 75
<210> 209
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 209
Met Ala Ile Pro Gly Arg Gln Asn Ile Val Leu Arg Ser His Arg Lys
1 5 10 15
Arg Val Gly Ile
20
<210> 210
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 210
atggcgattc cgggcaggca gaatattgtt ctgagaagcc acagaaaaag ggtaggcata 60
<210> 211
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 211
Glu Ala Glu Phe Asp Lys Thr Thr Arg Thr Phe Leu Gln Ile Phe Asn
1 5 10 15
Arg Lys Arg Gly Lys Ile Gln
20
<210> 212
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 212
gaggctgaat ttgataagac cactagaaca tttctacaaa ttttcaatcg caaaagagga 60
aaaatacaa 69
<210> 213
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 213
Lys Leu Leu Tyr Glu Val Ser Gln Lys Met Val Leu
1 5 10
<210> 214
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 214
aaactgctgt atgaagtttc ccagaaaatg gtctta 36
<210> 215
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 215
Trp Ala Phe Ile His Ser Leu Pro Ala Leu Leu Gly Ile Phe Ser Tyr
1 5 10 15
Pro Pro Ser Arg
20
<210> 216
<211> 60
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 216
tgggccttca tccattcttt gcctgcacta ctgggtattt tctcataccc cccaagtcga 60
<210> 217
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 217
Ser Ser Leu Gln Glu His Arg Lys Leu Leu Ser
1 5 10
<210> 218
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 218
tcaagcctac aggaacatag aaagcttctc tcc 33
<210> 219
<211> 58
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 219
Arg Phe Ser Arg Arg Tyr Pro Cys Ser Ala Arg Thr Ser Leu Gly Arg
1 5 10 15
Glu Glu Ser Glu Pro Pro Gly Glu Ala Ala Met Trp Arg Trp Arg Leu
20 25 30
Trp Arg Gly Arg Ala Ser Gly His Pro Ser Gly Glu Gly Arg Pro Pro
35 40 45
Glu Thr Asn Gln Gly His Ser Thr Gly Arg
50 55
<210> 220
<211> 174
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 220
cgattttctc ggcggtatcc atgcagtgct aggaccagcc ttgggagaga ggaaagtgag 60
ccaccaggag aagctgccat gtggaggtgg aggctctgga ggggtcgggc atcaggacac 120
ccttcaggag aggggagacc tcctgagaca aaccaagggc attccactgg gaga 174
<210> 221
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 221
Glu Arg Ser His Ser Lys Lys Lys Asp Gly Leu Val Arg Asn Asp Gly
1 5 10 15
Pro Gly Phe Pro Pro Met Phe Ser Thr Ser Glu Asn Thr Asn Leu Asp
20 25 30
<210> 222
<211> 96
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 222
gaaagaagcc actccaaaaa gaaggatggt cttgtgagaa atgacggacc tggattccca 60
cctatgtttt ccacatcaga aaataccaac ttggat 96
<210> 223
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 223
Ala Gly Asp Val Leu Phe Ile Pro Gly Ile Ser Leu Lys Val His Lys
1 5 10 15
Val Gln His Ser Lys Val Ile Asn Ile Cys Asn
20 25
<210> 224
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 224
gctggtgatg tattattcat tcctggcatt agtttgaaag tccataaagt tcaacacagc 60
aaggtaatta acatctgtaa t 81
<210> 225
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 225
Ile Glu Asn Glu Gly Gly Gln Val Arg Ser Arg Pro Ala Pro Ser
1 5 10 15
<210> 226
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 226
atcgagaacg aaggcggcca ggtgaggtcc cgccccgctc cctcc 45
<210> 227
<211> 57
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 227
Leu Ile Ser Val Val Gln Asn Gly Lys Glu Ser Pro Ser Leu Arg Glu
1 5 10 15
Glu Gln Lys Gly Arg Phe Ser Leu Met Val Val Trp Lys Ser Gly Leu
20 25 30
Asn Asn Cys Val Cys Val Cys Ala Cys Thr Asn Thr Phe Thr Leu Ser
35 40 45
Leu Phe Ser Ser Phe Tyr Leu Asn Val
50 55
<210> 228
<211> 171
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 228
ctcatcagcg tggtccagaa tggtaaggaa agcccttcac tcagggaaga acagaagggg 60
agattttctt tgatggttgt ttggaagtca ggcttaaaca attgtgtctg tgtgtgcgca 120
tgcacaaaca cttttacctt atctttattt tcttcttttt atttgaatgt a 171
<210> 229
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 229
Glu His Gln Arg Asn Ser Ser Lys Val Phe Tyr Gly Val Ile Asp Cys
1 5 10 15
Val Ile Lys Glu Thr Ile Thr Trp His Asp
20 25
<210> 230
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 230
gaacatcaaa gaaatagcag taaggtattt tatggtgtta ttgactgtgt cataaaggaa 60
actattactt ggcacgat 78
<210> 231
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 231
Asp Ser Leu Pro Lys Thr Glu Met Val Ser Gly Ser Tyr Arg Met Gly
1 5 10 15
Leu Cys Glu His Cys Leu Asn Gln
20
<210> 232
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 232
gactcgcttc ccaaaactga aatggtgagt gggtcataca gaatgggtct gtgtgagcac 60
tgtcttaatc aa 72
<210> 233
<211> 54
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 233
Arg Pro Arg Lys Asp Thr Trp Lys Val Arg Asp Pro Ala Leu Arg Tyr
1 5 10 15
Thr Pro Leu Leu Ile Gln Ser Leu Asp Ser Arg Leu Ala Glu Ser Cys
20 25 30
Ala Val Phe Ile Trp Tyr Cys Ile Phe Thr Leu Gly Asp Thr Cys Arg
35 40 45
Ser Arg Pro Val Glu Asn
50
<210> 234
<211> 162
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 234
cgcccgcgga aagacacctg gaaggttaga gatccagcat tgcgctacac ccctttgtta 60
attcagtcac tggacagccg cctagccgag agctgtgcgg tttttatatg gtattgtatc 120
tttactttag gcgatacatg cagaagtcgt ccggtagaaa ac 162
<210> 235
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 235
Pro Val Gly Ser Val Ser Phe Gln Val Gly Cys Val Gln Leu Phe Pro
1 5 10 15
<210> 236
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 236
cccgtgggca gtgtcagctt ccaggtaggg tgtgtgcagc ttttccct 48
<210> 237
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 237
Gln Arg Ile Gln Ala Gln Glu Gly Lys Cys Pro Val Asn Leu Ser Gln
1 5 10 15
Pro Leu
<210> 238
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 238
cagaggattc aggcacagga aggtaagtgt cctgtaaatc tctcccagcc cctt 54
<210> 239
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 239
Asn Leu Lys Pro Asp Arg Lys Gly Lys Glu Ser Met Ala Lys
1 5 10
<210> 240
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 240
aacctcaagc cagacagaaa aggtaaggag agcatggcaa ag 42
<210> 241
<211> 48
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 241
Asp Leu Asn Gln Asp Gly Tyr Asn Gly Asn Leu Asn Gln Ser Val Glu
1 5 10 15
Val Ile Tyr Val Ser Ser Pro Leu His Lys Gly Asp His Ala Cys Phe
20 25 30
Lys Val Phe Ser Met Val Cys Val Gly Ala Val Ile Ile Thr Asp Phe
35 40 45
<210> 242
<211> 144
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 242
gacctgaacc aagatggata caatggtaat ttaaaccaaa gcgtggaagt catttatgtg 60
tcgtcaccac tgcataaagg agaccatgcc tgttttaaag tattcagtat ggtgtgtgtg 120
ggtgcagtta ttattactga tttt 144
<210> 243
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 243
Ala Pro His Leu Leu Arg Leu Phe Gly Asn Met Ser Cys Arg Lys
1 5 10 15
<210> 244
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 244
gcgccacatc tcctgagatt atttggtaat atgtcatgta gaaaa 45
<210> 245
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 245
Ser Leu Lys Lys Val Val Lys Glu Val Gly Val Glu Ser Trp Arg Gly
1 5 10 15
Arg Gly Ala Trp Arg Gly Ala
20
<210> 246
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 246
tccctgaaga aagttgtgaa ggaggtgggt gttgagagtt ggagagggag aggtgcgtgg 60
aggggagcc 69
<210> 247
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 247
Pro Val Ile Leu Phe Lys Gly Lys Val Arg Pro Ile Pro
1 5 10
<210> 248
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 248
ccagtaatcc tgttcaaggg caaggtaagg cccatacca 39
<210> 249
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 249
Gln Ile Leu Glu Gln Pro Lys Gln Val Arg Leu Lys Gly Trp Asp Phe
1 5 10 15
Lys Cys
<210> 250
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 250
caaatattag agcaacctaa acaggtaaga ttaaaggggt gggactttaa atgt 54
<210> 251
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 251
Ile Ala Thr Gly Ala Gln Val Val Thr Gln Asp Thr Asn Tyr Phe Leu
1 5 10 15
Phe Cys Phe Glu Lys Phe Val Pro Val His
20 25
<210> 252
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 252
atagcaactg gagctcaggt agtaacacag gatactaatt atttcttatt ttgctttgaa 60
aaatttgttc cagtccac 78
<210> 253
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 253
Leu Leu Tyr Glu Val Ser Gln Val Ser Ala Gly Ser Asp Thr Ser Asn
1 5 10 15
<210> 254
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 254
ctgctgtatg aagtttccca ggtgagtgca gggtctgata ccagcaac 48
<210> 255
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 255
Trp Lys Leu Lys Ala Thr Lys Val Asn Gly Thr Pro Asp Ala Tyr Gly
1 5 10 15
Glu Ser Met Arg Ala Leu Trp Gly Gly Ser Ala Phe Gln Leu Gly Gly
20 25 30
Phe Gln
<210> 256
<211> 102
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 256
tggaagctaa aggccactaa ggtaaacggc actcctgatg cttatggaga gagtatgagg 60
gccttgtggg gagggtctgc attccaactt gggggtttcc ag 102
<210> 257
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 257
Ser Pro Ala Ile Tyr Lys Leu Lys Val Asn Ile Gln Asn Ile Lys Gly
1 5 10 15
Glu Asn Leu Arg His Asn His Phe
20
<210> 258
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 258
agtcctgcaa tttataaact aaaggtaaac atacaaaaca taaagggaga aaacttaaga 60
cataaccatt tc 72
<210> 259
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 259
Asp Met Glu Val Phe Leu Lys Glu Ala Ser Thr Asn Gln His Asn Thr
1 5 10 15
Leu Ile His Leu Thr Leu Thr Phe Ser Thr
20 25
<210> 260
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 260
gatatggagg ttttcctcaa agaggcaagt actaaccaac acaacacttt gattcacttg 60
acacttactt tcagcact 78
<210> 261
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 261
Leu Gln Ala Asn Gln Leu Gln Gly Val Ser Lys Gly Asn Pro Val Cys
1 5 10 15
<210> 262
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 262
cttcaagcga atcagctaca aggggtaagt aaaggaaacc cagtttgt 48
<210> 263
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 263
Leu Thr Asp Asp Gln Val Ser Gly Lys Leu Val Ser Asn Ser Phe Thr
1 5 10 15
Pro Phe Val Ser Phe Ile Phe Pro Phe Phe Pro Phe Leu Leu Ser Leu
20 25 30
Ile Glu Glu
35
<210> 264
<211> 105
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 264
ttaacagatg atcaggtttc aggtaagttg gtttccaact cctttacacc cttcgtttcc 60
ttcatctttc cgttcttccc tttccttctt tctttaattg aagaa 105
<210> 265
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 265
Gln Arg Asp Arg Asp Ser Ile Lys Val Gly Leu Lys Ile Tyr Arg Leu
1 5 10 15
Arg Asn Gly Leu Lys Gly Leu
20
<210> 266
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 266
caaagagaca gagactccat caaggtagga ctcaaaattt acagactaag gaatggctta 60
aaagggctg 69
<210> 267
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 267
Lys Arg Tyr Gly Cys Val Phe Gln Val Ser Ile Arg His Leu Ser Phe
1 5 10 15
Pro Val Thr Asp Ile Leu Pro
20
<210> 268
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 268
aagcgctatg gctgcgtttt tcaggtcagt atccgacatt tgtccttccc agtcactgac 60
attctgcca 69
<210> 269
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 269
Glu Gly Thr Pro Phe Glu Asp Gly Lys Ser Tyr Ser Leu Cys Phe Leu
1 5 10 15
<210> 270
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 270
gaagggacac cttttgaaga tggtaagtca tactcattat gttttcta 48
<210> 271
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 271
Ser Met Thr Gln Ala Leu Cys Arg Tyr Phe Phe Met Thr Leu Leu Met
1 5 10 15
Val Ile Val Asp Leu Gly Lys Arg Lys Tyr Phe Val Phe Cys Glu
20 25 30
<210> 272
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 272
agtatgaccc aagccctttg caggtacttc ttcatgacac tattaatggt aattgtagat 60
ttggggaaga ggaagtattt tgtattttgt gag 93
<210> 273
<211> 29
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 273
Leu Leu Asp Gly Met Ile Phe Gln Val Ser Arg Ser Val Ser Asp Cys
1 5 10 15
Asn Ser Gly Ala His Ile Arg Arg Gln Ser Ser Glu Leu
20 25
<210> 274
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 274
ttactggatg gaatgatatt ccaggtaagt aggtctgtat cagactgtaa cagtggggct 60
catattagac gacaaagctc agaatta 87
<210> 275
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 275
Glu Ile Pro Arg Lys Thr Ile Phe Gly Lys Asn Gln Val Asp Met Arg
1 5 10 15
Pro
<210> 276
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 276
gaaataccaa ggaagactat ttttggtaag aaccaggtag atatgaggcc a 51
<210> 277
<211> 29
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 277
Ser Gln Lys Gln Pro Ala Glu Lys Cys Leu Leu Arg Asn Asn Gln Leu
1 5 10 15
Arg Arg Leu Gln Val Thr Arg Lys Ile Leu Phe Gln Ile
20 25
<210> 278
<211> 87
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 278
tctcagaaac aaccagctga gaagtgtctt ctcagaaaca accagctgag aaggctacaa 60
gtgacgagaa agattctgtt tcaaata 87
<210> 279
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 279
Ser Arg Lys Lys Pro Ala Leu Lys Cys Leu Leu Arg Asn Asn Gln His
1 5 10 15
<210> 280
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 280
tctcggaaaa aaccagcctt gaagtgtctt ctccgaaaca accagcat 48
<210> 281
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 281
Ser Gln Lys Gln Pro Ala Leu Lys Cys Leu Leu Arg Asn Asn Arg Pro
1 5 10 15
<210> 282
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 282
tctcagaaac aaccagcctt gaagtgtctt ctcagaaaca accggcct 48
<210> 283
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 283
Ser Glu Gln Pro Pro Gly Leu Lys Cys Leu Leu Gly Lys Lys Gln Pro
1 5 10 15
<210> 284
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 284
tctgagcaac caccaggctt gaagtgtctt ctcggaaaaa agcagcct 48
<210> 285
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 285
Val Tyr Tyr Leu Tyr Lys Asn Val Ala Tyr Lys Gly Ser Asp Ile Asp
1 5 10 15
<210> 286
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 286
gtgtactacc tctacaagaa cgtggcctat aagggctctg atatagat 48
<210> 287
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 287
Gln Leu Ser Val Val Thr Arg Asp Asp Tyr Asn Ser Ser Glu Leu Lys
1 5 10 15
<210> 288
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 288
cagctgagcg tggtgacaag ggatgattac aacagcagtg aattgaaa 48
<210> 289
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 289
Leu Glu Asp Lys Glu Leu Gly Arg Ile Ser Val Cys Pro Trp Thr Glu
1 5 10 15
Gly Leu Glu Lys Met Glu Lys Thr Leu Leu Cys Ser Ser Ser Gly
20 25 30
<210> 290
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 290
ctggaagata aagaactggg aaggatatct gtatgccctt ggacagaagg tttggaaaag 60
atggaaaaaa cgttactttg ttctagttca ggt 93
<210> 291
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 291
Glu Asn Gln Arg Leu Ser Lys Lys Asp Leu Val Ser Glu Lys Leu Lys
1 5 10 15
<210> 292
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 292
gaaaatcaaa ggctcagtaa aaaggatttg gtgagtgaaa agttgaag 48
<210> 293
<211> 99
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 293
Met Ser Ala Thr Thr Gly Ser Gln Asp Asn Pro Glu Gly Lys Arg Asp
1 5 10 15
Pro Ser Arg Lys Phe Gln Glu Gln Lys Ala Leu Pro Lys Arg Pro Pro
20 25 30
Leu Gln Lys Asn Leu Arg Asn Gly Val Gly Gln His Tyr Pro Ala Thr
35 40 45
Leu Thr Ser Arg Thr Arg Asn Ser Ile Lys Met Arg His Ser Arg Thr
50 55 60
Thr Arg Ala Arg Arg Pro Pro Pro Ser Pro Val Leu Pro Trp Ala Ala
65 70 75 80
Ser Asn Ser Gln Ala Arg Pro Glu Thr Ser Ser Leu Ser Glu Lys Ser
85 90 95
Pro Glu Val
<210> 294
<211> 297
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 294
atgtcggcga ctacaggttc ccaagacaac ccagaaggga aaagggaccc gtcaaggaag 60
ttccaggaac aaaaggctct ccctaaaaga ccaccgcttc aaaaaaacct gaggaatgga 120
gtgggccaac actatccagc cactctgacc agccgaacga ggaactcaat caaaatgcgc 180
catagcagga ccacaagggc aaggagacca ccgccttctc cagtgcttcc ttgggcagcc 240
agtaattccc aggcaaggcc agagacttca agtctatctg aaaagtctcc agaagtc 297
<210> 295
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 295
Gln Asp Leu Ala Thr Glu Asp Thr Gly Ser Val Thr Lys
1 5 10
<210> 296
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 296
caggacctcg ccacagagga taccggaagt gtgacaaaa 39
<210> 297
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 297
Asp Pro Thr Thr Lys Arg Ser Arg Leu Thr Pro Lys Leu His Phe Leu
1 5 10 15
Val Glu Arg Asn Pro Arg Trp Ser Gln Glu Gln Arg Lys Tyr Leu
20 25 30
<210> 298
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 298
gatcccacta cgaaacgctc cagattgacc ccaaagttgc atttcctcgt cgagcgcaac 60
ccaagatggt cacaagaaca aagaaaatat ttg 93
<210> 299
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 299
Ile Leu Ala Gln Lys Lys Lys Asp Glu Leu Ser Ser
1 5 10
<210> 300
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 300
atattggctc agaagaagaa ggatgagctg agcagc 36
<210> 301
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 301
Ala Lys Phe Trp Ser Asp Ile Ser Ile Asn Arg Ala Pro Ser Phe Gly
1 5 10 15
<210> 302
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 302
gctaagtttt ggagtgatat ttcaattaac cgagccccaa gctttgga 48
<210> 303
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 303
Leu Asp Pro Pro His Asp Glu Lys Ala Leu Ala Cys Pro Gln Trp Thr
1 5 10 15
Leu Leu Trp Ile Phe Trp Thr Ala Lys Ala Leu
20 25
<210> 304
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 304
ctggatccac ctcatgatga aaaggctctg gcatgccctc aatggacatt attgtggata 60
ttttggacag cgaaggctct t 81
<210> 305
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 305
Lys Lys Glu Asp Val Asn Phe Gln Val Lys Gln Leu Ile His
1 5 10
<210> 306
<211> 42
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 306
aagaaagaag atgttaactt tcaggtaaaa cagttaattc ac 42
<210> 307
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 307
Gly Asn Val Leu Val Arg Tyr Val Ser Leu Tyr Val Tyr Tyr Ile Leu
1 5 10 15
Leu Asn
<210> 308
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 308
ggaaatgtat tggtaagata tgtaagttta tatgtttact atattctact gaac 54
<210> 309
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 309
Gln Arg Ser Phe Ile Lys Ala Ala Ser Lys Ser Phe Leu Ser Gln Phe
1 5 10 15
<210> 310
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 310
caaagaagtt tcatcaaagc agcaagtaag tcttttttgt ctcagttt 48
<210> 311
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 311
Phe Ser Gly Arg Ser Arg Ser Arg Gly Lys Thr Arg Arg Asp Gly Phe
1 5 10 15
Leu Arg Ala Thr Arg Asn Asn
20
<210> 312
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 312
ttctcgggtc gttcaagaag ccgaggtaag acacgccgcg acgggtttct gcgggctacc 60
aggaacaat 69
<210> 313
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 313
Arg Glu Ser Lys Arg His Gln Gly Lys Arg Trp Thr Leu Phe Pro His
1 5 10 15
Arg
<210> 314
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 314
cgagaaagta agaggcacca gggtaaacga tggactctct ttcctcatcg t 51
<210> 315
<211> 52
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 315
His Leu Ala Ile Pro Ala Lys Ile Ser Glu Cys Arg Ser Pro Ala Gln
1 5 10 15
Ser Arg Leu Pro Arg Gln Arg Asp Pro Gly Ala Gly Arg Ser Pro Gly
20 25 30
Phe Ser Ser Cys Pro Gln Pro Gly Arg Ser Trp Thr Lys Trp Arg Gln
35 40 45
Gln Cys Thr Arg
50
<210> 316
<211> 156
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 316
cacctggcca tccccgccaa gatcagtgag tgccggagcc cagcccagtc ccgactaccc 60
cgccagcgag accccggggc aggccggtca cctggcttct cctcctgccc gcagcccggg 120
agaagctgga ccaagtggcg acagcagtgt accaga 156
<210> 317
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 317
Leu Asp Leu Ala Asn Pro Gln Gly Lys Gly Pro Lys Gly Glu Leu Arg
1 5 10 15
Asp Phe Ala Pro Arg Thr Glu Glu Ala Pro Val Cys Pro Ala Leu Pro
20 25 30
<210> 318
<211> 96
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 318
ttagacctgg ccaatcctca aggtaagggc cctaagggag aactgaggga cttcgcacca 60
aggacagaag aagccccggt ctgccctgcg ctgcca 96
<210> 319
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 319
Arg Asp Leu Arg Ser Ile Val Glu Val Arg Arg Ala Asp Thr Arg Gly
1 5 10 15
Gln Trp Val Pro Arg Pro Ala Pro Trp Pro Pro
20 25
<210> 320
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 320
agggacctcc gcagcatcgt ggaggtaagg cgggcagaca ccagagggca gtgggtaccc 60
aggccagccc cttggccccc a 81
<210> 321
<211> 60
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 321
Leu Leu Thr Glu Met Asp Asn Lys Val Arg Gln Gly His Gly Gly Ala
1 5 10 15
Leu His Pro Thr Ala Leu Pro Pro Gly Ser Gly Gln His His Leu Leu
20 25 30
Leu Gly Gln Pro Pro Thr Cys Phe Leu Arg Gly Pro Leu Ala Pro Leu
35 40 45
Ser Pro Pro Gln Leu Asp Arg Leu Glu Leu Asp Pro
50 55 60
<210> 322
<211> 180
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 322
ctgctcacag agatggacaa caaggtgagg caggggcatg gcggggctct ccatcccaca 60
gccttgcccc caggatcggg acagcaccac cttctcctgg gtcagccccc tacctgcttc 120
cttagaggtc ccctggcccc tctttccccg ccacagctgg accgcctgga gctggaccca 180
<210> 323
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 323
Met Leu Arg Arg Cys Pro Cys Val Thr Asn Val Val Leu Ala Leu
1 5 10 15
<210> 324
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 324
atgctcagaa ggtgcccatg tgtgacaaat gtggtcctgg cattg 45
<210> 325
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 325
Ala Gly Lys Glu Arg Ser Thr Gln Val Arg Val Gly Pro Thr Leu
1 5 10 15
<210> 326
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 326
gcaggaaagg agcgtagcac ccaggtaagg gtgggtccca ctctg 45
<210> 327
<211> 74
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 327
Ala Gly Arg Ser Leu Cys Leu Thr Val Ser Ser Thr Pro Gly Ser Trp
1 5 10 15
Gly Ala Ser Gly Phe Arg Arg Leu Gly Arg Leu Thr Ser Phe Asn Phe
20 25 30
Gly Ser Glu Ser Leu Trp Leu Phe Tyr Arg Glu Ala Ala Phe Gln Gly
35 40 45
Leu Arg Ser Arg His Pro Phe Ser Asn Pro Leu His Leu Asp Pro Thr
50 55 60
Ser Ser Pro Trp Arg Lys Asn Ile Ser Val
65 70
<210> 328
<211> 222
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 328
gcggggcgaa gtctgtgtct cacggtcagt tcaactccag gctcctgggg agcgtctggg 60
ttccggcgac taggacgcct aacttccttt aacttcgggt ctgaaagtct gtggctcttt 120
tacagagaag cagcgttcca gggactccgt tcccgccacc cgttcagcaa ccctctacac 180
ctggacccga cctcctcgcc ttggaggaag aatataagcg tt 222
<210> 329
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 329
Val Glu Asp Glu Glu Lys Lys Glu Ala Gly Thr His Phe Ile His Leu
1 5 10 15
Thr Gly Thr Thr Val Ser Ala Gly Val Pro Glu Glu Met Pro Ala Thr
20 25 30
Thr Leu Arg Arg Glu Val Phe
35
<210> 330
<211> 117
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 330
gttgaagatg aggagaagaa agaggcaggg actcatttca tccacctgac tggaaccact 60
gtctcagctg gagtccctga ggagatgcca gccacaactc tccgaagaga agtattc 117
<210> 331
<211> 57
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 331
Thr Ala Ile Leu Phe Thr Arg Gln Gln Ser Lys Ala Leu Pro Ser Leu
1 5 10 15
Gly Ile Thr Asn Arg His Gly Phe Trp Ala Gly Gln Gly Asn Thr Val
20 25 30
Met His Gly Arg Asp Ser Asp Gly Lys Gln Val Lys Gly Thr Val Val
35 40 45
Ile Leu Ala Gln Gly Ala Phe His Gln
50 55
<210> 332
<211> 171
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 332
actgccatcc tcttcaccag gcagcaaagc aaggccctcc catccttggg gattacaaac 60
agacatggat tttgggctgg acaaggaaat acagtgatgc atggcagaga ttcggatggg 120
aaacaagtta aaggtacagt agtaatacta gcgcagggtg cttttcacca g 171
<210> 333
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 333
Asn Ala Ser Leu His Glu Val Lys Asp Phe Phe Val Pro Phe Pro Leu
1 5 10 15
Pro Leu Leu His Leu Thr Ser Leu Lys Arg Asn Lys Leu Phe Asn
20 25 30
<210> 334
<211> 93
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 334
aatgcttcac tacatgaagt caaagatttc tttgttcctt tcccactccc actacttcat 60
ttgactagcc ttaaaagaaa taaattattt aat 93
<210> 335
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 335
Gly Thr Thr Arg Leu Leu Ser Gly Glu Asp Phe Ser
1 5 10
<210> 336
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 336
ggtactaccc gtcttctatc tggggaggac ttttcc 36
<210> 337
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 337
Ser Glu Met Val Ala His Glu Arg Tyr Val Phe Glu Ala Thr Gly Asn
1 5 10 15
Asp Ser Phe Arg Thr Leu Cys Leu Leu Met Lys
20 25
<210> 338
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 338
tctgaaatgg tggcacatga aaggtatgtt tttgaagcta ccggaaatga ttcttttaga 60
actctttgtt tattgatgaa a 81
<210> 339
<211> 33
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 339
Ile Ile Met Ala Leu Ala Ile Leu Asp Leu Phe Ala Val Leu Lys Ile
1 5 10 15
Glu Ala His Lys Gln Leu Leu Leu Lys Ser Phe Cys Tyr Gly Ala Gly
20 25 30
Lys
<210> 340
<211> 99
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 340
ataattatgg cattagccat cctggacctc tttgcagtct taaaaattga agcccacaaa 60
cagctcttac ttaagagttt ctgctatggt gctggaaaa 99
<210> 341
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 341
Gln Ile Arg Val Pro Ser Tyr Ser Asp Glu Gly
1 5 10
<210> 342
<211> 33
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 342
caaattaggg taccatcata ttcagatgaa ggc 33
<210> 343
<211> 84
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 343
Arg Gln Arg Glu Val Val Asp Leu Val Lys Lys Asp Leu Val Met Arg
1 5 10 15
Ala Val Ser Leu Gly Thr Gln Arg Gly Asp Gln Asn Gly Arg Pro Ser
20 25 30
Trp Ser Gly His Ala Ile Trp Ala Arg Ile Met Glu Cys Ala Tyr Lys
35 40 45
Gly Gln Gln Glu Cys Leu Val Glu Thr Gly Ala Leu Gly Pro Met Ala
50 55 60
Phe Arg Val His Leu Gly Ser Gln Val Gly Met Asp Ser Lys Glu Lys
65 70 75 80
Arg Gly Asn Val
<210> 344
<211> 252
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 344
cggcagaggg aggtggtgga cctggtgaag aaggacctgg ttatgcgtgc agtgagtctt 60
ggaactcaga ggggagacca aaatgggagg ccatcgtgga gcggacatgc gatatgggcc 120
cgtataatgg aatgtgctta caagggccag caggagtgcc tggtcgagac gggagccctg 180
gggccaatgg cattccgggt acacctggga tcccaggtcg ggatggattc aaaggagaaa 240
agggggaatg tc 252
<210> 345
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 345
Val His Leu Asp Phe Ser Ser Ala Glu Met Gly Phe Pro His Ala Ala
1 5 10 15
Gln Ala Asn Val Glu Leu Leu Gly Ser Ser Asp Leu Leu Thr
20 25 30
<210> 346
<211> 90
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 346
gtgcacttgg atttttcttc agcagagatg ggatttcctc atgctgccca ggctaatgtt 60
gaactcctgg gctcaagtga tctgctcacc 90
<210> 347
<211> 34
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 347
Gly Glu Lys Ile Leu Phe Ile Arg Gly Leu His Gly Cys Asp Tyr Ile
1 5 10 15
Ser Thr Ala Lys Ala Lys Gln Thr Phe Lys Met Leu His Asn Lys His
20 25 30
Val Met
<210> 348
<211> 102
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 348
ggagaaaaga tcctcttcat taggggtctt catggttgtg actatatctc cacagccaaa 60
gcaaagcaga catttaagat gctgcacaac aaacatgtca tg 102
<210> 349
<211> 33
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 349
Gly Phe Phe Glu Thr Glu Met Ala Val Pro Phe Phe Ser Arg Lys Ile
1 5 10 15
Arg Lys Val Arg Arg Ala Ile Met Lys Trp Thr Phe Cys Cys Tyr Phe
20 25 30
Tyr
<210> 350
<211> 99
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 350
ggcttctttg agactgaaat ggcagtcccc ttcttttcca gaaaaattag aaaagtcaga 60
agagcaataa tgaaatggac attttgctgt tatttctat 99
<210> 351
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 351
Asp Ser Gln Val Glu Thr Thr Val Trp Gly Val Gly Asn Arg Gln Glu
1 5 10 15
Trp Arg Glu Ile Leu Tyr Gly Ser Thr Gln Asn Phe Ala Ser Leu Leu
20 25 30
<210> 352
<211> 96
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 352
gacagtcaag tggaaacaac tgtctgggga gttggaaata ggcaagaatg gagagaaatt 60
ttgtatggca gtacacagaa ttttgcaagt ttattg 96
<210> 353
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 353
Trp Thr Arg Pro Glu Lys Gln Glu Leu Asn Ser Ser Cys Cys Ser Leu
1 5 10 15
Ile Leu
<210> 354
<211> 54
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 354
tggactcgac cagagaagca agagctcaac tcatcttgtt gctcacttat ttta 54
<210> 355
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 355
Leu Gly Arg Leu Glu Glu Ala Lys Ser Phe Glu Thr Glu Glu Asn
1 5 10 15
<210> 356
<211> 45
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 356
ctgggtcgct tggaagaagc caagtccttt gaaactgagg aaaac 45
<210> 357
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 357
Leu Gly Arg Leu Glu Glu Ala Lys Val Pro Leu Lys Met Leu Leu Phe
1 5 10 15
<210> 358
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 358
ctgggtcgct tggaagaagc caaggtgcca ttgaaaatgc tgctcttc 48
<210> 359
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 359
Trp Leu Leu Arg Thr Trp Glu Arg Ala Asp Ser Gly Leu
1 5 10
<210> 360
<211> 39
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 360
tggctcctgc gcacctggga gagagctgac agtggcctt 39
<210> 361
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 361
Leu Val Ala Arg Pro Glu Ile Gln Ile Phe Met Glu Glu Asp Val Met
1 5 10 15
Lys Val Glu
<210> 362
<211> 57
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 362
cttgttgcaa ggccagagat tcagatcttt atggaagaag atgtcatgaa agtagag 57
<210> 363
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 363
Arg His Gln Glu Asn Val His Thr Val Leu Val His Gly Lys Val Lys
1 5 10 15
Gly Leu Phe Tyr Ile
20
<210> 364
<211> 63
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 364
agacaccagg aaaatgtcca cactgtatta gtacatggaa aagtgaaagg cctgttttat 60
ata 63
<210> 365
<211> 35
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 365
Ile Met Leu Ile Gly Asn Lys Ser Asn Cys Gln Lys Gln Leu Leu Arg
1 5 10 15
Asp Met Lys Ile Leu Asn Glu Phe Tyr His Gly Leu Ile Leu Thr Leu
20 25 30
Gln Leu Ser
35
<210> 366
<211> 105
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 366
atcatgctca ttgggaataa gagcaactgc cagaaacagc ttctcagaga tatgaagata 60
ttgaacgaat tttatcatgg tctgatattg acattgcaac tgtct 105
<210> 367
<211> 23
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 367
Pro Lys Val Phe Pro Lys Asn Gln Val Ile Ser Leu Ile Pro Lys Ala
1 5 10 15
Gln Glu Asp Pro Glu His Thr
20
<210> 368
<211> 69
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 368
ccaaaagtgt ttcccaaaaa tcaggtaata tctttaattc caaaagcaca ggaagaccct 60
gagcatact 69
<210> 369
<211> 66
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 369
Gly Trp Lys Ile Cys Arg Glu Gly Ile Gly Pro Val Met Leu Thr Met
1 5 10 15
Thr Ser Gly Glu Trp Ser Phe Ser Phe Leu Glu Ala Ile Cys Gly Val
20 25 30
Ser Arg Glu Pro Val Pro Arg Arg Arg His Cys Ile Trp Asp Thr Arg
35 40 45
Gly Gly Val Gly Leu Cys Glu Ala Ser Cys Trp Arg Pro Thr Ser Glu
50 55 60
Val Gly
65
<210> 370
<211> 198
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 370
ggctggaaga tttgccggga aggcattggg cctgttatgc tcacaatgac ttcaggtgaa 60
tggagtttca gtttcctgga ggccatctgt ggagtttcca gggaacctgt accgaggaga 120
aggcattgta tatgggacac tagaggaggt gtgggactgt gtgaagccag ctgttggagg 180
cctacgagtg aagtggga 198
<210> 371
<211> 45
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 371
Ile Asp Pro Ser Ser Pro Leu His Thr Tyr Tyr Glu Arg Ile Thr Lys
1 5 10 15
Gly Arg Asn Pro Glu Arg Arg Tyr Met Lys Pro Glu Arg Ile Ser Pro
20 25 30
Gly His Glu Ala Met Glu Lys Asn Leu Glu Asp Asn Leu
35 40 45
<210> 372
<211> 135
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 372
attgatccaa gctctccctt acatacctac tatgaaagaa ttactaaagg acgtaatcca 60
gaaagaagat atatgaaacc ggaacgaatc agtccgggac acgaggccat ggaaaaaaac 120
cttgaagata actta 135
<210> 373
<211> 47
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 373
Asn Met Ala Asp Met Leu Tyr Asn Phe Leu Ser Gln Thr Ser Ala Ala
1 5 10 15
Ala Lys Leu Asn Leu Gln Phe Glu Met Ile Thr Ala Val Phe Arg Leu
20 25 30
Asn Arg Cys Ala Glu Cys Leu Gly Leu Leu Leu Gln Glu Asn Ser
35 40 45
<210> 374
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 374
aacatggctg acatgcttta taatttcctt tcacagacct cagcagctgc caagttgaat 60
ctgcaatttg agatgataac agcagtattc aggctcaata gatgtgcgga atgtctaggg 120
ctacttctcc aggagaacag c 141
<210> 375
<211> 36
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 375
Gln Ile Leu Gln Gln Ala Leu Lys Lys Leu Pro Phe Ser Leu Cys Ile
1 5 10 15
Thr Glu Cys Glu Thr Ile Ala Tyr His Leu Ala Arg Asp Ser Asn Gly
20 25 30
Asn Leu Glu Leu
35
<210> 376
<211> 108
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 376
cagatactac agcaagcctt gaagaaactg cctttttcat tatgtattac tgagtgtgag 60
accatagcct atcaccttgc cagggatagt aatggaaact tggaatta 108
<210> 377
<211> 27
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 377
Gln Ile Leu Gln Gln Ala Leu Lys Ile Ala Phe Leu Lys Val Val Val
1 5 10 15
Pro Leu Lys Leu His Pro Tyr Ser Phe Cys His
20 25
<210> 378
<211> 81
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 378
cagatactac agcaagcctt gaagatagca tttttgaaag tggtggtgcc tttgaaactg 60
catccttact ccttttgtca c 81
<210> 379
<211> 98
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 379
Tyr Glu Ser Pro Ile Phe Ser Arg Asp Arg Val Asn Pro Gly Ala Leu
1 5 10 15
Ser Gly Ser Leu Gly Gln Ala Arg Ala Ala Cys Trp Arg Thr Leu Gly
20 25 30
Ser Leu Lys Pro Gly Gly Glu Phe Arg Ala Ala Glu Gln Arg Arg Ala
35 40 45
Gly Trp Val Pro Gly Ala Pro Gly Phe Thr Cys Ser Leu Ile Ser Ser
50 55 60
Arg Phe Pro Arg Glu Arg Phe Cys Leu Arg His Arg Ser Ser Trp Arg
65 70 75 80
Gly Ala Arg Arg Val Gln Cys Val Cys Pro Gly Gln Thr Glu Gly Leu
85 90 95
Trp Leu
<210> 380
<211> 294
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 380
tatgagagtc ccatcttcag cagagaccga gtgaatccag gtgccctgag tggctcgctg 60
ggtcaggccc gcgcggcctg ctggaggacc ttggggtctt tgaagcctgg gggagagttc 120
agagcggcag aacagcgcag ggctggctgg gtgccaggcg ctcccgggtt cacctgcagt 180
ttaataagct cgaggtttcc gagagagcgc ttttgcctac gccatcgcag cagctggcgt 240
ggtgcacgcc gtgtccaatg cgtgtgccct gggcaaactg aaggcctgtg gctg 294
<210> 381
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 381
Phe Ser Gln Asn Met Asn Thr Lys Met Ile Arg Gly Thr Glu Arg Lys
1 5 10 15
Gln Gln Tyr Tyr Gly Leu Gln Ile Leu Glu
20 25
<210> 382
<211> 78
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 382
ttttctcaga atatgaatac gaaaatgatt agaggaacag aaagaaagca acagtactat 60
ggactacaaa ttttggaa 78
<210> 383
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 383
Gly Glu Pro Gly Glu Asp Ala Gly Ile Gly Arg Pro Glu Glu Arg Glu
1 5 10 15
Arg Glu Glu Glu Met Ala Asp Gln
20
<210> 384
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 384
ggggagccag gggaggacgc aggaataggg aggcctgagg agagggagag agaggaggag 60
atggctgatc ag 72
<210> 385
<211> 24
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 385
Pro Pro Gly Gly His Ser Pro Gln Asp Leu Ser Ile Arg Glu Ile Phe
1 5 10 15
Cys Leu Gly His Lys Glu Val Cys
20
<210> 386
<211> 72
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 386
cctccgggtg gacattcccc tcaggatttg tctattagag agatcttttg ccttgggcat 60
aaagaagtct gc 72
<210> 387
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 387
Asn Tyr Arg Asn Leu Val Phe Leu Asp Pro Cys Phe Gln Glu Asn Leu
1 5 10 15
<210> 388
<211> 48
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 388
aactacagaa acctggtctt cctggatccc tgttttcaag aaaatctt 48
<210> 389
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 389
Tyr Lys Leu Val Val Val Gly Ala Ala Gly Val Gly Lys Ser Ala Leu
1 5 10 15
Thr
<210> 390
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 390
tataaacttg tggtagttgg agctgctggc gtaggcaaga gtgccttgac g 51
<210> 391
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 391
Tyr Lys Leu Val Val Val Gly Ala Asp Gly Val Gly Lys Ser Ala Leu
1 5 10 15
Thr
<210> 392
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 392
tataaacttg tggtagttgg agctgatggc gtaggcaaga gtgccttgac g 51
<210> 393
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 393
Lys Leu Val Val Val Gly Ala Gly Asp Val Gly Lys Ser Ala Leu Thr
1 5 10 15
Ile
<210> 394
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 394
aaacttgtgg tagttggagc tggtgacgta ggcaagagtg ccttgacgat a 51
<210> 395
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 395
Lys Leu Val Val Val Gly Ala Gly Arg Val Gly Lys Ser Ala Leu Thr
1 5 10 15
Ile
<210> 396
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 396
aaacttgtgg tagttggagc tggtcgcgta ggcaagagtg ccttgacgat a 51
<210> 397
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 397
Leu Asp Ile Leu Asp Thr Ala Gly His Glu Glu Tyr Ser Ala Met Arg
1 5 10 15
Asp
<210> 398
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 398
ttggatattc tcgacacagc aggtcacgag gagtacagtg caatgaggga c 51
<210> 399
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 399
Leu Asp Ile Leu Asp Thr Ala Gly Arg Glu Glu Tyr Ser Ala Met Arg
1 5 10 15
Asp
<210> 400
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 400
ttggatattc tcgacacagc aggtcgagag gagtacagtg caatgaggga c 51
<210> 401
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 401
Leu Asp Ile Leu Asp Thr Ala Gly Lys Glu Glu Tyr Ser Ala Met Arg
1 5 10 15
Asp
<210> 402
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 402
ttggatattc tcgacacagc aggtaaagag gagtacagtg caatgaggga c 51
<210> 403
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 403
Tyr Thr His Phe Thr Ser Pro Ile Lys Arg Tyr Ala Asp Val Ile Val
1 5 10 15
His
<210> 404
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 404
tacacacatt ttacttcacc cattaaaaga tacgcagatg tcattgttca t 51
<210> 405
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 405
Ile Gly Asp Phe Gly Leu Ala Thr Glu Lys Ser Arg Trp Ser Gly Ser
1 5 10 15
His
<210> 406
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 406
ataggtgatt ttggtctagc tacagagaaa tctcgatgga gtgggtccca t 51
<210> 407
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 407
Gln Arg Ile Gly Ser Gly Ser Phe Ala Thr Val Tyr Lys Gly Lys Trp
1 5 10 15
His
<210> 408
<211> 51
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
олигонуклеотид»
<400> 408
caaagaattg gatctggatc atttgcaaca gtctacaagg gaaagtggca t 51
<210> 409
<211> 9
<212> Белок
<213> Homo sapiens
<400> 409
Cys Thr Glu Leu Lys Leu Ser Asp Tyr
1 5
<210> 410
<211> 9
<212> Белок
<213> Homo sapiens
<400> 410
Asn Leu Val Pro Met Val Ala Thr Val
1 5
<210> 411
<211> 9
<212> Белок
<213> Homo sapiens
<400> 411
Leu Ile Tyr Arg Arg Arg Leu Met Lys
1 5
<210> 412
<211> 9
<212> Белок
<213> Homo sapiens
<400> 412
Leu Tyr Ser Ala Cys Phe Trp Trp Leu
1 5
<210> 413
<211> 9
<212> Белок
<213> Homo sapiens
<400> 413
Asn Pro Lys Ala Ser Leu Leu Ser Leu
1 5
<210> 414
<211> 9
<212> Белок
<213> Homo sapiens
<400> 414
Glu Leu Arg Ser Arg Tyr Trp Ala Ile
1 5
<210> 415
<211> 9
<212> Белок
<213> Homo sapiens
<400> 415
Asn Pro Lys Ala Ser Leu Leu Ser Leu
1 5
<210> 416
<211> 9
<212> Белок
<213> Homo sapiens
<400> 416
Ile Val Thr Asp Phe Ser Val Ile Lys
1 5
<210> 417
<211> 9
<212> Белок
<213> Homo sapiens
<400> 417
Asn Pro Lys Ala Ser Leu Leu Ser Leu
1 5
<210> 418
<211> 9
<212> Белок
<213> Homo sapiens
<400> 418
Asn Leu Val Pro Met Val Ala Thr Val
1 5
<210> 419
<211> 9
<212> Белок
<213> Homo sapiens
<400> 419
Leu Ile Tyr Arg Arg Arg Leu Met Lys
1 5
<210> 420
<211> 9
<212> Белок
<213> Homo sapiens
<400> 420
Asn Leu Val Pro Met Val Ala Thr Val
1 5
<210> 421
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полипептид»
<400> 421
Thr Gln Arg Leu Pro Gly His Lys Val Ser Asn Ser Cys Met Thr Gly
1 5 10 15
Leu Val Leu Thr Phe Thr Lys Arg Asp Pro Phe His Lys Pro Val Thr
20 25 30
Trp Cys Gly Gln Leu Ala Asp Val Arg Gln Cys Met Phe His Ser Ile
35 40 45
Arg Glu Arg Ala His Pro Leu Gln Arg Ala Leu Ala Thr Leu Asn Phe
50 55 60
Phe Phe Val Ser Phe Tyr Thr Ala Leu Tyr Leu Thr His Pro Leu Leu
65 70 75 80
Thr Leu Gln Thr Trp Glu Val Val Val Thr Gly Gln Glu Ser Arg Met
85 90 95
Phe Thr Leu Leu Leu Glu Ile Ser Tyr Val Ser Tyr Tyr Cys Met Tyr
100 105 110
Leu Val Met Arg Gly His Val His
115 120
<210> 422
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
полинуклеотид»
<400> 422
actcaacggt tgccaggaca caaagtaagc aacagctgca tgaccggttt agtcctgacg 60
tttacaaaga gggacccttt ccataagcct gtaacttggt gtgggcagct tgccgatgtc 120
aggcagtgca tgtttcactc gattagggag agagcgcacc ctctccagag ggctttggcc 180
acgcttaatt ttttctttgt ttccttctat actgctttat atctcacaca tcccctctta 240
actctccaga catgggaagt tgttgtgaca ggtcaggaaa gtcgtatgtt tacccttctc 300
ctagaaatta gttatgtaag ctattattgt atgtatttag taatgagggg acatgtgcat 360
<210> 423
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 423
Met Ala Cys Pro Gly Phe Leu Trp Ala Leu Val Ile Ser Thr Cys Leu
1 5 10 15
Glu Phe Ser Met Ala
20
<210> 424
<211> 77
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 424
Met Gln Ile Phe Val Lys Thr Leu Thr Gly Lys Thr Ile Thr Leu Glu
1 5 10 15
Val Glu Pro Ser Asp Thr Ile Glu Asn Val Lys Ala Lys Ile Gln Asp
20 25 30
Lys Glu Gly Ile Pro Pro Asp Gln Gln Arg Leu Ile Phe Ala Gly Lys
35 40 45
Gln Leu Glu Asp Gly Arg Thr Leu Ser Asp Tyr Asn Ile Gln Lys Glu
50 55 60
Ser Thr Leu His Leu Val Leu Arg Leu Arg Gly Val Arg
65 70 75
<210> 425
<211> 28
<212> Белок
<213> Искусственная последовательность
<220>
<221> источник
<223> /note=«Описание искусственной последовательности: синтетический
пептид»
<400> 425
Met Gly Gln Lys Glu Gln Ile His Thr Leu Gln Lys Asn Ser Glu Arg
1 5 10 15
Met Ser Lys Gln Leu Thr Arg Ser Ser Gln Ala Val
20 25
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ АФРИКАНСКОЙ ЧУМЫ СВИНЕЙ | 2020 |
|
RU2819672C2 |
| ВИРУСНЫЕ ВЕКТОРЫ, КОДИРУЮЩИЕ РЕКОМБИНАНТНЫЕ ВАРИАНТЫ FIX С ПОВЫШЕННОЙ ЭКСПРЕССИЕЙ, ДЛЯ ГЕНОТЕРАПИИ ГЕМОФИЛИИ В | 2018 |
|
RU2773956C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ НА ОСНОВЕ АКТИВИРУЮЩИХ Т-КЛЕТКИ БИСПЕЦИФИЧЕСКИХ АНТИГЕНСВЯЗЫВАЮЩИХ МОЛЕКУЛ ПРОТИВ CD3 И ФОЛАТНОГО РЕЦЕПТОРА 1 (FOLR1) И АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХСЯ С ОСЬЮ PD-1 | 2015 |
|
RU2753902C2 |
| НОВЫЙ ВАРИАНТ MdtH И СПОСОБ ПОЛУЧЕНИЯ О-ФОСФОСЕРИНА, ЦИСТЕИНА И ПРОИЗВОДНОГО ЦИСТЕИНА С ЕГО ПРИМЕНЕНИЕМ | 2021 |
|
RU2835524C2 |
| АНТИТЕЛА К ENTPD2, ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ И СПОСОБЫ ПРИМЕНЕНИЯ АНТИТЕЛ И ВИДОВ КОМБИНИРОВАННОЙ ТЕРАПИИ | 2019 |
|
RU2790991C2 |
| КОНСТРУКТЫ Т-КЛЕТОЧНОГО РЕЦЕПТОРА И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2785954C2 |
| МИКРООРГАНИЗМ, ПРОДУЦИРУЮЩИЙ ЛИЗИН, И СПОСОБ ПРОДУЦИРОВАНИЯ ЛИЗИНА | 2021 |
|
RU2797843C9 |
| C3-СВЯЗЫВАЮЩИЕ АГЕНТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2802307C2 |
| КОМБИНИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, НАЦЕЛЕННЫЕ НА PD-1, TIM-3 И LAG-3 | 2018 |
|
RU2795232C2 |
| НОВЫЕ КОНСТРУКЦИИ ХИМЕРНОГО АНТИГЕННОГО РЕЦЕПТОРА, СОДЕРЖАЩИЕ ДОМЕНЫ TNFR2 | 2019 |
|
RU2808254C2 |
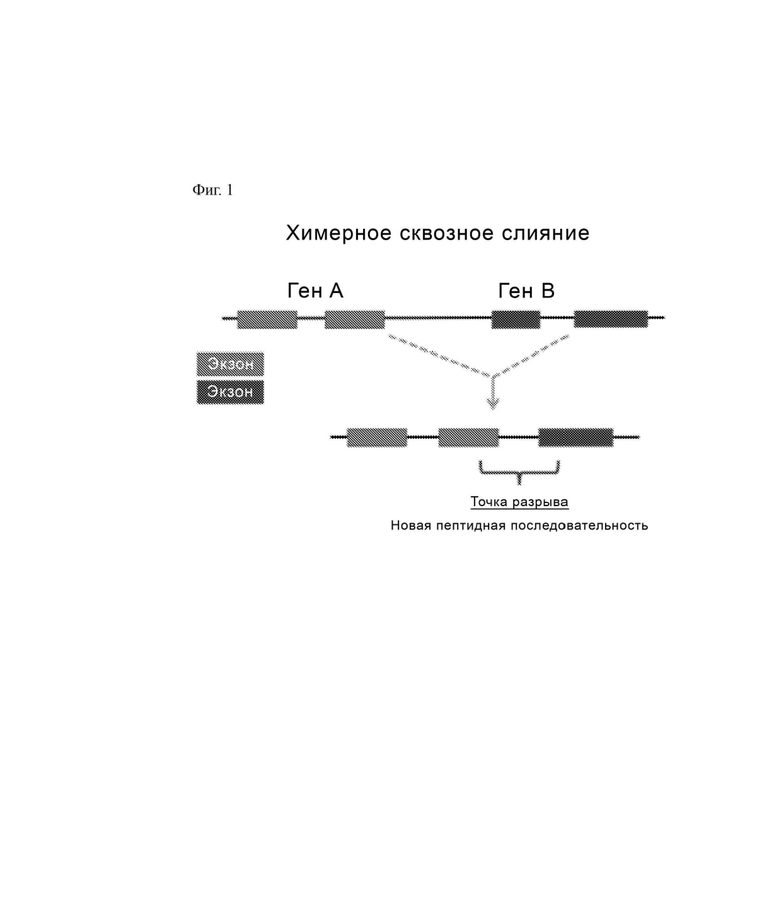

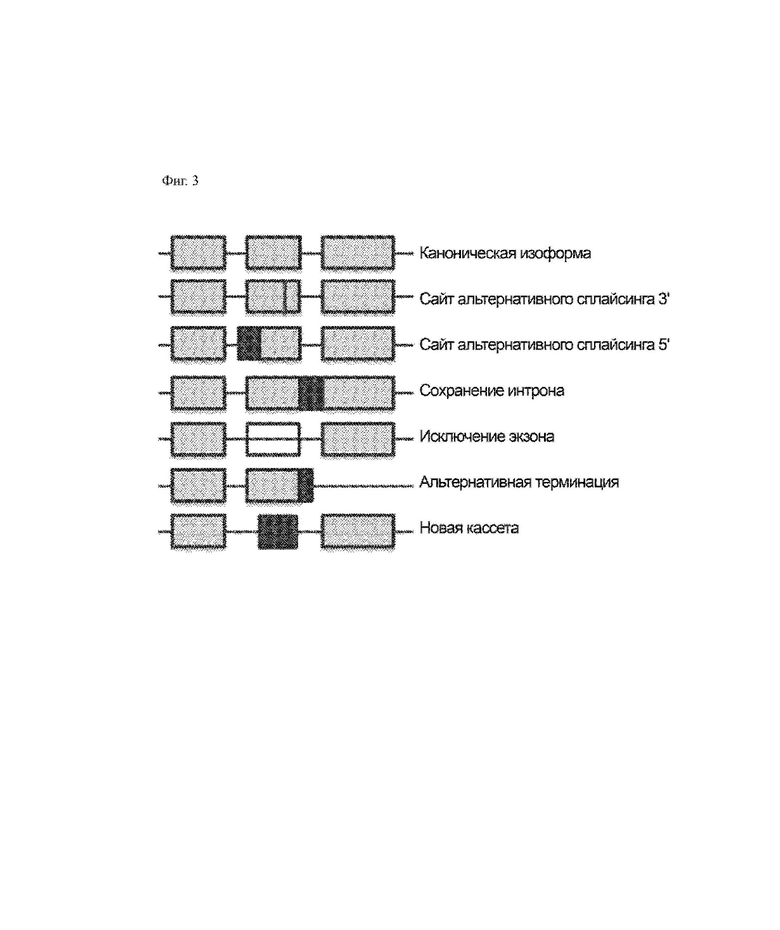









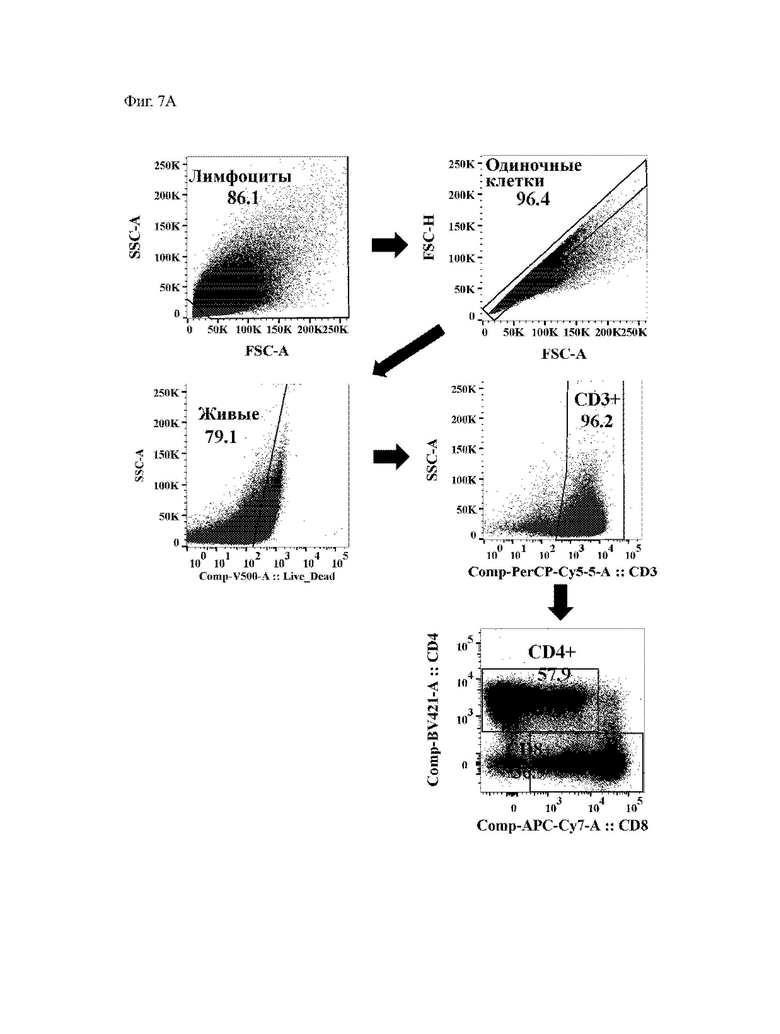
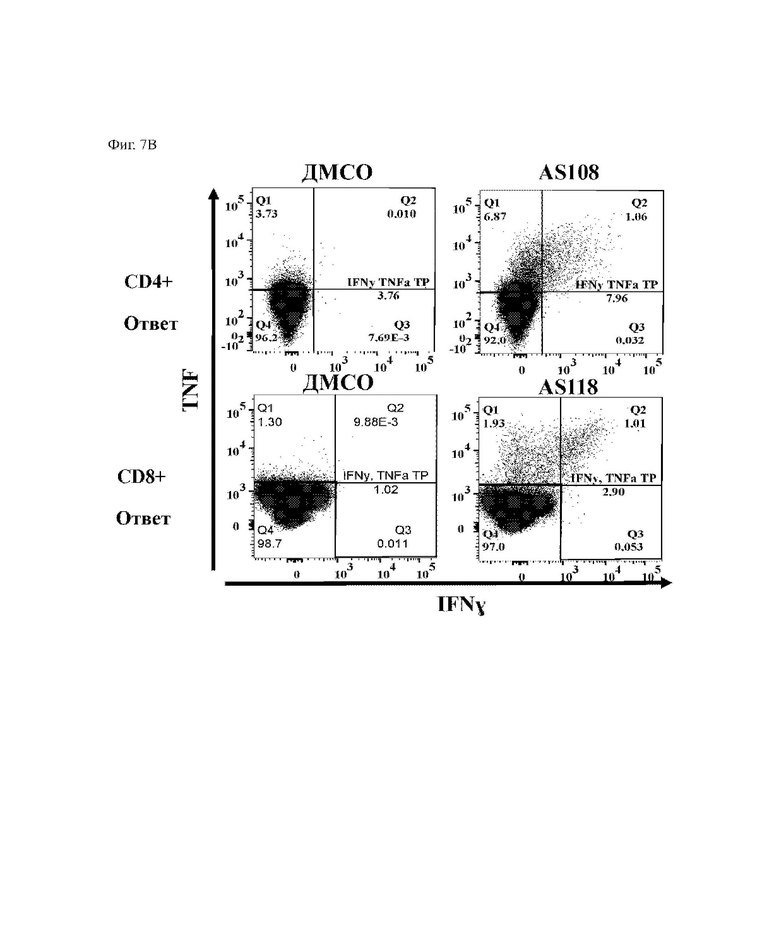
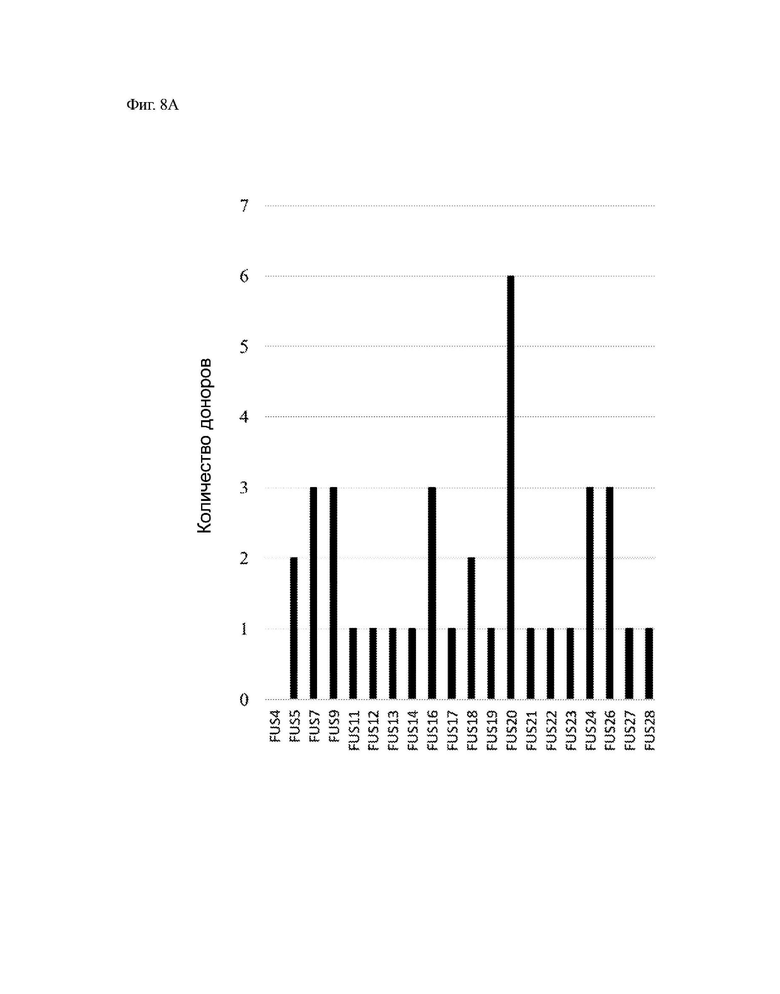
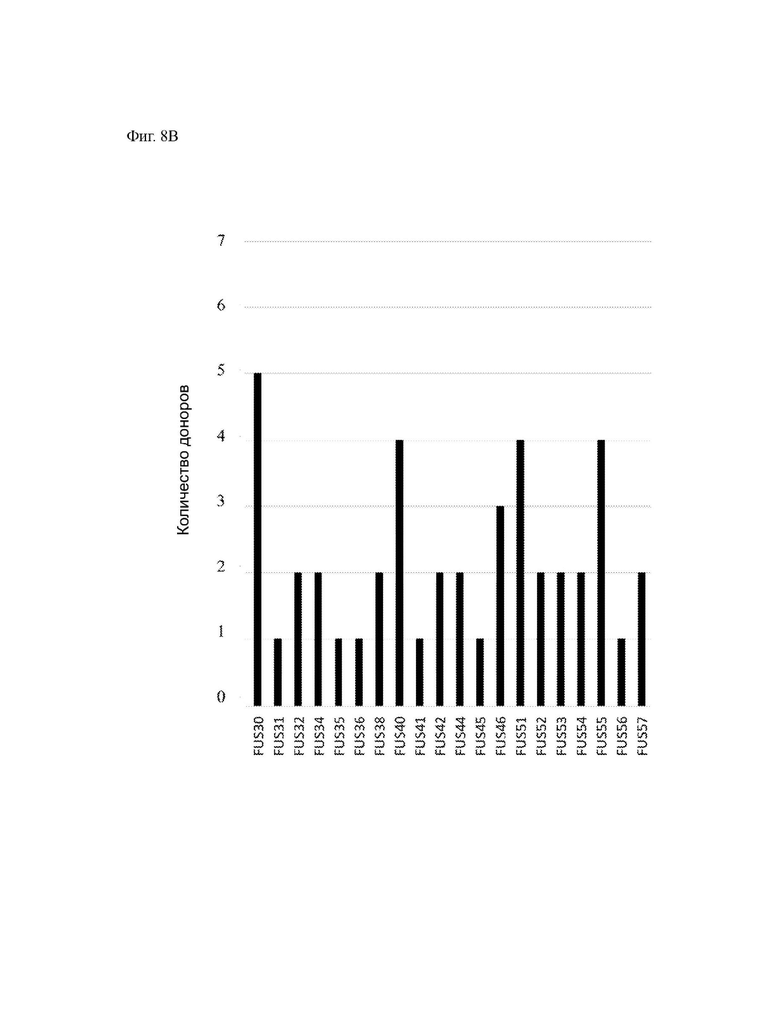
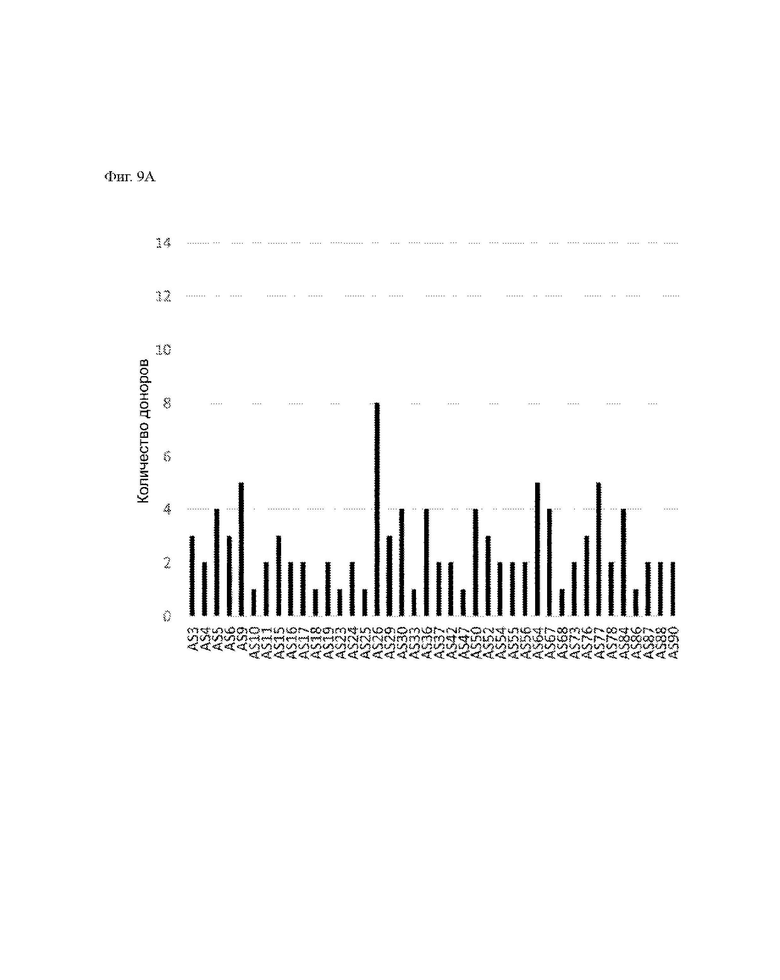
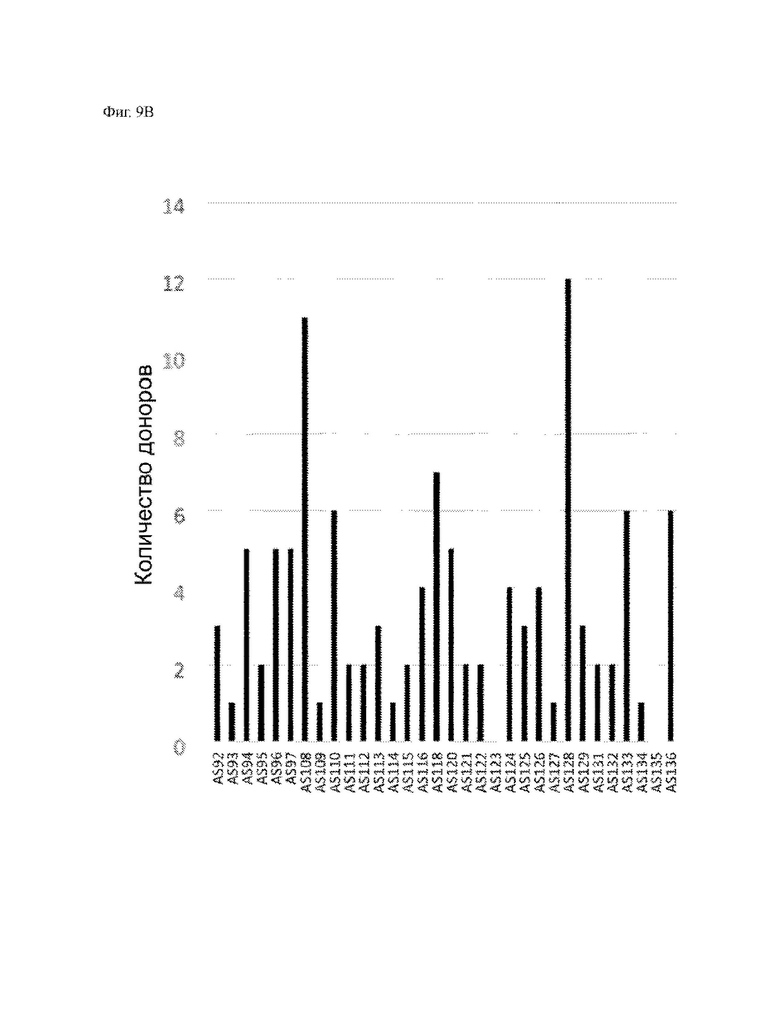
Изобретение относится к области биотехнологии, в частности к полипептидам для снижения риска и для отсрочки возникновения множественной миеломы у субъекта. Также раскрыты полинуклеотиды, кодирующие вышеуказанные полипептиды, вектор экспрессии, фармацевтические композиции для снижения риска и для отсрочки возникновения множественной миеломы у субъекта. Изобретение также относится к способу индукции иммунного ответа против множественной миеломы у субъекта. Изобретение позволяет обеспечивать индукцию иммунного ответа против множественной миеломы у субъекта. 12 н. и 23 з.п. ф-лы, 9 ил., 12 табл., 5 пр.
1. Полипептид для снижения риска возникновения множественной миеломы у субъекта, где полипептид содержит:
a) одну или более аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 403, 407 и 421; или
b) одну или более аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421;
где полипептид индуцирует иммунный ответ против множественной миеломы у субъекта.
2. Полипептид для отсрочки возникновения множественной миеломы у субъекта, где полипептид содержит:
а) одну или более аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45, 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257, 259, 261, 263, 265, 267, 269, 271, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 295, 297, 299, 301, 303, 305, 307, 309, 311, 313, 315, 317, 319, 321, 323, 325, 327, 329, 331, 333, 335, 337, 339, 341, 343, 345, 347, 349, 351, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 373, 375, 377, 379, 381, 383, 385, 387, 389, 391, 403, 407 и 421; или
b) одну или более аминокислотных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421;
где полипептид индуцирует иммунный ответ против множественной миеломы у субъекта.
3. Полипептид по п. 1 или 2, в котором одна или более аминокислотных последовательностей соединены друг с другом в любом порядке.
4. Полипептид по п. 3, в котором одна или более аминокислотных последовательностей соединены друг с другом без линкера.
5. Полипептид по любому из пп. 1-4, который содержит одну или более обратных пептидных связей, D-изомеров аминокислот, химических модификаций или любую их комбинацию.
6. Полинуклеотид, кодирующий полипептид по любому из пп. 1-5.
7. Полинуклеотид по п. 6, содержащий:
а) одну или более полинуклеотидных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70, 72, 74, 76, 78, 80, 82, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104, 106, 108, 110, 112, 114, 116, 118, 120, 122, 124, 126, 128, 130, 132, 134, 136, 138, 140, 142, 144, 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 192, 194, 196, 198, 200, 202, 204, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224, 226, 228, 230, 232, 234, 236, 238, 240, 242, 244, 246, 248, 250, 252, 254, 256, 258, 260, 262, 264, 266, 268, 270, 272, 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298, 300, 302, 304, 306, 308, 310, 312, 314, 316, 318, 320, 322, 324, 326, 328, 330, 332, 334, 336, 338, 340, 342, 344, 346, 348, 350, 352, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 374, 376, 378, 380, 382, 384, 386, 388, 390, 392, 404, 408 и 422; или
b) одну или более полинуклеотидных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 8, 10, 12, 14, 18, 22, 24, 26, 28, 32, 34, 36, 38, 40, 42, 44, 46, 48, 52, 54, 56, 60, 62, 64, 68, 70, 72, 76, 80, 82, 84, 88, 90, 92, 102, 104, 106, 108, 110, 112, 114, 120, 122, 124, 126, 132, 134, 136, 144, 146, 148, 150, 152, 158, 162, 164, 166, 172, 174, 180, 186, 188, 198, 200, 208, 214, 218, 222, 224, 226, 242, 248, 250, 260, 266, 268, 270, 282, 286, 288, 290, 294, 298, 300, 302, 304, 306, 308, 330, 332, 334, 336, 338, 340, 342, 344, 346, 350, 354, 356, 358, 360, 362, 364, 366, 368, 370, 372, 376, 378, 380, 382, 384, 386 и 422.
8. Полинуклеотид по п. 7, где полинуклеотид содержит ДНК или РНК.
9. Полинуклеотид по п. 8, в котором РНК представляет собой мРНК.
10. Вектор экспрессии, содержащий полинуклеотид по любому из пп. 6-9.
11. Вектор по п. 10, который выбирают из аденовирусного вектора, поксвирусного вектора, аденоассоциированного вирусного вектора, ретро вирусного вектора, самореплицирующейся молекулы РНК и их комбинации.
12. Вектор по п. 11, в котором аденовирусный вектор происходит из hAd5, hAd7, hAd11, hAd26, hAd34, hAd35, hAd48, hAd49, hAd50, GAd20, GAd19, GAd21, GAd25, GAd26, GAd27, GAd28, GAd29, GAd30, GAd31, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAd146, ChAd147, PanAd1, PanAd2 или PanAd3.
13. Вектор по п. 11, в котором поксвирусный вектор выбирают из вектора вируса оспы, вектора вируса осповакцины, вектора вируса коровьей оспы, вектора вируса оспы обезьян, вектора вируса осповакцины Копенгаген (W), вектора аттенуированного вируса осповакцины Нью-Йорк (NYVAC) и вектора модифицированного вируса осповакцины Анкара (MVA).
14. Вектор по п. 11, который представляет собой аденовирусный вектор.
15. Вектор по п. 11, который представляет собой поксвирусный вектор.
16. Вектор по п. 11, который представляет собой самореплицирующуюся молекулу РНК.
17. Вектор по п. 12, где аденовирусный вектор происходит из hAd26 и где аденовирусный вектор содержит полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421.
18. Вектор по п. 12, где аденовирусный вектор происходит из GAd20 и где аденовирусный вектор содержит полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421.
19. Вектор по п. 13, где поксвирусный вектор представляет собой вектор MVA и где вектор MVA содержит полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421.
20. Вектор по п. 11, где вектор представляет собой самореплицирующуюся молекулу РНК и где самореплицирующаяся молекула РНК содержит полинуклеотид, кодирующий один или более полипептидов, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421.
21. Фармацевтическая композиция для снижения риска возникновения множественной миеломы у субъекта, содержащая эффективное количество полипептида по любому из пп. 1-5 и фармацевтически приемлемое вспомогательное вещество.
22. Фармацевтическая композиция для отсрочки возникновения множественной миеломы у субъекта, содержащая эффективное количество полипептида по любому из пп. 1-5 и фармацевтически приемлемое вспомогательное вещество.
23. Фармацевтическая композиция для снижения риска возникновения множественной миеломы у субъекта, содержащая эффективное количество полинуклеотида по любому из пп. 6-8 и фармацевтически приемлемое вспомогательное вещество.
24. Фармацевтическая композиция для отсрочки возникновения множественной миеломы у субъекта, содержащая эффективное количество полинуклеотида по любому из пп. 6-9 и фармацевтически приемлемое вспомогательное вещество.
25. Фармацевтическая композиция для снижения риска возникновения множественной миеломы у субъекта, содержащая эффективное количество рекомбинантного вируса, содержащего вектор по любому из пп. 10-20, и фармацевтически приемлемое вспомогательное вещество.
26. Фармацевтическая композиция для отсрочки возникновения множественной миеломы у субъекта, содержащая эффективное количество рекомбинантного вируса, содержащего вектор по любому из пп. 10-20, и фармацевтически приемлемое вспомогательное вещество.
27. Фармацевтическая композиция по п. 25 или 26, в которой вирус или рекомбинантный вирус выбирают из вируса hAd26, вируса MVA, вируса GAd20 и их комбинаций.
28. Способ индукции иммунного ответа против множественной миеломы у субъекта, где способ включает введение субъекту, нуждающемуся в этом, фармацевтической композиции по любому из пп. 21-27.
29. Способ индукции иммунного ответа против множественной миеломы у субъекта, где способ включает введение субъекту, нуждающемуся в этом, композиции, содержащей рекомбинантный вирус или самореплицирующуюся молекулу РНК, содержащую полинуклеотид, кодирующий по меньшей мере одну или более полипептидных последовательностей, выбранных из группы, состоящей из SEQ ID NO: 7, 9, 11, 13, 17, 21, 23, 25, 27, 31, 33, 35, 37, 39, 41, 43, 45, 47, 51, 53, 55, 59, 61, 63, 67, 69, 71, 75, 79, 81, 83, 87, 89, 91, 101, 103, 105, 107, 109, 111, 113, 119, 121, 123, 125, 131, 133, 135, 143, 145, 147, 149, 151, 157, 161, 163, 165, 171, 173, 179, 185, 187, 197, 199, 207, 213, 217, 221, 223, 225, 241, 247, 249, 259, 265, 267, 269, 281, 285, 287, 289, 293, 297, 299, 301, 303, 305, 307, 329, 331, 333, 335, 337, 339, 341, 343, 345, 349, 353, 355, 357, 359, 361, 363, 365, 367, 369, 371, 375, 377, 379, 381, 383, 385 и 421, и при этом введение включает одно или более введений композиции.
30. Способ по п. 28 или 29, в котором субъект экспрессирует или предположительно экспрессирует один или более полипептидов по п. 1.
31. Способ по п. 30, в котором один или более полипептидов по п. 1 присутствуют с частотой около 1% или более, около 2% или более, около 3% или более, около 4% или более, около 5% или более, около 6% или более, около 7% или более, около 8% или более, около 9% или более, около 10% или более, около 11% или более, около 12% или более, около 13% или более, около 14% или более, около 15% или более, около 16% или более, около 17% или более, около 18% или более, около 19% или более, около 20% или более, около 21% или более, около 22% или более, около 23% или более, около 24% или более, около 25% или более, около 26% или более, около 27% или более, около 28% или более, около 29% или более, около 30% или более, около 35% или более, около 40% или более, около 45% или более, около 50% или более, около 55% или более, около 60% или более, около 65% или более или около 70% или более у популяции субъектов, страдающих множественной миеломой.
32. Способ по п. 28 или 31, дополнительно включающий введение субъекту дополнительного противоракового терапевтического агента.
33. Способ по п. 32, в котором дополнительный противораковый терапевтический агент представляет собой химиотерапевтический агент, иммуномодулирующий агент, производное глутаминовой кислоты, ингибитор протеасом, алкилирующий агент, ингибитор микротрубочек, кортикостероид, лучевую терапию, таргетную терапию, высокодозную химиотерапию (ВДХТ) и трансплантацию стволовых клеток (ТСК), ингибитор контрольной точки, онколитический вирус, конъюгат антитело-лекарственное средство, хирургическое вмешательство или любую их комбинацию.
34. Способ по п. 33, в котором дополнительный противораковый терапевтический агент представляет собой антитело к CTLA-4, лиганд CTLA-4, ингибитор оси PD-1, ингибитор оси PD-L1, агонист TLR, агонист CD40, агонист ОХ40, гидроксимочевину, руксолитиниб, федратиниб, агонист 41ВВ, агонист CD28, антагонист STING, антагонист RIG-1, терапию TCR-T, терапию CAR-T, лиганд FLT3, сульфат алюминия, ингибитор BTK, антитело к CD38, ингибитор CDK, антитело к CD33, антитело к CD37, антитело к CD25, ингибитор GM-CSF, IL-2, IL-15, IL-7, молекулы перенаправления CD3, помалимиб, IFNγ, IFNα, TNFα, антитело к VEGF, антитело к CD70, антитело к CD27, антитело к ВСМА, антитело к GPRC5D или любую их комбинацию.
35. Способ по п. 33, в котором ингибитор контрольной точки представляет собой ипилимумаб, цетрелимаб, пембролизумаб, ниволумаб, синтилимаб, цемиплимаб, торипалимаб, камрелизумаб, тислелизумаб, достралимаб, спартализумаб, пролголимаб, бальстилимаб, будигалимаб, сасанлимаб, авелумаб, атезолизумаб, дурвалумаб, энвафолимаб, йодаполимаб или любую их комбинацию.
| US 9757439 B2, 12.09.2017 | |||
| US 9775892 B2, 03.10.2017 | |||
| EP 3419656 A1, 02.01.2019 | |||
| Perumal D et al., Mutation-derived Neoantigen-specific T-cell Responses in Multiple Myeloma, Clin Cancer Res, 2020, v | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Двигатель внутреннего горения | 1921 |
|
SU450A1 |
| WO 2017173321 A1, 05.10.2017 | |||
| Барышникова М.А | |||
| и др., Неоантигены в иммунотерапии опухолей, Российский биотерапевтический | |||
Авторы
Даты
2025-06-06—Публикация
2021-02-12—Подача