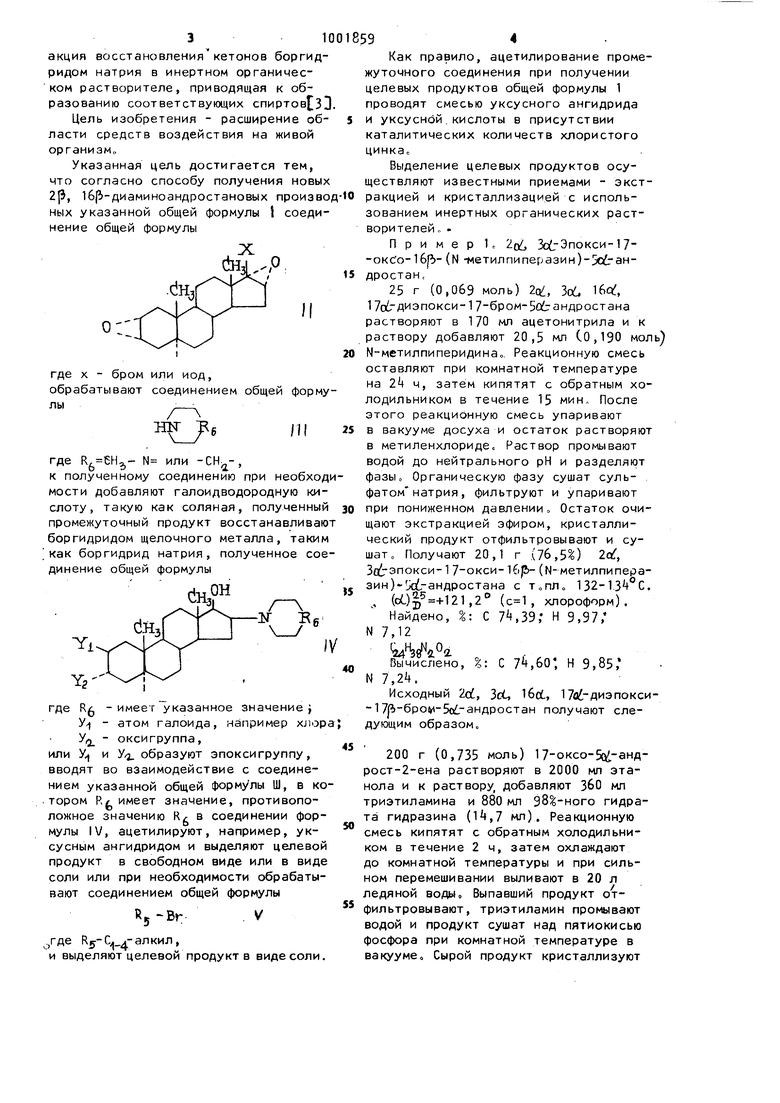
3100 акция восстановлениякетонов боргидридом натрия в инертном органическом растворителе, приводящая к образованию соответствующих спиртов ЗЗ. Цель изобретения - расширение области средств воздействия на живой организм Указанная цель достигается тем, что согласно способу получения новых , 1б(Ь-диаминоандростановых произв ных указанной общей формулы { соеди нение общей формулы где X - бром или иод, обрабатывают соединением общей форм лы,:, где ,,- N или , к полученному соединению при необход мости добавляют галоидводородную ки слоту, такую как соляная, полученны промежуточный продукт восстанавливаю боргидридом щелочного металла, таки как боргидрид натрия, полученное со динение общей формулы йн,н где R - имеет указанное значение j y/j - атом галоида, например хлор y/j - оксигруппа, или У и y/j. образуют эпоксигруппу, вводят во взаимодействие с соединением указанной общей формулы Ш, в ко . тором Р./ имеет значение, противоположное значению К в соединении формулы IV, ацетилируют, например, уксусным ангидридом и выделяют целевой продукт в свободном виде или в виде соли или при необходимости обрабатывают соединением общей формулы Rj-Br /де К5-Ц 4-алкил, и выделяют целевой продукт в виде соли 9 Как правило, ацетилирование промежуточного соединения при получении целевых продуктов общей формулы 1 проводят смесью уксусного ангидрида и уксусной.кислоты в присутствии каталитических количеств хлористого цинка Выделение целевых продуктов осуществляют известными приемами - экстракцией и кристаллизацией с использованием инертных органических растворителей,. Пример К ZQ/, ЗсСЭпокси-17-окс;о-1б)- (N -метил пи пер азин) андростан, 25 г (0,069 моль) 2Q/, Зоб 1бо, 1 Уобдиэпокси-1 7 6poM-5ot андростана растворяют в 170 мл ацетонитрила и к раствору добавляют 20,5 мл С0,190 моль) N-метилпиперидинао. Реакционную смесь оставляют при комнатной температуре на ч, затем кипятят с обратным холодильником в течение 15 мин. После этого реакционную смесь упаривают в вакууме досуха и остаток растворяют в метиленхлориде. Раствор промывают водой до нейтрального рН и разделяют фазы о Органическую фазу сушат сульфатом натрия , фильтруют и упаривают при пониженном давлении Остаток очищают экстракцией эфиром, кристаллический продукт отфильтровывают и сушат. Получают 20,1 г .(7б,5%) 2af, За1гэпокси- 1 7-окси- (N- метилпиперазин):хз6 андростана с ТоПЛ 132-13+ с. , (о(,)+121,2 ( , хлороформ). Найдено, %: С 7,39; Н 9,97, N 7,12 Вычислено, % С 7,60; Н 9,85, N 7,2i|. Исходный 2(, Зоб, I6ct, 17а -диэпокси-17р-бро -5о1 -андростан получают следующим образом, 200 г (0,735 моль) 17-оксо-5й1-андрост-2-ена растворяют в 2000 мл этанола и к раствору, добавляют ЗбО мл триэтиламина и 880 мл 98%-ного гидрата гидразина (1,7 мл). Реакционную смесь кипятят с обратным холодильником в течение 2 ч, затем охлаждают до комнатной температуры и при сильном перемешивании выливают в 20 л ледяной воды. Выпавший продукт отфильтровывают, триэтиламин промывают водой и продукт сушат над пятиокисью фосфора при комнатной температуре в вакууме. Сырой продукт кристаллизуют 5 1 из гексана. Получают 185 г (91%) 1 -гидразон-5сз6-андрост-2-ена, ст.пл. 12 132°С. U} -98° (, хлороформ). , %: С 7Э,2; Н 10,60, N 9,61, . Вычислено, -%: С 79,60; Н 10,50; N 9,70 30 г (0,100 моль) 17-rMflpa30H-5d-андрост-2-ена растворяют в 200 мл безводного пиридина, раствор охлаждают до , При температуре от О до -10°С добавляют раствор 30 г(,0 ,1б8мол М--бромсукцинимида в 330 мл пиридина. Реакционную смесь перемешивают до прекращения выделения азота, затем добавляют 3 л 5%-ной охлажденной соляной кислоты. Выпавший продукт экстрагируют 300-i 00 мл чётыреххлористого (лерода Соединенные экстракты сначала промывают до нейтральной (рН 7) реакции водной соляной кислотой, затем водой Промытый раствор сушат над сульфатом натрия, фильтруют, фильтрат упаривают досуха« Маслянистый остаток растирают с 100 мл гек сана, выделившийся при этом побочный продукт отфильтровывают. Фильтрат выпаривают досуха, и остаток растирают со смесью этанола и ацетона 9:1 (50 мл). После фильтрования и сушки получают 23, г (66%) 17-бром-5с6-андроста-2,1б-диена с т.пл. 7б-77 С. (oL) +7 ,2° (, хлороформ). Найдено, %: С 71,21; Н 8,15, Вг 23,57 вычислено; %: С 71,35; Н 8,07, Вг 23,80 Таким же образом из 17тидразон-5(-андрост-2-ена и N-иодсукцинимида получают соответственное и од нор соединение. Выход 66% 17 иод-5с -андроста-2,16-диена с т„пл, 71-71С. (oL) +56,3 (, хлороформ). Найдено, %: С 59,52; Н 6,90;з 32,9 0,.7 Вычислено, %: С 59,70; Н 7,07;D 33,13. 90 г (0,27 моль) 17-бром-5оЬ-андроста-2,1б-диена растворяют в 1100 мл хлороформа. При комнатной температуре добавляют 7,2%-ный раствор 0,81 мл М-хлорнадбензойной кислоты (1600 мл) в хлороформе. Реакционную смесь выдер живают при комнатной температуре в 59« течение 2Ц ч, затем охлаждают до и промывают сначала при охлаждении льдом, 10%-ной водной гидроокисью натрия, затем водой, не содержащей кислоты (рН 7). Фазы разделяют, органическую фазу сушат рульфатом натрия, фильтруют, фильтрат выпаривают досуха. Масляный остаток растирают с 100 мл эфира, фильтруют и отфильтрованный ырой продукт кристаллизуют из ацетрнитрила. Получают 85,7 г С 87%- 2oL, 3d 1бо 1Я -диэпокси-17р-бром-5оС андростана с т,пл. 1бО-1б2С (о:) +73,5 (, хлороформ). Найдено, %: С 61,79, Н 7,20; Вг 21,7 C HnBrO Вычислено, %: С 62,00, Н 7,35, Вг 21,80 Таким же образом из 17-иод-5а андроста-2,1б-диена получают с выходом 8U 20/, Ы, 1ба;, 1 Ъ -диэпокси-17р-иод 5-с -андростан, П р и м е р 2, 2/ -Хлор-Зл Окси-17-оксо- 16()-пиперидин-5с -андроста на гидрохлорид, 12,5 г (0,03 моль) 2а:, Зй, 1баГ, 17с -диэпокси-17-бром-5с -андростана растворяют в 85 мл ацетонитрила и добавляют 10 мл (0,1 моль) пиперидина. . Реакционную смесь кипятят с обратным холодильником в течение 1 ч, затем выпаривают при пониженном давлении. Остаток после упаривания растворяют в диэтиловом эфире и раствор промывают водой до нейтральной реакции (рН 7). Фазы разделяют, из органической фазы 6%-ным эфирным раствором соляной кислоты высаживают продукт в виде гидрохлорида. Его отфильтровывают, пробывают эфиром и сушат при в вакууме. Получают 10,3 г (70,0%) гидрохлорида 2|5 хлор-Зо -окси-17-оксо-1бЗ-пиперидин-5об7андростана ст,пЛо 237-239«С (разл.). Найдено, %: С 6i,6 Н 9,0, С1 15,7 C Hj O NCIjz. йГчислено, %: С 6,8, ,Н 8,7, С 16,0 Примерз. 2csL, Зо -Эпокси-1; 3-окси-1б|Ь-.(Н-метилпиперазин -5оЬандростан,. . 15 г (С},038 моль) 2:, Зо -эпокси-17-оксо-166-(N-метилпиперазин) -андростана растворяют в смеси 45 мл метиленхлорида и 120 мл метанола и к раствору добавляют при температуре ниже 12 г (0,31 моль) боргидрида натрия. К концу добавления выкри таллизовывается продукт восстановления. Кристаллизационную смесь интен сивно перемешивают в течение 12 ч, затем отгоняют растворитель при пони женном давлении при температуре ниже , Остаток обрабатывают водой, кристаллы отфильтровывают, растворяют в хлороформе, раствор сначала про мывают 5 -иь1м раствором едкого натра, затем водой до нейтральной реакции Отделенную органическую фазу сушат сульфатом натрия, фильтруют и фильтрат упаривают досуха. После перекристаллизации остатка из ацето нитрила получарт 11,7 г (77,5 %} 2oL, Зо -эпокси-17| гокси-I6pr (N-метилпиперазин -Ьс -андростана с т.пл. Ui9-153°C, (ci) +27,1 (, хлороформ). °- С 7,01 ; Н 10,1; Найдено, %: N 7.07. С 7,2о; Н 10,30; Вычислено, N 7,22 П р и м е р 4, 2|УХлор-Зо6 7р-диоксЛ- 1б| пипепазин-5о -андростан. 25 г (1),05б моль) гндрохлорида 2J -xлop-3(t-oкcи-1 7-0 ксо- 16)5-пипе-ридин-5с6 андростана растворяют в смеси 52 мл метиленхлорида и 125 м метанола К раствору при интенсивном перемешивании добавляют 2,75 г (0,0б9 моль) порошковой гидроокиси натрия, .затем при 15-20 0 12,5 г (0,33 моль) боргидрида натрия Сра зу начинается выпадение продукта. Содержащий кристаллы раствор перемешивают в течение 5 м, затем проду отфильтровывают и промывают его водой« Маточный раствор упаривают при пониженном- давлении при темпера туре ниже , остаток растирают с водой„ После фильтрования оставшу юся на фильтре вторую фракцию проду та промывают водой. Обе фракции соединяют, сушат в вакууме при 50°С и кристаллизуют из ацетона. Получаю 20,2 г (88,0) 2 Vxлop-ЗQ, 17р-диок си-1б|3-пиперидин-5с -андростана с т.пл. 232-23 4 с. С 70,о; и э,9; о 8, Найдено, AW С 70,3, Н 9,7, С1 8 Вычислено, П р и м е р 5. 2р|-иперидин 1бри- (1 -метилпиперазин)-М, 17 Диокси-5.с гандростан„ 1i|,8 г (0,038 моль) Ы, Зо(гэпокси-1 7р -окси-1бр (N -метилпиперазин) 5 зС-андростана растворяют в смеси 168 мл (1,б5 моль)пиперидина и 2А мл воды. Раствор нагревают при я автоклаве в течение 72 ч затем упаривают при пониженном давлении. Остаток после упаривания экстрагируют ацетонитрилом и отфильтровывают Твердое вещество, суспендированное в ацетонитриле, нагревают с обратным холодильником Затем кристаллический продукт отфильтровывают и сушат. Получают 12, Г:(69,0) 2 -пиперидин-1б| - (Н-метилпиперазин)-ЗсА 1 7 3-диокси-5 --андростана с т„пл. . (oL)| +81 ,5 (, хлороформ). Найдено, |: С 70,8; Н 10,97, N 9,10 .0-Вычислено, I: С 71,0; Н 10,80; N 9,26 П р и м е р 6о 2)-(М-метилпиперазин)Нб(пиперидин-Зс1, 17 |Ъ-диокси-5о6-андростан„Это соединение получают по описанной в примере 5 методике из 2pr tnop-. 3fl, 1 7р-диокси-1б Ь-пиперидин-5оС андростана и N-метилпиперазина с выходом 671 Т.пл, 230-23t°Co (cL) +81,7° (, хлороформ), С 70,8, Н 10,70: Найдено, 9,05 A.jOa : С 71,0, Н 10,80, ычисленО; 2 Пиперидин- I6fiи м е р 7. -(N-метилпиперазин) - 3d, 1 7| |-диацвтокси - 5ci.-ан дрост ан , 3 г (0,ООбЗ моль) .-пиперидин-1брг- (N-метилпиперазин)-3с1, 1 7/5-диокси-|хэЬандростана растворяют в смеси 13 мл уксусного ангидрида и 1 мл уксусной кислоты и к раствору добавляют 0,3 г хлористого цинка Реакционную смесь перемешивают в течение 12 ч, затем избыток уксусного ангидрида разлагают добавлением-.0 мл воды. Раствор охлаждают до и при этой температуре добавляют водный раствор едкого натра до -рН 9-10о Хлопьеобразный осадок сразу экстрагируют эфиром,. Эфирный экстракт промывают насыщенным раствором поваренной соли до нейтральной реакции. После разделения С-аз органическую фазу сушат сульфатом натрия, фильтруют, фильтрат делают прозрачным с помощью 3 г силикагеля, снова фильтруют и упаривают досуха. Из 9 полученнсго остатка продукт кристал лизуют растиранием с гексаном, отфильтровывают и сушат. Получают 2,6 (73,3) 2| -пиперидин- 1бр1- (N-метилпи раэин)-3()/, 17р-диацетокси-5 -андростана с ТаПЛ. 95-98 С. Ы.} +33,9° ( хлороформ) Найдено, %: С 71 ,01 , Н 8,87, N 7,36 (hUA04 Вычислено, %: С 71,20, Н 9,0, N 7,: П р и м е р 8. 2р {N-Метилпипера зин- 161 -пиперидин-За, 17с6-Диацетокси iAPQCTaH, Эт J соединение получают по методике примера 7 ацилированием 2|i-(N-метил пиперазин) 1б| -пиперидин-3с(,, 17/ -диокси 5фандростана, Выход 72, W) +29,4 ( , хлороформ). о- Найдено, %: С 70,9, Н 8,8; N 7,3 Вычислено, %: С 71 ,20, N9,00, N7, П р и м е р 9о Дибромид 2j3-(N-метилпиперидиний) 46|V (4, -диметил перазиний -3(/, 17р-диацетокси-5о г -андростана. 1- г (0,0018 моль) 2р -пиперидин -1бр-(Ы-мётилпиперазин)-Зс, 1 -диацетокси-5о.-андростана растворяют в 20 мл ацетона К раствору добавляют 10 мл 5 -ного ацетонового раствора метилбромида Реакционную смесь выдерживают при комнатной температуре в течение 48 ч„ Выпаривают четверти ную соль, отфильтровывают, pacтиpaю сначала с ацетоном, затем с эфиром и отфильтровывают. Отфильтрованный осадок кипятят с обратным холодильНИКОМ в ацетоне, затем раствор, содержащий кристаллы охлаждают до ком натной температуры, продукт отфильтровывают и сушат. Получает 1,2 г (87,2) дибромида 2fi)-(Ы-метилпиперид ний) (4,-диметилпиперазиний)-3oL, 1 71Ь-диааетокси-5о1-андростана с т.пло 260-26 С (разл,) Найдено, %: С 5,81; Н 8,10; Вг 20,51, N 5,0 N3Br04HiO UI числен о, %: С 55,0, Н 8,2V Вг 20,90, N 5,500 Пример 10, Дибромид 2pi-{i(,i| -диметилпиперазиний) - ТбрЬг-ДМ-метил.пи перидиний)-3о/, 17&-Диацетокси-5с(ганд ростана, 1,3 г (2,3 моль) (N-мeтилпиnepaзин)- 1бр-пиперидин-3о(., 7р)-ди5910ацетокси-5а(;-андростана растворяют в смеси 10 мл ацетона и 20 мл ацетонитрила и к раствору добавляют 32 мл 8,4%-ного раствора метилбромида (28 ммоль). Реакционную смесь выдерживают при комнатной температуре в течение 9 ч, затем выделяют четвертичную соль, по методике, описанной в примере 9. Получают г (78,5) дибромида 4,4-димeтилпипepaзин й . (М-метилпиперидиний)-Зо1, 17/ -диацетокси-5а -аидростаиа с.т.п.1, 2 +8252С (разл,) (d.),3(, этанол), Найдено. %i С 5,75, Н,7,9б; N 5,2; В г 20,6 Вычислено,: С 55,00; Н 8,24; N 5,5, В г 20,9 Пример 11, 2г (3,6 моль) 2/V - (N-метилпиперазин) 16 Упиперидин-30(.17р -диацетокси-5ойандростана растворяют в 20 мл ацетона и к раствору добавляют 12 мл 8,4%-ного ацетонового раствора и метилбромида С. 10,6 моль), Реакционную смесь выдерживают при комнатной температуре в течение 1б ч, затем отфильтровывают выпавшую четвертичную соль, промывают ее сначала ацетоном, потом эфиром, экстрагируют ацетоном, отфильтровывают и сушат. Получают 1,5 г (62,5) бромида 2JJ-(4 -диметилпиперазиний)-1бр-пиперидин -Зо, 17fЬ-диaцeтoкcи-5cli-aндpocтaнa с т,пл., 234-231 С (разл,). (о)+12,8 (, хлороформ) Найдено,: С 61,1; Н 8,9, N 5,9; Вг 11,3 . (L,hLBrN,,0/H,0 Счислено; %: С 61,4, Н 8.7,N6,Г Вг 11,7 Соединения общей формулы 1 оказывают курареподобное, недеполяризирующее нейро-мышечное блокирующее действие, т.е они ингибируют прохождение нервных раздражителей в мышцах. Эти соединения не освобождают гистамин, не снижают кровяное давление, не влияют на гормоны, их действие можно нейтрализовать действием неости гмина Для определения силы действия и длительности проводят испытания с искусственным дыханием на получивших наркоз кошках, Перонезный нерв раздражают электричеством и регистрируют вызванное взаимное притяжение тибиальных мышц. С помощью внутривен11 J ного введения блокирующих веществ в разных дозах определяют дозу полного связывания взаимного притяжения мышц (ЕДурд). Определяют время между началом действия и полным прекращением нормальной реакции мышц. Приведенные в таблице данные относятся к дозам полного подавления„ В качестве сравнительного соединения применяют панкуронийбромид. 2р- ,-Диметилпиперазиний - (N-мeтилпипepидиний),-ЗQ, 17р-диацетокси-Зо -андростана дибромид (N-Метилпиперидиний )- 16р-(4,4-диметил пиперази НИИ) 7|Ь-диацетокси-5о1 -андростанадибромидПанкуронийбромид Из таблицы видно, что пре емые соединения в дозах 2,меньших действуют так же, ка куронийбромид, а длительност ствия при этом всего лишь на меньше. Формула изобретения Способ получения 2р, 1бр андростановых производных об мулы 1 п и А имеют следу где чения: -, то R,NS если R NS, R.CH,-N или Rj- CHj/ если R. CH.j-N или Rj -- jj R, или Ry-N, g -сн/2., причем, СН,/ то R4 если -М,: то R. Rc Cf -4 ,1,2, А - анион одноосновной кислоты, или их солей отличающийс я тем, что соединение общей формулы П to ,f --: ЧхКх где X - бром или иод, обрабатывают соединением общей формулы III иО где R(,CK,j-N или -СН,-, к полученному соединению при необходимости добавляют галоидводородную кислоту, такую как соляная, полученный промежуточный продукт восстанавливают боргидридом щелочного металла, таким как боргидрид натрия, полученное соединение общей формулы IV где R имеет указанное значение, y/f--галоид, например хлора, оксигруппа, и УО образуют эпокси группу, вводят во взаимодействие с соединением формулы 1, в котором R имеет значение, противоположное значению R в соединении формулы IV, ацетилируют, например, уксусным ангидридом и выделяют целевой продукт в свободном виде или в виде соли или, при необходимости обрабатывают соединением общей формулы У Rg-Br, где R (Г- ал ки л , и выделяют целевой продукт в виде соли.
131001859I
Источники информации,2. Бюлер К, Пирсон Д, Органичеспринятые во внимание при экспертизекие синтезы, ч. К Мир, 1973, с.
1, Машковский М,Д. Лекарственныес.529.
средства, ч. 1, М., Медицина, 1972, с. .3. Там же, с. 222.





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных триаминоандростана,их солей или четвертичных аммониевых солей | 1976 |
|
SU967276A3 |
| Способ получения производных биспиперазиноандростана | 1973 |
|
SU582768A3 |
| Способ получения производных 3-амино-17а-аза- -гомо-5 - андростана или их солей, или их четвертичных солей | 1978 |
|
SU722487A3 |
| Способ получения 5 ,17 -диацетокси6 -хлор-2 ,3 ,16 ,17 диэпоксиандростана | 1976 |
|
SU612635A3 |
| Способ получения эпоксиандростанов | 1976 |
|
SU634675A3 |
| Способ получения 17 @ -алкилстероидов | 1980 |
|
SU973025A3 |
| СССРОпубликовано 28.XI 1.1972. Бюллетень N° 5за 1973Дата опубликования описания 30.VIII.1973УДК 547.6iS9.6.07(C.S8.8) | 1973 |
|
SU365067A1 |
| Способ получения 3- кетоандростенов | 1982 |
|
SU1189353A3 |
| Способ получения 2-замещенных 5-сульфамоилбензойных кислот | 1972 |
|
SU484686A3 |
| Способ получения производных прегнана | 1972 |
|
SU514573A3 |


Авторы
Даты
1983-02-28—Публикация
1976-07-30—Подача