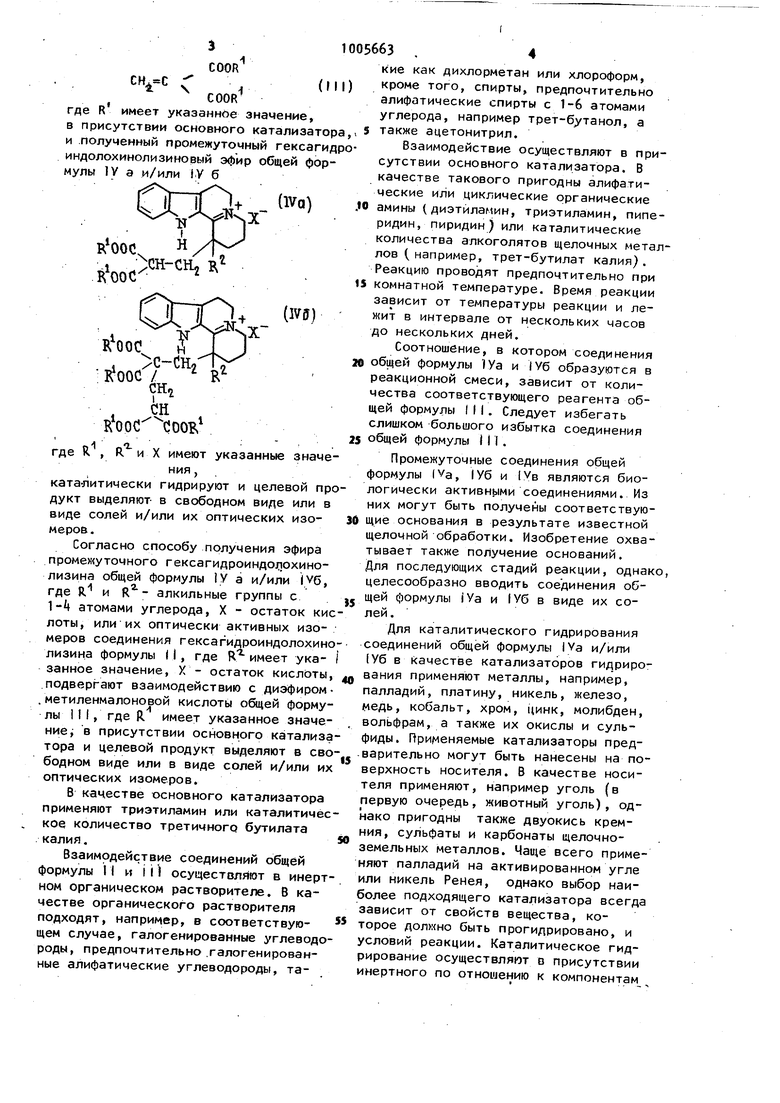
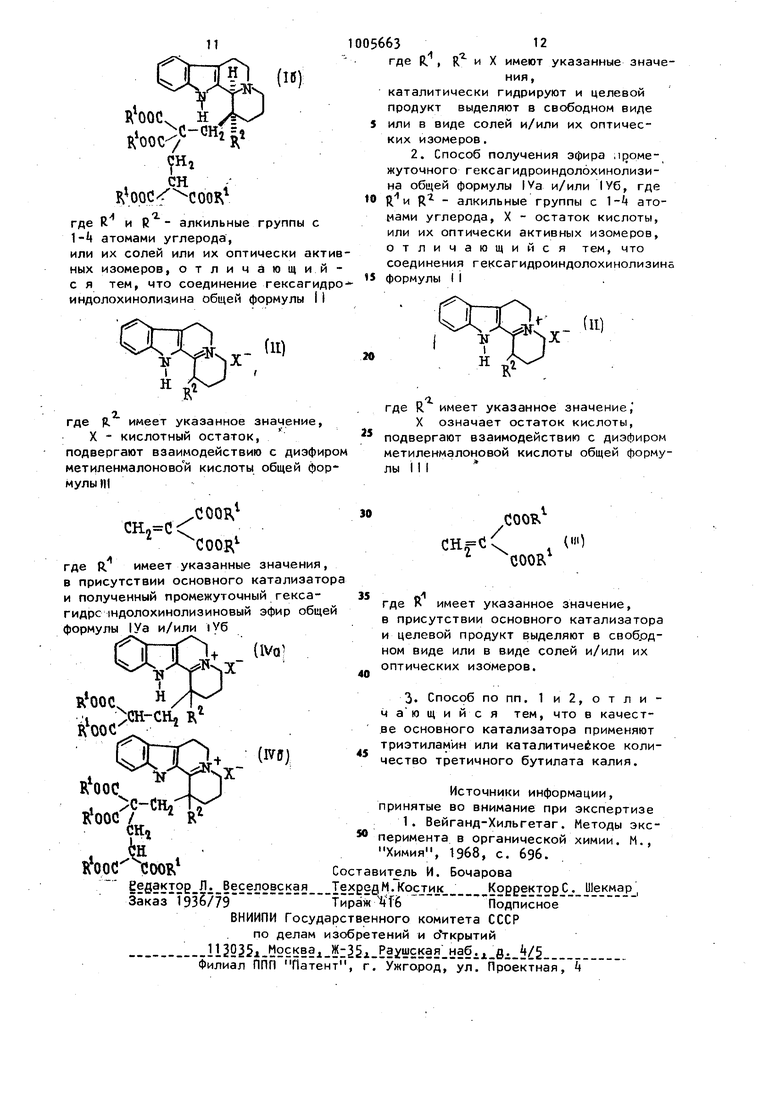
1 (Ml где R имеет указанное значение, в присутствии основного катализатора и полученный промежуточный гексагидр индолохинолизиновый эфир общей формулы IV а и/или IV б .U..H-Cll2 К . In leooc /. R . й , где R , R и X имеют указанные значения, ката 1итически гидрируют и целевой про дукт выделяют в свободном виде или в виде солей и/или их оптических изомеров. Согласно способу получения эфира промех уточного гeкcaгидpoиндoJ;1Oxинoлизина общей формулы 1У а и/или 1.6, где R и R - алкильные группы с l-t атомами углерода, X - остаток кис лоты, или их оптически активных изомеров соединения гексагидроиндолохино лизина формулы (I, где R имеет указанное значение, X - остаток кислоты подвергают взаимодействию с диэфиром метиленмалоновой кислоты общей формулы III, где R имеет указанное значение j в присутствии осйовного катализа тора и целевой продукт выделяют в сво бодном виде или в виде солей и/или их оптических изомеров. В качестве основного катализатора применяют триэтиламин или каталитичес кое количество третичного бутилата калия. Взаимодействие соединений общей формулы II и ii) осуществляют в инерт ном органическом растворителе. В качестве органического растворителя подходят, например, в соответствующем случае, галогенированные углеводо роды, предпочтительно .галогенированные алифатические углеводорюды, та63кие как дихлорметан или хлороформ, кроме того, спирты, предпочтительно алифатические спирты с 1-6 атомами углерода, например трет-бутанол, а также ацетонитрил. Взаимодействие осуществляют в присутствии основного катализатора. В качестве такового пригодны алифатические или циклические органические амины (диэтйламин, триэтиламин, пиперидин, пиридин) или каталитические количества алкоголятов щелочных металлов (например, трет-бутилат калия). Реакцию проводят предпочтительно при комнатной температуре. Время реакции зависит от температуры реакции и лежит в интервале от нескольких часов до нескольких дней. Соотношение, в котором соединения общей формулы 1Уа и IV6 образуются в реакционной смеси, зависит от количества соответствующего реагента общей формулы III. Следует избегать слишком большого избытка соединения общей формулы III. Промежуточные соединения общей формулы (Va, 1Уб и 1Ув являются биологически активными соединениями. Из них могут быть получены соответствующие основания в результате известной щелочной обработки. Изобретение охватывает также получение оснований. Для последующих стадий реакции, однако, целесообразно вводить соединения общей формулы 1Уа и 1Уб в виде их соДля каталитического гидрирования соединений общей формулы 1Уа и/или 1Уб в качестве катализаторов гидрироаания применяют металлы, например, палладий, платину, никель, железо, медь, кобальт, хром, цинк, молибден, вольфрам, а также их окислы и сульфиды. Применяемые катализаторы предварительно могут быть нанесены на поверхность носителя. В качестве носителя применяют, например уголь (в первую очередь, животный уголь), однако пригодны также двуокись кремния, сульфаты и карбонаты щелочноземельных металлов. Чаще всего применяют палладий на активированном угле или никель Ренея, однако выбор наиболее подходящего катализатора всегда зависит от свойств вещества, которое быть прогидрировано, и условий реакции. Каталитическое гидрирование осуществляют в присутствии инертного по отношению к компонентам 100 реакции растворителя, который хорошо растворяет вещество, подлежащее гидрированию. В качестве растворителя пригодны, например, вода, алифатические спирты с 1-6i атомами углерода, галогенированнме алифатические углеводороды с 1-6 атомами углерода, этил ацетат, диоксан, яедяИая уксусная кислота или сиесь указанных растворителей. При применении в качестве ката лизатора окиси платины работают предпочтительно в нейтральной или слабо кислой среде. Если применяют никель Ренея, то целесообразно, чтобы реакционная среда была нейтральной. Температура и давление каталитического гидрирования зависят от исходных -соединений, так же, как и время реакции. Предпочтительно гидрировать при комнатной температуре при атмос-. ферном давлении до поглощения стехиометрического количества водорода. Если гидрируют чистое соединение общей формулы 1Уа или соединение общей формулы 1Уб (т.е. не смесь обоих то получается соответствующее соеди нение общей формулы 1а или 16. Если же исходные соединения IVa и 1Уб находятся в смеси, то при гидрировании получают смесь соответствующих соединений общей формулы I а и I в. .-. ..... .. 1- .. , Пример 1Л) -1о6-Этил-1 -(2(2 -диэтоксикарбонил-этил)-1,2,3, ,6,7,12,12bo -октагидроиндоло(2,3-а хинолинин и (,г)-1о -этил-1| -(2,2, 4 ,4 -тетраэтоксикарбонил-бутил)1,2,3,,6,7,1 2,121)о1-октагидроиндоло(2,3 а хинолизин. Суспензию из 10,00 г (28,4 ммоль 1-ЭТИЛ-1 ,2,3,,6,7-гексагидро-12Н-индоло(2,3-а) хинолизин-5-иум-перхлората в 60 мл дихлорметана и 3,6 мл (2,60 г; 25,7 ммоль) триэтиламина при перемешивании смешивают с раствором 8,0 мл (8,.г; 48,8 ммоль) диэтилового эфира метиленмалоновой кислоты в 10 мл дихлорметана. Реакционную смесь выдерживают при комнатной температуре в течение 2 дней. Растворитель отгоняют в, вакууме и оставшееся после испарения окрашенное в оранжевый цвет масло трижды растирают с 30 мл эфира и трижды с 30 мл .петролейного эфира. Таким образом, получают в виде мае ла смесь из 1-этил-1-(2,2 -диэтоксикарбонил-этил)-1,2,3,4,Г1,7-гоксагидро -12Н-индоло(2,3-а)-хинолиг.ин-5-иум31-ЭТИЛ-1-2 {2/ 21 перхлората и -тетраэтоксикарбонил-бутил)-1,2,3 ,6,7-гексагидро-12Н-индоло(2,3-а ) хинолизин-5 иум-перхлората, которую без очистки можно применять в последующих стадиях реакции. ИК-спектр (в 32бО (индол-NH). 1735, 1715 (СО), 1615, 1520 (С-М) смЧ 18 г маслянистой смеси растворяют в смеси, состоящей из 200 мл этанола и 50 мл дихлорметана, и гидрируют в присутствии 8 г предварительно прогидрированного 10%-ного палладия . на угле в качестве катализатора. После поглощения теоретического количества водорода катализатор отфильтровывают и промывают сначала трижды этанолом порциями по 3 мл, затем трижды дихлорметаном порциями по 30 мл. Фильтрат соединяют с промывной жидкостью и испаряют в вакууме досуха. . Остаток после испарения кристаллизуют из 50 мл этанола. Продукт промывают этанолом и затем высушивают. Та«им образом .получают 9,0 r(±)-l4t-этил-1р -(2,2 ,it ,-тeтpaэтoкcикapбoнил-бyтил)-1,2,3,,6,7,12,12bti-6ктaгидpoиндoлo-( 2,3-а)хинолизин-перхлората, что соответствует выходу 45,3, считая на 1-этил-1,2,3,t,6,7-гексагидро-12Н-индоло-{2,3-а)хинолизин-5-иум-перхлорат. Т.пл. 21б-218 С (этанол).. Рассчитано, %: С 56,68; Н 6,63; ,01. СззН4бНрв (Мол.вес.699,18Х Найдено, %: С 57,00; Н 6,55; 1,10. Гидрохлорид соединения п плавится 211-212°С (этанол). при Масс-спектр (т/е, %): 426 (м -172; 6), 425 (3)ЛО,3) 397 (0,3), 381 (2), 353 (1), 267 (100), 253 (3), 197 (8), 185 (6), 184 )6), 170 (10), 169 (10), 156 (6), 144 (5), 127 (10), 99 (10). (±)-1а -этил-1{Ь-С2,2,4,4-тетраэтоксикарбонил-бутил -1 ,2,3,4,6,7,12. 12в оСоктагидроиндоло(2,)-хинолиновое основание получают растворением перхлората или гидрохлорида в дихлорметане при встряхивании с раствором карбоната натрия, органическую -фазу отделяют, высушивают над твердым сульфатом магния и испаряют в вакууме.. Н-ПМР (CDC,f): 7,86 (1Н, индол-|4Н) , 4,30-3,85 ( ПН, т, О-СИ), 1,45-1,0 (15Him, ). 71С Из этанольного маточника (,-) - d-этил-1/5-{2,2 ,, -тетраэтоксикарбонил-бутил)-1 ,2 ,3 ,,7,12,12в-октагидроиндоло() хинолизин-перхлората отгоняют этилооый спирт. Остаток после отгонки растворяют в 30 мл дихлорметана. Раствор встряхивают с 20 мл водного раствора карбоната натри а, органическую фазу отделяют, высушивают над твердым сульфатом магния и затем испаряют в вакууме. Ос таток растворяют в 10 мл этилового спирта, раствор подкисляют этанольным раствором соляной кислоты до рН S, и затем осаждают гидрохлорид добавлением 10 мл эфира. Продукт отфильтровы вают $ промывают эфиром и затем высу- шивают. i-i Получают 4 г (±)1с/-этил-1 р (2 ,2 -диэтоксикарбонил-этил)-7,2,314,6,7, 12,12всз -октагидроиндоло(2,3-а)хиноли зин-гйдрохлорида, что соответствует выходу 30,4, считая на 1-этил-1,2, 3,4,6,7-гексагидро-12Н индоло(2,3-а) хинолизин-5-иум-перхлорат. Т.пл. 202204°С (эфир). ИК-спектр (КВг): 330Q (индол-NH), 1720 (СО) см-. Масс-спектр (т/е, ) : 426 (М, 15), 425 (12), 411 (1), 397 (1), 381 (8), 365 (0,5), 363 (2), 307 (0,6), 267 (100), 253 (2), 237 (4), 197 (12) 185 (8), 184 (7), 170 (10), 169 (12), 156 (5), 145 (0,6), 144 (5), 14з (3), 127 (1), 124 (3). ( -1с -Этил-1|Ь-(2 ,2 -диэтоксикарбонил-этил)-1 ,2,3,4,6,7,12,12во. -окта гидрриндоло (2,3-а)хинолиновое основание получают растворением гидрохлорида в дихлорметане, раствор встряхивают с водным раствором карбонага натрия, органическую фазу отделя ют, высушивают над твердым сульфатом магния, фильтруют и затем испаряют досуха. -«И-ПИР (CDCE:j, (Г): 7,82 (1Н, индолН И),7,2-6,85 (4Н, т, аром.), 3,90 (4Н, q, j 7,3 cp.S , 0-CH,j.), 1,20,S (9Н,Я1, СН,,). Полученное описанным способом 1)1о1-этил-1|Ь-(2 ,2 -диэтоксикарбонил-этил)-1,2,3,4,6,7,12,12в ci-октагидроиндоло (2,3-а)хинолизиновое основание обрабатывают тонкослойной хроматографией (К 60, -366-254, бензол: метанол - 14:3, элюируют ацетоном ). После элюирования и испарения элюирующей жидкости остаток после ис6638парения перекристаллизовывают из эта.пола. Продукт с большим значением рефракции R является С -1о -этип,-1(г(2 ,2 гдиэтоксикарбонил-этил/-1,2,3,,7,12,12в о -октагидро-индоло (2,) хинолизином. Выход: 0,Г.5 г, т.е. 2%, на 1-ЭТИЛ-1 ,2,, 6,7 гекеагидро-1 2Н-индоло( 2, jfxинoлизин-5 иyм-пepхлорат. Т.пл. Т27-128 С (этанол). ИК-спектр UBh): 3280 (индол-NH), 1730, 1705 (СО) ctr . . (м 18) Масс-спектр (т/е, %}: 426 7,1, ill (0,8), 397 (0,8), 381,) (4,2), 366 (0,9), 353 (1,8),, 337 (0,8), 355 (0,5), 307 (0,6), 2б7 (100). р 2.()-1о/-Этил-1р--(2 . П р и м, е 2 -диэтоксикарбонил-этиЛ)-1 ,2,3 ,4, 6,7,12,12оо/.-октагидро-индоло(2,3-а } хинолизин и(±)-1о(.-этил-1р)(2,2 ,4, 4. тетраэтоксикарбонил-бутил)-1 ,2,3, 4,6,7,12,}2eoi-октагидроиндоло(2,3-а) хинолизин. 5,00 г (14,2 моль) 1-ЭТИЛ-1,2,3, 4,6,7-гексаридро-12Н-индоло(2,3-а) хинолизин-иум-перхлората суспензируют в смеси, состоящсгй из 30 мл дихлорметана и 0,080 г/0,715 ммоль) трет-бутилата калия. К суспензии при перемешивании добавляют раствор 0,03 мл (3,12 г; 18,4 ммоль) диэтилового эфира метиленмалоновой кислоты в 5 мл дихлорметана. Реакционную смесь выдерживают при комнатной температуре в течение одного дня. Затем растворитель отгоняют в .вакууме и оставшееся после-испарения ; органическое масло растирают трижды с 5 мл петролейного эфира. Получают 9 г смеси, состоящей из 1-этил-1-(2 , (. / 2 -диэтоксикарбонил-этил)-1,2,3,4,6, 7-гексагидро-12Н-индоло-(2,3-а -хинолизин-5-иум-перхлората и.;1-этил-14.,2 ,2 ,4 ,4 -тетраэтоксикарбонилбутил)-1,2,3,4,6,7-гексагидро-12Ниндоло(2,3-а)хинолизин-5-иум-перхлората в виде масла. Ее без дополнительной очистки можно применять в последующей стадии реакции. ИК-спектр (КВг): 32бО (индол-МН),. 735, 17Т5 (СО, 1615, 1520 (C-N) см. 9 г полученного масла растворяют в смеси из 10 г этанола и 25 мл дихлорметана и гидрируют в присутствии 6 г предварительно прогидрированного 10 -ного палладия на угле. 100 После поглощения желаемого количества водорода катализатор отфильтровывают из раствора и промывают сначала трижды этанолом порциями по 3 мл; затем трижды дихлорметаном порциями по-10 мл. Фильтрат объединяют с промывной жидкостью, испаряют в вакууме досуха и остаток после испарения кристаллизуют из 30 мл этанола. Продукт отфильтровывают, промывают этанолом и затем высушивают. Таким образом получают, смесь 8 г (± -1 ог-этил-1fV( 2 , 2 , it,6-тетраэтоксикарбонил-бутил}- ,2,3,,6,7,12, 12в (-октагидроиндоло(2,3-а)хиноли7 зин-перхлората и (±)-1(-этил-1р -(2 , 2-диэтоксикарбонил-этил)-1,2,3,,6, 7,12,12во октагидроиндоло(2,3-а) хинолизин-перхлората, которая плавится при 181-185 С. Смесь солей без выделения, и разделения можно применять в последующей стадии реакции в виде раствора, полученного после отфильтровывания катализаторал. Чтобы установить состав смеси перхлоратов, 0,8 г смеси растворяют в 6 мл дихлорметана и встряхивают раствор с мл 5 -ного водного раствора карбоната натрия. Органическую фазу отделяют, высушивают над твердым.суль фатом магния, отфильтровывают и фильт рЗт испаряют в вакууме досуха. Остаток после испарения разделяют с помощью тонкослойной хроматографии (окись алюминия типа Т, текущая жидкость дихлорметан и бензол в соотношении 20:.-1, элюирующая х идкость - дихлорметан и метэнол 20:1) на составные части. Соединение с большим значением рефракции Я{ растворяют в 1,2 мл этилового спирта и раствор подкисляют спиртовым раствором (этанольным) соля ной кислоты до рН 5. Гидрохлорид осаж дают добавлением 1,2 мл эфира, отфиль ровывают, промывают эфиром и затем высушивают. Получают 0,16 г(±)- iL-этил-1 Р- (2, 2 -диэтоксикарбонилэтил )-1 ,2,3,4,6,7,12,1 2в -c.-oктaгидpdиндoло(2,3-а)хинолизин гидрохлорида, кото рый плавится при 302-20 С (этиловь1Й спирт, .эфир). Выход 70,5%. Из соединения с меньшим значением рефракцииR получают с 70%-ной водной перхлорной кислотой перхлорат и затем перекристаллизовывают из этанола. Получают 0,26 г (26%)(±)-U-этил-1|У(2 ,2 ,V ,+ -тетраэтоксикар10бонил-бутил )-1,2,3,t,6,7,12,12в J.-oKTaгидроиндоло(2 ,3-а)хинолизин-перхлора- . та, который плавится при 216-218 С (этиловый спирт). Пример 3.(.-Ь1-Этил-1р; -12, 2 ,-диэтоксикарбонил-этил)-1 ,2,3,, 6,7,12,12во1октагидроиндоло (2,3-а)хинолизин. 600 мл (1 ммоль) полученного аналогично примерам 1 и 2 (-t) -W-этил-1p)-(2 ,2 , ,4 -тетраэтоксикарбонилбутиг.)- ,2 ,3 , ,6,7 ,12,1 :.в ot-октагидроиндоло ( 2,3-а) хинолизина растворяют в В мл этанола. К раствору добавляют раствор 120 мл гидроокиси калия в смеси, состоящей из 1 мл воды и 1 мл этанола. Реакцию проводят с помощью тонкослойной хроматографии (окись алюминия типа Т, текущая жидкость дихлорметан и бензол 3. 1, R{ значение диэтоксикарбонилэтильного производного больше, чем утетраэтоксикарбонилбутильного производного) и осуществляют ее в течение 20 мин. Реакционную смесь подкисляют уксусной кислотой до значения рН 6 м и. отгоняют растворитель в вакууме. Остаток после испарения растворяют в 8 мл воды, раствор подщелачивают вод ным раствором соды до значения рН 9 и затем трижды экстрагируют 5мл дихлорметана . Органические фазы объединяют, высушивают над безводным сульфатом магния, отфильтровывают и растворитель отгоняют в вакууме. Полуценное в качестве остатка после испарения масло растворяют в 3 мл этанола и раствор смешивают с солянокислым этанолом. Полученный гидрохлорид осаждаЮт эфиром. Получают 0,25 г (53) (±)-Ы-этил-1| -(2 ,2 -диэтоксикарбонилэтил}-1,2,,7,12,12вс -октагидроиндоло- (2,За) хинолизин-гидрохлорида, который плавится при 201-204 С. ИК-спектр (КВг): 3300 {индол-NH), 1720 (СО) Формула изобретения 1. Способ получения эфира октагидроиндолохинолизина общей формулы 1а и/или 16





Авторы
Даты
1983-03-15—Публикация
1981-04-16—Подача