Далее полученный рацемат цис- или транс-октагидронвдол 2,3-аДхинолизи- на формулы II при необходимости разделяют на оптически активные изомеры с использованием D-винной кислоты или подвергают щелочному гидролизу до соответствующей кислоты. Последнюю эте- рифицируют в -алкиловьш эфир. В другом случае оптически активные . ; производные формул II а-г или указан - ные переэтерифицированные производные обрабатывают сначала трет-бутилнитрилом в растворе ароматического угле- водорода (толуола) с добавлением, если необходимо, катализатора - диме- тилформамида при , а затем спиртом: R-OH, где R - С,. - алкил, при 20-60 С с вьщелением целевого продукта формул II или Иа-г, в которых К - R-0-C(0)C(N-OH) R,Y имеют указанные значения,в свободном виде или виде гидрохлоридов .Способ обеспечивает хорощий выход (до 80%) целевых продуктов из доступных реагентов.





Изобретение касается замещенных индолС2,3-а хинолизина, в частности транс-гидроксииминооктагидроин- ,3-а хинолизина или соответствующих оптически активных производных или их гидрохлоридов, которые являются промежуточными продуктами для получения рацематов сложных эфиров цис- или транс-ановинкаминовой кислоты. Цель - создание новых промежуточных веществ указанного класса для синтеза ценных фармакологических веществ. Синтез соединений ведут из соедине- НИИ формул AW /v.x® --U (IJj где K CHi-0-C C -HjC-c Hzi У СгНу, X бензоилтартрат клипер- хлорат, которые либо гидрируют на 10%-ным Pd/C при 20-60 С и атмосферном давлении с получением промежуточных соединений общих формул (II) (рацемическое цис-производное) , (На) или (116) (цис-производные), либо восстанавливают боргидридом натрия с выделением промежуточных соединений общих формул (II) (рацемическое транс-производное), (Ив) и.пи (Иг) (транс-производные): i W NH Н N ©rtD к т у (П) Г ...f --t7i .-л IIII Л / -..- . . ..I S у Со 05 о 4: Kj Ы у,/. (}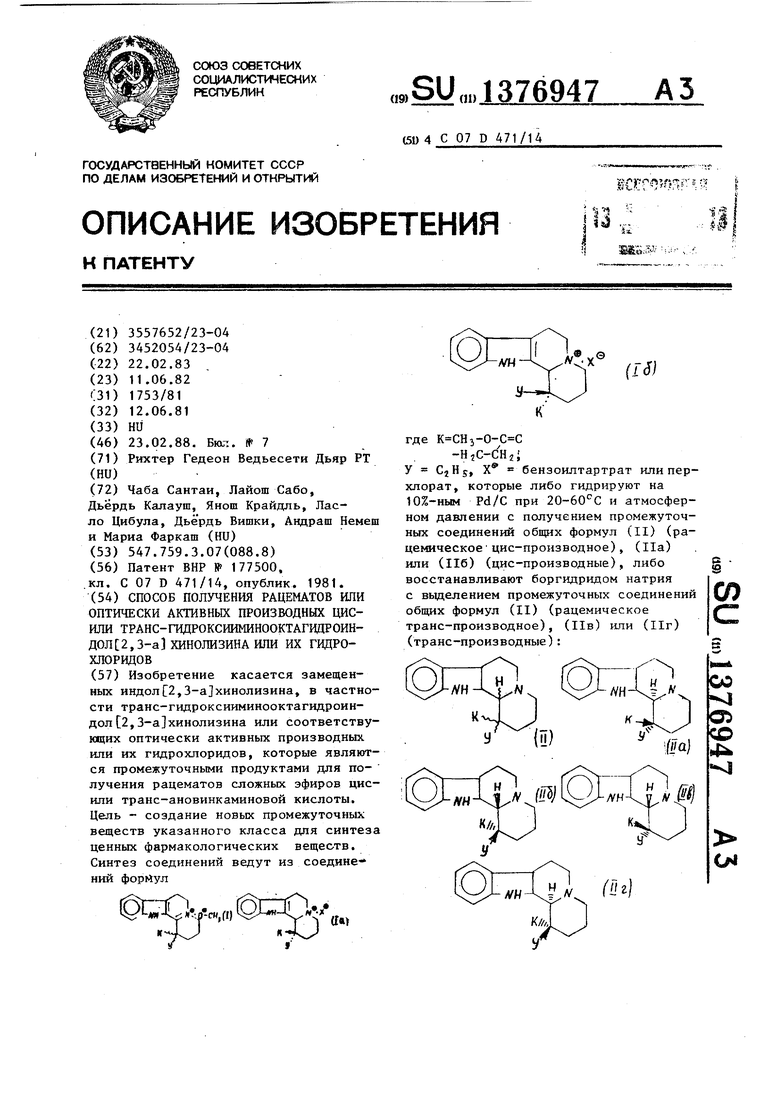

1
Изобретение относится к органической химии биологически активных сое- динений, а именно к способу получения рацематов производных цис- или транс-гидроксииминооктагидроиндол 2, 3-а хинолизина общей,формулы
ROOCCCHo г U
11
N-OH
R - Ci-G -алкил, соответствующих оптически активпроизводных общих.формул
О
И
ROOCCCH, N-OH (16)
-N-OH (IB)
N-OH
(Ir)
где R - С -C -алкил, или их гидрохлоридов.
Эти соединения являются промежуточными при получении рацематов сложных эфиров цис- или транс-ановинка- миновой кислоты.
Целью изобретения является синтез новых соединений, являющихся промежу0
5
0
5
0
5
точными продуктами в синтезе ценных фармакологических веществ.
Пример 1. Разделение 1-(2-ме- токсикарбонилэтил)-1-этил-1,2,3,4,6, 7-гексагидро-12Н-индол 2,3-а хиноли- зинметанолята.
100,0 г (0,2699 моль) 1-(2-меток- сикарбонилзтил)-1-этил-1,2,3,4,6,7- -гексагидро-12Н-индол 2,3 1хиноли- зинметанолята растворяют в 200,0 мл дихлорметана при комнатной температуре, после чего добавляют к смеси при перемешивании раствор 100,0 г дибензоил-с/-винной кислоты (моногидрат) (0,2673 моль) в 400,0 мл дихлорметана. Смесь перемешивают при комнатной температуре в течение 1 ч, отфильтровывают выпавшие в осадок продукты, промывают их дихлорметаном и сушат.
Таким способом получают 91,84 г (0,1322 моль) 1/}-(2-мeтoкcикapбoнил- этил)-1c/-зтил-1 ,2,3,4,6,7-гексагид- ро-12Н-ИНДОЛ Г2,3-а хинолизиндибензо- илтартрата. Выход 98,0% (из расчета на о/-этильную форму), of / -68,6° (, в диметилформамиде). Содержание основания 48,49% (по теории 48,73%). Т.пл. 139,5-140°С.
Из полученной соли освобождают основание, которое затем переводят в метанолят и перхлорат, имеющие следующие свойства: 1 |3-(2-мeтoкcикapбo- ншIэтил)-1ol -этил-1 ,2,3,4,6,7-гекса- гидро-12Н-ИНДОЛГ2,3-а хинолизинмета- нолят - Т.пл. 151-152 С, о п° -27,6° (С 1, диметилформамид)J 1/1-(2-метоксикарбонилэтил)-1 ,2,3,4,6,7-гексагидро-12Н-индол-Г 2, 3-а хинолизинперхлорат - т.пл. 178- , o/ll -23,5 С (С 1, диме- илформамид).с
Из маточной жидкости, остающейся в результате разделения, можно ввде- ить соответствуюпще соли /5-этш1анти- ода (после освобождения основания).
П р и м е р 2. Разделение 1-(2-ме-1о токсикарбонилэтил)-1-этил-1,2,3,4,6, 7-гексагидро-12Н-индол 2,3-а хиноли- зинметанолята.
100,0 г (6,2699 моль) 1-(2-меток- сикарбонилэтил)-1-этил-1,2,3,4,6,7- |5 -гексагидро-12Н-индол 2,3-а хиноли- зинметанолята растворяют в 200,0 мл ихлорметана при комнатной температуре, после чего добавляют в полученный раствор 100,0 г (0,2673 моль) ди-20 бензоил-/1-винной кислоты в 400,0 мл ихлорметана. После перемешивания при комнатной температуре в течение 1 ч реакционную смесь отфильтровывают, промывают дихлорметаном и сушат. 25
Таким способом получают 91,7 г (0,1320 моль).
Ы-(2-метоксикарбонилэтил) этил-1,2,3,4,6,7-гексагидро-12Н-ин- ,3-а хинолизиндибензоилтартрата. о Выход 97,8% (из расчета на ft, -этиль- ное производное), +68,8° (С 1, диметилформамид). Содержание основания 48,5% (по теории 48,73%), т.пл. 139-140°С.
Из полученного неочищенного соединения могут быть получены метанолят и перхлорат (после освобождения соот- ветствуклцего основания): (метокси- карбонилэтил)-1 -этнл-1,2,3,4,6,7- . -гексагидро-12Н-индол 2,3-а хиноли- зинметанолят - т.пл. 150-152°С, Crf D +27,8 (С 1, диметилформамид); 1 о(метоксикарбонилэтил) -этил-1,2,3,4,6,7-гексагидро-12Н-ИН- д, дол t2,3-а хинолияинперхлорат,- т,пл. 178,5-180°С, j +24 (С 1, диметилформамид) .
Из маточного раствора, остающегося после разделения, после освобождения основания можно получить также соответствующие соли о -этилантипо а.
Пример 3. (-)-1/1-(2-Метокси- карбонилэтил)- с(-этил-1,2,3,4,6,7,12, 12Ъо -октагидроиндапо 2,3-а хинолизин- дибензоилтартрат.
34,7 г (0,05 моль) (-)-1о(-(2-ме- токсикарбонилэтил)-1 /ь-этил-1,2,3,4, 6,7 гексагидро-12Н-индол Г2,3-aJ хино35
50
0 5
о
,
5
0
лизин-5-(-)-дибензоилтартрата в 70 мл диметилформамида подвергают гидрированию в присутствии 0,25 г 10%-ного палладия на активированном угле в качестве катализатора в течение 2,5 ч при 40°С и атмосферном давле- НИИ. Катализатор отфильтровьгоают и промьшают 10 мл диметилформамида в виде двух порций. К фильтрату добавляют при интенсивном перемешивании 200 мл 5%-ного водного раствора метанола. При этом осаждается (-)-дибен- зоилтартрат указанного соединения. Продукт промьшают 10 мл холодного метанола в виде двух порций и сушат.
Выход 26 г (75%), т.пл. 150-1 2 с, -120,1 (С 2, диметилформамид) .
П р и м е р 4. (+)-Ы-(2-Метокси- карбокклэтил)-1 -зтил-1,2,3,4.6.7, 12,12Ь -октагидроиндол 2,3-а хиноли- зин.
Согласно способу по примеру 3, но исходя из 34,7 г (0,05 моль) (+)-1о( - - (2-метоксикарбонилэтил) -1/5-1,2,3,4, 6,7-гексагидро-12Н-индол 2,3-а хино- лизина-5 в В1ще (+)-дибензоилтартрата получают 25,5 г указанного соедине- .ния (выход 73,5%). Т.пл. 150-151°С, 0/ +119,8° (С 2, диметилформамид) .
П р и м е р 5. (+)-1/5-(2-Метокси- карбонилэтил)-1о -этил-1 ,2,3,4,6,7, 12,12Ь/ь-октагидроиндол Г2, 3-а хиноли- зин.
4,39 г (0,01 моль) (-)-1/з-(2-ме- токсикарбонилэтил)-1 о -зтил-1,2,3,4, 6,7-гексагидро-12Н-ИНДОЛ 2,3-а хино- лизин-5-перхлората суспендируют в 100 мл метилового спирта при 60°С, добавляют при той же температуре в течение 1 ч 1,2 г боргидрида натрия в виде нескольких порций, после чего реакционную смесь перемешивают еще в течение 1 ч. От реакционной смеси отгоняют 70 мл метилового спирта и пе- -ремешивают полученный остаток при , промывают его, наливая сверху охлажденный метиловый спирт, после чего промьшают до нейтральной реакции дистиллированной водой.
Таким образом получают 1,7 г (50%) указанного соединения, т.пл. 108- 109°С. с д +69,7° (С 1, трихлор- метан).
П р и м е р 6. (-)-1(х -(2-Метокси- карбонипэтил)-1/5-этил-1 ,2,3,4,6,7,12, 12Ьс/-октагидроийдол 2, 3-а1хинолизин.
Согласно способу по примеру 5, но исходя из 4,39 г (0,01 моль) ( + )-1о - -(2-метоксикарбонилэтил)-1/1-этнл-1 , 2,3,4,6,7-гексагидро-12Н-индол 12,3- -а хинолизин-5-перхлората получают 1,73 г (выход 51%)указанного соединения, т.пл. Юв-ЮЭ С, -68,9 (С 1, трихлорметан).
П р и м е р 7. Разделение рацемата транс-1-(2-метоксикарбонилэтил)- -1 этил-1,2,3,4,6,7,12,12Ь-октагидро- индол 2,3-а хинолизина.
34 г (0,1 моль) указанного соединения суспендируют в 400 мл метилового спирта при и добавляют к пот лученной суспензии при той же температуре 15 г (0,1 моль) D-винной кислоты в 40 мл метилового спирта
6,8 г (0,02 моль) ()-1/5-(2-меток- сикарбоНИЛэтил)-1-ЭТИЛ-1,2,3,4,6,7, 12,12Ь/з-октагидроиндол 2,3-а хиноли- зина, 80 мл метанола, 4 мл воды и 2 г гидрата окиси натрия кипятят с обратным холодильником в течение 1 ч, после чего из смеси отгоняют 50 мл при пониженном давлении, добавляют к ней 80 мл воды и доводят рН до 6,5
(при 55 С). Гомогенный раствор охлаж-20 посредством 1 М водного раствора лимонной кислоты (при )-, Указанное соединение отфильтровьшают при 20°С, после чего промывают двумя порциями дистиллированной воды об1цим количеством 50 мл.
Таким способом получают 6,34 г указанного соединения (выход 99%), т.пл. 144° С (с разложением), Ы - +52,4 (С 1, этанол).
П р и м е р 9. (-)-Ы-(2-Карбок- сиэтил ) -1 fi-этил-1 ,2,3,4, f.., 7,1 2,1 2Ь/i- -октагидроиндол 2,3-а хинолизин.
Согласно способу по примеру 8, но исходя из 6,8 г (0,02 моль) (-)-Ы- -(2-метоксикарбонипэтил)-1 /5-зтил-1, 2,3,4,6,7,12,1 2Ь/1-октагидроиндол 2, 3-а хинолизина получают указанное соединение, т.пл. 144 с (с разложением), -48,6 (С 1, этанол).
Пример 10. (-)-1 ь-(2-Меток- сикарбонил-2-гидроксиимино)-этил -1 с(- -этил-1,2,3,4,6,7,12,1 2Ьо -октагидро- индол 2,3-аЗхинолизин и его хлоргид- рат.
К 34 г (0,1 моль) (-)-1/5-(2-меток- сикарбонил этил )-1 « -этил-1 ,2,3,4,6,7, 12,12Ьа -октагидроиндол 2,3-а хиноли- зина в 20 М.П абсолютированного толуола добавляют сначала раствор (55- 60%-ный) в толуоле 30 м.п трет-бутилдают до 15 С. Осаждающийся при этом (+)-1/з-(2 метоксикарбонилзтил)-1с/- -этил-1 ,2,3,4,6,7,12,1 2Ь/5-октагидро- индол 2,3-а хинолизин-5-1 -тартрат от- фильтровьгеают и промьшают двумя пор- 25 циями холодного метанола (всего 50 мл).
Таким способом получают 24,1 г (выход 98,3%) указанного соединения, т.пл. 213-215 С, o( j, +,8 (С 1,30 диметилформамид).
Соответствующее основание освобождают следующим образом. Продукт растворяют в 200 мл воды, рН доводят до 9 водным раствором аммиака, после чего смесь экстрагируют тремя порция ми дихлорметана общим количеством 120 мл. После сушки раствора из него отгоняют растворитель и полученньй маслообразньй остаток кипятят с 30 мл метанола.
Таким способом получают 15,5 г (выход 91,5%) (+)-1 р,-(2-мётоксикарбо- - нилэтил)-Ы-этил-1,2,3,4,6,7,12,12Ьр,- -октагидроиндол 2,3-а хинолизина, т.пл. 108,5-109 С, ,°3 +70,1 (С 1, трихлорметан).
Из маточного метанольного раствора, остающегося после разделения, выделяют другой оптический изомер
,-35
40
Указанный раствор разгоняют до объе- нитрила, а затем 17 г (0,15 моль)
ма, равного 100 мл, разбавляют 200 мл воды и после доведения рН до 9 водным раствором аммиака экстрагируют тремя порциями дихлорметана общим количеством 120 мл. Смесь сушат, отгоняют из нее растворитель и кипятят полученный маслообразный остаток с 30 мл метанол я.
Таким способом получают 15,1 г (выход 89%) (-)-Ы-(2-метоксикарбо- нилэтил ) -1 -этил-1,2,3,4,6,7,12,12Ьо/- -октагидроиндол Г 2,3-а хинолизина, т.пл. , -69,4 (С 1, трихлорметан).
П р и м е р 8. ()-Ift-f 2-Карбокси- этил)-Ы-этнп-1,2,3,4,6,7,12,12Ь;9-ок- тагидроиндол 2,3-а хинолизин.
6,8 г (0,02 моль) ()-1/5-(2-меток- сикарбоНИЛэтил)-1-ЭТИЛ-1,2,3,4,6,7, 12,12Ь/з-октагидроиндол 2,3-а хиноли- зина, 80 мл метанола, 4 мл воды и 2 г гидрата окиси натрия кипятят с обратным холодильником в течение 1 ч, после чего из смеси отгоняют 50 мл при пониженном давлении, добавляют к ней 80 мл воды и доводят рН до 6,5
посредством 1 М водного раствора лимонной кислоты (при )-, Указанное соединение отфильтровьшают при 20°С, после чего промывают двумя порциями дистиллированной воды об1цим количеством 50 мл.
л
,-35
40
трет-бутилата калия. Реакционную смесь перемешивают при 25-30 С в течение 20 мин, после чего медленно добавляют 150 мл абсолютированного метанола и реакционную смесь перемешивают при 40 С в течение 3 ч. Затем реакционную смесь охлаждают до 20°С, подкисляют до рН 1 концентрированной
указанного соединения, 2104, o( i, 3 -62 (С 1,
соляной кислотой, добавляют 50 мл воды и перемешивают при +5°С в течение 2 ч. Остаток отфильтровывают, отмывают от хлористого калия водой и сушат полученный при этом осадок.
Таким способом получают 32,5 г (выход 80%) хлоригидрата указанного соединения, т.пл. 265-272°С (с разложением), Г -57 (С 1, диме- тилформамид).
Из полученного гидрохлорида можно получить свободное основание в результате суспендирования соли в 80 мл метанола и добавления к полученной суспензии по каплям при перемешива ни смеси 25 мл 25%-ного водного раствора гидрата окиси аммония и 40 мл воды. После перемешивания в течение 1 смесь охлаждают до 10°С, фильтруют, промывают водой и сушат.
Таким способом получают 24-25 г
т.пл. 208диметил-формамид).
Пример 11. (-)(2-Меток- сикарбонил-2-гидроксиимино)-этил -1с/ -этил-1,2,3,4,6,7,12,12Ьв(-октагидро- индол 2,3-а хинолизин.
Согласно способу по примеру 10, но при замене трет-бутилата калия на 15 г трет-бутилата натрия получают 24 г (выход 60%) указанного соединения.
При добавлении к реакционной смес также 7 мл диметилформамида получают 32,5 г (выход 80%) указанного соединения..
П р и м ер 12. (-)-1р-(2-Этокси карбонип-2-гидроксиимино)-этил -1 -этил-1,2,3,4,6,7,12,12Ьо -октагидро- индол 2,3-а.хинолизин и его хлоргид- рат.
Согласно способу по примеру 10, но при замене метанола на 150 мл абсолютированного этанола получают 25 солянокислой соли указанного соеди- нения (выход 60%), т.пл. 257-260 С, Св( ° -55 (С 1, диметилформамид)
Соответствующее основание освобождают в водном растворе этанола с добавкой 25%-лого раствора гидрата окиси аммония согласно способу, описанному, в примере Ш. При этом получают 21 г указанного соединения.
3 -118° (С 1
Т.ПЛ. 172-173°С, трихлорметан).
Пример 13. (ь)-1о((2-Эток сикарбонил-2-гидроксиимино)-этил -1 j
-зтил-1,2,3,4,6,7,12,12Ьл-октагилро- иядолГ2,3-а хинолизин и его хлор1чщ- рат.
Согласно способу по примеру 10, но исходя из 34 г (+)-1п -(2-метокси- карбонилэтил)-1 -этил-1,2,3,4,6,7,12, 12Ьр-октагидроиндол 2,3-а хинолизина и, используя 150 мл абсолютированного
спирта, получают 25,2 г хлоргидрата указанного соединения, т.пл. 258- 260°С, +55° .(С 1, диметилформамид) .
Соответствующее основание освобождают в водном этаноле с добавкой 25%- ного раствора гидрата окиси аммония согласно способу, описанному в примере 10. В результате получают 2Г, 3 г указанного соединения, т.пл. 171- , +118° (С 1, трихлорметан) .
Пример 14. (-)-Ы-С(2-Меток- сикарбонш1-2-гидрок сиимино)-этил - -1 / -этил-1,2,3,4,6,7,12,1 2Ьо -октагид- роиндол 2,3-а хинолизин и его хлор- гидрат.
Согласно способу по примеру 10, но исходя из 34 г (0,1 моль) (-)-1о/- -(2-метоксикарбонилэтил)-13-этил-1, 2,3,4,6,7,12,1 2bf -oктaгидpoиндoлt2, 3-а хинолизина получают 24,3 г (выход 60%) хлоргидрата указанного соединения, т.пл. 214-215 С, о1 д -46° (С 1, диметилформамид).
Полученный хлоргидрат суспендируют в 50 мл воды, добавляют к полученной суспензии 100 мл хлороформа, после чего доводят рН до 9 посредством 25%-ного водного раствора гидрата окиси аммония. Фазу в хлороформе отделяют и экстрагируют водную фазу 20 мл хлороформа. Объединенные органические слои сушат над сульфатом натрия, отгоняют растворитель в вакууме и перекристаллизовьшают остаток из 30 мл дихлорэтана. В результате получают 16 г указанного соединения, .т.пл. 1б6-168 С, ld ° -54° (С 1, диметилформамид).
Пример 15. (+)(2-Меток- сикарбонил-2-гидроксиимино)-этил}-1 Ы- этил-1,2,3,4,6,7,12,12Ьр-октагидроиндол С 2, 3-а хинолизин и его хлоргидрат.
Согласно способу по примеру 10, но исходя из 34 г (0,1 моль) (-t-)-1/i- -(2-метоксикарбонилэтил)-1ч-этнл-1, 2,3,4,6,7,12,12Ъ/ь-октагидроиндолГ2, 3-а}хинапизина получают 25 г (вькод
61,5%) хлоргидрата указанного соединения, т.пл. 214-215 С, +46° (с 1, диметилформамид).
Из хлоргидрата получают соответ- j ствующее свободное основание согласно описанному в примере 14 способу. Таким образом получают 19,2 г указанного соединения, т.пл. 166-168°С, с 0° +53,2 (С 1, диметилформаг- 10 мид). -
П р и м е р 16. (-)-1о(-Г(2-Этокси- карбонш1-2-гидроксиимино)-этил J-1 -этнл-1,2,3,4,6,7,12, 12Ь« -октагидро- индол Г2,3-а хинолизинхлоргидрат. j 5
Согласно способу по примеру tO, но исходя из 35,4 г (0,1 моль) (-)- -1о(-(2-этоксикарбонилэтш1)-1 /}-этш1- -1,2,3,4,6,7; 12,12Ь/.-октагидроин- ,3-а хинолизина и, используя 20 в качестве спирта 150 мл абсолютированного этанола, получают 23 г (выход 55%) указанного соединения, т.пл. 247-249 С, -44 (С 1, диметилформамид) .25
Пример 17. ()(2-этокси- карбонш1-2-гидроксиимино)-этил -1о/- -этип-1,2,3,4,6,7,12,12Ь р-октагидро- индол 2,3-а хинолизинхлоргидрат.
Согласно способу по примеру 10, но .JQ исходя из 35,4 г (0,1 моль) (+) -(2-этаксикарбонилэтил)-Ы-этил-1,2,- 3,4,6,7, 12, 12Ь/5-октагидроиндол 2, хинолизина и, используя в качестве спирта 150 мл абсолютированного эта- , нола, получают 23,2 г указанного соединения, т.пл. 248-249 С, о( +45 (С 1, диметилформамид).
Пример 18. Рацемат транс-1- - (2-этоксикарбонип-2-гидроксиимино)- Q -этил -1-этил-1,2,3,4,6,7,12, тагидроиндол 2,3-а хинолизинхлоргид- рата.
Согласно способу по примеру 10, но исходя из 35,4 г (0,1 моль) рацемата транс-1-(2-этоксикарбонилэтил)-1- -этш1- 1,2,3,4,6,7,12,12Ь-октагидро- индол12,3-а хинолизина и, используя 150 мл абсолютированного спирта, получают 25,1 г (выход 60%) указанного соединения, т.пл. 226-228 С (с разложением), с( в° О (С 1, диметилформамид) .
П р и м е р 19. Этиловый эфир (+)-транс-аповинкаминовой кислоты.
4,75 г (0,025 моль) моногидрата 55 п-толуолсульфоновой кислоты нагревают с обратным холодильником в колбе, оборудованной водяным холодильником
Маркуссона, при атмосферном давлении, после чего добавляют толуол до 70 мл и вводят 4,2 г (0,01 моль) (-)-Ы- - (2-этоксикарбонил-2-гидроксиимино)- -этнл -1/5-этил-1,2,3,4,6,7,12, 12Ь/5- -октагидроиндолГ2,3-а хинолизинхлор- гидрата. Реакционную смесь нагревают с обратным холодильником в течение 1,5 ч и добавляют к ней при комнатной температуре 30 мл воды. Значение рН смеси доводят до 9 водным раствором гидрата окиси аммония. После отделения толуольной фазы растворитель отгоняют при пониженном давлении, а маслообразный остаток кипятят с 5 мл этанола и фильтруют смесь при . В результате получают 3,14 г (выход 90%) указанного соединения, т.пл. 120-122 с, +144,4° (С 1, трихлорметан).
П р и м е р 20. Рацематный транс- -1-(2-метоксикарбонилэтил)-1-этил-1, 2,3,4,6,7,12,12Ь-октагидроиндолГ2,3- -a гyaнoлизин.
2 г рацематного транс-1-(2-карбок- сиэтил)-1-этил-1,2,3,4,6,7,12,12Ь-ок- тагидроиндол 2,3-а хинолизина растворяют в тионилхлориде при 0-5° С и раствор перемешивают в течен 2 1,5 ч. Полученный рацематный траяс-гидрохло- рид 1-(2-хлорокарбонил)-1-этил-1,2, 3, ,7,1 2,12Ь-октагидроиндол 2, хинолизина кристаллизуется в результате добавления к смеси 40 мл бензола. Смесь фильтруют и дважды промывают бензолом порциями по 10 мл. Полученный гидрохлорид растворяют в 10 мл метанола и раствор перемешивают при комнатной температуре в течение 1 ч. Путем добавления к полученному раствору 20 мл воды и водного раствора NH40H рН устанавливают равным 9. Осаж- денньй продукт отфильтровьшают, промывают водой и метанолом и затем сушат. Получают 1,58 г целевого соединения (выход 76%), т.пл. 147,.
Пример 21. (-)-1(1-(2-Метокси- карбонилэтшт)- о -этил-Т ,2,3,4,6,7, . 12,12Ьс/-октагидроиндол 2,3-а j хино- лизин.
Проводят аналогично примеру 3 при каталитическом гидрировании 2 ч при . Выход 70%, физические константы аналогичны указанным в примере 3.
Ир им е р 22. (-)-1/ь-(2-Метокси- карбонилэтил)-1 о(-этш1-1,2,3,4,6,7, 12,12Ь о -октагидроиндол 2,3-а хино- лизин.
Проводят аналогично примеру 3 при каталитическом гидрировании 4 ч при 20°С. Выход 75%, физические константы аналогичны указанным в примере 3.
Пример 23. (-)-1/1-(2-Меток- сикарбонил-2-гидроксиимино)-этил - . Ы-этил-1,2,3,4,6,7,12,12Ь(ъ-октагид роиндолС2,3-а хинолизин и его хлор- гидрат.
Поступают аналогично примеру 10, Ьднако реакцию с трет-бутилнитрилом проводят 30 мин при 10°С. Выход и физические константы такие же, как указано в примере 10.
Пример 24. (-)-1/)-(2-меток- сикарбонип-2-гидроксиимино)-этил - -1 о(-этш1- 1,2,3,4,6,7,12,12Ь /ь-октагид роиндол 2,3-а хинолизин и его хлор- гидрат.
Поступают аналогично примеру 10, однако метанольную обработку проводят 3 ч при 60°С. Выход 75%, иденти- фицир5пощие данные аналогичны указанным в примере 10.
Пример 25. Целевой продукт тот же. Поступают аналогично примеру 10, только метанольную обработку проводят 4 ч при 20 С. Выход 80%, идентифицирующие данные аналогичны указанным в примере 10.
Формула изобретения
Способ получения рацематов или оп тйчески активных производных цис- или транс-гидроксиминооктагидроин- ,3-а хинолизина общей формулы
(I)
, V
где R - С -С -алкил, или формул
CCCH V ROOCCCH/Vi
.oH
где R - С,-С4-алкил,
или их гидрохлоридов, отличающийся тем, что рацемат производ- ного гексагидроиндолС2,3-а хинолизина общей формулы
10
Xj
Н
сн ооссн сн
или полученные разделением с использованием оптически активной дибензо- 15 илвинной кислоты оптически активные производные формул
20
СНзООССН2СН7
С2Н5
25
(116)
СНзООССН СН
30
35
40
где Х - бензоилтартрат или перхлорат,
либо гидрируют на активированном угле в присутствии катализатора - 10%-ного палладия при 20-60 0 и атмо- сферном давлении с вьщелением соответственно рацемических или цис-про- изводных с получением промежуточных соединений общих формул (III) (рацемическое цис-производное), (Ilia) или (III6) (цис-производные), либо восстанавливают боргидридом натрия с вьщелением соответственно рацемических или транс-производных с вьщелением промежуточных соединений общих формул (III) (рацемическое транс-про- д5 изврдное) (Шв) или (Шг) (транспроизводные)
(III)
50
СНзООССН2СН
55
(Ilia)
СНаООССН.СН
13
(III6)
CHiOOCCH CHf
(Ills)
CH OOCCH2CH
2 I
CiHs
(Illr)
CH OOCCH CHf
полученный рацемат цис- или транс- октагидроиндолС 2,3-а хинолизина фор10
376947 А
мулы (ill) при необходимости разделяют на оптически-активные изомеры с использованием D-винной кислоты или подвергают щелочному гидролизу до соответствующей кислоты с последующей ее этерификацией до С -С -алкило вого эфира, или оптически-активные производные общих формул (Ша), (III6), (Шв) или (Illr), ИЛИ указанные переэтерифицированные производные обрабатывают сначала трет-бу- тилнитрилом в растворе ароматического углеводорода, предпочтительно в толуоле, с добавлением, если необхо-. димо,.каталитических количеств диме- тилформамида при 10-30 С, а затем спиртом общей формулы
R-OH ,
где R имеет указанное значение, при 20-60 С с выделением целевого продукта в свободном виде или в виде гидрохлорида.
15
20

| БЛОКИРУЮЩЕЕ УСТРОЙСТВО ПОЛОЖЕНИЯ РАБОЧИХ | 0 |
|
SU177500A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
Авторы
Даты
1988-02-23—Публикация
1983-02-22—Подача