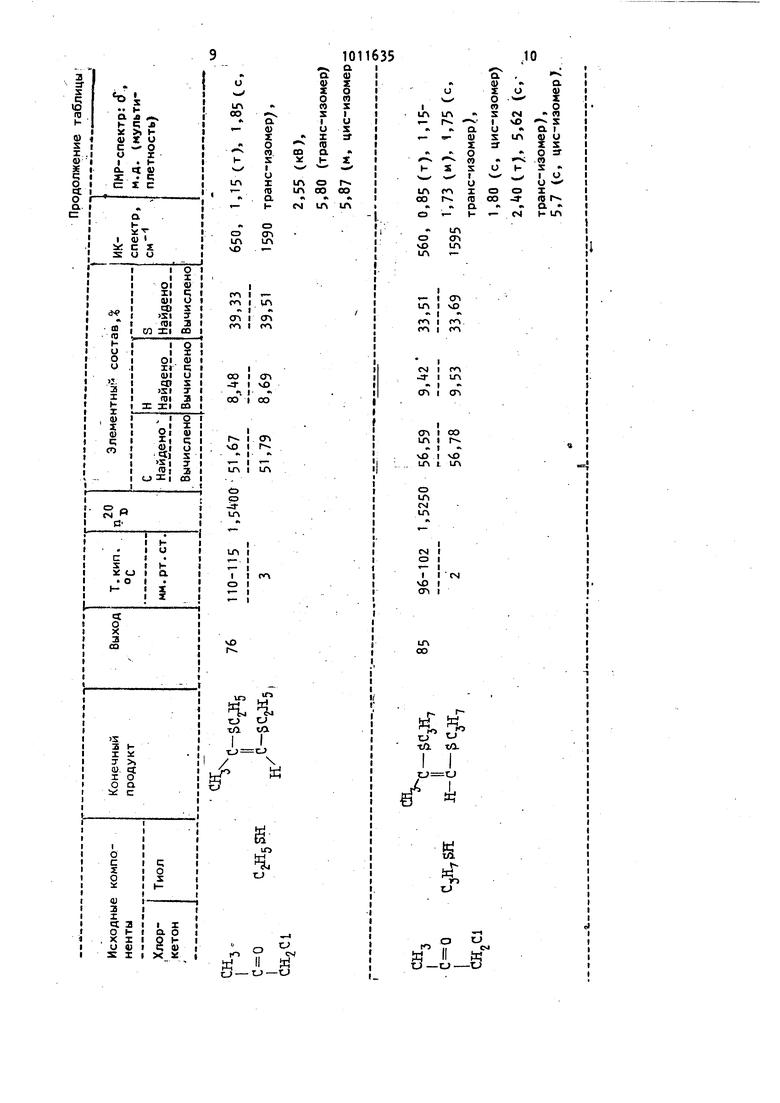
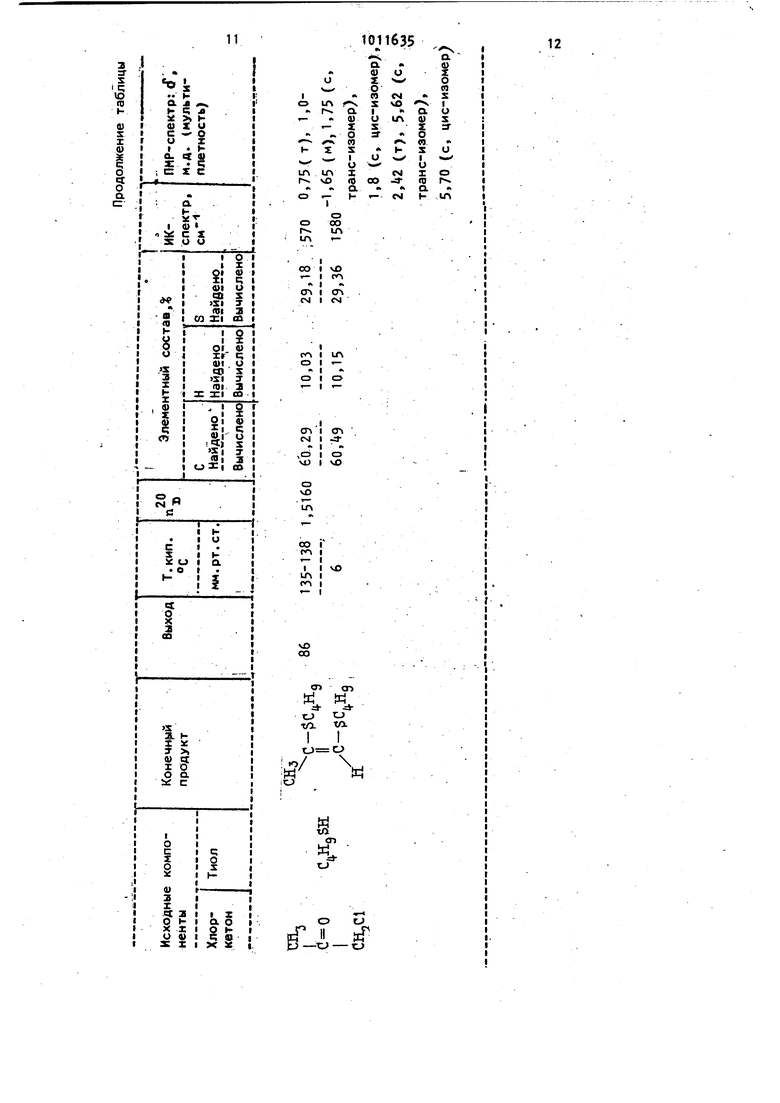
Изобретение относится к усоверше ствованному способу получения 1, -д тиенов формулы 1 или 1,2-бис-(алкил тио)-алкенов-1 формулы М х Ъил. JL ,С- . .где R - атом водорода, E..j,- низший алкил или R и Я,вместе образуют триметиленовую илп тетраметиленовую .цепочку, RO,-низший алкил, которые находят широкое применение в к честве исходных соединений для произво ства дефолиантов и десикантов хлопчат нйка и картофеля, вспомогательных химикалиев для уборки урожая, регуляторов роста растений гербицидов, а также полупродуктов синтеза разно образных биологически активных веществ. Известен способ получения циклических 1 , -дитиенов формулы Л Х ГЧгде Ry -.атом водорода и R -метил или R и ,- фенил, взаимодействием этйндитиола с о -бромкетоном tО Недостатками способа являются меньшая доступностьс6 ромкетонов по сравнению coL-хлоркетонами, и низкие выходы 1 . -дитиенов (.не более бО). Известен также способ получения .циклических 1,4-дитиенов формулы где R-, 9 R Q-независимо друг от друга атом водорода, метил или этил, или R и Rg или Rg и Я. вместе образуют триметиленовую или тетраметиленовую цепочку,(которЪ1Й заключается в том, что соответствуюи ийа хлоркетон подвергают вза модействию с 1 ,2-дитиолом в присутствии катализатора пара-толуолсульфокислоты при , с последующим выдерживанием реакционной массы при комнатной температуре, и кипяче нием ее в бензоле 23 Недостатками этЬгб способа являются сложность процесса, обусловленная использованием Henejseгоняемого катализатора и последующим его удалением, длительность процесса, низкие выходы целевых продуктов (30-60).. Наиболее близким по технической сущности и достигаемому результату к изобретению является способ получения 1,4-дитиенов формулы XIX, который заключается в том, чтос -хлорке -тон формулы III BI-C-CI где R,, и Rj имеют вышеуказанные зна чения, подвергают взаимодействию с тиолом формулы 1У НЗ-СН- -СН ЗН (IV . при кипячени в среде бензола в присутствии катализатора пара-толуолсульфокислоты | 3 Недостатками этого способа являются относительно невысокий выход до 70%) продуктов, сложность процесса, обусловленная необходимостью применения неперегоняющегося катализатора дополнительных операций по его удалению. Кипячение реакционной смеси в присутствии катализатора вызывает частичное осмоление продуктов реакции, что снижает выходы целевых продуктов. Соединения формулы II не были получены и являются новыми соединениями. Целью изобретения является упрощение технологии процесса, повышение выхода и расширение ассортимента целе вых продуктов. Эта цель достигается согласно способу получения 1 ,-дитиенов формулы 1 или 1,2-бис-(алкилтио)-алкенов-1 формулы (I, который заключается в том чтосз -хлоркетон формулы Ш BI-C-CI I где R и Я-2. имеют вышеуказанные зна.чения, подвергают взаимодействию с тиолом формулы IУ или У 310 HS-Cffj-CH H (IV) МАИ Я,5Н , (V где R. имеет вышеуказанные значения7 в среде циклогексана при с последующим выдерживанием реакционной .смеси при комнатной температуре. Согласно настоящему способу к перемешиваемому раствору тиола в циклогексане, охлажденному до О- , в течение часа прикапывают раствор с -хлоркетона в циклогексане. Температуру поддерживают в интервале О- После прибавления всегоо(,-хлоркетона температуру повышают до комнатной и выдерживают реакционнуюсмесь 8ч, выделившийся водный слой у(СЕ удаляют а растворитель отгоняют. П р и м е р 1 . К перемешиваемому раствору 9 г (1,0,моль) этандитиола в 750 мл циклогексана, охлажденному ледяной водой до О- +2°С, в течение 1 ч прикапывают раствор 118,5 г р,0 моль )а6-хлорциклопентанона в 250 мл циклогексана. Скорость прикапы вания и интенсивность охлаждения ледяной водой регулируют таким образом, чтобы температура реакционной смеси поддерживалась в интервале О- +5°С, После прибавления всего of -хлорциклопентанона охлаждение убирают, постепенно (в течение 0,5 ч доводят температуру реакционной смеси до 20С и оставляют на 8 ч. Выделившийся водный слой НС (1617 мл удаляют, а циклогексан перегоняют под атмосферным давлением. При этом, в виде азеотропной смеси с цикле j-ексаном выделяют еще мл водной нес. Остаток после удаления цикло гексана перегоняют в.вакууме. Получают 139 г (выход 88 ) 2,3-триметилен -1,-дитиена-2; т.кип. 85-87С/2 мм. рт.ст., rj,6l35. 54 Найдено,: С 55,93 Н 6,31, S 0,29. Вычислено,: С 53,11, Н 6,37/ S 0,52. .. ИК-спектр: ПОЛОСЫ поглощения при 1б10Сл с с)и 530 см-- ) ПМР-спектр: мультиплеты при 1,60 :-CHj V /CHi/ и 1,95 I i а такV -сн -/-S-fA3,0 м.д. е синглет V-S-CHj/ с относительными интегральными интенсивностями 1:2:2. П р и м е р 2 . Аналогично примеру 1 из 118,5 г (1,0 моль)о -хлорциклопентанона и 152 rQ2,0 моль) пропилмеркаптана получают 188 г г выход 87) соответствующего дитиена-1,2-дипропилтиоциклопентена-1, т.кип. 105ПО С/З мм. рт.ст., 1,. Найдено,I: С 60,87; Н 9,21, S 29,6. Вычислено,%: С 61,05 И 9,32; is 29,63. . . ПМР-спектр: триплет при 0,90 м.д. |(концевые -СКз)мультиплеты при 1,68 /-% l(CHa,) и 2,10 ( а такЧ-СН . /--С-СК2 же триплет (f 2,55 м.д. ,1 -V -сНгУ ИК-спектр: 1590 и 530 смПо примеру 1 получаю.т и другие соединения формулы I и II. Вьход, физико-химические и спектрО скопические характеристики соединений i1 и tl представлены в таблице.
1Л
f
- К
ил
1Л
vO (ОOO
1
ъ Q,M «ч
т -
о OO r in in .-
vO
CO
rr,
r
CTi
CM CM
. g
M S vO
a
и lA
r
«0
s
{,
о
I
r
ID O.
1Л
ь




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дитиенилалкиламинов или их солей | 1978 |
|
SU747426A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ КУМЕРМИЦИНОВ | 1972 |
|
SU342339A1 |
| Способ получения производных уксусных кислот | 1973 |
|
SU627749A3 |
| Способ получения производных конденсированных индолов или инденов | 1973 |
|
SU728716A3 |
| Способ получения производных 1-/3-(3,4,5-триметоксифенокси)-2-пропил/-4-арилпиперазина | 1978 |
|
SU893133A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛОВЫХ ЭФИРОВ3- | 1971 |
|
SU430543A1 |
| Способ получения 3-тиовинилцефалоспоринов или их солей | 1980 |
|
SU1114339A3 |
| Способ получения 1-алкокси-1-алкилтиоалканов | 1982 |
|
SU1011637A1 |
| Способ получения тиенилалканпроизводных | 1971 |
|
SU455540A3 |
| Способ получения стероидов | 1979 |
|
SU860708A1 |
Способ получения 1,4-дитиенов (формулы 1 или 1,2-бис-(алкилтиб)-алкенрв-1 ФОРМУЛЫ Л где Ri - водород, R,,. - низший алкил ил R и R-Xвместе образуют тримети-; леновую или тетёоаметиленовую цепочку ,- R,j - низший алкил, взаимодействием oL-хлоркетона фор мулы III -Y (ill) Д,С1 н где R и R.4 имеют вышеуказанные значения с тиолом в среде органического раствоЬителя, отличающий c я тем, что, с целью упрощения техноэ § логии процесса, повышения выхода О) и расширения ассортимента цeJC.eвыx про дуктов, используют тиол формулы V или У IHS-CHj-OLiSH (IV) MNW R,,SH,CV) где Ri имеет вышеуказанные значения. Э качестве органического растворителя Од используют циклогексан, и процесс оо сд ведут при , с последующим выдерживанием реакционной смеси при комнатной температуре.
1Л
tv-1
о
ri
о
чО
OO ff
vO
ил
PO
Or T
CJtJ
to.to.
-O/
;S
ao
о cj
iПриведенные в примере 1 условия получения дитиенов являются оптимальными, обеспечивающими наибольшие выходы целевых продуктов. Проведение серии экспериментов, отличных по уело ВИЯМ, от оптимальных, позволяет устйновить, что изменение соотношения of-хлоркетон (. тиол больше или меньше по отношению к стехиометрии) уменьшает выходы целевых продуктов на lO-fO, причем в условиях избытка, тиола выходы уменьшаются в результате реакции присоединения избыточного тиола к конечному дитиену, что приводит к неперегоняемым продуктам уплотнения, а избыток -хлоркетона приводит к побочной реакции образования 2-алкилтиозамещенного кетона, применение других растворителей (.бензол, толуол).также уменьшает, причем в некоторых случаях очень резко, выходы
дитиенов, уменьшение температуры прибавления о -хлоркетона к тиолу нецелесообразно, так как не увеличивает выход целевого продукта и не сокращает существенно продолжительность реакции, а увеличение температуры прибавления приводит к снижению выходов целевых продуктов за счет осмоления, проведение реакции в аналогичных примеру 1 условиях, но с применением катализатора (пара толуолсульфокислоты) уменьшает на 5-20 выходы целевых продуктов за счет большего осмоления.
Преимуществом предлагаемого способа является то, что он позволяет упростить технологию процесса, исключив применение катализатора.и стадии требуемые для его удаления, повысить выход ( на 5-10%) и расширить ассортимент целевых продуктов.
Авторы
Даты
1983-04-15—Публикация
1981-12-18—Подача