Изобретение относится к новым соединениям - 2- замещенным 3-окси -5 мети:г-4-тиофенуксусным кислота формулы Г НООСН2С ОН зС S COR где R -этокси, нафтиламино- или незамещенная, или- замещенная в па положении хлором, -метокси или это группой аншшногруппа,. .которые проявляют,; противоврспалительную и анальгетическую актив ность и могут поэтому найти приме нение в медицине, а также к новом способу их получения. . В литературе опис алы. ближайшие структурные аналоги новьк соединв кий формулы 1 из класса тиофенукс ных кислот, например производные й-тиофенуксусной кислоты формулы ROOCCH от Rj где R и R -. каждый водород, метил или этил, RJ- алкил с атомами углерод или незамещенньй, или замещенный метил-, одной или двумя метоксигру пами фенил; RJ- окси-, этокси или анилино- группа, , которые могут -быть использованы в синтезе биологически активных веща Описан также способ получения указанных известных веществ формулы Та, з.аключающийся в том, что эфир формулы Па ROOCCHCH COR где R, R, и Rj, имеют вьшеуказанны значения, подвергают взаимодействию с хлорокисью фосфора в присутствии диметилформамида при температуре снача , а затем 50-75 С и образующееся соединение формулы 1 Т Та ROOCCH-C-CHO I II Ri Cl где R, R, и R имеют .вьшеуказанные значения, ... .. обрабатывают производным тиогликолевой кислоты формулы 1Уа: , где Rj - этокси- или анилиногруппа, в присутствии слабого основания с пос.ледую111;им выделением целевого продукта или, в случае необходимости, с последующим.гидролизом спиртовым, раствором щелочи при, кипячении. Однако невозможно было предположить осуществление внутримолекулярной сложноэфирной конденсации по Дикману в присутствии слабого основания, как это имеет место в предложенном новом способе получения новых соединений формулы Г, так как известно, что конденсацияпо Дикману протекает только в присутствии сильных оснований.. Целью изобретения является расширение арсенала средств воздействия на живой организм и разработка нового способа- получения новых производных тиофенуксусной кислоты фдрмулы Л. Поставленная цель достигается новыми соединениями формулы Т, которые обладают противовоспалительной и анальгетической активностью, и новым способом ух получения, который заключается в том, что этиловый эфир 3-хлор-2-(карбэтоксиметил.кротоновой кислоты формуды 11 CH2-COQC2H5 СНз-С С-СООС Н5 Cl подвергают взаимодействию с производным тиогликолевой кислоты формулы m , где R. - имеет вы-/ шеуказанные значения, в присутствии слабого основания в среде полярного растворителя при кипячении с последующим гидролизом полученного при этом этилового эфира 2-замещенной 3-окси-5-метил-4-тиофенуксусной кислоты формулы 1У де R - имеет вышеуказанные значения, одно-спиртовым раствором щелочи ри кипячении.
Предпочтительно в качестве слабого основания используют углекислый калий или триэтиламин.
В качестве полярного растворителя использзтот этиловый спирт, диме- тилформамид или диметилсульфоксид..
Соединения формулы II и 1У также являются новыми соединениями.
Пример 1. Получение, 2-карб.этокси-3-окси-З-т етил-А-тиофенуксус- ной кислоты (). ,
а) Получение исходного соединения - этилового эфира 3-хлор-2-(кapб эJ oкcимeтил) кротоиовой кислоты IТ.
К 108 г (0,5 моль) диэтилового эфира ацетоянтарной кислоты; в 74 мл сухого бензола в течение 2,5 ч добавляют порциями при перемешивании 91,3 г (0,44 моль PClj-). Смесь выдерживают 40 мин при комнатной температуре , охлаждают в смеси льда с солью от О до +5с) и прикапывают постепенно 65 мл воды. Верхний слой тделяют, нижний - экстрагируют бензолом (2x150 мл). Объединенные бензольные экстракты промьшают 4%-ным .раствором NaOH и водой, затем упаривают бензол ч остаток перегоняют.
Получают 48,18 г (41,2%) соединения Л I .в виде бесцветной подвижной мacляниcтoй жидкости .с ароматршм заnaxoMf смешивающейся с органическими растворителями, устойчивой при хранении. Т.кип. 135-14lc / 22 мм рт.ст
п л
24
1,4565 ..
Найдено,.%: С 50,75; Н 6,20; С1. 15,20. . .
SV4C1Вычислено, %: С 51,16; Н 6,45;
С1 15,11.
ИК-сп ктр, см : Ло . 740,:. 1630. .,
Уа спектр (спирт) 1„д,-(1ве), нм: 225 (3,87).
б) Получение этилового эфира 2 2-карбэтокси-3-окси-5-метил-4-тио- фенуксусной кяслоты (IV, .
Смесь 9,36 .(0,04 моль)этилового эфира 3-хлор 2-(карбэтоксиметш1) кротоновой кислоты, 5,8 г. (О,04 мол этилового эфира тиогликолевЬй кислоты и 8,25 г (0,06 моль) прокаленного углекислого калия в 60 мл абсолютного этилового:спирта кипятят 3 ч, осадок отфильтровывают, .спирт упаривают.
Получают 9jl5 г (84%) этилового эфира 2-карбэтокси-3-Окси-5-метил-4-тиофенуксусной кислоты, т.пл. 8586 С (петролейный эфир,40-70 с).
При использовании в качестве конденсирующего агента триэтиламина продукт получают с выходом 50%.
Найдено, %: С 52,90; Н 6,00; S 11,58.
Вычислено, %: С 52,92; Н 5,92;
S 11,76.
ИК-спектр (вазелиновое масло),
см-: он 3240Лоос,Н5 730.
УФ-спектр (спирт), -Д (lg6), нм: 272 (4,22). ЯМР-спектр с (CDC1,),S , м.д.:
166,0 (С-4), 143,2 (С-2), 121,4 (С-4), 97,6 (С-5.)..
в) Получение 2-карбэтоксй-3-окс -. -5-метил-4-тиофенуксусной кислоты; 9,15 г (0,0336 моль) этилового
эфира 2-карбэтоксй-3-окси-5-метил- 4-тиофенуксусной киблоты и 2,69 г (0,067 моль) NaOH в 65 мл 50%-ного метилового спирта кипятят 50 мин. Смесь охлаждают, вьшивают в воду и подкисляют концентрированной соляной кислотой (рН 1-2). Осадок отфильтровывают, промывают водой.
Получают 5,25 г (65%)целевого продукта в виде.кристаллического веществй белого цвета с-розовым оттенком, растворимого в спирте, хлоро форме, ацетоне, диметилформамиде. Т.пл. 156-158 С (вода), М 244.
В условиях, аналогичных примеРУ1 Сстадии (б) ) получают соединения № 2-6 общей формулы I.
Пример 2. б) Получение этилового эфира 2-(4-этоксифенил)-кар- бамОил-3-окси-5 метил-4-тиофенук;сусной кислоты (-Ту, п-этокрианилино- группа).
Смесь 2,34 г (0,01 моль) этилового- эфира 3-хлор-2-(карбэтоксиме- тил) кротоновой кислоты, 2,1- г (0,01 моль) Ы-(4-этоксифенил)-2-меркаптоацетамида и 2,07 г (0,015 моль) прокаленного углекислого калия в 15 мл диметилсуПьфоксида кипятят 1,5 ч.Охлаждают, выпивают в воду и подкисляют концентрированной с.олянрй кислотой. Экстрагируют бензолом, бензол упаривают. .
Получают 2,13 г (58,5%) этилоэого эфира 2-(4-этоксифенил)-карбамош1-3-оксиг5гметш1-4-тиофенуксусной кислоты в виде кристаллического вещества белого цвета с розовым оттенком. Т.пл. 163-165°С (этанол).
Найдено, %: С 59,46; Н 6,02; S 8,83. .
. .,. .
Вычислено, %: С 59,48; Н 5,83; S В , 82.
ИК-спектр (вазелиновое масло),
. 3340, сои Н 1700.
УФ Спектр (спирт), Ti (ig), нм: 205 (4,28), 285 (4,2б).
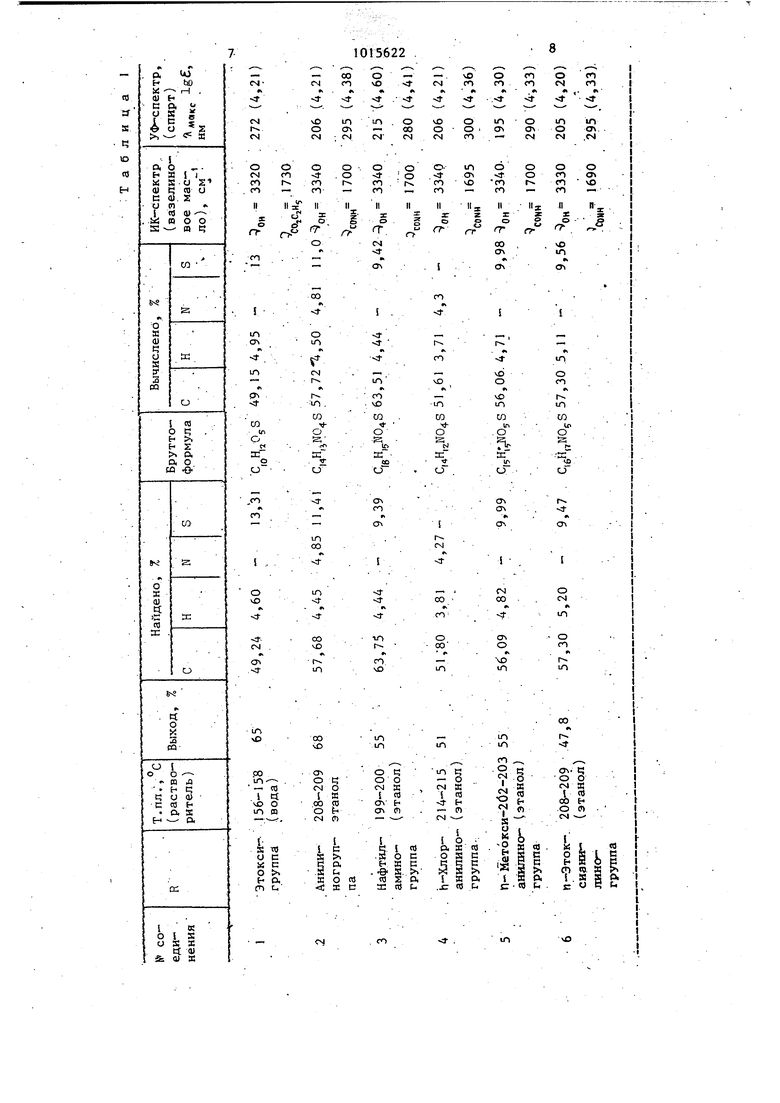
Физико симические константы предлагаемых соединений представлены в табл. 1.
Соединения формулы I представляют собой кристаллические вещества белого цвета со слегка кремовым отт ёнком растворимые в органических растворителях (спирт, ацетон, диметилформамид, хлоруглеводорода), устойчивые при хранении.
Исследование противовоспалительной активности соединений формулы Т проводят на моделях острого экссу- дативного воспаления, в опытах на крысах-самцах (8-10 животных в группе j массой 100-120 г по влиянию на отек лапы, вызванный каррагенином. Онкометрическое измерение объема стопы проводили через 1, 2 и 3 ч после введения каррагенина.
Анальгетическое действие новых со единений изучали на мьшах самцах (8-10 животных в группе) массой 1820 г по влиянию на болевой эффект, вызванный внутрибрюшинньм введением уксусной кислоты и порог болевой чувствительности при тепловом par дражении (м%тод горячей пластянки).,
Во всех опытах новые соединения вводят внутрь за 1 ч до индукции воспаления при нанесении болевого раздражения в дозах, составляющих 0,1 ЛД(дозы, вызывающей гибель 50% животных), определяемой при том же способе введения на мышах-самцах мае сой 16-18 г. Расчет. ЛД цпроводят по известному методу..
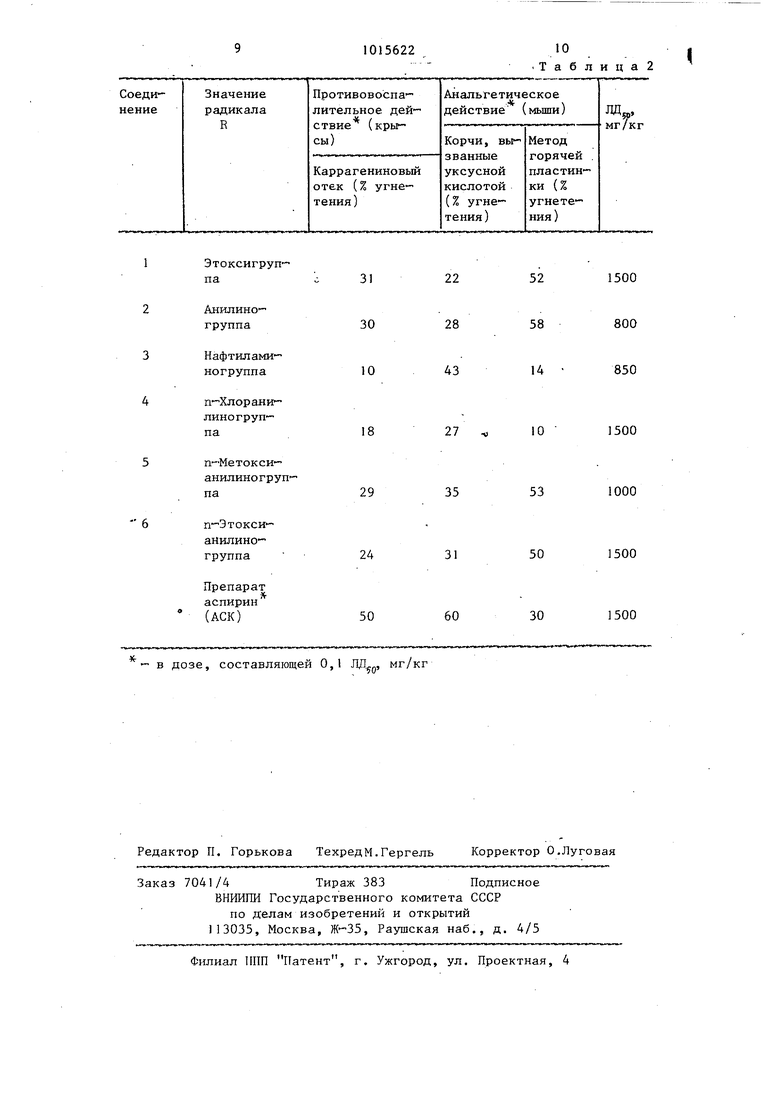
В табл. .2, приведенной ниже, представлены данные о противовоспалительной и анальгетической активности за- являемых соединений и токсичности (Jlfljjj) при введении внутрь в сравнении с известным противовоспалительным препаратом аспирином.Экспериментальные данные показьшают, что все новые соединения уменьшают выраженность каррагенинового отека, что свидетельствует о наличии у них противовоспалительной активности, которая наиболее выражена у соединений 1,2,5.Новые соединения наряду с противо- восп 1лительным (антиэкссудативным) действием обладают и аральгетической активностью.. Это свойство подтверждается тем, что соедийения I уменьшают выраженность корчей, вызванных уксусной кислотой и увеличивают порог болевой чувствительности при термическом раздражении. На модели корчей все новые соединения проявляют выраженное ай1альгетическое действие. Наиболее выражена эта способность У соединения 3, уменьшающего число корчей на 43%.
При термическом раздражении новые соединения 1,2,5, в 1,5-2 раза более активны, чем АСК, из них наиболее активным является соединение 2.
Новые соединения относятся к числу малотоксичных веществ и по токсичности сопоставимы с аспирином.
Из представленных результатов видно, что как по противовоспалительной, так и по анальгетической активности новые соединения приближаются к действию лекарственногр препарата, что является положительным эффектом дляНОВЫХ соединений, так как впервые в ряду окситиофенуксусных кислот найдены соединения, обладающие биологической активностью, а именно противовоспалительной и анальгетической
Этоксигруп
па
Анилино группа
Нафтилами ногруппа
П Хлорани-
линогруп
па
п-Метокси анилино группа
п Этокси анилиногруппа
Препарат
аспирин
(АСК)
дозе, составляющей 0,1 ДП.,.,, мг/кг
1500
52
22
800
28
58
14
43
850
1500
10
27
1000
53
35
1500
50
31
1500
30
60


1. 2-Замещенные 3-окси-5-метил- -4-тиофенуксусные кислоты формулы Т: нооснаС он ПГ НзС соя где R - этокси-, нафтиламино- или незамещенная, или замещенная в параположении хлором,метокси- илиэтоксигруппой анилиногруппа, обладающие противовоспалительной и анальгетической активностью. 2. Способ получения 2-замещенньгх-3-окси-5-метил-4-тиофенуксусных кислот формулы I ноосн с он где R - этокси-, нафтиламино- или незамещенная, или замещенная в пара-, положении хлором, метокси- или эток- сигруппой анилиногруппа, отличаю щ. ийся тем, что этиловый эфир 3-хлор-2-/карбэтокси- метил)кротоновой кислоты формулы Г Г СН -СООС Нб СНз-С С-СООС2Н5 SS С1 (Л подвергают взаимодействию с производным тиогликолевой кислоты формулы I 1 I HSCH 2COR где R имеет вьшеуказанные значения, в присутствии слабого основания в среде полярного растворителя при кипячении с последующим гидролизом поел лученного при этом этилового эфира 2-замещенной З-окси-5-метил-4-тиоа фенуксусной кислоты формулы ГУ ю 1с Нр,С ООСН2С ОН где R имеет вышеуказанные значения, водно- спиртовым раствором щелочи при кипячении, 3. Способ по п. 2, о-тлича- ю щ и и с я тем, что в качестве слабого основания используют углекислый калий или триэтиламин.
| Способ получения производных @ -тиофенуксусной кислоты | 1978 |
|
SU753091A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| К.В | |||
| Вацуро, Г.Л | |||
| Мищенко Именные реакции в органической химии, М., изд | |||
| Химия, 1976, с | |||
| Ручной прибор для загибания кромок листового металла | 1921 |
|
SU175A1 |
Авторы
Даты
1985-11-30—Публикация
1981-07-02—Подача