Предлагается усовершенствованный способ получения конденсированных имидазольных систем, а именно 2-гетерилзамещенных имидазо[4,5-b]пиридинов, имидазо[4,5-c]пиридинов и бензимидазолов, которые могут найти применение в медицине в качестве болеутоляющих, противовоспалительных или фунгистатических средств.
Известен способ получения 2-гетерилзамещенных бензимидазолов, заключающийся во взаимодействии о-фенилен- диамина с гетероциклическими кислотами или их производными в присутствии дегидратирующих средств.
Наиболее близким к описываемому способу по технической сущности является способ получения 2-гетерилзамещенных имидазо[4,5-l] пиридинов и имидазо[4,5-c] пиридинов, заключающийся в циклизации о-диаминопиридинов с гетероциклами, содержащими активную метильную группу, и элементной серой при температуре 170-210оС.
Недостатком указанных способов является использование в качестве исходных соединений о-диаминопиридинов или о-фенилендиамина, которые необходимо предварительно получать восстановлением соответствующих о-нитроаминопроизводных.
Целью изобретения является упрощение процесса с одновременным повышением выхода целевых продуктов, а также расширение их ассортимента.
Описываемый способ получения 2-гетерилзамещенных имидазо[4,5-l]пиридинов, имидазо[4,5-c]пиридинов и бензимидазолов общей формулы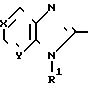 R где при Х=Y=CH R1=H, R=хинолил-2, пиридил-2, 6-метилпиридил-2, 5-этилпиридил-2;
R где при Х=Y=CH R1=H, R=хинолил-2, пиридил-2, 6-метилпиридил-2, 5-этилпиридил-2;
при Х=СН, Y=N R=хинолил-2, R1=H, CH3;
при Х=N, Y=CH
R1=H, R=хинолил-2 или
R1=CH3, R=5-этилпиридил-2, или
R1=бензил, R=пиридил-4, или
R1=бензил, R=5-этилпиридил-2, или
R1= фенил, R=хинолил-2, заключается в том, что о-нитроанилин или о-нитроаминопиридины нагревают с азотистым гетероциклом, содержащим активную метильную группу, в присутствии серы или смеси серы и сульфида натрия, взятого в стехиометрическом соотношении с нитроаминосоединением, при температуре 140-180оС.
Преимуществом данного способа является получение 2-гетерилзамещенных имидазо[4,5-b] пиридинов, имидазо[4,5-c]пи- ридинов и бензимидазолов из о-нитроаминопиридинов и о-фенимидиамина в одну стадию, минуя их восстановление в диаминопроизводные.
Также данный способ позволяет получать новые ранее не описанные в литературе соединения.
Общая методика получения 2-гетерилзамещенных имидазо[4,5-b]пиридинов, имидазо[4,5-c]пиридинов и бензимидазолов.
Нагревают смесь, состоящую из 0,01 моль о-нитроаминопиридина или о-нитроанилина, 0,012 моль гетероцикла с активной метильной группой, 0,03 г-ат серы и 0,01 моль сульфида натрия. Реакционную смесь охлаждают до комнатной температуры. Затвердевший плав тщательно смешивают с разбавленной (1:1) соляной кислотой (на 1 г плава 8-10 мл раствора кислоты), отфильтровывают избыток серы и смолистых веществ. Фильтрат осветляют углем и нейтрализуют аммиаком. Осадок отфильтровывают, сушат и перекристаллизовывают из растворителя.
П р и м е р 1. 2-(Хинолил-2')имидазо[4,5-b]пиридин получают при нагревании смеси, состоящей из 1,39 г (0,01 моль) 2-нитро-3-аминопиридина, 1,7 г (1,6 мл, 0,012 моль) хинальдина, 0,96 г (0,03 г-ат) серы и 2,4 г (0,01 моль) Na2S ˙ 9H2O, при температуре 140-155оС в течение 8 ч. Выход продукта составляет 2,33 г (95%), т.пл. 277оС.
П р и м е р 2. 2-(Хинолил-2')-3-метилимидазо[4,5-b]пиридин получают при нагревании смеси, состоящей из 1,57 г (0,01 моль) 3-нитро-2-метиламинопиридина, 1,7 г (1,6 мл, 0,012 моль) хинальдина, 0,93 г (0,03 г-ат) серы, 2,4 г (0,01 моль) кристаллического сульфида натрия, при температуре 140-155оС в течение 20 ч. Выход 1,82 г (70%), т.пл. 148-149оС (декан).
Найдено, N 21,45; 21,35.
C16H12N4.
Вычислено, N 21,52.
П р и м е р 3. 2-(Хинолил-2')имидазо[4,5-c]пиридин получают по описанной общей методике при нагревании смеси, состоящей из 1,39 г (0,01 моль) 3-нитро-4-аминопиридина, 1,7 г (1,6 мл, 0,012 моль) хинальдина, 0,96 г (0,03 г-ат) серы и 2,4 г (0,01 моль) девятиводного сульфида натрия, при температуре 140-155оС в течение 17 ч. Выход 2,14 г (87%), т.пл. 227-229оС.
П р и м е р 4. 2-(5'-Этилпиридил-2')-1-метилимидазо[4,5-c]пиридин получают при нагревании смеси, состоящей из 0,78 г (4,9 моль) 4-метиламино-3-нитропиридина, 0,65 г (5,3 ммоль) 2-метил-5-этилпиридина, 0,48 г (15 г-ат) серы и 1,2 г (5 ммоль) кристаллического сульфида натрия, при температуре 140-155оС в течение 25 ч. Выход 0,88 г (75%), т.пл. 112-113оС (октан).
Найдено, C 70,27; H 6,23; N 23,4.
C14H14N4.
Вычислено, C 70,56; H 5,92; N 23,51.
П р и м е р 5. 2-(Пиридил-4')-1-бензилимидазо[4,5-c]пиридин получают по описанной методике при нагревании смеси, состоящей из 1,15 г (5 ммоль) 3-нитро-4-бензиламинопиридина, 0,75 г (5,2 ммоль) γ-пиколина, 0,48 г (15 г-ат) серы и 1,2 г (5 ммоль) девятиводного сульфида натрия, при температуре 140-155оС в течение 30 ч. Выход 1,0 г (72%), т.пл. 137оС (декан).
Найдено, N 19,69; 19,36.
C18H14N4.
Вычислено, N 19,57.
П р и м е р 6. 2-(5'-Этилпиридил-2')-1-бензилимидазо[4,5-c]пиридин получают при нагревании смеси, состоящей из 1,15 г (5 ммоль) 3-нитро-4-бензиламинопиридина, 0,64 г 2-метил-5-этилпиридина, 0,48 г (15 г-ат) серы и 1,2 г (5 ммоль) Na2S ˙ 9H2O, при температуре 140-155оС в течение 24 ч. Выход 1,1 г (70%), т.пл. 97,5оС (декан).
Найдено, N 17,92; 18,22.
C20H18N4.
Вычислено, N 17,82.
П р и м е р 7. 2-(Хинолил-2')-1-фенилимидазо[4,5-c]пиридин получают при нагревании 0,35 г (1,6 ммоль) 3-нитро-4-фенил- аминопиридина, 0,26 г (1,8 ммоль) хинальдина, 0,154 г (4,8 г-ат) серы и 0,39 г (1,6 ммоль) Na2S ˙ 9H2O, при температуре 140-155оС в течение 24 ч. Выход 0,42 г (84%), т.пл. 167-168оС (декан).
Найдено, С 78,33; Н 4,49; N 17,44.
C21H14N4.
Вычислено, C 78,24; H 4,37; N 17,38.
П р и м е р 8. 2-(Хинолил-2')бензимидазол.
А. Смесь, состоящую из 1,43 г (0,01 моль) хинальдина, 1,75 г (0,012 моль) о-нитроанилина и 0,96 г (0,03 г-ат) серы, нагревают при температуре 170-180оС в течение 15 ч до прекращения выделения сероводорода. Реакционную смесь охлаждают, растворяют в 7-8 мл разбавленной соляной кислоты (1:1), отфильтровывают от не вступившей в реакцию серы, нейтрализуют аммиаком. Осадок отфильтровывают и кристаллизуют из диоксана. Выход 1,1 г (60%), т.пл. 220-222оС.
Б. Смесь, состоящую из 1,38 г (0,01 моль) о-нитроанилина, 1,75 г (0,012 моль) хинальдина, 0,96 г (0,03 г-ат) серы, 2,4 г (0,01 моль) Na2S ˙ 9H2O, нагревают при 140-155оС в течение 10 ч. Продукт выделяют аналогично примеру 8а. Выход 2,35 г (96%), т.пл. 220-221оС.
П р и м е р 9. 2-(6'-Метилпиридил-2')бензимидазол.
А. Получают аналогично примеру 8А из 1,38 г (0,01 моль) о-нитроанилина, 1,3 мл (0,012 моль) 2,6-лутидина и 0,96 г серы (0,03 г-ат). Выход продукта реакции 0,4 г (50%), т.пл. 221оС.
Б. Получают аналогично примеру 8Б из 1,38 г (0,01 моль) о-нитроанилина, 1,2 мл (0,012 моль) 2,6-лутидина, 0,96 г (0,03 г-ат) серы, 2,4 г (0,01 моль) Na2S ˙ 9H2O, при нагревании в течение 15 ч при 145-155оС. Выход продукта реакции 1,89 г (90%), т.пл. 222-223оС (бензол).
П р и м е р 10. 2-(Пиридил-2')бензимидазол.
Смесь, состоящую из 1,38 г (0,01 моль) о-нитроанилина, 1,2 г (0,012 моль) γ-пиколина, 0,96 г (0,03 г-ат) серы, 2,4 г (0,01 моль) Na2S ˙ 9H2O, нагревают в течение 15 ч при температуре 140-155оС. Выход продукта реакции 1,75 г (90%), т.пл. 221-222оС (бензол).
П р и м е р 11. 2-(5'-Этилпиридил-2')бензимидазол.
Смесь, состоящую из 1,38 г (0,01 моль) о-нитроанилина, 1,45 г (0,012 моль) 2-метил-5-этилпиридина, 0,96 г (0,03 г-ат) серы, 2,4 г (0,01 моль) Na2S ˙ 9H2O, нагревают в течение 18 ч при температуре 140-155оС. Выход продукта реакции 1,9 г (85%), т.пл. 172оС (бензол).
Таким образом, предложенный способ позволяет получать 2-гетерилзамещенные имидазо[4,5-b]пиридины, имидазо[4,5-c]пиридины и бензимидазолы с высокими выходами (60-90%) из о-нитроанилина или о-нитроаминопиридинов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Стирильные производные имидазо(4,5- @ )пиридиний иодида,обладающие фунгицидной активностью | 1979 |
|
SU813921A1 |
| Имидазо(4,5-7,8)имидазо (1,2-а)-пиридины | 1980 |
|
SU891671A1 |
| Производные имидазо(4,5- @ ) индолов | 1982 |
|
SU1068439A1 |
| Способ получения имидазо (4,5- )пиридинов или их солей | 1975 |
|
SU634673A3 |
| Способ получения N-арилзамещенных 3H-имидазо[4,5-b]пиридинов | 2016 |
|
RU2642456C2 |
| Способ синтеза пиридо[1,2-а]имидазо[4,5-f]бензимидазола и его производных | 2017 |
|
RU2645917C1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА И ИМИДАЗО[4,5-с]ПИРИДИНА, В КАЧЕСТВЕ АНТАГОНИСТА ПУТИ HEDGEHOG | 2010 |
|
RU2533825C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ИМИДАЗО/4,5-B/ПИРИДИН-2-ОНОВ | 1980 |
|
SU921235A1 |
| ТРИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И ПРОИЗВОДНЫЕ ТЕТРАГИДРОХИНОЛИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2023712C1 |
| Способ получения имидазо /4,5- / или/4,5- с/ пиридина или их производных | 1977 |
|
SU717055A1 |
СПОСОБ ПОЛУЧЕНИЯ 2-ГЕТЕРИЛЗАМЕЩЕННЫХ ИМИДАЗО[4,5-B]ПИРИДИНОВ ИЛИ ИМИДАЗО [4,5-C]ПИРИДИНОВ, ИЛИ БЕНЗИМИДАЗОЛОВ общей формулы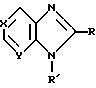
где при X Y CH и R′= H R хинолил-2, пиридил-2, 6-метилпиридил-2, 5-этилпиридил-2;
при X CH и Y N R-хинолил-2, R′= H, CH3;
при X N и Y CH R′= H, хинолил-2;
R′= CH3, R 5-этилпиридил-2;
R′= бензил, R пиридил-4;
R′= бензил, R 5-этилпиридил-2;
R′= фенил, R хинолил-2,
взаимодействием производного аминосоединения с азотистым гетероциклом, содержащим метильную группу R CH3, где R имеет указанные значения, и элементной серой при повышенной температуре, отличающийся тем, что, с целью упрощения процесса, повышения выхода и расширения ассортимента целевых продуктов, в качестве производного аминосоединения используют о-нитроаминопиридин или о-нитроанилин и процесс ведут при температуре 140 - 180oС.
| Способ получения 2-гетерилзамещенного имидазо(4,5-в)пиридина или имидазо(4,5-с)пиридина | 1975 |
|
SU545646A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-07-25—Публикация
1981-02-24—Подача