СХ) 4
Изобретение относится к новому способу получения новых биологически активных соединений - производных трипептидов, которые могут найти при менение в медицине.
В синтезе пептидов мироко исполь- 5 эугот при конденсации N-защищенных аминокислот и пептидных фрагментов карбодиигдадный метод и метод активированных эфиров Cl с последук4цим удалением блокирующих групп обработ- 10 кой фтористоводородной кислотой в : присутствии анизола при 0°С защищен-, ной по аминогруппе пептидной цепи Czl.
Цель изобретения - получение новых производных трипептидов, облада1д-15 цщх интересными фармакологическими свойстваг-га.
Поставленная цель достигается согласно способу получения производных ±рипептидов общей формулы20
Н-Д-Х-Фен-Арг-У где.
X - Про, Фен}
У - ,ORz,
R. - Меразветвленный или развет- с вленный алкил или циклогексил;
водород, циклогексил, неразветвленный или разветвленный алкил,
заключакщийся в том, что С-защищент ные производные аминокислоты или пеп- тида конденсируют в растворе в любой последовательности с активированными сложными эфирами N-защищенных аминокислот или с N1-защищенными амино- i кислотами и дициклогексилкарбодиими- 35 дом в качестве конденсирунвдего агента с последу5ащим удалением защитных групп обработкой фтористоводородной числотой и выделением конечных соединений с помо11ью. ионообменной хромато-40 -Трафии.
Сокращения, применяемые в описании:
Аминокислоты при отсутствии заний на обратное, речь идет о фигурации) : Apr - аргинин
Фен - фенилаланин
Про - пролин
АсОН - уксусная кислота Бок - трет-бутилоксикарбонил Кбо - карбобензокси ДИКИ- дициклогексилкарбодиинид даф - диметилформамид ЛНСО - диметилсульфоксид триэтиламин ЭтОАс - этилсщетат этОН - этанол
НЕТ - М-гидроксибензотриазол МеОН - метанол ОпНФ- п-нитрофенокси и - ПрОН - изопропиловый спирт ТФА - трифторуксусная кислота тех - тонйослойная хроматографи
Тонкослойная хроматография Для проведения анализов методом тонкослойной хроматографии используются готовые к употреблению стеклянньте пластинки с нанесенным на них силикагелем (Фирма Мерк) . В качестве растворителя используются следующие смеси (соотношения даны в объемных единицах :
А - н-бутанол : АсОН : вода (3:2:1 Р - хлороформ : МеОН (9:1) Ра - хлороформ : МеОН : АсОН (l7:2:3 Pag . - хлороформ : МеОН : АсОН : НО
(34:4:У:2)
М - н-бутанол : АсОН : : пири. дин (30.)
После окончания хроматографического разделения стеклянную пластинку исследуют в УФ-области (254 нм,. после чего обрабатывают ее хлор/0-толуидиновым реагентом согласно извес ныгл способа -. Конечным результатом проведения хроматографического разделения являются значения .
Пример 1 . Н-Д-Про-Фен-Арг-1 -0-гептил2НС1, мол.вес 589,6,
1а; Кбо-Фен-Арг(М02)-ОМе, мол.вес; 514,5
27 г (о, 10 моль) H-Apr(NO.i.-OMei. IHCl растворяют в 4 t/in диметилформамида и нейтрализуют.лри охлаждении 18 мл тризтилагдана..Получающийся при этом нс1 отделяют фильтрованием и добавляют к реакционной смеси 42 г (0,1и5 гюль) Кбо-Фен-ОпНФ. Ре акционную смесь оставляют на ночь при перемешивании, после чего из нее отгоняют в вакууме растворитель с по- . лучением маслообразного остатка, который растворяют в 500 мл этилацетата. Фазу в этилацетате промывают последовательно 2%-ным раствором МаН(Х) в воде, водой разбавленным раствором соляной кислоты в воде и водой. После сушки над сульфатом натрия из смеси отгоняют этилацетат до объема около 200 мл и осаждают продукт вве дением эфира. Кристаллический осадок промывают эфиром и сушат. В соответствии с данным тех получается чистое вещество. .
Выход: 37,6 г (73%) вещества 1а.
тех: R.i 0.52 (Р1) ib. Кбо-Фе Арг(М04.)-ОН, Мол. вес Ь00,5.
3,1 г .С6,и ммоль) ведества 1а . растворяют в примерно 150 мп мета-нола и добавляют к полученному раствору 7,3 ммоль (7,3 мл/л 1 М WaOH в воде). епустя примерно 4 ч из реакционной смеси отгоняют в вакууме растворитель, растворяют остаток в не-: большом количестве воды и дважды промывают этилацетатом. Водную фазу подкисляют не1 до рН 2 и экстрагируют образующийся при этом Кбо-Феь -Apr (МО,г)-он тремя порциями этилацетата. Фазу в зтилацетате прогя шают 10%-ным раствором хлористого натрия в воде, сушат над сульфатом натрия и отгоняют растворитель досуха. Образугациеся при этом кристаллы сушат после выщелачивания эфиром. Полученный продукт в соответствии с данными тех не содержит одимесей.
Выход:-2,8б (95% ) продукта Ib.
тех: ,14(FQ)
1с. Кбо-Фен-Арг (И(0 0 1 ептил, мол.йес Ь98,7.
0,60. мл перегнан-ного SOCl ДО) бавляют к 10 мл Гггептанола в условиях, исключэкядах проникновение влаги и при охлаждении смеси на .бане со льдом. После перемешивания реакционной, смеем в течение 1 ч при комнат;ной температуре добавляют к ней .1,00 г (2,0 ммоль) вещейхва 1б, Реакцию продолжают еще в течение 1ч,, по. его реакционная смесь загустевает белой массы. Эту массу разбавляет эфиром и образующиеся при этом кристаллы отфильтровывают. Кристаллическую массу растворяют в метаноле и осалсдают водой (удаляя образующуюся НС1). Полученные после осаждения кристаллы отфильтровывают. В соответствии с данными ТСХ получают чистый гептиловнй эфир.
Выход: 962 мг (аО%) вещества 1с.
ТСХ:, «г60 (el) .
id . Бок-Д-Про-,Фен-Арг(К02)-0-t тгёптИЛ мол.вес 661,8.
60U мг (1,0 ммоль) вещества 1с растворяют в 2 мл уксусной кислоты и добавляют к. раствору 1,4 мл 5,6 м НВг в уксусной кислоте. Реакционную сзмесь выливают в около 100 мл сухого эфира и сушат в вакууме над .аОН. Полученную соль броглистоводородной кислоты и Н-фен-Лрг ( WOj)-и-гептила : растворяют в 2 /lл диметилформамида и нейтрализуют при пониженной температуре () триэтиламином до появления основной реакции. Полученныйпри этом Эт.,НВг отфильтровывают. К .реакционной смеси добавляют 215иг (ifО ммоль) Вок-Д-Про-ОН и 135мл .,1,0 мг-юль) НЕТ, а .аатем при понижениой тегшературе - 250 мг (около 1, ммоль) дициклогексилкарбодиш/шда. .Реакция заканчивается в течение ночи, после чего отфильтровывают обра-, зующийся ДНУ (после охлаждения реакционной смеси) , и из указанной реакционной смеси отгоняют в вакууме растворитель с образованиеммаслообразногсГ остатка. Маслообразный остаток смешивают с неболыиим количеством раствора NaHCOj в воде и растворяют полученную массу в нёбольшом количестве метанола, после чего хроматографируют ее на колонке, заполненной Сефадексом ЛН-20 в метаноле с использованием метанола в качестве элюента. Фракцию, содержащую
чистое вещество 1(3 растворяют в воде и метаноле и отгоняют растворители в вакууме. 1с1 осаждается в виде тяжелого порошка, который собирают М сушат в-вакууме. . .
Выход: 570 мг ( 86) вещества id. .
ТСХ: R 0,65 Ра , 0,Ь2 Р1 .
1. Н-Д-Про-Фен-Арг-О-гептил2НС1, мол. 58У,6. .
Осуществляют снятие защитных группу 400 мг (0,6 млюль) вещества id в .
0 результате воздействия 30 г/ш фторис- товодородной кислоты -при ос в тече,ние часа в присутствии 0,4 мл анизо- ла. После отгонки растворителя в ва-. кууме продукт растворяют в 20 мл .
5 2%-ной уксусной кислоты в воде и
промувают несколько раз небольшими. количествами эфира. Водную фазу хроматографируют на колонке, заполненной Сефадексом Г-15 в уксус0ной кислоте с использованием той же среды в качестве элюента. При этом i получают фракцию, содержащую aбcoлю1 но чистое вещество .--Выход: 318 мг (sS) продукта 1
5 ,4 (с 0,7, 50%-ая уксусная кислота).
ТСХ: R 0,27 (А), только одно пятно.
Анализ на ам1-{нокислоты: Apr 1,00{ .Фен 1,025 Про 0,9У..
Пример 2. Н-Д-Про-Фен-Арг-гептил 2НС1, мол.вес 5ЭЙ,6.
2а. Кбо-Фен-Арг(МО -МН-гептил, i мол.вес Ь97,7..
5
1,0 г (2,0 ммоль) Кбо-Фен-Арг(МО)-ОН (16) и 0,27 мг (2,0 ммоль; HRT . растворяют ,0 tvi диметилформамида, после чего добавляют к полученному ; . раствору при о У1аждении на бане со льдом 0.50 г {около 2,4 ммоль) логексйлкарбодиимида. Спустя 1ч к реакционной смеси добавляют 0,33 мл (2,2 ммоль) гептиламина, после чего реакционную очесь оставляют при перемешивании на ночь и отфильтровыва5ют образующийся ДСУ, а затем отгоняют растворители до образования маслообразного остатка. Указанный маслообразный остаток обрабатывают водой, 2%-ным раствором VIаНСО, водой,
0 2%-ным раствором КН5О, водой, и в
коице чистой водой. Полученную массу кристаллизуют из смеси метанола с водой. По данным тех-в ней содержится незначительная примесь побочного
5
jпродукта с Rjf 0,54 (Ра) наряду с главным продуктом, для которого Rr 0,58 ( Ра. .
.Выход: 1,13 г (94%) вер ества 2а. 2b. Бок-Д-Про-Фен-АргЧ О -Мн-геп0тил, мол.вес 660,8.
Проводят удаление защитных групп у 1,0 г (1,67 мглоль) cetiecTBa 2а в результате обработки 4 мл уксусной кислоты и 2,8 мл HBf согласно приме5 РУ 1с. По данным ТСХ следует, что
соль ёромистоводородной кислотн и Н-Фен-Лрг-(м5.1.)МИ-гептила содержитнаряду с основным продуктом, тлеющим R,-U,61 (Рп), также .небольшое количество ПОГШЧНОГО ПрОДУКТа с R.J;
0,72 fPa). Соль бромистоводородной кислоты подвергается ионообмену на колонке, заполненной ОДЕ-25 в хлоридной фо15г/ е в смеси SK}.% этанола и 10% воды, с использованиемтой же средьз в качестве элюента. Фракция, содержащая в.основном главный- продукт в форме хлорида ртделяется в коли- . честве 496 мг (ii,Q ммоль),, после чбго полученный; продукт растворяют в 2 мл диметилформамида и нейтрализуют 0,15 мл триэтиламина. Затем.к полученному .таким способом раствору, до- . бавляют 215 мг (1,0.ммоль;) Бок-Д-Про ОН, 135 мг (1,0 ммоль) НБТ и при охлаждении - 2ЬО мг (около 1,2 ммоль) дициклогексилкарбодиимида. Реакцию продолжают в течение 20 ч, после чего реакционную .смесь фильтруют и отгоняют растворитель. в вакууме е образоэанием маслообразной масси, ко- . тсзруго обрабатывают 2.-ным раствором j aHCOi в воде и чистой водой. Полу.ченную Маасу растворятот- в метаноле и, хрокатографируют на колонке, запоЛненной Сефадексом ЛН-20 в метаноле с использованием метанола в качесгве элюента. Из фракции,, содержащ ;й чис1ое вешеств.о 2.1), отгоняют растворитель в вакуут е и выщелачивают остаток водой. Полученную кристаллическую массу суыат в вакууме,- .
.Выход: 457 мг. (6У%) вещества 2Ъ.
тех: R 0,35 (fl) , ..
2. Н Д--Про--Фен-Лрг-МН-гептиЛ2НС1 MOvi. вес 588,6.
Для1 300 мг соединения 2bпроводят удаление .защитных групп и б истку согласно примеру 1.
В1;1ход: 263 мг (98%) продукта 2. (C.D,6, уксусная кислота),
ТСХ: 0 ,25 (,Л), -только одно пятн
Анализ на аминокислоты: Лрг 1,00; Фен 0,S7; Про 0,98.
При и ер 2. Н-Д-Про-Фен-Арг-МН,-2НС1, мол. вес- 490,5. . .
За. Бок-Д-Про-Фен-ОМе, мол.вес 376,4,
4,2 .г (ig, 5 ммоль) Бок-Д-Про-ОН и 2,7 гЧ2о,0 ммоль) НБТ растворяют в 50 глл диметклсульфоксида и добёвляют к полученному раствору-при перемешивании и охлаждении 4,4 г (около 21 ммоль) дициклогексилкарбодиимида. К реакционной смеси добавляют раствор 4,3 г (20,0 ммоль) Н-Фе.н-ОМе-НС1 в 50 мл диметилформамида, предварительМО нейтрализованного при охлаждении / добавлением 2,8 мл (20,0цмоль) три-: зтиламина с последующим фильтрованием. Реакционную смесь оставляют йа ночь и отфильтровывают образующийся i
ДВДУ. Растворитель отгоняют досуха с . получением из реакционной смеси маслообразного остатка, котордлй растворяют в 300 /ш .зтилацетата.. Раствор в
этилацетате последовательно промывают 2%-ным водным раст-вором Я.аНСОз,
водой, 2%-ным водным раствором KHSQj. и наконец водой., по.слечего cyitiaT над сульфатом кальция..Раствор в
этилацетате подвергают вакуумной разгонке досуха с получением кристаллической массы, которую обрабатывай петролейным эфиром,- фильтруют и промывают петролейным эФир.ом. Полу ченную кристаллическую массу . сушат в, вакууме.- .- . . . .Выход: 5,Ь г (75%) вещества За. 0,53 Pl) . 3b. Бок-Д-Про-Фей-рНу-мбл. вес
362,4. . .. . . -. :
4,5 г (12,0 ммоль) вещества За рас.тнорйют в 50мл МеОН и добавляют к полученному раствору 15 мл I -н-. NaOH 5 ммоль ). После перейёшивания рёакционной смеси при кЬмна1тной .температуре в те.чение 2-3 ч растворитель отгоняют досуха., а полученщлй остаток растворяют в 10Q мл воды, и дважды промывают 50 мл-эфира, после чего подкисляют водную фазу KHSO до рН. 3. После перемешивания при 0°С в течение 30 мин реакционной смеси образу- Ю1-1ИЙСЯ в ней осадок отфи-льтронавают и прогнивают небольшим количеством холодной воды, после чего cj/шат указанный осадок в вакууме.
Выход: 3,3 г (74%) соединения 6,
T.CX:R 0,й1 (Pag). .
3с/ Бок-Д-Про-Фен-Л-рг (N() -NH., мол.вес 562,6. ;
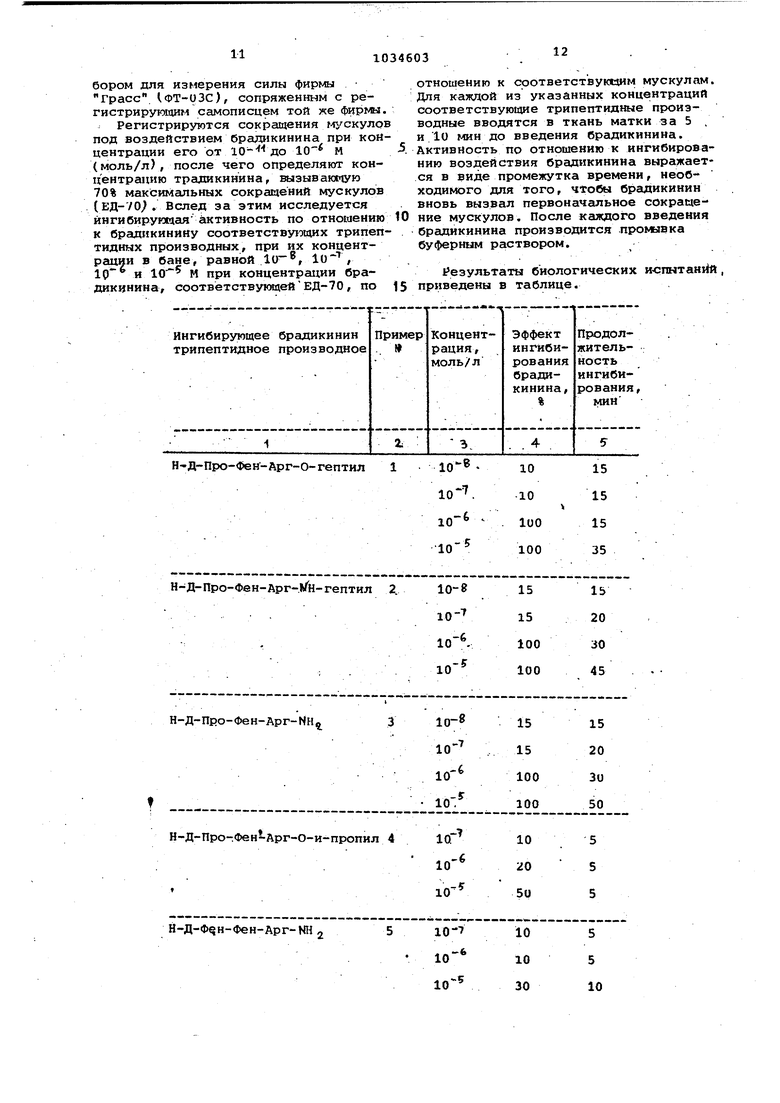
0,65 г (1,8 ммоль) соединения 36 и 0,26 г (l,y ммоль) НБТ растворяют в 10 мл диметилформамида и добавляют к полученному раствору при перемег-швании и охлаждении 0,38 г (около 1,8 мг/1оль) дициклогексилкарбодиимида, К реакционной смеси добавляют раствор 0,6 г (2 ммоль) H-Apr(NO,j,)-HH2; НВг в 10 мл диметилформамида (который следует нагреть и вновь охладить перед нейтрализацией), который предварительно нейтрализуют при охлаждении 0,3 мл (2,2 ммоль) тризтиламина, и который затем фильтруют. Р.еакционную смесь оставляют на ночь и отфильтровывают затем образующийся ДНУ. Из реакционной смеси отгоняют растворитель с образованием маслообразного остатка, который растворяют в кипящем этилацетате ( 100 мл. При охлаждении образуется осадок, который прог-мвают зтилацетатом и эфиром. Затем указанный осадок (около 0,5 г) растворяют. в большом количестве этилацетата и про№авают последовательно 2%-ным водным раствором NaHCO, водой, вод-; Н1ЛМ 2%-ным раствором KHQ04 и снова водой. Раствор в зтилацетате Ьушат .над сульфатом натрия и затем отг6няют растворитель в вакууме досуха. . Выход: 480 мг 48%) .вещества 3с. тех: R 0,73 ( Pafe) . 3. Н-Д-Про-.Фен-Лрг-МН2 -2НС1, мол. вес 490,5. в 160,0 мл (о,28 мoль) соединени 3с производят снятие защитных групп в результате -взаимодействия с 10 мл HF при 0°С в течение 50 мин в присут ствии 0,3 мл .анизола. После от.гонки растворителя в вакууме остаток раст. воря.ют в примерно 5 мл смеси 50% этанола и 50% воды; и проводят ионный обмен на колонке, содержащей ОАЕ-2 в форме хлорида в смеси 50% этанола и 50% воды с использованием той же смеси для- элюирования. Из фракции, содержащей соединение 3, отгоняют в вакууме растворитель, растворяют остаток в около 5 мл метанола и хрома.тографируют раствор на колонке напол V ненной Сафддексом ЛН-20 в метаноле с использованием метанола в качестве среды -для элюирования., Фракцию,. содержагтую соединение 3, csraaT при 3аморажива«ИИ. Внход: 100 мг (71%). соединения 3 ; tot3|. 4-12,1 (С 0,5,метанол/, ТСХ: R..g 0,34 (. М j, только одно , пятно. Анализ на аьданокислоты: Apr 100, Фен 1,01; ПРО . .. П р-и м е р 4. Н-Д-Прол;Фен-Арг -О-и-проп.и5Г 2НС1, мол. вес 533,5. .-. .4. Н-АргЛ С)-о-и-пропил2НС1, 1«эл.вес 297,8.. г.(25 гфюль) . .) раствopя т в 250 мл изопррпанола и про-ВОДЯТ этерификацию повторной обрабс кой сухим газообразным НС1 согласна, известным способам. Когда реакция заканчивается, из реакционной смеси отгьняпт досуха в вакууме все Летучие компонент.ы. Полученный сложный эфир (4а) кристаллизуют в результате растворения массы, полученной после . отгонки растворителя,- в небольшом ко личестве горячего из-опропилового спирта и осаждают при добавлении сухого эфира при охлаждении раствори теля. Отделенные кристаллы трижды промыва - сухим эфиром.. Выход: 5,8 г ) соединения 4а. . Т.пл.: 179 - 181С. - . .. Бок-Д-Про-Фен-Арг( -О-и-пропил, мол.вес- 605,7. Способ, реагенты и количества их полностью аналогичны тем, которые ис пользуются в примере 3с, однако вмес те H-Aprl.NOa.)-Nir НВг используют 0,60 г 2,0 ммоль) . соединения 4а. Выход: 440 мг U0%) соединения 46 тех: Rj 0,41 PI .., .4. Н-Д-Про-.Фен-Арг-О-и-пропил, мол.вес 533,5. В ЗиО мг (0,50 ммбль соединения :4Ъ осуществляют удаление защитных зтрупп в результате вбздействййНР-в, присутствии анизола согласно способу 1. Продукт подвергается очистке и взаимодействию с ионообменной смолой аналогично способу 1. Вгтход: 180 мг (68%) соединения 4. ,9 (С 0,5-50.%-ая уксусная кислота). тех: RJ 0,21(А), только ОДНО пятно. Анализ на аминокислоты. Apr 1,0(Г, Фен 1,00 П.ро 0,98. Пример 5. Н-Д-Фен-Фвн-Арг-NH j -2Heij мол.вес 5.40,5.. 5а. Кбо-Д-Фен Фен-ОМе, мол. вес 460 ,.5.. епособ, реагенты и их количества полностью аналогичны тем, котьрые используются в примете . .однако вместо Бок-Д-Про-ОН используют 6,0 г (;20 ммоль) Кбо-Д-Фен-Он. Выход: 6,2 Дб7%). соединения .5а. тех: R 0,60 .(PlJ. iSb. Кбо-Д-Фен-Фен-ОН,мол. вес 446 ,5. 6,0 г (13,0 №юль) соединения 5а гидролизуют НаОН соглаеао способу 36. Выход; 4-,9.,г (84%) соединения зЬ. . тех: RC 0,85 (Ра) . 5с. К&о-Д-Фен-Фен-Лрг (MOg)-HH,j, мол.вес 646/7. . елособ, реагенты и их количества полностью аналогичны тем, используются в примере 3с, за исклю чением того, что вместо соединения 31з испбльзуют соединение. 5Ь в количёстве 0,98 г 42,0 мноль). Выход: 505 мг (39%) соединения 5с тех: Rj 0,80 (.Ра). 5. Н-Д-Феи-Фен-Арг-«%:,2Не1, мол.вес 540,5. -Для 400 мг (0,62 ммоль) соединения 5с проводят снятие защитных rpyrtn очистку и обработку , ионообменной смолой согласно примеру 1.. Выход: 296 г (88%) соединения 1. ,4. (е а,5,,метанол). , тех: R 0,37 (.М), только ОДНО пятно. Анализ на аминокислоты: Apr 1,0о; Фен 1,97. При мер 6. Н-Д-Фен-Фен-Арг-Нн-гептил-2Не1/. мол.вес 638,7. 6а. Кбо-Д-Фен-Фен-Арг(К10,2.)-NH-renтил, мол.вес 744,9. епособ, реагенты и их количества полностью аналогичны тем, которые. использованы в приккре 2Ь,,. за исклюением того, что вместо Бок-Д-Про-ОН используют Кбо-Д-Фен-ОН. Выход: 470 мг (бЗ%) соединения 6а. тех: R.-0,42 (Pi). . 6. Н-Д-Фен-Фен-Арг-ЫН-тептил 2Не1, ол.вес 638,/. Для 300 г (о,40 ммоль) соединения 6а проводят снятие защитных групп. очистг у и обработку ионообменной смо лой согласно примеру 1.. Выход: 1 /6 М-Г (59%) соединения (С 0,5, Ь0%-ая уксусная, кислота). тех: 0,2В (А), только одно пятно. Анализ на аминокислоты: Лрг 1,00; Фен 1,У8. .Пример 7, Н-Д-Про-Фен-Лрг-WH-лаУрилv2HCl , мол.вес 658,7. 7. Кбо-Фен-Арг{М02,)- Н-лаурил, мол.вес 667,8. Способ, реагенты и их количество полностью аналогичны тем, которые использованы в примере 2а, за исключением того, что вместо гептиламина качестве атшна используют 0,51 г (2,2 гулопь) лауриламина, Выход: 1,17 г (88%) соединения 7а TCX:R 0,60 Ра) ; гомогенная хро матограмма. (7Ь.Бок-Д-Прр-Фен-Арг(Ы01) - Ч 1-лаурил, мол. вес. 7 30 ,9. Способ, реагенты и их количество аналогичны тем, которые использованы .в примере 2Ь, за- исключением того, что вместо 1,67 ммоль вещества 2Ь вместо 1,67 Г/1МОЛЯ вещества 2а, использованного в примере 26, употреблено 0,Ь7 г (1,0 1®-1оль) вещества 7а в качестве исходного пептида. Кроме того, соль НВг и Н-Фен-АргСНОй.) -МН-лаурила может быть использована без дополдительной очистки с использованием ионообменной смолн. Выход: 5й5 мг (80%) аещества7Ь. тех: Pv 0,39 IPl). 7. Н-Д-Про-Фен-Лрг Н-лаурил-2Не1 мол.вес 65а,7. Для ЗОи мг (0,41 ммоль) вещества 7Ь проводят удаление загдатных групп, очистку и обработку ионообмен ной смолой согласно способу, описанному в 1. Выход: ii30 мг (85%) соединения 7 ,4 (е и, 5, уксусная кислота) . ТСХ: R, 0,27 (А), только одно пятно. Анализ на а1У инокислоты: Apr 1,00 Фен 0,98} Про 0,99. Пример 8. Н-Д Фен Фен-Арг- Н-и-пропил, мол.вес 541,6. Способ, реагенты и их количества аналогичны примеру 2а, за исключением того, что в качестве амина вместо петиламина используют 130 мг (2,2 мoль) изопропилат-лина. Выход: 0,95 г 188%) соединения 8а ТСХ: ЯР 0,51 СРаЬ только одно пятно. 8б. Кбо-Д-Фен-Фен-Арг(НОа) -Кн-и-пропил, мол,вес 688,8. Способ, реагенты и их количества, аналогичны примеру 6а, за исклйчением того, что в качестве защ1оденнЬго дипептида используют вместо соедивения 2а 0,54 г (1,0 ) соединения 8а. , Выход: 470 мг (68%) соединения 8Ь. ТСХ: Rj- 0,38 (PI) . 8.П-Д-Фен-Оен-Арг- Н-и-пропил 2НС1, мол.вес 582,6. „. Для 300 мг (0,44 лмoль}J соединения 8Ь проводят удаление защитных групп, очистку и обработку ионообменной смолой согласно примеру 1. Выхода 205 г (80%) соединения 8. ,7 (с 0,5, металол . . ТСХ: ,23 (А), только oднoi пятно. Анализ на аминокислоты: Лрг 1,00, Фен 1,97. . ,Пример 9. Н-Д-Фен-Фен-Арг-Т Н-циклогексил-2нС1,, 622,7 Способ, реагенты и их количества аналогичны примеру 2а, за исключением того, что в качестве амина вместо гептилагдана исгюльзуют 218мг (2,2 ммоль) цикло1; ексила11ина. Выход: 0,90 г t77%) соединения 9а ТСХ: ,бО (Ра), только одно i пятно. l9b. Кбо-Л-Фен-Фен-Арг fwOa)- Н-цик-, логексил, мол. вес 728,8. Споспб, реагенты и их количества. аналогичны примеру 6а, за исключением того, что в качестве защищенного дипептида используют вместо соединения 2а.0,58 г (1,0 ммоль) соединения 9а.. .Выход: 520 мг (71 %) Соединения 9Ь) ТСХ: R. 0,49 (Pi) . 9.Н-Д-Фен-Фён-Арг-МН-циклогексил i 2HCi f мол. вес 622,7. Для 300 1ЛГ 1.0,41 ммоль) соединения 96 проводят удаление защитных групп, очистку и обработ,ку ионообмейной смолой согласно примеру 1.. Выход: 1 Зь мг (72%) соединения 9, ,2 1с 0,5, метанол) тех: R 0 ,28 (А ). Анализ на аминЪкцслоты: Apr 1,00 Фен 1,96. Проведены биологические испытания предлагаег тх соединений. Активность соединений по отношению к ингибиррванию брадикинина изучалась на изолированной матке крыс. За 12-15 ч до проведения эксперимента крысам вводилось подкожно 0,2 мг/кг диэтилстилбэстрола. Мускулы матки, разрезанные в продольном направлении на две части, помещают в баню для гладких мускулов, заполненную буферным раствором по Де-Жалону, в которую пропускают карбогенизированный газ (5% двуокиси углерода, 95% кислорода) для окисления. Температура поддерживается на уровне 35°С. Затем на мускул накладывается нагрузка для его растяжения, соответствугачая 0,5г. Величина напряжения измеряется прибором для измерения силы фирмы Грасс 1,ФТ-оЗС), сопряженннм с регистрирукяцим самописцем той же фирмл. Регистрируются сокращения (скулов под воздействием брадикинина при концентрации его от 10- до 10 М (моль/л), после чего определяют концентрацию традикинина, вызываюгтую 70% максимальных сокращений мускулов (ЕД-70. Вслед за этим исследуется йнгибируий1с1Яактивность по отношению к брадикинину соответствукедих трипептидных производных, при их концентрации в бане, равной 10, Ю , 10 и Ю М при концентрации брадикинина, соответствующейЕД-70, по
отношению к срответствугадим мускулам. Для каждой из указанных концентраций соответствую1аде трипептидные производные вводятся в ткань матки за 5 . и 1U мин до введения брадикинина. Активность по отношению к ингибированию воздействия брадикинина выражается в виде промежутка времени, необходимого для того, чтобы бргщикинин вновь вызвал первоначальное сокращение мускулов. После каждого введения брадикинина производится .промлвка буферным раствором.
Результаты биологических и-спытанйй приведены в таблице.
Продолжение таблицы





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пептидов или их солей | 1975 |
|
SU957762A3 |
| Способ получения трипептидов или их солей | 1973 |
|
SU671721A3 |
| Способ получения пептидов | 1976 |
|
SU673165A3 |
| Способ получения пептидов | 1985 |
|
SU1433415A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ 13,14-ДИГИДРО-15(R)-17-ФЕНИЛ-18,19,20-ТРИНОР PGF2 13,14-ДИГИДРО-15(R)-17-ФЕНИЛ-18,19,20-ТРИНОР PGF2 СОЕДИНЕНИЯ. | 1993 |
|
RU2099325C1 |
| Способ получения пептидов или их солей | 1976 |
|
SU700060A3 |
| Способ определения активности протеаз серина | 1977 |
|
SU736889A3 |
| Способ определения тромбина, плазмина, трипсина и тромбиноподобных ферментов в биологических жидкостях | 1977 |
|
SU1099839A3 |
| Способ получения пептидов или их солей или амидов или сложных бензиловых эфиров | 1973 |
|
SU651691A3 |
| Способ получения трипептидов | 1980 |
|
SU1277904A3 |
СПОСОБ ПО.ЛУЧЕНИЯ ПРОИЗ«Э НЫХ ТРИПЕПТИДОБ общей формулы Н-Д-Х-Фен-Арг-У, где X - Про, Фен; S - ORi, VJMRa; ) - неразветвленный или разветвленный С -С- -алкил или циклогексил; . водород, циклогексил, неразветвлентгый или разветвленный Ci,-.C. -алкил, отличающийся тем-, что С-заадипённые производные аминокислоты или пептиды конденсируют в растворе в любой последовательности с активированными cлoжны ш эфирагш N-защищенных аминокислотили с N-защиценныгда аминокислотш-ш и дициклогексилкарбодиимидом в качестве конденсирунадего агента с последующим удалением защитных групп обработкой фтористоводородной кислотой и выделением конечных соединений с помощью ионообСО менной хроматографии.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Э.Шредер, К.Любке Йептидал М | |||
| ,.Мир , 1967, ч.1, с | |||
| Способ получения бензидиновых оснований | 1921 |
|
SU116A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Там же, с | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
Авторы
Даты
1983-08-07—Публикация
1980-08-21—Подача