о со
Изобретение относится к синте у новых химических соединений, а именно Н-акрилоилдифениламинов общей формулы
о-С- н-йНг
где X -н, -СН,
которые могут быть использованы для синтеза полимеров, находящих применение при получении фоточувствительных материалов в несеребряных способах записи информации.
Известны мономеры на основе дифениламина - н-винилдифениламин,1 и. Ы- аллилдифениламин .
N-Винилдифениламин легко полимер.зуется по катионному механизму, а также в присутствии инициаторов радикального типа и при нагревании. Полимер,на. основе N-винилдифениламина, как и сам мономер, нестоек к окислению и при хранении в обычныхусловиях быстро теряет свои первоначальные свойства, поэтому он не может применяться.в электрофотографии.
В отличие от N-винилдифениламина N-аллилдифениламин полимеризуется с трудом, образуя поли-М-аллилдифеН1;1ламин с низким выходом (не более &%) ..
Цель изобретения - изыскание соединений, являющихся полупродуктом для синтеза фотрчувст-вительных материалов, обладающих повышенной устойчивостью при хранении, освещении и нагревании.
Поставленная цель достигается тем, что И-акрилоилдифениламины исг ользуют как полупродукт для синтеза фоточувствительных материалов .
Соединения формулы 1 получают реакцией дифениламина с хлорангидридом акриловой (или метакриловой) кислоты в среде . растворителя (бензол, гексан, ацетон и др.) без катализа,тора в присутствии щелочных дрбавок без внешнего нагревания в течение 30-40 мин с последующим лением целевого продукта известными методами.
В качестве ацилирующего агента используют хлорангидрид акриловой .(или метакриловой) кислоты, причем для полного протекания реакции необходимо брать не менее чем двукратный мольный избыток последнего по отношению к дифениламину, поскольку часть хлорангидрида гидролизуется в условиях реакции, давая хлористый водород и неактивную в этих условиях непредельную кислоту. Оптимальное количество хлорангидрида3 моля на один моль дифениламина.
Для связывания хлористого водорода, выделяющегося в реакции, во избежание протекания побочных про5 цессов в реакционную смесь необходимо вводить добавки основного характера, в качестве которых могут служить как органические основания (пиридин, триэтиламин и др.),, так и
0 неорганические (щелочь либо неорганические соли, обладающие щелочной реакцией). Использование органических оснований затрудняет процесс выделения целевого продукта из реак5 ционной смеси, присутствие же щелочи вызывает чрезмерное осмоление реакционной массы.
Поэтому в данном случае предпочтительнее использовать неорганичес- кие соли (например, бикарбонат нат рия, которые, с одной стороны,
обладают мягким действием, с другой сторона, позволяют легко и просто отделять их от реакционной смеси фильтрованием. Оптимальным количест5 вом бикарбоната является 2,5-кратный избыток его по отношению к дифениламину (из расчета того, чтобы весь хлористый водород, выделившийся и в результате ацилирования дифенил0 амика и в результате гидролиза хлорангидрида, мог бы полностью связаться бикарбонатом натрия). При использований меньшего количества бикарбо. ната как и в отсутствие его получить
5 И-акрилоилдифениламин не удается,
увеличение же количества бикарбоната сверх оптимального .ведет к перерасходу хлорангидрида непредельной кислоты вследствие гидролиза последнего в присутствии бикарбоната натрия. . .
изданной реакции могут быть, исполь: зованы различные растворители - бен; зoл, гексан, ацетон и др. Заметного i влияния выбранный растворитель не
оказывает. Выбор aifeTOHa в данном случае диктуется исключительно соображениями простолл и , удобства выделения целевого продукта из реакционной смеси, поскольку при выливании
0 ацетонового раствора в воду избыток хлорангидрида гидролизуется, при этом продукт реакции быстро затвердевает и далее легко отделяется фильтрованием, причем выход его знс;чительно выше.
5 чем в случае использования других,
не смешивающихся с водой, растворите-лей.
Реакция ацилирования дифениламина хлорангидри дом акриловой (или мет0 -акриловой) кислоты протекает с достаточна большой скоростью уже при комнатной температуре и нетребует ни внешнего нагревания, ни катализатора. Время реакции составляет 305 40 мин. Разработанный способ позволяет получать н-акрилоилдифениламины с высоким выходом в мягких услови ях. Пример. В трехгорлую колбу снабженную обратньл холодильником, механической мешалкой, те рмометром и капельной воронкой, загружают 34 г (0,2 м) дифениламина, 100 мл ацетона, 42 г (0,5 М бикарбоната натрия и в пocJieднюю очередь при перемешивании постепенно добавляют 50 мл (о,63 М) хлорангидрида ак риловой кис лоты. Контроль за ходом реакции осуществляют хроматографически ( ТСХ,силу фол, хлористый метилен:ацетон-15:0,2). Реакцию ведут до полного исчезновения пятна дифениламина на хроматограммё, время реакции при это составляет 30-40 мин. Затем осадок неорганической соли отфильтровывают, промывают его 100 мл ацетона, фильтрат и промывной ацетон объединяют и выливают в 1000 мл холодной воды.. Продукт реакции отфильтровывают, промывают водой и сушат. Выход сырого продукта 44 г (98% от.теор.), т.пл. 85-85, (две перекристалли;зации из гексана). Строение подтверж дено ИК-спектром. Найдено, %: С 80,70, Н 5,89; Д 6,29;.О 7,17. : Вычислено, %: С 80,70; Н 5,86 N 6,27; О 7,17 С гН.(225,37-) . П р и м е р 2. По способу, описан ному в примере 1, из 3,4 г (0,02 М) дифениламина, 10 мл ацетона, 2 г (0,05 М) едкого, натра и 5 мл (0,063М хл91рангидрида акриловой кислоты в те чение 40 мин получено 3,66 г 82%) N-акрилоилдифениламина. П р и м е р 3. По способу, описан ному в примере 1, в реакцию вводят 3.4г (о,02 М дифениламина, 10 мл бензола, 4,2 г (о,05М) бикарбоната , натрия и 5 мл (0,063 м хлорангидрида акриловой кислоты и перемешиваиот в течение 40 мин.По окончании реакции осадок неорганической соли отфиль.тровывают, промывают его 10 мл бензола. Фильтрат и промывной бензол объединяют, промывают водой, сушат поташом, после чего растворительотхЧ няют, а твсардый остаток перекристаллизовывают- из гексана. Выход N-акри.лоилдифениламина 3,26 г (73%). г . / 1Гример41По способу, описан ному в примере 1, из 1,83 г (o,01Mj 4-метилдифениламина, 10 мл ацетона, 2,52 г (0,03м) бикарбоната натрия и 2.5мл (0,0315 м) хлорангидрида акриловой кислоты в течение 3D мин по ,лучено 2,21 г (93,3%) N-акрилоил-4-метилдифениламина. Т.пл. 93, (одна перекристаллизация из гексана). Строение подтверждено ИК-спектром. Найдено, %: С 83,52 Н 6,61 N 5,91. C 6H|rNO Вычислено, %: С 80,95 Н 6,37, К 5,90 . П р и м е р 5. По способу, описанному в примере 1, из, 9 г (0,053М) дифениламина, 27 мл ацетона, 18 г (0,21 м)бикарбоната натрия и 24 мл (0,26М) хлорангидрида метакриловой кислоты в течение 6 ч,получено 12,1 г (95,20i) N-метакрилоилдифе ниламина. Т.пл. 79-8lc (одна перекристаллизация из гексана). Строение подтверждено ИК-спектрсмч. Найдено, %jC 79,80; Н 6,82, N 5,27. . Вычислено, %: С 80,98 нб,87 N 5,90.:: СцН,.;КО N-акрилоилдифениламкн легко полимеризуется в присутствии инициаторов радикального типа, например динитрила азобисизомасляной кисло- ; ты (ДАК). Полимеризацию можно проводить в массе или в растворе толуола в присутствии 1-2% инициатора при 80-85с в течение 5 мин. Затем полимер растворяют в толуоле (Ю мл растворителя на 1 г мономера) и выливают в этиловый спирт или гексан (10 мл спирта или гексана) на 1 мл толуольного раствора, ыход 65-70% (от теор.у. Т.разм. 250-280°С. . Из растворов ароматических угле-водородов поли-Н-акрилоилдифениламин образует прозрачные, прочные бесцветные пленки с хорошей адгезией к подложке, обладающие фоточувствительными свойствами (см. табл.1). Так, пленки, приготовленные из 10%-ныХ толуольных растворов с добавлением 20% от веса поли-к-акрилоилдифениламина сополимера N-винилдифениламина с К- -4-((}-нитрофенил)аза -винилдифениламином имеют потенциал зарядки 130-150 В при времени полуспада первоначального потенциала при освещении полихроматическим светом 1,5 с. Пленки, приготовленные из 10%-ных толуольных растворов поли-н-винилдифениламина с добавлением 5% сополимера N-винилдифениламина с (o-нитрофенил)a3aj винилдифениламином в качестве сенсибилизатора имеют потенциал зарядки 250-300 В и время полураспада первоначального потенциала 1,5-3 с.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения полиаминов | 1971 |
|
SU514853A1 |
| Способ получения @ -аллилдифениламина | 1981 |
|
SU1028660A1 |
| Способ получения поли- @ -алкенилдифениламинов | 1982 |
|
SU1047919A1 |
| Способ получения поли- винилдифениламина | 1970 |
|
SU434748A1 |
| Способ получения аминополимеров | 1974 |
|
SU507593A1 |
| Производные 1,4-бис-(5-арилоксазолил-2)-бензола в качестве органических люминофоров сине-зеленого свечения | 1983 |
|
SU1082787A1 |
| Клеевая композиция | 1987 |
|
SU1565868A1 |
| Способ получения непредельных @ -дикетонов | 1989 |
|
SU1726472A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛИГОЭФИРАКРИЛАТОВ | 1972 |
|
SU328122A1 |
| Способ получения 2-/2',2',2'-тригалогенэтил/-4-галогенциклобутан-1-онов | 1978 |
|
SU917695A3 |
N-акрилоилдифениламины общей формулы где X -Н, -СН, как полупродукт для синтеза фоточувствительных материалов. (Л
П р и м е ч а н и е; В пленки добавлено 20% сополимера N-винилдифениламина с Я-(-( - о -нитро)фенйлазо винилдифениламином,
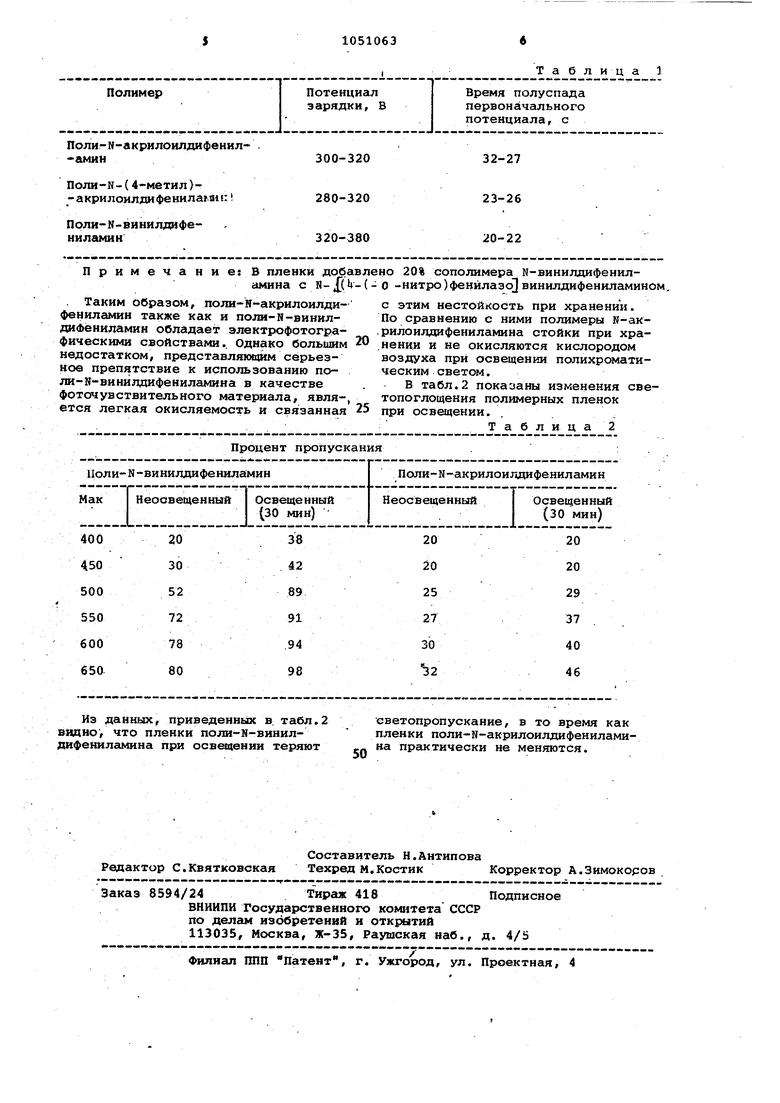
Таким образом, поли-Н-акрилоилди- с этим нестойкость при хранении, фениламин также как и поли-н-винил- По сравнению с ними полимеры N-акдокЬёниламин обладает электрофотогра- .рилоилдифениламина стойки при храфическими свойствами.. Однако большим 20 нении и не окисляются кислородом недостатком, представляющим серьез- воздуха при освещении попихроматиное препятствие к использованию по- ческим светом.
ли-Н-винйддифениламина в качестве . В табл.2 показаны изменения свефоточувствительного материала, явля-, топоглощения полимерных пленок ется легкая окисляемость и связанная 25 при освещении.
Процент пропускания.; .
-к-винилди фенил амин
I
Неосвещенный I Освещенный (30 мин)
2038
42 89 91
30 52 72 78 80 .94 98
Из данных, приведенных в. табл.2 видно, что пленки поли-Н-винилдифениламина при осв цении теряют
Таблица2
Поли-Ы-акрилоиддифениламин
НеосвещеннЕ 1й
Освещенный (30 мин)
20 20 29 37 40 46
20 20 25 27 30 2
светопропускание, в то время как пленки поли-н-акрилоилдифениламина практически не меняются.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Сироткина В.Е., Коган P.M., Ковошевич Л.И., Галкина Г.Ф | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| Вага для выталкивания костылей из шпал | 1920 |
|
SU161A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Сироткина Е.В., Коган ., Ковалевич Л.И., Галкина Г.Ф | |||
| - В кн.: Минерах ьное сырье и нефте- химия | |||
| Томск, 1980, с | |||
| Раздвижной паровозный золотник с подвижными по его скалке поршнями между упорными шайбами | 1922 |
|
SU148A1 |
Авторы
Даты
1983-10-30—Публикация
1981-12-25—Подача