можно использовать в-качестве исход ного продукта, Элюат, полученный из слоя с ацетоном, имеющего пониженную реакционную способность, сушат и осадок.растирают с эфиром; получают 0,7 г Н-десметил-Н-формилвиндолина (ZkfQ%)j продукт, кристаглизованный из эфира, плавится при Пример 2„ Н-Десметил8индолин г (1,19 ммоль) N-десметил-Н-формилвинролина в атмосфере азота растворяют при в 110 мл метанольной соляной кислоты. В течение 3 ч раствор выдерживают при далее с помошью метанольного 10%-ного аммиачного раствора устанавливают зна чение рН 7 Нейтрализованный раствор при низком давлении испаряют до объема 20 мл и к остатку добавляют 30 мл ледяной воды, а далее с помощью разбавленного водного раствора гидроокиси аммония (1:1) устанавливают значение рН 9.Полученный щелочной раствор экстрагируют троекратно 20 MJ. дихлорметана (каждый раз по 20 мл), органические экстракты очищают, сушат с помощью сернокислого магния, фильтруют и фильтрат выпаривают при пониженном давлении. Остаток кристаллизуют из 10 мл эфира, получают 00 мг N-десметилвиндолина (78,7) Т.пл П8°С(иэ эфира). П р и м е р -Десметилвиндолин Обработку производят, как и в примере 2 с той лишь разницей, что гидролиз проводят в присутствии водной 2%-ной серной кислоты вместо соляной , при Выход М-десметилвиндолина составляет 79,1% Пример „N -Десметил-Я -ангидровинбластин. мг (1,01 ммоль j катарантина растворяют в 17 мл безводного дихлорметана. Раствор охлаждают до и при помешивании в азотной атмосфере в течение 15 мин вводят в ра.створ мг 82%-ной перпеларгоновой кислоты (1,1 экв) в 3 мл дихлорметана. Смесь охлаждают до , смешивают с Af2 мг (1,0 ммоль) N-десметилвиндолина с 0,82 мл (3,8 ммоль) свежеперегнанного трифторуксусного ангидрида. Смесь реагентов выдерживают в течение 18 ч при температуре между -10 и , затем в смесь добавляют раст вор из l4o мг натрийборгидрида в мл безводного метанола при -10 С, Течение реакции контролируют посредством послойной хроматографии (адсорбент:си ликагель:растворитель:смесь дихлорметана и метанола в соотношении соответственно 20:2). По окончании реакции смесь концентрируют на четверть объема при а Остаток промывают 15 vn дихлорметана и потом с помощью разбавленного в соотношении 1:1 водного раствора гидроокиси аммония устанавливают значение рН 3 Фазы разделяют, органическую фазу дважды-экстрагируют по 10 мл воды, водную фазу собирают и дважды экстрагируют по 10 мл дихлорметана, Дихлорметановые фазы сушат с помощью сульфата магния, фильт.руют и фильтрат выпаривают при женном давлении. Выпаренный остаток очищают посредством послойной хроматографии (адсорбент, растворитель и , элюент те же, что и в примере 1). Элюат, получаемый из ацетона и содержащий продукт, выпаривают и остаток перекристаллизовывают из метанола, получают 315 мг М-десметил-3 аигидровинбластина (0.2 от теории); т,пл. 202-20 4; , (с 1,06 в хлороформе). Вместо N-десметилвиндолина при использовании эквивалентного количества виндолйна выход 3, -ангидровинбластина cocтaвляet , Т. -215-21б°С;№° +71°С (с в хлороформе), . Пример 5oN -Десметил-, ангидровинбластинсульфатf0,1 г И-десметип-З j ангидровинбластин суспендируют в 1 мл безводного метанола, далее добавляют метанольную серную кислоту до достижения рН 5 После добавлег ния 3 мл эфира образуется кислая аддитивная соль. Полученные кристаллы отфильтровывают и сушат, N-десметил-3 ,-ангидровинбластинсульфат плавится при , Выход составляет 95 от теории. Пример боМ -Десметил-М-формиллейрозин, 100 мг (0,012Ц смольУ N -десметил-Н-формил-З , -ангидровинбластина растворяют в 3 мл бензола, далее к раствору добавляют/ мг 2,2-азобис-изобутиронитрила. Смесь охлаждают до , потом добавляют раствор из 160 мг (о,75 ммоль) 70%-ного кумилгидроперекиси в 1 мл бензонитрила при перемешивании в атмосфере азота Смесь реагентов выдерживают в токе азота дня при С, доб5в- ляют 6 мл бензола и далее смесь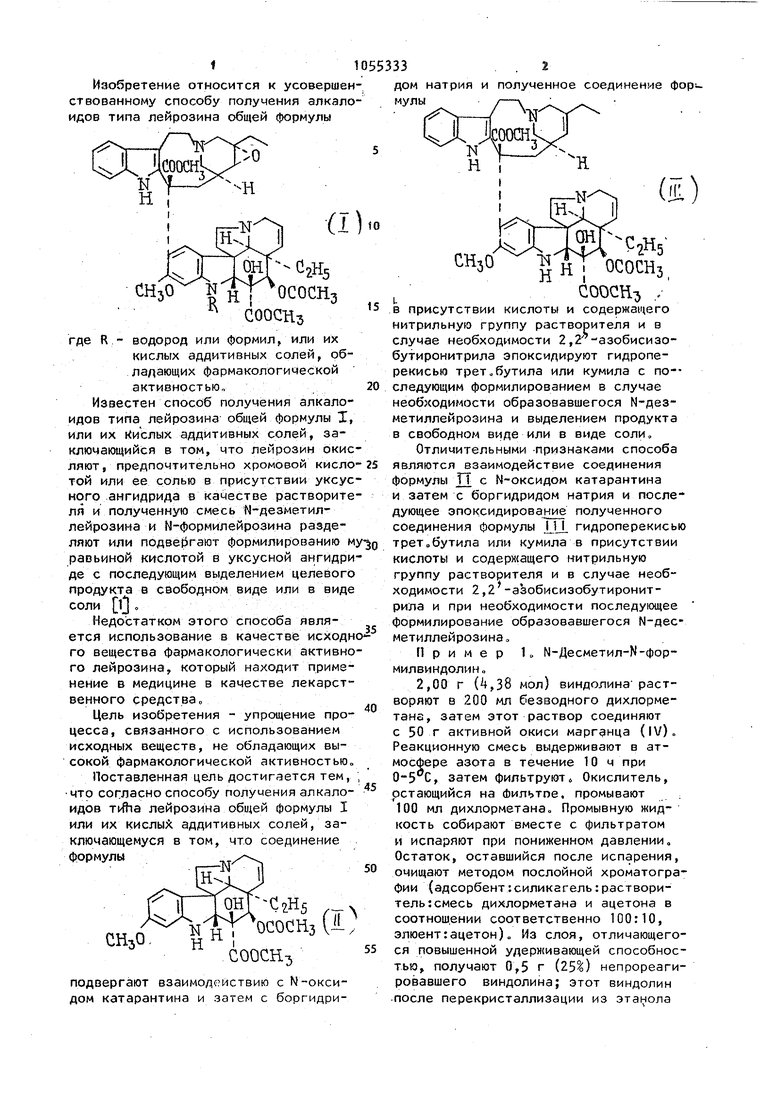


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения N-формиллейрозина или его солей | 1978 |
|
SU969166A3 |
| Способ получения сложных эфиров алкоксивинкаминовой кислоты и/или сложных эфиров алкоксиаповинкаминовой кислоты или их эпимеров,рацематов,оптически активных изомеров или их кислотных физиологически приемлемых солей | 1982 |
|
SU1189348A3 |
| Способ получения винкамина или его производных | 1972 |
|
SU460626A3 |
| ПРОИЗВОДНЫЕ АМИДА АКРИЛОВОЙ КИСЛОТЫ ИЛИ ИХ СОЛИ С ОРГАНИЧЕСКИМ ИЛИ НЕОРГАНИЧЕСКИМ ОСНОВАНИЕМ, ОБЛАДАЮЩИЕ ЦИТОПРОТЕКТОРНОЙ И ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ, И СОСТАВ, ОБЛАДАЮЩИЙ ЦИТОПРОТЕКТОРНОЙ И ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ | 1990 |
|
RU2021259C1 |
| Способ получения 1-алкил-1( -алкоксикарбонилэтил)1,2,3,4,6,7,12,12в-октагидроиндоло (2,3-а) хинолизина или его солей | 1976 |
|
SU619107A3 |
| Способ получения производных винбластина или их эпимеров | 1981 |
|
SU1138033A3 |
| Способ получения производных 3-азабицикло 3,3,1 нонана,или их изомеров,или их фармацевтически приемлемых солей присоединения кислот (его варианты) | 1984 |
|
SU1395141A3 |
| Способ получения метиловых эфиров октапептидов | 1981 |
|
SU1041030A3 |
| Способ получения производных октагидроиндоло(2,3-а)-хинолизина, или их солей | 1977 |
|
SU694074A3 |
| Способ получения производных 9-или 11-нитроаповинкаминовой кислоты или их солей | 1985 |
|
SU1440347A3 |
Способ получения алкалоидов типа лейрозина общей формулы I Где R .водород или формил, или их кислых аддитивных солей, включающий формилирование N-десметиллейрозина муравьиной кислотой в уксусном ангидриде и выделение целевого продукта в свободном виде или в вмде кислой аддитивной соли, о т л и. чающийся тем, что, с целью упрощения процесса соединения общей формулы и. СООСНз подвергают взаимодействию с N-окси- i дом катарантина и затем с боргидри- дом натрия и по лученное соединение общей формулы JK со СП СП СаНб ОСОСНз СНзО N Н I со оо н I СООСНз со в присутствии кислоты и содержащего нитрильную группу растворителя и, в случае необходимости, 2,2 азобисизобутиронитрила эпоксидируют гидроперекисью трет.бутила или кумила с последующим формилированием в случае нео1 ходимости образовавшегося N-десме,тиллейрозина.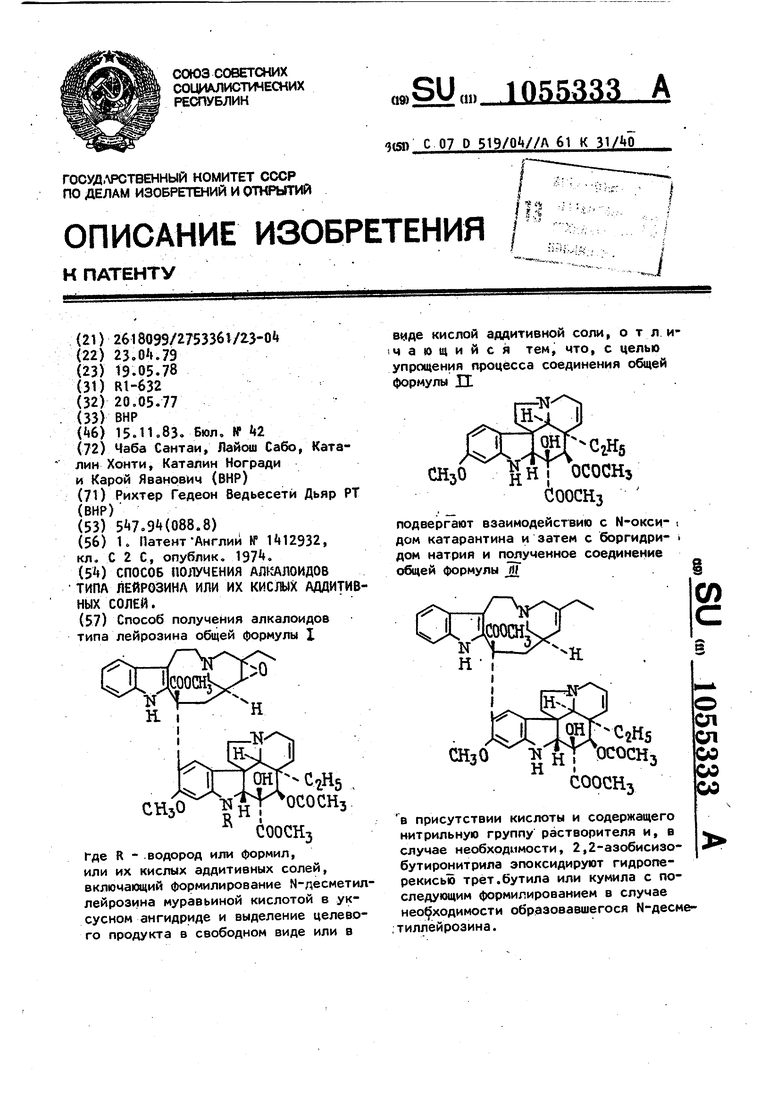
| Переплет | 1929 |
|
SU12932A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ утилизации отработанного щелока из бучильных котлов отбельных фабрик | 1923 |
|
SU197A1 |
Авторы
Даты
1983-11-15—Публикация
1979-04-23—Подача