Изобретение относится к способу получения l-3aMeu;eHHoro cnHpotHivmflB эолидин-4 , З-индолинД -2 ,2, 5-триока общей формулы где R - ,алкил J фенил, нафтилметил или цинамил, ароматические кольца которых при необкодимости несут один или два галогека, или, в бензил, при необходимости несущий одни, два или три заместителя, независимо выбранных из группы,вклю чающей галоген, трифторметил С.,-Gf алкил, Сд-О -апкоксил р нитро, циано и гидроксил, бензольное кольцо А при необходимости несет один заместитель, выбранный из группы, включающий галоген, Сц-Сг -алкил, Q-Сц-- -алкоксил, нитро и гидроксил, или несет два заместителя, независимо выбранных из группы, включающей галоген, Сл-Сн-алкил, или нитро, при условии, что, когда R - метил, этил Ц-пропил или незамещенный бензил, .бензольное кольцо А является незамещенным, иди его солей, рацематов или оптически активных изомеров, об ладающих физиологической активность Известен способ образования имидазольного кольца, взаимодействием кетонов с цианатом щелочного метахш в р&створителя при нагревании ilji. Цель изобретения - син.тез новых соединений, обладающих ценных свойств, позволяющих предположить возможность применения ик в медицин Поставленная цель достигается те что согласно способу получения соединен:пй формулы 1, основанному на известной реакции, индолин-2,3-дио общей формулы где R и бензольное кольцо А имеют приведенные выше значения вводят в реакцию с цианидом щелочного металла и карбонатом или карбс матом аммония с выделением целе.вого продукта в знде рацемата или обрабатывают рацемат оптически активной формой соответствующего основания с выделением целевого продукта в виде оптически активной форгчш или в виде фармацевтически допустимой СОЛРТ . .В том случае, когда требуются фармацевтически. приемлемые соли,осуществляют реакцию соединения фор мулы 1 с соответствующим соединением:, обладающим фармацевтически приемлемым катионом, используя стандартную методику. Более того, когда требуется попучить оптически активную форму соедине нкя формулы 1, возможно осуществление реакции рацемической формы укс1занного соединения с оптически ак- ; тивной формой приемлемого органического основания, например брущ1на, кониина или 2-пипеколина, с последуюи(им стандартным разделением диаствреоизомерной смеси полученных таким путем солей, например путем дробной кристаллизации из приемле:мого растворителя, например Сц-С -алканола, после чего оптически ак-в тивная форма указанного соединения может быть выделена путем обработки кислотой по стандартнойметодике, например водной минеральной кислотой, Тс1кой как разбавленная соляная. Изобретение иллюстр.ируется приме- рг1ми, в которых, если особо не ого- . -ворено, выпаривание осуществляют ротационным выпариванием в вакуум€, все операции проводят при комнатнсй5 температуре, т.е. в диапазоне температур 18-26° С; петролейный эфир чс т кип „ 60-80с) именуется как бензин 60-80, другие фракции петролей- ного, эфира именуются соответственно/ все соединения 1 полностью охарактеризованы на основании даниьах микроанализа и ЯМР- и ИК-спекTPOBJ выход стам, где приведен) указан с целью иллюстрации и не обяза тельно является максимально достигшMtJM о , - Пример 1. В течение 3 ч при 95-100 с кипятят с обратным холодильником смесь 1- (Зг4-диxлopбeнзил| -индoлин-2, 3-диона С12,0 г , карбоната аммония С36,0 г и цианида калия С5,2 г) в 300 мл метанола и 300 :NUI воды.. Полученный темный растврр несколько охлаждают и добавляют, обест цвечивающий древесный уголь С.3,0 .г). Смесь затем нагревают до 95-100 С,. позволяют отогнаться sceiwy метанолу. Горячую смесь затем фильтруют, и остаток промывают горячей водой. Объединяют фильтрат и промывочные воды, охлаждают и подкисляют концентрированной, соляной кислотой до рН 2, Темно-желтое твердое вещестно, оторое -отделяется, собирают, npoi«i В.2ЮТ водой, .сушат на воз,пухе и дваж. перекристаллизовывают из этилацетата/бензила 60-80 об/об.У. В результате получает 3,3 г 1-СЗ,4-дихлорбензилJ-спиро1имидазолидйн-4,3инд.рлигт1-2 ,2 ,5-триона с т.пл. 26927ГС. Исходный реагент получают слец /ющ;.-1М образом.
К перемешиваемому раствору 14,7 г индолин-2,3-диона С изатина) в 200 мл диметилсульфоксида добавляют этанольный раствор гидроокиси калия (100 мл 1 М раствора). Спустя 10 мин добавляют раствор 21,5 г 3,4-дихлорбензилхлорида в 10 мл диметилсульфоксида. Смесь перемешивают в течение 72 ч и затем вливают в воду С600 мл). Образующееся твердое вещество собирают прозывают водой, сушат на воздухе
и перекристаллизовывают из этилацетата/бензина 60-80 (3:2 об./об1 . В результате получают 13,8 г 1-СЗ,4-дихлорбензил)-индолин-2,3-диона с т.пл. 183-184 С.
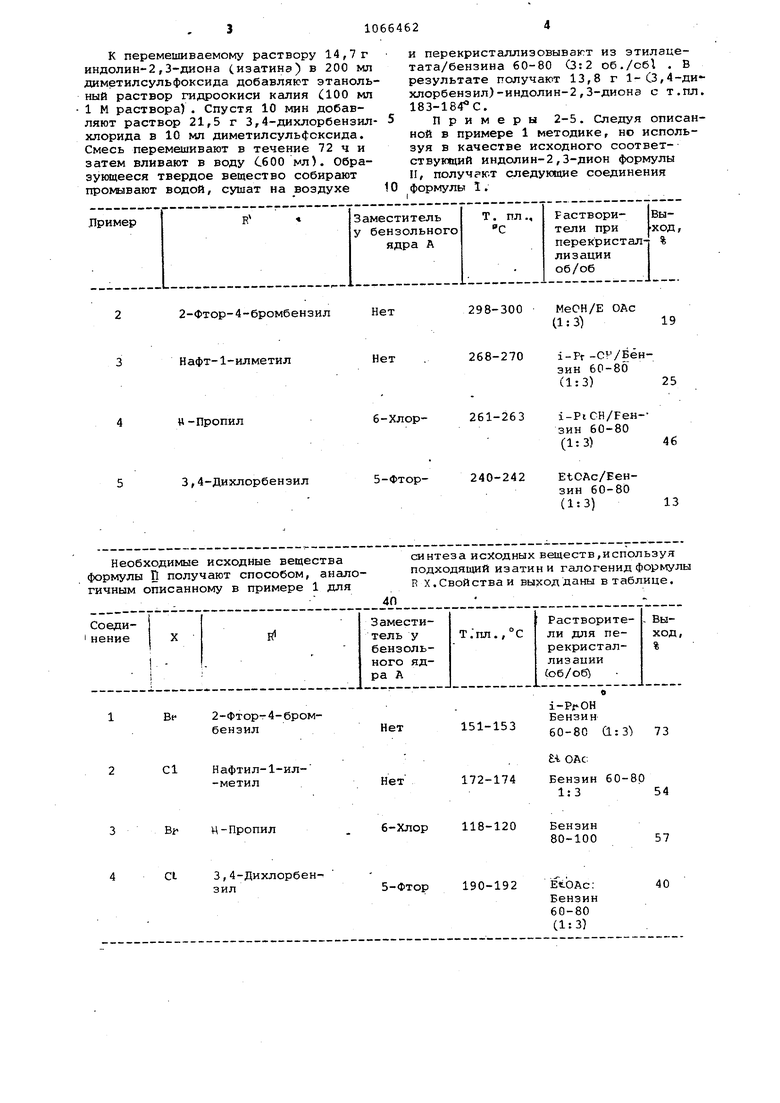
Примеры 2-5. Следуя описанной в примере 1 методике, но используя в качестве исходного соответствующий индолин-2,3-дион формулы II, получрют следующие соединения
формулы 1.





Способ получения 1-замешенного спиро Lимидазолидин-4,3-индолин -2,2, 5-триона общей формулы О II 0 тХг. где R - с - С - алкил, фенил, нафтил метил или цинамил, ароматические коль1} а которых при- необходимости несут один или два галогена, или R -бензил/ при необходимости несущий один, два или три заместителя, независимо выбранных из группы,включакяцей галоген, трифторметил C -Q -алкил, Сд-С -алкоксил, китро, циано и гидроксил; бензольное кольцо А .при необходимости несет один заместитель, выбранный из группы, включающей галоген, Сд-С -алкил, С -С алкоксил, нитро или гидроксил, или несет два заместителя, независимо набранных из группы, включающей галоген, ал кил или нктро, при условии, что, когда В-метйл, этил, J -пропил или незамещенный бензил, бензольное кольцо А является незамещенным, ил и его солей ,рацематов или оптически активных изомеров, отличающийся тем, что ийдолин-2,3-дисо он общей формулы -л- С где R и бензольное кольцо А имеют приведенные значения, вводят в реакцию с цианидбм щелочного металла и карбонатом или карбама-. том аммония с выделением целевого продукта в виде рацемата или об- . рабатывают рацемат оптически активной формой соответствукмего основания с выдeлeниe целевого продукта в виде оптически активной формы или в виде фармацевтически допустимой соли.;
2-Фтор-4-бромбензил Нет
Нафт-1-илметил
Необходимые исходные вещества формулы 11 получают способом, аналогичным описанному в примере 1 для
М-Пропил
CL3,4-Дихлорбензил
298-300 МеСН/Е ОАс
(.1:3) 19
268-2701-Рг-СР/Бёнзин 60-80 (1:3)25
синтеза исходных веществ,используя подходящий изатин и галогенид формулы R X.Свойства и выход даны в таблице.
6-Хлор 118-120 Бензин
57
80-100
EtLOAc:
190-192
40 Бензин 60-80 (1:3}
f10664626
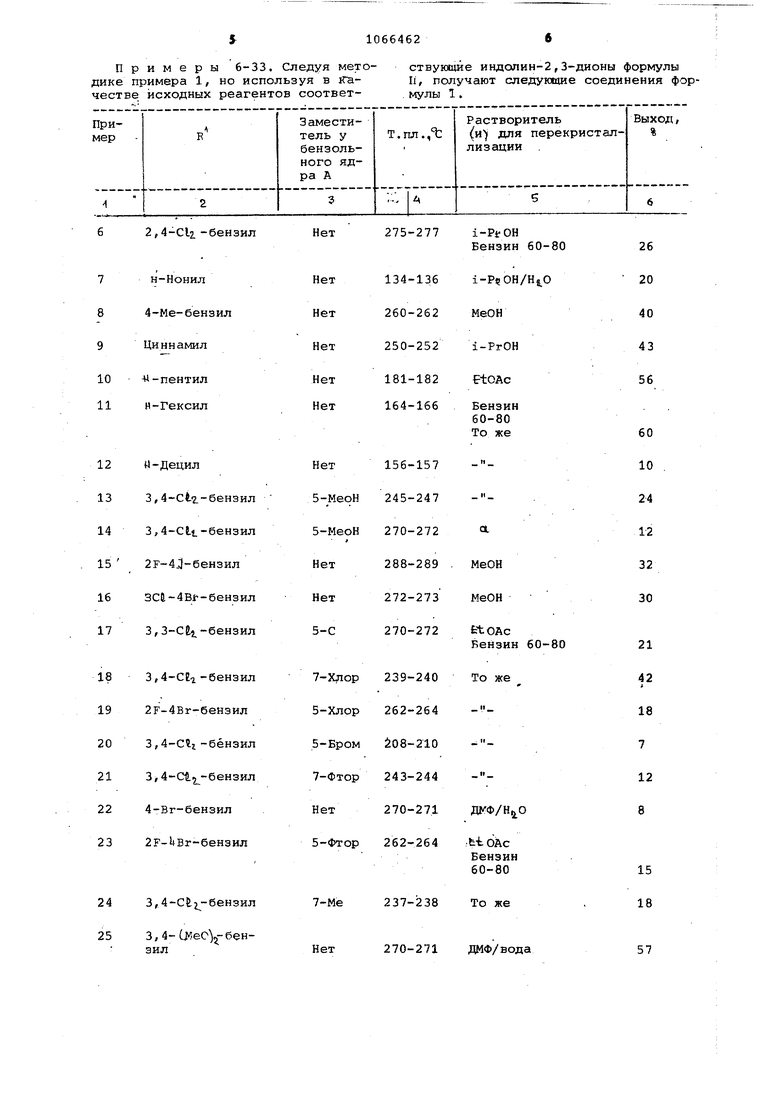
Примеры 6-33. Следуя мето- ствующйе индолин-2,3-дионы формулы дике примера 1, но используя в ira-ц, получают следующие соединения форчестве исходных реагентов соответ-мулы 1.
2,4-Cl2. -бензил
Нет
253, 4-(5есу бенНет
зил
275-277
i-PtOH
270-271 ДМФ/вода
57 Нет276 26С-СГ -бензил 273,4-саг-бензил 4-Хлор 264282-СН-бенэил29Нафт-2-илметил 30Бензил 5-Бром 250314-се-бензил323,4-С22 -цина1 1ил 33Фенил Примечание. Выход дан для перекристаллизованного продукта.
ел - очистка на хроматографической колонке с насадкой силикагель, 1:3 (об./об.) этилацетата/толуола в каче.стве элюирующего растворителя.
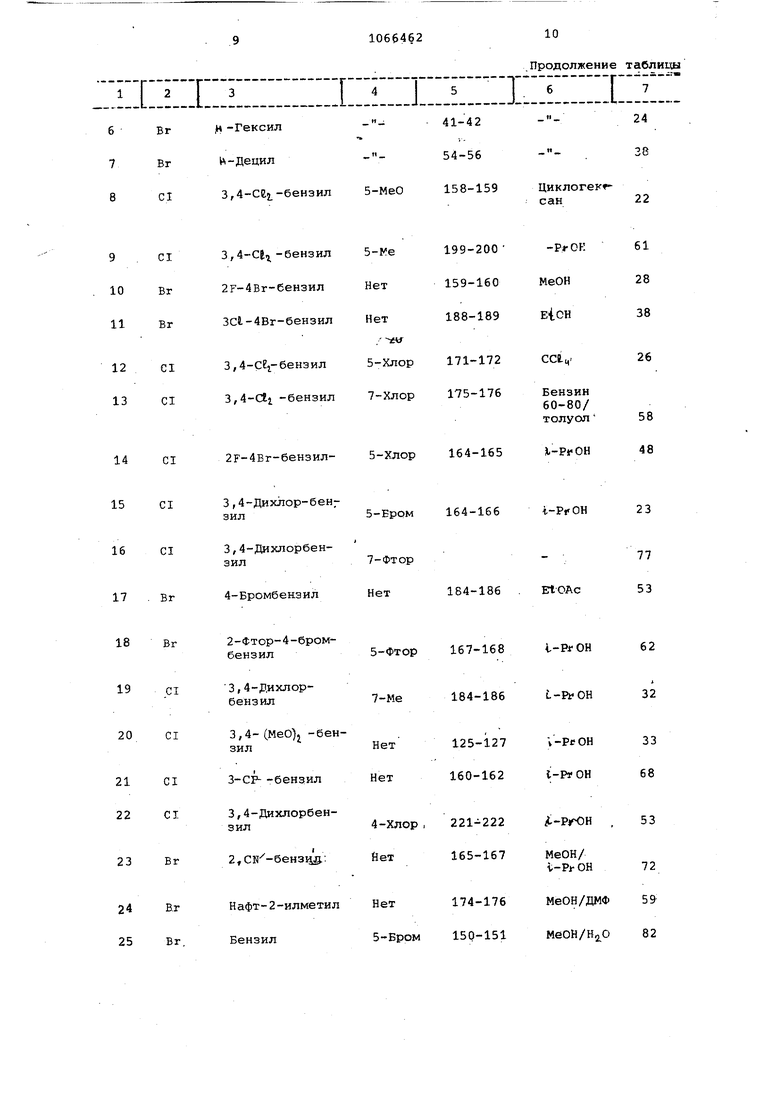
Необходи1 вле исходные вещества щенные индолин-2,3-дионы и галогеформулы II получают способом, анало -ниды формулы R X. гичным описанному в примере 1 дляСвойства псшученный исходсинтеза исходных веществ, исполь- 0 ных вещ-ств указаны в табзуя при этом соответствующие заме- лице.
С12,4-C(lj-бензилНет
Бгц-НонилНет
CI4-Ме-бензил
ВгЦинамил
Вг -Пентил
Продолжение таблицы
Т Г 2482502822322571АсОН EtOAc 266 EtOAc 250 Бензин 252 Бензин 60-80 Et СРс 252 Бензин 60-80 283 tOAc 233 Бензин 259 То же
намилНет 194-196 E-tOAc . 55
Примечание. Выход дан для перекристаллизованного продукта.
а -в1аделяют в виде воскообразного твердого вещества, очищают тонкослойной хроматографией на кремнеземе, используя в качестве элкиругщего растворителя этилацетат/толуол 1:1 об./об.) .
С,
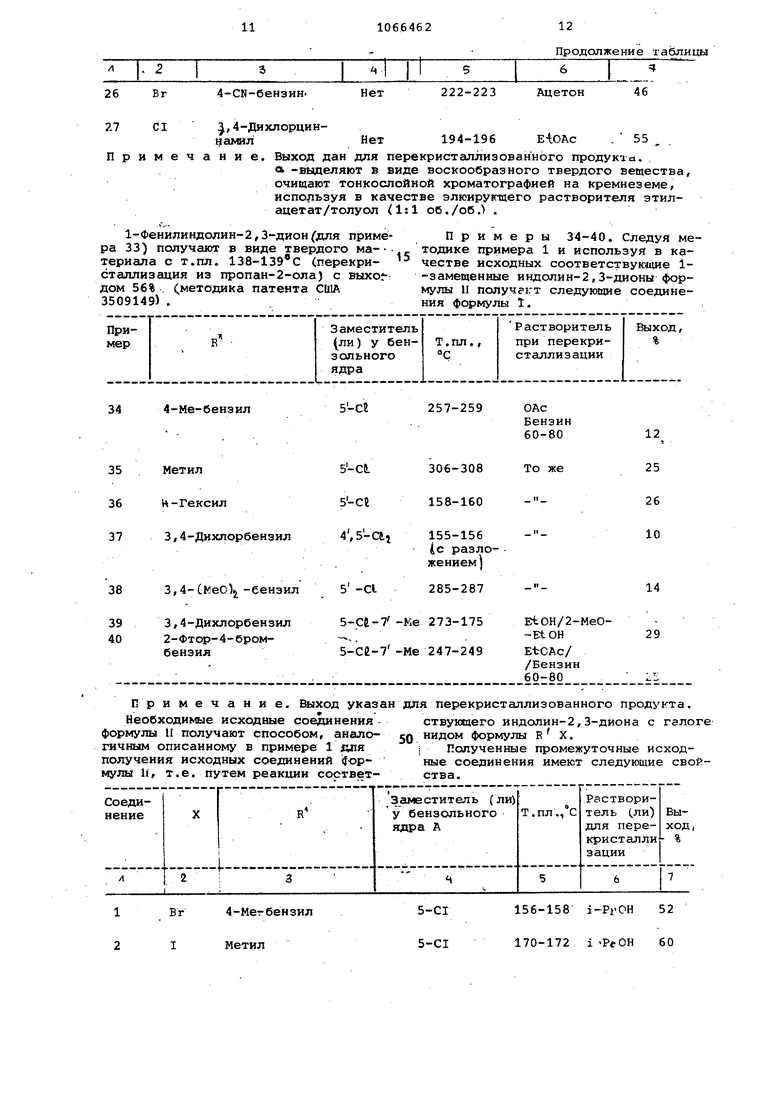
1-Фенилиндолин-2,3-дион для приме- Примеры 34-40. Следуя мера 33) получают в виде твердого ма-тодике примера 1 и используя в катериала с т.пл. 138-139 С (перекри- - честве исходных соответствующие 1сталлизация из пропан-2-ола) с выхог -замещенные индолин-2,3-дионы фордом 56% (методика патента CU1Aмулы П получегт следующие соедине3509149). .ния формулы 1. 383,4-СКеО)-бензил 5-CU-7 -Ке 393,4-Дихлорбензил 402-Фтсчр-4-бром5-се-7 -Me бензил
Примечание. Выход указан для перекристаллизованного продукта. Необходимые исходные соединения- ствующего индолин-2,3-диона с галоге формулы II получают способом, анало- ел нидом формулы в X. гичным описанному в примере 1 для i Полученные промежуточные исходполучения исходных соединений (fop- ные соединения имеют следующие своймулы li, т.е. путем реакции соствет- ства.
4-Мегбензил
Вг
Метил
Продолжение таблицы
156-158 i-PrOH 52
5-СГ
170-172 i PfOH 60
5-CI 285-287 EtOH/2-МеО273-175-EtOH Е-ЬСАс/ 247-249 /Бензин 60-80
3Вгн-Гексил
4CI3,4-Се -бензил
CI3,4-{Meo)j бензил
CI 3,4-Ctij-6eHзил
CI 2-F-4-Br-6eHЗИЛП.Р и M e ч a и и e. Выход указан для Пример 41. Выпаривают фильтрованный раствор 3,76 г 1-СЗ,4-дихлорбензил) -спиро :имидазолидин-4,3-индолил 1-2,2,5-триона в 20 мл воды, содержаний 0,40 г едкого натра, причем оставшиеся следы воды удаляют азеотропной перегонкой с толуолом. В результате получают соответствующую мононатриевую соль с количест венным выходом в виде аморфного гигр скопического твердого вещества, имею мего удовлетворительные данные микро анализа. Пример 42. dI-1- (3,4-Дихлор бензил)-спироСимидгзрлидин-4 З-индолинЗ2,2,5-трион (4,4 г) добавляют к 61,,5 мл 0,18 М раствора гидроокиси I-N, N, Н-триметил-С1-фенилэтил-аммония. Смесь подогревают для обле чения растворения и затем выпаривают Осадок растворяют- в- теплом пропан-2-апе СИ мл. Полученный раствор охлаждают до ОС в течение 48 ч. Образоравшееся кристаллическое твердое вещество собирают путем фильтрации и промывают холодным пропан-2-олом (.5 мл) , затем петролейным эфиром 4060 (20 мл) И дважды перекристаллизовывают из пропан-2-ола. Поручают . «а-диастереоизомерную соль гидроокиси 1-Ы, N, к-триметил-Ц-фенилэтил)--аммония и at. -1-СЗ/4-дихлорбензил)-сгироСимидазолидин-4,3-индолинЗ-2,2, 5-триона 0-,6 г), т.пл. 148-150 С. Dili + 32,8 (с, 1,4; МеОН).
Продолжение таблищ
5-CI86-88i-PfOH 49
4,5-CIt, 185-187 EtOAc/
/Бензин 60-8071
5-CI162-164 i-РгОН/
/ДМФ 33
5-CI-7-ME 191-194 MeON/-MeO-EtOH 41
5-CI-7-iWE 179-182 MeCK/2-MeOEtOH ,43 перекристаллизованного продукта Соль (J.,6 т} растворяют в воде ClC мл и метаноле СЗ мл 1 и раствор подкисляют концентрированной qoляной кислотой С1 мл). Осажденное твердое вещество собирают, промьшан-т водой и перекристаллизовывакт из этанола, получая dL-1- (3 , 4-дихлорбензил) -спиро.имидазапидин-4 ,3-индолин,-2,2.,5-трион, т.пл. 199-200 С,tijLl +41 Сс, 1,6 MeCh). Исходный раствор гидроокиси четвертичного получают путем пропускания водного ра створа иодида 1 - К, N, N-триметил- 11-фенилэтилЗ-аммония (27,8 г) через колонку из анионообменной смолы Amberlite IRA 401, 200 гУ, вновь превра1г,аютв гидроОкисную форму CAraberlite является торговой маркой). Другие отдельные энантиомеры оптически гидроокисей четвертичного аммония, Hanpt(Mep гидроокиси N, и, М-триметил-(1-метил-2-окси-2-фенилэтил О-аммония, могут также быть использованы для расщепления рацемических форм соединений формулы Г. Примеры 43-55, Используя методику, аналогичную описанной в примере 1, но исходя из подходясцего индолин-2,3-диона формулы Г, получают соединения формулы 1 с выходами 1570%,
-бромбенэил
44 3,4-Дихлор. бензил
45 3,4-Дихлорбенэил
46 3,4-Дихлорбензил
47 3,4-Дихлор бензил.
48 2-Фтор-4-бром-5-нитробензил
49 4-Нитробензил
50 3,4-Дихлорцинамил
514-Гидроксйбензил
523,4-Дихлорбензил
533,4 -Дихлорбензид 543,5-Дихлорбензил 553,4-Дихлорбензнл
Отсутствует 290-242
Водный диметилформамид
286-287 Этилацетат/бензин
4-Хлор 60-80
5,6-Диметил 262-263 Этилацетат/бензин
60-80
232-233 Этилацетат/бензин
7-Этил 60-80
5-Нитро 249-251 Этилацетат/бензин
60-80
5-Нитро 180-181 Изопропанол/бензин
60-80
5-Бром-7-нитро 254-246 Этилацетат/бензин
60-80
5-Хлор
295-297 Водный диметилформамкд
285-286
Метанол 244-245
Этилацетат/бензин 80-100
5,6-Дихлор 255-256
Этилацетат/бензин 60-80 Отсутствует 5-Гидрохло 237-238 Толуол 296-298 Этилацетат/бензин 60-80
Исходные индолин-2,3-дионы формулы 11 могут быть получены аналогично примеру 1, но исходя из.
подходящего 1-незамещенного ин3,5-Дихлор-4-бромбензил
3, 4-Дихлор6ензиЛ
3,4-Дихлорбензил
3,4-Дихлорбензил
3,4-Дихлорцинамил
3,4-Дихлорбензил
3,4-Дихлорбензил
3,5-Дихлорбензил .1- С4-Гидроксибензил) -индолин-2 ,3-дион, необходимей в качестве исходного материала для примера 51, может быть, получен следующим образом. Эта нольный раствор гидроокиси калия С16,6 г в 400 мл) добавлякт к переме шиваемому раствору 43,6 г индолин2,3-диона Сизатин)в диметилсульфоксиде (400 МЛ). Спустя 10 мин добавляют раствор 4-ацетоксибензилбромида (76,3 гЗ в диметилсульфоксиде (.40 мл Смесь перемешивают в течение 72 ч, а затем выливают в лед с водой (около 1000 мл). Образующийся вначале смолоподобный продукт медленно кристаллизуется. Полученное твердое вещест-во перекристалли.зовывают из метанола С500 мл), что дает 1-(4-aцeтoкcибeнзил)-индoлин-2,3-диoн в виде твердого вещества, т.пл. 1591бГс-. Это твердое вещество, вместе с дополнительным материалом, полученным из маточного раствора, хроматографируют на двуокиси кремния С500 rt используя толуол, содержащий возрастающее количество этилацетата BV качестве элюента Сдо 25 об./об.%). Комбинируют фракции алюата,собранные с использованием, элюента, содержаще го 20-25 об./об.% этилацетата, и упа ривают с получением 1-(4-гидроксибензилЧ -индолии- ,3-диона в виде киз коплавкого твердого вещества (т.пл.
долин-2 , 3-диона и гагюгенида формулы К X .
Характерными исходными материала1 1к формулы П являются следующие.
24 -243Метанол
180-182Изопропанол
218-220Этилацетат
124-126Бензин 60-80
194-196Этилацетат
170-171ТОЛУОЛ
197-200 Этилацетат/ бензин 60-80
192-193 Этанол 28-35 С) после перекристаллизсщии из смеси толуола и этилацетата. Следует иметь в виду, что ацетоксильная группа во время хроматографирования на двуокиси кремния гидролизуется до требуемой гидроксильной группы. Способность подавлять ферментную редуктазу альдов может быть установлена следующим стандартным лабораторным испытанием. Так, у крыс вызывали диабет свидетельством чего была сильная глюкозурия), вводя . стрептозотоцин. Животным затем в течение 5 дн. вводили ежё дневйо испытуемое соединение, после чего их умертвляли и удаляли хрусталики глаз и седалищные нервы. После стандартной процедуры обработки в каждой ткани опред еляют остаточное содержание сорбита методом газожидкостной хроматографии, предварительно превращая в политриметилсилильные производные. Подавление редуктазы альдоз in vivoоценивают путем сравнения остаточного содержания сорбита в тканях диабетной группы крыс, которым вводят лекарственный препарат, с теми диабетными крысами, которые не получали препарата, и со здоровыми к|эысамм, не получавшими препарата . В соответствии с другим вариантом модифицированной методики испытания крысам, у которых вызван диабет с помощью стрептозоцина, ежедневно
| Эльдерфйльд Р | |||
| Гетероциклические соединения | |||
| Т | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Пылеочистительное устройство к трепальным машинам | 1923 |
|
SU196A1 |
Авторы
Даты
1984-01-07—Публикация
1980-11-12—Подача