где На - галоген, X, а также замес тители в бензольных кольцах А и В имеют указанные значения, подвергают гидролизу и выделяют целевой продукт в свободном виде или в виде соли. 2. Способ по п. I, о т л и ч а ю щ и и с я тем, что процесс 1 4 присутствии водной проводят кислоты при 45минеральной. 3. Способ по п. 1, отличаю щ ии с я тем, что процесс проводят в присутствии гидроокиси или карбоната щелочного м€1Тапла при 18ПО С.












1. Способ получения производньпс фталазин-4-ил-уксусной кислоты общей формулы различные галогеновые радикалы и водород; :) R - водород или фторрадикал, Rj и R - одинаковые или различные галогеновые радикалы и R, - водород; д) R, водород, R, и R - независимо друг от друга фтор или хлоррадикал, и R хлор, бром или йодрадикал и в бензольном кольце В заместители Rg, Rg и R выбраны из радикалов; водород, галоген, С -С алкил или С, -С алкоксирадиI кал при условии, что по крайней мере один из R , О) R и R - водород и X кислород или сера, или их солей, отличающийс я тем, что сложный эфир общей формулы СН2С (I) где R,Ri в бензольном кольце А выбраны из любого из следующих сочетаний: а) R - фтор или метоксирадикап, Rj - водород, RJ - хлор, бром или йодрадикал, R водород или галогеновый радикал; fi) R , ЕЗ и Rji - водород и RJ бром или йодрадикал; R) R, - водород или фторрадикал, Rj и Rj, - одинаковые или // V НаС -осн. Hat

Изобретение относится к способу получения производных фталазин-4-ил-уксусной кислоты, которые способствуют торможению ферментативной альдозоредуктазы в живом организме, и могут найти применение в медицине. Цель изобретения - способ получения новых производных фталазин-4-ил-уксусной кислоты,которые способствуют торможению ферментативной альдозоредуктазы в живом организме. Пример 1. Смесь этил-1,2-дигидро-1-о КС офт алазин-4-ил-ацет ат а (11,5 г) и гидрида натрия (2,7 г, дисперсия с 50%-ным соотношением массы в нефти) в диметилформамиде (125 мл) перемешивают при в течение .1 ч в азотной среде. Полученный раствор охлаждают до комнатной температуры, затем в него добавляют бромистый 4-бром-З-хлорбензил (15,0 г), после чего смесь перемешившот при в течение 2 ч. После охлаждения до реакционную смесь вьтиваю1Т в воду (500 мл). Полученную водную смесь, экстрагируют зтилацетатом (400 мл). Экстракты промьшают водой, высушивают MgSO и вьтаривают, в результате чего получают твердое вещество, которое кристаллизуют из пропан-2-ола с получением этип-2-(3-клop -4-бpoмбeнзил)- ,2-дигидро-1-а1Ксофталазин-4-ил-ацетата (7,3 г), т.пл. 142-145°С. Примеры 2 иЗ, Процесс про водят аналогично примеру 1„ Получают соединения, имеющие формул CH CO-iEi которых кольцо в является незаменным, из этил-1,2-дигидро-2-оксоалазин-4-ил-ацетата и соответствуего бромида, имеющего формулу абл. 1). Вг--СН2 /А (V) Таблица 1 3,4-Ди- 40 i-PrOH хлор 2-Фтор-4-бром В качестве исходного вещества используют хлористый 3,4-дихлорбенПример 4, Раствор этил-2-. 3-хлор-4 бромбеизнл)-1,2-дигидро-оксофталазин-4-ил-ацетата (7,0 г) этаноле (70 мл), содержалщй гидроись капия (7,0 г), нагревают с об31272ратным холодильником в течение 30 мин. Поспе этого раствор выливают в воду (250 мл) и водный раствор экстрагируют простым эфиром (2x150 мл). Водную фазу подкисляют до рН 2 концентриро- ; ванной соляной кислотой. Твердое вещество, которое осаждалось, в результате этого процесса отделяют, промывают водой, высушивают в вакууме, а затем перекристаллизовывают из смеси Ю толуола, пропан-2-ола и петрола (6080) с соотношением объемов 6:2:3, в результате чего получают 2-(3-хлор-4-6poM6eH3Hji)-1,2-ДИГИДРО-1-ОКСОфталазин-4-ил-уксусную кислоту(5 (3,9 г), т.пл. 186С.
2-Фтор-4-бром Прим Пример 2-(3,4-д1гхлорбензил )-7-метокси-1,2-дигидро-1-оксофталазин-4-ил-уксусной кислоты (1,9 г) в хлористом ти ониле (10 мл), содержащую диметилформамид (0,1 мл), нагревают с обратным холодильником в течение 3 ч. После этого полученный раствор выпаривают. Остаток растворяют в сухо толуоле и раствор выпаривают. Эту процедуру выполняют три раза, позволяя получить хлорангидрид 2-(3,4-дихлор-бензил)-7-метокси-1,2-ди;гидро-1-оксофталазин-4-ип-карбоновой кислоты в виде твердого вещества, имеющего удовлетворительный инфракрасный спектр. Раствор указанного хлорангидрида в сухом тетрагидрофуране (50 мл) по каплям добавляют к перемешанному раствору диазометана в сухом просто эфире (200 мл), охлажденном до N-мeтил-N-нитpoзoтepeфтaлaтoм (10 г
184-185
Метанол ечание: Соединение может кристаллизоваться в полиморфных формах, т.е. приобретая форму т.пл. 184-185С (из метанола, содержащего некоторое количество воды) и форму т.пл. 180-182°С (в результате двух кристаллизации из сухого метанола). . Перемешанную смесь После окончания добавления смесь еще 4 Примеры 5 и 6. Процесс; проводят аналогично примеру 4, Получают соединения, имеющие формулу СНаСО Н в которых кольцо в является незамещенным. Соединения получены посредством гидролиза соответствующего простого этилового эфира, имеющего формулу (I) (табл. 2). Таблица2 раз перемешивают и оставляют для нагревания до комнатной температуры в течение 2 ч. После этого смесь разделяют посредством фильтрования. Полученный остаток промьшают сухим тетрагидрофураном (20 мл), после чего соединенные вместе промьшные воды и фильтрат выпаривают с образованием 2-(3,4-дихлорбензил)-4-(с(-диазо)-ацетил-7-метокси-1,2-дигидро-1-оксофталазина в виде твердого вещества,, которое используют без очистки или идентификации. Раствор бензоата серебра (0,2 г) в триэтиламине (1 мл) медленно по каплям добавляют к раствору указанного производного 4-(а-диазо)-ацетИла в абсолютном этаноле (50 мл) и тетрагидрофуране (30 мл), нагреваемом с обратным холодильником, (После такого добавления происходит бурное вьщеление газа, последующее добавление раствора проводят только после окончания этого процесса). После окончания добавления реакционную смесь еще раз перемешивают и нагревают с обратным холодильником в течение 30 мин, после чего ее горячую фильтруют. Фильтрат выпаривают и полученный остаток растворяют в этилацетате (200 мл). Раствор этил:ацетата промьшают водой (3x100 мл), высушивают MgSO и выпаривают. Этот остаток очищают посредством хроматографии на силикагеле (100 г) с использованием увеличивающейся концент рации этилацетата в толуоле в качест- 15 ной ве элюента. В результате этого из со ответствующих фракций (судя по резул татам тонкослойной хроматографии) TLC на силикагельных пластинах с использованием соотношением этилацетата и толуола 1:3 (в качестве элюента) получен этил-2-(3,4-дихлорбен.зил)-7-метокси-1,2-дигидро-1-оксофталазин-4-ил-ацетат (0,9 г), т.пл. 129-130°С. Исходное вещество получают следующим образом. а) Смесь 7-метокси-1,2-дигидро-1,-оксофталазин-4-ил-карбоновой кислот (10,0 г), бикарбоната натрия (15,0 г и йодистого метила (15,0 г) в сухом диметилформамиде (200 мл) перемешивают при комнатной температуре в течение 16 ч. Затем эту смесь выливают в воду (600 мл). Осажденное твердое вещество отделяют, промывгшэт сна чала водой, а затем холодным метанолом, после чего оно перекристаллизовьшается из метанола с образованием метил-7-метокси-1,2-дигидро-1-оксофтапазин-4-ил-карбоксилата (8,6 г) т.пл. 222-225 С. S) Раствор сложного метилового Эфира (8,29 г), полученный по п.о , в сухом диметилформамиде (200 мл) об рабатьшают гидридом натрия (1,75 г, дисперсия в нефти с соотношением мас сы, равньпм 50%). Эту смесь перемешивают при в течение одного часа охлаждают до комнатной температуры, после чего в нее добавляют хлористый 3,4-дихлорбензш1 (7,0 г). Полученную смесь перемешивают при комнатной тем пературе в течение 2 ч, после чего ее выливают в воду (600 мл). Образовавшееся твердое вещество отделяют, промывают водой, высушивают в в кууме, а затем перекристаллизовьшают из смеси пропан-2-ола и петрола (60-80) с соотношением объемов 3:3 с образованием метил-2-(3,4-дихлорбенэил)-7-метокси-1,2-дигидро-1-оксофтапазин-4-ил-карбоксилата (9,0 г), т.пл. 144-146°С. Б) Раствор Сложного метилового эфира (9,0 г), полученньм по п.S , в этаноле (100 мл) и воде (100 мл), содержащий гидроокись калия (10,0 г), нагревают с обратным холодильником в течение 4 ч. Полученный раствор разбавляют водой (200 мл) и подкисляют до рН 2 концентрированной солякислотой. Осажденное в результате этого твердое вещество отделяют, промьшают водой, высушивают в вакууме и перекристаллизовьшают из смеси пропан-2-ола и диметилформамида с соотношением объемов 1:1 с образованием 2-(3,4-диxлopбeнзил)-7-мeтoкcи-l ,2-дигидро-1-оксофталазин-4-ил-карбоновой кислоты (6,1 г), т.ют. 238240°С. 7-Метокси-1,2-дигидро-1-оксофталазин-4-ил-карбоновую кислоту получают в виде твердого вещества, т. шт. 229-230°С, в соответствии с методом, разработанным Ваганом и др. Пример 8. Процесс проводят аналогично примеру 7, но начинают с 2- (3,4-дихлорбенэил)-7-хлор-1,2-дигидро- 1-оксофтапазин-4-ил-карбоновой кислоты (А). При этом получен 8%-ньй выход этил-2-(3,4-дихлорбензил)-7-хлор-1,2-дигидро-1-оксофталазин-4ил-ацетата в виде твердого вещества, имеквдего удовлетворительньй спектр ядерного магнитного резонанса. Исходное, производное карбоновой кислоты (А) получают по пп.а -6, но выполнение процедуры начинают с 7-хлор-1,2-дигидро-I-оксофталазин-4-ил-карбоновой кислоты (В). Промежуточные вещества характеризуются следукицими температурами плавления: по п, а : метил-7-хлор-1,2-дигидро- 1-оксофтал азин-4-ил-карбоксилат, т.пл. 255-257°С (перекристаллизовывают из сме.си метанола и диметилформамида с соотношением объемов,2:1); по п.S : метил-2-(3,4-дихлорбензил)-7-хлор-1,2-дигидро-1-оксофталазин-4-ил-карбоксилат, т.пл. 178-180°С (перекристаллизовьшают из смеси пропан-2-ола и петрола (60-80) с соотношением объемов 1:3); по П.& : 2-(3,4-дихлорбеизил)7-1,2-днгидро-1-окЕофталазин-4-ил-кар боновая кислота, т.пл. 260-262С (перекристалл гзпвывают из смеси метанола и диметилформамида с соотношением объемов 1:1). Карбоновую кислоту (Б) получают в виде твердого вещества, . 241243 С; в соответствии с методом, раз работанным Ваганом и др., но выполнение процедуры начинают с 4-хлор-2метиладетофенона. Примеры 9и10. Процесс проводят аналогично примеру 4, но его начинают с соответствующего слож ного этилового эфира. По примеру 9 получают 2-(3,4-дихлорбензш1)-7-метокси-1,2-дигидро-1-оксофталазин-4-ил-уксусную кислоту, т.пл. 193-200°С (перекристаллизовывают из пропал-2-ола), выход 50%. По примеру 10 получают 2-(3,4-дихлорбензил)-7-хпор-1,2-дигидро-1-оксофталазин-4-ил-уксусную кислоту, т.пл. 203-205°С (перекристаллизовывают из смеси пропан-2-ола и петрола (60-80) с соотношением объемов 1:1), выход 43%. Примеры 11 и 12. Процесс проводят аналогично примеру 1. В результате применения бромистого или хлористого бензила получают следующие сложные эфиры. По примеру 11 получают этил-2-(2-фтор-4-хлорбензил)-1,2-дигидро-1-ок софтапазин-4-ил-аце,тат, т.пл. 102 С (перекристаллизовывают из петрола (60-80), а затем из этанола), выход 45%. По примеру 12 получают этил-2-(2-фтор-4-иодбензил)-1,2-дигидро-1-оксофталазин-4-ил-ацетат, т.пл. 113°С (перекристаллизовьшают из петрола (60-80), выход 50%. Примеры 13-15. Процеее проводят аналогично примеру 4, но его начинают с соответствующего слож ного этилового эфира. По примеру 13 получают 2-(2-фтор-4-хлорбензил)-1,2-дигидро-1-оксофталазин-4-ил-уксусную кислоту, т.пл. 193-194С (перекристаллизовь вают из смеси этанола и воды с соотношением объемов 3:1), выход 63%. По примеру 14 получают 2-(2-фтор-4-иодбензил)-I,2-дигидро-1-оксофталазин-4-ил-уксусную кислоту, т.гш. 189С (перекристаллизовьтают из смеси этанола и воды с соотношением объемов 3:1), вьгход 55%. По примеру 15 получают 2-(3-хлор-4-бромбензил)-1,2-дигидро-1-тиоксофталазин-4-ил-уксусную кислоту, т.пл. 197-199°С (перекристаллизовьшают из пропан-2-ола), выход 25%. При этом гидролиз осуществляют при помощи водного раствора гидроокиси натрия в метаноле в течение 10 мин с обратным холодильником. Пример 16. Смесь этил-2-(3-хлор-4-бромбензил)-1,2-дигидро-1-оксофталазин-4-ил-ацетата (1,8 г) и пятиcepниctoгo фосфора (2,5 г) в ксилоле (.100 мл) перемешивают и нагревают с обратным холодильником в течение 1 ч. Реакционный раствор затем охлаждают до комнатной температуры, в него добавляют этилацетат (25 мл), после чего смесь фильтруют через хроматографический силикагель (20 г), полученньй фильтрат выпаривают, и полученное твердое вещество перекристаллизовьшают из этанола с образованием этил-2-(З-хлор-4-бромбензил)-1,2-дигидро-1-тиоксофтапазин-4-ил-ацетата (1,1 г), т.пл. 124126°С. Примеры 17-22. Процесс проодят аналогично примеру I, но с приенением соответствующего бромистого ензила, имеющего формулу (V). Полуают соединения, имеющие формулу (IV), которых кольцо В является незамеенным (табл. 3). ТаблицаЗ Примеры 23-25. Этил-4-метил 3-оксо-д1а-фталанацетат (2,29 г) нагревают и перемешивают с обратным холодильником в толуоле (200 м.л) в процессе добавления по каплям раство ра 3,4-дихлорбензилгидразина (1,9 мл в толуоле (50 мл). Смесь продолжают нагревать с обратным холодильником в течение 3 ч, охлаждают и выпаривают. Остаток из твердого вещества перекристаллизовьюают из CMecji изопропанола и петрола (60-80) с соотношением объемов 1:2 с образованием этил -2-(3 ,4;-дихлорбензил) -8-метш1-1,2-ди гидро-1-оксофтапазин-4-ил-ацетата (пример 23) (1,4 г), т.пл. 1341370С. Ан.алогичным образом, но начиная с этил-4-фтор-З-оксофталанацетата, получают этил-2-(3,4-дихлорбензил)-8-фтор-1,2-дигидро-1-оксофтапазин-4-Ш1-ацетат (пример 24), т.пл. 177178°С (перекристаллизовывают из смеси изопропанола и петрола (60--80) с соотношением объемов 1:2), выход 37%. Аналогичным образом, по начиная . со смеси 1: 1 5-метил- и 6 метш1-3-окco-ula-фталаначетата, получают смесь 1:1 этил-6-метил- и 7-метил-2-(3,4дихлорбензил)-1,2-дигидро-1-оксофт алазин-4-1ш-ацетата (пример 25), т.пл 120-122°С (перекристаш1изовыв.ают из изопропанола), выход 33%. Исходные вещества получают следую щим образом. Раствор 3-фторфталевого ангидрида (7,35 г) и (карбэтоксиметилен)-трифенилфосфорана (17,5 г) в сухом 1,2диметоксиэтане (200 мл) перемешивают и нагревают с обратным холодильником в атмосфере азота в течение 16 ч Растворитель затем выпаривают и остаток адсорбируют на хроматографический силикаг(11ь (20 г). Этот силикагель затем добавляют в верхнюю часть колонки такого же силикагеля (300 г), после чего колонку элюируют толуолом. Элюат анализируют посредством тонкослойной хроматографии (силикагель : элюат из смеси толуола и этилацетата с соотношением объемов 9:1), после чего первые фракции, содержащие видимое в ультрафиолетовом спектре вещество, соединяют и выпаривают. Полученное твердое вещество перекристаллизовывают из изопропанола с образованием по примеру 24 этил-4-фтор-3-оксо- CilQ-фталанацетата (2,3 г), т.пл. 101-103°С. Аналогичным образом в виде твердого вещества получают этил-4-метил-3-оксо- ulQ-фтапанацетат (пример 23), т.пл. 84-86°С, выход 56% после перекристаллизации из изопропанола, причем выполнение процедуры начинают с 3-метилфталевого ангидрида. Аналогичньм образом получают смесь 1:1 этил-5-метил- и 6-метил-3-оксо-л1а-фталанацетат (пример 25) в виде твердого вещества, вькод 40% т.пл. 84-86 С (перекристаллизовьшают из изопроцанола), причем выполнение процедуры начинают с 4-метш1фталевого ангидрида. Примеры 26-28. Процесс проводят аналогично примеру 1 из соот,ветствующего замещенного 1,2-дигидро-1.-оксофталазин-4-ил-ацетата и 2-фтор-4-бромбензштгидразина. По примеру 26 получают этил-2- . -(2-фтор-4-бромбеизш1)-8-фтор-1,2-дигидро- 1-оксо-фталазин-4-ил-ацетат, т.пл. 128-130°С (перекристаллизовьшают из смеси изопропанола и петрола (60-80) с соотношением объемов 1:3) выход 36%. По примеру 27 получают этил-2-(2-фтор-4-бромбензил)-8-метил-1,2-дигидро-1-оксофталазин-4-ил-ацетат, т.пл. 120-122С (г1ерекристаллизовьшают из смеси изопропанола и пет рола (60-80) с соотношением объемов 1:3),выход 4 3%. По примеру 28 получают этил-2-(2-фтор-4-бромбензш1)-6,7-метилендй окси-1,2-дигидро-1-оксофталазин-4-ил ацетат, т.пл. 163-165°С (перекристаллизовьшают из этилацетата), выход 50%. Исходные вещества получают следукяцим образом. Q) Этш1-8-метил-1,2-дигидро-1-оксофталазин-4-ил-ацетат (пример 27). Раствор этил-4-метил-З-оксо-Д1а--фтапанацетата (3,5 г) в этаноле (100 мл) перемешивают и нагревают с обратным холодильником в процессе добавления по каплям гидразингидрата (15 мл 1М раствора в этаноле). После окончаниядобавления смесь продолжают перемешивать и нагревать с обратным холодильником в течение 3 ч а затем оставляют остьгеать до комнатной температуры. Осажденное твердое вещество собирают и хорошо промьшают петролом (60-80) и перекристаллизовьгоают из смеси изопропанола
3,4-Дихлрр 26
7-Фтор
29
- -10
2-Фтор-4- 60 бром
Диазометан получают из 5ис -(N-мeтил-N-нитpoзo)-тepeфтaлaмидa при помощи метода Моора и Рида.
Исходные фталазин-4-ил-карбоновые7-Фтор-1,2-дигидро-1-оксофталакислоты получают следующим образом. зин-5-ил-карбоновую кислоту (полус) 2-(3,4-Дихлорбензнл)-7-фтор-ченную в виде твердого вещества,
-1,2-дигидро-1-оксофталазин-4-карбо-т.пп. 241-243С, выход 52%, посредстновая кислота.,вом процедуры разработанной Ваганом
i-PrOH
160-162 и петрола (60-80) с образованием этил-8-метил-1,2-дигидро-1-оксофталазин-4-ип-ацетата (1,0 г), т.гш. 197-199°С. 5) Этил-8-фтор-1,2-дигидро-1-оксофталазин-4-ил-ацетат (пример 26), Этот сложный эфир получают в виде твердого вещества, т.пп. 207-210°С (перекристаллизовывают из этилацетата), вьгеод 51%, из этш1-4-фтор-3-оксо-д1а-фталанацетата и гидразингидрата с использованием процедуры, описанной в п. Q (пример 27). В) Этил-6,7-метилендиокси-1,2-дигидро- I -оксофталазин-4-ил-ацетат (пример 28). Этот сложный эфир получен в виде твердого вещества, т.пл. 226-228С, выход 70%, из этил-5,6-метилендиокси-3-оксо-а1а-фталанацетата (А) и гидразингидрата. Фталанацетат (А) получен в виде твердого вещества, т.пл. 189-191 с (перекристаллизовывают из этанола), выход 64%, из 4,5-метилен-диоЛсифталевого ангидрида с использованием промежуточных веществ, описанных в примерах 23-25. Пример 29-32. Процесс проводят аналогично примеру 7. Из соответствующих исходных веществ получают сложные эфиры, имеющие формулу (IV) (табл. 4). Таблица 4
и др.) превращают н ее соль натрия и подвергают взаимодействию с иодметаном по примеру 8й, с образованием cooтвeтcтвyюп eгo сложного метилового эфира в виде твердого вещества, т.пл. 234-237С (перекристаллизовывают из смеси метанола и диметилформамида с соотношением объемов 3:1), выход 68%. Этот сложный эфир затем алкилируют хлористым 3,4-дихлорбенз5-шом в соответствии с процедурой, описанной в примере ёб с образованием мети.л-2-(3,4-дихлорбензил)-7-фтор-1,2-дигидро-1-оксофталазин-4-ил-карбоксилата, т.пл. 147-149°С (перекристаллизовывают из смеси т.олуола и петрола (60-80) с соотношением объемов 1:1), выход 68%. Этот сложный эфир затем подвергают гидролизу с использованием смеси водного раствора карбоната калия и диоксана в соответствии с процедурой, описьшаемой в примере 36, с об.разованием 2-(3,4-дихлорбензил)-7-фтор-1,2-дигидро-1-оксофталазин-4-ил-карбоновой кислоты в виде твердого вещества, т.пл. 222-224 С (перекристаллизовьгоают из изопропанола), выход 87%.
S) 2-(3,4-Дихлорбензил)-6,7-дихлор-1,2-дигидро-1-оксофтапазин-4-ил-карбоповая кислота.
Эту кислоту получают аналогично п.а, и соответству ощие промежуточные вещества, температура плавления, растворители и выход следующее:
6,7-дихлор-15 2-дигидро-1-оксофталазин-4-карбоновая кислота: т.пл. 294296°С (перекристаллизовьш:ают из диметилформамида), выход 42%5 соответствуняций сложный метиловый эфир: т,гш. 234-236°С (перекристаллизовывс1ют из диметилформамида), выход 51%;
метил-2-(3,4-дихлорбензш1)-6,7-дихлор-1,2-дигидро-1-оксофталазин-4-илкарбоксилат: т.пл. 155-156С (перекристаллизовьшают из диметилформамида), выход 85%;
2-(3,4-дихлорбензил)-6,7-дихлор-1,2-дигидро-1-оксофталазин-4-ил-карбоновая кислота: т.пл. 240-242°С
(перекристаллизовывают из этанола), выход 62%.
) 2-(3,4-Дд1Хлорбензил)-6-:хлор-1,2-дигидро-1-оксофталазин-4-Ш1карбоновая кислота.
Раствор литий бутила в гексане (165 мл 1,6М раствора) медленно добавляют в перемешиваемый раствор
2-(4-хлорфенил)-4,4-диметил-2-оксазолина (50,5 г); в натриевой соли высушенного эфира (600 мл) содержится при (-5)-(0)С и в атмосфере сухого аргона. После окончания добавления перемешивание продолжают при этой температуре в течение 30 мин, после чего этот раствор медленно добавляют к перемешиваемому раствору сухого диэтилоксалата (326 мл) в простом эфире (500 мл), находящемуся при температуре 0°С. При переносе воздействия воздуха и воды устраняется использованием атмосферы сухого аргона. После окончалия добавления реакционную смесь продолжают перемешивать и оставляют нагреваться до комнатной температуры в течение 1 ч. Эфирную смесь промьшают затем водой (2x150 мл), высушивают MgSO и выпаривают при пониженном давлврши (10мм рт.ст.), до тех пор, пока не удаляется весь избьпок диэтилоксалата.Это остаток растворяют в диоксане (.500 мл и этот раствор добавляют к 5 н. соляной кислоте (500 мл). Эту смесь нагревают с обратным холодильником в течение 18 ч, выпаривают до половины объема, после чего остаточньм раствор фильтруют. Фильтрат доводят до рН 8 в результате добавления гидразингидрата, и раствор нагревают в течение 30 мин при 90°С, а затем подкисляют до рН 4 концентрированной соляной кислотой. Эту смесь охлаждают и отделившееся твердое вещество собирают посредством фильтрации, промьшают водой (2x500 мл) и высушивают в вакууме над пятиокисью фосфора с образованием 6-хлор-1,2-дигидро-1-оксофталазин-4-ил-карбоновой кислоты (21,0 г.).
Эту кислоту суспензируют в диметилформамид (250 мл) и смесь обрабатывают бижарбоне.том натрия (21,0 г и изометаном (40 мл). Соединенную смесь перемешивают в течение ночи, а затем разбавляют водой (250 мл).Осажденное твердое вещество собирают, промьгоают водой (2x200 мл) и перекристалл из овьшают из смеси изопропанола и диметилформамида с соотношением объемов 2:1, в результате чего получают метил-6-зшор-1,2-дигидро- -оксофтал:азин-4-ил-карбоксш1ат (17,0 г), т.пл. 248-250°С.
Этот сложный эфир реагирует затем с хлористым 3,4-д11схлорбензилом аналс;гичн(1 тому, КПК описано в п. о и д После этого получают метил-2-(3,4-днхлорбензш1)-6-хлор-1,2-дихлор-1-оксофтапазип-4-ил-карбоксилат, т.пл. 168-170 С (перекристаллизовывают из толуола) с 45%выходом. Это сложный эфир подвергают затем гидролизу по п.а, с образованием 2-(3,4-диxлopбeнзил)-6-xлop- 1,2-дигидро-1-оксофталазин-4-карбо новой кислоты, т.пл. 222-223°С (перекристаллизовьшают из этанола) с 60% выходом. г) 2-(2-Фтор-4-бромбензил)-6-фто -1,2-дигидро-1-оксофталазин-4-илкарбоновая кислота. Эту кислоту получают аналогично п. & , а относящиеся промежуточные вещества, температуры плавления,рас ворители и величины выхода следующе метил-6-фтор-1,2-дигидро-1-оксофтапазин-4-ил-карбоксилат : т.пл.221 223 С (перекристаллизовьшают из смеси метанола и диметилформамида с соотношением объемов 2:1), выход 15%; метил-2-(2-фтор-4-бромбензш1)-6-фтор-1 ,2-дигидро-1-оксофталазин-4-ил-карбоксилат: т.пл. 131-134°С (перекристаллизовывают из метанола), выход 51%; 2-(2-фтop-4-бpoмбeнзил)-6-фтop-1,2-дигидро-1-оксофталазин-4-ил-карбоновая кислота: т.пл. 210-2 1°С (перекристаплизовьшают из изопропанола), выход 70%. Пример 33. Процесс проводят аналогично примеру 16. Получают этил-2-(2-фтор-4-бромбензил)-,2-дигидро- 1-тиоксофталазин-4 -ил-ацетат, т.пл. 97-99°С (перекристаллизовывают из этанола) с 22% выходом в результате тиатирования этил-2-(2-фтор-4-бромбензил)-,2-дигидро-1-оксофтал азин-4-ил-ацетата. Примеры 34-37. Смесь карбоната калия (1,5 г), воды (16 мл), диоксана (50 мл) и зтил-2-(2-фтор-4Таблица 5 -бромбензил )-8-фтор- 1 , 2-диг1щрс)- 1 -ovсофтапаз1 н-4-ил-аце.тата (1,0 г) нагревают с обратным холодильником н течение 24 ч, а затем выпаривает.0статок растворяют в воде (100 мп), и раствор промывают простым эфиром (2x100 мл). Водную фазу подкисляют до рН 2 в результате добавления концентрированной соляной кислоты. Образовавшееся твердое вещество собирают фильтрованием, промьшают водой и перекристаллизовывают из смеси толуола, изопропанола и петрола (60-80) с соотношением объемов 7:1:5, в результате чего получают 2-(2-фтор-4-бромбензил)-8-фтор- 1 , 2-дигидро- 1 -оксофталазин-4-ил-уксусная кислота (пример 34) (0,5 г), т.пл. 173-175°С. Используя аналогичную процедуру и начиная ее выполнение с соответствующих сложных этиловых эфиров, получают следующие производные уксусной кислоты: Пример 35. 2-(3,4-Дихлорбензил)-7-фтор-1,2-дигидро-1-оксофталазин-4-ил-уксусная кислота, Т.Ш1. 20)-202°С (перекристаллизовывают из смеси этилацетата и петрола (60-80) с соотношением объемов 1:2), выход 90%. Пример 36. 2-(3,4-,Ll Jxлopбензил)-6, 7-дихлор-1 ,2-д} Г1-щро-1-оксофтапазин-4-ил-уксусная кислота, т.пл. 204-205°С (перекристаялизовывают из смеси метанола и диметилформамида). Вькод 76%. Пример 37. 2-(3,4-Дихлорбензил)-6-хлор-1,2-дигидро-1-оксофталази} -4-1ш-уксусная кислота, т.пл. 208-209°С (перекристаллизовывают из изопропанола), выход 55%. Примеры 38-50. Процесс проводят аналогично примеру 4. Посредством гидролиза соответствующих сложных этиловых эфиров с гидроокисью калия получают следующие производные уксусной кислоты, имеющие формулу VI (табл. 5). Никакого 2-Фтор-4,5- 71 дибром - - 3,5-Дихлор- 60 -4-бром - - 2-Метокси- 55 -4-хлор 8-Фтор 3,4-Дихл:ор 68 6-Метил 3,4-Дихлор 43 7-Метил - 2-Фтор-48-Метилбром 3,4-Дихлор 44 47 6,7-Метн- 2-Фтор-4- 70 лендиокси бром 6-Фтор 8-Этокси 3,4-Дихлор 65 Смесь 1:2 6-метил и 7-метилпроизводных. Экзо-таутомер, определенный посредством
Аналогичным образом посредством гидролиза соответствующего сложного эфира с водным раствором гидроокиси натрия в метаноле получают 2-(2-фтор-4-бромбензил)-1,2-дигидро-1-тиоксофталазин-4-ил-уксусная кислота (пример 50) в внце твердого вещества, т.пл. 194-196°С (перекристаллизовывают из метанола) с 30% выходом.
Пример 51. Этил-2-(3,4-дихлорбензил)-8-фтор-1,2-дигидро-1-оксофтапазин-4-ил-ацетат (1,8 г) добавляют к раствору натрия (1,5 г) в сухом этаноле (150 мл). Полученный раствор нагревают с обратным холодильником в течение 3 ч, а затем выпаривают. К остатку добавляют воду (100 мл), полученное твердое вещество собирают посредством фильтрования и высушивают с образованием этипПродолжение табл.5 1842191831.43182195203209187204-2-(3,4-дихлорбензил)-8-этокси-1,2-дигидро-1-оксофтапазин-4-ил-ацетата(0,5 г).
Пример 52. Раствор метилата натрия (25 М.П 1,0 М раствора в метаноле) добавляют к раствору 2-(2-фтор-4-бромбензил)-1,2-дигидро-1-оксофтапазин-4-ил-уксусной кислоты (9,87 г) в метаноле (300 мл), после чего смесь нагревают до своей температуры кипения. Метанолу дают выкипеть до тех пор, пока объем смеси не составляет -приблизительно 100 мл. После этого к этой смеси добавляют изопропанол (150 мл), за которым (Следует петрол (60-80), до тех пор пока смесь не становится непрозрачной. Затем смесь оставляют остьгеать до комнатной температуры. Образовавшееся твердое вещество отделяют i-PrOH 186 i-PrOH 220 i-PrOH 184 EtOA / толу145ол (1:2) , 184 i-PrOH i-PrOH/пет197рсл 60-80 (1:2) i-PrOH/пет205рсл 60-30 (1:2) i-PrOH 210 i-PrOH 188 i-PrOH 206 спектроскопии ЯМР.
филь грп.1;)иием, 131 П1а) с помощью толуола (.2x400 мл), а затем Промывают простым эфиром (300 мл) с образованием 2-(2-фтор-4-бромбензнл)-1,2-дигидро-1 -оксофталазнн-4-1Ш-адетата натрия (6,5 г), т.пл. 2-44-247 С.
Пример 53. 2-(Фтор-4-бром бензил )-2-(2-фтop-4-бpoмбeнзиJI)- 1,2-дигидро-1-оксофталазин-4-ил-ацетат (0,9 г) растворяют в этаноле
(40 мл), содержащем гидроокись калия (2,0 г), после чего эту смесь нагревают с обратным холодильником в течение 90 мин. Растворитель выпаривают и добавляют воду (100 мл). Полученный светльй раствор подкисляют концентрированной соляной кислотой до достижения рН 2. Осадившееся твердое вещество отделяют фильтрованием, хорошо промывают водой и высушивают в вакууме с образованием 2-(2-фтор-4-бромбензил)-1,2-дигидро-1-оксофталазин-4-ил-уксусной кислоты (0,35 г) т.пл. 181-183°С (после двух перекристаллизации из метанола).
Исходное вещество получают следующим образом.
1,2-Дигидро-1-oкcoфтaпaзин-4-ил-yкcycнyю кислоту (2,0 г) добавляют к раствору карбоната калия (4,0 г) в днметилфломамиде (50 мл). К этому раствору добавляют бромистый 2-фтор-4-бромбензил (6,0 г), после чего эту смесь перемешивают в течение 15 ч при 60-70°С. Полученный раствор выливают в воде (400 мл). Осадившееся твердое вещество отделяют, хорошо промьшают водой, высушивают в вакууме и растворяют в эт1-тацетате. Полученный раствор фильтруют через колонку с сухим хроматографическим силикагелем (50 г), после чего собирают фракции. Через колонку пропускают дополнительное количество этштацетата, соединяют фракции, содержащие ос новной неполярный компонент (определенный с помощью тонкослойной хроматографии (SiO : толуол/EtOAc; процентное отношение объемов 3:1), и вьшаривают. Полученное твердое нещество дважды перекристаллизовьшают из пропан-2-ола с образованием 2-фто-4-бромбензил-2-(2-фтор-4-бромбензил)-,2-дигидро-1-оксофталазин-4-Ш1-ацетата (1,1 г), т.пл. 125-127°С
(размягчается при 85°С). I
Пример 54. Раствор этил-2-(2,4-дихлорбензил)-1,2-дигидро-1-оксофталазин-4-1 л-ацетата (Л) (1,0 г) .в метаноле (50 мл), содержащем 1М ipacTBOp гидроокиси натрия (10 мл), перемешивают при комр{атной температуре (18-20 С) в течение 36 ч. Этот раствор затем выпивают в воду (250 мл), и полученный водный раствор экстрагируют простым эфиром (2x100 мл). Водную фазу подкисляют концентрированной соляной кислотоГ (до рН 2). Выделившееся твердое вещество собирают, промьшают водой, высушивают в вакууме, а затем перекристаллизовывают из метанола с образованием 2-(2,4-дихлорбензил)-1,2-дигидро-1 -оксофталазин-4-ил-уксусной кислоты (0,8 г, 82%), т.пл. 192193°С.
Пример 55. Процесс проводят аналогично примеру 54, но исходным продуктом является раствор 0,55 г вещества А в диоксане (50 мл), содержащем 2М раствор соляной кислоты (10 мл). Реакционную смесь нагревают при 45°С в течение 36 ч, и без экстрагирования простым эфиром получают 2-(2,4-д1рслорбензил)-1,2-дигидрО-1-оксофталазин-4-ил-уксуснуто кислоту (0,39 г, 73%), т.пл. 192-194°С (рекристаллизованную из метанола).
Исходный материал (А) получен в виде твердого вещества, т.пл. , аналогично примеру 1.
Описанная методика может быть повторена при в течение 18 ч с достижением 60%-ного выхода 2-(2,4-дихлорбензил)-,2-дигидро-I-оксофталазин-4-ил-уксусной кислоты.
I
Пример 56. Процедуру, описанную в примере 54, выполняют с использованием раствора бутил-2-(2-фтор-4-бромбензил)-1,2-дигидро-1 -оксофталазин-4-ил-ацетата, полученного в виде твердого вещества, т.пл. 87-88°С, в результате применения процедуры, аналогичной процедуре, описанной в примере 1 (1,0 г) в этаноле (50 мл), содержащем 1М раствор гидроокиси натрия (10 мл); причем перемешивание производят при 40С в течение 1 ч. При применении той же разработанной процедуры, что и в примере 54, получают 2-(2-фтор-4-бромбензил)-1,2-диг1адро-I-оксофталазин-4-ил-уксусную кислоту (0,6 г, 69%), т.пл. 184-186 с (рекристаллизованную из метанола). 2112 Способность ингибирования ферментативной альдозоредуктазы может быть продемонстрирована в следующем стандартном лабораторном испытании. Так, крысам прививается диабет в результате введения стрептозотоцина, после чего им в течение пяти дней вводится испытуемое соединение. Затем животных убивают и удаляют у i-гих хрусталики глаза и седалищные нервы. После стандартной процедуры обработки в каждой ткани определяются остаточные уровни сорбита, что осуществляется посредством газожидкостной хроматографии после превращения его в производное политриметилсилила. Ингибирование альдозоредуктазы в живом организме затем оценивается посредством сравнения остаточных уровней сорбита в тканях, взятых у страдающей диабетом группы крыс, которым вводилось испытуемое соединение, с группой страдающих диабетом крыс, которым не вводилось испытуемое соединение , и с группой, здоровых крыс, которым не вводилось испытуемое соедине 1ие. Альтернативно может Использоваться модифицированное испытание, в соответствии с которым страдающем диабетом крысам, вызванным введением стрептозотоцина, в течение двух дней ежедневно вводились дозы испьпуемого соединения. Через 2-А ч после вве дения последней дозы животных убивали, удаляли у них седалищные нервы и определяли в них остаточные уровни сорбита в соответствии с описанным Bbmie методом. Активные соединения, используемые в любом из этих испытаний, снижают остаточные уровни сорбита до уровней аналогичным уровням у здоровых; крыс, которым не вводилось это соединение. Однако в общем соединения, имеющие формулу (I), обеспечивают значительное Ингибирование ферментативной аль дозоредуктазы при дозе, вводимой через ротовую полость, равной 100 мг/кг или меньше. Таким образом, посредством иллюстрирования быпо установлено, что 2-(2-фтор-4-бромбензил)-1,2-дигидро-1-оксофталазин-4-ил-уксусная кислота позволила получить ос таточный уровень сорбита в седалищном нерве, равный примерно 60% уровня, обнаруженного у контрольных стра даюпщх диабетом крыс, которым не вво дилось это соединение, через пять дней после приема этого соединения через ротовую полость в количестве, равном 100 мг/кг. При приеме соединений, имеющих формулу (I), . в количестве, равном 100 мг/кг, в процессе описанных испытаний не было обнаружено явных токсических или других нежелательных явлений. Способность ингибирования ферментативной альдозоредуктазы можно также продемонстрировать в лабораторных условиях. Для этого очищенная альдозоредуктаза вьщеляется известным способом из бычьих хрусталиков глаз. Затем посредством стандартных спектрофотометрических методов производится определение процентного значения ингибирования этого фермента в лабора;торных условиях в результате восстановления альдозов в многоатомные спирты, в частности в результате восстановления глюкозы в сорбит под воздействием испытуемого соединения. В этом испытании соединения формулы (I), в которой R представляют гидроксильный радикал, показьшают значительное Ингибирование ферментативной альдозоредуктазы при концентрации в диапазоне 10 -10 моль или меньше. Таким образом, 2-(2-фтор-4-бромбензил)-,2-дигидро-1-оксофталазин-4-ил-уксусная кислота характеризуется коэффициентом ингибирования (К J), равным 2,0x10 моль. Когда предлагаемое соединение используется для оказания воздействия на ферментативную альдозоредуктазу у теплокровных животных, оно может вводиться прежде всего через ротовую полость при ежедневной дозе 2-50 мг/кг, что эквивалентно для человека общей ежедневной дозе в диапазоне 20-750 мг на человека, даваемой при необходимости отдельными дозами. Данные об ингибирующих альдозоредуктазу свойствах, характерных для фталазин-4-ш1-уксусных кислот. Испытания проводят в течение 2-5 дней. В течение этого периода явные признаки токсическог.о действия отсутствовали при использовании любого Из испытуемых -соединений. Ингибкрующая активность характерных фталазин-4-ил-уксусных кислот по отношению к альдозоредуктазе. Q) Самцов крыс (110-130 г, линия Alder ey Park специфическая патогенность отсутствует) приводят в диабетическое состояние известным способом, вводя стрептозотоцин, и вьщерживают в течение двух недель, после чего проверяют наличие у них состояния тяжелой глюкозурий. После этого группам по шесть животных ежедневно орально вводят испытуемое соединение в течение 5 дней. Затем животных забивают и быстро удаляют у них седали ные нервы. Образцы ткани взвешивают и углеводы экстрагируют кипячением в воде, в которую добавляют известное количество о( метил-В-маннозида в качестве внутреннего стандарта. Белковые соединения удаляют, после чего свободные от белка растворы лио филизуют. Оставшееся углеводное соединение после этого превращают в со ответствующее тринетилсилильное производное и остаточную концентрацию сорбита определяют газожидкостной хр матографией на колонке с носителем 2,5% SE-52,(диатомит, С 80-100 меш) полученным с кислотой и затем силированным с помощью дихлорметилсилана при 185°С. Ингибирование апьдозоредуктазы оценивают затем, сравни вая остаточные концентрации сорбита в тканях группы крыс-диабетиков с введенным соединением и в тканях группы крыс-диабетиков, которым вводили только инвертньй фармацевтический носитель. Это испытание известно как Пятидневное испытание.
4-Вг
ет 4-13-Ct-4-Br ОН О
2-F-4-Br ОН S
ет
Таблица 6
36 66 32 80 33 31
50
ОН О 100 20 50 20 ОН О
10
66 100
36
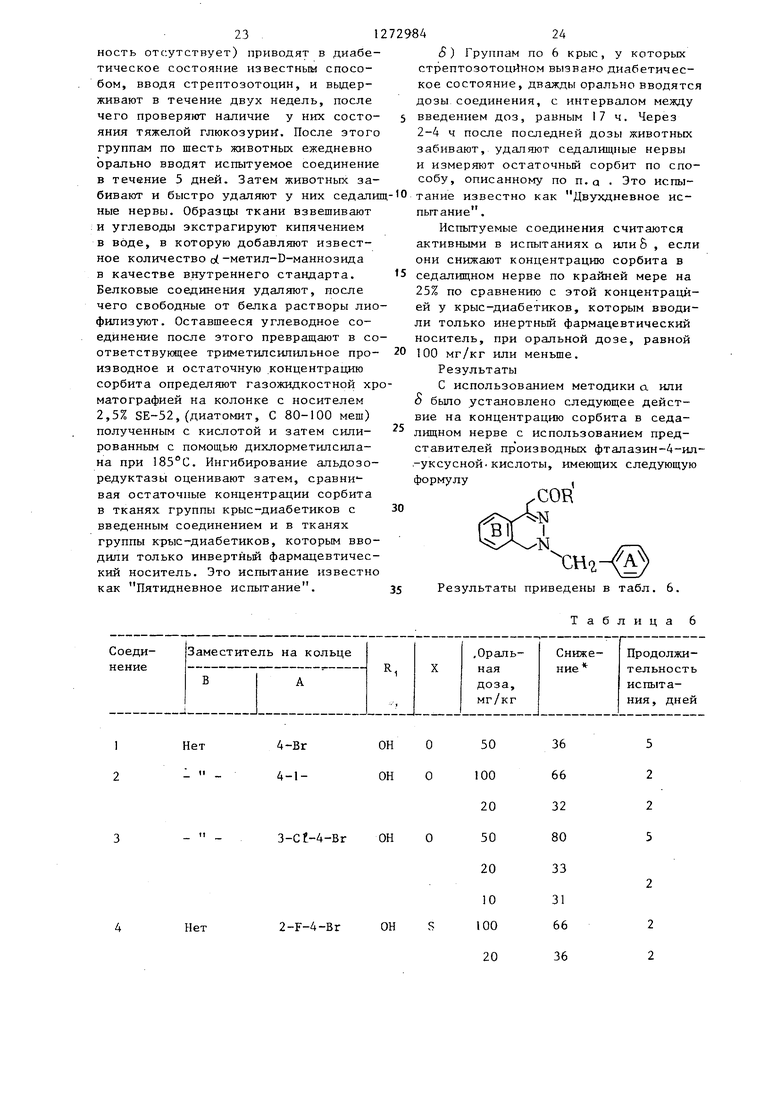
20 5) Группам по 6 крыс, у которых стрептозотоцйном вызвано диабетическое состояние, дважды орально вводятся дозы соединения, с интервалом между введением доз, равным 17 ч. Через 2-4 ч после последней дозы животньсх забивают, удаляют седалищные нервы и измеряют остаточный сорбит по способу, описанному по п.Q . Это испытание известно как Двухдневное испытание . Испытуемые соединения считаются активными в испытаниях а или 5 , если они снижают концентрацию сорбита в седалищном нерве по крайней мере на 25% по сравнению с этой концентрацией у крыс-диабетиков, которым вводили только инертный фармацевтический носитель, при оральной дозе, равной 100 мг/кг или меньше. Результаты С использованием методики а или S было установлено следующее действие на концентрацию сорбита в седалищном нерве с использованием представителей производных фталазин-4-ил-уксусной-кислоты, имеющих следующую формулу. Результаты приведены в табл. 6.
25
26
1272984 Продолжение табл.6
Процент снижения концентрации сорбита в седалищном нерве по сравнению с концентрацией у контрольных крыс-диабетиков, которым не вводили лекарства (,1, обычно 0,01); Смесь 1:1 6-метильного и 7-метильного производных. Для сравнения указываем, что струк турно подобное соединение 1-бензил-1,2-дигидро-1-оксофталазин-4-ил-уксусная кислота вызывает повышение на 2% (при оральной дозе 200 мг/кг) и повьшение на 12% (при оральной дозе 100 мг/кг) концентрации сорбита в седалищном нерве по сравнению с концентрацией у, контрольных- животных.

| Вейганд-Хильгетаг | |||
| Методы эксперимента в органической химии | |||
| - М.: Химия, 1968, с | |||
| Станок для нарезания зубьев на гребнях | 1921 |
|
SU365A1 |
Авторы
Даты
1986-11-23—Публикация
1981-12-04—Подача