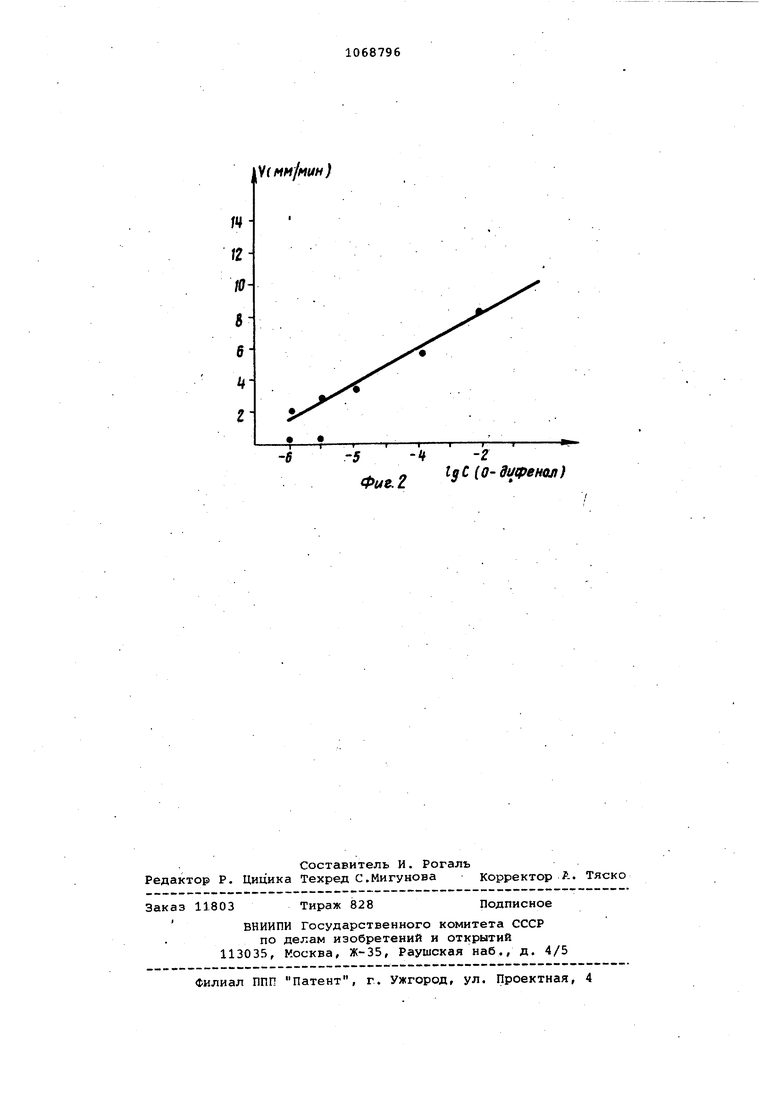
Изобретение относится к анализу сточных вод и может быть использов но для количественного определения 0-дифенолов - основных компонентов сточных вод предприятий целлюлозно бумажной , нефтехимической и других отраслей промышленности. Известен способ определения 0-дифенолсв колориметрическим метод основанным, на реакции О-дифенолов ионами железа в кислой среде. В ре зультате.этой реакции ргствор окраш вается в фиолетовый цвет, интенсивно которого пропорциональнё содержанию многоатомных фенолов.. Результаты опр деления этого метода не всегда воспро ИЗВОДИМЬ fl . Недостатком этого метода являетс низкая чувствительность ,(интервал определяемых концентраций 1-10 К )и точность определения, которая- обусловлена тем, что аналитические Лолосы поглощения анализируемых веществ перекрываются с полосами поглощения сопутствующих компонентов стоков. Наиболее близким техническим решением к изобретению является способ определения о-дифенолов в водных растворах, включающий измерение электрохимического сигнала. Сущность этого способа заключается в измерении скоростей окислительновосста.новительного потенциала при введении, в анализи уемую пробу ацетонового препарата о-дифенолоксидазы при концентрации 100300. мг/л, рН 5,5-6,8 2. Недостатком известного, способа является применение неустойчивого ферментного препарата, который необходимо специально готовить, Лранить при определенных условиях {устойчив на воздухе до месяца), чтобы избежать инактивирования. Целью изобретения является упрощение определения. Поставленная цель достигается тем, что согласно способу определения о-дифенолов в водных растворах, включакэде}му измерение эйектрохиммческого сигнала, устанавливают рН 6-8анализируемого раствора, вводят 1-10- - 1. о-бензохинона или о-хлоранила или о-броманиЛа, а. в качестве сигнала фиксируют изменение тока при 0,23 0,01 В.. / Сущность способа заключается в применении в качестве реагента о-бензохинонов или 0-броманила или о-хлоранила и фиксирования кинетики их распгда при катализе о-дифенолов, присутствующих в пробе. о-Дифенол катализирует реакцию распада Отбензохинонов при рН 6,5-7,0. В оптимальных условиях проведения реакции наблюдается пропорциональная зависиMOCTj между скоростью распада О-бен3охинона и концентрацией о-дифенола в интервале 10 - 10 М. Предел обнаружения составляет 0,1 мг/л. На фиг. 1 приведены кинетические кривые распада о-бензохинона С1 ) при введении различных добавок о-дифенола {1-0 Мг/л, 2-1-10 К, 3-1.-10 М, 4-1-10 М, 5-J., 6-1-10 М, 7-1-16 м); на фиг. 2 - градуировочная кривая скорости распада о-бензохинолина от IgC О-дифенола. В табл. 1 приведена зависимость скорости распада о-бензохинона от концентрации О-дифенола. В табл. 2 приведена зависимость скорости распада о-бензохинона от его концентрации при С п/1 1 -Ю- . Таблица 1
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения цианидов | 1982 |
|
SU1057838A1 |
| Способ определения церия ( @ ) | 1982 |
|
SU1056038A1 |
| Способ получения бутилкаучука | 1973 |
|
SU505371A3 |
| Способ определения активностиНАдН- и НАдфН-гЕНЕРиРующиХ дЕгидРОгЕНАз | 1978 |
|
SU794071A1 |
| МОДИФИЦИРОВАННАЯ 4- | 1979 |
|
SU825543A1 |
| Способ определения меркаптанов и аминов в смеси | 1981 |
|
SU972384A1 |
| Способ определения активности фенолоксидаз | 1981 |
|
SU1027208A1 |
| Способ определения кватерона в фармацевтических препаратах | 1980 |
|
SU938150A1 |
| ЭКСПРЕСС-СПОСОБ БИОТЕСТИРОВАНИЯ ПРИРОДНЫХ, СТОЧНЫХ ВОД И ВОДНЫХ РАСТВОРОВ | 2009 |
|
RU2413771C2 |
| Способ определения растворенного в воде кислорода | 1980 |
|
SU945063A1 |
СПОСОБ ОПРЕДЕЛЕНИЯ О-ДТЛФЕНОЛОБ В ВОДНЫХ РАСТВОРАХ, включающий измерение электрохимического Сигнала, отличающийся тем, что, с целью упрощения определения, устанавливают рН 6-8 анализируемого раствора, вводят lld3 d о-бензохинона или о-хлоранила, или о-броманила, а в качестве сигнала фиксируют изменение тока при 0,23 1 0,01 В. (Л О5 00 ф о: S т, мин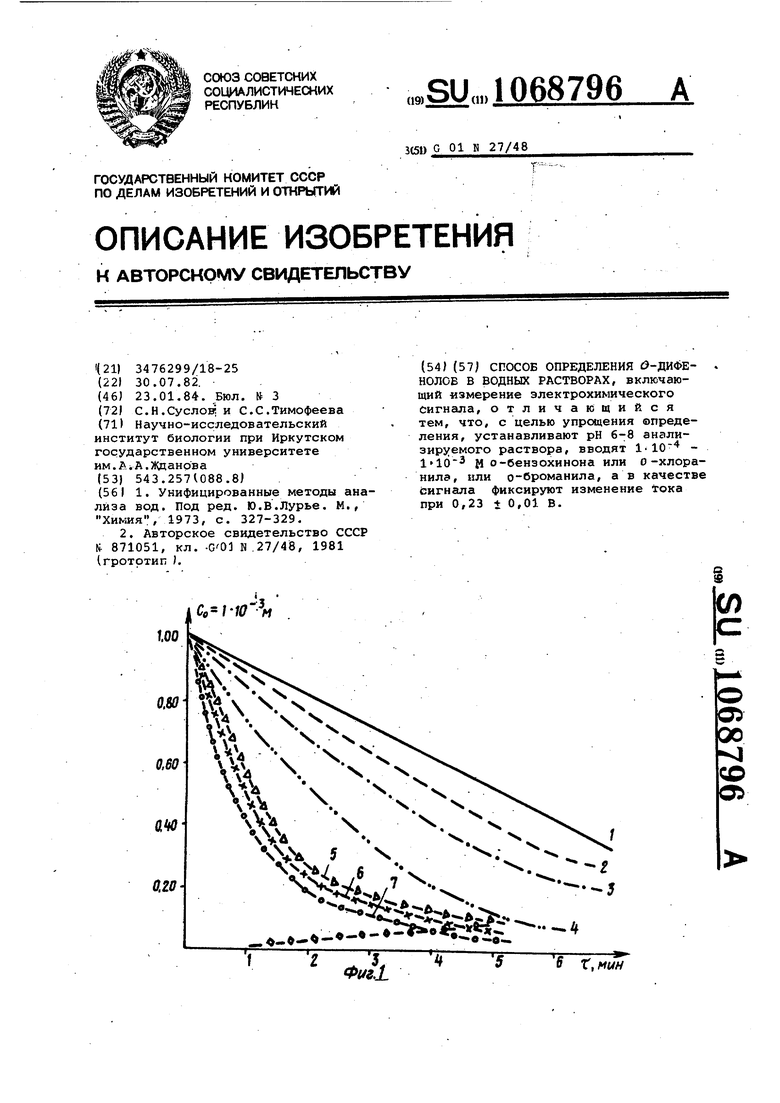
3,2
2,0
Скорость распада О-бензохиноча
6,9
мМ/мин
5,4
6,9
8,0
Таблица 2
6,9
6,9 Область рН 6,5-7,0 выбирается с учетом скорости и периода полураспада хинонов. В табл. 3 указаны .значения скорости распада о-бензрхинона, которые достигают максималь ного значения при рН.8-9 и минималь ного при рН 4-5, однако вести анализ в этих условиях затруднительно так как в первом- случае идет интенсивная побочная реакция гидроксилирования о-хинонов, а во втором кислотный катгшиз, маскиру1Ш1Ий ускоряющее действие 0-дифенолов, поэтому наиболее приемлемым оказывается диапазон рН 6-7, где имеет место ярко выраженный автокаталитический характер реакции распада О-хинонов. Концентрация о-хинона; требуемая для ангшиза, варьируется от I-IQ-
:i::::i::: :::L:::i:i::::i:: ::: :: :::i
Скорость распада
0-бензохинона,
мМ/мин
4,0
П р и м е р. Пробу, содержащую 0,011-;0,1 мг/л О-дифенола, доводят рН фосфатным буфером до 6,0-8,0 и отбирают для анализа 9 мл. В стакан, ем.костью 50 мл вводят 9 мл пробы и при перемешивании на магнитной мешалке(и; 1000-1200 об/мин ), вводят в течение 1-2 с 1 мл раствора 0-бензохинона или ортохлоранила или о-бр6манила, прй этом концентрация их поддерживается в диапазоне 1-10 - 1., и фиксируют изменение величины тока при E-IJ, в течение мин (в зависимости от концентрации О-дифенола i). В стаканПредлагаемый способ позволяет исключить использование малодоступного ферментного препарата, сокра7,И
6,9
7,0
чики опускают два электрода: индикаторный - платиновый или пирографитовый, электрод сравнения - насыщенный каломельный. Концентрацию 0-дифенолов определяют по гредуировочному графику скорость распада т концентрация 0-дифенолов (фиг. 2).
ГХ -дифенолы и другие фенолы определению не ме1иают, так как не проявляют каталитического действия
в исследуемом интервале концентраций.
Результаты определения о-дифеноов ,95, п 9 приведены в табл. 4, Т а б л и ц а 4
тить время, затрачиваемое на приготовление препарата, и упростить определение о-дифенолов. до i., хотя начальные скорости распада о хинонов в присутствии о-дифенола равны (табл. 2Ги не зависят от начальной концентрации о-хинона, но глубина превращения и периоды полураспада ( f различны, (возрастают по мере уменьшения концентрации от 1, до 1. почти в сто раз) и работать с коицентрацией о-хинона 1-10 М неудобно, «следствие увеличения времени для анализа. Концентрации выше применять также нецелесообразно ввиду указанной зависимости V / от концентрации и очень быстрого самопроизвольного распада. В табл. 3 приведена зависимость скорости распада о-бёнзохинона от рН растворе (С х,„оног I-IO M, С n/tf в 1г10-М). Таблица 3
у (мм/мин)
w
/2105
бitг-6 -5 -t -2
Фиг. 2 3f(0-di/9eH(ui)
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Под ред | |||
| Ю.В.Лурье | |||
| М., Химия, 1973, с | |||
| Перепускной клапан для паровозов | 1922 |
|
SU327A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ количественного определения пирокатехина в водном растворе | 1979 |
|
SU871051A1 |
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1984-01-23—Публикация
1982-07-30—Подача