Изобретение относится к нитрофенилимидазолам, а именно 4(5)- (3-нитро-4-(3,3-диметилтриазено-1)фенил)имидазол формулы: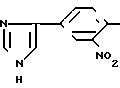 N N-N(CH3)2
N N-N(CH3)2
(I) обладающему противоопухолевой активностью.
Известен гидрохлорид L- α -амино-β -(пара-бис( β -хлорэтил)аминофенил)пропионовой кислоты (сарколизин), обладающий противоопухолевой активностью.
Ближайшим структурным аналогом соединения (I) является 4(5)-(3,3-диметилтриазено-1)имидазол-5(4)-карбоксамид (ДТИК), применяемый в клинике при лечении злокачественной меланомы.
Однако ДТИК, как и сарколизин, существенно угнетает костно-мозговое кроветворение, влияет на желудочно-кишечный тракт, вызывая анорексию, тошноту и рвоту.
Цель изобретения расширение арсенала средств воздействия на живой организм.
Поставленная цель достигается предлагаемым новым соединением (I), которое получают диазотированием 4(5)-(3-нитро-4-аминофенил)имидазола нитритом натрия в соляной кислоте с последующим взаимодействием полученной диазониевой соли с диметиламином.
Чистоту соединения (I) проверяют тонкослойной хроматографией на силуфоле UV-254 в системе растворителей н-бутанол уксусная кислота вода 4:1:5 (проявление ультрафиолетовым светом); молекулярный вес соединения (I) определяют на приборе МХ-1303 с прямым вводом образца в ионный источник; ПМР- и УФ-спектры сняты на спектрометре "Varian-Т-60" и спектрофотометре "Specord UV Vis".
П р и м е р. 4(5)-(3-Нитро-4-(3,3-диметилтриазено-1)фенил)имидазол (1).
В колбу, снабженную мешалкой, термометром и капельной воронкой, помещают 3,2 мл концентрированной соляной кислоты, 12 мл воды и при перемешивании добавляют 2,1 г (0,01 моль) 4(5)-(3-нитро-4-аминофенил)имидазола. Затем колбу охлаждают льдом с солью и при температуре (-3)-(-4)оС добавляют по каплям раствор 0,8 г нитрита натрия в 4 мл воды. Смесь перемешивают при этой температуре 4-5 мин и выливают на мелко раздробленный лед, содержащий 4 г 33%-ного раствора диметиламина. Выпавший осадок отфильтровывают, перемешивают с 20 мл метанола при температуре 50-55оС и отфильтровывают. Выход 1,2 г (46,1%), т. пл. 174-176оС (с разложением), Rf 0,45.
Найдено, C 50,50; H 4,41; N 32,11.
C11H12N6O2
Вычислено, C 50,76; H 4,65; N 32,29.
М-260 (масс-спектрометрически).
В ПМР-спектре (снят в дейтерированном диметилсульфоксиде, внутренний эталон ТМС) наблюдаются сигналы ароматических протонов гетероцикла и бензольного кольца в области 7,25-8,10 м.д. (5 протонов, мультиплет) и три сигнала двух метильных групп при 3,13; 3,30 и 3,46 м.д. (6 протонов). Расщепление сигналов протонов метильных групп можно объяснить инверсией у атома N2 и заторможенным вращением вокруг связи N2-N3 (N-N(CH3)2)
В УФ-спектре присутствуют три максимума в области 333, 282 и 205 нм.
Биологические исследования проводили на белых беспородных мышах и крысах обоего пола весом 18-20 и 90-110 г соответственно.
Соединение (I) вводили животным внутрибрюшинно, а в отдельных опытах перорально, в 0,5%-ном растворе карбоксиметилцеллюлозы. Сарколизин применяли в 0,9%-ном растворе хлорида натрия.
Острая токсичность изучалась на мышах при однократном внутрибрюшинном введении. При этом установлены абсолютно смертельная (ЛД100), средняя смертельная (ЛД50) и максимально переносимая (МПД) дозы.
Противоопухолевая активность определялась на 7 моделях перевиваемых опухолей мышей и крыс.
Лечение животных с лимфосаркомой Плисса, лейкозом Швеца, саркомой 37 и асцитной карциномой Эрлиха проводили через 24 ч после перевивки, а с саркомами 45, 180 и карциносаркомой Уокера на 4-5 сутки роста опухоли. Соединения вводили ежедневно в течение 6 (для мышей) и 8 (для крыс) дней в эквитоксических дозах 1/12-1/15 от ЛД100. Подопытные и контрольные группы состояли из 8-10 животных.
В химиотерапевтических опытах с солидными опухолями через день после последней инъекции животных забивали эфиром и определяли вес животного и опухоли. О терапевтическом эффекте судили по проценту торможения роста опухоли (Т%), а об общетоксическом действии по коэффициенту роста (Кр).
Мышей с асцитными формами опухолей (саркома 37, асцитная карцинома Эрлиха) после окончания курса лечения оставляли на выживаемость. Погибших в течение опыта животных взвешивали и вскрывали для установления наличия или отсутствия асцитической жидкости. Противоопухолевое действие оценивали по увеличению средней продолжительности жизни мышей (СПЖ).
Полученный цифровой материал подвергали статистической обработке по методу Стьюдента-Фишера.
В результате проведенных исследований установлено, что заявляемое соединение по токсичности практически не отличается от ДТИК. Вместе с тем оно в 40-50 раз менее токсично, чем сарколизин (табл. 1). Так, абсолютно смертельная доза соединения I и сарколизина составляет 1250 и 30 мг/кг соответственно.
В табл. 1 приведены показатели острой токсичности соединения (I), сарколизина и ДТИК.
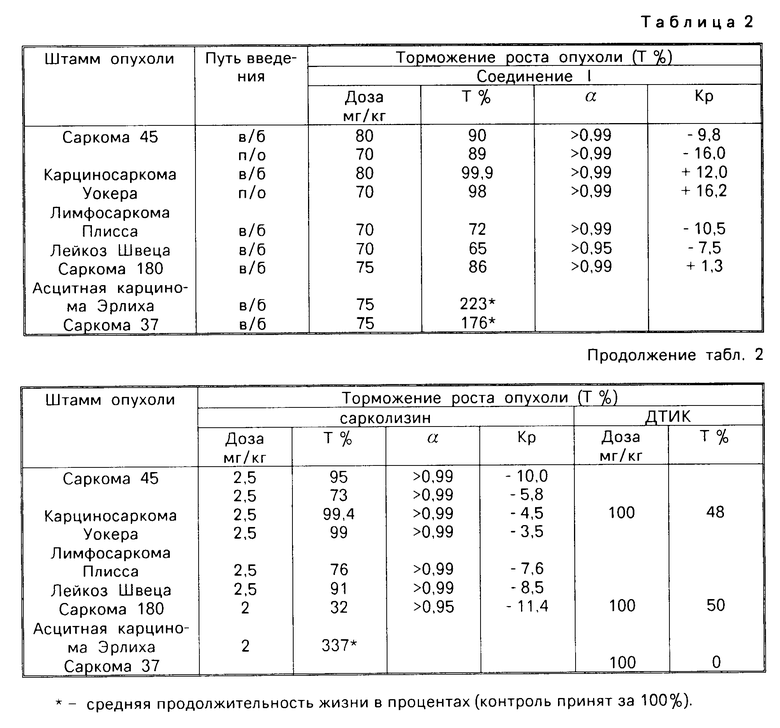
В табл. 2 приведены показатели противоопухолевой активности соединения (I), сарколизина и ДТИК.
В химиотерапевтических опытах выявлено, что заявляемое соединение, подобно сарколизину, проявляет высокую противоопухолевую активность в отношении саркомы 45 и карциносаркомы Уокера, угнетая их рост на 90-99,9% Согласно литературным данным ДТИК в оптимальных терапевтических дозах на карциносаркоме Уокера 256 оказывает слабое противоопухолевое действие, ингибируя ее рост на 52-55% На вышеуказанных моделях соединение (I) сохраняет высокую антибластическую активность (Т% 89-98) и в случае перорального применения, в то время как при воздействии сарколизина торможение роста саркомы 45 снижается на 22%
На лимфосаркоме Плисса соединение (I) оказывает равную с сарколизином активность (Т 72 и 76 соответственно), а по терапевтическому действию на лейкоз Швеца и асцитную карциному Эрлиха несколько уступает ему.
Заявляемое соединение по ингибирующему действию на рост саркомы 180 существенно превосходит как ДТИК, так и сарколизин. Так, в адекватных дозах сарколизин и ДТИК угнетают рост данной опухоли на 32 и 50% соответственно, а соединение (I) на 86%
Выраженное преимущество заявляемого соединения по сравнению с ДТИК установлено также при лечении мышей с саркомой 37. Данная экспериментальная модель практически не чувствительна к действию ДТИК при подкожном способе его введения. Соединение (I) вызывает достоверное увеличение (1,8 раза) средней продолжительности жизни животных с саркомой 37.
Таким образом, заявляемое соединение малотоксично, обладает широким спектром терапевтического действия и по активности близко к известному в клинике препарату сарколизину. Одновременно по ингибирующему действию на ряд перевиваемых опухолей животных соединение (I) значительно превосходит 4(5)-(3,3-диметилтриазено-1)имидазол-5(4)-карбоксамид.

4(5)-(3-Нитро-4-(3,3)-диметил-триазено-1) фенил)имадазол формулы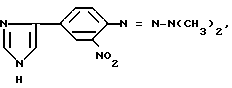
обладающий противоопухолевой активностью.
| М.А.Ирадян, С.А.Саргисян, А.П.Енгоян, В.С.Мирзоян | |||
| Производные имидазола | |||
| XIV | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
1995-10-10—Публикация
1982-07-29—Подача