О 00
ел
Изобретение относится к аналит -ческой химии, в частности к инверсионно-электрохимическим методам анализа, и может быть использовано в химической, металлургической, горной и пищевой промшиленности для определение микро- и ультрамикроколичеств элементов в растворах электролитов .
Известен способ формирования электрода для определения микроколичеств амальгаммо-образующих элементов, например свинца, кадмия, цинка, путем нанесения на графитовый стержень микроколичеств ртути из водного раствора электролита, содержащего 1.10-2 MHg (HOjj.c последующим концентрированием на электроде определяемого элемента, дальнейшим его анодньпи растворением с получением на полярографе кривой анодного электрорастворения, аналитический сигнал на которой пропорционален концентрации определяемого элемента в растворе. Присутствие ртути на электроде обеспечивает концентрирование определяемого элемента на поверхности электрода за счет образования амальгамм определяемого элемента с ртутью
С помощью этого электрода можно определить микроколичества элементов, концентрация которых в электролите составляет 1 мкг/л и более при времени их накопления на электроде в течение 10-60 мин 1.
Недостатком сформированного данным способом электрода является его невысокая чувствительность в связи с невозможностью создания на его поверхности устойчивых сорбционных центров концентрирования определяемого элемента, что не позволяет получить четкую нераздвоенную кривую его электрорастворения и иметь достоверный результат определения.
Наиболее близким к предлагаемому по технической сущности является способ формирования электрода для инверсионно-электрохимического определения микро- и ультрамикроколичеств элементов, заключающийся в нанесении из электролита на графитовый стержень микроколичеств металла, стоящего в электрохимическом ряду напряжений ниже определяемого элемента , Металл служит для удержания определяемого элемента после концентрирования его на электроде благодаря химическому взаимодействию между определяемым элементом и металлом и способствует дальнейшему анодному растворению определяемого элемента. При определении микроколичест свинца (Рв), ионов сульфидов (3), никеля (Ni), мышьяка (As), ионов фосфатов(РО д ) в качестве металла, нанесенного на графитовый стержень,
используют соответственно ртуть, серебро, платину, золото, висмут C2J
Недостатком сформированного известным способом электрода является его низкая чувствительность, ,ко±орая не позволяет получить четкую нераздвоенную кривую анодного электрорастворения определяемого элемента и судить по ней о достоверности результатов количественного анализа из-за отсутствия на поверхности электрода устойчивых сорбционных центров концентрирования. Количественное определение элемента с помощью электрода, сформированного известным способом, является длительным, так как связано с продолжительным {1-1,5 ч) накоплением элемента на электроде.
Целью изобретения является повышение чувствительности электрода за счет получения на нем устойчивых сорбционных центров концентрирования определяемого элемента.
Поставленная цель достигается тем, что согласно способу формирования электрода для инверсионноэлектрохимического определения микрои ультрамикроколичеств элементов путем нанесения из электролита йа графитовый стержень микроколичеств металла, стоящего в электрохимическом ряду напряжений ниже определя емого элемента, на графитовый стержень из электролита дополнительно наносят ультрамикроколйчества металла, стоящего в электрохимическом ряду напряжений выше металла нанесенного на графитовый стержень.
Кроме того, концентрация наносимого дополнительного металла в электролите составляет 0,1-10,0 мкг/л.
Дополнительное нанесение из электролита на графитовый стержень ультрамикроколичеств металлов более электроотрицательных, чем нанесенный на него металл, способствует повышению чувствительности определения за счет создания на поверхности электрода устойчивых сорбционных центров концентрирования, на которых накапливается и удерживается определяемый элемент, что позволяет при дальнейшем анодном электрорастворении сконцентрированного элемента получить четкую, нераздвоенную кривую, пропорциональную концентрации элемента в растворе, кроме того, ускоряется процесс концентрирования, продолжительность которого сокращается в 6 раз и составляет 5-10 мин. Таким образом, с помощью сформированного предлагаемым способом электрода появляется возможность определять элементы, концентрация которых в растворе .составляет менее 1 мкг/л, а именно 0,01-1 мкг/л. При концентрации в электролите ультрамикроколичества металлов наносимых на графитовый стержень, менее 0,1 мкг/л чувствительность определения на сформированном элек роде еще невелика, так как количес ва металлов недостаточно для созда ния на поверхности электрода устой чивых сорбционных центров концентрирования. В то же время введение в электролит ультрамикроколичеств металлов более 10,0 мкг/л нецелесо образно, так как достигнутая максимальная чувствительность определения при увеличении вводимых в раствор ультрамикроколичеств метал лов более 10,0 мкг/л не изменяется. Примеры. Осуществлялось формирование электрода для определения ультрамикроколичеств свинца, кадмия и цинка в растворах электролитов, содержащих 100 мг/л Hg (КОзЬ Если в растворе содержатся микро количества элемента, то количество покрытия, образующегося на электрод равно 10 -10 г/см, для ультрамикроколичеств эта величина меньше .чем 10 г/см. Понятия микроколичест vi ультрамикроколичество относятся к концентрации элементов в растворе Понятие микроколичество элементов означает, что концентрация элемента в растворе составляет 10 или 10-100 мкг/л. Понятие ультрамикроколичество означает, что концентрация элемента в растворе меньше, чем 10 моль/г или 10,0 мкг/л. На графитовый стержень из раство ров электролитов при потенциале 1,5 В наносились кшкроколичества ртути - металла, стоящего в электро химическом ряду напряжений ниже определяемых элементов. Определение свинца осуществлялось в О,1 М растворе НС1, определение кадмия и цинка в 0,1 М растворах . Затем в каждый из растворов электролитов поочередно добавлялись 0,09; 0,1; 10; 20 мкг/л ультрамикроколичеств металлов, стоящих в электрохимическом ряду напряжений выше ртути, которые из электролитов дополнительно наносились на графитовый стержень при потенциале 1,5 В. При определении свинца в качестве ультрамикроколнчеств использовались висмут (Bi), медь (Си), цинк (Zn), кадмий (Cd), галлий (Gal, для определения кадмия - галлий, для определения цинка - .железо. Затем осуществлялось концентрирование каждого из определяемых элементов иэ исследуемого раствора . .-. . электролита на поверхность сформированного указанным способом электрода. Концентрирование свинца и кадмия осуществлялось при потенциале 1,5 В, а цинка - при потенциале 1,7В. Продолжительность концентрирования каждого из определяемых элементов на сформированном электроде составляет 2 мин. Сконцентрированный на электроде осадок каждого из определяемых .- ментов подвергался анодному электрорастворению в дифференциальном режиме при скорости развертки электрорастворения 0,4 в/с, в процессе которого регистрировалась кривая электрорастворения, высота аналитического сигнала на которой пропорциональна концентрации определяемого элемента в растворе и времени концентрирования. В таблице представлены сравнительные данные по определению концентраии перечисленных элементов с помощью электрода, сформированного предлагамым и известным способами.
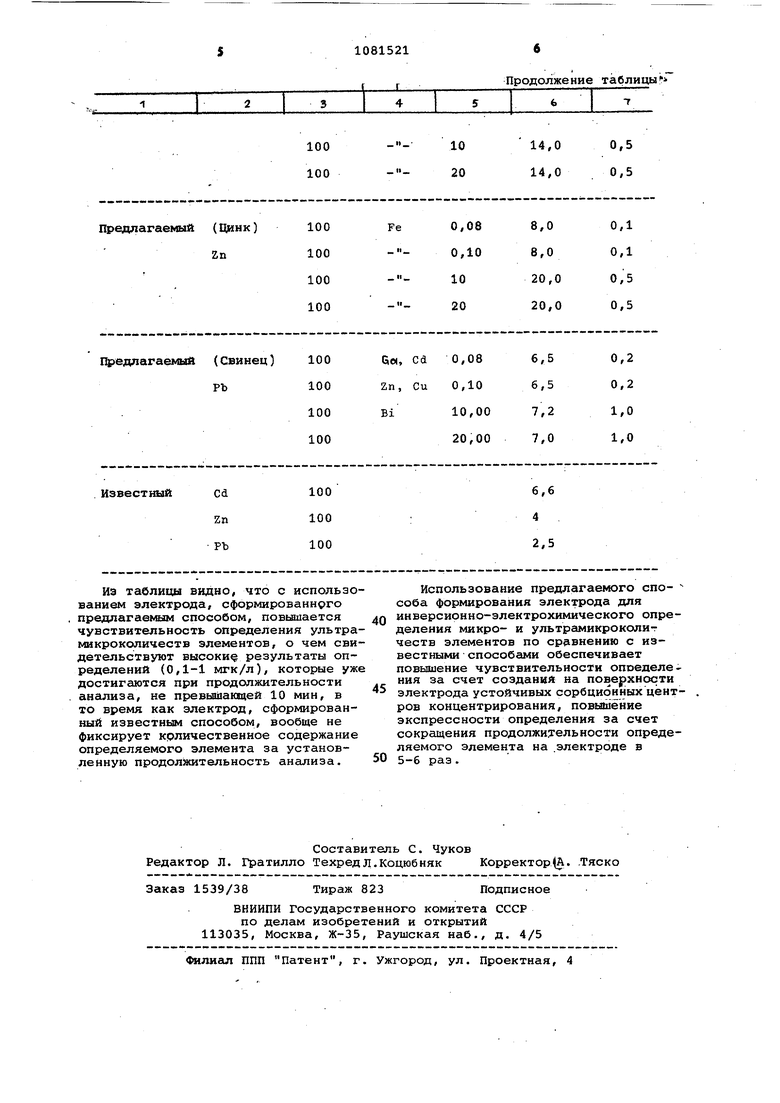
Продолжение таблицы

1. СПОСОБ ФОРМИРОВАНИЯ ЭЛЕКТРОДА ДЛЯ ИНВЕРСИОННО-ЭЛЕКТРОХИ- . МИЧЕСКОГО ОПРЕДЕЛЕНИЯ МИКРО- И УЛЬТ- . РАМИКРОКОЛИЧЕСТВ ЭЛЕМЕНТОВ путем нанесения из злектрюлита на графитовый стержень микроколичеств металла, стоящего в электрохимическом ряду напряжений ниже определяемого элемента, отличающийся тем, что, с целью повышения чувствительности электрода за счет получения на нем устойчивых сорбционных центров концентрирования определяемого элемента, на графитовый стержень из электролита дополнительно наносят ультрамикроколичества металла, стоящего в электрохимическом ряду напряжений выше металла, нанесенного на графитовый стержень. 2. Способ поп.1,отличаю щ и и с я тем, что используют электролит, содержащий дополнительно )) наносимые металлы в количестве 0,110,0 мкг/л.
100 100
(Цинк)
100 100 Zn 100 100
(Свинец)
100 100 РЪ 100 100
100
Cd Zn РЪ 100 100 Иэ таблицы видно, что с использованием электрода, сформированнрго предлагаем 1М способом, повышается чувствительность определения ультрамикроксличеств элементов, о чем свидетельствуют высоки результаты определений (0,1-1 мгк/л), которые уже достигаются при продолжительности анализа, не превышающей 10 мин, в то время как электрод, сформированный известным способом, вообще не фиксирует крличественное содержание определяемого элемента за установленную продолжительность анализа.
-
10 20
14,0 0,5 14,0 .0,5
0,08
0,1
8,0 0,10
- 0,1 8,0 10 20 20,0 0,5
U 20,0 0,5
0,08
6,5
0,2
Cd 0,10 6,5 0,2
Си 10,00 7,2 1,0 20,00 7,0 1,0
6,6
4 2,5 Использование предлагаемого спо- соба формирования электрода для инверсионно-электрохимического определения микро- и ультрамикроколиг честв элементов по сравнению с известными способами обеспечивает повышение чувствительности опоеделе ния за счет создания на поверхности электрода устойчивых сорбциоиных центров концентрирования, повышение экспрессности определения за счет сокращения продолжительности определяемого элемента на .электроде в 5-6 раз.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Chem | |||
| Progress in Potarography, 1970, p | |||
| ТЕЛЕФОННЫЙ АППАРАТ, ОТЗЫВАЮЩИЙСЯ ТОЛЬКО НА ВХОДЯЩИЕ ТОКИ | 1920 |
|
SU273A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Патент CDJA № 3855099, КЛ | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство станционной централизации и блокировочной сигнализации | 1915 |
|
SU1971A1 |
Авторы
Даты
1984-03-23—Публикация
1983-01-25—Подача