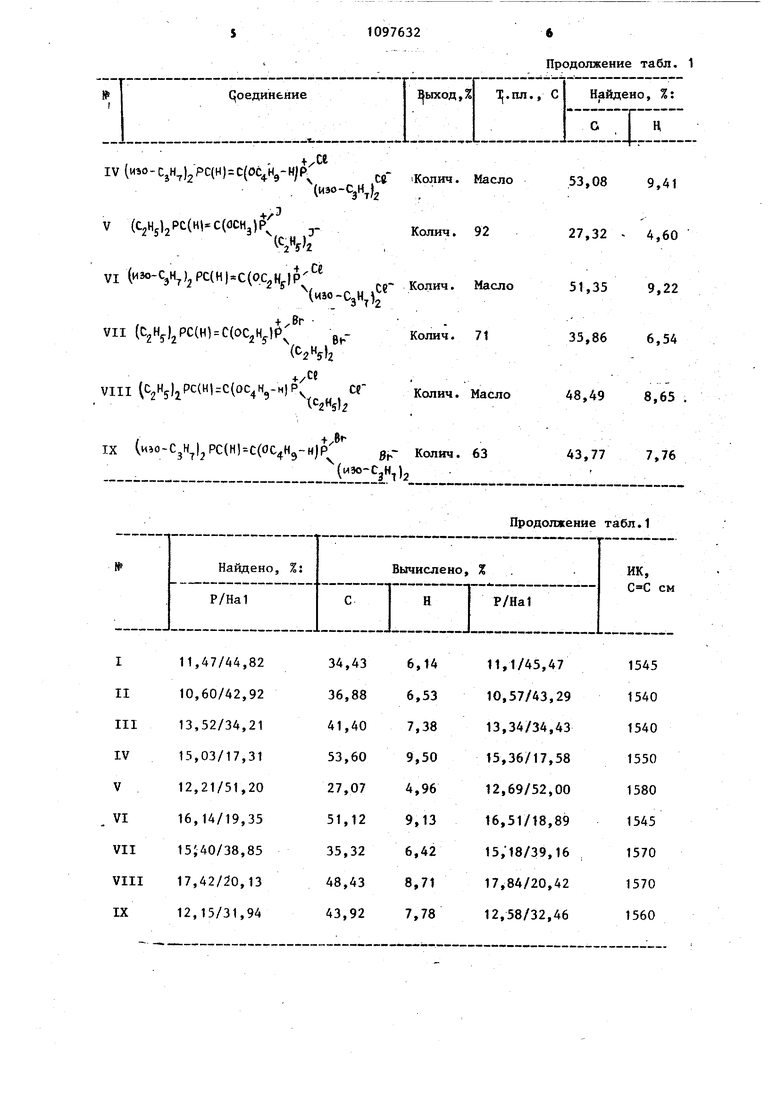
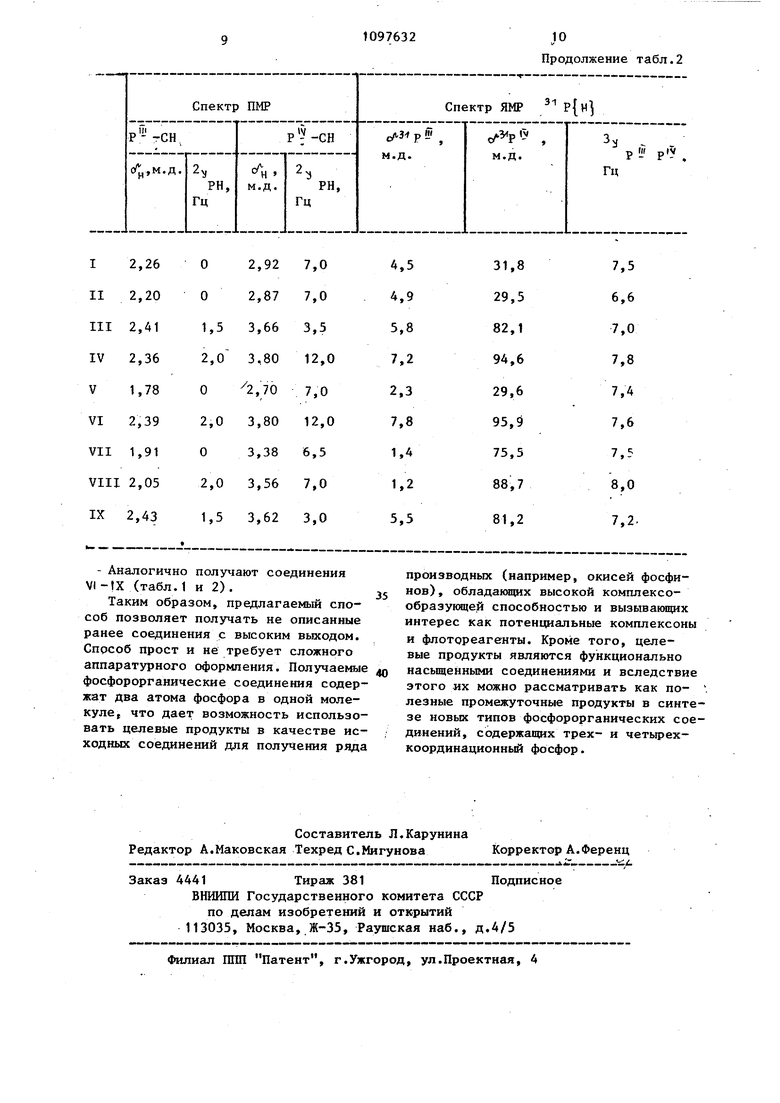
110 Изобретение относится к химии фосфорорганических соединений с С-Р свя зью, а именно к новому способу получения бисфосфорилированных винилалкиловых эфиров общей формулы C(, , (; где R - этил, изопропил R - алкил ., X - хлор, бром, иод. Эти соединения в литературе не описаны, являются новыми и могут найти применение в качестве полупродуктов для фосфорорганического синтеза, Известен способ .получения бисдиэтилфосфиноэтилена гидрированием бисдиэтилфосфиноэтина над катализатором Никель-Ренея в этиловом спирте при атмосферном давлении, выход целевого продукта составляет 57% f1 . Известен также способ получения бисдифенилфосфиноэтилена взаимодействием дифенилфосфида лития с 1,2-дихлорэт1шеном при нагревании в среде тетрагидрофурана, выход целевого продукта 80% 2. Этим же способом получен бисдибутилфосфиноэтилен (25%) 3. Со.единение, содержащее два атома фосфора различной координации (моноокись бисдибутилфосфиноэтилена), полу чено двумя способами: присоединением дибутилфосфина к окиси дибутилзтинилфосфина в запаянной ампуле при 150160 С в течение 24 ч (выход 22%) или V,/ (.IV-AliIAV. r Я lb «./a / присоединением дибутилфосфористой кис лоты к дибутилэтинилфосфину в присутствии азобисизобутиронитрила (катализатора радикального присоединения) в запаянной ампуле при 110°С (выход 17%) 23. Известен также способ получения монофосфорилированных винилалкиловых эфиров взаимодействием пятихлористого фосфора с винилалкиловыми эфирами с последующим разложением образующегося комплекса сернистым газом или уксусной кислотой 4. Однако все эти способы не дают возможности получать предлагаемые би фосфорилированные винилалкнловые эфи ры. Цель изобретения - разработка доступного общего метода синтеза соеди нений нового типа - бисфосфорилирова ных винилалкиловых эфиров 1-алкокси-диалкилфосфиноэтенилдиапкилгалогенфосфоний галогенидов. 2 Поставленная цель достигается согласно способу получения бисфосфорилированных винилалкиЛовых эфиров общей формулы (1), который заключается в том, что диапкилгалогенфосфин подвергают взаимодействию с терминальными алкоксиацетиленами при температуре от минус 35 до плюс 25с в среде инертного органического растворителя в ат- мосфере инертного газа. В качестве инертного органического растворителя желательно использовать диэтиловый или петролейный эфир. Предлагаемый способ в литературе не описан и позволяет получать новые типы фосфорорганических соединений бйсфосфорилированные винилалкиловые эфиры. Получение бисфосфорилированных винилалкиловых эфиров при взаимодействии диапкилгапогенфосфинов с терминальными алкоксиацетиленами является неожиданной реакцией, поскольку вза- имодействие диалкилиодфосфинов с алкилалкоксиацетиленами приводит к моиофосфорилированнсму апкилвиниповому эфиру 5. Реакция может быть выражена следующим уравнением: нс (ор-)Цх хгде R, R и X имеют вьшеуказанные значения,и представляет собой первый пример сопряженного присоединения ди,алкилгалогенфосфинов по кратным свяРеакция следует приведенному уравнению независимо от количества взятого алкоксиацетилена, т.е. при соотношении диалкилгалогенфосфин - алкоксиацетилен равном 1:1 (т.е. двукрат1|ый избыток алкоксиацетилена) образуется тот же целевой продукт, а апкоксиацетипен возвращается непрореагировавшим. Выбранный температурный интервал обусловлен тем, что при температуре ниже минус скорость реакции мала и, следовательно, использование более низких температур является нецелесообразньпч, тогда как при-температурах выше целевые продукты подвергаются разложению и перегруппировкам. Целевые продукты представляют собой легкоплавкие кристаллические соединения или масла, которые устойчивы при хранении в отсутствие влаги и кислорода воздуха в течение длительного времени не изменяются. Данные элементного анализа, ИК-, ПМР-, ЯМРС и Р-спектроскопии подтверждают состав и строение целевых продуктов. Все реакции проводят в атмосфере инертного газа (сухого аргона) в абсолютных растворителях. Пример 1. К раствору 4,5 г (0,02 моль) диизопропилиодфосфина в 30 мл абсолютного диэтилового эфира, охлажденному до минус 35 С, при перемешивании добавляют по каплям в течение 10 мин раствор 0,9 г (0,013 моль) этоксиацетилена в 10 мл диэтилового эфира. Реакционную смесь перемешивают при этой температуре в течение 10 мин, температуру поднимают до комнатной, выпавший осадок декантируют, промьшают 10 мл диэтилового эфира, сушат в вакуум-эксикаторе,, получают 5,5 г (количественно) 1-этокси-2-диизопропилфосфиноэтенилдиизопропилиодфосфоний иодида (J), т.пл. 84-85°С. Пример 2.К раствору 1,2 г (0,012 моль) бутоксиацетилена в 25 м абсолютного петролейного эфира, охлажденному до , при перемешивании добавля81т по каплям в течение 10 мин раствор 4,5 г (0,02 моль) диизопропилиодфосфина в 15 мл абсолютного петролейного эфира. Температуру реак ционной смеси поднимают до комнатной выпавший осадбк .декантируют, промыва 10 мл петролейного эфира, сушат в вакуум-эксикаторе, получают 5,8 г (количественно) 1-бутокси-2-диизопропилфосфиноэтенилдиизопропилиодфосфоний иодида (П ), т.пл. 80-81 С. Пример 3. К раствору 0,8 г (0,012 моль) этоксиацетилена в 10 мл диэтилового эфира при 20-25 С при ин тенсивном перемешивании добавляют по каплям в течение 10 мин раствор 4,0 (0,02 моль) диизопропилбромфосфина в 20 мл диэтилового эфира. Реакционную смесь перемеошвают при этой температуре в течение 3-4 ч, выпавший осадок декантируют, промывают 10 мл диэтилового эфира, сушат в вакуум-эксикаторе, получают 4,6 г (количественно) 1-этокси-2-диизопропилфосфиноэтеннлдиизопропилбромфосфоний бромида ( Ш ) т.пл. 78-79°С.Пример 4. К раствору 4,6 г (0,03 моль) диизопропилхлорфосфина при 25°С и перемешивании добавляют по каплям в течение 5 мин раствор 2,0 г (0,02 моль) бутоксиацетилена в 10 мл диэтилового эфира. Реакционную смесь перемешивают при этой температуре в течение 48 ч, растворитель отгоняют в вакууме, получают 6,0 г (количественно) 1-бутокси-2-диизопропилфосфиноэтенилдиизопропилхлорфосфоний хлорида ( iv ) , в виде некристаллизующегося масла. Пример 5. К раствору 1,7 г (0,03 моль) метоксиацетилена в 50 мл петролейного эфира, охлажденному до минус 20°С, при перемешивании по каплям добавляют в течение 15 мин раствор 6,45 г (0,03 моль) диэтилиодфосфина в 50 мл петролейного эфира. Реакционную смесь перемешивают при этой температуре в течение 15 мин, поднимают температуру до комнатной, выпавший осадок декантируют, промы-. вают дважды 10 мл петролейного эфира, сушат в вакуум-эксикаторе, получают 7,2 г (количественно) 1-метокси-2-диэтилфосфиноэтенилдиэтилиодфосфони иодида (V), т.пл. 92 С. Данные элементного анализа, ИК- и ЯМР-спсктроскопии полученных соединений приведены в табл.1 и 2. Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диалкил-2-бром-2-алкоксиалкенилфосфонитов | 1982 |
|
SU1074880A1 |
| Способ получения диалкил-2-иод-2-алкоксиалкенилфосфонитов | 1981 |
|
SU1004400A1 |
| Способ получения кетенилидентриалкилфосфоранов | 1983 |
|
SU1154286A1 |
| Способ получения 1-галоген-2-триалкилсилилалкенилалкиловых эфиров | 1983 |
|
SU1122661A1 |
| Способ получения дигалогенангидридов 2-алкоксиалкенилфосфонистых кислот | 1982 |
|
SU1033498A1 |
| Способ получения тетразамещенных метилендифосфинов | 1979 |
|
SU854931A1 |
| Способ получения замещенных 1,3-оксафосфоленов | 1983 |
|
SU1114681A1 |
| ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЛМЕТИЛХРОМАНА В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫХ ИЗОМЕРОВ ИЛИ ИХ СОЛИ | 1992 |
|
RU2089549C1 |
| Способ получения -триалкил-Силил /гЕРМил/ - -гАлОидВиНил-АлКилОВыХ эфиРОВ | 1979 |
|
SU808502A1 |
| Способ получения элементзамещенных фосфэтиленов | 1980 |
|
SU910639A1 |
1. СПОСОБ ПОЛУЧЕНИЯ БИСФОСФОРИЖРОВАННЫХ ВИНИПАЛКИЛОВЫХ ЭФИРОВ общей формулы Гр2р-сн c(oR«|pi 2x ;( , где R - этил, изопропил R1 - алкил , X - хлор, бром, иод, . заключающийс я в том, чтодиалкилгалогенфосфин подвергают взаимодействию с терминальным алкоксиацетиленом при температуре от минус 35 до плюс в среде инертного органического растворителя в атмосфере инертного газа. 2. Способ ПОП.1, заключающийся тем, что в качестве . сл инертного органического растворителя используют диэтиловый или петролейньш эфир. со О) со to
Соединение (изо.СД)РС(Н)С( .J I{иэо-СзН) (M3 -CjHj2PC((( J.. II(« -CjH-tlj, зт Вг -с.,((( g, (изо-СзН)
Найдено, %;
Т.пл., С
Выход, % Д1Т 84-5 34,79 6,34 Колич. 80-1 36,91 6,20 Колич. 78-9 41,42 7,30 Колич.
се
/
VIII(C Hjl P HIzCioc H -HlP cr Колич.
)
IX(.,РС(Н)С()Р g- Колич.
(изо-СзН)
Продолжение табл. 1
48,49
8,65
43,77
7,76
Я + ,
(сиз), (
н
( (снз),2
5,43 Н OCHjCH CH CM
,,, ( (%У. . ,01
IIIс СВг °°1
Н . OtHjCHj
,се +
IV(C«32C 2Pv (СНз),6,22
С .
Н ОСН2СН2СН СНз
V ()2Рх,,()2-,. . 5,21
н оснз се
VI WjCHj P (СНз),26
с сгр/
- н осн2СНз (CH.eH.ljPv Р(сн2СНз)2 н «vi .. (CHjCH IjP Р(СН2СНз), нOCHjCHjCHj (CH,y, j51,0
н
Таблица 2
5,36О19,04,48 3,0
о19,04,37 2,0
1,3 26,04,55 3,0
1,5 28,34,42 3,0
1,0 20,04,08
1,5 27,54,46 3,0 5,95 1,0 25,04,58 2,0 2,0 28,04,40 2,0 27.04,40 2,0
- Аналогично получают соединения VI -tX (табл.1 и 2).
Таким образом, предлагаемый способ позволяет получать не описанные ранее соединения с высоким выходом. Способ прост и не требует сложного аппаратурного оформпения. Получаемые фосфорорганические соединения содержат два атома фосфора в одной молекуле, что дает возможность использовать целевые продукты в качестве исходных соединений для получения ряда
производных (например, окисей фосфинов), обладакяцих высокой комплексообразукяцей способностью и вызывакнцих интерес как потенциальные комплексоны и флотореагенты. Кроме того, целевые продукты являются функционально насыщенными соединениями и вследствие этого их можно рассматривать как полезные промежуточные продукты в синтезе новых типов фосфорорганических соединений, содержащих трех- и четьфехкоординационный фосфор.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения окрашенного полимерного материала-полиметилметакрилата,полистирола или поливинилацетата | 1976 |
|
SU859391A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1984-06-15—Публикация
1983-05-26—Подача