Изобретение относится к новому химическому соединению, конкретно к дигидрохлориду 3-/2-диэтиламиноэтилтио/-5-/2-морфолиноэтил/-1,2,4-триазино/5,6-в/ индола формулы I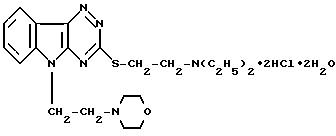
обладающему стресс-протективной активностью.
Указанные свойства позволяют предполагать возможность применения его в медицине.
Известны производные 1,2,4-триазино/5,6-в/ индола, обладающие противовирусной активностью [1]
Известен также ближайший структурный аналог гидрохлорид 3-/2-диэтиламиноэтилтио/-1,2,4-триазино/5,6-в/-индола, повышающий устойчивость организма к гипоксии [2]
Целью изобретения является поиск новых производных в ряду 1,2,4-триазино/5,6-в/ индола, обладающих стресс-протективной активностью.
Поставленная цель достигается новым дигидрохлоридом 3-/2-диэтиламиноэтилтио/-5-/2-морфолиноэтил/-1,2,4-триазино/5,6-в/ индола формулы I, обладающим стресс-протективной активностью.
Указанное соединение формулы I получают аминоалкилированием 3-/2-диэтиламиноэтилтио/-1,2,4-триазино/5,6-в/ индола гидробромидом 2-морфолиноэтилбромида в диметилформамиде в присутствии гидрида натрия, далее превращают полученное основание в гидрохлорид действием хлористого водорода.
Пример. Смешивают 4,12 г (13,7 ммоль) 3-/2-диэтиламиноэтилтио/-1,2,4-триазино/5,6-в/ индола с 15 безводного диметилформамида и постепенно при перемешивании и наружном охлаждении, поддерживая температуру 20oC, прибавляют 0,395 г /16,4 ммоль/ порошкообразного гидрида натрия. Одновременно таким же образом готовят раствор 2-морфолиноэтилбромида путем добавления 0,461 г /19,3 ммоль/ гидрида натрия к смеси 4,88 г/17,7 ммоль/ гидробромида 2-морфолиноэтилбромида и 15 мл безводного диметилформамида. Полученные растворы смешивают и нагревают на кипящей водяной бане в течение 30 мин. При этом раствор приобретает темно-красную окраску. Растворитель отгоняют при нагревании на водяной бане /температура бани 50-60oC/ под вакуумом. Остаток перемешивают с 50 мл изопропилового спирта, осадок бромида натрия отфильтровывают и фильтрат при перемешивании насыщают газообразным безводным хлористым водородом. Выпавший осадок продукта реакции отфильтровывают, промывают изопропиловым спиртом /2x1 мл/, эфиром /2х5 мл/ и сушат в вакуум-эксикаторе над фосфорным ангидридом. Из фильтрата при выдерживании в течение 36 ч при комнатной температуре выпадает дополнительное количество продукта реакции, который выделяют таким же образом. Получают сырой дигидрохлорид 3-/2-диэтиламиноэтилтио/-5-/2-морфолиноэтил/-1,2,4-триазино/5,6-в/-индола в виде мелких бледно-желтых кристаллов, выход 6,27 г /95,1%/.
Полученное вещество /5,46 г/ обрабатывают при кипении смесью изопропилового спирта /23,8 мл/ с водой /1,2 мл/, нерастворенный остаток отфильтровывают, сушат и получают 2 г вещества, 1,89 г образца кристаллизуют из 20 мл смеси изопропилового спирта с разбавленной /1:20/ соляной кислотой в объемном соотношении 10:1. Вещество выделяется при охлаждении в виде коричневатого масла, переходящего при растирании в легкие бледно-желтые кристаллы, выход 1,32 г, т. пл. 242oC. После перекристаллизации из этилового спирта /около 7,2 мл на 1 г/ и высушивания на воздухе получают дигидрохлорид 3-/2-диэтиламиноэтилтио/-5-/2-морфолиноэтил/-1,2,4-триазино/5,6-в/ индола /дигидрат/ в виде бледно-желтых кристаллов, т.пл. 247oC. Выход при перекристаллизации 53%
Вещество легко растворяется в воде, устойчиво при хранении, однородно по данным тонкослойной хроматографии на силуфоне. Условия тонкослойной хроматографии: растворитель для нанесения спирт, подвижный растворитель - этиловый спирт концентрированный водный аммиак-вода 20:1:4, Rf 0,56. Вещество как в видимом, так и в УФ-свете не содержит примесей, в том числе исходных веществ.
Строение вещества подтверждается данными элементного анализа, потенциометрического титрования щелочью, а также УФ-спектров.
Найдено C 47,86, 47,92; H 6,56, 6,67; Cl 13,47, 13,55; N 15,78, 15,84; S 6,25, 6,34. C21H36Cl2N6O3S Вычислено, C 48,18; H 6,93; Cl 13,54; N 160,5; S 6,12.
УФ-спектр, λмакс, нм /lgε/:221 пл /4,418/,268 /4,641/342/4,155/. УФ-спектр снят для раствора в воде на приборе СФ-20. Положение полос поглощения характерно для 3-S-алкильных производных 1,2,4-триазино/5,6-в/ индола.
Изучение стресс-протективной активности и токсичности.
Фармакологические исследования выполнены на модели хронического стресса, обусловленного 2-суточным воздействием комплекса экстремальных факторов - лишение крыс сна, пищи и воды в медленно /0,2 км/ч/ вращающемся барабане.
Оценку эффективности соединения I в сравнении с диазепамом /Седуксен фирмы Гедеон Рихтер/ проводили по комплексу показателей, характеризующих функциональную активность ЦНС и развитие основных патофизиологических проявлений стресс-синдрома. Опыты выполнены на взрослых крысах-самцах массой 150-200 г. Параллельно исследовали три группы животных. Животных первой и второй групп подвергали воздействию экстремальных факторов, третьей - содержали в обычных условиях.
К концу 2 суточного эксперимента определяли общую поведенческую активность /по тесту "открытого поля"/; состояние высшей нервной деятельности /по тесту выработки условной реакции избегания в водном V-образном лабиринте/; количество язв на слизистой оболочке желудка; массовый коэффициент надпочечников.
Соединения вводили четырехкратно (два раза в сутки) в оптимальных дозах (диазепам 1 мг/кг; соединение I- 5 мг/кг) внутрибрюшинно в объеме 2,5 мл/кг животным, находившимся в экстремальных условиях /первая группа/. Контрольные животные получали физиологический раствор в экстремальных /вторая группа/ и обычных условиях /третья группа/ в те же сроки и в том же объеме.
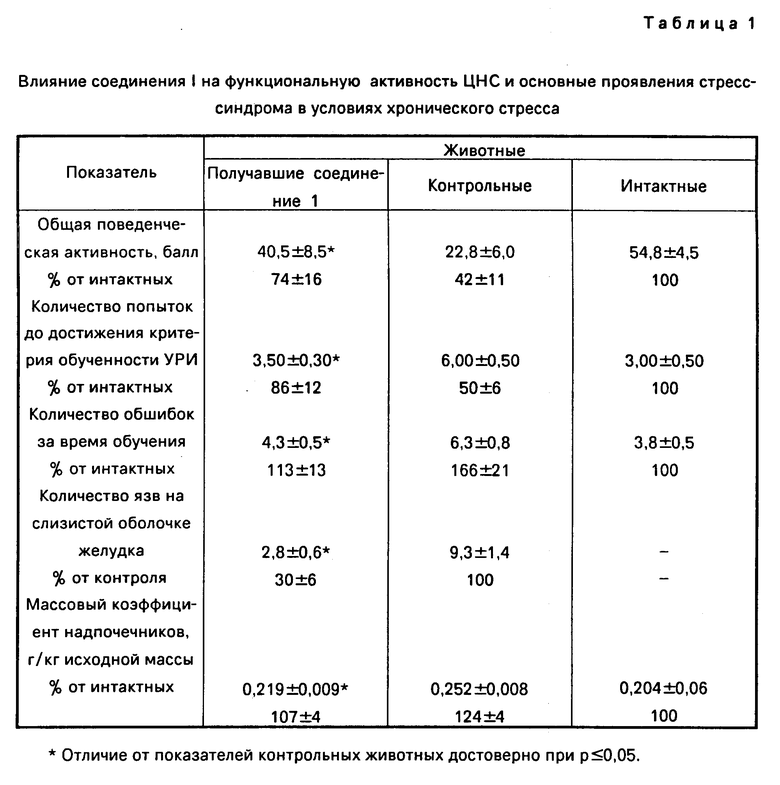
Результаты проведенного исследования представлены в табл. 1. Двухсуточное воздействие экстремальных факторов привело к существенному ухудшению всех исследованных показателей, развитию основных патофизиологических проявлений стресс-синдрома. При этом отмечено снижение общей поведенческой активности на 46% скорости обучения на 53% Отмечено также язвообразование на слизистой оболочке желудка /5,0-0,8/ и увеличение массового коэффициента надпочечников на 28% по сравнению с интактными животными.
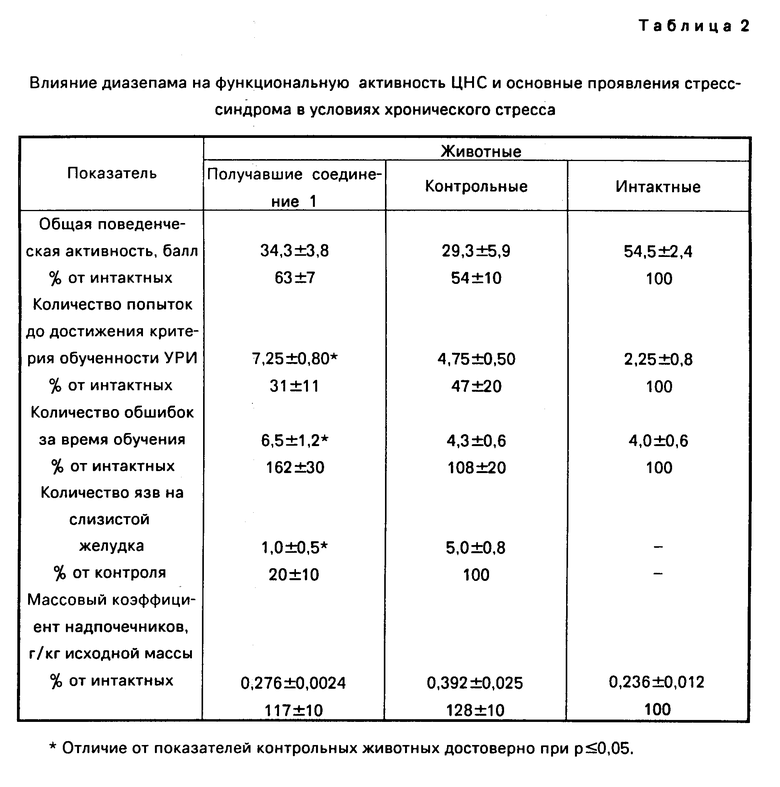
Введение диазепама способствовало уменьшению основных патофизиологических проявлений стресс-синдрома: уменьшило язвообразование на слизистой оболочке желудка и гипертрофию надпочечников /табл. 1/, однако его применение привело к еще большему ухудшению показателей высшей нервной деятельности. Введение соединения I также способствовало уменьшению язвообразования на слизистой оболочке желудка и гипертрофии надпочечников, но в отличие от диазепама достоверно улучшило высшую нервную деятельность в экстремальных условиях, о чем свидетельствуют данные табл. 2.
Острую токсичность соединения I определяли на мышах, вводя его внутрибрюшинно. Статистическую обработку полученных данных проводили по методу Беренса. Найдено, что ЛД50 соединения I равно 200 мг/кг /рабочая доза вещества составляет 1/40 от ЛД50).
Таким образом, дигидрохлорид 3-/2-диэтиламиноэтилтио/-5-/2-морфолиноэтил/-1,2,4-триазино/5,6-в/ индола обладает выраженной стресс-протективной активностью, которая сопровождается положительным влиянием на высшую нервную деятельность животных в экстремальных условиях, что выгодно отличает его от известного препарата диазепама, стресс-протективная активность которого сопровождается депримирующим влиянием на ЦНС.
Вещество обладает низкой токсичностью и достаточной фармакологической широтой и может найти применение в качестве стресс-протективного средства.
Дигидрохлорид 3-(2-диэтиламиноэтилтио)- -5-(2-морфолиноэтил)-1,2,4-триазино (5,6-в) индола формулы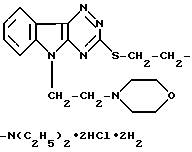
обладающий стресс-протективной активностью.
Дигидрохлорид 3-(2-диэтиламиноэтилтио)-5-(2-морфолиноэтил)-1,2,4-триазино (5,6-в) индола формулы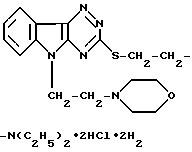
обладающий стресс-протективной активностью.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для обработки экспонированных фотоматериалов | 1988 |
|
SU1645935A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Контрольный висячий замок в разъемном футляре | 1922 |
|
SU1972A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ГИДРОХЛОРИД 3-(2-ДИЭТИЛАМИНОЭТИЛТИО)-1,2,4-ТРИАЗИНО[5,6-B] ИНДОЛА, ПОВЫШАЮЩИЙ УСТОЙЧИВОСТЬ ОРГАНИЗМА К ГИПОКСИИ | 1981 |
|
SU978567A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1996-09-20—Публикация
1982-11-04—Подача