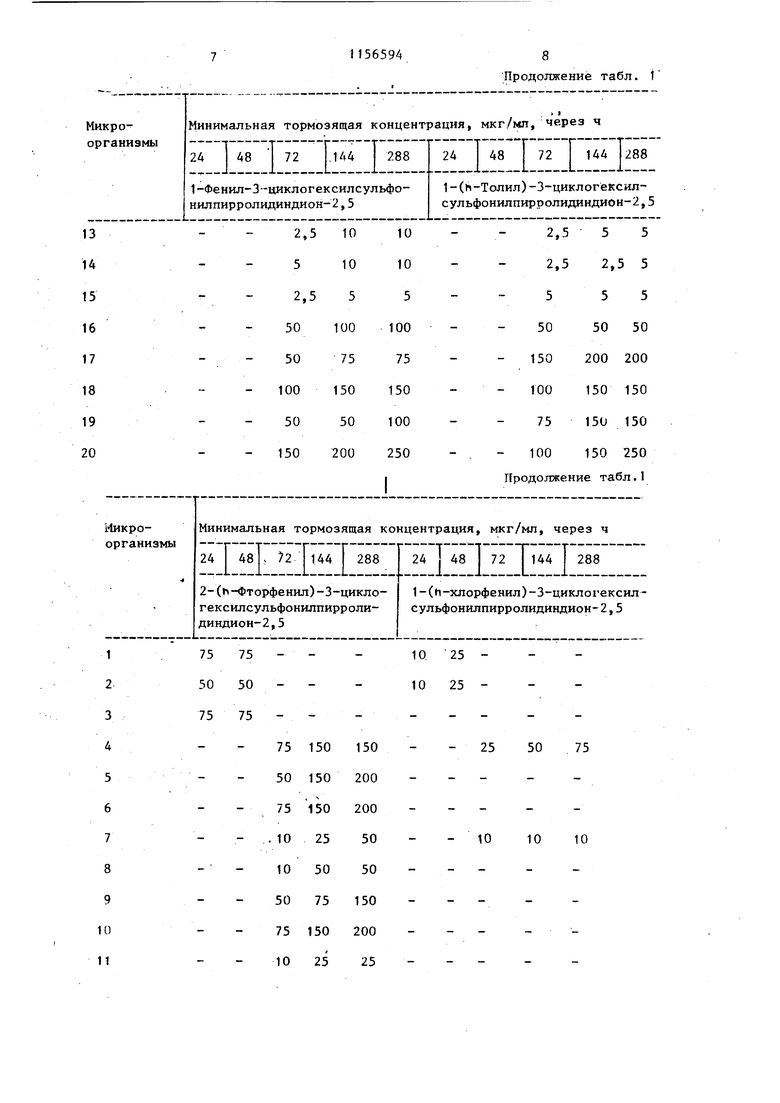
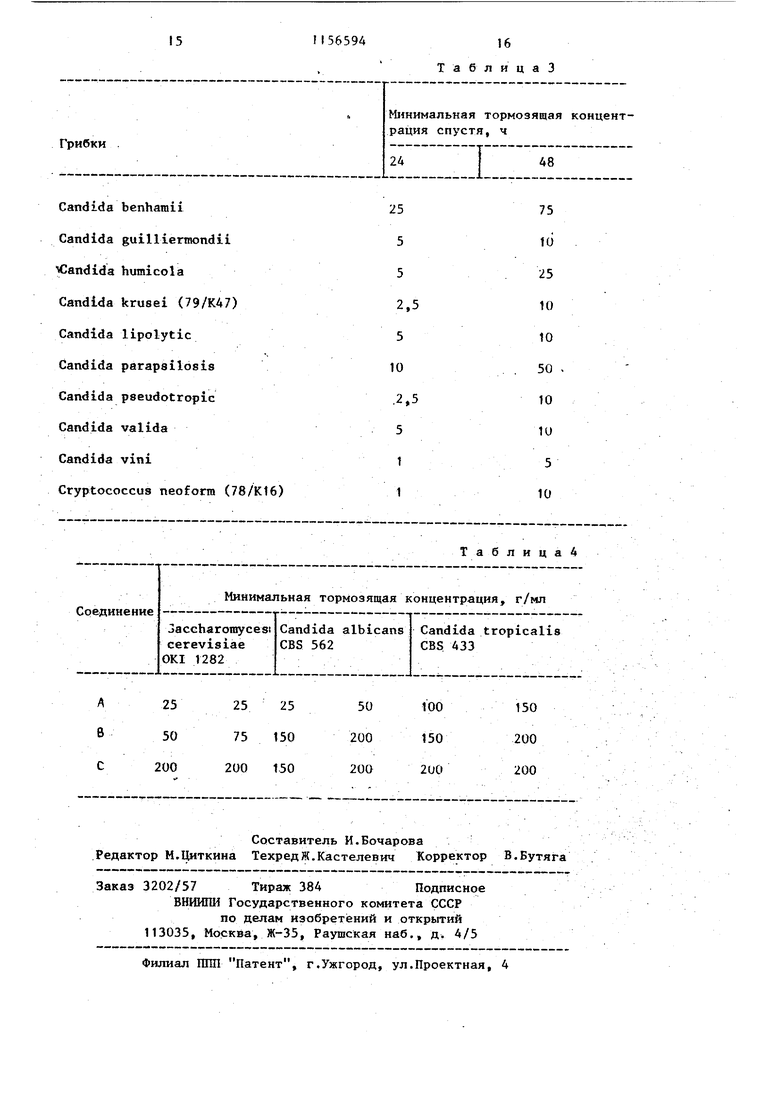
Изобретение относится к получени новых производных пирролидинового ряда, обладающих фунгицидными свойствами. Эти соединения могут быть использованы для борьбы с грибковым заболеваниями. Известно, что N-арилмалеинимиды и фенилсульфокислоты вступают в реа ции присоединения DTЦелью изобретения является созда ние способа получения новых соедине ний, обладающих фунгицидными свойст вами. Поставленная цель достигается способом получения Нтзамещенных 3-циклоалкилсульфонилпирролидиндионов-2,5 общей формулы .0 Т О где /А - циклопентил или циклогексил R - этил, гексил, фенил, бензил толил, 4-метил-2-сульфофени 3,4-метш1ендиоксифенил, 4-метш1-3-карбоксифенил, 4-метил-2-окси-метилфенил или фенил, замещенный в по ложении 4 метильной, метокс аминосульфонил-, ацетил-, этоксикарбониламиносульфонн или сульфогруппами, в положении 2 - хлором, в положении 3 - нитрогруппой, заключающимся в том, что N-замещенный З-галоген-пирролидиндион-2,5 общей формулы где X - галоген; R имеет указанные значения, подвергают взаимодействию с сульфинатом щелочного металла общей фсрму ль1 МеО - SO - А, где Me - атом, щелочного металла; А - имеет указанные значения, в среде инертного полярного апротон ного растворителя. Соединенная, которые образуются во время реакции, выделяются из ре 942 ционной смеси в осадок и могут быть отделены от реакххионной смеси посредством фильтрования или центрифугирования или же остаются в растворе. В этом случае посредством фильтрования отделяют побочные продукты, затем реакционную смесь выливают, например, на лед, после чего производят отделение вьщелившегося в осадок продукта. В соответствии с другим способом из реакционной смеси удаляют посредством отгонки летучие компоненты и растворитель и полученный остаток подвергают очистке, например, перекристаллизацией. Конечные продукты также могут быть выделены и подвергнуты очистке другими известными способами. Пример Ч 1-Фенил-З-циклогексилсульфонилпирролидиндион-2,5. К раствору 2,54 г (0,01 ммоль) 1-фенил-3-бромпирролидиндиона-2,5 в 50 мл диметилформамида при и перемешивании прибавляли раствор 1,7 г (0,01 моль)циклогексилсульфината натрия. Затем смесь дополнителько перемешивали при указанной температуре 2 ч. Непосредственно после этого реакционную смесь разбавляли водой до увеличения объема в десять раз и выделившееся в осадок целевое соединение отделяли посредством фильтрования. После промывки и сушки получали 2,63 г (82%) целевого соединения, т.пл. 148-15lG. Указанным способом также могут быть получены следующие соединения: 1-этил-З-циклогексилсульфонилпирролидиндион-2,5, выход 47,6%, т.пл. П8-120С; 1-н-гексил-3-циклогексилсульфонилпирролидиндион-2,5, выход 39,8%, т.пл. 127-130 С; 1-(2-хлорфенил)-3-циклогексилсульФонилпирролидиндион-2,5, выход 71,4%, т.пл. 153-155С; 1-(3-нитрофенил)-3-циклогексилсульфонилпирролидиндион-2,5, выход 92%, т.пл. 145-14бС; 1-(4-ацетилсифеннл)-3-циклогексилсульфонилпиррол индион-2,5, выход 79,1%, т.пл. 203-206С; 1-(4-аминосульфонилфенил)-3-циклогексилсульфонилпирролидиндион-2,5, выход 71,8%, т.пл. 208-2I(JC; 1-(4-метоксифенил)-3-цпклогексилсульфонштирролидиндион- 2,5, выход 85,7%, т.пл. 1 :i9-ТАОЧ.; 5 1 - 4-1 -этоксикарбоннламиносулъфо нилфенил 1-3-1Шклогексштсульфонилпир ролидиидион-2,5, выход 42,6%, т.пл. 115-118 С; 1-бензил-3-циклогексилсульфонилг1ирролидиндион-2,5, выход 84%, т.пл, leo-iez c; 1-фенил-З -циклопентилсульфонилпирролидиндион-2,5, выход 60,2%, т.пл. 158-159 с (из этилового спирта) ; 1-(п-толил)-3-циклoneнтилсульфонш1пирролидиндион-2,5, выход 86,1%, т.пл. 178-180С (после перекристаллизации из зтилового спирта); 1- ( -сульфофенил)-3-циклогексш1сульфонилпирролидиндион-2,5, выход 56,2%, т.пл. 230-236°С; 1-(4-метил-2-сульфофенил)-3-цикл гексилсульфонилпирролидиндион-2,5, выход 33,1%, т.пл.. 244-247С; 1-(3,4-метилендиоксифенил)-3-цик логексилсульфонилпирролидиндион-2,5 вькод 91,8%, т.пл. 186-188С; 1-(4-метил-3-карбоксифенил)-3циклогексилсульфонилпирролидиндион2,5, выход 46,7%, т.пл. 184-188°С; 1.Saceharomyces cerevisiae 2.Candida albicanc 3. tropicalis 4.Aspergillus niger 5.Aspergillus fumigatus 6.Aspergillus flairis 7.Penicillium digitatum 8.-Penicillium digitatum 9. Penicillium chrysogenum 10.Penicillium chrysogenum 11.Microsporum gypseum. var. vinosum 12.Sporotrichum schenkti 13.Trichophyton rubrum . 14. Trichophyton mentagrophytes 15.Epidermophyton floccosvm 16.Fusarium graminorum 17.Fusarium oxysporum 18.Fusarium monili forme 19.Fusarium culmorum 20.Aspergillus niger 21.Candida krusei 22.Cryptococcus neoform Использованные сокращения: CBS - Gentralbureau voor Schimmelcultures, сем - Czechoslovak Collection of Microorgan sity Brno, ЧССР. DSM - Deutsche Sammlung fur Mikroorganismen Берлин-Далем, ФРГ. OKI - K fzegfeezsegtani Inte;iet, Буд 944 1-(4-метил-2-оксиметилфенил)-3циклогексилсульфонилпирролидиндион2,5, выход 86,2%, т.пл. 174-177С. Установлено, что Новые замещенные в положении 1 производные 3-циклоалкилсульфонилпирролидиндиона-2,5, отвечающие общей форму ле (1), проявляют противомикробную и, прежде всего, фунгицидщто активность против таких штаммов микроорганизмов, которые устойчивы по отношению к обычным фунгицидным биологически активным веществам. Фунгицидную активность новых соединений исследовали следующим :образом. Питательную почву инокулировали с применением микробов и проросшие грибки исследовали через 24 48, 72, 144 и 288 ч, после чего определяли минимальную тормозящую койцентрацию. Полученные результаты представлены в табл. 1 и 2. В тестах были исследованы следуюие организмы: ерн, Нидерланды. sm, J.E. Pyrkyne UnifrerInstitution of Mycology пешт, BHP При внутрибрюшинном введении значение Н-фенил 3-циклогексил-сульфонилпирролидиндиона-2,5, определенное на самках мьш1ей, состав «ляет 382 мг/кг, на самцах мьппей 461 мг/кг. При применении per os соединения не проявляют токсичности. В табл. 3 приведены минимальные тормозящие концентрации 1-(п-толил) 3-циклогексилсульфонилпирролидиндиона-2,5 в 1 мкг/мл среды спустя 24 и 48 ч наблюдения за важнейшими патогенными грибками. Указанные минимальные тсрмозящие концентрации полностью тормозят развитие микроорганизмов. В качестве питательной почвы применяли Sabourod питательную почву. 1-(п-толнп)-3-цикл6гексилсульфони пирролидиндион-2,5 и 1-фенилциклогек силсульфонилпирролидиндион-2,5 также обладают активностью против следующи фитопатогенных грибков: Минимальная тормозящая i Михро организмы 24 I 48 Т 72 I 144
1-Феннл-З-циклогексилсульфонилпирролндиндион-2,5
50
50
75 100 150 Т50 11
1-(-Толил)-3-циклогексилсульфонилпирролидиндион-2,5
.25
50
150
75 75 100 150
1010
25. 75
7575
150150 4. « Botrytis cinerea, ascochyta pisi. Carcospora beti.cola, Taphrina deforraans, Phytophtora infestans, Sclerotinia sclerotiorum. Verticillium alsoatrum, Verticillium dahliae, Venturia. Наиболее предпочтительным целевым соединением по предложенному способу является 1-р-толил-3-(циклогексилсульфонил)пирролидин-2,5-дион (соединение А). Для сравнения были взяты следуюгдие соединения: хлортримазол 1( 2-хлорфенил)-дифенил-метил -1Н-имидазол (соединение В); толнафтат р-нафтиловый эфир М-мётил (N-м-толил)тиокарбаминовой кислоты (соединение О, Результаты сравнительных опытов приведены в таб:;, 4. Как видно из приведенных данных, соединения формулы (1) более высокой эффективностью против грибков, вызывающих большую часть грибковых заболеваний, чем известные фун1:ициды., Т а- блица концентрация, ьосг/мл, через ч 24 Т 48 Г 72 Г 144 |288 1 288
и 56594
8 Продолжение табл. 1
I5659A
10
Продолжение табл.
g g ; 2
-1|
о а
-4 I о X
§ о о
1Л rJ о
- Iа5 1Л о (Ч , Iчо
IIГМ
Iка
I ISа
IиX
-Iке
3
о о Э Ю с( о
I о X
о .ч
«п in
fl
I t л t 1 I Ч
IX. i и и I
I M
3 ° i и
I I I I t I t I
n
I о
r
Ч M
I I I II
о о 4 i lO to U-I r r
S
I I I
-I I
о о «л о 1Л
4Л1ЛГ . ПV-N
I I I
о о о о 1Л
14 ч tn П1А Г1РЧ
I-- I S,
t I I о
I I I
I I I I
S
I I I I I I I I
о о о
р ш ш о п
ШМ
О О П tn
П Л rN|
А
in ш ш
§
чЭ о (Л Р4 о Э
1Л ч
Р О Ю М М «1
I I
««
о о -: гчгчCJ
1Л - 1П Чг
I I I I I
- ft ОUl
i §I I I
ло о о о ш о
t;, 1л in irt - .I I и
3 о о о «о irt
г tn in
in ю ю
о
in -ч -
II
т о Г-. ш
I I I г I I
ш о
I I
о о in о in «о in л сч 1Л М г II - о о ш «ч in р ш о гч «S Ы л
ш ш то о 1Л г - г





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения @ -замещенных 3-циклоалкилсульфонилпирролидиндиона-2,5 | 1981 |
|
SU1192616A3 |
| Способ получения @ -замещенных 3-циклоалкилсульфонилпирролидиндиона-2,5 | 1981 |
|
SU1165231A3 |
| 3-Циклоалкилсульфонилпирролидиндионы-2,5,обладающие фунгицидной активностью | 1980 |
|
SU1373704A1 |
| Способ получения N-замещенных 3-циклоалкилсульфонилпирролидиндионов-2,5 | 1980 |
|
SU1007555A3 |
| Способ получения замещенных мочевины | 1980 |
|
SU1176831A3 |
| Способ получения производных угольной кислоты | 1982 |
|
SU1186085A3 |
| Способ получения геминальных дигалоидных производных конденсированных пиримидин-4-онов,рацематов или оптически активных антиподов | 1980 |
|
SU1151210A3 |
| Способ получения конденсированных производных пиримидина или их солей | 1980 |
|
SU1082324A3 |
| Способ получения производных пиридо/1,2-а/пиримидина или их солей с щелочными металлами или их оптических изомеров | 1980 |
|
SU1024007A3 |
| Способ получения производных мочевины | 1980 |
|
SU1158039A3 |
СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ 3-ЦИКЛОАЛКИЛСУЛЬФОНИЛПИРРОЛИДИНДИОНОВ-2,5 общей формулы 80гА I R где А - циклопентил или циклогексил; R - этил, гексил, фенил, бензил, толил, 4-метил-2-сульфофенил, 3,4-метилендио1ссифенил, 4-метил-3-кapбcкcифeнI Лj 4 -м& кл2-окси-метштфенш1 или фенил, замещенный в положении 4 метильной, метокси-, аминосульфонил-, ацетил-, этоксикарбониламиносульфонил- -или сульфогруппами, в положении 2 хлором, в положении 3 - нитрогруппой, отличающийся тем, что, N-замещенный 3-галоген-пирролидиндион-2,5 общей формулы .X § СО R где X - галоген; R имеет указанные значения, подвергают взаимодействию с сульфина.том щелочного металла общей формулы Мао - SO - А СП где Me - атом щелочного металла; О А - имеет указанные значения, еж в среде инертного полярного апротон ного растворителя. 4аь
О О
ш ш I I I
1
I о
ш л - 4
.-4 г III. III
«
-С - Г ЧМ-««П
I I t I
о «f
I I I I I I
М- с ш
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Bull, of the Chem | |||
| Soc | |||
| of Japan, 48/12/, 3675-3677 | |||
Авторы
Даты
1985-05-15—Публикация
1981-08-12—Подача