00
а ю
4
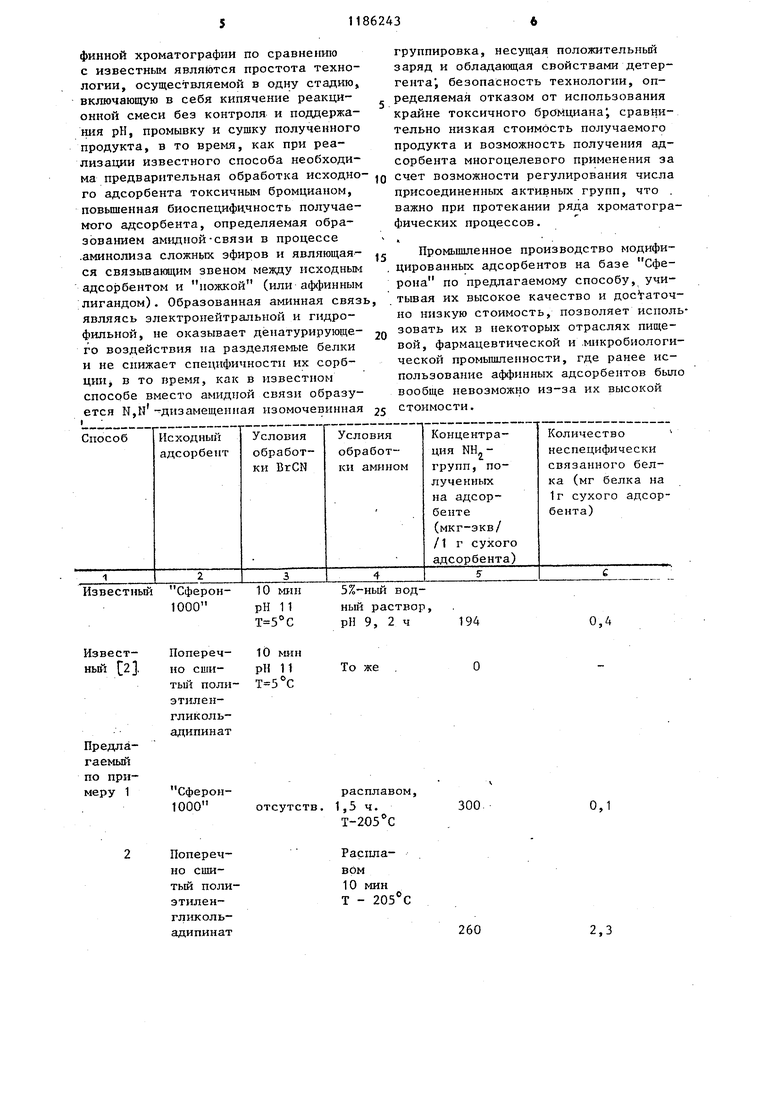
СО 11 Изобретение относится к биологической химии, .а именно к способам получения адсорбентов для аффинной хроматографии, которые могут быть использованы при исследованиях, полу чении и анализе белков и различных :биологически- активных веществ, а так же в медицинской, фармацевтической, микробиологической и пищевой промышленности для выделения, очистки и им мобилизации антител, антигенов ферментов,их субстратов, других белков и низкомолекулярных веществ. Известен способ получения адсорбе тов для биоспецифической хроматографии, заключающийся п образовании химической пространственной группы (ножки) путем взаимодействия исход ного носителя с инертныьш водорастворимыми полисахаридами, содержащими функциональные группы, обеспечивающи ми ковалентное связывание пространст венной группы с носителем, активации полисахаридов бромцианом и последующ го присоединения аффинного лиганда к носителю через активированную пространственную группу lJ. Недостатками этого способа являются сложность технологии, высокая стоимость исходных реагентов, необходимость применения высокотоксичных веществ (бромциапа), возможность неспецифичного взаимодействия за счет образования N,N-замещенных гуанидинов. Наиболее близким к предлагаемому является способ получения адсорбента для .аффинной хроматографии, заключающийся в модификации Сферона (полиоксиалкилметакрилата) путем обработки его поверхности воднььм раствором бромциана при рН 11 и охлаждении льдом с последующей промывкой и обра боткой водным раствором связываемого вещества, содержшцего аминогруппу, при рН 9,0 и комнатной температуре в течение нескольких часов 2 J. Недостатками известного способа являются сложность процесса модификации, предусматривающего строгое поддержание рН реакционной смеси, вы сокая токсичность используемых цеактивов (бромциана), что вызывает необ ходимость применения ряда мер предосторожности, усложняющих процесс модификации, пониженная биоспецифичность получаемых адсорбентов, обусловлеш ая образованием N,N -дизаме3:щенных гуанидинов, несущих положительные заряды и действующих в определенных условиях как детергенты, в результате чего возникает неспецифическая сорбция и возможна денатурация разделяемых белков. Цель изобретения - упрощение технологии процесса получения адсорбента и повышение селективности его биоспецифического действия. Поставленная цель достигается тем, что согласно способу получения адсорбента для аффинной хроматографии путем модифицированияполимера-носителя, содержащего сложноэфирные группы, первичным амином, модифицирование полимера-носителя осуществляют обработкой расплавом первичного амина при температуре, не превышающей температуру разложения носителя. Сущность предлагаемого способа заключается в термохимической модификации исходного носителя полиэфирной природы первичным амином, в результате чего происходит аминолиз части сложноэфирных групп, в то время,как сущность известного способа состоит в предварительной активации исходного носителя водным раствором бромциана, приводящей к образованию на нем цианатных jpynn, последующей обработке водным раствором гексаметилендиамина при комнатной температуре, в результате чего возникает гуанидиновая структура. В качестве полимера-носителя могут использоваться любые полимеры со сложноэфирной группой, в частности эфиры полиакриловьк кислот, поперечно сшитые этиленгликолевые эфиры дикарбоновых кислот. В качестве аминов используют первичные моно- и диамины. Пример 1. Перегоняют гексаметилендиа ин при нормальном давлении и добавляют к расплаву 5 вес.ч. гексаметилендиамина, 2 вес.ч. сухого адсорбента - полиоксиалкилметакрила.та Сферон-1000 с размером частиц 60-100 мкм. Смесь нагревают в колбе с обратным холодильником при 205 С в течение времени, определяемого необходимым количеством аминогрупп в конечном продукте. В данном примере кипяче1ше смеси производят в течение 1,5 ч. Переносят реакционную смесь в воронку со стеклянным фильтром, установленную в колбе Бунзена, и промывают ее последовательно 20 объемами воды, 5 объемами ацетона и 5 объемам диэтилового эфира. Полученный препарат высушивают при комнатной температуре и осуществляют качественный и количественный анализ полученного адсорбента стандартнЕЛми методами. Пример 2. Осуществляют аналогично тфимеру 1 за исключением того, что в качестве полимера используют полиэтиленгликольадипинат и обработку ведут 10 мин. Количественный анализ полученных адсорбентов проводят с помощью нинги ринового реактива и осуществляют непрямым иодатометрическим способом. Для этого к 10 мг сухого адсорбента добавляют 2 мл раствора НС1 (20 MKI- экв/мл) и инкубируют смесь в течение 5 мин при 25 С и при легком перемешивании. Далее суспензию отстаивают по 1 мл жидкости, находящейся над осадком, переносят во флаконы, куда затем добавляют по 1 мл смеси 1%-ног NaU и 1%-ного KJOj . Вьщелившийся йод титруют 0,01М раствором тиосульфата натрия. Рассчитывают количество связанной с адсорбентом кислоты и по не му судят о содержании аминогрупп в адсорбенте. При этом учитывают также результаты контрольного титрования н модифицированного адсорбента. Присоединение аффинного лиганда к модифицированным адсорбентам, полученным по известному и предлагаемому способам, проводят методом карбодиимидного связывания. В качестве аффинного лиганда используют п-анисовую кислоту. Полученный предлагаемым способом биоспец фический адсорбент успешно используют для вьщеления анизолсвязывающего белка обонятельного эпителия собаки согласно методу Прайса. Количество неспецифически связавшегося с адсорбентом белка определяют путем его элюирования из хроматографической колонки раствором 5М моч . вины и ЗМ NaCl и измерения ультрафио летового поглощения элюата проточной кюветой Увикорд. Пример 3. В качестве исходны адсорбентов используют полиоксиалкил метакрилат типа Сферон-300 и поперечно сшитый полиэтиленгликольтерефталат. Модифицирующим реактивом слу жит путресцин (1,4-диаминобутан). Модификацию известным и предлагаемым способами, а также количественный и качественный анализ полученных адсорбентов проводят аналогично примеру 1, но при температуре расплава 160°С. Пример 4, Осуществляют аналогично примеру 3 за исключением того, что в качестве полимера используют полиэткленгликольтерефталат и обработку ведут 10 мин. Пример 5. В качестве исходного адсорбента используют Сферон1000. Модифицирующим реактивом служит бензиламин, который в данном случае является и аффинным лигандом. Модификацию адсорбента предлагаемым способом осуществляют аналогично примеру 1.. Концентрацию бензиламина на полученном аффинном адсорбенте определяют методом исчерпывающего сульфирования . Полученные данные процесса модификации адсорбентов приведены в таблице. Приведенные в таблице результаты подтверждают повьш1ение биоспецифич- ности адсорбента, неспецифическое связывание белка с которым уменьшилось в 4 раза (с 0,4 мг белка/г сухого адсорбента до О,1 мг белка/г сухого адсорбента), и расширение количества типов адсорбентов, пригодных для использования в аффинной хроматографии (в частности поперечно сшитый полиэтиленгликольадипинат). Количество биоспецифически связанно о белка при использовании адсорбентов по известному способу и примеру 1 составляет t4 мкг/мл геля. Изменяя время термохимической обработки исходного адсорбента модифицирующим реагентом, можно варьировать концентрацию аффинного лиганда в широких пределах, что позволяет точно регулировать свойства получаемого аффинного адсорбента. Таким образом, варьируя типы адсорбентов, типы первичных аминов и время модификации, можно получать, реализуя предлагаемый способ, широкий спектр адсорбентов для аффинной хроматографии с заранее заданными свойствами. Преимуществами предлагаемого способа получения адсорбента для аффинной хроматографии по сравнению с известным являются простота технологии, осуществляемой в одну стадию, включающую в себя кипячение реакционной смеси без контроля и поддержания рН, промывку и сушку полученного продукта, в то время, как при реализации известного способа необходима предварительная обработка исходно го адсорбента токсичным бромцианом, повышенная биоспецифи.чность получаемого адсорбента, определяемая образованием амидной-связи в процессе .аминолиза сложных эфиров и являющаяся связывающим звеном между исходным адсорбентом и ножкой (или аф(1)инным лигандом). Образованная аминная связ являясь злектронейтральной и гидрофильной, не оказывает дёнатурирующего воздействия на разделяемые белки и не снижает специфичности их сорбции в то время, как в известном способе вместо амидной связи образуется N,N - дизамещениая изомочевинная
группировка, несущая положительньп заряд и обладающая свойствами детергента, безопасность технологии, определяемая отказом от использования крайне токсичного бромциана, сравнительно низкая стоимость получаемого продукта и возможность получения адсорбента многоцелевого применения за счет возможности регулирования числа присоединенных активных групп, что . важно при протекании ряда хроматографических процессов.
Промьшшенное производство модифицированньк адсорбентов на базе Сферона по предлагаемому способу, учитывая их высокое качество и достаточно низкую стоимость, позволяет использовать их в некоторых отраслях пищевой, фармацевтической и .Ш1кробиологической промышленности, где ранее использование аффинных адсорбентов было вообще невозможно из-за их высокой стоимости.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения сорбентов для аффинной хроматографии сериновых протеаз | 1977 |
|
SU734215A1 |
| Способ очистки трипсина | 1989 |
|
SU1742329A1 |
| Способ получения биоспецифических адсорбентов для выделения фибронектина и коллагеназ | 1986 |
|
SU1419717A1 |
| Способ очистки протеолитических ферментов | 1976 |
|
SU644796A1 |
| Способ очистки протеолитических ферментов | 1978 |
|
SU942427A1 |
| Биоспецифический полимерный адсорбент для выделения протеиназ (его варианты) | 1982 |
|
SU1137388A1 |
| Способ получения адсорбентов,содержащих аминогруппы | 1982 |
|
SU1054353A1 |
| Способ получения биоспецифического сорбента для очистки аминопептидаз | 1981 |
|
SU1074877A1 |
| НОВЫЕ АФФИННЫЕ ЛИГАНДЫ И ИХ ПРИМЕНЕНИЕ | 1996 |
|
RU2175261C2 |
| АФФИННЫЙ СОРБЕНТ ДЛЯ УДАЛЕНИЯ ФАКТОРА НЕКРОЗА ОПУХОЛИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2123860C1 |
СПОСОБ ПОЛУЧЕНШ АДСОРБЕНТА ДЛЯ АФФИННОЙ ХРОМАТОГРАФИИ путем модифицирования полимера-носителя, содержащего сложноэфирные группы, первичным амином, отличающийся тем, что, с целью упрощения технологии процесса получения адсорбента и повышения селективности его биоспецифического действия, модифицирование полимера-носителя осуществляют обработкой расплавом первичного аъшна при температуре, не превышающей температуру разложения носителя. (Л
Сферон10 мин
5%-ный вод1000рН 11 ный раствор, рН 9, 2 ч
То же .
Сферонрасплавом, 1000 1,5 ч.
отсутств, Т-205С
Расгшавом10 мин Т -
194
0,4
3000,1
260
2,3
10 мин
СферонрН 11 300
Предлагаемый по
примеру 3 Сферон300
9
215
Расплавом 1,5 ч
326
Расплавом
233 10 мин Т -
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения адсорбентов для хроматографии | 1975 |
|
SU520370A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ja Turkova | |||
| Immobilization of enzymes on Hydroxyalkylraethaci-ylate Gels, - Methods in Enzyraology, 1976, V | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
Авторы
Даты
1985-10-23—Публикация
1982-12-29—Подача