Изобретение относится к способу :получения новых производных гекси тов 8 а конкретнее новых производных дульцита, содержащих свободные карбоксильные группы, или.их солей, обладающих способностью подавлять р витие злокачественных опухолей.
Цель изобретения - получение нов производнь х ряда дульцита, содержащих свободные карбоксильные группы, обладающих усиленным подавляющим развитие злокачественных опухолей .действием.
Пример 1, Получение катализатора палладий на угле.
А, О,2 г хлористого палпадия растворяют в 2 мл дистиллированной 5s7 н, хлористоводородной кяслоты при нагревании раствор разбавляют водой в пятикратном размере, затем добавляют 0,9 г активированного угля (Мерк, для анализа) и суспензию кипятят в течение нескольких минут. Суспензию охлаждают, а затем подщелачивают (до рН 9) используя 20%-ный водньй раствор гидроокиси натрия 5 встряхивая таКр чтобы раствор над твердым веществом стал совершенно бесцветным.
Б. 0,2 г хлористого палладия рас воряют в 2 мл дистиллированной
5,7 н, хлористоводородной КИСЛ01 Ы
при нагревании, раствор разбавляют 80 мл дистиллированной воды и до баеляют 9,0 г активированного угля (,, для анализа , Полученную суспензию подщелачиваю г описанным в пункте А путем.
Суспензии, полученные в соответс ВИИ с методиками по пунктам А и Б, тщательно перемешивают, катализа.- тор отфильтровывают, промывают до устранения хлоридов на фильтре и после этого промывают 200 Ш1 7, ког раствора уксусной кислоты Мокрый катализатор сушат над концентрированной серной кислотой в эксикаторе Получают катализатор, содержащий 2,4% палладия на угле
П р и м е р 2 „ Получе ние 3,25j 6-диангидро 3,4-бис(-карбокси- лропионил)-дульцита.
IK6 г (3 ммоль 152-5,6-диaнгид- :po-3j4-бис-(Р -бeнзилoкcикapбoнилпpo :fшoнилJ-дyльцитa растворяют в 150 м сухого метанола, к раствору добавляют 0,3 г катализатора, приготовле
057692
ного по примеру 1, и полученную смесь гидрируют до отбора теоретичес кого количества водорода (1,5 ч). Катализатор отфильтровывают, раствор 5 испаряют в вакууме, получакяцееся белое кристаллическое вещество суспендируют в диэтиловом эфире и твер- №ie частицы отфильтровывают. Полученное вещество подвергают перекрис10 таллизации из смеси диэтилового эфира и петролейного эфира. Получают 1,0 г 1, 2-5,6-диангидро-3,А-бис-(/3 карбоксипропионил)-дульцита; выход 96%, Т.пл. 138-139°С. По данным анаtS ЛИЗа методом тонкослойной хроматографии ( Rf О,15, с использованием смеси (9:2) бензола и метанола и проявлением hi -нитробензилпиридином продукт однороден.
20 Вычислено,%: С 48,78; Н 5,73; О 46,49,
Найдено : С 48,35; Н 5,25; О 46,60.
25 Эквивалентная масса; вычислено 173, найдено 180„
ИК-спектр: 3350 см карбоксил), 1235 см (эпокси), бензильные и гидроксильные полосы отсутствуют.
30 Растворимость: хорошо растворимо в спирте и тетрагидрофуране, плохо растворимо в диэтиловом эфире и воде,
П р и м е р 3, Получение 1,2-5,635 диангидро-3-(Э карбоксипропионил)- 4-ацетилдульдита.
3,78 г С10 ммоль 1,2-5,6-диан- гидро-З-ГЭ-бензилоксикарбонилпро- пиокил -4-ацетилдульцита гдцрнруют
40 аналогично примеру 2 до прекращения отбора водорода. Катализатор отфильтровывают, фильтрат упаривают в вакууме, кристаллический остаток подвергают перекристаллизации из сме45 си тетрагидрофурана и этилацетата, Получают 2,5 г (выход 88%) 1,2-5,6- диангидро-З- р) -карбоксипропионил) - 4-ацетшщульцита5 Т,пл. 134°С. По данным тонкослойной хроматографии
SO использованием смеси (6;4| зтилацетата и 1щклогек- сана 1ШИ смеси (8:2) бензола и метанола соответственно и проявлением .1-нитробензш1пиридином) продукт од
нороден,
Вьгц;исленоД: С 50,00; Н 5,59; Oi,44,40.
Найдено,%: С 49,48; Н 5,26; О 44,70.
Эквивалентная масса: вычислено (288 MB 288,26), найдено 296.
П р и м е р 4. Получение 1,2-5,6- диангидро-З-Ср-карбоксипропионил) -4 (/3 -карбометоксипропионил)-дульцита.
4,50 г (10 ммоль) 1,2-5,6-диан- гидро-3-(/3-бензилоксикарбонилпропио- нил)-4(-карбометоксипропионил)- дульцита гидрируют аналогично примеру 2 до отбора расчетного количества водорода. Катализатор отфильтровывают, и растворитель удаляют из фильтрата. Получают 3,1 (выход 86%) кристаллического 1,2-5,6-диан- гидро 3-(-карбоксипропионил)-4- (/3 -карбометоксипропионил.) -дульцита; Т.пл. 87-89°С. По данным тонкослойной хроматографии ( Rf 0,25 или 0,4, с использованием смеси (6:4) этилацетата и циклогексана или смеси (8:2) бензола и метанола соответственно) продукт однороден.
Вычислено,%: С 49,72; Н 6,12; О 44,16,
20
Найдено,%: С 49,87; Н 5,39; 043,91.
Эквивалентная масса: вычислено 362 (MB 362,34), Найдено- 363.
Приме р 5. Получение 1,2-5,6- диангидро- 3(/Ь-карбоксипропионил) - 4-( -фенилпропионил)-дульцита.
4,68 г (10 ммоль) 1,2-5,6-диaнгид po-3-(-бeнзилoкcикapбoнилпpoпиoниJ:) 4-(Д-фенилпропионил)-дульцита гидрируют аналогично примеру 2. Катализатор отфильтровывают, и растворитель удаляют из фильтрата. Получают 3,3 г (выход 84%) кристаллического 1,2-5,6-диангидро-3-Y/ -карбок- сипропионил)-4-(Э -фенилпропионил - дульцита; Т.пл. 80 С. По данным тонкослойной хроматографии(Rf 0,3 или;0,7 с использованием смеси (6:4) этилацетата и циклогексана или смеси (8:2) бензола и метаног- ла соответственно) . продукт однороден.
Вычислено,%: С 60,31; Н 5,86; О 33,83. НггОв
,ч
Найдено,X: С 60,60; Н 5,49; О 34,50.
Эквивалентная масса: вычислено 373(МВ 378,ЗЗ;, найдено 390.
2057694
П р и м е р 6. Получе 1ие трис- соли 1,2-5,6-диaнгидpo-3,4-биc- ((-карбоксипропионил) -дульцита.
3,46 г (10 ммоль) 1,2-5,6-диан- 5 гидро-3,4-бис-(р-карбоксипропионил)- дульцита растворяют в 20 мп 96% этанола, осторожно нагревая, раствор охлаждают и добавляют раствор 1,2 кг (10 ммоль) трис-(гидроксиме- 10 тиламино)-метана в 10 мп воды. После отстаивания в холодильнике кристаллы отфильтровывают и высушивают в эксикаторе. Получают 3,7 г ( выход 80%) трис-соли.
15 Пример7. Получение динат- рий-1,2, -5,6-диангидро-3,4-бис-( карбоксипропионил дульцита .
246,29 г (1 моль 1,2-5,6-диан- гидро-3 , 4-бис- (I -карбоксипропионил - 20 дульцита,раствориют в 3360,3 мл (5 вес.7,) бикарбоната натрия с постоянным перемешиванием при комнатной температуре до тех пор, пока не прекратится выделение двуокиси углерода. 25 Полученный раствор отфильтровывают и лиофилизуют. Получают 426,29 г (1 моль(100%) динатрий-1,2-5,6- диангидридо-3,4-бис-( р -карбоксипропионил)-дульцита . В стазе бильном негигроскопичном (при комнатной температуре) веществе определено число колец, которое составляет 99%.
ИК-спектр: 1725 см сложный, 3 эфирный карбонил), 1680 см (кислот- ный карбонил). Характерная для кислотных гидроксилов полоса в 3500- 2800 см отсутствует.
Вычислено,%: С 39,447; Н 3,783.
40
С,, .. ЗН.О
Найдено,%: С 39,440; Н 3,780. П р и м е р 8. Аналогично примеру 1 получают катализатор палладий на угле, но используют 0,25 г хлорис45 того палладия. В результате получают катализатор с содержанием 1,5% палладия.
П р и м е р 9. Аналогично примеру 1 получают катализатор, но исполь50 зуют ,0,58 г хлористого палладия. В результате получают катализатор с содержанием 3,5% палладия.
Приме р 10, Аналогично примеру 2 получают 1,2-5,6-диaнгидpo-3,4- 55 бис-(р,-карбоксипропионил)-дул ьцит
с использованием катализатора по примеру 8. Выход целевого продукта составляет 0,85 г (81,6%).
S
Пример 11. Аналогично примеру 2 получают 1,2-5,6-диaнгидpo-3|4- биc-( карбоксипропионил -дульцит, используя катализатор примера 9, Вы™ ход целевого продукта составляет 0,79 г (75,8/..
Полученные соединения обладают более сильным подавляющим развитие злокачественных опухолей действием по сравнению с известными производными дуль-
.jjyUTa, не имеющими свободных карбоксильных групп, например, 1,2-5,6 диангидро-3,4-диацетш1дульцитом (А) и 1, 2-5, 6-диангидро-3,4-бис-(;й-кар бометоксипропионил/- дуЛьцитом ( Bj, Результаты испытаний приведены ниже.
Оценены терапевтические свойства следующих соединений:
А 1,2-5,6-диангидро-3,4-диаце тилдульдит.
в 1,2-5,6-Диангидро-3,4-бис- (/Э -карбоксипропионил -дульцит.
С I,2-5,6-диaнгидpo-3,4-биc-( фeнилпpoпиoнил -дульцит.
С-2 I,2-5,6-диангидро-3,4-бис- (f -карбоксипропионил -дульцит.
С-4 1,2-5, 6-диянгидро-3-(/Э- карбоксипропионил)-4-ацетилдульцит.
С-5 1,2-5,6-диангидро-3-( карбоксипропионил -4-(,В-карбо- мeтoкcипpoпиoнилj-дульцит,
С-6 1,2-5,6-диангидро-3-( - карбоксипропионил) -4-f 5-фенил-- пролионил)-дульцит.
Указанные соединения, где А,В и С являются дисложными эфирами в 3,4-положении 1,2-5,6-диангидро- дульцитола(ЛАД), не содержат никаких свободных карбоксильных jгрупп. Соединения С-2, С-4, .С-5 и С-6 также являются дис™ пожными эфирами в 3,4-положе- НИИ ДАД, но соединение содержит две, соединения С-4, С-5 и С-6 содержат одну карбокс.иль- ную группу.
Осуществлены .следунвдие .исследования:
а.Усвоение энзима,
б.Тест на токсичность,
в.Определение дозовой зависимоети ингибирования роста опухоли, ге- матоксичности и летальных эффектов для близких соединений, полученной отдельно на одинаковых моделях.
057696
г. Терапевтические индексы, полученные на различнь х твердых способных к трансплантации опухолях грызунов.
5 д. Ингибирование роста опухоли в твердой системе Саркома 180; влияние отдельной и повторяемых инъекций.
е) Мутагенность.
fO Полученные экспериментальные результаты представлены в табл.1-6.
а.Усвоение энзима. Соединение В пытались превратить
в соединение С-2 с помощью энзим- 15 ного гидролиза при следующих условиях-; время 0,5,1,0, 2,0, 4,О,6,О, 24,0 ч, температура 37 С; буфер 1/15 М фосфат. Энзим: химотрипсии, трип сии, ацилаза 1, ацилаза П. 20 Согласно оценке при вышеуказанньк условиях все сложноэфирные связи соединения В расщепляются с одинаковой скоростью. Следовательно, метиловый сложный эфир не может быть се- 5 лективно разложен и трансформирован f в кислотную форму.
б.Острая токсичность,
В табл.1 приведены данные по острой токсичности соединений.
30 Л650определяли на нормальных самцах мыши Swiss весом 27-31 г. После одной инъекции группа из 6 мьппей при одной дозе была прослежена в течение 21 дня.
5 ЛО ропределяли на крысах Wistar Walker, больньп; раком. Инъекции лекарства давали через 24 ч после трансплантации опухоли группе из 6 крыс и вели наблюдения в течение
0 0 дней,
Из данных табл.1 видно, что соединение С-2 наименее токсично из всех близких по структуре соединений, как для мьпией, так и для крыс.
5 в. Дозовая зависимость ингиби- рования роста опухоли, гематоксич- ности и летальных эффектов для близких соединений, полученная отдельно на одинаковых моделях,
Метод .Самцам крысы Wistar лекарства были введены через 24 ч после заражения 2 х 10 клетками Walker. Эффективность определяли по дозам, вызывающим 50%-ное ингибирование опухоли при взвещивании на десятый день. Дозы, приводящие к 50%-ному зт еньшению гранулоцитов, оцененно- ьгу на четвертый день, служили в качестве основы для сравнения гематок сичности. Отношение минимальной летальной дозы ГЛР,) к минимальной эффективной дозе (MEJ) EPjo- рассматривали как терапевтический индекс. Результаты приведены в табл.2.
Согласно табл.2 соединение С-2 активно против опухоли в такой же дозовой области, как производные близких по структуре соединений А,В и С (ЕРэо 13-17 мкмоль/кг) , в то время как соединение С-2 более чем в два раза менее токсично, чем все другие вещества, указанные здесь. Следовательно, терапевтический индекс С-2 в два раза предпочтительнее, индекса любого другого члена группы.
г.Терапевтические индексы .
д.Ингибирование роста опухоли в твердой системе Саркома 180; влияние отдельной и повторяемых инъекций.
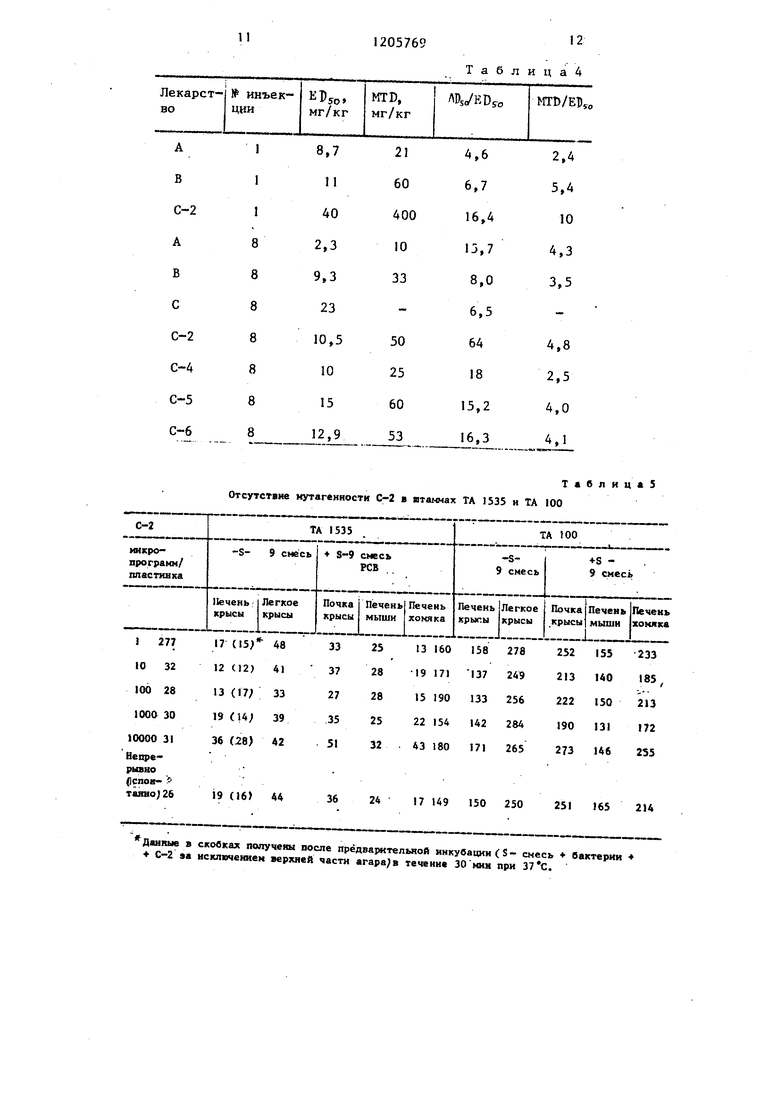
Метод. Небольшие образцы твер- дои Саркомы 180 были инокулированы на кожу самца мьшш Swiss. Интра- перитональное применение лекарства к группе из шести животных- начали на следующий день, на 1 1-й день опу холи были удалены для оценки. Данные приведены в табл.4.
е.Отсутствие мутагенности соединения С-2 в анализе салмонелла/мик- росома.
Все испытуемые производные алкил рующих сахарных спиртов за исключением С-2 были мутагенны в штаммах ТА 1525 и ТА 100 по результатам ана лиза салмонелпа/микросома. Даже с использованием микросомных энзимов, полученных не только из печени крысы, но также из легкого крысы, почки мыши или печени хомяка, соедине- ние С-2 не проявляет мутагенности к штаммам ТА 1535 и ТА 100. Соедине- ние С-2 также не проявляло мутагенности к штаммам : ТА 1537, ТА 1538 и ТА 98 в присутствии или отсутстви смеси S -9, полученной из печени крысы.
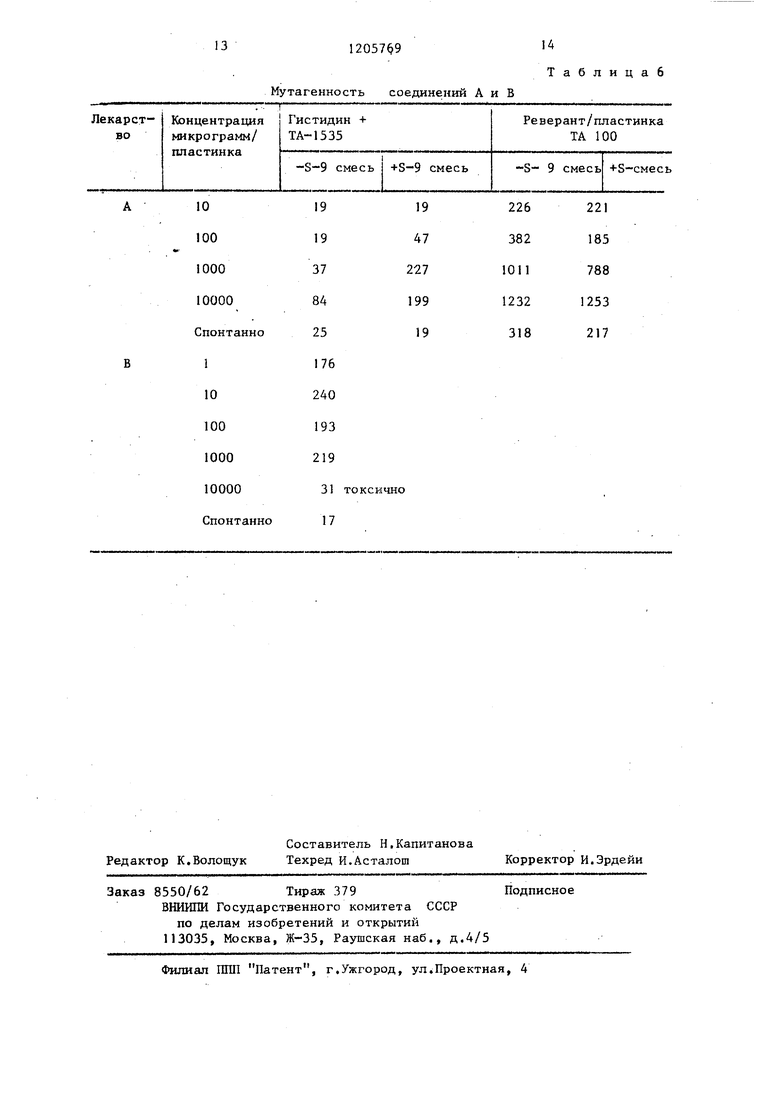
Мутагенность соединений А, В и С представлена в табл. 5 и 6.
Согласно зксперименту соединение С-2 оказалось немутагенным, так как концентра1щя соединения С-2 вплоть до -10 микрограим/Пластинка не уменьшает числа бактериальных кпеток, произрастаюншх в нормальной среде. Однако, соединение В вызывает 10-14-кратное увеличение числа бактериальных клеток, произрастающих в нормальной среде.
С другой стороны, соединение В вызывало 10-14-кратное увеличение числа реверантных пластинок, в то время как высокая концентрация 10 микрограмм/пластинка, как было найдено, является токсичной.
Сравнения токсикологических свойств и фармакологических данных таблиц и мутагенности, экспериментов по усвоению энзимов видно, что свободные карбоксильные группы в соединениях С-2, С-4, С-5 и С-6 проявляют такие биологические свойства молекул, которыми не обладают молекулы, не содержащие свободных карбоксильных групп.
Таблица 1
91205769
Исследование дозовой зависимости роста опухоли, гематоксичности и эффектов
.Терапевтический индекс, указанный в Декларации относительно соединений Аи С-2.
Терапевтические индексы, полученные на различных твердых трансплантируемых опухолях грызунов
Величины, указанные в скобках, опубликованы и в тоже время модифицированы в результате повторения зкспериментов.
ТаблицаЗ
II
2
4
5
6
1
1 1 8 8 8 8 8 8 8
8,7
11
40 2,3 9,3
23 10,5
10
15 12,9
-2
кро-
рограмн/
пастияха
1 277 10 32 100 28 1000 30
0000 31
епреывноcnoir- f ajmo) 26
Отсутствие мутагенности С-2 в штаммах ТА 1535 и ТА 100
ТА 1535ТА 100
-S- 9 смесь
11ечень:| Легкое крысы I крысы
17 (
12(12)41
13(17;33 19 (Ц)39 36 (28)42
19 (16) 44
+ S-9 смесь РСВ
Почка Печень Печень
крысы
мыши
хомяка
-S- 9 смесь
Печень Легкое
крысы
крысы
Почка крысы
3325
3728
2728
3525
5132
13160158278
19171 137249
15190133256
22154142284
43180171265
252 213
222 190 273
36
2417 149 150 250
251
Данные в скобках получены после предварительной ннкубацин(5- смесь бактерии + С-2 sa исключением верхней части агара;в теченн 30 мин при 37 С.
1205769
12
Таблица4
4,6 6,7 16,4 13,7
8,0
6,5
64
18
15,2 16,3
2,4 5,4 10 4,3 3,5
4,8 2,5
4,0 4,1
Т«блиц«5
-S- 9 смесь
+S - 9 смесь
Печень Легкое
крысы
крысы
Почка Печень Печень крысы мышн хомяка
158278
137249
133256
142284
171265
252 155 233 213 140 185
222 150 213 190 131 172 273 146 2S5
2417 149 150 250
251 165
214
1312057 9
Мутагенность соединений А и В
но
нно
19 19
37
84
25
176
240
193
219
31 токсично
17
Редактор К.Волощук
Составитель Н.Капитанова Техред И.Асталош
Заказ 8550/62 Тираж 379Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д.4/5
Филиал ШШ Патент, г.Ужгород, ул.Проектная, 4
14 Таблицаб
19
47
27
99
19
226
382
1011
1232
318
221 185 788 1253 217
Корректор И.Эрдейи




| название | год | авторы | номер документа |
|---|---|---|---|
| Производные дульцита,обладающие ингибирующим действием в отношении злокачественных опухолей | 1982 |
|
SU1194863A1 |
| Способ получения 1,2-5,6-диангидро-3,4-бис-( @ -карбоксипропионил)-дульцита или его динатриевой соли | 1982 |
|
SU1225487A3 |
| Способ получения замещенных ксилита или гексита | 1980 |
|
SU1075975A3 |
| Производные дульцита или ксилита,обладающие цитостатическим действием | 1980 |
|
SU979315A1 |
| Способ получения ацильных производных диангидрогекситов | 1975 |
|
SU581860A3 |
| Способ получения производных аминокислот, их солей рацематов или оптически-активных антиподов | 1976 |
|
SU670214A3 |
| Способ получения производных мочевины | 1980 |
|
SU1158039A3 |
| Способ получения -6-дезокси-5-окситетрациклина или его солей | 1974 |
|
SU632298A3 |
| Способ получения замещенных мочевины | 1980 |
|
SU1176831A3 |
| Способ получения N-нитрозо-N-(бэта-хлорэтил)-карбамоилпептидов или их кислотно-аддитивных солей | 1982 |
|
SU1424739A3 |
Способ получения производных дулыцита общей формулы СН -СН-СН-СН-Ш-СНп Х I I X о . ORi OR О где -f) - карбоксипропионил; или I - Д) - карбоксипропио- нил; или или R, - /Ь - Rj - Э (,-Р - R -р, - ацетил, карбоксипропио- нил; карбонетокси- пропионил; карбоксИпропионил; фенилпропионил, g иди их солей, отличающий - с я тем, что соответствующий бензило- вый эфир подвергают расщеплению действием водорода в присутствии в качестве катализатора палладия на угле при содержании палладия от 1,5 до 3,5% в безводном метаноле при 20-25 0. СО
| Вейганд-Хильгетаг | |||
| Методы эксперимента в органической химии | |||
| М.: Химия, 1968, с.368-369. |
Авторы
Даты
1986-01-15—Публикация
1981-11-03—Подача