где R имеет указанные значения, подвергают обработке галогенводо-. родной кислотой в водно-ацетонозвом растворе при (-5) -( и рН 6,57 с образованием соответствукщего дигалогензамещенного соединения.
2. Способ по п. l,oтличaю щ и и с я тем, что процесс обработки галогенводородной кислотой ведут в водной среде иэ соответствукщего галогенида щелочного металла и сильной кислоты, например серной, при 5-25°С и рН среды 6,5-7.






| название | год | авторы | номер документа |
|---|---|---|---|
| Производные дульцита или ксилита,обладающие цитостатическим действием | 1980 |
|
SU979315A1 |
| СПОСОБ ПОЛУЧЕНИЯ РАЦЕМАТОВ ОПТИЧЕСКИ АКТИВНЫХ/ | 1971 |
|
SU320997A1 |
| Способ получения ацильных производных диангидрогекситов | 1975 |
|
SU581860A3 |
| Способ получения 3- кетоандростенов | 1982 |
|
SU1189353A3 |
| Способ получения 4,5-диарил-2-нитроимидазолов | 1979 |
|
SU940647A3 |
| Способ получения 1-оксадетиацефалоспоринов | 1978 |
|
SU833162A3 |
| Способ получения оптически активныхпРОСТАглАНдиНОВ или иХ ОпТичЕСКиХАНТипОдОВ, или иХ РАцЕМАТОВ | 1978 |
|
SU843736A3 |
| Способ получения производных конденсированных индолов или инденов | 1973 |
|
SU728716A3 |
| Способ получения производных 4 @ -(1 @ -алкен-1 @ -ил)-2 @ ,5 @ -дигидрокси-3,3 @ ,4,5,6,6 @ -гексагидро-2Н-циклопента (в) фурана | 1985 |
|
SU1447282A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛОВЫХ ЭФИРОВ НЕНАСЫЩЕННЫХ КИСЛОТ | 1968 |
|
SU207827A1 |
1.СПОСОБ ПОЛУЧЕНИЯ ЗАМНФЕННЬЗХ КСИЛИТА ИЛИ ГЕК СИТА общей формулы 1А или 1Б OS, I R, СНГСН-СН- СН-СНгН, или RrJHfCH-iJH-CH-CH-CHjR. / I I I Iь 2 3 г где И - галоген гидроксил или вместе с Rкислородный мостик; R - метил; R - метил, водород, ацетил, бензоил, фенилбутирил. Причем в соединении формулы 1Б стерическое расположение атомов соответствует конфирурации дульцита, мапнита или 1 -сорбита, отличающийся т:&л, что соединение формулы R А или п Б ОН СНгСн-сн-сн-снг или 0- снг-сн-сн св-сн ен Ло iffiH Y подвергают метилированию диазометаном в среде эфира или диоксана в присутствии эфирата трехфтористого бора или диметилсульфатом в присутствии гидрида натрия в среде эфира, или йодистым метилом в присутствии бкиси бария в среде диметилформамида с получение 3-метокси-1,2-4,5-дианг1Щроксилита или монои/или ди-метоксизамещенных 1,2-5,6-диан1|идрогексита, приче моноо меток сизамеценное 1,2-5,6-диангидрогексита подвергают ацилированию соответствунвдими агентами, выбранныел ми из группы хлористый ацетил, хлористый бензоил или фенкл(Уутйрил) лактон в среде бензола в присут ствии триэтиламина при 40-50 с, ел а полученные после метилирования Эсшещенные ксилита и после дополнительного ацилирования замещенные гексита формулы (В или 5 ООН, СНгСН-СН-СК-СИ, или Ч V СНгСН-СВ-СИ-СИ-СН; п i L. ./ OR. СИ,

Изобретение относится к способам получения новых замещенных ксилита или гексита, которые обладают цитостатической активностью. Известен ряд замещенных гекситаг 1,2-5,б-диангидропаннитол, 1,2-5,6-диангидродульцитол, которые проявля ют цитостатические свойства С13 Известно также, что производные 1,2-4,5-диангидроксилита общей форм лы CHf-CH-CH-CH-CMg 0 ОСОБ.О где R -.метил, 3-фенилпропил, фенил, п-дифенил, особенно 3-(п-фенилбензоил)-,2-4,5-диангидроксилит проявляет цитостатическое действие, (его 1-D 50 1000 мг/кг, в то время как незамещенный, т.е. 1,2-4,5-диангидроксилит имеет LD 200 мг/кг) С23. Известно, что диэпокси- и дигалоген-3,4-0-изопропилиденгек ситы не проявляют цитостатической активности 3.. Способы получения различных заме щенных многоатомных спиртов основаны на известных методах. Так, ацилирование многоатомных спиртов ведут галоидными ацилами в присутствии акцептора галоидвсдор да, например пиридина, при 60-65 0 4 3 или при 45°С в среде сухого .бензола. Этим способом велут получе ние указанных соединений, т.е. 3-Сп фенилбензоил)-,2-4,5-ксилита. Метилирование гидроксилсодержащих соединений осуществляют с помощью либо дна3ометана в среде эфира в присутствии катализаторов, либо диметилсульфатом или галоидалкилом в присутствии щелочного агента в среде растворителя. Раскрытие оксирановых колец ведут, как правило, в присутствии кислых катализаторов, а замыкание их - в присутствии основных катализаторов с получением циклических простых эфиров. Обработка послед;€их галоидводородными кислотами,.например ней или НВг , приводит к раскрытию эпоксидного кольца и присоединению HCft или НВг с образованием галогенгидринной группировки Г5Д. Целью изобретения является получение новьах замещенных ксилита или гексита - потенциально физиологически активных веществ. Поставленная цель достигается способе получения замещенных кфилита или гексита общей формулы.А илиГБ; 9H-R2 CHj-R, где R - галоген; R гидрок сил или EIместе с кислородный мостик; - метил R - водород, ацетил, метил, бензоил, фенилбутирил, причем стерическое расположение атомов в 1,2-5,6-диангидрогексита соответствует конфигурации дульцита, маннита или D- сорбита,, за слючающим|СЯ в том, что соединение формулы S А или IБ подвергают метилированию диазометаном в среде эфира в присутствии эфиратата трехфтористого бора или диметилсульфатом в присутствии гидрида натрия в среде эфира или диокса-г на или йодистым метилом в присутствии окиси бария в среде диметилформамида с получением 3-метокси1,2-4,5-диангкдроксш1ита или монои/или ди-метоксизамещенных 1,2-5,6диангйдрогексита, причем моно-метоксизамещенное 1,2-5,6-диангндрогексита подвергают ацилированию iX OTветствующими агентами, выйранньми из группы хлористый ацетил,хлористый бензоил или фенилбутириллактон в среде бензола в присутствии триэтиламина при 40-50с, а полученные после метилирования замещенные ксил та и дополнительного ацилирования э мещенные гексита формулы ij или iv v HaCO-CH CH-OCH, I r CH-OK CH, где R имеет указанные значения, подвергают обработке г алогенводородной кислотой в водно-ацетоновом растворе при (-5) -(25fc к рН. среды 6,5 - 7 с образованием при этом дигалогензамещённого соединения. При этом процесс обработки галогенводородной кислотой ведут в водной среяе из- соответствуквдего галогенида щелочного металла и сильной кислоты, например серной, при 525.С и рН среды 6,5 - 7. В случае необходимости дигалоген Зс1мещенные соединения могут быть обратно превращены в диангндросоединения с помощькз щелочного агента например анионобменной смолы (в OfO содержащей аминогруппы на основе полистирола. Пример 1 . 1,2-5,6-Диангидро-3-меток сидульцит и 1,2-5,6диангидра-3,4-диметоксидульцит. 12 г (0,032 моль) 1,2-5,6-диангидродульцита суспендируют в 1500 мл безводного эфира и при в реакционную смесь при перемешивании пропускают газообразный диазометан. После насыщения эфира диазометаном добавляют несколько капель эфирата трехфтористого бора в эфире при непрерывном пропускании газообразного диаэометана через реакцконную смесь. Когда реакционная смесь насыпается диазометаном, повторяют добавку эфирата трехфторис того бора. По окончании взаимодейСТВИЯ 1,2-5,б-диангидродульцита к реакционной смеси добавляю т насыденный водный раствор бикарбоната натрия, необходимый для разложения добавленного эфкрата трехфторис того бора, и реакционную смесь пере мешивают в течение получаса, затем сушат над безводна ка;рбонатом натрия. Профильтрованный эфирный выпаривают и остаток хроматографируют на колонке с силикагелем при двадцатикратном разбавлени остатка смесью бензола с этилацетаТОМ (1:1). Содержащиеся 1,2-5,6гдиаигидро-3-метоксидульцит- и 1,2-5,6-диангидро-3,4-яиметок сидул ьцит-фракции выпаривают досуха. Получают 4,0 г 1,2-5,6-диангидро-3-метоксидульцита в вкде бесцветного масла. Выход 30,48%; ,47 (растворитель бензолэтилацетат 1:1). Кроме того, получают 6,0 г 1,2-5,6-диангидро- 3,4- диметоксидульцита в виде белых кристаллов. Вы(ход 42,05%; т.пл. 38-40 С (гексан). ,75 (растворитель бензол:этилацетат 1:1). Пример 2 . 1,2-5,6-дигидро-3,4-диметоксидульцит. 12 г 1,2-5,6-Дигидродульцита метилируют диазометаном ангшогично примеру 1. Метилирование осуществляют до тех пор, пока первоначально образующийся 1,2-5,6-диангидро3-метоксидульцит не превратится в 1,2-5,6-диангидро-3,4-диметоксидульцит. Полученную реакционную смесь обрабатывают аналогично примеру 1. Выход 77,1%; R г 0,75 (растворитель как в примере 1). Найдено,%8 С/Я 55,4/8,0. Cgag)4 Вычислено,%: С/Н 55,2/8., I П р riм е р 3 . 1,2-5,6-Диангидро-3,4-диметок сидульцит. 5 г (0,031 моль) 1,2-5,6-диангийро-3-метоксидульцита метилируют диазометаном аналогично примеру 1. Получают 4,0 г 1,2-5,6-диангидро-3, 4-диметоксидульцита. ВЕЛСОД 75%; т.пл. 38-40 С; «. 0,75 (растворитель как в примере 1). Найдено,%: С/Н 55,3/8,2 Вычислено, %: с/Н 55,2/8,1. Пример 4. 1,, 6-Диан гидро- 3-метокси-4-ацетилдульцит. 1,6 г (0,01 моль) 1,2-5,6-диaнгlщpo-3-мeтoкcидyльцитa растворяют в 25 мл абсолютного бензола, и к реакционной смелей при перемешивании добавляют 1,4 мл (0,01 моль} безводного триэтиламина. Реакционную смесь затем нагревают до и при этой температуре в течение часа прикапывают 0,78 г(О,01 моль)безводного хлорис ТОГО ацетила в 3 мл безводного бенэола. Реакционную смесь перейешива- ют в течение 30 мин , затем отсасывают выпавшее в осадок вещество и промывают бензолом. Объединенные бензольные фазы выпаривают в вакууме и оставшийся сироп хроматограФируют на колонке с силикагелем при тридцатикратном разбавлении сиропа смесью бензола с этилацетатом (95:5). Фракцию, содержащую 1,2-5,6-диaнгl цpo-3-мeтoкcи-4-aцeтилдyльциt, выпаривают досуха. Получают 1,3 г бесцветного масла. Выход 63%; RJ г 0,77 (растворитель как в примере 1 Пример 5. 1,2-5,6-Диангид -3-метокси-4-6енэоилдульцит. 1,6 г 2,2-5,6-диангидро-З-меток сидульцита растворяют в 25 мл безв ного бензола, и к реакционной смес при перемешивании добавляют 1,4 мл (0,01 моль) безводного триэтилгичин Реакционную смесь нагревают до 45 и при этой температуре в течение часа при перемешивании прикапывают 1,4 г (0,01 моль) хлористого бензо ила в 5 мл безводного бензола. Реа ционную смесь перемешивают в течение 30 мин при 45°С, затем отсасывают выпавшее в осадок .воцествр и промывают бензолом. Объединенные бензольные фазы выпаривают в вакууме и оставшийся сироп хроматографируют на колонке с силикагелем при тридцатикратном разбавлении сиропа смесью бензола с этилацетатом (95:5), Фракцию, содержащую 1,2-5,6-диангидро-3-метокси-4-бензоилдульцит, выпаривают досуха.По лучают 1,72 г бесцветного масла. В ход 65%; f 0,88 (растворитель как в примере 1) . Пример 6. 1,2-5,бтДиангид ро-3-метокси-4-5-фенилбутирилдульцит. 1,6 г 1,2-5,6-диангидро-3-меток сидульцита растворяют в 25 мл безводного бензола и добавляют при пе ремешивании раствор 1,4 мл (0,01 моль) безводного триэтиламина. Затем к реакционной смеси при 45 С и в течение часа при перемешивании прикапывают 1,85 г (0,01 моль) -фенилбутирчллактона в 5 мл безвод ного бензола. Реакционную смесь перемешивают еще 30 мин при , затем выпавшее в осадок вещество о сасывают и промывают бенэолотл. Объ диненные бензольные фазы выпариваю в вакууме. Остагацийся сироп хро- матографируют на колонке с силикаг лем при тридцатикратном разбавлеНИИ сиропа смесью бензола с этилаце гатом (95:5). Фракции, содержащие 1,2-5,6-диангидро-3-метокси-4-и -фенилбутирилдульдит, выпаривают досуха. Получают 1,4 г бесцветного масла. Выход 39%; Rf 0,92 (растворитель как в примере 1). И р и м е р 7. 1,2-5,б Диангид ро-3,4-диметоксидульцит. 8,78 г (0,36 моль) гидрата натрия (55%-ная.суспензия) промывают 3 раза по 400 мл безводным эфиром, затем в течение часа при комнатной (20-25 0 температуре переме шивают в 40Q мл С5езводного эфира с 6,2 г 1,2-5,6-диангидродульцита. К таким образом полученной реакционной смеси сначала добавляют 40 капель безводного изопропанола, затем в течение 2 ч прикапывают.16 мл (0,17 моль) диметилсульфата. Далее реакционную смесь перемеишвают 72 ч, и при перемешивании добавляют 40 мл безводного этанола, затем 100 мл воды. После этого реакционную смесь при сильном перемешивании прикапывают к смеси 5000 мл этилацетата и 500 г безводного карбоната натрия, а после окончания прикапывания смесь перемешивают вце полчаса. Полученный отфильтрованный раствор сушат над безводным сульфаРом натрия и выпаривают. Полученный сироп хрома тографируют на колонке с силикагелем при тридцатикратном разбавлении сиропа смесью бензола с этилацетатом (1:1). Фракции,содержащие 1,25,6-диангидро-3,4-диметоксидульцит, выпаривают досуха и кристаллический осадок кристаллизуют из гексана. Получают 2,9 г 1,2-5,6-диангидро-3,4диметоксидульцита. Выход 40%. Найдено,%: С/Н 55,1/8,1 Св%04 Вычислено,%: С/Н 55,2/8jJ. Т пл. 38-4б°С,R 0„75 (растворитель как в примере 1)„ Пример 8. 1,2-5,6-Диангидро-3,4-диметрксидульцит. 4,8 г 1,2-5,6-диангидродульцита растворяют в 24 мл безводного диметилфо1 1амида, и при перемешивании и 20-25С смешивают с 24 мл диоксана, 24 г окиси бария и 8,7 мл йодисTOIXD метила, полученную реакционную смесь затем фильтруют и полученный раствор смешивают с этилацетатом. Этилацетат сливают с масла и масло промывают два раза по 10 мл этилацетатом. Объединенные этилацетатные растворы выпаривают и остаток хроматографируют на колонке с силикагелем при пятидесятикратнсм его разбавлении смесью бензола с этилацетатом (1:1). Фракции, содержащие 1,2-5,6-диангидро-3,4-д:иметоксидульцит, выпариваются, и продукт кристгиплизуется из гексана. Получают г 1,2-5,6-диангидро-З,4-диметилдульцита. Выход 35,8%; т.цл. 38-40с. Найдено, %: С/Н 55,3/8,1. Вычислено, %: 55,2/8,1. Пример 9. 1,2-5,6-Диаигидро-3-метокси-1)-маннит и 1, 2-5,6-диангидро-3,4-диметил-Г-маниит. 12 г (0,032 моль) 1,2-5,6-дианггидро-В -маннита суспендируют в 1500 мл безводного эфира, при О С в реакционную смесь при перемешивании пропускают газообразный диазометан. После выделения эфира диазометаном добавляют несколько капель эфирата трехфтористого бора в эфире при непрерывном пропускании газообразного диаэометана через реакционную смесь. Когда реакционная смесь
насыцается диазометаном, то снова повторяют добавку эфирата трехфторитого бора. По окончании взаимодействия 1,2-5,6-диангидро-1)-маннита к реакционной смеси добавляют необходимый для разложения добавленного эфирата трехфтористого бора насьащенный водный раствор бикарбоната натрия. Реакционную смесь перемешивают в течение получаса, затем сушат над прокаленным карбонатом натрия. Профильтрованный эфирный раствор вьшаривают и остаток хроматогрфируют на силикагелевой колонке при двадцатикратном его разбавлении смесью бензола с этилацетатом (1:1). Фракции, содержащие 1,2-5,6диангидро-3,4-диметок си-Б-маннит, выпаривают досуха. Получают 3,5 г 1, 2-5,6-диангидро-3-метил-1)-маннита в виде бесцветного масла. Выход :2б,7%; R : 0,43 (растворителькак в примере 1).
Кроме того, получают 4,9 г 1,2-5,6-диангидро-3,4-диметокси-Dманнита в виде бесцветного масла.
Выход 35%; Р 0,74 (растворитель как в примере 1).
Пр и м е р 10. 1,2-5,6-Диангвдро-3,4-диметокси-Г-сорбит.
12 г (0,082 моль) 1,2-5,6-диангидро-D-сорбита суспендируют в 1500 мл безводного эфира, и в полученную суспензию при 0°С и перемешивании пропускают газообразный диазометан. После насыщения эфира диаэрметаном добавляют к реакционной смеси несколько капель эфирата трехфтористого бора в эфире при непрерывном пропускании диазометана. Когда реакционная смесь насытится диазсялетаном, снова добавляют эфират трехфтористого бора. По окончании взаимодействия первоначально образуицееся монометильное соединение превращают в диметильноё соед1|н ние добавлением к реакционной сме-/си необходимого для разложения эфирта трехфтрристого бора насьяценного водного раствора бикарбоната натрия, и реакционную смесь перемешива ют в течение получаса, после чего сушат над прокаленньм карбонатом натрия. Отфильтрованный эфирный раствор выпаривают, и остаток хрома тографируют на колонке с силикагелем двадцатикратным разбавлением остатка смесью бензола с этилацетатом (1:1). Фракции, содержащие 1,2-5,6-диангидро-3,4-диметокси-1)-сорбит, выпаривают досуха. Получают 4,8 г 1,2-5,6-диангидро-3,4-. диметокси-В-сорбита в виде бесцветного . Выход 33,6%; ,74 (растворитель как в примере
1). Пример И. 1,2-4, 5-Диангидро-3-меток сиксилит.
20 г (0,17 моль) 1,2-4,5-диангидроксилита растворяют в 1500 мл безводного эфира, и раствор при комнатной (20-25 С) температуре и при перемешивании насыцают газообрньм диазометаном. Затем добавляют к реакционной смеси несколько капель эфирата трехфтористого бора в эфире при непрерывном пропускании газообразного диазометана через реакционную смесь. Когд реакционная смесь насытится диаэометаном, снова повторяют добавку эфирата трехфтористого б.ора. По окончании взаимодействия 1,2-4,5-диангидроксилита к реакционной смеси добавляют необходимый для разложения добавленного эфирата трехфтористого бора насыщенный водный раствор бикарбоната натрия, и реакционную см перемешивают в течение получаса, после чего сушат над прокаленным карбонатом натрия. Отфильтрованный эфирный раствор выпаривают и остаток перегоняют в вакууме. Получают 15 г 1,2-4,5-диaнгидpo-3-мeтoкcи|kcилитa в виде бесцветного масла. Выход 67%; т.кип. 48°С/1,5 мм рт.с.
Пример 12. 1,5-Дибром-1,5дидезок си-3-метоксик силит.
К раствору 1,0 г (0,0077 моль) 1,2-5,6-диангидро-З-метоксиксилита в 2 мл ацетона при температуре ниже (-5) - (0)°С и при перемешивании прикапывают 6 мл охлажденного (-5) - (0)°.С раствора бромистоводородной кислоты, затем реакционную смесь перемешивают в течейие получаса при температуре ниже 0°С. К таким образом полученному раствору добавляют бикарбонат натрия и устанавливают рН равньг- 6. Выпавшее в осадок вещество отфильтровывают и без высушивания смешивают с 50 мл дихлорэтана. Дихлорэтан сушат над прокаленным сульфатом , затем концентрируют до объема 10 мл и смешивают с гексаном до начинающегося опалесцирования раствора. После охлаждения выпавший в осадок материал отсасывают и рекристаллизуют из смеси дихлор этана с гексаном (1:1). Получают 1,4 г 1,5-дибром-1,5-дидeзoкcи-3 мeтoкcикcилитa в виде бесцветных кристаллов. Выход 62%; т.пл. 78БО С; R 0,59 (растворитель как в примере 1).
Пример 13. 1,5-Дихлор-1,5-дидезокси-3-метоксиксилит.
К раствору 1,0 г (0,0077 моль) 1,2-5,6-диангидро-3-метоксиксилита в 2 МП ацетона при (-5) - (0) С и при перемешивании прикапывают 8 мл охлажденного ниже О °С концентрированного раствора соляной кислоты, затем реакционную смесь перемешивают в течение получаса при температуре ниже . Таким образом полученный раствор вьшаривают в вакууме и полученное масло хроматографиру ют на колонке с силикагелем при двадцатикратнсм разбавлении масла смесью бензола с этилацетатом. Объединенные фракции содержащие 1,5-ДИХЛОР-1,5-дидезокси-3-метоксиксилит, выпаривают. Получают 0,8 г 1, 5-дихлор-11 5-дидезокси-3-метС)Кси ксилита в виде бесцветного масла.Вы1соД 51 %;( 0,52 (растворитель как в примере 1}.
Пример 14. 1,5-Дийoд-l,5дидeзoкcи-3-мeтoкcикcилит. :15 1,2-5,6-ДиангидроЗ-метоксидульцит НВЬ 16 1,2-5,6-Диангидро3-мeтoкcидyльцит нее 1,2-5,6-Диангидро3-меток сцдуль цит НЗ
1,2-5,6-Диангидро-1,6-Дибром-1,6-диде3,4-диметок сидуль-зок си-3,4-диметок сиНВг дульцит1 37
цит
1,6-Дийод-1,6-диде1,2-5,6-Диангидро- . зокси-3,4-диметок3,4-Д1 1етоксисидульцнтIf 66 дульцитНД
20 1,2-5,6-Диангидро-1,6-Дибром-1,6-ди- ,
З-метокси-4-аце-дезокси-3-метоксиНВг 4-ацетилдульцит1,4
тилдульцит
1,6-Дийод-1,6-диде1,2-5,6-Диангидрозокси-З-метокси-43-метокси-4-ацетилацетилдульцит1,8 дульцитЮ
1,2-5,6-Диангидро-1,66-Дихлор-1,6-ди-
22
З-метокси-4-ацетил- дезокси-3-метоксидульцитнее 4-ацетилдуяьцит0,9 Примечание: Растворитель смесь
К раствору 1,0 г (0,0077 моль) 1,2-4,5-диангидроксилита в 2 мл ацетата при (-5) - (0)С и при перемешивании прикапывают. 8 мл охлажденного до (-5) - (0)С концентрированного раствора йодистоводородной кислоты, затем реакционную смесь перемешивают в течение получаса. Вьщелившиеся кристаллы отсасывают и рь)ристаллизуют из этилацетата. Получают 1,5 г 1,5-дийод1,5-дидезйкси-З-метоксиксилита в виде бесцветных кристаллов. Выход 50,5%; т.пл. 105-10бс.
В табл. 1 представлены продукты примеров 15-22 с их характеристиками.. .
Таблица
0,8
160
0,83
165
0,
Масло
77 0,65
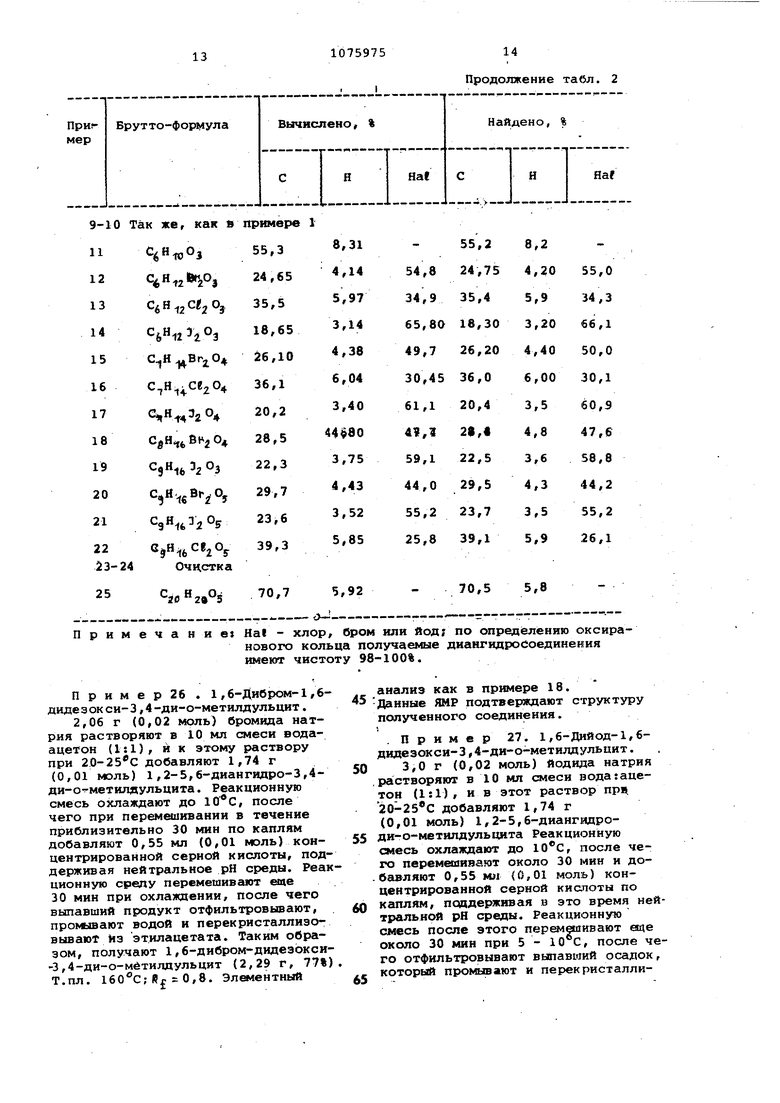
65 0,52 1,б-Дибрсж1-1,6-дидезокси-3-метоксидульцит1,6-Диxлop-l,6-диД зокси-3-метоксидульцит1,6-Дийод-1,6-диде-1,4 зоксй-З-метоксидуль цит 52 130-1 0,42 49 1360,38 54 132 0,46 бензола с этилацетатом (1:1J. Пример 23. 1,2-5,6-Диангидро-3,4-диметоксидульцит. 14,4 г 1,6-дибром-1,6-дидeзoкcи 3,4-димeтoкcидyльцитa, 100 мл воды 100 МП анионообменника(ОН -форма)т па AD (содержащая сильные щелочные аминогруппы:винтетическая смола на основе полистирола,выпускаемая фир Tfitrokemia Jpartelepek, Balatx nfuzfо) перемешиваются в течение 15 мин при 20-25с. Затем анионообменник отсасывают и промывают 3x30 мл дистиллированной воды.Водный раствор объединяют с проливньм водами, и объединенный раствор выпаривают при пониженном давлении до объема 40 мл, после чего при перемешивании добавляют суспензию 1200 мл этилацетата и 120 г карбоната натрия. После отфильтрювыванн этилацетатный раствор обезвоживают над прокаленным сульфатом натрия, затем выпаривают досуха. Остаток 1рекристаллизуют из гексана. Получают 4,3 г 1,2-5,б-диангидро-3,4диметоксйдульцита. Выход 58%; т. пл. 38-40 С. Найдено, %: С/Я 55,1/8,3, Вычислено,: С/Н 55,2/8,1. П р и м е р 24. 1,2-5,6-Диангидро- 3-метоксидульцит.. 13,8 Г 1,б-дибром-1,6-дидезокси-З-метоксидульцита, 100 мл воды и 100 мл анионообменника (ОН форма) типа перемешивают в течение 15 мин. Анионообмвнник отсасывают и промывают 3-30 мл водой. Водный раствор и промывные воды объединяют, и этот раствор выпаривают при пониженном давлении до объема 40 мл, при перемешивании добавляют суспензию 1200 мл этилацетата и 120 г карбоната натрия. После фильтрования этилацетатный раствор обезвоживают над прокаленным сульфатом натрия, после чего выпаривают досуха. Полученный сырой продукт хроматографируют на колонке с силикагелем с помощью тридцатикратного объема смеси бензола с этилацетатом (1:1). Получают рацемат (3,6 г) чистого 1,2-5,6-диан гидро-3-метоксидуз1ьцита. Найдено,%: С/Н 52,7/7,40 C Hl204 Вычислено,%: С/Н 52,4/7,54. Выход 52%. Пример 25. 1,2-5,6-ДиангидроЗ-метокси-4(п-фенилбензоил)-дульцит. 1,6 г (0,01 моль) 1,2-5,6-диангидро-3-метоксидульцита растворяют в 25 мл безводного бензола. При перемешивании и 20-25°С к этой реакционной смеси добавляют 1,4 мл безводного триэтиламина. Реакционную смесь эат&л перемешивают 30 мин при 45°С, затем выпавшее в осадок йещество отсасывают и промывают бензолом. Объединенные бензольные фазы выпаривают в вакууме, и оставшийся сироп хроматографируют на колонке С силикагелем с помосдью тридцати- . кратного объема окиси бензола с этилацетатом (95:5). Содержащее 1,25,б-диангидро-3-метркси-4-(rt-фенилбензоилУ-дульцит фракции выпаривают досуха, и остаток рекристаллизуют из этанола. Получают 1,46 г 1,25,б-диангидро-3-метокси-4- (п-фенилбензоил)-дульцита.-Выход 43%; т.пл. 75-78C;Rf 0,9 .(растворитель, как в примере 1). Данные элет ентного анализа получаемых по примерам соединений представлены в табл. 2. Таблица 2 Примечание}
П р и м е р 26 . 1,6-Дибpoм-l,6дкдeзoкcи-3 ,4-ди-о-метилдульцит .
2,06 г (0,02 моль) бромида натрия растворяют в 10 мл смеси водаацетон (1:1), и к этому раствору при 20-25 С добавляют 1,74 г (0,01 моль) 1,2-5,б-диaнгидpo-3,4ди-o мeтилдyльцитa. Реакционную смесь охлаждают до , после чего при перемешивании в течение приблизительно 30 мин по каплям добавляют 0,55 мл (0,01 моль) концентрированной серной кислоты, поддерживая нейтральное рН среды. Реакционную перемешивают еще 30 мин при охлаждении, после чего выпавший продукт отфильтровывают, прокьшают водой и перекристаллиэовывают Из этилацетата. Таким образом, получают 1,6-дибром-дидеэокси-3,4-ди-о-мётилдульцит (2,29 г, 77%) Т.пл. 16 0,8. Элементный
Продолжение та(5л. 2
анализ как в примере 18. -Данные ЯМР подтвесосдают структуру полученного соединения.
.Пример 27. 1,б-Дийод-1,6дидеэокси-3,4-ди-о-метилдульцит.
3,0 г (0,02 моль) натрия растворяют в 10 мл смеси вода:ацетон (1:1) , ив этот раствор при. 20-25 С добавляют 1,74 г (0,01 моль) 1,2-5,б-дианг здроди-о-метилдульцита Реакционную
смесь охлаждают до , после чего перемешивают около 30 мин и добавляют 0,55 мл (0,01 моль) концентрированной серной киапоты по
каплям, псщдерживая это время нейтральной рН среды. Реакционную смесь после этого перемешивают еще около 30 мин при 5 - 10 С, после чего отфильтровывают выпавший осадок,
который промьшают и перекристаллиHal - хлор, бром или йод; по определению оксиранового кольца получаемые диангидросоединения имеют чистоту 98-100%.
1 51075975 16
зовывают из. гексана. получают таким Т.пл. Rj 0,83. Элементный образом 1,б-дияолвд 1,б-дидеэокс -- анализов пределах ошибки c6oTBeTCTBj -3,4-ди-о-мвТ11пдульцит (3,44 г 80%). ет рас считанным данным примера 19.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Institoris I | |||
| and al | |||
| InoesstMgation into the Correlation of Cytostatic Actiorty with the in irtro Diepoxide Formation on Some Tereninally Substituted Hexitols.- Neoplasma, 17, 1, 1970, p | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Arznermittel Porschung, 17, 1967, 145-149 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Под ред | |||
| Н.К.Кочеткова, 1967, с | |||
| Солесос | 1922 |
|
SU29A1 |
| S.BKuiep К.,Пирсон Д | |||
| Органически синтезы | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Катодная трубка Брауна | 1922 |
|
SU330A1 |
Авторы
Даты
1984-02-23—Публикация
1980-08-15—Подача