I . 1
Изобретение относится к способу получения гидрата окиси трициклогек- силолова, который применяется в органическом синтезе.
Цель изобретения - увеличение выхода и чистоты целевого продукта.
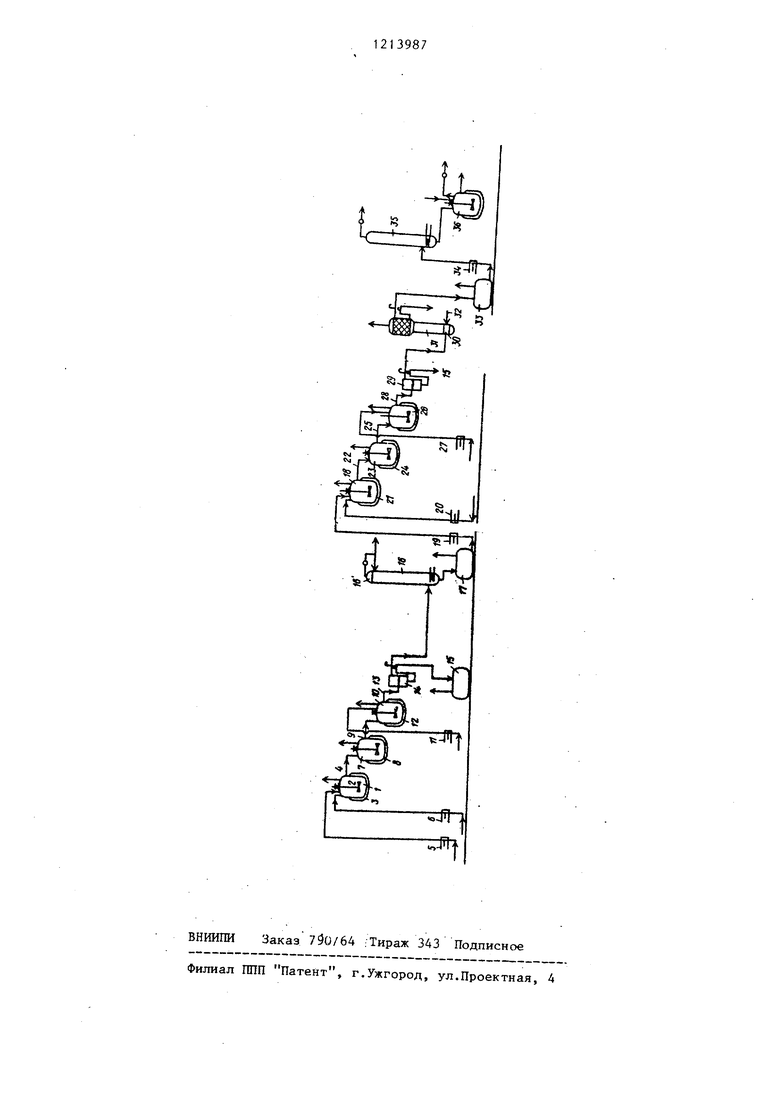
На чертеже показано оборудование для осуществления предлагаемого способа
П р И м е р 1 . Непрерывньй способ.
. В реактор 1, снабженный мешалкой 2, термометром, конвенционной о слаж- дающей системой, внешней охлаждающей рубашкой 3 и боковой отводной линией 4 слива, имеющий полезР ую емкость 15 и слива, при перемешивании загружают 3 л толуола н 1 л тетрагидрофурана с целью запуска оборудования, чтоб облегчить перемешивание и не начинать работу с пустым реактором. Затем после запуска оборудования с помощью мерных насосов 5 и 6 одновременно добавляют 23,8 л/ч раствора хлорида циклогексилмагния в тетра- гидрофуране, вытекающего из з строй- ства для непрерывного производства реактива Гриньяра, причем это соединение соответствует 7,63 кг/ч реактива Гриньяра при 100% или 0,053 кмощ /ч и 35 л/ч раствора тетрага- логенидолова в толуоле, что соответствует 4,64 кг/ч SnCl при 100% или 0,0178 кмоль/ч. Поэтому реагенты вводят таким образом, что они реагируют при молярном отношении тетра- галогенидолова к реагенту/Гриньяра, равном 3:1. Температуру в реакторе Поддерживают равной 42-46°С путем циркуляции воды в рубашке 3 этого реактора. Перемешивание проводят эффективно у чтоб облегчить теплообмен и избежать локальных перегревов.
Когда реактор заполнен, реакционную композицию выводят наружу че. p€t3 боковой слив и переводят во второй реактор 7, подобный реактору 1, В Этом реакторе 7 завершается реакция и достигается температура 65 - 68 С. Это значение температуры в реакторе поддерживается постояннь:(м за счет циркуляции горячей воды в .рубашке 8 реактора 7,
Соединение, которое выводят через боковой слив 9 реактора 7, подают в реактор 10 гидролиза, имеющий такие же размеры как и предьщущий реактор но выполненный из кислотоупорного
0
5
0
5
987
материала. Одновременно с выводом композиции из реактора 7 в реактор 10 с помощью мерного насоса 11 добавляют 14 л/ч 5%-ной соляной кислоты. В реакторе 10 температура поддерживается .,.- равной 35 - 40 С путем охлаждения его водой, циркулирующей в рубашке 12 этого реактора,
Гидролизованную композицию, полученную в реакторе 10 состоящую из органической фазы, включающей Хлорид трициклогексилолова и дихлоридцикло- гексилолово, и водной фазы, содержащей хлористый магний, вьшускают через боковой слив 13 реактора 10 в сепаратор 14 жидкость жидкость, в кото- осуществляется разделекие двух фаз. Затем кислотную фазу выводят в емкость 15, и органическую фазу подают в пер егонную колонку 16 для концентрирования и ангидризации. Отогнанные растворители выводят из верхней части 16 колонки 16 и подают в сборник, а со дна колонки концентрированный раствор выводят со скоростью 30 л/ч и собирают его в емкости 17.
В реактор 18 (подобный реактору 1 и расположенный ниже по потоку относительно колонны 16) с помощью мер ных насосов 19 и 20 соответственно одновременно подают 30 л/ч концентрированного раствора, полученного в емкости 17, и 5,6 л/ч хлорида циклогексилмагния в растворе тетрагидро5 фурана, соответствующего 1,792 кг/ч при 100% или 0,0125 кмоль/ч.
Температуру в реакционной емкости ггоддерживают равной 40 - 45°С путем циркуляции воды в рубашке 21 реакто0 ра 18.
Композицию выводят через боковой слив 22 реактора 18 и подают в реактор 23, подобный реактору 1, где завершается реакция. В реакторе 23 тем5 пература поддерживается равной 45 - путем циркуляции горячей воды в рубашке 24 этого реактора.
Из бокового слива 25 реактора 23 реак-гионную композицию выводят в сле50 дующий реактор 26, который подобен ргактору 12 и в который одновременно с помощью мерного насоса 27 подают 3,5 л/ч соляной кислоты.
Гидролизованная кo шoзиция, полу55 ченная в реакторе 26, состоит из органичесв:ой фазы, содержаш.ей хлорид
, трицик,по1 ексилолова и кислой водной
фазы, содержащей хлористый магний.
при этом упомянутую композицию выЬо- |дят из бокового слива 28 реактора 26 и подают в сепаратор 29 жидкость - жидкость, в котором осуществляют разделение фаз.
Кислотную фазу сбрасывают в емкость 15, а органическую фазу пропускают через пористую диафрагму 30 в днище колонны 31 диаметр которой, составляет 10 см, а высота 150 см, причем колонна заполнена кольцами Рашига и 15%-ным раствором каустической соды вплоть до верхнего .сливного отверстия. Затем через вход 32 для загрузки в днище колонны 31 одновременно с органическим раствором добавляют 8,15 л/ч 15%-ной NaOH. Температуру в емкости поддерживают равной с помощью горячей воды, циркулирующей по рубашке, кроме того добавляемые реагенты предварительно подогревают.
Верхняя часть колонны 31 сконструирована таким образом, что служит сепаратором жидкость - жидкость, так что раствор органического гидрата окиси трициклогексилолова и водная щелочная фаза выводятся из колонны одновременно, ио отдельно друг от друга. Затем щелочную водную фазу удаляют.
Органическую фазу, собранную в емкости 33, подают с помощью мерного насоса 34 в дистилляционное устройство, состоящее из осуществляющей предварительное концентрирование колонны 35 и дистиллятора 36, где остаточные растворите.гги отгоняются путем перегонки в потоке водяного пара.
После этого гидрат окиси трициклогексилолова фильтруют и сушат. При этом получают кг/ч гидрата окиси трициклогексилолова 96,8% . Производные олова в концентрированном растворе имеют состав, %: Хлорид трициклогексилолова85Дихлорид дициклогексил- олова1,5 Тетрациклогексилолово 0,5 Производные олова в органической фазе после второго гидролиза имеют состав, %:
Хлорид трициклогексил. олова96 , Тетрациклогексилолово О, 5 Дихлорид дициклогексил- олово2,5
Полученный гидрат окиси трицикло- гексилолова 1-теет ацидиметрический титр 96,8%.
Найдено, %: Sn 31,03; С 55,93; Н 8,86; О 4,18.
Вычислено, %: Sn 30,81; С 56,13; Н 8,98; О 4,15.
Выход,расчитанный по тетрахлориду олова, составляет 95% от теоретичес- кого значения.
П р и м е р 2. Периодический процесс..
400 мл безводного толуо.па и 80 г тетрахлорида олова (0,307 моль) загружают в реактор, снабжешгьцг средством для перемешивания, термометром и средством для термосифонного охлаждения. В полученный раствор добавляют 60 мл тетрагидрофурана (0,.7.4 моль-) при ,
Получают комплекс в форме белого кристаллического осадка.
Поддержгшая температуру 38 - 42 С, к этой смеси в течение 30 мин. добав- ляют 411 г раствора хлористого гексилмагния в тетрагидрофуране (131,5 г при 100% или 0,921 моль)(получен путем смешения 650 г тетрагид- рофурака и 290 г хлористого циклогек- силмагния,причем хлористьй циклогек- сил пропускают вверх по течению через термостатную колонну, содержащую стружки магния).
Смесь нагревают при 70°С и выдерживают при этой температуре в тече- ние 30 минут. После охлаждения смеси в нее добавляют 200 мл 5%-ной НС1. Органический слой отделяют от водной фазы. Органическую фазу концент- примерно до половины ее перво- начального объема путем дистилляции.
71 г раствора хлористого цнклогек- силмагния в тетрагидрофуране (22,7 г при 100% рши 0,159 моль) добавляют в этот концентрированный раствор в те- ченне 30 мин при 40 - . Смесь вьщерживают при 40 - 45 С в течение 30 мин. Затем к ней добавляют 50 мл 15%-ной НС1.
Органический слой отделяют от вод- ного. Зачтем в него добавляют 82 г
15%-ной NaOH (0,614 моль). Смесь нагревают до и выдерживают при этой температуре в течение 1ч.
Органический слой отделяют от вод- Ного. Растворители отгоняют в потоке водяного пара. Полученный белый кристаллический продукт отфильтровывают, промывают водой и высушивают.
51 1 I i
Получают 113 г гидроокиси трицик- лофенилолова.
Выход 95,6%. Титр продукта 96%.
П р и м е р Зо Проводят аналогично примеру 2, Но во второй части процесса используют 0,276 моль раствора циклогекснлмагнийхлорида в тетрагид- рофуране, что соответствует 123,3 г.
Получают 114,6 г гидроокиси три- циклогексилолова.
13987 , 6
Выход 97%. Титр продукта 97.
П р и м е р 4. Проводят аналогично примеру 2, но во второй части процесса используют 0,215 моль раствора 5 циклогексилмагнийхлорида в тетрагид- рофуране, что соответствует 96 г.
Получают 114 г гидроокиси трицик- югексилолова, 10 Выход 96,5%. Титр продукта 96%.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ очистки 1-хлор-2,6-динитро-4-(трифторметил)бензола | 1982 |
|
SU1616514A3 |
| КАТАЛИЗАТОР ДЛЯ КОНВЕРСИИ УГЛЕВОДОРОДОВ | 1973 |
|
SU381196A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ОЛОВА (IV) ИЗ СОЛЕЙ ОЛОВА (II) | 2022 |
|
RU2797089C1 |
| Способ получения магнитного порошка для магнитной записи | 1980 |
|
SU1419510A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ТИТАНА | 1996 |
|
RU2102324C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИХЛОРСИЛАНА | 2004 |
|
RU2280010C1 |
| Способ получения катализатора для гидрогенизационной переработки алифатических и ароматических соединений | 1980 |
|
SU1060096A3 |
| Способ получения производных гексагидроазепина или пиперидина, или пирролидина (его варианты) | 1978 |
|
SU1301311A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1,1-ДИФТОРЭТАНА | 1997 |
|
RU2187488C2 |
| Способ получения легированной двуокиси кремния | 1977 |
|
SU698922A1 |
1. Способ получения гидрата окиси трициклогексилолова взаимодейст- .вием циклогексилмагнийхлорида с тет- рахлоридом олова при молярном соотношении 3: 1 в смеси толуола итетрагид- рофурана при 25 - с последующими гидролизом 5%-ным водным раствором соляной кислоты, разделением неорганической и органической фаз, гидролизом 15%-ным водным раствором едкого натра и концентрированием с использованием очистки и выделения целевого продукта, отличающийся тем, что, с целью увеличения выхода и чистоты целевого продукта, после концентрирования к органической фазе повторно добавляют циклогексилмагний- хлорид при молярном соотношении к тетрахлориду олова (3,5 - 3,9):1 соответственно при 40 - 50 С, проводят гидролиз 15%-ным водным раствором соляной кислоты, разделяют неорганическую и органическую фазы, обрабатывают последнюю 15%-ным водным раствором едкого -натра, очищают и выделяют целевой продукт путем перегонки с водяным паром. 2. Способ получения гидрата окиси трициклогексилолова взаимодействием циклогексилмагнийхлорида с тетрахло РИДОМ олова при молярном соотношении 3:1 в смеси толуола и тетрагидрофу-. рана при 25 - 60 С с последующим гидролизом 5%-ным водным раствором соляной кислоты, разделением неорганической EI органической фаз, гидролизом 15%-ным водным раствором едкого натра и концентрированием с использованием очистки и вьщеления целевого продукта, отличаю щ-ийся тем, что, с целью увеличения выхода и чистоты целевого продукта, цикло- гексилмагнийхлорид вводят в реакцию в виде предварительно приготовленного комплекса его с тетрагидрофураном, тетрахлорид олова используют также IB виде предварительно приготовленного комплекса его с тетрагидрофураном, повторно добавляют к органической фазе после концентрирования комплекс циклогексилмагнийхлорида с тетрагвд- рофураном при молярном соотношении с тетрахлоридом олова (3,5 - 3,9):1 соответственно, при 40 - 45 С, гидролизе 15%-ным водным раствором соляной кислоты, разделяют неорганичес-. кую и органическую фазы, обрабатывают последнюю 15%-ным водным раство- ром едкого натра, очищают и выделяют целевой продукт путем перегонки с водяным паром. О) СО ;О эо 
С r
Mrat
| Способ получения концентрированных органических растворов хлорфенолов для фотометрического анализа | 1987 |
|
SU1432047A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1986-02-23—Публикация
1980-06-26—Подача