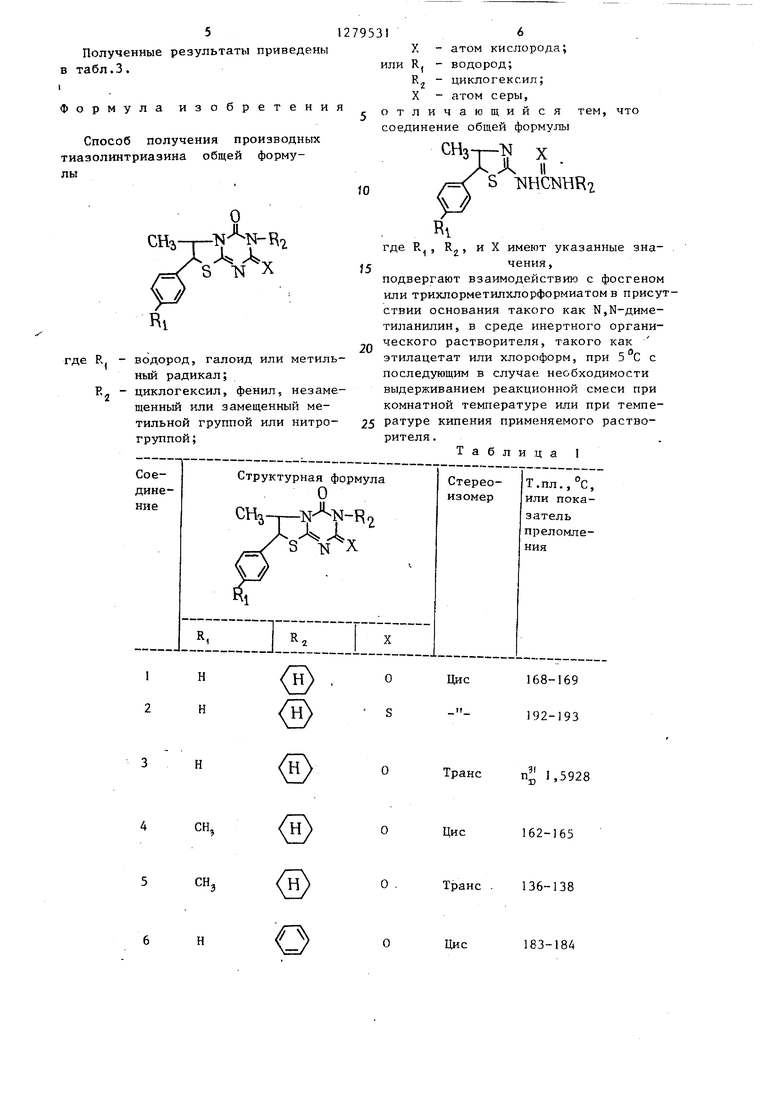
см 1 Изобретение относится к способу получения новых производных тиазолинотриазина общей формулы где R. - водород, галоид или метиль ный радикал; R - циклогексил, фенил, незаме щенный или замещенньш метильной группой или нитрогруппой;X - атом кислорода; или R, водород; R - циклогексил; X - атом серы, обладаюищх фунгицидной активностью. Цель изобретения - получение новых производных тиазолинотриазйна, обладающих фунгицидной активностью. Пример 1. Получение 3-цикло гексил-6-метил-7-фенил-3,4-дигидро2-Н-тиазолино-(3,2-а)-1,3,5-триазин 2,4-диона. 3,4 г 1-(5-фенил-4-метил-Д -тиаз Лин-2-ил)-3-циклогексилмочевины и 2,6 г N„К-диметиланилина растворяют в 70 мл этилацетата и при 5 С при перемешивании добавляют по каплям 10 мл этилацетата, в котором раство рено 1,3 г трихлорметилхлорформиата После перемешивания 1 ч при 5 С полученную реакционную смесь промывают водой, сушат над безводньм сул фатом магния и,отгоняют растворител Полученный остаток перекристаллизовывают из этанола, в результате чег получают 2,8 г целевого продукта с т.пл, 168-169°С. Пример 2. Получение 3-цикло гексил-6-метил-7-(4-метилфенил)-3,4 дигидро-2Н-тиазолино(3,2-а)-1,3,5триазин-2,4-диона. 0,9 г 1-(4-метил-5-)4-метилфенил (& -тиаз олино-2-ил)-3-цикло г ек силмо чевины и 0,6 г Н,Ы-диметиланилина растворяют в 30 мл этилацетата и пр при перемешивании по каплям добавляют 10 мл этилацетата, в которо растворено 0,4 г трихлорметилхлорфо миата. 312 После перемепгавания 1 ч при 5с полученную реакционную смесь промывают водой, сушат над безводньм сульфатом магния и растворитель отгон яют. Затем полученные кристаллы промывают лигроином и в результате получают 0,45 г целевого продукта с т.пл.162165°С. П р и м е р 3. Получение 3-циклогексил-6-метил-7-фенил-3,4-дигидро2Н-тиазолино(3 5 2-а)-J,3,5-триазин2-тиоксо-4-она. 2,0 г 1-(5-фенил-4-метил-Л -тиазолин-2-ил)-3-циклогексилтиомочевины и 1,45 г Ы,К-диаметиланилина растворяют в 80 мл этилацетата и при 5 С при перемешивании по каплям добавляют 10 мл этилацетата, в котором растворено 1,2 г трихлорметилхлорформиата. Через 30 мин перемешивания при указанной температуре; реакционную смесь нагревают с обратным холодильником в течение 3 ч и затем охлаждают до комнатной температуры. Затем реакционную смесь промывают водой и сушат над безводным сульфатом магния, а растворитель отгоняют. Полученньш остаток церекристаллизовывают из метанола и в результате получают 1,0 г целевого продукта с т.пл.192П р И М е р 4. Получение транс-7(п-хлорфенил)-6-мети-З-циклогексил3,4-дигидро-2Н-тиазолино(3,2-а)-1,3, 5-триазин-2,4-диона. 4 г 1-(транс-5)-п-хлорфенил-(4-метил U -тиазолин-2-ил)-3-циклогексилмочевины и 3,3 г N,N-димeтиланилина растворяют в 50 мл этилацетата и затем по каплям добавляют 1,25 г трихлорметилхлорформиата .Полученную смесь выдерживают 30 мин при перемешивании при и еще 30 мин при комнатной температуре. Затем к масляному слою добавляют воду. Масляный слой выделяют, промывают водой и сушат над безводным сульфатом магния, а растворитель удаляют дистилляцией. Полученные в результате кристаллы промывают лигроином и получают 3,5 г целевого продукта с т.пл. 132-134°С. П р и м е р 5. Получение транс-7(п-хлорфенил)-6-метил-З-циклогексил3,4-дигидро-2Н-тиазолино(3,2-а)-1, 3,5-триазин-2,4-диона. 4 г 1- транс 5-(п-хлорфенил)-4метил-& -тиазолин-2-ил1-3-циклогексилмочевины и 3,3 г Ы,Ы-диметиланил на растворяют в 50 мл хлороформа и 1,25 г фосгена вводят в смесь при при перемешивании. Полученную смесь перемешивают 30 мин при 5 С и затем еще 30 мин при комнатной те пературе. Полученную смесь обрабаты вают согласно методике, описанной в примере 4, и в результате получают 3,8 г целевого продукта с т,шт.132134 0. В табл. перечислены типичные со динения, полученные согласно предла гаемому способу. Получение исходного сьфья: транс 6-транс-2-амино-5-(пара-хлорфенил)4-мётил-й -тиазолин. В 180 мл этанола растворяют 2,65 металлического натрия и добавляют к перемешиваемому раствору 27,4 г трео-1-хлор-1-(пара-хлорфенил)-2пропиламингидрохлорида и 8,7 г тиомочевины. После кипячения смеси с обратным холодильником 3 ч реакцион ную смесь охлаждают и выпивают в воду. Ее подщелачивают 10%-ным раствором гидроокиси натрия и экстрагируют хлороформом. Растворитель удаляют и к остатку добавляют смешанный раство ритель бензол-гексан и получают 16,7 г неочищенных кристаллов. Их очищают на хлор-хроматографической. колонке и в результате получают 7,1 г целевого продукта с т.пл. 122-123С. П р и м е р 7. Получение цис-2амино-5-(пара-хлорфенил)-4-метил-Л тиазолина. В 60 мл метилцеллосольва добавляют 10,5 г трео-1-хлор-1-(пара-хлорфенил) -2-пропиламиногидрохлорида и 10,5 г тиоцианата калия и смешанный раствор выдерживают при 5 ч при перемешивании. Смешанный раствор выливают в ледяную воду и экстрагируют этилацетатом. Растворитель отгоняют и остаток промьшают лигроином, в результате чего получают 4,7 г целевого продукта с т.ш1.143145С. П р и м е р 8. Получение 1- транс 5-(пара-хлорфенил)-4-метил-Л -триазо лин-2-ил2 -3-циклогексилмочевины. В 50 мл ТГФ растворяют 5 г транс2-амияо-5-(пара-хпорфенил)-4-метилД -тиазолина и добавляют при перемешивании при к раствору 2,8 г ци„ ., ч. . /Среднее % эффективной защиты -(---Среднееклогексилизоцианата. После того, как реакционную смесь выдерживают при комнатной температуре 30 мин, ее выливают в воду и осевшир кристаллы отфильтровывают и суша;. В результате получают 7,2 г целевого продукта с Т.ПЛ.112-1IB C. Фунгицидное действие предлагаемых соединений иллюстрируются следующими испытаниями. Испытание на контролирование должной мучнистой росы огурцов. 5 мл водной суспензии, содержащей желательное количество каждого соединения, распрыскивали на посаженные в чаще сеянцы огурцов (разновидность Сатсукимидори), находящиеся в стадии 1,5-листника, и каждое обработанное растение супшли на воздухе. Затем инокулировали возбудитель ложной мучнистой росы Pseudoperonospora cubensis и испытуемые растения выдерживали в теплице с тем, чтобы вызвать заболевание. Исследовали внешний вид огуречных растений, зараженных ложной мучнис-той росой, и фитотоксическое действие и эффект регулирования заболевания оценивали в сравнении с состоянием заболевания листвы необработанных огуречных растений. Полученные результаты приведейы в табл.2 . Тест по борьбе с ложной мучнистой росой винограда. Двухлетние лозы винограда (вид Delaware) опрыскивали водным раствором каждого из соединений 3,11 и 18 сентября. После опрыскивания эти лозы были естественно заражены в полевых условиях. Развитие заболевания ложной мучнистой ростой на каждой из лоз оценивали 18 и 28 сентября. Защитное действие каждого из соеинений оценивали следующим образом. оказатель заболе- % пораженных аниялистьев 0О (Здоровы) 211-25 326-50 тепень заболевания (Д.1)-(Каждый оказатель заболевания х Количество аблюдавших листьев) 4 х Количесто наблюдавшихся листьев. Д. 1 у обработанных лоз ,„ S-, )х 100. Д.1 у необработанньпс лоз 12795 Полученные результаты приведены в табл.3. Формула изобретения Способ получения производных тиазолинтриазина общей формулыО Т4 I 1 S -Nf X 15
R. - водород, галоид или метильный радикал;
циклогексил, фенил, незамеR. щенный или замещенный метильной группой или нитрогруппой;
ческого растворителя, такого как этилацетат или хлороформ, при 5 С с последующим в случае необходимости выдерживанием реакционной смеси при комнатной температуре или при темпе25 ратуре кипения применяемого растворителя .
Таблица I 16 X- атом кислорода; или R,- водород; циклогексил; X - атом серы, отличающийся тем, что соединение общей формулы сНз-г-1 X А II S тянтаиКг где R , R, и X имеют указанные зна ™«подвергают взаимодействию с фосгеном или трихлорметилхлорформиатомв присутствии основания такого как N,N-димeтиланилин, в среде инертного органи



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гетероциклических соединений | 1982 |
|
SU1075974A3 |
| Способ получения производных 3-хлор-1-формил-4-фенилпирролов | 1984 |
|
SU1299504A3 |
| Способ получения гетероциклических соединений | 1981 |
|
SU999970A3 |
| Способ получения производных пирролина | 1985 |
|
SU1329618A3 |
| Способ получения производных тиадиазола | 1986 |
|
SU1746884A3 |
| Способ получения производных карбаминовой кислоты | 1974 |
|
SU520912A3 |
| Способ получения производных имидазола или их комплексов с солями металлов | 1978 |
|
SU745364A3 |
| Способ получения производных оксима | 1974 |
|
SU577976A3 |
| Способ получения производных циклогексана или их солей | 1979 |
|
SU884567A3 |
| Способ получения альдегидов | 1983 |
|
SU1225479A3 |
Изобретение относится к производным тиазолинотриазина (I) общей формулы О НзСу- Л- -, (Ri) где R, - И, галоид, метил; Я -циклогексил, фенил, незамещенный или замещенный метильной группой или нитрогруппой; X - О, или R, - Н, Hj - циклогексил; X - S, которые обладают фунгицидной активностью. Для выявления биологической активности синтезированы новые соединения I на основе реакции соединения Ti f (BjPh iS greR, с фосфогеном или трихлорметилхлорформиатом в присутствии основания, такого как Ы,К-диметш1анилин, в среде инертного органического раствориСО теля такого, как этилацетат или хлороформ, при температуре 5с с последующим в случе необходимости выдерживанием реакционной смеси при комнатной температуре или при температуре кипения применяемого растворителя. Вещества кристаллические, ю т.пл.132-297 С, фитотоксичность соединений не обнаружена. 3 табл. ;о 01 со
СН,
СН,
Транс
п 1,5928
Цис
162-165
О Транс . 136-138
Цис
183-184
Шо
Н
8
1279531 Продолжение табл.1
180-182
ГЛ
Таблица 2
1279531О
Продолжение табл.2„
II
Сравнительное
соединение
А
Сравнительное
соединение
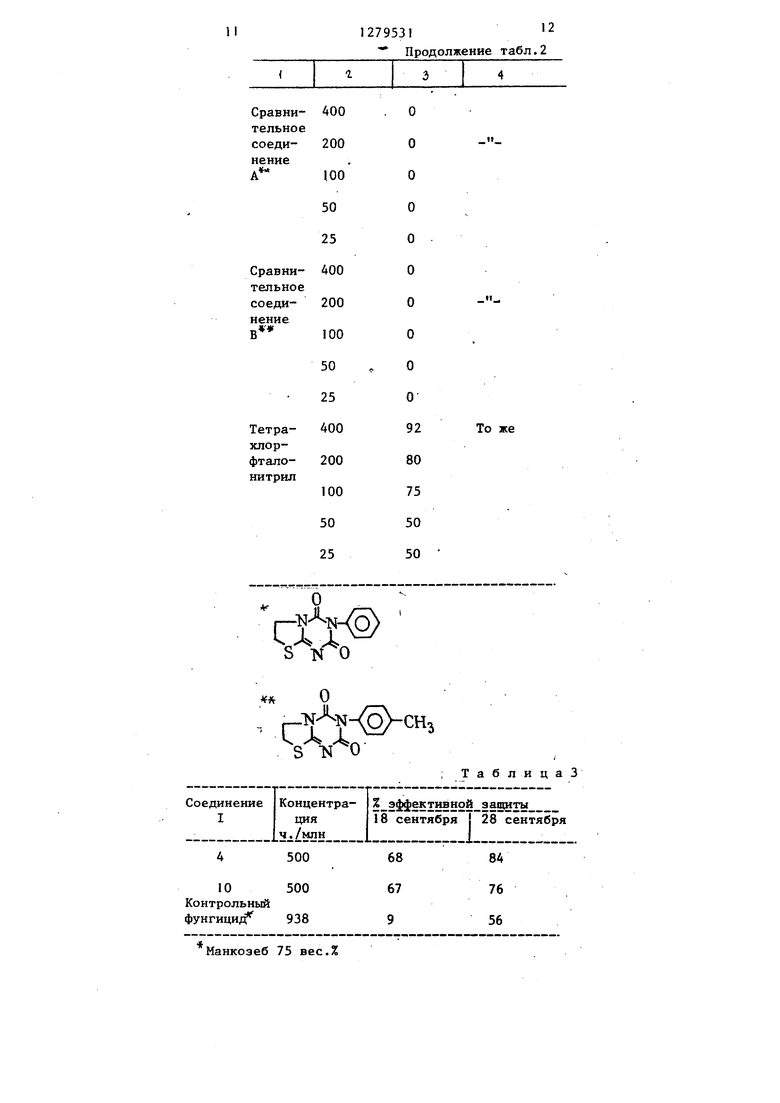
Тетрахлорфталонитрил
12795312
Продолжение табл.2
11
То же
О
r-N-%- 5)-CH3
4Vo
ТаблицаЗ
| Мельников Н.Н | |||
| Химия и технология пестицидов | |||
| - М.: Химия, 1974, с.665, 672 | |||
| Chem.Ber., 1970, 103/11/ 3525-32. |
Авторы
Даты
1986-12-23—Публикация
1983-02-14—Подача