Изобретение относится к новому способу получения новых хлорсодержа- щих альдегидов общей формулы (I)
RZ О Г //
R,OCHa-C-C-H I
RI
где RI R :р - С1;
Кз - CjHy, .Изо-С Н или R -
Rn
Кз CjHf, , н-СуН ,
CjHgCHj,
которые могут быть использованы как полупродукты органического синтеза, в химии полимеров.
Целью изобретения является разработка простого способа получения новых соединений с высоким выходом.
Цель достигается тем, что триме- тилсилан общей формулы (II)
R,
.озиснзЪ н
где R и К , имеют указанные значения,
подвергают взаимодействию с aJ -хлор- эфиром общей формулы (ЦТ) .
78 fA-iS 1,2168 l.-liSA (5)
Цример2, В реакционную колбу с форштосом, снабженную мешалкой,
обратным холодильником, капельной воронкой и термометром, вносят све- жеприготовленньш раствор (0,01 г-моль) хлористого цинка в 12 мл этилацетата.
5
RjOCH Cl,
где Кд имеет указанные значения, в среде органического растворителя в присутствии катализатора - хлористого
j цинка.
Пример 1. Приготовление раствора катализатора - хлористого цинка в этилацетате.
В реакционную колбу с форштосом,
снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, вносят 2 г (0,03 г-атома) измельченного в мелкую стружку цинка и 10 мл этилацетата. Затем туда же по каплям при периодическом перемешивании добавляют смесь 1,5 г (0,01 г- моль) хлораля и 1,1 г (0,01 г-моль) триметилхлорсилана в 2 мл этилацетата. Реакционную смесь подогревают до 40-45 С, после чего реакция протекает самопроизвольно. По окончании прибавления смесь греют при этой же температуре 15 мин, охлаждают до комнатной температуры, сливают с остатков цинка в другую колбу, и получают раствор (0,01 г-моль) хлористого цинка в 12 мл этилацетата. Аналогичным образом получают раствор 0,01 г-моль хлористого цинка в 20 мл эфира.
0 Получают 2,2-дихлор-З-бутокс.ипро- паналь (соединение 4, табл. 1).
Соединения общей формулы 1а приведены в табл. 1.
Таб-лица 1
0
5
9,23 3,99 1743 41,20 .CjHjCl Oj 41,46 9,23 3,97 1743 38,07 ,оС1,0., 38,32
9,22 3,97 1742 38,14 СдМ,, 38,32
затем к нему добавляют сначала раствор 9,3 г (О,П5 г-моль) триметил (В,(Е-дихлорвинилокси)силана в 3 мл этилацетата, а затем медленно по каплям при переметивании, поддерживая температуру 30 с,- раствор 6,7 г
(0,055 г-моль) ot-хлорметилбутилово- го эфира в 5 мл зтилацетата. По окончании реакции смесь перемешивают при 30-35 С в течение 0,5 ч, охлаждают ледяной водой, добавляют 3 мл диок- з сана, 30 мл гексана, отфильтровьгоают от вьтавших солей цинка, отгоняют растворитель в вакууме (водоструйный насос), и продукт-очищают перегонкой в вакууме.
Выход 80% (8,8 г), т. кип. 75-76 С (6 мм рт. ст.), 1,4450.
С1 35,54.
10
df
1,1432, п2
Найдено, %:
Вычислено, %: С1 35,62.
ПМР-спектр (cf, М.Д., СС1):9,25 (Cf°); 3,98 (ОСН); 3,55, 1,48, 0,91
i(). .
ИК-спектр ()), 1745 (С).
ПримерЗ. В реакционную колбу Ьносят раствор (0,01 г-моль) хлорис15
20
9,.1 г (0,05 г-моль) триметил (В,В- -дшслорвинилокси)силана в 3 мл этил- ацетата, а затем медленно по каплям при перемешивании, поддерживая температуру ,- раствор 9,2 г (0,075 г- моль) ({,-хлорметилбутилового эфира в 5 мл этилацетата. Дальнейшие операции проводят аналогично примеру 2. Выход 66% 9,2 г;
Получают 2,2-дихлор-З-этоксипропа- наль (соединение 1, табл. 1).
Пр,им ер 5. В реакционную колбу вносят раствор (0,01 г-моль) хлористого цинка в 12 мл этилацетата, затем к нему добавляют сначала раствор 9,3 г 0,05 г-моль триметил(в,В-дихлор винилокси)силана, а затем медленно по каплям при перемешивании, поддерживая температуру ,- раствор 5,7 г (0,06 г-моль) d -хлорметилэти- лового эфира в 5 мл этилацетата. Дальнейшие операции проводятся аналопгчно примеру 2. Выход 78% (7,3 г), т.-кип.
.44-45 (5 мм рт.ст.), 1,2168,
того цинка в 12 мл этилацетата, затем ,- ,, ,,-,,4
- - nj 1,4434.
-,20
D
Найдено, %: С1 41,20.
CjHgGI Ojo
Вычислено, %: С1 41,46.
ПМР-спектр (,, М.Д., СС1): 9,23
(с/О; 3,99 (осн); 3,61, i,20
к нему добавляют сначала раствор 9,3 г (0,05 г-моль) триметил (В,В-дихлор- -винилокси) сштана в 3 мл этилацетата, а затем медленно, по каплям, при перемешивании-, поддерживая температуру - - раствор 9,8 г (0,08 г-моль) et-хлорметилбутилового эфира в 5 мл этилацетата. Дальнейшие операции проводят аналогично примеру 2. Выход 63% (6,9 г).
Пример 4. В реакционную колбу динения 2 и 3 общей формулы 1а вносят раствор (0,04 г-моль) хлорис- (табл. 1).
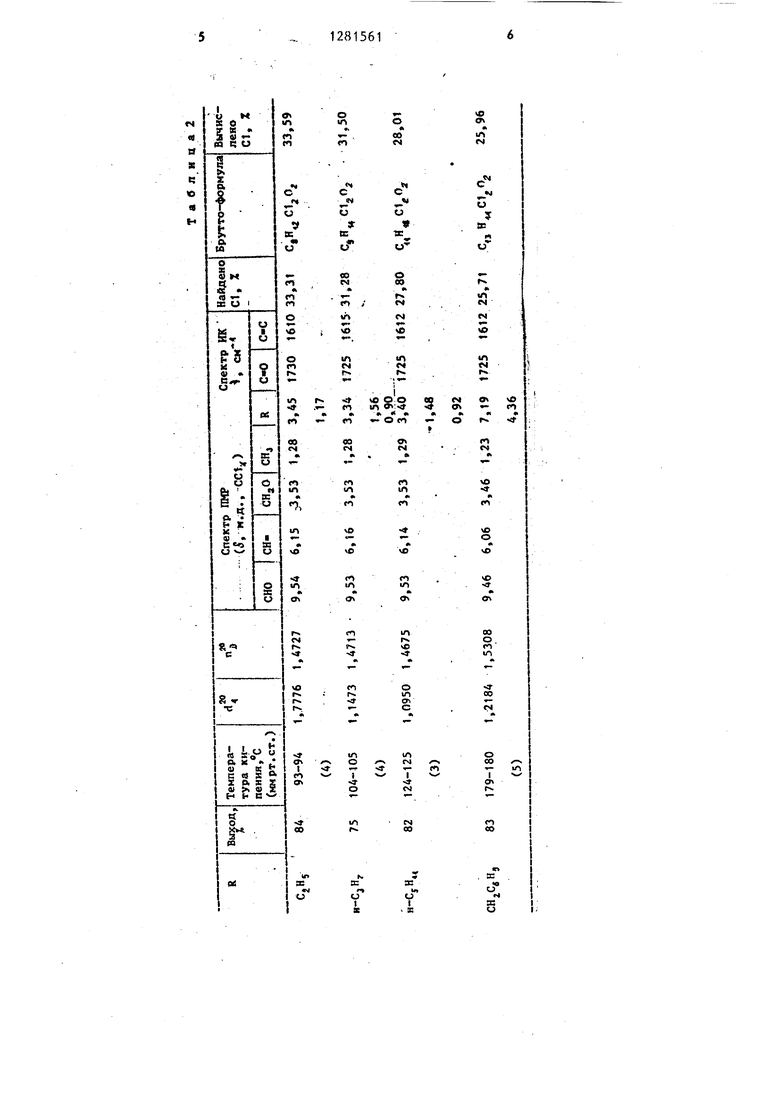
того цинка в 20 мл этгшацетата, затем Соединения общей формулы 16 приве- к нему добавляют сначала раствор дены в табл. 2.
(CpHjO).
ИК-спектр (-), 1743 (c t ). Аналогичным образом получают соез
0
5
0
9,.1 г (0,05 г-моль) триметил (В,В- -дшслорвинилокси)силана в 3 мл этил- ацетата, а затем медленно по каплям при перемешивании, поддерживая температуру ,- раствор 9,2 г (0,075 г- моль) ({,-хлорметилбутилового эфира в 5 мл этилацетата. Дальнейшие операции проводят аналогично примеру 2. Выход 66% 9,2 г;
Получают 2,2-дихлор-З-этоксипропа- наль (соединение 1, табл. 1).
Пр,им ер 5. В реакционную колбу вносят раствор (0,01 г-моль) хлористого цинка в 12 мл этилацетата, затем к нему добавляют сначала раствор 9,3 г 0,05 г-моль триметил(в,В-дихлор- винилокси)силана, а затем медленно по каплям при перемешивании, поддерживая температуру ,- раствор 5,7 г (0,06 г-моль) d -хлорметилэти- лового эфира в 5 мл этилацетата. Дальнейшие операции проводятся аналопгчно примеру 2. Выход 78% (7,3 г), т.-кип.
,,
j
-,20
D
Найдено, %: С1 41,20.
CjHgGI Ojo
Вычислено, %: С1 41,46.
ПМР-спектр (,, М.Д., СС1): 9,23
(с/О; 3,99 (осн); 3,61, i,20
(CpHjO).
ИК-спектр (-), 1743 (c t ). Аналогичным образом получают сое7
П р.и м е р 6. 4,4-Дихлор-2-метил -2-пропоксиметил- З-бутеналь (соединение 2, табл. 2).
В реакционную колбу с форштосом, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, вносят свежеприготовленньй раствор (0,01 г-моль) ZnCl.p в 20 мл этилацетата, затем к нему добавляют сначала 11,3 г (0,05 г-моль) Tpm-ie- тил (4,4-дюслор-2-метил-1,3-бутади- енилокси)силана, а затем медленно по каплям, поддерживая температуру З5 с, раствор 6,5 г (0,06 г-моль) ct-хлор- метилпропилового эфира в 5 мл этил- ацетата. По окончании реакции смесь перемешивают при 30-35 0 в течение
,20
В
0,5 ч, охлаждают ледяной водой, добавляют 3 мл диоксана, 50 мл гексана отфильтровьгеают от вьтавших солей цинка, отгоняют растворитель в вакууме (водоструйный насос) и продукт очищают перегонкой в вакууме. Выход 23% (2,6 г), т. кип, 104-105 е (4 мм рт. ст.), df 1,1473, 1, 4713, ),
ПМР-спектр (f, М.Д., CCI): 9,53 (СНО); 6,16 (СН); 3,53 (); 1,28 (CHj); 3,34; 1,56, 0,90 (ОСзН.).
ИК-спектр (), 1725 (), 1615 ().
Пример. В реакционную колбу с форштосом, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, вносят свежеприготовленный раствор (0,01 г-моль) ZnC.2 в 20 мл эфира, затем к нему добавляют сначала 11,3 г (0,05 г-моль) триметил (4,4-дихлор-2-метил-1,3-бу- тадиенилокси)силана при охлаждении водой со льдом, поддерживая температуру в интервале , раствор 6,5 г (0,06 г-моль) сС-хлорметилпропилово- го эфира в 10 мл эфира. По окончании реакции смесь перемешивают при 5- в течение 0,5 ч, охлаждают ледяной водой, добавляют 3 мл диоксана, 50 мл гексана, отфильтровывают от вьтавших солей цинка, отгоняют растворитель в вакууме водоструйного насоса, и продукт очищают перегонкой в вакууме. Выход 75% (9,2 г).
Аналогичным образом получают соединения 1 и 4 общей формулы 1б (табл. 2).
Пример 8. В реакционную колбу с -форштосом, снабженную мешалкой, обратным холодильником, капельной
воронкой и термометром, вносят свежеприготовленный рсчствор (0,01 г-моль) ZnCl в 20 мл эфира, а затем к нему добавляют сначала 11,3 г (0,05 г- моль) триметил(4,4-дихлор-2-метил-1,3- бутадиенилокси)силана при охлаждении водой со льдом, поддерживая температуру в интервале , раствор 7,5 г (0,055 г-моль) с -хлорметилпентилового эфира в 10 мл эфира. По окончании реакции смесь перемешивают при 5-10 С в течение 0,5 ч, охлаждают ледяной водой, добавляют 3 мл диоксана, 50 мл
гексана, отфильтровьшают от выпавших солей цинка, отгоняют растворитель в вакууме (водоструйный насос) и продукт очищают перегонкой в вакуь ме. Выход 82% (11,4 г), т. кип. 124-1254
(3 мм рт. ст.), df 1,0950, 1,4675, C,,0.
ПМР-спектр (Г, м.д. CCI): 9,53 (СНО); 6,14 (СИ); 3,53 (); 1,29 (CHg); 3,40, 1,48, 093 (.
ИК-спектр (), см: : 1725 (), 1612 ().
Пример9. В реакционную колбу вносят свежеприготовленный раствор (0,01 г-моль) ZnClg в 20 мл эфира, а затем добавляют 0,05 г-моль (11,3 г) трнметил(4,4-дихлор-2-метил-1,3-бу- тадиенилокси)силана при охлаждении водой со льдом, поддерживая температуру в интервале , раствор 10,9 г (0,08 г-моль) ((,-хлорметилпентилового эфира в 10 мл эфира. Дальнейшие операции проводят аналогично примеру 7.
Предлагаемый способ позволяет получить новые соединения с высоким выходом .
Формула изобретения
Способ получения хлорсодержащих альдегидов общей формулы
г ;
(I)
НзОСН2-С-С-Н
R,
где R j R - Cl;
или Rj - С Н, H-CjHy, изо-С,Н-,
R, -
R - GCl, СН-; Ь - СзН
CjHj-CH, заключающийся в том, ан общей формулы
, H-CjH
II
что тринетилси9 128156110
R, DSUCH-J R,OCH,C1 (III)
Г (-гт)
y где R, R и R имеют указанные знаR Пчения,
где R,, R, имеют указанные значения 5в среде органического растворителя в
подвергают взамодействию с (i-хлорэфи-присутствии катализатора - хлористором общей формулыго цинка.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения @ -алкоксиметил- @ -( @ , @ -дихлорвинил)-ацетоуксусного эфира или @ -алкоксиметил- @ -( @ , @ -дихлорвинил)-ацетилацетона | 1984 |
|
SU1198055A1 |
| Способ получения 1-фенил-2,2-дихлор-3-алкоксипропанонов | 1986 |
|
SU1442517A1 |
| Способ получения диалкиловых эфиров 2-(2,2-дихлорвинил)малоновой кислоты | 1987 |
|
SU1549946A1 |
| Способ получения 4,4-дихлор-2-метил-1-ацилокси-1,3-бутадиенов | 1985 |
|
SU1245566A1 |
| Способ получения производных 3,7,11-триметил-2,4-додекадиеновой кислоты | 1981 |
|
SU1069621A3 |
| Способ получения производных карбаминовой кислоты | 1985 |
|
SU1402253A3 |
| Способ получения 1-N-ациламино-1-гидрокси-2-силилциклопропанов | 1985 |
|
SU1365681A1 |
| Способ получения бензил-2,2-диметокси ацетамидов | 1976 |
|
SU663299A3 |
| Способ получения 6 @ - @ (1 @ R),(трет-бутилдиметилсилилокси)этил @ -ангидропенициллина | 1985 |
|
SU1400504A3 |
| Способ получения бис-( @ -диалкиламиноалкил или циклоалкил)дисульфидов | 1988 |
|
SU1608185A1 |
) Изобретение касается галоидзаме- щенных альдегидов, в частности хлор- содержащих альдегидов общей формулы (I) R -0-CH2-C(R)(R2)-C(0)H, где R Kg - Cl; Rj - , изо- -CjH, H-C+Hg или R - CHj; R - CC1 CH-; RJ - этил, н-пропил, н-пентил или СН СН-СН СН-СН С-СН2, которые как полупродукты могут быть использованы, например, в производстве полимеров. Для получения новых соединений указанного класса был разработан новый способ, предусматривающий использование доступного исходного сырья - три- метилсилана обгцей формулы (II) СН-0-51(СНз) J и о(.-хлорэфира общей формулы (III) Rj-n-CHjCl, где R, R, RT указаны выше, в среде органического растворителя в присутствии катализатора - хлористого цинка. Способ позволяет получить соединения формулы (I) с выходом 74-84% и с высокой степенью чистоты, 2 табл. $ л ю 00


| Вартанян С.А | |||
| и др | |||
| Присоединения et-хлорэЛиров к винилацетату | |||
| Изв | |||
| АН АрмССР,, хим., 1965, т, 18, 4, с | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОГО ТАРТАНИЯ | 1915 |
|
SU415A1 |
| Патент CTIA № 2967890, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Судно | 1925 |
|
SU1961A1 |
Авторы
Даты
1987-01-07—Публикация
1985-10-14—Подача