. Изоб1)етение относится к способу получения 2-метилциклопентен-2-она-1, который представляет интерес как по- лупродуУт органического синтеза.
Целью изобретения является поры- шение выхода целевого продукта.
Пример 1. Смесь 4,2 г (0,05 моль) циклопентанона и 6,2 г (0,05 моль) о/-хлорметнлбутилового эфира нагревают в запаянной ампуле, помещенной в термостатированный шкаф, за счет чего и системе создается повышенное давление при в течение 0,5 ч. Перегонкой реакционной смеси собирают фракцию, кипящую при 140- (760 мм рт.ст.), из которой повторной перегонкой выделяют 4,5 г 2-метилциклопентен 2-она-1 (выход
10
15
Пример 4, Аналогично приме ру I процесс проводят с 16,8 г (0,20 моль) циклопентанона и 6,2 г (0,05 моль) о -хлорэфира. Выделяют 13,1 г (93%) 2-метилциклопентен-2- -она-1. Конверсия циклопентанона 94
Пример 5, Аналогично приме ру 1 проводят процесс с 2,5 г (0,03 моль) 1Ц1клопентанона и 6,2 г (0,5 моль) 01 -хларэфира, Выделяют 27 г (93%) 2-метилциклопентен-2- -она-1, Конверсия циклопентанона 100%,
Пример 6, Аналогично приме ру 1 берут 0,8 г (0,01 моль) циклопентанона и 6,2 г (0,05 моль) «/-хло эфира. Выделяют 0,8 г 2-метилцикло- пентен-2-она-1 (выход 89%), Конверси
94Z). Конверсия исходного циклопента- 20 Ци нтанона 100%.
П р и м е р 7, Аналогично примеру 1 процесс проводят с 4,2 г
и -гг Vf f ,
найдено
158-160°С (760 мм рт,ст,);п ь° 1,А751, d
нона 100%, Т.кип,
4° 0,8645, MRj,: 31,38, вычислено 31,27, мол, масса: найдено 96, вычислено 96,12,
Строение синтезированного соединения подтверждают спектральные данные
Спектр ПНР (СС, с/, м,д,) :1 (|
О 3
Метиновая группа при двойной связи (С-3) резонирует в области 6,44 м,д, в виде мультиплета, Метиль- ная группа (С-6) резонирует в виде синглета в области 1,30 м,д,, а ме- тнпеновые группы циклопентанового кольца (С-4-5) - в области 1,26- 1,31 м,д, в виде мультиплета,
Спектр С ЯМР: 198,39 с, (С-1); 184,42 с, (С-2); 147,52 (С-3) I - 149 Гц; 25,81 т, (С-4) 1 129 Гц; 31,78 т, (С-5) I 127 Гц; 13,33 кв, (С-6) I 129 Гц.
Пример2, Аналогично примеру 1 берут 8,4 г (0,1 моль) циклопентанона и 6,2 (0,05 моль) о -хлорме- тилбутилового эфира. Выделяют 8,9 г 2-метилциклопентен-2-она-i (выход 92%), Конверсия исходного циклопентанона 98%,
Пример 3, Аналогично примеру 1 берут 12,6 г (0,15 моль) циклопентанона и 6,2 г (0,05 моль) о -хлор- эЛира, Выделяют 13,0 г (93%) 2-метил- диклопентен-2-она-1, Конверсия циклопентанона 95%,
35
40
(0,05 моль) циклопентанона и 12,4 г (0,1 моль) о -хлорметилбутилоБОго эфи 25 ра. Выход 2-метилциклопентен-2-она4,4 г (92%), Конверсия циклопентяно на 99%.
П р и м е р 8, Аналогично примеру 1 берут 4,2 г (0,05 моль) цикло- 2Q пентанона и 18,6 г (0,15 моль)
эфира. Выделяют 4,5 г 2-метилцикло- .. алкен-2-она-1 (выход 94%), Конверсия циклопентанона 100%,
Пример 9, Аналогично примеру 1 берут 4,2 г (0,05 моль) циклопентанона и 24,8 г (0,20 моль) oi-хло эфира. Выделяют 4,5 г 2-метилциклопе тен-2-она-1 (выход 93%). Конверсия циклопентанона 99%,
Пример 10. Аналогично примеру 1 процесс проводят с 4,2 г (0,5 моль) циклопентанона и 2,8 г (0,03 моль) (/-хлорэфира. Выход 2-ме тилциклопентен-2-она-1 составляет 4,4 г (выход 93%), Конверсия исходного циклопентанона 96%.
Пример 11, Аналогично приме ру 1 берут 4,2 г (0,05 моль) циклопентанона и 1,2 г (0,01 моль) oif-хло метилбутилового эфира. Выделяют 4,3 2-метилпиклоалкен-2-она-1 (выход 90%), Конверсия циклопентанона 93%.
На основании примеров 1-11 видно что оптимальным является соотношени исходных реагентов циклопентанона и ci-хлорметилбутилового эфира 0,03- 0,15 к 0,03-0,20 моль.
Пример 12, Аналогично приме ру 1 процесс проводят при 85 с, По45
50
55
5
Пример 4, Аналогично примеру I процесс проводят с 16,8 г (0,20 моль) циклопентанона и 6,2 г (0,05 моль) о -хлорэфира. Выделяют 13,1 г (93%) 2-метилциклопентен-2- -она-1. Конверсия циклопентанона 941,
Пример 5, Аналогично примеру 1 проводят процесс с 2,5 г (0,03 моль) 1Ц1клопентанона и 6,2 г (0,5 моль) 01 -хларэфира, Выделяют 27 г (93%) 2-метилциклопентен-2- -она-1, Конверсия циклопентанона 100%,
Пример 6, Аналогично примеру 1 берут 0,8 г (0,01 моль) циклопентанона и 6,2 г (0,05 моль) «/-хлор- эфира. Выделяют 0,8 г 2-метилцикло- пентен-2-она-1 (выход 89%), Конверсия
f f ,
35
40
(0,05 моль) циклопентанона и 12,4 г (0,1 моль) о -хлорметилбутилоБОго эфи- 25 ра. Выход 2-метилциклопентен-2-она1 4,4 г (92%), Конверсия циклопентяно- на 99%.
П р и м е р 8, Аналогично примеру 1 берут 4,2 г (0,05 моль) цикло- 2Q пентанона и 18,6 г (0,15 моль) о -хлорэфира. Выделяют 4,5 г 2-метилцикло- .. алкен-2-она-1 (выход 94%), Конверсия циклопентанона 100%,
Пример 9, Аналогично примеру 1 берут 4,2 г (0,05 моль) циклопентанона и 24,8 г (0,20 моль) oi-хлор эфира. Выделяют 4,5 г 2-метилциклопен тен-2-она-1 (выход 93%). Конверсия циклопентанона 99%,
Пример 10. Аналогично примеру 1 процесс проводят с 4,2 г (0,5 моль) циклопентанона и 2,8 г (0,03 моль) (/-хлорэфира. Выход 2-ме- тилциклопентен-2-она-1 составляет 4,4 г (выход 93%), Конверсия исходного циклопентанона 96%.
Пример 11, Аналогично примеру 1 берут 4,2 г (0,05 моль) циклопентанона и 1,2 г (0,01 моль) oif-хлор метилбутилового эфира. Выделяют 4,3 г 2-метилпиклоалкен-2-она-1 (выход 90%), Конверсия циклопентанона 93%.
На основании примеров 1-11 видно, что оптимальным является соотношение исходных реагентов циклопентанона и ci-хлорметилбутилового эфира 0,03- 0,15 к 0,03-0,20 моль.
Пример 12, Аналогично примеру 1 процесс проводят при 85 с, По45
50
55
лучают 4,4 г (93%) 2-метилциклопеи- тен-2-она-1. Конверсия циклопента- ноиа 98%.
Пример 13, Аналогично примеру I процесс проводят при 90°Г,. Получают 4,4 г (92%) 2-метилциклопен- тен-2-она-1. Конверсия циклопента- нона 99%.
Пример 14. Аналогично примеру 1 процесс проводят при . Получают 4,4 г (93%) 2-метилциклопен- тен-2-она-1. Конверсия исходного цик лопентанона 97%.
П р и м е р 15. Аналогично примеру 1 процесс проводят при 70°С. Выделяют 4,3 г (выход 90%) 2-метилцик- лопентен-2-она-1. Конверсия цикло- пентанона 95%.
На основании примеров 1, 12-15 видно, что оптимальная температура проведения реакции 70-90°С.
П р и м е р 16. Аналогично примеру 1 процесс проводят в течение 1,0 ч. Выделяют 4,4 г 2-метилцикло- пентен-2-она-1 (выход 92%). Конверси циклопентанона 100%.
Пример 17, Аналогично примеру 1 процесс проводят в течение 1,5 ч. Выделяют 4,3 г 2-метилцикло- пентен-2-она-1 (выход 90%). Конверсия исходного циклопентанона 99%.
Пример 18, Аналогично примеру 1 процесс проводят в течение 0,25 ч, Вьщеляют 4,3 г (91%) 2-метил циклоцентен-2-она-1, Конверсия исходного циклопентанона 97%.
Пример 19, Аналогично примеру 1 процесс проводят в течение 0,15 ч. Выделяют 4,0 г (86%) 2-метил циклопентен-2-она-1, Конверсия цикло пентаиона 92%,
На основании примеров 1, 16-19 видио, что оптимальная продолжительность проведения реакции 0,5-1,5 ч.
Пример 20, Аналогично примеру I процесс проводят в присутствии 0,3 г (3% от массы смеси) катализатора - катионообменной смолы КУ-2 в Н- форме. Выделяют 4,5 (94%) 2-метил- циклопентен-2-она-1, Конверсия циклопентанона 100%,
Пример 21, Аналогично примеру 1 процесс проводят в присутствии 0,5 г (5% от массы смеси) катализатора КУ-2, Выделяют 4,5 г (94%) 2-мети циклопентен-2-она-1, Конверсия циклопентанона 100%.
II р и м е р 22. А}ТЯЛОГИЧИО примеру 1 процесс проводят в присутствии 0,6 г (7% от общей массы смеси) КУ-2. Виделяют 4,3 г (94%) 2-мстилцикло- пеитен-2-она-1. Конверсия циклопента- иона 100%.
Из примеров 1, 20-22 следует, что катализатор не оказывает влияние на выход 2-метилциклопентен-2-она-1.
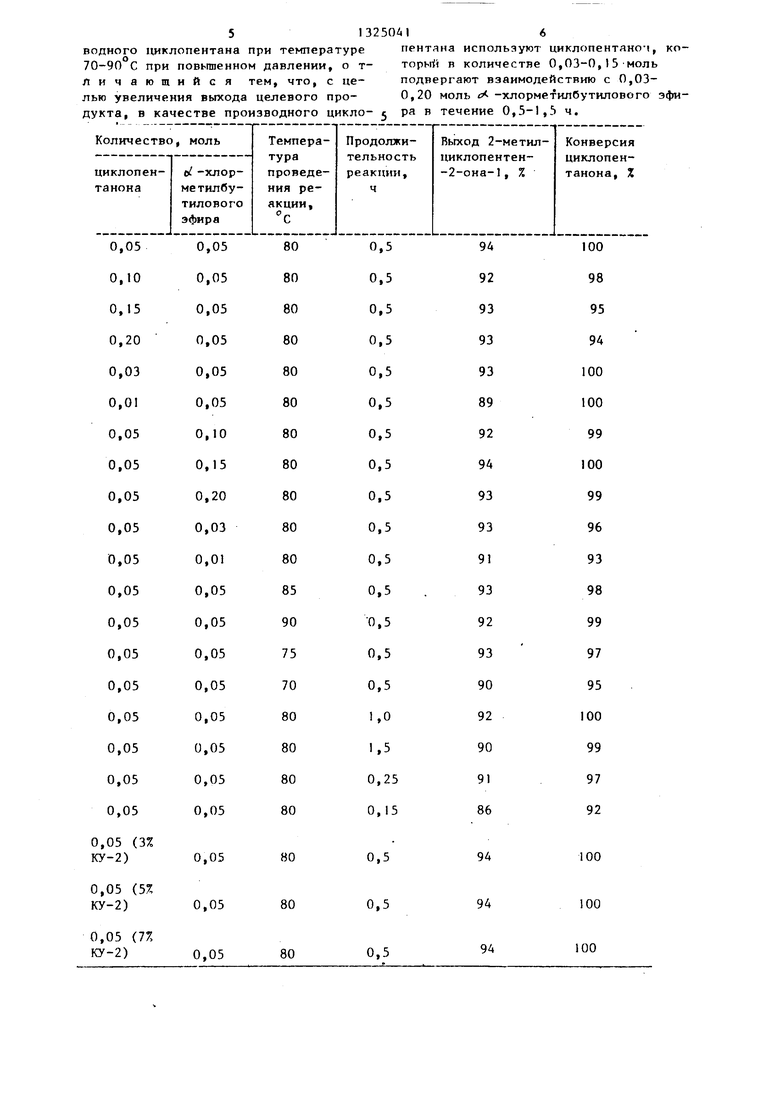
В таблице приведены обобщенные данные по влиянию различных технологических показателей на ход процесса.
g П р и м е р 23, Аналогично примеру 1 процесс проводят при 60°С, Выделяют 3,8 г (85%) 2-метилциклопентен- -2-она-1, Конверсия циклопентанона 90%.
Q П р и м е р 24. Аналогично примеру 1 процесс проводят при 100°С. Выделяют 4,0 г (86%) 2-метилцикло- пентен-2-она-1. Конверсия циклопентанона 1 00%,
5 На основании приведенных примеров 1, 12-14, 23, 24 можно сделать вывод, что оптимальным температурным режимом процесса является интервал 70- 90 С.
Q П Р И М е Р 25. Аналогично примеру 1 берут 4,2 г (0,05 моль) циклопентанона и 31,0 г (0,25 моль) о(-хлор- эфира. Выделяют 4 г (86%) 2-метилцик- лопентен-2-она-1. Конверсия циклопеи- танона 90%,
Из приведенных примеров 1-П, 25 видно, что оптимальным является соотношение циклопентанона и о/ -хлорметил- бутилового эфира 0,03-0,15 к 0,03Q 0,20 моль.
Из таблицы следует, что высокий выход 2-метилциклопентен-2-она-1 (до 92-94%) может быть получен при взаимодействии 0,03-0,15 моль циклопентанона с 0,03-0,20 моль о/-хлорметил- бутнлового эфира в течение 0,5-1,5 ч при 70-90°С.
Использование предлагаемого способа позволяет увеличить выход 2-ме- тилциклопентен-2-она-1 с 75 в известном способе до 92-94%, т.е. на 17- 19%, сократить время реакции с 5,0 до 0,5-1,5 ч, т.е. на 4,5-4,0 ч, отказаться от использования катализатора.
5
0
5
Формула изобретения
Способ получения 2-метилциклопен- тен-2-она-1 с использованием произ513250Д16
водного циклопентана при температуре пентяна используют циклопентаноч, ко- 70-90°С при повьппенном давлеиии, о т- Topbrti в количестве 0,03-0,15 моль Личающийся тем, что, с це- подвергают взаимодействию с 0,03- лью увеличения выхода целевого про- 0,20 моль -хлорметилбутилового эфи- дукта, в качестве производного цикле- ра в течение 0,5-1,3 ч.
0,05 0,10 0,15 0,20 0,03 0,01 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05 0,05
,05 (3% У-2)
,05 (5% У-2)
,05 (7% У-2)
0,05
0,05
0,05
0,05
0,05
0,05
0,10
0,15
0,20
0,03
0,01
0,05
0,05
0,05
0,05
0,05
0,05
0,05
0,05
0,05 0,05 0,05
80 80 80 80 80 80 80 80 80 80 80 85 90 75 70 80 80 80 80
80 80 80
94
92
93
93
93
89
92
94
93
93
91
93
92
93
90
92
90
91
86
94 94 94
100 98 95 94
100
100 99
100 99 96 93 98 99 97 95
100 99 97 92
100
100 100

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3-метилциклопентена | 1979 |
|
SU910571A1 |
| Способ получения (2-хлорэтил) ацетата | 1985 |
|
SU1286591A1 |
| Способ получения циклогексадиена-1,3 или метилциклогексадиенов-1,3 | 1983 |
|
SU1133253A1 |
| Способ получения замещенных эфиров хризантемовой кислоты | 1971 |
|
SU437273A1 |
| Способ получения непредельных алкил-зАМЕщЕННыХ циКличЕСКиХ KETOHOB | 1979 |
|
SU833943A1 |
| Способ получения циклопентена и метилциклопентена | 1975 |
|
SU591446A1 |
| Способ получения 2-/6-карбметокси (этокси)-гексил/-циклопентен2-она-1 | 1978 |
|
SU789510A1 |
| Способ получения диалкиловых эфиров метилциклопентилфосфоновой кислоты | 1984 |
|
SU1268589A1 |
| Способ получения 2-(6-карбалкоксигек-Сил) циКлОпЕНТЕН-2-OHOB-1 | 1978 |
|
SU806672A1 |
| Способ получения 1,1-дикарбалкокси-2-экзометилен-3-циклопентенов | 1980 |
|
SU925934A1 |
Изобретение относится к гетероциклическим соединениям, в частности к получению 2-метилциклопентен-2- -она-1 (МП), который является полупродуктом органического синтеза. Повышение выхода МЦ достигается использованием другого исходного реагента. Синтез МП ведут из 1шклопентанона 

Авторы
Даты
1987-07-23—Публикация
1985-12-03—Подача