(CHjS) с
5 табл.
С - С (О) - S - .
г
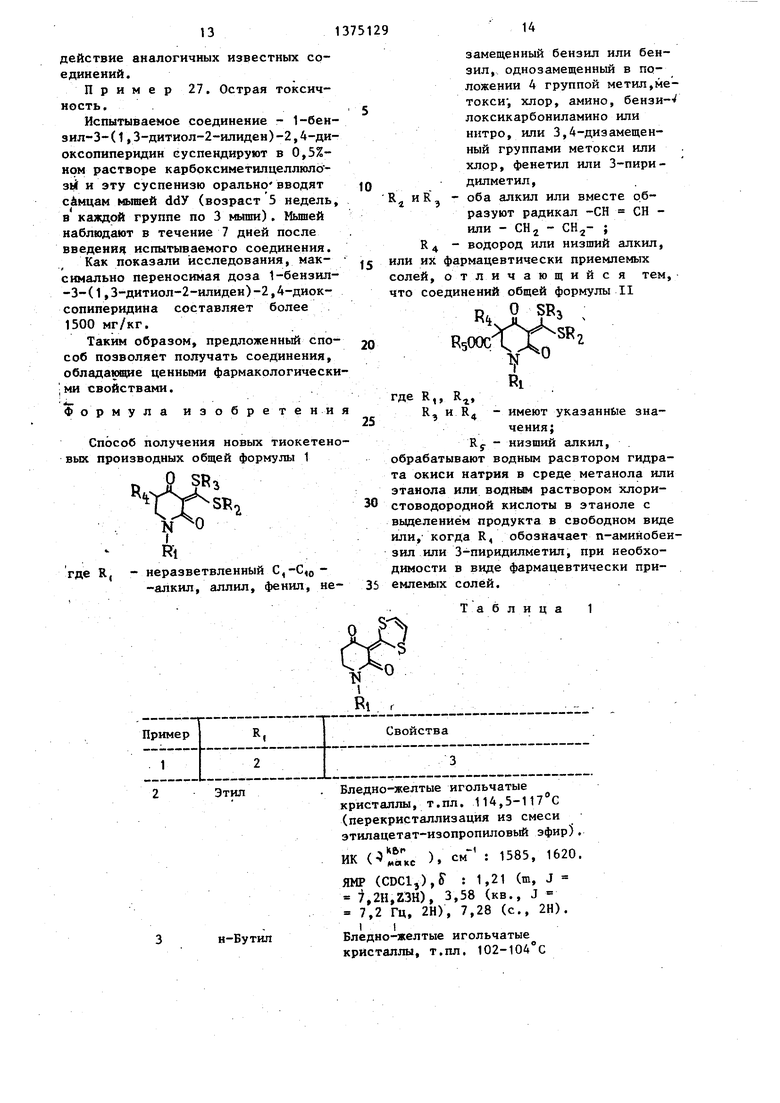
Изобретение относится к области химии гетероциклических соединений, в частности к способу получения новых тиокетеновых производных общей формулы 1
О SRy
ipo
Ri
где R, - неразветвленный С4-С, кил, аллил, фенил, незамещенный бензил или бензил, однозамещенный в положении А группой метил, метокси, хлор, амино, бензилоксикарбонилами- но или нитро или 3,4-дизамещенный группами метокси или хлор, фенетил или 3-пиридилметил,
R
и R, оба низший алкил или
вместе образуют радикал -СН СН - или - СНг - ,
R - водород или низший алкил, или их фармацевтически приемлемых солей, которые могут быть использованы в качестве терапевтических и профилактических средств при заболеваниях печени.
Целью изобретения является создание на основе известных методов способа получения новых соединений общей формулы I, обладающих ценными фармакологическими свойствами. П р и м е р 1.
1. Смесь 43,24 г бензиламина и 300 мл хлористого метилена охлаждают смесью воды со льдом и добавляют в нее по каплям раствор 29,63 г этокси карбонилацетилхлорида в 150 мл хлористого метилена. Эту смесь перемеши вают при -той же температуре в течение 2 ч, затем фильтруют для удаления осадка (бензиламингидрохлорида) Фильтрат промывают 2%-ной соляной кислотой и насыщенным раствором хлористого натрия, сушат и выпаривают для удаления растворителя. Остаток перекристаллизовывают из смеси ди- этилового эфира с н-гексаном, в результате чего в виде бесцветных игольчатых кристаллов получают 42,15 этИл(К-бензилкарбамоил)ацетата. Выход 96,8%, т.пл. 50-52 с.
ИК-спектр (;j;t, ;c ),см : 1735, 1650.
ЯМР-спектр (CDC1,)S : 3, 34 (с., 2Н, - COgHiCO-), 4,47 (д., ,7 Гц
2Н,
N-CHo
10
15
20
25
30
35
40
45
50
55
Масс-спектр (т/1) : 221 () .
2.39.00 г этил(К-бензилкарба- моил)ацетата и 14,03 г сероводорода растворяют в 390 мл диметилсульфокси- да. В этот раствор добавляют по каплям при 20-40 С раствор 21,52 г гидрата окиси калия в 39 мл воды. Смесь перемешивают при той же температуре
в течение 30 мин, а затем по каплям в нее добавляют 17,84 г цис-1,2-ди- хлорэтилена. Конечную смесь перемешивают при 50°С в течение 5 ч. Далее спустя 3 ч после начала реакции в реакционную смесь добавляют 3,24 г цис-1,2-дихлорэтилена. После охлаждения смесь выливают в воду и водный раствор подвергают экстракционной обработке этилацетатом. Экстракт промывают водой, сушат, а затем выпаривают для удаления растворителя. Остаток очищают в хроматографической колонке с силикагелемс использованием в качестве элюента смеси н-гексана с этилацетатом в соотношении 2:2, после чего перекристаллизовывают из смеси н-гексана с этилацетатом, получая в виде бледно-желтых призматических кристаллов 33,77 г этил-2-(1,3- -дитиол-2-илиден)-2(К-бензилкарбамо- ил)ацетата. Выход 62,8%, т;пл. 78,5 - 80,5°С.
ИК-спёктр ( 9 J j.p ) 1600.
ЯМР-спектр (CDC1 )S
S-.-H 2Н, ЦТ
Масс-спектр (т/1) : 321 (М). .
3.60%-ную дисперсию 1,50 г гидрида натрия в масле суспендируют в
100 мл К,Кгдиметилформамида и добавляют в нее по каплям при раствор 10,0 г этил-2-(1,3-дитиdл-2-или- дeн)-2-(N-бeнзилкapбaмoил)aцeтaтa в 250 мл диметилформамида. Далее смесь перемешивают при той же температуре в течение 30 мин. В эту смесь по каплям добавляют затем раствор 4,1 мл этилакрилата в 100 мл диметилформамида и конечную смесь перемешивают при той же температуре в течение 1 ч и при комнатной температуре в течение 5 ч. Смесь выливают в смесь воды со льдом и водный раствор подвергают экстракционной обработке этил- ацетатом. Экстракт промывают водой, сушат и затем вып аривают для удаления растворителя. Остаток перекрис -iсм
1665, 7,07 (с..
таллизовывают из смеси н-гексана с этилацетатом, в результате чего получают 8,76 г этил-1-бензил-5-(1,3- дитиол-2-илиден)-4,6-диоксопипери- дин-3-карбоксилата в виде бледно- желтых игольчатых кристаллов, выход 75%, т.пл. 127-129 С.
ИК-спектр ( ), : 1730, 1630, 1595,
ЯМР-спектр (СВСЦ) S : 4,83 (д., J 15 Гц, 1Н, -СН -бензол), 4,63 (д., J 15 Гц, 1Н, N - CHi-бензол) (с., 2Н, H-r-S )
н
Масс-спектр (т/1) : 375 (М).
4. 2,0 г этил-1-бензил-5-(1,3-ди- тиол-2-илиден)-4,6-диоксипиперидин- -3-карбоксилата растворяют в 160 мл этанола и добавляют в раствор 8,0 мл 10%-ного водного раствора гидрата окиси натрия. Смесь кипятят с обратным холодильником в течение 2 ч, затем охлаждают, нейтрализуют добавлением 10%-Hofl соляной кислоты и выпаривают под пониженным давлением для удаления растворителя. Остаток растворяют в этилацетате, раствор промывают водой, сушат, а затем выпаривают для удаления растворителя. Полученный остаток перекристаллизо- вывают из изопропанола,в результате чего в виде бледно-желтых игольчатых кристаллов получают 1,26 г 1-бензил- -3-(1,3-дитиол-2-илиден)2,4-диоксо- пиперидина, выход 78%, т.пл. 123 124 с
, ХлоРочрорм .
ИК-спектр ( ддо,« ), см : 1630, 1590.
ЯМР-спектр (CDC1,)S :
(с., 2Н, -СН -бензол),7,29 (с.,
S-pH 8Н, / , бензольное кольS- -H
цо) .
Масс-спектр (т/1): 303 (М).
Примеры 2-20. Аналогично примеру 1 получают соединения, приведенные в Табл.1 и 2.
Пример 21.
1, 60%-ную дисперсию 175 мг гидрида натрия в масле суспендируют в 10 мл диметилформамида и в суспензию добавляют по каплям раствор 1,3 г эт.ил-1-бензил-5( 1,3-дитиол- -2-илиден)-4,6-диоксопиперидин-З- -карбоксилата в 30 мл диметилформамида при одновременном охлаждении
0
5
0
5
0
0
5
0
5
), : 1725,
льдом. Смесь перемешивают при комипт- ной температуре в течение 20 мин, затем в нее добавляют 0,27 мл иоди- стого метила и перемешивают с одновременным охлаждением льдом в течение 1,5 ч, а затем при комнатной температуре в течение 1,5 ч. Смесь выливают в воду и подвергают экстракционной обработке этилацетатом. Экстракт промывают насыщенным раство- рЪм хлористого натрия,сушат,а затем отгоняют растворитель.Остаток пере- кристаплизовывают из смеси этилацета- тас н-гексаном,в результате чего в виде бледно-желтых игольчатых кристаллов получают f,15r (выход85,2%) этил- -1-бензил-5-(1,3-дитиол-2-илиден)- -З-метил-4,6-диоксопиперидин-З-кар- боксилата, т.пл. 111-113°С.
ИК-спектр ( J 1625, 1595.
ЯМР-спектр (CDC1 ),S : 1,39 (с., ЗН).
2. 245 мг этил-1-бензил-5-(1,3- -дитиол-2-илиден)-З-метил-4,6-диок- сопиперидин-3-карбоксилата растворяют в 5 мл этанола и в этот раствор добавляют 2,5 мл 10%-ного раствора гидрата окиси натрия. Смесь перемешивают при комнатной температуре в течение ночи, затем подкисляют 10%-ной соляной кислотой и выпивают в воду. Водный раствор подвергают экстракционной обработке этилацетатом. Экстракт промывают насьш1енным раствором хлористого натрия, сушат, а затем отгоняют растворитель. Остаток растворяют в 20 мл этанола и раствор кипятят с обратным холодильником в течение 1 ч. Затем смесь перегоняют для удаления растворителя. Остаток очищают в хроматографической колонке с силикагелем с использованием в качестве растворителя смеси этилацетата с н-гексаном в соотношении 1:1 и перецристаллизовывают из смеси этилацетата с н-гексаном, в результате чего в виде бледно-желтых игольчатых кристаллов получают 138 мг (выход 69,1%) 1-бензил-З- -(1,3-дитиол-2-илиден)-5-метил-2,А- -диоксопиперидина, т.пл. 168-170°С.
ИК-спектр (11акс. см- : 1625, 1585.
ЯМР-спектр (CDC1,),S : 1,18 (д., J 6,4 Гц, ЗН), 4,76 (д., J 15 Гц, 1Н), 4,81 (д., J 15 Гц, 1Н), 7,35 (с., 7Н).
П р и м е р 22.
1.2,70 г этил-1-бензил-5-(.1,3- дитиол-2-илиден)-4,6-диокс6пипери- дин-3-карбоксилата и 0,71 мл йодистого этила обрабатывают аналогично примеру 21.1, в результате чего в виде бледно-желтого маслоподобного продукта получают 2,30 г (выход 79,3%) этил-1-бенэил-5-(1,3-дитиол- -2-илиден)-3-этил-4,6-диоксопипёри- дин-3-карбоксилата.
ИК-спектр ( ), см- : 1725, 1625, 1595.
ЯМР-спектр (CDC1,),S : 0,89 (т., J 7,3 Гц, .ЗН).
2.170 мг этил-1-бензил-5-(1,3- -дитиол-2-илиден)-З-этил-4,6-диоксо- пиперидин-3-карбоксилата обрабатывают аналогично примеру 21.2,в результате чего в виде бледно-желтых игольчатых кристаллов получают 455 мг (выход 78%) 1-бензил-3-(1,3-дитиол- -2-илиден)-5-этил-2,4-диоксопипериди на, т.пл. 139,5-141 С.
ИК-спектр ( ). : 1625, 1590.
ЯМР-спектр (CDC1,),S : 0,83 (т., J « 7,2 Гц, ЗН), 4,69 (д., J 15 Гц 1Н), 4,81 (д., J 15 Гц, 1Н), 7,28 (с., 2Н).
Пример 23.
1.10,81 г 3-пиридилметиламина растворяют в 50 мл метанола и в раствор по каплям добавляют 8,60 г метил акрилата при охлазвдении льдом. Эту смесь перемешивают при комнатной температуре в течение 18 ч, затем перегоняют для удаления растворителя. Полученный остаток перегоняют под пониженным давлением с получением 16,02-г (выход 82,5%) метил-3- -(З-пиридилметиламино)пропионата,
с т.кип. 119-120. С при остаточном давлении 0,3 мм рт.ст.
2.Смесь 28,72 г метил-3-(3-пири- дилметиламино) пропионата с 22 мл тризтиламина и 240 мл хлористого метилена охлаждают до и добавляют в нее по каплям раствор 23,38 г этоксикарбонилацетилхлорида в 60 мл хлористого метилена. Смесь перемешивают при комнатной температуре в течение 1 ч, затем ее фильтруют для удаления осадка - тризтиламингидро- хлорида. Фильтрат промывают водой, сушат и затем перегоняют для .удаления растворителя. Остаток очищают в хроматографической колонке с силика
5
0
5
0
5
0
5
0
5
гелем с использованием в качестве растворителя этилацетата, в результате чего в виде маслоподобного продукта получают 35,22 г (выход 77,3%) этил-N-(3-пиридилметил)(метилок- сикарбонилзтил) карбамоил ацетата.
ИК-спектр ( ). см- : 1730, 1645.
Масс-спектр (т/1) : 308 (М).
3. 1,0 г этил-N-(3-пиридилметил)- -LN-(метоксикарбонилэтил) карбамо- ил ацетата и 0,2 мл сероуглерода растворяют в 12 мл диметилсульфокси- да, после чего в раствор добавляют раствор 378 мг гидрата окиси калия в 1 МП воды. Смесь перемешивают при комнатной температуре в течение
20 мин. Раствор 0,245 мл цис-1,2- дихлорэтилена в 2 мл диметилсульфок- сида по каплям добавляют в смесь, которую далее перемешивают при 50-55 С в течение 6 ч. После охлаждения смесь выливают в воду и водный слой подвергают экстракционной обработке этилацетатом. Экстракт промывают во дои, сушат, а затем перегоняют для удаления растворителя. Остаток очищают в хроматографкческой колонке с силикагелем с использованием в качестве растворителя зтилацетата, в результате чего в виде маслоподобного продукта получают 429 мг зтил-2- -(1,3-дктиол-2-ш1иден)(3-пиридилметил) -Ы-(метоксикарбонилзтш1)
карбамоилТ ацетата.
,,.,/л жидкость ч-(
ИК-спектр (V ), см :
1730, 1655, 1620.
Масс-спектр (т/1) : 408 (М).
4. 156 мг натрия добавляют в 5 мг метанола и в эту смесь вводят раствор 2,21 г зтил-2-(1,3-дитиол-2-или- ден)-2- N-(3-пиридилметил)-Я-(ме- токсикарбонилэтил) карбамоил ацетата в 35 мл бензола. Смесь кипятят с обратным холодильником в течение 3 ч и перегоняют для удаления растворителя. Остаток растворяют в этил- ацетате и раствор промывают водой, сушат, а затем перегоняют для удаления растворителя. Остаток перекрис- таллизовывают из смеси этилацетата с н-гексаном, в результате чего в виде бледно-желтых игольчатых кристаллов получают 1,0 г (выход 51%) метил- -1-(3-пиридилметил)-5-(1,3-дитиол- -2-илиден)-4,6-диоксопиперидин-З- -карбоксилата, т;.пл. 111-114 с.
ИК-спектр (;)в«еликоме масло
).
макс
: 1740, 1620, 1585.
ЯМР-спектр (CDC1),S : 3,69 (с. ЗН), 4,76 (с., 2Н), 7,39 (с., 2Н).
Полученное соединение обрабатываю смесью соляной кислоты с диэтиловым эфиром, в результате чего в виде желтых игольчатых кристаллов получают соответствующий гидрохлорид, т.пл 204-205,5°С (после перектисталлиза- ции из метанола).
5. 244 мл метил-1-(3-пиридилме- тил)-5-(1,3-дитиол-2-илиден)-4,6- -диоксопиперидин-3-карбоксилата, по- лученного аналогично примеру 27,растворяют в 15 мл метанола и в раствор добавляют 2 мл 10%-ного раствора гидрата окиси натрия. Затем смесь кипятят с обратным холодильником в те- чение 2ч, выливают в воду и подвергают экстракционной обработке хлороформом. Экстракт промывают водой, сушат и затем перегоняют для удаления растворителя. Остаток перекри- сталлизовывают из смеси этилацетата с н-гексаном, в результате чего в виде желтых пластинчатых кристаллов получают 114 мг (выход 66,1%) 1-(3- -пиридилметил)-3-(1,З-дитиол-2-или- ден)2,4-диоксопиперидин, т.пл. 131,5 133-0.
ИК-спектр ( , ). : 1620, 1590.
ЯМР-спектр (CDC1 ),S : 4,75 (с. 2Н), 7,31 (с., 2Н).
Полученное соединение обрабат1 ва- ют соляной кислотой и диэтиловым эфиром, в результате чего в виде бледно-желтых игольчатых кристаллов получают соответствующий гидрохлорид, т.пл. 243,5°С (с разложением, после перекристаллизации из метанола).
Пример 24. Смесь зтил-1- -бензип-5-(1,3-дитиол-2-илиден)-3- -метил-4,6-диоксипиперидин-З-карбок- силата (650 мг), этанола (15 мл) и 10%-ной НС1 (7,5 мл) кипятят с обратным холодильником в течение 6 ч и перегоняют для удаления растворитет- ля. Остаток растворяют в этилацетате полученный раствор промывают водой, сушат, а затем перегоняют для удаления растворителя. Остаток перекри- сталлизовывают из смеси этилацетата. и н-гексана. Получают 1-бензил-З- -(1,З-дитиол-2-илиден)-5-метил-2,4- -диоксопиперидин (323 мг, 61%) в виде желтых иголок, т.пл. 168-170 С.
,
т .Ю
)5 2025-
, 5
, 55
30
40
45
50
Пример 25. Смесь этил-1- -бензил-5-(1,4-дитиол-2-илиден)4,6- -диоксопиперидин-3-карбоксилата (2,0 г), этанола (160 мл) и 10%-ной НС1 (80 мл) кипятят с обратным холодильником в течение 8 ч После этого смесь обрабатывают аналогично примеру 24,в результате чего получают 1-бензил-3-(1,3-дитиол-2-илиден)- -2,4-диоксопиперидин (1,12 г,69,4%) в виде бледно-желтых иголок, т.пл. 123-124°С (перекристаллизован из изопропанола).
Печень является органом, который выполняет различные фнукции, в частности обезвреживания ядов, углеводного, липидного и белкового обмена, продуцирования и секреции желчи, продуцирования, факторов свертывания крови, контроля гормонов, регенерирования клеток печени, накопления элементов строения живого организма (например, жиров, гликогена, белков, витаминов) . Эти функции подвергаются острым или хроническим расстройствам по различным причинам, например под действием вирусов, лекарств, ядов, спиртов, вследствие недостаточного питания, сосудистой дисфункции печени, закупорки желчного протока. Расстройства функции печени клиниче- ски проявляются, например, в форме вирусных гепатитов,вызванной лекарствами гепатопатии,алкогольных гепатитов, гиперемических гепатитов, печеночных заболеваний, вызванных застоем желчи, ожирения печени, желтухи, цирроза печени.
Существует множество различных известных причинных факторов, которые вызывают токсическое повреждение печени, гепатиты и ожирение печени. Превалирукмцими изменениями, которые наблюдаются при таких заболеваниях, являются некроз клеток печени, ме- зенхимальная реакция и накопление липида. Некроз зависит от причинного фактора и может быть классифицирован как центродольчатый, перипор- тальный и дискретно-дольчатый. При проведений экспериментов центродольчатый некроз вызывают четыреххлори- стым углеродом и степень повреждения печени определяют измерением веса печени и визуально (по цвету). Пе- рипортальный некроз и дискретно-дольчатый некроз, связанные с мезенхи- мальной реакцией, вызывают соответственно аллиловым спиртом и D-галак- тозамином, а степень повреждения печени определяют по изменению активности глутаминопировиноградной транс аминазы (ГПТ) и глутаминощавелево- уксусной трансминазы (ГЩТ) в плазме крови..
Предлагаемые соединения или их соли проявляют сильное действие в OT ношении профилактики и ослабления различных заболеваний печени, в особенности, связанных с центродольчаты перипортальным и дискретнодольчатым некрозом и мезенхимальной реакцией, ожирением печени, вызванной лекарствами гепатопатией и застойными гепатитами и могут быть использованы в качестве терапевтических или профилактических агентов при гепатитных заболеваниях у животных, включая человека, например, для лечения или профилактики различных заболеваний, в частности вирусных гепатитов, ге- патопатии, вызванной лекарствами, ал когольных гепатитов, ожирения печени, желтухи, а также конечного симптома, т.е. гепатоцирроза. Кроме того, предлагаемые соединения проявляют также способность стимулировать ; функцию печени при низкой токсичности и,, следовательно, высокой безопасности. Например, при пероральном введении мышам 1-бензил-3-(1,2-ди- тиол-2-илиден)-2,4-диоксопиперидина в дозировке 1500 мг/кг в течение 7 дней наблюдений после этого не погибает ни одно животное.
При использовании в качестве ле
карственных препаратов предлагаемых
соединений или их солей их можно вводить в организм перорально или парентерально, например, подкожно, внутримышечно или внутривенно. Дозировку этих соединений можно изменять в зависимости от возраста, пола, веса и состояния пациента, от метода введения в организм, серьезности заболевания и т.п, однако обычно доза составляет примерно 0,01-250 мг/кг/ /день, предпочтительнее от 0,1 до 50 мг/кг/день.
Предлагаемые соединения или их соли можно использовать в составе обычных фармацевтических препаратов в смеси. Например, с такими наполнителями или разбавителями, как желатин, лактоза, глюкоза, хлористый натрий, крахмалы,стеарат магния,тальк,рас
0 5 Q
5
0
5
с
тительные масла. Фармацевтические препараты могут представлять собой твердые продукты, в частности таблетки, покрытые сахаром, капсулы, пилюли или поршки, или жидкости, в частности растворы, суспензии или эмульсии. Такие препараты могут быть стерилизованы. Кроме того, в эти препараты могут быть добавлены различные вспомогательные добавки, стабилизаторы, смачивающие агенты, эмульгаторы и т.п.
Испытания на биологическую активность предлагаемых соединений.
Пример 26. Защита от острого гепатитного повреждения, вызываемого действиями четыреххлористого углерода.
Испытываемые соединения суспендируют в 0,5%-ном растворе карбокси- метилцеллюлозы и полученную суспензию с содержанием испытываемого соединения 100 мг/10 мл/кг через рот вводят самцам мышей разновидности ddy (возраст 5-6 недель, вес. 25 - 30 г, в каждой группе по 3 особи), после чего животным не дают корма. По истечении 3 ч животным через рот вводят раствор четыреххлористого углерода в оливковом масле (50 мкг/ /5 мл масла/кг). По истечении 3 ч через рот животным вводят испытываемое соединений в такой же дозировке. Вес животных измеряют через 24 ч после введения четыреххлористого углерода, после чего животных убивают. Сразу же после этого у них удаляют печень, взвешивают ее и подвергают макроскопическому исследованию.
Животным контрольной группы (нормальной) вместо суспензии испытываемого соединения и раствора четырех- хлористого углерода вводят 0,5%-ный раствор карбоксиметилцеллюлозы и оливковое масло (перорально). Кроме того, исследуют контрольную группу животных, которым вводят раствор четыреххлористого углерода и 0,5%-ный раствор карбоксиметилцеллюлозы.
Терапевтическое действие испытываемых соединений на эффект повреждения печени оценивают как степень подавления в процентах увеличения относительного веса печени, рассчитанную с помощью нижеследующего
уравнения. Термин относительный вес печени обозначает вес (в граммах)
печени /100 г живого веса животного.
11.137512912
Подавление увеличения относительного веса печени (%) 









Изобретение касается производных пиперидина (ПР), в частности получения соединений общей формулы: R2S-C(SRj) C-C(0)-NR,-CH2-CR4- С О, где R - I неразветвленный С, - - С,о -алкил, аллил, фенил, фенетил, З-пиридилметил, бензил, не- или 4-за- мещенный СИ,, СН,0, С1, NH, бензил- оксикарбониламино группой, N0, или 3,4-дизамещенный или С1; R и RJ - низший алкил или Rj + R -СН СН - или -CHj- CHj-; R - Н или низший алкил, или их фармацевтически пpиeмлe ыx солей, которые могут быть использованы как терапевтические и профилактические средства при заболеваниях печени. Цель - создание новых активных веществ указанного класса. Синтез ведут декар- боксилированием ПР с эфирной группой в 5-положении в среде метанола или этанола водным раствором КОН. Испытания показывают, что ПР не токсичны и могут быть использованы для более эффективного лечения и профилактики заболеваний печени, например вирусных гепатитов, гепатопатии, вызванной лекарствами, ожирения печени, желтухи и цирроза печени, чем в случае применения известных веществ, например, соединения формулы: в О) СП
Средний относительный вес печени в группе тестовых соединений
- 4
Средний относительный в печени в контрольной грпе (СС)
Оценка результатов макроскопического исследования печени приведена
в табл. 3.
В эксперименте использовали следующие соединения:
(по примеру 21).
Средний относительный вес печени в нормальной контрольной группе 1
30
Средний относительный вес печени в нормальной контрольной группе
(по примеру 16). 15 lS. 1-(4-Аминобензил)-3-(1,3-дитиол-2-илиден)-2,4-диоксопиперидин
(по примеру 17).
21-. 1-Бензил-3-(1,3-дитиол-2-или- ден)-4-оксопиперидин.
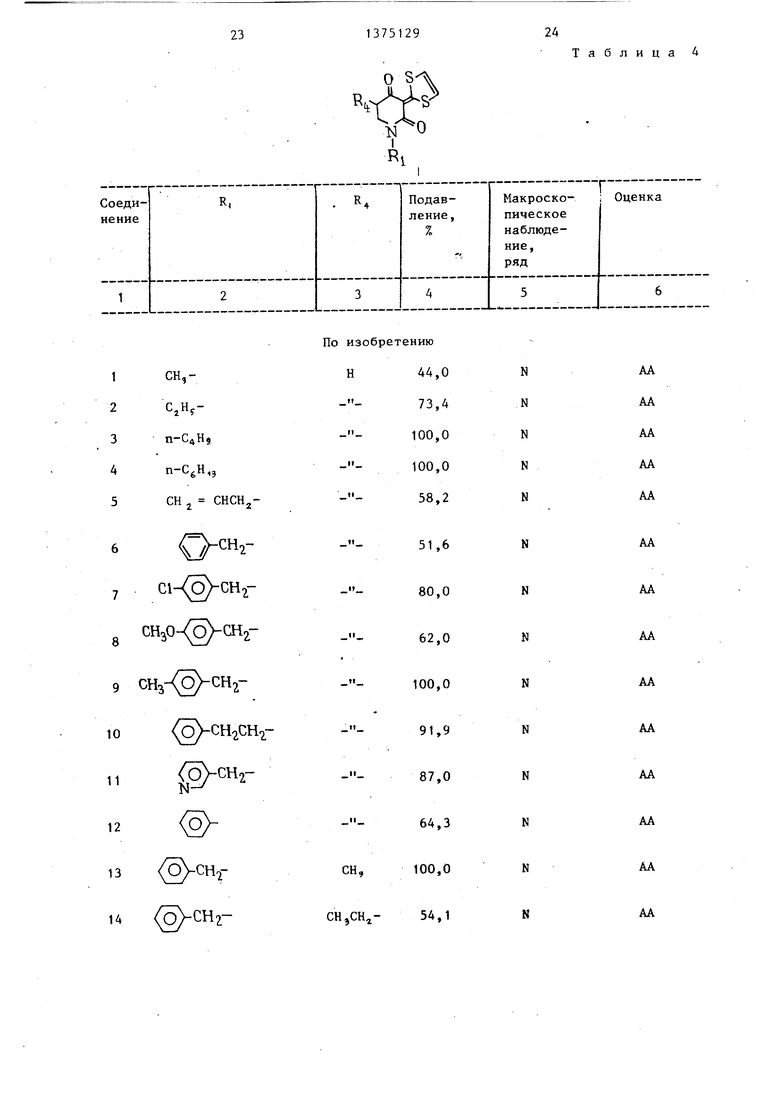
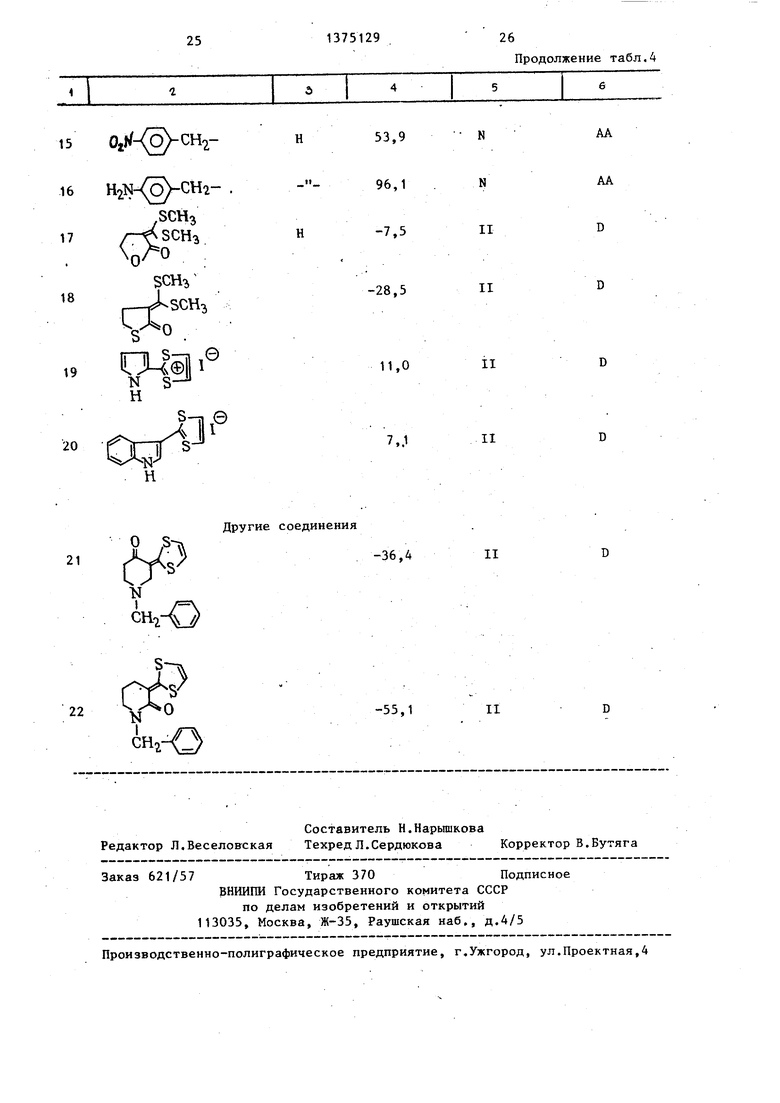
Результаты описанного эксперимента представлены в табл.4.
Как видно из полученных данных, подавление увеличения относительного веса печени соединениями по изобретению (1-16, табл.4) составляет 44,0-100%, тогда как эти значения для аналогичных известных соединений (17-22, табл.4) составляют 28,3 - 11%. Таким образом, ингибирующая активность соединений по изобретению более чем в 4 раза выше активности аналогичных известных соединений.
При макроскопическом исследовании соединения по изобретению оценива- ются как ряд N (почти такие, как нормальная контрольная группа), тогда как аналогичные известные соединения оцениваются как ряд II.
Таким образом, очевидно,действие соединений по изобретению сильнее, чем действие, аналогичных известных соединений.
Соответственно, соединения 1-16 (табл.4) имеют оценку АА, тогда как все соединения-аналоги (17-22, 5 табл.4) - D. I
Таким образом, терапевтическое
действие на печень соединений по изобретению значительно превосходит
35
40
45
50
действие аналогичных известных соединений.
Пример 27. Острая токсичность.
Испытываемое соединение - 1-бен- зил-3-(1,З-дитиол-2-илиден)-2,4-ди- оксопиперидин суспендируют в 0,5%- ном растворе карбоксиметилцеллкшб- sbi и эту суспенизю орально вводят самцам мышей ddY (возраст 5 недель в каждой группе по 3 мыши). Мышей наблюдают в течение 7 дней после
введения испытываемого соединения. Как показали исследования, мак-
симально переносимая доза 1-бензил- -3-(1,3-дитиол-2-илиден)-2,4-диок- сопиперидина составляет более 1500 мг/кг.
Таким образом, предложенный способ позволяет получать соединения, обладающие ценными фармакологически ;ми свойствами.
.
Формула изобретени
Способ получения новых тиокетено вых производных общей формулы 1
где R, - неразветвленный С,-С,о-алкил, аллил, фенил, не
Бледно-желтые игольчатые кристаллы, т.пл. 114,5-117 G (перекристаллизация из смеси этилацетат-изопропиловый эфир)
ИК (-3
ЯМР (CDC1,),J : 1,21 (m, J :,2H,Z3H), 3,58 (кв., J 7,2 Гц, 2Н), 7,28 (с., 2Н).
I Бледно-желтые игольчатые
кристаллы, Т.Ш1. 102-104 с
замещенный бензил или бензил, однозамещенный в положении 4 группой метил,ме- токси , хлор, амине, бензи- локсикарбониламино или нитро, или 3,4-дизамещенный группами метокси или ХЛОР, фенетил или 3-пири- дилметил,
оба алкил или вместе образуют радикал -СН СН - или - СН - CHj- ; R4 - водород или низший алкил, или их фармацевтически приемлемых солей, отличающийся тем, что соединений общей формулы II
R иК,
5
R RsOOC
где R
Л
Y RI
SR3 . SRz
1
R, и
Ч R
4
0
5
имеют указанные значения;
Rf - низший алкил,
обрабатывают водным расвтором гидрата окиси натрия в среде метанола или зтанола или водньм раствором хлористоводородной кислоты в этаноле с выделением продукта в свободном виде или, когда R, обозначает п-аминобен- 3ил или 3-пиридилметил, при необходимости в виде фармацевтически приемлемых солей.
Таблица 1
КбР
макс
), : 1585, 1620.
15
н-Гексил
н-Октил
н-Децил
Аллил
4-Метил- бензил
3,4-Дихлор- бензил
Продолжение табл.1
(перекристаллизация из смеси этилацетат-н-гексан)
ИК ( ). см : 1590,1625.
ЯКР (СВС1,)Д : 0,96 (м., ЗН) , 7,27 (с., 2Н). Бледно-желтые игольчатые кристаллы, т.пл. 88-89,5°С (перекристаллизация из смеси этилацетат-Н гексан).
ИК ( ). : 1595,1625
IP (CDC1,), S : 0,98 (м., ЗН) 7,24 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 86-87,5°С (перекристаллизация из смеси этилацетат-н-гексан). -(
ИК ( :°:, ), см : 1590,1620.
KBh
макс
ЯМР (CDC1,),S : 0,86 (м., ЗН), 7,25 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 93,5-94,5 С (перекристаллизация из смеси этилацетат-н-гексан)
ИК ( 1Гкс ). 1590,1620.
ЯМР (CDC1,), : 0,87 (м., ЗН), 7,25 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 133-134,5 С (перекристашлизация из смеси этилацетат-н-гексан),
ИК .1eb см : 1590,1620.
ЯМР (CDCl,), : 5,0-5,15 (м., 1Н), 5,25-5,4 (м., 1Н), 6,6-6,3 (м., tH), 7,28 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 137-138 С (перекристаллизация из изопропилового спирта).
ИК (i;, ), см : 1590,1625
ЯМР (CDCl,), : 2,31 (с., ЗН) 4,68 (с., 2Н), 7,25 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 175-176,5 С (перекристаллизация из этил- ацетата) .
0
3,4-Диметок- сибензил
1
Фенетил
ЯМР (CDC1,),S : 4,69 (с., 2Н), 7,34 (с., 2Н).
Бледно-желтые игольчатые кристаллы, т.пл, 195-196,5 С (перекристаллизация из смеси зтилацётат-н-гексан).
ИК ( 12кс). : 1590,1625.
ЯМР (CDClj), S : 3,86 (с., 6Н), 4,68 (с., 2Н), 7,35 (с., 2Н)
Бледно-желтые игольчатые кристаллы, т.пл. 147-148°С. (перекристаллизация из изопропилового спирта).
ИК (; „ ,е). смЯМР (CDCl), S :
2
Метил
3
4-ХлорбензШ1
4-Метокси- бензил
Бледно-желтые игольчатые кристаллы, т.пл. 148,5-153 с (перекристаллизация из смеси этилацетат-н-изооропиловый эфир).
ИК ( 5,), : 1595,1630.
ЯМР (CDCl,), : 3,11 (с., ЗН), 7,28 (с., ан)
Бледно-желтые игольчатые кристаллы, т.пл. 143-149 С (перектисталлизация из этанола) .
ИК (). с« 1585,1620.
ЯМР (CDCl,), : 4,72 (с., 2Н), 7,28 (с., 4Н), 7,32 (с., 2Н).
Бледно-желтые игольчатые кристаллы, т.пл. 160-162 С (перекристаллизация из смеси этнпацетат-изопропиловый эфир).
ИК (7ГЛ,см : 1585,1625.
ЯМР (CDCl:), S . 3,77 (с., ЗН), 4,67 (с., 2Н), 7,28 (с., 2Н)
Продолжение табл.1
: 1585,1625. 7,24 (с.,7Н)
19
15
Фенил
16
п-Нитробен- зил
17
п-Аминобен- эил
п-Аминобен- зил гидрохлорид
п-Аминобен- эил гидробромид
18
п-(Н-Бензил- оксикарбо- ниламино)бензил
Продолжейие табл.1
Желтые игольчатые кристаллы, т.пл. 150,5-152 с. . .
ИК (lt,« ). см- : 1630,1&00.
ЯМР (CDC1,),5 : 7,3-7,6 (к.,
7Н), 2,91 (м., J 6,5 Гц,
2Н), 3,92 (м., J 6,5 Гц,
2Н)
Масс-спектру(т/е):289 (М)
Желтые игольчатые кристаллы, т.пл. 192-193°С (перекристаллизация из этилацетата).
ИК ( 1580.
-I
макс
), СМ : 1620,
ЯМР (CDC1,),J : 4,85 (с., 2Н), 7,34 (с., 2Н). Масс-спектр (ш/е) 348 (М)
Свободное основание, кристал т.пл, 156,5-158,5®С (перекристаллизация из этанола).
ИК (К ), см : 3440, 3355, 1625, 1585. ЯМР (CDC1,), У : 4,64 (с., 2Н), 7,26 (д., J - 6 Гц, 1Н) 7,32 (д., J 6 Гц, 1Н). Масс-спектр, (т/е): 318 (М) Бледно-желтые игольчатые кристаллы, т.пл. 212°С (разложение, перекристаллизация из смеси метанол-простой эфир)
Бледно-желтые игольчатые кристаллы, т.пл. 210-214 с (разложение).
ИК (Ё ). см 1620,
ЯМР (DMSO-dfc) 4,68 (с., 2Н), 7,68 (д., Н - 6 Гц, 1Н), 7,74 (д., J- 6 Гц, 1Н). Масс-спектр (т/е){ 318 (М) Бледно-желтые пластинчатые кристаллы, т.пл. 175-176,5 с (перекристаллизация из этил- ацетата) .
ИК (Йс ), см- 1725, 1760, 1580.
ЯМР (CDC1,), : 4,69 (с., 2Н), 5,18 (с., 2Н), 7,15 - 7.5 (м.. 11Н)
21
137512922
Таблица 2
19
-СН СН 20-СН, -СН,
Цвет и вид почти такие, как в нормальной контрольной группе
Имеются признаки улучшения по сравнению с контрольной (СС1) группой
Цвет и вид такие,- как в контрольной (СС1) группе
АА - значительно эффектив-но; А, В, С - эффективно; D - неэффективно.
Бледно-желтые игольчатые кристаллы, т.шт. 148-150 С (перекристаллизация из этанола).
ИК (1С ). см- : 1609,
ЯМР (CDC1,),S : 3,33 (с., 4Н), 4,73 (с., .2Н), 7,30 (с., 5Н)
Бледно-желтое масло.
„ / -ч хлороформ
ИК ( я7с). см :
1620, 1655.
ЯМР (CDClj),S : 2,50 (с., 6Н), 4,71 (с., 2Н), 7,29 (с., 5Н)
АА
СН,С,Н,,
n-CgH,3
СН J CHCHj-СНо
С1-ХО)-СН СНзО- 0 СН2СНз-Х О)-СНп,
О/СН2СН2
{0 -СН2- NS)
(оУснг
По изобретению Н 44,0 73,4 100,0 100,0 58,2
51,6 80,0 62,0
100,0 91,9 87,0 64,3
100,0 54,1
it
сн.
CHjCH,Таблица 4
Л
«,s
1 о Rt
N N N N N
N
АА АА АА АА АА
АА АА АА АА АА АА АА АА АА
,SCH3
н
н
другие соединения
21
N CH;,
s
ЛЛ
CHo-v
г
Продолжение табл.4
53,9 96,1 -7,5
28,5
11,0
7,.1
II
II
II
II
АА
АА
D
D
-36,4
II
-55,1
II
| Ph | |||
| Rioult et J.Vialle | |||
| Composes organigues sulfures | |||
| XXIV | |||
| Condensation des lactones, thiolacto- nes et thiolannethiones-2 avec les aldehydes aromatigues et le sulfure de carbons | |||
| - Bull | |||
| Soc | |||
| chim, 1968, № 11, p.4477 | |||
| J.Nakayataa, Y.Watabe and M.Hoshi- no | |||
| Heterofulvalenes | |||
| I | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| - Bull | |||
| Chem | |||
| Soc, Jpn., 1978, 51(5), 1427- 1432 | |||
| J | |||
| Nakayama, M | |||
| Iroura and M.Hos- hino | |||
| Heterofulvalenes | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - Bull | |||
| Chem | |||
| Soc | |||
| Jpn., 1980, 53, 16611665 | |||
| Вейганд - Хильгетаг | |||
| Методы экспериыента в органической химии | |||
| М.: Химия, 19bb, с.814. | |||
Авторы
Даты
1988-02-15—Публикация
1985-05-24—Подача