1
Ё



Изобретение касается получения производных добутамина ,в частности, получения добутаминов тартрата или лактобионата, используемых для лечения сердечной недостаточности. Цель - создание новых солей добутамина, обладающих лучшей растворимостью в воде. Синтез ведут нейтрализацией добутамина винной или лактобионовой кислотой с образованием рацемата. В случае, когда используют (+)винную кислоту, то получают (+)стереоизомер с удельным вращением [α]25=8,8° и растворимостью 100 мг/мл против 25 мг/мл для гидрохлорида добутамина. Период хранения при 5°С составляет 12 мес. Активность в отношении сердечной недостаточности достигается при дозе 2 мкг/кг. 1 з.п. ф-лы, 1 ил., 1 табл.
Изобретение относится к фармацевтической химии, а именно к получению растворимых в воде солей добутамина N (4-гидроксифенил)-1-метоксипро- (3,4-дигидроксифенил)-этил- амика, взятого в виде (-)- или (+)- стереоизомера или рацемической смеси, или добутамина лак тоб иона та, используемых в качестве ионотропного препарата для лечения сердечной недоста1- точности.
Целью изобретения является получение новых солей добутамина с повышенной растворимостью в воде.
Способ осуществляют следующим обра зом,
Приме р 1. 17 г гидрохлорида добутамина суспендируют в 500 мл деаэрированной воды. Добавляют 150 мг
перекисной присадки - сульфита натрия. Суспензию перемешивают при постоянном положительном давлении Nt и добавляют по каплям в течение более 2,5 ч 50 мл 1 н. водного раствора гидроокиси натрия, разбавленного до 120 мл деаэрированной водой. По завершении добавления нейтралиэацион- 1ную смесь дополнительно перемешивают в течение 2 ч.)при этом отделяется бе- лое твердое кристаллическое вещество, включающее добутамин в виде свободного основания. Верхний слой декантируют и кристаллический остаток тщательно промывают 600 мл деаэрированной воды. Верхний слой снова декантируют. Затем твердый остаток фильтруют в атмосфере азота Отфильтрованную лепешку дважды промывают водой порциями по
ь
00
О
1
9
Ы
100 мл и затем сушат при под вакуумом в течение 3 ч. Получают 14,5 г добутамина в виде свободного основания.
Повторное приготовление осуществляют в трехкратном размере, вместо сульфита натрия используют бисульфит натрия (0,5 г) ,
Выход сукого кристаллического до- бутамина в виде свободного основания составляет 4380 г (96%).
8S3 ммоль добутамина в виде свободного основания и 8,7 ммоль (+)винной кислоты смешивают в атмосфере азота с,0е035 г водного бисульфита натрия, растворенного в воде для инъ- екции9 так, чтобы конечный объем тавлял 25 мл (т„е, содержал 100мг/мл основания добутамина). При необходи- мости солеобразующую смесь нагревают для ускорения растворения основания добутамина. Твердую соль можно получить из раствора выпариванием растворителя. Растворимость полученной соли добутамина превышает 100мг/мл.
При повторении способа с (-)вин- ной кислотой 58,6 г гидрохлорида добутамина в деаэрированной воде нейтрализуют разбавленным водным раство- ром гидроокиси натрия в присутствии перекисной присадки в атмосфере азота, рН 1К09„ Осадок добутамина основания промывают деаэрированной водой и сушат. Для получения соли
добутамина основание смешивают в деаэрированной воде с 26,10 г (-)винной кислоты и 0В8 г бисульфита натрии, рН 3,65 Раствор отфильтровывают и хранят при комнатной температу- ре в атмосфере азота. При 5°С раствор сохраняет стабильность в течение 2 нес, л более.
При получении основания добутамина предпочтительно использование трис-(оксиметил)-метиламина вместо водного раствора гидроокиси натрия. Приготовление осуществляют следующим образом,,
500 мл свободной от кислорода во- ды для инъекции помещают в трехгор- лую круглодоиную колбу емкостью 2л, снабженную отверстием для азота, капельной воронкой, устройством для перемешивания и зондом, ведущим к рНметру. Процесс проводят в атмосфере азота, После растворения 50 мг NaHSOj через У-трубку добавляют 80,16 г добутамина гидрохлорида.трубч
ку дополнительно промывают 500 мл свободной от кислорода воды, полученный шлам перемешивают в течение 15- 20 мин и добавляют по каплям в течение 1-2 ч 250 мл 1М водного трис- (оксиметил)-метиламина (30,3 г в 250 мл свободной от кислорода воды), следя за тем, чтобы рН раствора не превышала 8,5. По завершении добавления нейтрализуемую смесь охлаждают до и фильтруют. Отфильтрованную лепешку, содержащую основание до- бутамина,, промывают 1200 мл воды, сврбодной от кислорода (трижды порциями по 400 мл), и добавляют к раствору 35,56 г (+)винной кислоты и 1,3 г NaHS03 в 1 л свободной от кислорода воды при перемешивании в атмосфере азотаi После полного растворения свободного основания добутамина раствор анализируют на добутамин с помощью УФ-спектра и добавлением свободной от кислорода воды доводят концентрацию добутамина в растворе до значения 50 мг/мл.
Удельное вращение (+)-соли добутамина тартрата (oi) 8,8°.
Аликвоты полученного раствора в 5 мл переносят в атмосфере азота в комплекс ампул. Ампулы в атмосфере азота могут быть загерметизированы или лиофилизированы, в затем загерметизированы.
Свободное основание добутамина (фильтровальная лепешка) можно хранить и превращать в соль винной кислоты при необходимости. Вместо азота можно использовать аргон, а вместо сульфита натрия и бисульфита натрия другие антиоксиданты, такие как сульфиты щелочных металлов или бисульфиты, тиоглицерол, тиоэритритол и др.
Для осуществления предлагаемого способа применимы также (+)винная и мезовинная кислоты, которые также образуют соли добутамина с высокой растворимостью. Кроме того, из любой указанной кислоты могут использоваться не только их стереоизомеры, но и рацематы.
Содержание добутамина во всех растворах контролируют с помощью УФ-спектров, Типичный препарат для инъекцпй (in vivo) имеет следующий состав: 250 мг (основной эквивалент) тартрата добутамина; 4 мг бисульфита натрия; вода - до 5 мл.
Такие растворы помещают в стеклянные ампулы емкостью 5 мл, которые герметизируют, при этом поддерживают бескислородсодержащую атмосферу. Можно также использовать стеклянные пузырьки с резиновой пробкой. Ампулы при необходимости могут быть открыты для осуществления инъекции (in vivo) раствора для лечения сердечного щока. Раствор может быть лиофилизован, а перед использованием вновь приготовлен с помощью свободной от кислорода воды.
Сравнение воздействия на сердечнососудистую систему добутамина гидро- хлорида (партия №6ЕР04, ампула
№ 7051, Dobutrex® 250 мг) и добутамина тартрата (партия № Р-98435-2, 50 мг добутамина тартрата/мл) проведено на анестезированных собаках. Определяли сердечное сокращение (СТ), частоту сердцебиения (HR) и среднее значение артериального кровяного давления (MAP) после введения внутренние дозы 2, 4, 8, 16 мкг/кг каждой соли добутамина. Значительной разницы в реакции сердечно-сосудистой системы в результате применения этих двух солей не наблюдалось.
Методика испытаний.
Четырех непородистых собак муже- кой особи весом 10-12,2 кг анестезировали с помощью тиопентала натрия (15 мг/кг,внутривенно). Насосом обес- .печивали вентиляцию черезэндотрахеаль ную трубку (18 ударов/мин, 20 мл/кг/ Удар)
и нагревательной подушкой поддерживали температуру тела 37-38 С. Оба блуждающих нерва были рассечены при разрезе на шее. MAP фиксировали датчиком давления Statham, присоединенным к канюле, заполненной физиологическим раствором с гепарином (500 ед/мл) и введенной в аорту через первую бедренную артерию. Канюля, соединенная с 3-позиционным запорным краном, была введена в правую бедренную вену для введения препарата. Дз в минуту (KR) и среднего артериаце раскрыли через пятое межреберье, датчик растяжения Walton Brodie при- илк к правому желудочку после удаления перикарда. Датчик отрегулировали на 50 г в систоле, а самописец Berkman RO 12 откалибровали так, что напряжению 50 г соответствовало отклонение пера 10 мм. HR получали электронным способом по сигналу сер148076 6
дечньгх сокращений при помощи устрой
ства связи с кардиотахометром.
Оба добутаминовых образца разводи5 ли в подкисленной воде и вводили в виде инъекций (рН воды 6,0). Добут- амин вводили в дозах 2,4,8 и 16 мкг основания /кг. Двум животным сначала вводили добутамин НС1, а двум - до-
0 бутамин тартрат. Реакция, вызванная каждым соединением, восстанавливалась до контрольного уровня перед каждым введением. Для каждого ответа определяли средние значения и
5 среднюю квадратичную ошибку и при появлении существенной зависимости проводили исследование парных данных по критерию Стьюдента.
0В таблице представлены средние
значения и средние квадратичные ошибки.
Связь доза - ответ была получена для каждого параметра. Величины от5 ветов, вызванных каждым соединением, были почти одинаковы. Статистический анализ парных отвертов, вызванных соединением, не вызвал в этом тесте .значимых различий (,051) между
0 хлоридом добутамина и тартратом добутамина .
П р и м е р 2. Способ осуществляют аналогично примеру 1, только берут 8,3 мколь добутамина в виде свободного основания и 8,7 ммоль лакто05
бионовой кислоты.
Оптическое вращение добутамина лактобионата (рацемата) определяют в 00 мг/мл водного раствора указанной соли в диапазоне 589 нм (Na-ли- ния) в 10 см ячейке при комнатной температуре (). Оптическое вращение равно 3,243°,
Растворимость указанной соли добутамина превышает 100 мг/мл.
Сердечно-сосудистая активность.
Изменения сократительной способности сердца (СТ), число ударов сердльного кровяного давления (MAP)измеряли у четырех анестезированных собак после введения с лечебной целью каждой соли добутамина (внутривенно). Дозировки в виде крупной пилюли (bolus) содержат 2,4,8 и 16 мкг основания/кг.
Сравнивали сердечно-сосудистые изменения в результате применения указанной соли и добутамина гидрохлорида. Разницы не наблюдалось.
Методика испытаний.
Четырех самцов собак Монгрей ве- сом 11,0-13,5 кг анестезировали с помощью тиопентала натрия (15 мг/кг, внутривенно) и фенобарбитала натрия (100 мг/кг9 внутривенно). Насосом обеспечивали вентиляцию положительно- го давпения, вентиляцию через внутри- трахеальную трубку (18 ударов/мин, 20 мл/кг/удар) и нагревательной подушкой поддерживали температуру тела . Оба блуждающих нерва были рассечены посредством разреза на шее0 MAP контролировали датчиком давления Statham, присоединенным к каню ли„ заполненной солевым раствором с добавлением гепарина, препятствующего свертыванию крови (100 ед/мл), Каню- яя введена в аорту через правую бедренную артерию. Канюля, соединенная с 3-позиционным запорным краном, была введена в правую бедренную вену для введения лекарственного препарата, Сердце было экспонировано через пя- т ое правое межреберье. Датчик растяжения Walton Brodie пришили к правому желудочку Датчик растяжения отре- гулировали на напряжение 50 г в систоле и регистрирующий прибор Becktan R 612 откалибровали так, что усилие, равное 50 г, вызывало отклонен ние пера на 10 мм, значение HR полу- чают электронным способом по сигналу сердечных сокращений при помощи устройства связи с кардиотахометром.
Каждый испытуемый образец добут- гмина разводили в подкисленной воде и вводили путем инъекций ХрН 6}0). Дозировки добутамина составляли 2,4, 8 и 16 мкг основания/кг. Ответная реакция от действия каждого соединения восстанавливалась до контроль- кого уровня перед каждой дозировкой (bolus).
Средние значение и среднюю квадратичную ошибку определяли для каждой ответной реакции и проводили
исследования парных данных по критерию Стьюдента.
Значения МАР HR и СТ и ответных реакций, обусловленных добутамин лак5 0 5 0
о 5
0
тобионатом и добутамин Гидрохлоридом, отображены на графике корреляции доза - ответная реакция. Статистические анализы парных ответных реакций для обоих соединений не обнаруживают существенного различия () между ответными реакциями от действия добутамина лактобионата и добутамина гидрохлорида. Таким образом, в опыте с анестезированной собакой лактобионат, будучи введенным внутривенно, имеет такую же сердечно-сосудистую активность, что и добутамин гидрохлорида.
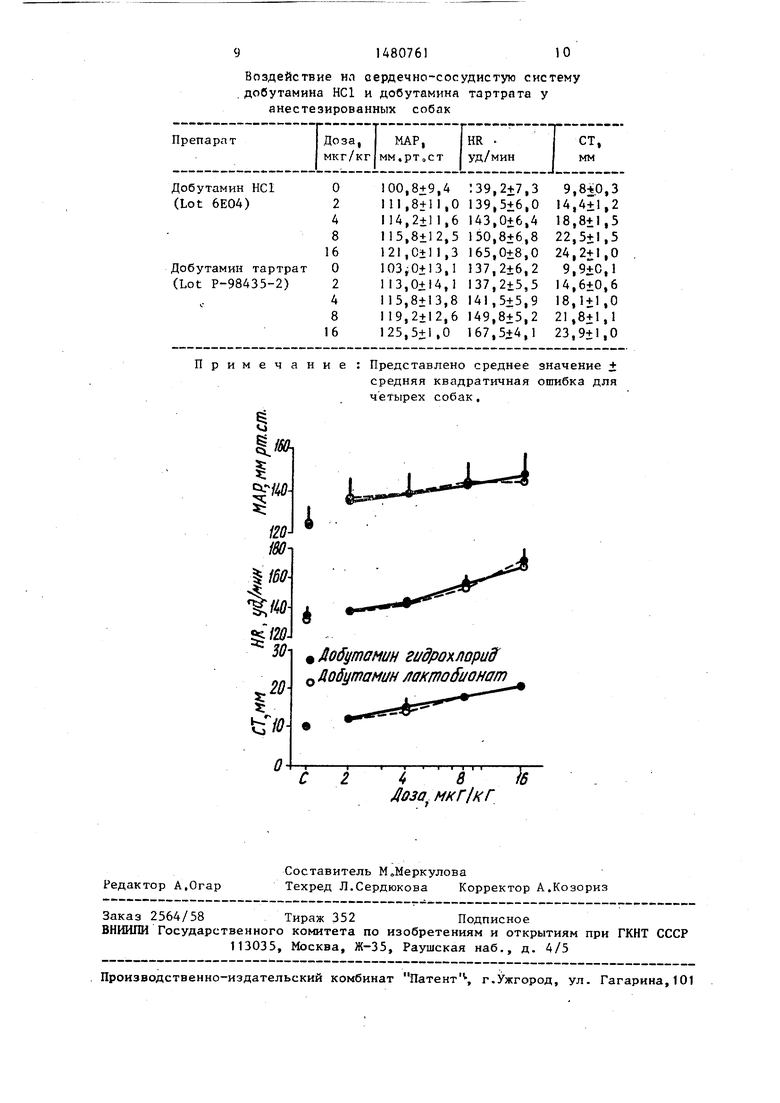
На чертеже дан график изменений MAP, HR и напряжений СТ,обусловленных внутривенным введением bolus добутамина гидрохлорида и добутамина лактобионата, у анастезированной гончей собаки (каждое значение представляет среднюю ответную реакцию, выведенную для четырех собак).
Таким образом, растворимость добутамина тартрата или добутамина лактобионата составляет более 100 мг/кг, в то время как растворимость добутамина гидрохлорида - только 25 мг/мл. При хранении ампул с водным раствором добутамина гидрохлорида при 5°С наблюдается его кристаллизация, в то время как пригодные для инъекций упаковки с водным раст- вором добутамина тартрата могут храниться в пунктах первой помощи в л больницах в течение длительного времени (12 мес.) при ,i
Увеличение растворимости добутамина тартрата или добутамина лактобионата не влияет на его воздействие на сердечно-сосудистую систему по сравнению с добутамином гидрохлоридом.
Формула изобретения
1,Способ получения добутамина тартрата или добутамина лактобионата, отличающийся тем, что . добутамин нейтрализуют соответственно винной или лактобионовой кислотой.
Воздействие на сердечно-сосудистую систему добутамина НС1 и добутамина тартрата у анестезированных собак
римечание : Представлено среднее эначение +
средняя квадратичная ошибка для четырех собак.
§
С,
I
ШЦ :
120 №л
i
Ш Добутамин гидрохлорид
0 Аобутамин лактойионат 
| Патент США № 3987200, кл | |||
| кл,424-330, опублик, 1976. |
Авторы
Даты
1989-05-15—Публикация
1985-12-18—Подача