Изобретение относится к биотехнологии, в частности к генной инженерии, и представляет собой рекомбинантную плазмидную ДНК, кодирующую синтез HBs-антигена вируса гепатита В, и рекомбинантный штамм ВОВ, синтезирующий этот антиген.
Целью изобретения является получение рекомбинантного штамма ВОВ, обеспечивающего повышенный уровень экспрессии HBs-антигена в эукариотических клетках. Повышение синтеза обеспечивается за счет трансформации рецепиентного штамма рекомбинантной плазмидой, содержащей две копии HBs-антигена.
П р и м е р 1. Способ получения плазмиды pLD 206.
Клетки E.coli НВ 101, содержащие плазмиду pVJ 11, выращивают в 1 л L-бульона с 50 мкг/мл ампициллина при 37оС и аэрации до концентрации клеток 5-6х108/мл среды, добавляют хлорамфеникол до конечной концентрации 170 мкг/мл до конечной концентрации 170 мкг/мл и продолжают инкубацию при интенсивной аэрации в течение 16-18 ч. Бактериальные клетки собирают центрифугированием (5000g, 20 мин, 4оС) и из них выделяют плазмидную ДНК. Далее ДНК плазмиды очищают методом равновесного центрифугирования в градиенте плотности хлорида цезия с бромидом этидия (700 мкг/мл).
1 мкг ДНК плазмиды pVJ 11 инкубируют при 37оС с рестрикционной эндонуклеазой EcoRI в буфере 1 (100 мМ трис-HCl, рН 7,5; 50 мМ NaCl; 6 мМ MgCl2; 6 мМ 2 меркаптоэтанол). После полного расщепления (анализ при помощи электрофореза в 1%-ном агарозном геле) препарат прогревают 10 мин при 65оС с целью инактивации фермента.
EcoRi-фрагмент, содержащий структурный ген HBs Ag под контролем промотора Р7,5 ВОВ, получают следующим образом. 5 мкг ДНК-плазмиды pLD 1 инкубируют с рестрикционной нуклеазой EcoRI в буфере 1. После анализа на полноту рестрикции препарат ДНК разделяют электрофорезом в 0,6%-ном геле из легкоплавкой агарозы. Участок геля, в котором локализован фрагмент ДНК в 1700 н. п. вырезают, добавляют к нему 5 мл 5 мМ ЭДТА, рН 8,0, и прогревают 20 мин при 60оС для растворения агарозы. Агарозу удаляют при помощи фенольной обработки. Далее раствор концентрируют бутанолом до объема 150 мкл и ДНК осаждают этанолом. Высаженную ДНК растворяют в 50 мл воды и используют для легирования и ник-трансляции.
0,3 мкг EcoRI-фрагмента обрабатывают ДНК-лигазой фага Т4 в буфере следующего состава: 66 мМ трис-HCl, рН 7,6; 5 мМ MgCl2, 5 мМ дитиотрейтол; 1 мМ АТФ, в течение 30 мин при 18оС с целью получения димеров. К этой смеси добавляют 1 мкг ДНК плазмиды pVJ 11, обработанной рестриктазой EcoRI, и проводят легирование при 8оС в течение 18 ч. Легированную смесь используют для трансформации клеток E.coli HB 101 (thi leu pro lac gal str rec A Endo I hsd R hsd M). Трансформанты высевают на L-среду с 2% агара и 50 мкг/мл ампициллина. По- лученные клоны переносят на нитроцеллюлозные фильтры и исследуют методом гибридизации колоний, используя в качестве зонда EcoRI-фрагмент в 1700 н.п. меченный 32Р методом ник-трансляции.
Плазмидную ДНК, выделенную из клонов, давших положительный сигнал гибридизации, анализируют при помощи рестрикционного анализа (использовали эндонуклеазы BamHI, EcoRI, Xва I, Hind III) и блот-гибридизации по Саузерну. Проведенный анализ позволяет отобрать клон, содержащий плазмиду pLD 206, cоcтоящую из векторной плазмиды pVJ 11 и двух EcoRI-фрагментов в противоположной по отношению друг к другу ориентации.
П р и м е р 2. Способ получения рекомбинантного штамма ВОВ.
Гомологичную рекомбинацию ДНК донорской плазмиды pLD 206 с геномом ВОВ проводят в перевиваемой культуре клеток почек обезьян (линия СУ-1).
Клетки выращивают на среде Игла МЕМ с добавлением 10% сывоpотки эмбрионов коров (СЭК) во флаконах площадью 25 см2. Клетки достигают состояния полного монослоя через 48 ч после посева. Культуральную среду из флаконов удаляют, клеточный монослой промывают фосфатным буфером (рН 7,1) и заражают ВОВ с множественностью 0,05 БОЕ/кл. Для заражения используют лабораторный штамм WR дикого типа, адаптированный к размножению в условиях культуры клеток.
Через 2 ч после заражения проводят трансфекцию инфицированных клеток ДНК плазмиды pLD 206. Для этого 5 мгк ДНК pLD 206 и 15 мкг ДНК тимуса теленка в качестве носителя растворяют в 1 мл буфера следующего состава: 20 мМ Hepes (рН 7,05); 0,14 М NaCl; 5 мМ KCl; 1 мМ Na2HPO4; 0,1% α- D глюкозы. Затем добавляют CaCl2 до конечной концентрации 125 мМ. Смесь оставляют на 30 мин при комнатной температуре для образования ДНК-кальциевого комплекса, а затем вносят в культуру зараженных клеток. Через 30 мин после трансфекции добавляют 10 мл ростовой среды МЕМ с 8% СЭК, инкубируют 3,5 ч при 37оС. Затем среду заменяют на свежую ростовую и продолжают инкубацию в течение 48 ч. Обычно к этому сроку вирус оказывает цитопатогенное действие на все клетки культуры. Клетки стряхивают со стекла и собирают центрифугированием при 800g в течение 10 мин. Осадок ресуспендируют в 0,5 мл среды, трижды замораживают, оттаивают для высвобождения вируса из клеток.
Селекцию рекомбинантов проводят в культуре клеток 143 ТК- в присутствии 30 мкг/мл 5-бромдезоксиуридина. Поскольку целостность гена тимидинкиназы (ТК-гена) в составе плазмиды pLD 206 нарушена, то вирусы рекомбинанты приобретают ТК-генотип, т.е. способность развиваться в присутствии 5-бромдезоксиурицидина в отличие от вируса дикого типа, имеющего ТК+ генотип.
Выделенные ТК- -клоны размножают в культуре клеток СУ-1 и иммобилизуют на нитроцеллюлозных мембранных фильтрах. Иммобилизованную ДНК клонов гибридизуют с BaMHI-фрагментом геном вируса гепатита В, содержащим ген HBd Ag, меченным 32Р. Доля клонов-рекомбинантов составляет около 20% всех выделенных ТК-клонов.
Клоны рекомбинанты анализируют на экспрессию HBs Ag в культуре зараженных клеток СУ-1 в реакции ИФА. Клон ВОВ, давший максимальную экспрессию антигена, подвергают последовательному двухкратному клонированию методом бляшек с целью получения генетически однородной популяции вируса.
П р и м е р 3. Уровень экспрессии HBs Ag в культуре клеток, зараженных рекомбинантным штаммом ГЛД-9331-HBs Ag-2.
В чашки Петри площадью около 20 см2 засевают культуру клеток СУ-1 в среде ДМЕМ с 10% СЭК из расчета 150000 кл/мл, а всего 750000 кл/чашку. Через 48 ч после посева в чашках образуется сплошной монослой. Из 3 чашек клетки снимают версеном и подсчитывают их количество в камере Горяева для каждой чашки отдельно. Количество выросших клеток составляет (2 ±0,1) х 106.
48-часовую культуру клеток заражают рекомбинантным штаммом ГЛД-854-HBs Ag-1 или ГЛД-9331-HBs Ag-2, содержащим соответственно одну или две копии экспрессируемого гена HBs Ag, с множественностью 30 БОЕ/кл (по 3 чашки соответственно на каждый вариант). Объем инокулята составляет 0,2 мл. По окончании периода адсорбции инокулят отсасывают, в чашки вносят по 5 мл среды МЕМ с 1% СЭК и инкубируют в термостате при 37оС в атмосфере СО2 при влажности 98%
Через 24 ч после окончания периода адсорбции из чашек отсасывают культуральную среду. Клетки ресуспендируют в 2 мл свежей среды и разрушают ультразвуком для экстракции из клеток HBs Ag. Полученную смесь центрифугируют при 2000 об/мин в течение 10 мин для удаления клеточного дебриса.
Содержание HBs Ag в клеточной фракции и в культуральной среде определяют методом ИФА.
Исследуемые образцы клеточных фракций и культуральной среды готовят в разведениях 1: 2 1:10240. Определяют средние значения оптических плотностей (ОП) при длине волны 490 нм на фотометрирующем устройстве для 2 образцов положительного контроля из 4 образцов отрицательного контроля, установив "ноль" по субстратному раствору в чистых лунках, т.е. за вычетом значений фона. Результаты ИФА считают отрицательными, если ОП исследуемого образца не превышает ОП отрицательного контроля более, чем в 2,5 раза. Минимальная выявляемая концентрация HBs Ag с помощью набора составляет 1 нг/мл.
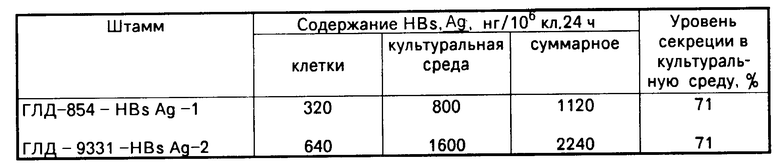
Результаты определения уровня экспрессии HBs Ag в культурах представлены в таблице.
Как видно из данных таблицы, уровень синтеза HBs Ag зависит от дозы гена: использование штамма с двумя копиями гена HBs Ag приводит к достоверному увеличению количества синтезируемого HBs Ag. В культуре клеток CУ-1 уровень HBs Ag при этом достигает 2240 нг/106 кл˙24 ч, причем свыше 70% его секретируется в культуральную среду. На более поздних сроках инфекции уровень секреции достигает 85%
П р и м е р 4. Плавучая плотность HBs Ag, синтезируемого рекомбинантным штаммом ГЛД-9331-HBs Ag-2.
50 мл осветленной культуральной среды, содержащей рекомбинантный HBs Ag, центрифугируют при 73000 g в течение 24 ч для осаждения HBs Ag. Полученный осадок ресуспендируют в 0,01 М трис-HCl буфере, рН 7,2; наносят на ступенчатый градиент плотности 1,1-1,6 г/см3 хлорида цезия и центрифугируют в роторе SW 40 Бекман при 170000 g в течение 64 ч. Полученный градиент фракционируют по 0,5 мл и определяют плотность хлорида цезия в каждой фракции. Затем аликвоты, взятые по 50 мкл из каждой фракции, разводят в 10 раз и определяют в них содержание HBs Ag методом радиоиммунного анализа. Плавучая плотность рекомбинантного HBs Ag составляет 1,2 г/см3, что соответствует плотности HBs Ag, получаемого из плазмы крови.
Изобретение относится к биотехнологии, в частности к генной инженерии, и представляет собой штаммпродуцент антигена HBs и рекомбинантную плазмиду для создания такого штамма. Рекомбинантная ДНК содержит лдве примыкающие копии гена HBs-антигена вируса гепатита B, каждой из которых предшествует промотор белка 7,5 кД вируса осповакцины, а обе копии фланкированы последовательностями Hind III-J-фрагмента ДНК вируса осповакцины. Рекомбинантный штамм продуцирует до 2200 нг HBs Ag/106 кл. 24 ч. 1 табл.
| Smihetal G.C | |||
| Nature, 1983, N 302, 490-795. |
Авторы
Даты
1995-09-10—Публикация
1988-01-27—Подача