форме (200 мл). Раствор промывают насыщенным водным раствором бикарбоната натрия. Водный слой экстрагируют хлороформом (3 х 200 мл). Объединенные экстракты сушат и концентрируют, затем кристаллизуют, добавляя этанол, в результате чего получают циклоартенил-4-окси-З-метокси- бензоат, содержащий молекулярный этанол (21,0 г), выход 87%, т.пл.132 133°С.
W
2&
61,3
Удельное вращение (с 1,00, СНС1,).
Вычислено, %: С 77,12; Н 10,03.
С38 Н5вО,,.(мол.м. 622,90)
Найдено, %: С 77,21; Н 10,12.
ИК(КВг) , см-1 : 3380, 2920, 2850 1705, 1683, 1607, 1590, 1510, 1280, 1225.
ПНР (CDClj),S : 0,39 (1Н, 1/2 АВ кв., 4,2 Гц); 0,60 (1Н, 1/2 АВ кв., 4,2 Гц); 0,70-2,40 (27Н, м); 0,91 (6Н, с);. 0,97 (ЗН, с); 1,03 (ЗН, с); 1,60 (ЗН, ш.с); 1,68 (ЗН, ш.с); 3,93 (ЗН, с); 4,60-5,30 (2Н, м); 6,08 (1Н, ш.с.); 6,78-7,80 (ЗН, м).
П р и м е р 9. Циклобранил-3,4- дигидроксициннамат.
а) Получение циклобранил-3,4-ди- пропионилоксициннамата.
17,43 мл тионилхлорида (2 экв.) добавляют к суспензии 3,4-дипропи- онилкофейной кислоты (35,07 г, 0,12 моль) в толуоле (150 мл), и реакционную смесь перемешивают при 60°С в течение 2 ч. Полученную смесь перегоняют при пониженном давлении для удаления растворителя. Остаток суспендируют в смеси толуола (240 мл и пиридина (50 мл). К этой суспензии добавляют циклобранол (40 г, 0,0908 моль), и полученную смесь перемешивают при 60°С в течение 2 ч. Затем растворитель отгоняют при по- ниженном давлении. Остаток экстрагируют хлороформом (300 мл). Полученны
5
0
5
0
5
0
Вычислено, %: С 77,27; Н 9,30.
C4ЈHfc6°& (мол.м. 714,99)
Найдено, %: С 77,34; Н 9,23.
ИК (КВг)} , 2920, 2850, 1770, 1710, 1250, 1170.
ПМР (CDC1,),S : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,62 (1Н, 1/2 АВкв. 4,8 Гц); 0,70-2,20 (27Н, м); 0,90 6Н, с); 0,96 (6Н, с); 1,25 (6Н, т, 7,2 Гц); 1,62 (9Н, с); 2,57 (4Н, кв., 7,2 Гц); 4,50-4,88 (1Н,м); 6,36 (1Н, 1/2 АВ кв., 16,6 Гц); 7,05 (ЗН, м); 7,60 (1Н, 1/2 АВ кв., 15,6 Гц).
б) Получение циклобранил-3,4-ди- оксициннамата.
Циклобранил-3,4-дипропионилокси- циннамат (35 г, 0,049 моль), полученный на стадии а, растворяют в ди- iокеане (600 мл). К этому раствору добавляют 25%-ный водный аммиак (70 мл) и полученную смесь перемешивают при 50°С в течение 2 ч. Затем растворитель отгоняют при пониженном давлении. Неочищенные кристаллы перекристаллиэовывают из смеси ацетон-вода (4:1, объем/объем), в результате чего получают 22,3 г циклобранил-3, 4-диоксициннамата, выход 75%, т.шт. 246-247,5°С.
(с
Удельное вращение е/Л-ц + 33,6
5
0
5
1,10, СНС13).
Вычислено, %: С 79,69; Н 9,70.
C HgeO-v (мол.м. 602,86)
Найдено, %: С 79,62; Н 9,68.
ИК (КВг) } , 3400, 2920, 2850, 1680, 1600, 1520, 1440, 1275, 1180, 970.
ПМР (CDC1 j), 8 : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,59 -(1Н, 1/2АВкв., 4,8 Гц); 0,69-2,20 (27Н, м); 0,85 (ЗН,.с); 0,90 (ЗН, с); 0,У6 (6Н, с); 1,60 (9Н, с); 4,36-4,80 (1Н, м); 6,16 (1Н, 1/2 АВ кв., 15,6 Гц), 6,60- 7,16 (5Н, м); 7,74 (1Н, 1/2 АВ кв., 15,6 Гц).
П р и м е р 10. Получение циклобранил-3 ,4-диоксициннамата.
Предлагаемое соединение получают по примеру 96, где циклобранил-3,4- диацетоксициннамат (35 г,0,051 моль) используют вместо циклобранил-3,4- дипропионилоксициннамата. Выход 22,1 г (64%), т.пл. 246-247°С.
Удельное вращение + 33,6° (с 0,11, CHClj).
Вычислено, %: С 79,69; Н 9,70.
С+0К6804 (мол.м. 602,86)
Найдено, %: С 77,78; Н 9,62.
Пример 11. Циклобранил-4- гидрокси-3-метоксибензоат.
а) Получение циклобранил-4-аце- токси-3-метоксибензоата.
К 4-ацетилванилиновой кислоте (18,60 г, 0,0885 моль), растворенной в толуоле (100 мл), добавляют тионил хлорид (12,86 мл, 2 экв) и перемеши- вают при 60°С в течение 2 ч. Полученную смесь выпаривают при пониженном давлении, а остаток растворяют в толуоле (150 мл) и пиридине (30 мл). К полученному раствору добавляют циклобраншт (30 г, 0,068 моль), и полученную смесь перемешивают при 60°С в течение 2ч, затем выпаривают при пониженном давлении, а остаток экстрагируют хлороформом (300 мл). Полученный экстракт сушат, концентрируют в вакууме и очищают на хромато- графической колонке с силикагелем (растворитель- этилацетат: гексан 1:6, объем/объем), в результате чего получают сложный эфир циклобранил- 4-ацетокси-3-метоксибензоата(33,38 г)
выход 77%, т.пл. 177-178 С.
об
2(,5
54,f
Удельное вращение (с 1,02, СНС13).
Вычислено, %: С 77,80; Н 9,56.
C4iH6005 (мол.м. 632,89)
Найдено, %: С 77,71,Н 9,64
ИК (КВг) } , см- : 2920, 2850, 1770,1710, 1285, 1190, 1170.
ПМР (CDClj),$ : 0,38 (1Н, 1/2 АВ кв., 4,8 Гц); 0,63 (1Н, 1/2 АВ кв., 4,8 Гц); 0,70-2,40 (27Н, м); 0,92 (6Н, с); 0,98 (ЗН, с); 1,04 (ЗН, с); 1,62 (9Н, с); 2,32 (ЗН, с) 3,83 (ЗН, с); 4,60-5,00 (1Н, м); 6,92-7,20 (1Н, м); 7,51-7,80(2Н,м).
б) Получение циклобранил-4-окси- 3-метоксибен зоата.
Циклобранил-4-ацетокси-З-метокси бензоат (30 г, 0,0474 моль), полученный на стадии а, растворяют в тетрагидрофуране (300 мл) и к полученному раствору добавляют 25%-ный
15
20 30
25
50
55
водный аммиак (60 мл). Полученную смесь перемешивают при 50°С в течение 2ч, затем выпаривают досуха при пониженном давлении. Оставшиеся кристаллы перекристаллизовывают из смеси ацетон-вода (5:1, объем/объем), в результате чего получают циклобранил- 4-окси-З-метоксибензоат (23,1 г), )0 выход 82%, т.пл. 191-193°С.
Удельное вращение & + 55,8° (с 1,02, CHClj).
Вычислено, %: С 79,27; Н 9,89. С,9Н5804 (мол.м. 590,85) Найдено, %: С 79,35; Н 9,80. ИК (КВг)} , 3400, 2920, 2850, 1700, 1590, 1510, 1275, 1220.
ПМР (CDC13),S : 0,38 (1Н, 1/2 АВ кв., 4,8 Гц); 0,64 (1Н, 1/2 АВкв., 4,8 Гц); 0,70-2,2 (27Н, м); 0,92 (6Н, с); 1,00 (ЗН, с); 1,05 (ЗН, с); 1,64 (9Н, с); 3,95 (ЗН, с); 4,6-5,0 (1Н, м); 6,06 (1Н, ш.с.); 6,74-7,04 (1Н, м); 7,44-7,77 (2Н, с).
П р и м е р 12. Циклобранил-3,4- гидроксибензоат.
а) Получение циклобранил-3,4-ди- ацетоксибензоата.
К диацетилпротокатеховой кислоте (21,08 г, 0,085 моль), суспенди- - рованной в толуоле (100 мл), добавляют тионилхлорид (12,86 мл, 2 экв) и перемешивают при в течение 2 ч. Затем полученную смесь выпаривают при пониженном давлении. Остаток суспендируют в толуоле (150 мл) и пиридине (30 мл), и к суспензии добавляют циклобранол (30 г, 0,068 моль). Полученную смесь перемешивают при 60&С в течение 2 ч. Затем полученный раствор выпаривают при пониженном давлении. Остаток экстрагируют хлороформом (300 мл). Полученный экстракт сушат, концентрируют в вакууме и очищают на хрома- тографической колонке с силикате- лем (растворитель- толуол), в результате чего получают циклобранил- 3,4-диацетоксибензоат (24,2 г), выход 54%, т.пл. 165-166°С.
Удельное вращение otj 51,3° (с 1,01, СНС1,).
Вычислено, %: С 76,32; Н 9,15. C42.Hto°5 (мол.м. 660,90) Найдено, %: С 76,45; Н 9,10. ИК (КВг) , 2920, 2850, 1770, 1715, 1280, 1195, 1160.
ПМР (CDC13),S: 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,62 (2Н, 1/2АВкв.,
35
40
45
4,9 Гц); 0,70-2,40 (27Н, м); 0,90 (6Н, с); 0,96 (ЗН, с); 1,00 (ЗН, с) 1,60 (9Н, с); 2,26 (6Н, с); 4,60- 4,98 (1Н, м); 7,08-7,40 (1Н, с); 7,73-8,06 (2Н, м).
б) Получение циклобранил-3,4-ди- оксибензоата.
Циклобранил-3,4-диацетоксибензоа (24,0 г, 0,0363 моль), полученный на стадии а, растворяют в диоксане (480 мл) и к этому раствору добавляют 25%-ный водный аммиак (48 мл). Полученную смесь перемешивгиот при в течение 1 ч, затем выпаривают досуха при пониженном давлении Оставшиеся кристаллы перекристаллиз вывают из этанола, в результате чего получают циклобранил-3,4-диокси
бензоат (17,5 г), выход 84%,т.пл„21 216°С.
Удельное вращение utj26 + 59,4° (с 0,98, СНСЬ).
Вычислено, %: С 79,12; Н 9,79.
С38Н56°4 (мол.м. 576,83}
Найдено, %: С 79,03}Н 9,87.
ИК (КВгН , см-1: 3350,2920,2850 1680, 1605, 1440, 1280, 1230, 1100, 875.
ПМР (CDC13),S : 0,38 (1Н,1/2 АВ кв., 4,9 Гц); 0,61 (1Н, 1/2 АВ кв., 4,8 Гц); 0,70-2,20 (27Н, м); 0,90 (6Н, с); 0,98 (ЗН, с); 1,02 (ЗН, с) 1,62 (9Н, с); 2,72-3,20 (2Н, ш.с); 4,60-4,90 (1Н, м); 6,70-6,96 (1Н,м) 7,40-7,64 (2Н, м).
Пример 13. Циклобранил-орто гидроксибензоат.
а) Получение циклобранил-орто- ацетоксибензоата.
К ацетилсалициловой кислоте (15,94 г, 0,088 моль), суспендированной в толуоле (100 мл), добавляют тионилхлорид (40 мл, 6,3 экв) и перемешивают при 80°С в течение 3 ч Полученную смесь выпаривают при пониженном давлении, остаток растворяют в толуоле (180 мл) и пиридине (40 мл), а затем добавляют циклобра нол (30 г, 0,068 моль). Полученную смесь продолжают перемешивать при 60°С в течение 2 ч, а затем выпаривают при пониженном давлении. Остаток экстрагируют хлороформом (300м и экстракт промывают 3%-ным водным бикарбонатом натрия, водой и насыщенным рассолом. Полученные экстракт сушат, концентрируют Е вакууме и полученный остаток очищают на хро
матографической колонке с силика- гелем (растворитель- гексан:толуол 1:1, объем/объем), в результате че- го получают циклобранил-орто-аце- токсибензоат (29,6 г), выход 72%, т.пл. 165-166°С. Удельное вращение ГеО + 58,4й (с 1,01, СНС1,).
Вычислено, %: С 79,69; Н 9,70. С4оИ58°4 (мол.м. 602,86)
Найдено, %: С 79,64; Н 9,78.
ИК (КВгИ , : 2920, 2850, 1770, 1720, 1260, 1190, 1080.
ПМР (CDC1,),S : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,60 (1Н, 1/2
АВ кв., 4,8 Гц); 0,70-2,40 (27Н,м); 0,89 (6Н, с); 0,96 (ЗН, с); 1,00 (ЗН, с); 1,62 (9Н, с); 2,33 (ЗН, с); 4,60-4,95 (1Н, м); 6,88-7,68 (ЗН,м);
7,82-8,10 (1Н, м)
5
стадии а, растворяют в 400 мл диок- сана, и к полученному раствору добавляют 25%-ный водный аммиак (60 мл) по каплям. Полученную смесь перемешивают при 50 С в течение 2 ч 0 и выпаривают досуха при пониженном давлении. Оставшиеся кристаллы пере- кристаллизовывают из смеси ацетона и воды (1:1, объем/объем), в результате чего получают сложный эфир циклобранил-орто-оксибензоата
J
0 7,82-8,10 (1Н, м)
б) Получение циклобранил-орто- оксибензоата.
Циклобранил-орто-ацетоксибензоат (24 г, 0,0398 моль), полученный на
0
5
(20,2 г), выход 90%, т.пл. 200-201 С.
Удельное вращение li + 69,3 (с 1,00, СНС1,).
Вычислено, %: С 81,38; Н 10,07.
СЗВН56° (мол.м. 560, 83)
Найдено, %: С 81.29; Н 10,02.
ИК (KBr) l , : 3120,2920, 2850, 1670, 1615, 1300, 1250, 1220, 1165, 1095.
ПМР (CDC13),S : 0,37 (1Н,1/2 АВ кв., 4,8 Гц); 0,62 (1Н, 1/2АВ,кв. 4,8 Гц); 0,7-2,20 (27Н, м); 1,05 (ЗН, с) 0,90 (6Н, с); 0,97 (ЗН, с); 1,60 (9Н, с); 4,60-5,00 (1Н, м); 6,67-7,93 (4Н, с); 10,92 (1Н, с).
П р и м е р 14. Циклобранил-пара- аминобензоат.
а) Получение циклобранил-пара- ацетамидобензоата.
К пара-ацетамидобензоатной кисло- те (15,85 г, 0,088 моль), растворенной в диоксане (150 мл), добавляют тионилхлорид (25,7 мл, 4 экв) и перемешивают при 60 С в течение J2 ч.
0
Смесь выпаривают при пониженном давлении, и к остатку добавляют диок- сан (150 мл) и пиридин (50 мл). К полученному раствору добавляют циклобранол (30 г, 0,069 моль), и полученную смесь перемешивают при 60°С в течение 2 ч. Реакционную смесь выпаривают при пониженном давлении, к остатку добавляют этил- ацетат (300 мл). Неочищенные кристаллы выделяют фильтрованием и очищают на хроматографической колонке с силикагелем (растворитель-хлор о
а) Получение циклобранил-пара- ацетоксибен зоата.
пара-Ацетоксибензойную кислоту (18,6 г, 0,103 моль) и тионилхлорид (40 мл) смешивают и перемешивают при в течение 12 ч. Затем избыток тионилхлорида удаляют перегонкой при пониженном давлении. К этому остатку, суспендированному в толуоле (220 мл) и пиридине (60 мл), добавляют циклобранол (35 г, 0,0794 моль) и перемешивают при 60°С в течение 2 ч. Затем раствор































| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения оптически активных @ -арилалкановых кислот | 1985 |
|
SU1598863A3 |
| Способ получения производных цефалоспорина или их солей, гидратов или солей их гидратов | 1986 |
|
SU1722229A3 |
| Способ получения замещенных алкановых кислот или их сложных эфиров (его варианты) | 1981 |
|
SU1340580A3 |
| Способ получения оптически активных кеталей | 1985 |
|
SU1431678A3 |
| Способ получения 4,5-диарил-2-нитроимидазолов | 1979 |
|
SU940647A3 |
| Способ получения альфасульфонилоксикетонацеталей | 1982 |
|
SU1331425A3 |
| Способ получения производных имидазола | 1989 |
|
SU1799383A3 |
| Способ получения производных пиридина или их фармацевтически приемлемых солей | 1987 |
|
SU1780535A3 |
| Способ получения 7-фенилглицинамидо-3-цефем-4-карбоновой кислоты или ее солей или функциональных производных | 1974 |
|
SU608478A3 |
| Способ получения сложных эфиров @ -эпимера 7 @ -малонамидо-7 @ -метокси-3-(1-метилтетразол-5-илтиометил)-1-детиа-1-окса-3-цефем-4-карбоновой кислоты | 1983 |
|
SU1225488A3 |
Изобретение касается ненасыщенных циклоалифатических веществ, в частности тритерпениловых эфиров кислот общей формулы I: CH=CH-CR1=CR2-CR3=CR4, где R1=C(O)OR6
CH=CR5-C(O)OR6
R2=H,OH
R3=H, OH, C1-C4-алкилогруппа, R4=H, OH, N H2
R5=H, C1-C4-алкил
R6-циклоартенил, циклобранил, 24-метиленциклоартанил, причем замещение в бензольном цикле может быть парой, выбранной из ряда: а) OH и C1-C4-алкоксигруппа
б) NH2 и C1-C4-алкоксигруппа
в) две OH-группы, за исключением тритерпениловых эфиров феруловой кислоты, или г) хотябы один из R2-R4=OH, или д) R4=NH2, которые обладают противотигиперлипидемической активностью, что может быть использовано в медицине. Цель - создание более активных веществ указанного класса. Синтез ведут деацилированием сложного эфира тритерпенилового спирта ф-лы II: CH=CH-CR1=CR7-CR8=CR9, где R1 - см. выше, R7=H, C2-C6 - ацилокси
R8=H
C1-C4 - алкокси- или C2-C6 -ацилокси
R9=H, C2-C6-ацилокси, C2-C5-ациламидогруппа, причем замещение в бензольном цикле может быть парой, выбранной из ряда: а) C2-C4-ацилокси и C1-C4-алкокси
б) C2-C5-ациламидо- и C1-C4-алкокси-
в) две C2-C6-ацилокси, г) один из R7-R9=C2-C6-ацилокси
д) R9-ациламидо-C2-C5-группой. Новые вещества 
форм). Полученные кристаллы перекрис- выпаривают при пониженном давлении, таллизовывают из этанола, в результате чего получают циклобранил-пара- ацетамидобензоат (32 г), выход 78%, т.пл. 197-198°С.
Удельное вращение Јji) + 54,7°
(с 1,01, CHClj).
Вычислено, %: С 79,82; Н 9,88;
N 2,32.
C40HS03N (мол.м. 601,88)
Найдено, %: С 79,75; Н 9,83, N 2,41.
ИК (КВг) , 3420, 2920, 28-50, 1710, 1690, 1680, 1600, 1535, 1280, 1175.
ПНР (CDC1}),8: 0,38 (1Н, 1/2 АВ кв., 4,8 Гц); 0,62 (1Н, 1/2 АВ кв., 4,8 Гц); 0,70-2,28 (27Н, м); 0,90 (6Н, с); 0,98 (ЗН, с); 1,04 (ЗН, с); 1,62 (9Н, с); 2,16 (ЗН,с); 4,50-4,96 (1Н, м); 7,37 (1Н, ш.с); 7,44-8,12 (4Н, м).
б) Получение циклобранил-пара- аминобензоата.
Циклобранил-пара-ацетамидобензоат (32 г, 0,053 моль), полученный на стадии а, растворяют в тетрагидро- фуране (300 мл), затем добавляют концентрированную соляную кислоту (60 мл) и перемешивают при 70°С в течение 2 ч. Смесь выпаривают при пониженном давлении. Остаток экстрагируют хлороформом (400 мл), затем полученный экстракт сушат и концентрируют. Остаток дважды очищают на хроматографической колонке с силикагелем (растворитель- смесь толуол, гексан этилацетат 5:3:1, объем/объем) , в результате чего получают циклобранил-пара-аминобензоат (17 г), выход 57%, т.пл. 190-19ГС.
Удельное вращение О26 + 58,4° (с 1,01, CHClj). D
Пример 15. Циклобранил-п- гидроксибензоат.
20
25
30
35
40
а полученный остаток экстрагируют хлороформом (400 мл). Полученный экстракт сушат и концентрируют в вакууме,а полученный продукт очищают на хроматографической колонке с силикагелем (растворитель- хлороформ) , в результате чего получают сложный эфир циклобранил-пара-аце- токсибензоата (44,1 г), выход 92%, т.пл. 192-193°С. 2г
Удельное вращение cij + 55,5° (с 0,93, CHClj).
Вычислено, %: С 79,69; Н .
С40Н560 |. (мол.м. 602-86)
Найдено, %: С 79,61; Н 9,79.
ИК (КВг)} , см- : 2920, 2850, 1765, 1715, 1270, 1190, 1160, 1115.
ПМР (CDC1),S : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,60 (1Н, 1/2 АВ кв., 4,8 Гц); 0,68-2,40 (27Н, м); 0,89 (6Н, с); 0,96 (ЗН, с); 1,01 (ЗН, с); 1,60 (9Н, с); 2,28 (ЗН, с); 4,60-5,00 (1Н, м); 6,96-7,32 (2Н, м) 7,90-8,25 (2Н,м).
б) Получение циклобранил-пара- оксибензоата.
Циклобранил-пара-ацетоксибензоат (24 г, 0,0398 моль), полученный на стадии а, растворяют в тетрагидро45 фуране (350 мл) и добавляют 25%-ный водный аммиак (50 мл). Полученную смесь продолжают перемешивать при 40|JC в течение 1 ч, а затем выпаривают досуха при пониженном давлении.
50 Оставшиеся кристаллы перекристалли- зовывают из этанола, в результате чего получают циклобранил-пара-ок- сибензоат (21,0 г) с выходом 94%, т.пл. 174-175 С.
55 Удельное вращение VJjj + 57,7 (с 1,10, СНС1Э).
Вычислено, %: С 79,16; Н 10,30. С38 Н56 0} СгН5ОН(мол.м. 606,9)
выпаривают при пониженном давлении,
20
5
0
5
0
а полученный остаток экстрагируют хлороформом (400 мл). Полученный экстракт сушат и концентрируют в вакууме,а полученный продукт очищают на хроматографической колонке с силикагелем (растворитель- хлороформ) , в результате чего получают сложный эфир циклобранил-пара-аце- токсибензоата (44,1 г), выход 92%, т.пл. 192-193°С. 2г
Удельное вращение cij + 55,5° (с 0,93, CHClj).
Вычислено, %: С 79,69; Н .
С40Н560 |. (мол.м. 602-86)
Найдено, %: С 79,61; Н 9,79.
ИК (КВг)} , см- : 2920, 2850, 1765, 1715, 1270, 1190, 1160, 1115.
ПМР (CDC1),S : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,60 (1Н, 1/2 АВ кв., 4,8 Гц); 0,68-2,40 (27Н, м); 0,89 (6Н, с); 0,96 (ЗН, с); 1,01 (ЗН, с); 1,60 (9Н, с); 2,28 (ЗН, с); 4,60-5,00 (1Н, м); 6,96-7,32 (2Н, м); 7,90-8,25 (2Н,м).
б) Получение циклобранил-пара- оксибензоата.
Циклобранил-пара-ацетоксибензоат (24 г, 0,0398 моль), полученный на стадии а, растворяют в тетрагидрофуране (350 мл) и добавляют 25%-ный водный аммиак (50 мл). Полученную смесь продолжают перемешивать при 40|JC в течение 1 ч, а затем выпаривают досуха при пониженном давлении.
Оставшиеся кристаллы перекристалли- зовывают из этанола, в результате чего получают циклобранил-пара-ок- сибензоат (21,0 г) с выходом 94%, т.пл. 174-175 С.
Удельное вращение VJjj + 57,7 (с 1,10, СНС1Э).
Вычислено, %: С 79,16; Н 10,30. С38 Н56 0} СгН5ОН(мол.м. 606,9)
23
Найдено, %: С 79,13; Н 10,42.
ИК (КВг)} , 3400, 2920, 2850, 1685, 1610, 1280, 1160.
IMP (CDC1,),5 : 0,38(1H,1/2AB кв., 4,8 Гц); 0,64 (1Н, 1/2 АВ кв., 4,8 Гц); 0,70-2,24 (27Н, м); 0,91 (6Н, с); 0,98 (ЗН, с); 1,02 (ЗН, с); 1,28 (ЗН, т, 7,2 Гц); 1,62 (9Н, с); 3,77 (2Н, кв., 7,2 Гц); 4,60-5,00 (1Н, м); 6,72-7,18 (4Н, м); 7,80- 8,12 (2Н, м).
Прим ер 16. Циклоартенил-3- этокси-4-гидроксибензоат.
а)Получение циклоартенил-й-аце- токси-3-этоксибензоата.
Предлагаемое соединение подучают по примеру 8а, где 4-ацетокси-З- этоксибензойную кислоту (13,9 г, 0,062 моль) используют вместо 4-аце- токси-3-метоксибензойной кислоты (13,0 г). Получают циклоартенил-4- ацетокси-3-этокси-бензоат г (выход 82%), т.пп. 140-141°С.
Удельное вращение Г +58,2 (с 1,00, СНС13).
Вычислено, %: С 77,80; Н 9,56.
с инбо°5 (мол.м. 632,89)
Найдено, %: С 77,91; Н 9,43,
б)Получение циклоартенил-З-эток- си-4-оксибензоата.
Циклоартенил-4-ацетокс71-,3--этокси бензоат (30 г, 0,047 моль), получен-; ный на стадии а, растворяют в тетра- гидрофуране (300 мл), и к полученной смеси добавляют 25%-ный водный аммиак (60 мл). Затем смесь перемешивают при 50 С в течение 2 ч и выпаривают досуха при пониженном давлении. Оставшиеся кристаллы пере- кристаллизовывают из смеси ацетона и воды (2:1, объем/объем), в результате чего получают сложный эфир цик- лоартенил-3-этокси-4-оксибензоата (20,5 г), выход 74%, т.пл. 128-130°С.
Удельное вращение СсО + 59,5° (с 1,00, СНС1Э).
Вычислено, %: С 79,27; Н 9,89.
C39Hse°4 (мол.м. 530,85)
Найдено, %: С 79,21; Н 9,82.
П р и м е р 17. Циклобранял-3- этокси-4-гидроксибензоат.
а) Получение циклобранил-4-аце- токси-3-этоксибензоата.
Предлагаемое соединение получают по примеру 8а, где 4-ацетокси-З- этгксибензойную кислоту (13,9 г, 0,062 моль) и циклобранол (20,0 г, 0,045 моль) используют вместо 4-аце
153889224
токси-3-метоксибензойной кислоты (13,0 г) и циклоартенола (20,0 г). Получают 23,4 г циклобранил-4-аце- . токси-3-метоксибензоата с выходом 80%, т.пл. 161-162°C.
Удельное вращение + 56,5° (с 1,00, CHClj).
Вычислено, %: С 77,97; Н 9,66. 10 с4-гн&г°5 (мол.м. 646,92)
Найдено, %: С 78,05; Н 9,61. б) Получение циклобранил-3-эток- си-4-оксибензоата.
Циклобранил-4-ацетокси-З-этокси- 15 бензоат (30 г, 0,046 моль), полученный на стадии а, растворяют в тет- рагидрофуране (300 мл) и к полученной смеси добавляют 25%-ный водный аммиак (60 мл). После перемешивания 20 при 50 С в течение 3 ч смесь выпаривают досуха при пониженном давлении, а кристаллы остатка перекрис- таллизовывают из смеси ацетона и воды (2:1, объем/объем), в результате 25 чего получают циклоартенил-3-этокси- 4-оксибензоат (20,8 г), с выходом 74%, т.пл. 175-176 С.
Удельное вращение + 57,5й (с 1,00, СНС13)
30 Вычислено, %: С 79,42; Н 10,00. С4.оН60°4 (моЪ.м. 604,88)
Найдено, %: С Н 10,12.
Пример 18. Циклобранил-3- этокси-4-гидроксициннамат.
а) Получение циклобранил-4-аце- токси-3-этоксициннамата.
К 4-ацетокси-З-этоксикоричной кислоте (27,0 г, 0,108 моль), суспен- ,„ дированной в 200 мл толуола, добавляют тионилхлорид (16,3 мл, 3 экв) и перемешивают при 60°С в течение 2 ч. Затем смесь выпаривают при пониженном давлении, а остаток суспендируют в толуоле (150 мл) и пиридине (30 мл). К суспензии добавляют циклобранол, и полученную смесь перемешивают при 60°С в течение 2 ч. После завершения реакции смесь выпаривают досуха при пониженном давле- 50 нии, а остаток экстрагируют 300 мл хлороформа. Полученный экстракт промывают, сушат и выпаривают досуха при пониженном давлении. Оставшиеся кристаллы перекристаллизовывают из этанола, в результате чего получают циклобранил-4-ацетокси-З-этоксицин- намат (43,1 г), выход 85%, т.пл.153- 154°С.
45
to
25153S892
Удельное вращение + 37,0 (с 1,00, СНС1,).
Вычислено, %: С 78,38; Н 9,48.
С4знбг°5- (мол-м- 658,93)
Найдено, %: С 78,44; Н 9,43.
б) получение циклобранил-3-эток- си-4-оксициннамата.
Циклобранил-4-ацетокси-З-этокси- циннамат (30,9 г, 0,046 моль), полученный на стадии а, растворяют в 300 мл тетрагидрофурана, затем добавляют 25%-ный водный аммиак (60мл) Полученную смесь перемешивают при 50 С в течение 2 ч. После завершения реакции смесь выпаривают досуха при пониженном давлении, а оставшиеся кристаллы перекристаллизовывают из смеси ацетона и воды (2:1, объем/объем) , в результате чего получают 22,8 г циклобранил-З-этокси-4- оксициннамата (выход 78%), т.п.181- 182°С.
Удельное вращение + 38,0° (с 1,00, СНСЦ).
Вычислено, %: С 79,95; Н 9,91.
С4гН6204 (мол.м. 630,92)
Найдено, %: С 79,91; Н 9,98.
П р им ер 19. Получение цикло- артенил-4-гидрокси-З-п-пропоксицин- намата.
Указанное соединение получают по примеру 18 а-б, используя циклоар- тенол, 4-ацетокси-З-п-пропоксикорич- ную кислоту, получая циклоартенил-426
К 4-ацетокси-З-метоксикоричной кислоте (26,5 г, 0,112 моль), суспе дированной в 200 мл толуола, добав- ляют тионилхлорид (16,3 мл, 3 экв.) и перемешивают при 60°С в течение 2 ч. Затем смесь выпаривают при пониженном давлении, а остаток суспен дируют в толуоле (150 мл) и пиридине (30 мл). К суспензии добавляют циклобранол, и полученную смеь пере мешивают при в течение 2, ч. После завершения реакции полученную смесь выпаривают досуха при пони- 5 женном давлении, а остаток экстрагируют 300 мл хлороформа. Полученный экстракт промывают, сушат и выпаривают досуха при пониженном давлении. Оставшиеся кристаллы пере- 20 кристаллизовывают из этанола, в результате чего получают циклобранил- 4-ацетокси-З-метоксициннамат (44,9 г выход 91%, т.пл. 175-176°С.
Удельное вращение оО +37 25 (с 1,00, CHClj).
Вычислено, %: С 78,38; Н 9,48. С4 нег05 (мол.м. 658,93) Найдено, %: С 78,44; Н 9,43. б) Получение циклобранил-4-окси- 30 3-метоксициннамата.
Циклобранил-4-ацетокси-З-метокси циннамат (44,9 г, 0,068 моль), полученный на стадии а, растворяют в 900 мл диоксана и к этому раствору добавляют 25%-ный водный аммиак
ацетокси-3-п-пропоксициннамата, ко- (90 мл) по каплям. Затем полученную торый в количестве 31,0 г(0,046 моль)смесь перемешивают при 50 С в течеобрабатывают по методике примера 186, ние 2 ч раствор выпаривают досуха выход 20,5 г (70%), т.пл.144-145°С.
при пониженном давлении. Оставшиеся кристллы промывают этанолом, в результате чего получают циклобранил- 4-окси-З-метоксициннамат (40,0 г), выход 95,2%, т.пл. 191-192°С.
Удельное вращение oi + 40,2 (с 1,00, СНС13).
Вычислено, %: С 79,95; Н 9,91.
С4гнбг.°4 (мол.м. 630,92)
Найдено, %: С 79,99; Н 9,85.
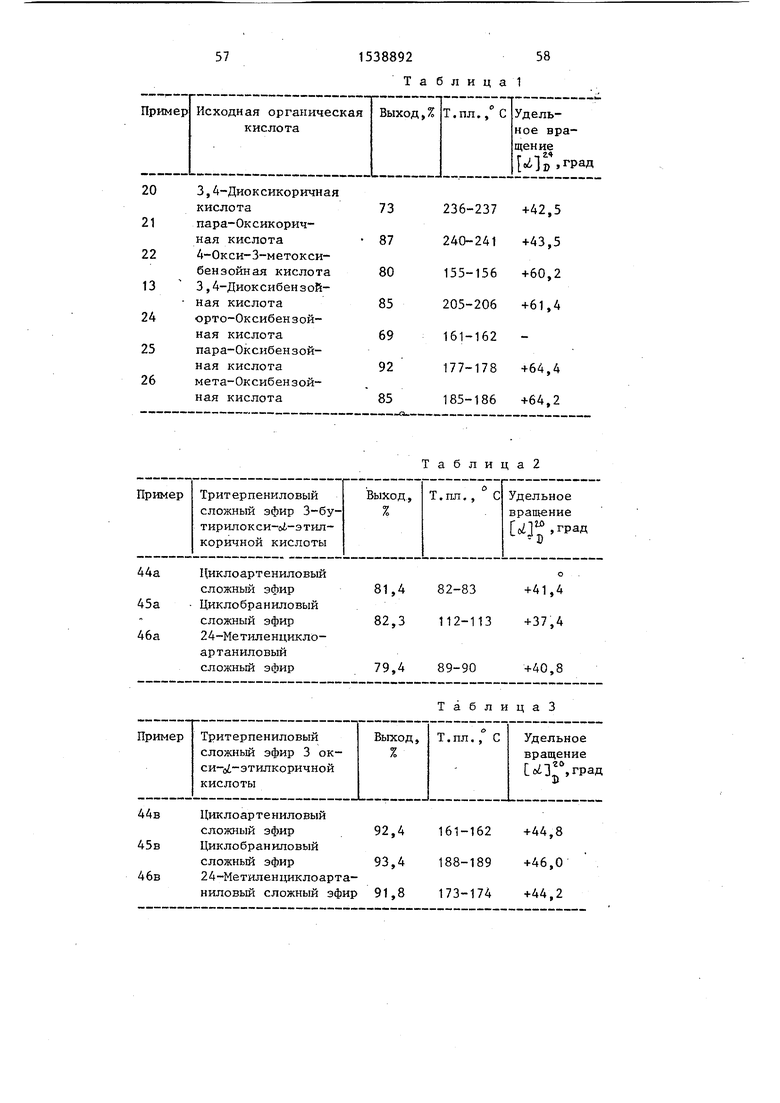
П р и м е р ы 20-26. Сложные эфи- ры 24-метиленциклоартанола в примерах 20-26 получают по способу, описанному ранее для циклобранолов. В этих способах используют вместо цик- лобранола те же самые количества (в молях) 24-метиленциклоартанола. Выходы, температуры плавления и удельные вращения (с 1,00, СНС1) этих соединений приведены в табл. 1.
40
45
50
при пониженном давлении. Оставшиеся кристллы промывают этанолом, в результате чего получают циклобранил- 4-окси-З-метоксициннамат (40,0 г), выход 95,2%, т.пл. 191-192°С.
Удельное вращение + 38,5 (с 0,99, СНС1,). Ъ
Вычислено, %: С 79,82; Н 9,80.
C4,HU04 (мол.м. 616,89)
Найдено, %: С 79,77; Н 9,83.
ИК (КВг)$ , см- : 3500, 2920, 2850, 1690,1 1600, 1510, 1265, 1155.
ПНР (CDC1,), Ј : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,60 (1Н, 1/2 АВ кв., 4,8 Гц); 0,68-2,20 (27Н, м); 0,89 (6Н, с); 0,96 (6Н, с); 1,62 (9Н, с;; 3,90 (ЗН, с); 4,50-4,90
Пример 27. Циклобранил-4-гид-55(1Н, м); 5,97 (1Н, ш.с.); 6,27
рокси-3-метоксициннамат.(1Н, 1/2 АВ кв., 15,6 Гц); 6,75-7,20
а) Получение циклобранил-4-аце-(ЗН, м); 7,9 (1Н, 1/2 АВ кв.,
токси-3-метоксициннамата.15,6 Гц).
2
26
К 4-ацетокси-З-метоксикоричной кислоте (26,5 г, 0,112 моль), суспендированной в 200 мл толуола, добав- ляют тионилхлорид (16,3 мл, 3 экв.), и перемешивают при 60°С в течение 2 ч. Затем смесь выпаривают при пониженном давлении, а остаток суспендируют в толуоле (150 мл) и пиридине (30 мл). К суспензии добавляют циклобранол, и полученную смеь перемешивают при в течение 2, ч. После завершения реакции полученную смесь выпаривают досуха при пони- женном давлении, а остаток экстрагируют 300 мл хлороформа. Полученный экстракт промывают, сушат и выпаривают досуха при пониженном давлении. Оставшиеся кристаллы пере- кристаллизовывают из этанола, в результате чего получают циклобранил- 4-ацетокси-З-метоксициннамат (44,9 г) , выход 91%, т.пл. 175-176°С.
Удельное вращение оО +37 (с 1,00, CHClj).
Вычислено, %: С 78,38; Н 9,48. С4 нег05 (мол.м. 658,93) Найдено, %: С 78,44; Н 9,43. б) Получение циклобранил-4-окси- 3-метоксициннамата.
Циклобранил-4-ацетокси-З-метокси- циннамат (44,9 г, 0,068 моль), полученный на стадии а, растворяют в 900 мл диоксана и к этому раствору добавляют 25%-ный водный аммиак
(90 мл) по каплям. Затем полученную смесь перемешивают при 50 С в течение 2 ч раствор выпаривают досуха
при пониженном давлении. Оставшиеся кристллы промывают этанолом, в результате чего получают циклобранил- 4-окси-З-метоксициннамат (40,0 г), выход 95,2%, т.пл. 191-192°С.
Удельное вращение + 38,5 (с 0,99, СНС1,). Ъ
Вычислено, %: С 79,82; Н 9,80.
C4,HU04 (мол.м. 616,89)
Найдено, %: С 79,77; Н 9,83.
ИК (КВг)$ , см- : 3500, 2920, 2850, 1690,1 1600, 1510, 1265, 1155.
ПНР (CDC1,), Ј : 0,36 (1Н, 1/2 АВ кв., 4,8 Гц); 0,60 (1Н, 1/2 АВ кв., 4,8 Гц); 0,68-2,20 (27Н, м); 0,89 (6Н, с); 0,96 (6Н, с); 1,62 (9Н, с;; 3,90 (ЗН, с); 4,50-4,90
(1Н, м); 5,97 (1Н, ш.с.); 6,27
2715
П р и м е р 28. Циклоартеяиловый сложный эфир 4-гидрокси-3-метокси-оЈ метилкоричной кислоты.
. а) Получение циклоартенилового сложного эфира З-метокси-4-пропио- нилокси-0Ј-метилкоричной кислоты.
К 3-метокси-4-пропионшгокси-оЈ-ме- тилкоричной кислоте (72,0 г, 0,272 моль) добавляют тионилклорид (40,0 мл, 2 экв.), толуол (400 мл) и диметилформамид (0,5 мл), и полу-. ченную смесь перемешивают при в течение 1,5 ч. После концентрирования при пониженном давлении ..к смеси добавляют диоксан (100 мл) и перемешивают при ОС. К этой смеси добавляют циклоартенол (80,0 г, 0,187 моль), растворенный в пиридине (300 мл), и перемешивают при 60 С в течение 3 ч. Реакционную смесь выпаривают при пониженном давлении, а остаток растворяют в хлороформе (800 мл). Полученный раствор промывают насыщенным водным NaHCO, a водный слой экстрагируют хлороформом (500 мл х 2). Объединенные хлороформ ные слои сушат и выпаривают при пониженном давлении, а остаток очищают на хроматографической колонке с силикагелем (растворитель- смесь гею сан:метиленхлорид 5:19 объем/объем), в результате чего получают циклоар- тениловый сложный эфир З-метокси-4- пропионилокси- -метилкоричноч кислоты (110 г), выход 87,1%,, т.пл.130- 131°С.
Удельное вращение °0 + 41,4° (с 1,00, СНС13).
Вычислено, %: С 78,53; Н 9,59.
(мол.м. 672,9Ь)
Найдено, %: С 78,59; Н 9S52.
ИК (КВгИ , : 2920., 2850, 1765, 1710, 1630,-1600, 1510, 1240, 1140, 1110.
ПМР (CDC1,), S : 0,39 (1Н, 1/2 АВ кв., 4,2 Гц); 0,60 (1Н, 1/2АВкв. 4,2 Гц); 0,60-2,20 (27Н, м); 0,90
(6Н, с); 0,98 (6Н,с); 1,27 (ЗН, т,
7,2 Гц); 1,58 (ЗН,ш.с), 1,68 (ЗН,,.
ш.с), 2,12 (ЗН, д,1,2 Гц); 2,62
(2Н, кв., 7,2 Гц);3,80 (ЗН, с);
4,50-5,30 (2Н, м);6,80-7,70 (4Н, м)
б) Получение циклоартенилового сложного эфира 4-окси-З-метокси- - метилкоричной кислоты (циклоартени- ловый сложный эфир-йб- метилферуло- вой кислоты). .
5
0
92
5
0
5
0
5
0
5
28
К циклоартениловому сложному эфиру 3-метокси-4-пропионилокси- Ј- метилкоричной кислоты (84,0 г, 0,125 моль), полученному на стадии а, растворенному в диоксане (1000мл), добавляют 25%-ный водный аммиак (200 мл), и полученный раствор перемешивают при 50°С в течение 2 ч. Затем реакционную смесь концентрируют при пониженном давлении до удаления растворителя, а остаток растворяют в хлороформе. Полученный хлороформный раствор промывают насыщенным солевым раствором (500 мл), и водный слой экстрагируют хлороформом (300 мл х 2), объединенные хлороформные слои сушат, концентрируют при пониженном давлении, а остаток перекристаллизовывают из смеси ме- тиленхлорида и метанола (1:4, объем/объем) , в результате чего получают циклоартениловый сложный эфир 4-окси-З-метокси-об-метилкоричной кислоты (73s,0 г), выход 94,8%, т.пл. 143- 144°С.
Удельное вращение «О +44,1° (с 1,00, СНС13). i Вычислено, %: С 79,82; Н 9,80.
С41 (мол. м. 616,93)
Найдено, %: € 79,88; Н 9,81.
ИК (КВгН , 3400, 2900, 2850, 1695, 1690, 1625, 1600, 1510, 1250, 1110.
ПМР (CDC14),S : 0,38 (1Н, 1/2 АВ кв., 4,2 Гц); 0,59 (1Н, 1/2 АВ кв., 4,2 Гц); 0,60-2,30 (27Н,м); 0,88 (6Н, с); 0,97 (6Н, с); 1,60 (ЗН, ш.с.); 1,66 (ЗН, ш.с.); 2,12 (ЗН, д, 1,2 Гц); 3,88 (ЗН, с); 4,50-5,30 (2Н, м); 5,80 (1Н, ш.с.); 6,70-7,70 (4Н, м).
Прим ер 29. Цикле бран иловый эфир 4-гидрокси-3-метокси-«Ј-метил- коричной кислоты.
а) Получение циклобранилового сложного эфира З-метокси-4-пропи- онилокси-ц -метилкоричной кислоты.
К З-метокси-4-пропионилокси-,- метилкоричной кислоте (15,59 г, 0S059 моль), суспендированной в 50 мл толуола, добавляют 50 мл тио- нилхлорида (20 мл, 4,5 экв.) и ди метилформамиц (5 капель), и полученную смесь перемешивают при 60 С в течение 2 ч. Затем растворитель отгоняют перегонкой при пониженном давлении. Остаток суспендируют в 150 мл толуола и 30 мл безводноголиплдина,и к
291538892
этой суспензии добавляют циклобранол (20 г ,0,045 моль) .Полученную смесь перемешивают при 60°С в течение 2 ч,затем концентрируют при пониженном давлении. Остаток экстрагируют хлороформом (300 мл), а хлороформный раствор промывают, сушат и выпаривают досуха при пониженном давлении. Кристаллический остаток промывают этанолом JQ (50 мл) и перекристаллизовывают из смеси ацетона и воды (19:1, объем/объем) , в результате чего получают сложный циклобраниловый эфир 3- метокси-4-пропионилокси-оЈ-метилко- 5 ричной кислоты (24,69 г), выход 79,2%, т.пл. 146-147°С.
Удельное вращение + 39,2°
30
35
(с 1,00, СНС13).
Вычислено, %: С 78,67; Н 9,68. 20
С45Н«.°5- (мол.м. 686,98)
Найдено, %: С 78,75; Н 9,62.
ИК (КВг) } , см 1: 3400, 2950, . 2850, 1760, 1710, 1630, 1600, 1240, 1150, 1120.25
ПМР (CDC14) 8 : 0,37 (1Н, 1/2 АВ кв., 4,8 Гц); 0,62 (1Н, 1/2 АВ кв., 4,8 Гц); 0,70-2,22 (27Н, м); 0,92 (6Н, с); 0,99 (6Н, с); 1,29 (ЗН, т, 7,2 Гц); 1,64 (9Н, с), 2,14 30 (ЗН, д, 1,2 Гц); 2,63 (2Н, кв., 7,2 Гц); 3,84 (ЗН, с); 4,84-4,88 (1Н, м); 6,80-7,08 (ЗН, м); 7,59 (1Н, кв., 1,2 Гц).
б) Получение сложного циклобрани- лового эфира 4-окси-3-метокси-сЈ- метилкоричной кислоты.
Сложный циклобраниловый эфир 3- метокси-4-пропионилокси- -метилко.- ричной кислоты (24,69 г, 0,036 моль), полученный на стадии а, растворяют в 400 мл диоксана, и к полученному раствору добавляют 25%-ный водный аммиак по каплям. Полученную смесь перемешивают при 50°С в течение 2ч, а затем растворитель удаляют перегонкой при пониженном давлении. Кристаллический остаток промывают этанолом и перекристаллизовывают из смеси ацетона и воды (19:1, объем/объем), в результате чего полу- 50 чают циклобраниловый сложный эфир 4-окси-3-метокси-оЈ-метшткоричной кислоты (21,72 г), выход 95%,
т.пл. 185-186°С.
i го
40,
45
Найдено, %: С 79,90; Н 9,98.
ИК (КВг) , см- : 3380, 2920, 2850, 1693, 1600, 1510, 1285, 1250, 1120.
ПМР (CDC13),Ј :0,36(1Н,1/2АВ кв., 4,8 Гц); 0,61 (1Н, 1/2 АВ кв., 4,8 Гц); 0,76-2,30 (27Н, м), 0,91 (6Н, с); 0,99 (6Н, с); 1,63 (9Н, с); 2,14 (ЗН, д, 1,2 Гц); 3,90 (ЗН, с); 4,48-4,84 (1Н, м ); 5,84 (1Н, ш.с); 6,80-6,98 (ЗН, м); 7,55 (1Н,0кв., 1,2 Гц).
П р и м е р 30. 24-Метиленцикло- артаниловый эфир 4-гидрокси-З-меток- C.K-L- метилкоричной кислоты.
а) Получение 24-метиленциклоар- танилового сложного эфира 3-метокси- 4-пропионилокси- -метилкоричной кислоты .
К 3-метокси-4-пропионилокси-оЈ- метилкоричной кислоте (0,8 г, 0,003 моль), суспендированной в 2 мл толуола, добавляют тионилхлорид (0,5 мл, 2,2 экв.) и 2 капли диме- тилформамида, и полученную смесь перемешивают при 60°С в течение 2 ч. Затем растворитель отгоняют перегонкой при пониженном давлении. Остаток суспендируют в толуоле (2 мл) и безводном пиридине (1 мл) и к полученной суспензии добавляют 24-ме- тиленциклоартанил (1 г, 0,0023моль). Полученную смесь перемешивают при 60°С в течение 2 ч, а затем растворитель отгоняют перегонкой при пониженном давлении. Полученный остаток экстрагируют хлороформом 20 мл, и хлороформный экстракт промывают бикарбонатом натрия, сушат и выпаривают при пониженном давлении. Кристаллический остаток промывают этанолом (5 мл) и перекристаллиэовы- вают из смеси ацетона и метанола (1:1, объем/объем), в результате чего получают 24-метиленциклоартанило- вый сложный эфир З-метокси-4-пропи- онилокси- -метилкоричной кислоты (1,35 г), выход 86,6, т.пл. 134-135°С.
Удельное вращение об + 41,2° (с 1,00, СНС13). в
Вычислено, %: С 78,67; Н 9,68.
C46Hfefe°s (мол.м. 686,98)
Удельное вращение (с 1,00, СНС1ОВычислено, %: С 79,95; Н 9,91. C4iH6204 (мол.м. 630,92)
Найдено, %: С 78,75; Н 9,62.
ИК (КВг)0 , см-Ч 3400, 2920, Т° +43,7° 55 2850, 1760, 1240, 1115.
ПМР (CDC14),S : 0,36(1H,1/2AB кв., 4,2 Гц); 0,61 (1Н, 1/2 АВ кв., 4,2 Гц); 0,70-2,22 (34Н, м); 0,88
30
Q 5
5
0
5
0
0
0,
5
Найдено, %: С 79,90; Н 9,98.
ИК (КВг) , см- : 3380, 2920, 2850, 1693, 1600, 1510, 1285, 1250, 1120.
ПМР (CDC13),Ј :0,36(1Н,1/2АВ кв., 4,8 Гц); 0,61 (1Н, 1/2 АВ кв., 4,8 Гц); 0,76-2,30 (27Н, м), 0,91 (6Н, с); 0,99 (6Н, с); 1,63 (9Н, с); 2,14 (ЗН, д, 1,2 Гц); 3,90 (ЗН, с); 4,48-4,84 (1Н, м ); 5,84 (1Н, ш.с); 6,80-6,98 (ЗН, м); 7,55 (1Н,0кв., 1,2 Гц).
П р и м е р 30. 24-Метиленцикло- артаниловый эфир 4-гидрокси-З-меток- C.K-L- метилкоричной кислоты.
а) Получение 24-метиленциклоар- танилового сложного эфира 3-метокси- 4-пропионилокси- -метилкоричной кислоты .
К 3-метокси-4-пропионилокси-оЈ- метилкоричной кислоте (0,8 г, 0,003 моль), суспендированной в 2 мл толуола, добавляют тионилхлорид (0,5 мл, 2,2 экв.) и 2 капли диме- тилформамида, и полученную смесь перемешивают при 60°С в течение 2 ч. Затем растворитель отгоняют перегонкой при пониженном давлении. Остаток суспендируют в толуоле (2 мл) и безводном пиридине (1 мл) и к полученной суспензии добавляют 24-ме- тиленциклоартанил (1 г, 0,0023моль). Полученную смесь перемешивают при 60°С в течение 2 ч, а затем растворитель отгоняют перегонкой при пониженном давлении. Полученный остаток экстрагируют хлороформом 20 мл, и хлороформный экстракт промывают бикарбонатом натрия, сушат и выпаривают при пониженном давлении. Кристаллический остаток промывают этанолом (5 мл) и перекристаллиэовы- вают из смеси ацетона и метанола (1:1, объем/объем), в результате чего получают 24-метиленциклоартанило- вый сложный эфир З-метокси-4-пропи- онилокси- -метилкоричной кислоты (1,35 г), выход 86,6, т.пл. 134-135°С.
Удельное вращение об + 41,2° (с 1,00, СНС13). в
Вычислено, %: С 78,67; Н 9,68.
C46Hfefe°s (мол.м. 686,98)
Найдено, %: С 78,75; Н 9,62.
311
(6Н, с); 0,96 (6Н, с); 1,26 (ЗН, м, 7,2 Гц); 2,11 (ЗН, д, 1,2 Гц); 2,60 (2Н, кв., 7,2 Гц); 3,80 (ЗН, с); 4,44-4,86 (1HS м); 4,86-5,26 (2Н, м 6,76-7,08 (ЗН, м); 7,55 (1Н, кв., 1,2 Гц).
б) Получение 24-метиленциклоарта нилового сложного эфира 4-окси-З-ме токси-оЈ-метилкоричной кислоты.
24-Метиленциклоартаниловый сложный эфир З-метокси-4-пропионилокси,-метилкоричной кислоты (1,35 г, 0,002 моль), полученный на стадии а растворяют вч диоксане (20 мл) $ и к этому раствору добавляют 25%-ный воный аммиак (2 мл) по каплям. Полученую смесь перемешивают при 50 С в тчение 2ч, затем растворитель отгоняют при пониженном давлении. Кристаллический остаток промывают этанолом и перекристаллизовывают из этанола, в результате чего получают сложный 24-метиленциклоартаниловый эфир 4- окси-3-метокси-«;-метилкоричной кислоты (1,02 г), выход 82,2%,т.пл.144145 с г 41
Удельное вращение I J (с 1,00, СНС13).
Вычислено, %: С 79В95; Н 9,91
D
44,8е
С43н&г.°4 (мол.м. 630,92)
Найдено, %: С 79,99; Н 9,84.
ИК (КВг) $ , см-( : 3400., 2900, 2850, 1690, 1600, 1510, 1250, 1110.
ПМР (CDC13)В : 0,37 (1Н, 1/2 АВ кв.,. 4,2 Гц); 0,61 (1Н 1/2АВкв. 4,2 Гц); 0,70-2,21 (34Н, м); 0,89 (6Н, с); 0,98 (6Н, с), 2,14 (ЗН, д, 1,2 Гц); 3,88 (ЗН, с); 4,50-4,88 (1Н, м); 4,88-5,28 (2Н} м); 5980 (1Н, ш.с); 6,82-7,10 (ЗН5 м), 7,59 (1Н, кв., 1,2 Гц).
Прим ер 31. Циклоартениловый эфир 4-гидрокси-3-метокси-т(-зтш1Ко- ричной кислоты.
а) Получение циклоартенилового сложного эфира 4-бутирилокси-З-ме- токси-4Ј-этилкоричной кислоты.
Тионилхлорид (15,0 мл, 3,3 экв.) по каплям добавляют к раствору 4- бутирилокси-3-метокси-оЈ-этилкорич- ной кислоты (18,0 г, 0,062 моль) в бензоле (40 мл) при 0°С, и полученную смесь нагревают до 60°С и оставляют при перемешивании в течение 2 ч. Затем избыток тионилхлори- да я растворитель удаляют перегонкой при пониженном давлении. 10 мл пиридина и 40 мл диоксана добавля
32
ют к остатку. При охлаждении смеси при 0°С по каплям добавляют к ней раствор циклоартенола (17,5 г, 0,041 моль) в пиридине (30 мл). Эту реакционную смесь оставляют при перемешивании при 20°С. Затем растворитель отгоняют при перегонке при пониженном давлении. Остаток экст- рагируют хлороформом (200 мл) и полученный экстракт концентрируют в вакууме. Остаток перекристаллизовывают из смеси ацетона и метанола (1:1, объем/объем), в результате че- 5 го получают циклоартениловый сложный эфир 4-бутирилокси-З-метокси- - этилкоричной кислоты (22,4 г) выход 77,9%, т.пл. 118,5-119,5°С.
Удельное вращение + 35,7° 0 (с ,1,00, СНС1,).
Вычислено, %: С 78,81; Н 9,78.
С44н&в°5 (мол.м. 701,00) р Найдено, %: С 78,72; Н 9,86.
ИК(КВг) } см( : 3400, 2920, 280Q, 5 1700, 1600, 1510, 1230, 1120.
ПМР (CDC1),S : 0,36(1H,1/2AB кв., 4,2 Гц); 0,52-2,26 (29Н, м); 0,61 (1Н, 1/2 АВ кв., 4,2 Гц); 0,90 (6Н, с); 0,96 (6Н, с); 1,04 (ЗН, т, 0 7,2 Гц); 1,18 (ЗН, т, 7,2 Гц); 1,60 (ЗН, с); 1,66 (ЗН, с); 2,26-2,82 (4Н, м); 3,79 (ЗН, с); 4,50-4,88 (1Н, м); 4,88-5,28 1Н, м); 6,70- 7,12 (ЗН, м); 7,48-7,68 (1Н, м).
б) Получение циклоартенилового сложного эфира 4-окси-3-метокси- - этилкоричной кислоты.
Циклоартениловый сложный эфир 4-бутирилокси-3-метокси оЈ-этилко- ричной кислоты (22,0 г, 0,0314 моль), полученный на стадии а, растворяют в диоксане (200 мл), и к полученному раствору добавляют 25%-ный водный аммиак (20 мл) по каплям. Получен5
0
ную смесь нагревают при 50 С в те
чение 5 ч. Затем растворитель удаляют перегонкой при пониженном давлении. Остаток экстрагируют хлороформом (200 мл), и полученный экстракт концентрируют в вакууме. Остаток перекристаллизовывают из смеси ацетона и метанола (1:1, объем/объем) , в результате чего получают циклоартениловый сложный эфир 4-ок- си-3-метокси-с4-этилкоричной кислоты (17,2 г), выход 86,8%, т.пл.136- 137 С.
Удельное вращение ci + 41,5°
(с 1,00, СНС15).
D
331
Вычислено, %: С 79,95; Н 9,96.
С«.Н62.°4 (мол.м. 630,92)
Найдено, %: С 79,90; Н 9,83.
ИК (КВгН , см. 1: 3400, 2830, 1700, 1595, 1510, 1240, 1120.
ПНР (CDC1,),S: 0,35(1H,1/2AB кв 4,2 Гц); 0,50-2,18 (27Н, м); 0,60 (1Н, 1/2 АВ кв., 4,2 Гц); 0,89 (6Н, с); 0,95 (6Н„ с), 1,19 (ЗН, т, 7,2 Гц); 1,57 (ЗН, с); 1,65 (ЗН, с) 2,56 (2Н, ш, с, кв., 7,2 Гц), 3,87 (ЗН, с); 4,47-4,85 (1Н, м); 4,85- 5,24 (1Н, м), 5,76 (1Н, ш.с); 6,96- 7,09 (ЗН, м); 7,24-7,64 (1Н, м).
. Прим ер 32. Циклоартениловый эфир 4-гидрокси- 5б-метилкоричной кислоты.
а) Получение циклоартенилового сложного эфира 4-пропионилокси- - метилкоричной кислоты.
Тйонилхлорид (18,1 мл 3,3 экв.) и диметилформамид (0,5 мл) добавляют по каплям к раствору 4-пропи- онилокси- -метилкоричной кислоты
(17,6 г, 0,075 моль) в бензоле (40 мл) при 0°С. Полученную смесь нагревают до 60°С и оставляют при перемешивании в течение 2 ч. Затем избыток тионилхлорида и растворитель удаляют перегонкой при пониженном давлении. К остатку добавляют 40 мл диоксана и 10 мл пиридина. При охлаждении смеси при 04С по каплям добавляют раствор циклоартенола (21,3 г 0,050 моль) в пиридине (40 мл). Реакционную смесь нагревают до 20°С и оставляют при перемешивании на ночь. Затем растворитель отгоняют пр пониженном давлении, а остаток экстрагируют хлороформом (200 мл). Полученный экстракт концентрируют при пониженном давлении, а остаток пе- рекристаллизовывают из смеси ацетона и этанола (1:2, объем/объем), и в результате чего получают циклоар- тениловый сложный эфир 4-пропионил- окси- -метилкоричной кислоты (27,0 г) выход 38,9%, т.пл. 87-88°С.
Удельное вращение 45,9 (с 1,00, СНС1,).
Вычислено, %: С 80,33; Н 9,72.
.°4 (мол.м. 642,93)
Найдено, %: С 80,31; Н 9,79.
ИК (КВг) $ , см 1: 3400, 2920, 2850, 1760, 1700, 1260, 1215, 1115,
ПНР (CDC13),& : 0,36(1Н,1/2АВ, 4,2 Гц); 0,52-2,20 (27Н, м); 0,61 (1Н, 1/2 АВ кв., 4,2 Гц); 0,89
34
0
(6Н, с), 0,97 6Н, с); 1,25 (ЗН, т, 7,2 Гц); 1,57 (ЗН, с); 1,65 (ЗН, с); 2,10 (ЗН, д, 1,2 Гц); 2,58 (2Н, , кв., 7,2 Гц); 4,28-4,84 (1Н, м);
4,92-5,24 (1Н, м); 6,92-7,09 (2Н,м); 7,11-7,50 (2Н, м); 7,50-7,70 (1Н,м).
б) Получение циклоартенилового сложного эфира 4-окси- -метилкорич- ной кислоты.
Циклоартениловый сложный эфир 4- пропионилокси-аЈ-метилкоричнойа кислоты (27,0 г, 0,042 моль), полученный на стадии а, растворяют в диок- 5 сане (200 мл), и к этому раствору добавляют 25%-ный водный аммиак по каплям. Полученную смесь нагревают до 50°С и оставляют при перемешивании в течение 2 ч. Затем растворитель отгоняют при пониженном давлении, остаток экстрагируют хлороформом (200 мл). Полученный экстракт концентрируют в вакууме, а остаток перекристаллизовывают из этанола, в результате чего получают Циклоартениловый сложный эфир 4-окси-0Ј- метилкоричной кислоты (20,5 г), выход (83,1%), т.пл. 190-191 0.
Удельное вращение 31 + 45,8 (с 1,00, СНС1).
Вычислено, %: С 81,86; Н 9,96.
C HsfcO, (мол.м. 586,86)
0
5
0
0
5
0
5
Найдено, %; С 81,77; Н 9,99.
, 1
ИК (КВг)З , см-1: 3400, 2992, 5 2985, 1700, 1675, 1600, 1510, 1260,
1200, 1170.
ПНР (CDC13),Ј : 0,36 (1Н, 1/2 АВ кв., 4,2 Гц); 0,52-2,24 (27Н, м); 0,61 (1Н, 1/2 АВ кв., 4,2 Гц); 0,90 (6Н, с); 0,98 (6Н, с); 1,61 (ЗН, с); 1,64 (ЗН, с); 2,13 (ЗН, д, 1,2 Гц); 4,50-4,88 1Н, м); 4-85-5,24 (1Н,м); 5,88-6,60 (1Н, м); 6,68-7,12 (2Н, м); 7,12-7,50 (1Н, м); 7,50-7,68 (1Н, м).
П р и м е р 33. 24-Метиленцикло- артаниловый эфир 4-гидрокси- у/-ме- тилкоричной кислоты.
а) Получение 24-метиленциклоарта- нилового сложного эфира 4-пропионил- окси- -метилкоричной кислоты.
Тйонилхлорид (18,1 мл, 3,3 экв.) и диметилформамид (0,5 мл) по каплям добавляют к раствору 4-пропионилок- си с/-метилкоричной кислоты (17,6 г, 0,075 моль) в бензоле (40 мл) при ОеС. Полученную смесь нагревают до и продолжают перемешивать в течение 2 ч. Затем избыток тионилхлорида и растворитель отгоняют при по3515
ниженном давлении. 20 мл диоксана и 40 мл пиридина добавляют к остатку. При охлаждении смеси при добавляют 24-метиленциклоартанол (0,050 моль), и полученную смесь нагревают до 20°С и продолжают перемешивать в течение ночи. Затем растворитель удаляют перегонкой в вакууме, а полученный остаток экст- рагируют 200 мл хлороформа. Полученный экстракт концентрируют при пониженном давлении, а остаток пере- кристаллизовывают из смеси ацетона и метанола ( 1:1, объем/объем) , в ре- зультате чего получают 24-метилен- циклоартаниловый сложный эфир 4-про- пионилокси-оЈ-метилкоричной кислоты (25,8 г), выход 78,5%, т.пл. 94-95°С
Удельное вращение 1 +34,7° (с 1,00, СНС1,).
Вычислено, %: С 80,44; Н 9,82.
С44.Н64°4 (мол.м. 656,95)
Найдено, %: С 80,39; Н 9,78.
б) Получение 24-метиленциклоар- танилового сложного эфира 4-окси-оЈ- метилкоричной кислоты.
24-Метиленциклоартаниловый сложный эфир 4-пропионилокси- -метилко ричн ой кислоты (24,0 г, 0,036 моль) полученный на стадии а, растворяют в диоксане (200 мл), и к полученному раствору добавляют 25%-ный водный аммиак но каплям. Полученную смесь нагревают при и продолжают перемешивать в течение 2 ч.За- тем растворитель удаляют перегонкой при пониженном давлении, а остаток экстрагируют хлороформом (200 мл). Полученный экстракт концентрируют в вакууме, а остаток перекристаллизо- вывают из смеси ацетона и метанола (1:1, объем/объем) до получения 24- метиленциклоартанилового сложного эфира 4-окси- Ј-метилкоричной кислоты (19,4 г), выход 89,6%, т.пл. 195 196°С.
Удельное вращение З-9 +43,8° (с 1,00, СНС13).
Вычислено, %: С 81,95; Н 10,07. С41нбо°з (мол.м. 600,89) Найдено, %: С 81,90; Н 10,14, Пример 34. Циклоартениловый эфир 4-гидрокси-бЬ-этилкоричной кислоты. , ,
а) Получение циклоартенилового сложного эфира 4-бутирил окси--о6- этилкоричной кислоты.
0
5
о 5 5
0 5
0
36
Тионилхлорид (4,8 мл, 5 экв.) добавляют по каплям к раствору 4- бутирилокси- -этилкоричной кислоты (3,5 г, 0,0133 моль) в бензоле (7 мл) при . Полученную смесь нагревают до 60°С и продолжают перемешивать в течение 2 ч. Затем из- . быток тионилхлорида удаляют перегонкой при пониженном давлении. После добавления 10 мл пиридина к остатку к этой смеси добавляют раствор циклоартенола (2,85 г, 0,0067 моль) в 10 мл пиридина по каплям при 0°С. Смесь нагревают до 20°С и продолжают перемешивать в течение ночи. Затем растворитель удаляют перегонкой при пониженном давлении, а остаток экстрагируют 40 мл хлороформа. Полученный экстракт концентрируют в вакууме, а остаток перекристаллизо- вывают из смеси ацетона и этанола (1:1, объем/объем), в результате чего получают циклоартениловый сложный эфир 4-бутирилокси-о -этилкорич- ной кислоты (3,63 г), выход 80,7%, т.пл. 88-89°С.го
Удельное вращение L + 41,2° (с 1,00, СНС13).
Вычислено, 80,55; Н 9,92.
С45нбь°4 (мол.м. 670-98)
Найдено, %: С 80,64; Н 9,84.
б) Получение циклоартенилового сложного эфира 4-окси-еЈ,-этилкоричной кислоты.
Циклоартениловый сложный эфир 4-бутирилокси-сЈ-этилкоричной кислоты (2,00 г, 0.,003 моль), полученный на стадии а, растворяют в диоксане (20 мл), и к полученному раствору добавляют 25%-ный водный аммиак (2 мл) по каплям. Затем смесь нагревают до 50° С и продолжают перемешивание в течение 5 ч. Растворитель удаляют перегонкой при пониженном давлении, а остаток экстрагируют хлороформом (20 мл). Полученный экстракт концентрируют в вакууме, а остаток перекристаллизовывают из ацетона, в результате чего получают циклоартениловый сложный эфир 4-ок- ,-этилкоричной кислоты (1,68 г), выход 93,2%, т.пл. 162-163°C.
Удельное вращение 46,1° (с 1,00, СНС13).
Вычислено, %: С 81,95; Н 10,07. С-ИН60° (мол.м. 600,89) Найдено, %: С 81,88; Н 10,12.
ИК (KBrH , 3300, 2920, 2800, 1760, 1710, 1625, 1500, 1280, 1240, 1165, 1120.
ПНР (CDC13),S: 0,36(1H,1/2AB кв 4,2 Гц); 0,52-2,22 (27Н, м); 0,61 (1Н, 1/2 АВ кв., 4,2 Гц); 0,90 (6Н, с); 0,96 (6Н, с); 1,19 (ЗН, т, 7,2 Гц); 1,60 (ЗН, с); 1,67 (ЗН,с,) 2,57 (1Н, кв., 7,2 Гц); 4,47-4,88 (1Н, м); 4,92-5,32 (1Н, м); 6,43- 6,77 (1Н, м); 6,68-7,04 (2Н, м); 7,12-7,48 (2Н, м); 7,52-7,69 (1Н,м)
П р и м е р 35. Получение цикло- бранилового сложного эфира 3-эток- си-4-окси- -метилкоричной кислоты.
Указанное соединение получают по примеру 316, однако, в качестве исходного соединения используют ццклобраниловый сложный эфир 3-эток си-4-пропионилокси-,у{-метилкоричной кислоты (21,7 г, 0,031 моль), выход 16,1 г (80,5%), т.пл. 174-175°С.
Удельное вращение г° +42,4° (с 1,00, СНС13).
Вычислено, %: С 80,07; Н 10,00.
(мол.м. 644,94)
Найдено, %: С 80,18; Н 10,05.
Прим ер 36. Получение цикло- артенилового сложного эфира 3-эток- си-4-окси- -пропилкоричной кислоты.
Указанное соединение получают по примеру 316, однако,в качестве исходного материала используют цикло- артениловый сложный эфир 3-этокси- 4-валерилокси-оЈ-пропилкоричной кислоты, выход 16,8 г (72,8%) ,т.шт. 111 112°С.
Удельное вращение + 40,7°
1
(с 1,00, СНС1,).
Вычислено, %: С 80,19; Н 10,10.
СНН&6° + (мол.м. 658,97)
Найдено, %: С 80,26; Н 10,02.
П р и м е р 37. Получение цикло- бранилового сложного эфира 3-этокси 4-окси-оЈ-пропилкоричной кислоты.
Указанное соединение получают по примеру 316, однако в качестве исходного материала используют цикло- браниловый сложный эфир З-этокси-4- валерилокси- -пропилкоричной кислоты (24,2 г, 0,032 моль), выход 16,7 г (72,8%), т.пл. 134-о135°С.
Удельное вращение оОр +37,1° (с 1,00, СНС1}).
Вычислено, %: С 80,31; Н 10,18.
С45Н6Й04 (мол.м. 672,99)
., ; .
10
3889238
Найдено, %: С 80,25; Н 10,24
П р и м е р 38. Получение цикло- артенилового сложного эфира 3-эток- си-4-окси-оЈгбутилкоричной кислоты.
Указанное соединение получают по примеру 316, однако в качестве исходного материала используют цик- лоартениловый сложный эфир 4-капри- локси-3-этокси-об-бутилкоричной кислоты, выход 16,2 г (80,2%), т.пл. 99-100°С.
Удельное вращение oij + 40,0° (с 1,00, СНС1,).
Вычислено, %: С 80,31; Н 10,18.
С45Нбе04 (мол.м. 672,99)
Найдено, %: С 80,21; Н 10,22.
П р и м е р 39. Получение цикло- артенилового сложного эфира 4-окси- 2Q 3-пропокси оЈ-метилкоричной кислоты.
Указанное соединение получают по примеру 316, однако, в качестве исходного материала используют цик- лоартениловый сложный эфир 4-про- 25 пионилокси-3-пропокси- -метилкорич- ной кислоты (23,1 г, 0,033 моль), выход 17,2 г (80,8%), т.пл. 138-139°С..
Удельное вращение + 43,7й (с 1,00, ).
Вычислено, %: С 80,07; Н 10,00.
15
30
C43H6404 (мол.м. 644,94)
35
40
45
Найдено, %: С 80,19; Н 10,04.
П р и м е р 40. Получение цикло- артенилового сложного эфира 4-окси- 3-бутокси-о -метилкоричной кислоты.
Указанное соединение получают по примеру 316, однако, в качестве исходного соединения используют циклоартениловый сложный эфир 4- ггропионилокси-З-бутокси- -метилко- ричной кислоты (22,9 г,0,032 моль) , выход 16,5 г (78%), т.пл. 126-ШаС.
Удельное вращение Г 1 + 39,7° (с 1,00, CHCL,).
Вычислено, %: С 80,19; Н 10,10.
С44Н66°4 (мол.м. 658,97)
Найдено, %: С 80,24; Н 10,03.
П р им е р 41. 24-Метиленцикло- артаниловый сложный эфир 4-окси-З- метокси-оЈ-этилкоричной кислоты.
а) Получение 24-метиленцикло- артанилового сложного эфира 4-бу- тирилокси-3-метокси-оЈ-этилкоричной кислоты.
Тионилхлорид (15,0 мл, 3,3 экв.) 55 по каплям добавляют к раствору 4- бутирилокси-З-метокси-о -этилкорич- ной кислоты (18,0 г, 0,062 моль) в 40 мл бензола при 0°С, а затем по50
39
лученную смесь нагревают при в течение 2 ч. Затем избыток тиснил хлорида и растворитель удаляют перегонкой при пониженном давлении. К остатку добавляют 40 мл пиридина и 40 мл диоксана. При охлаждении смеси при О С добавляют 24-метилен- циклоартанол (18,1 г, 0,041 моль), а затем полученную смесь нагревают до 20°С и оставляют при перемешивании в течение ночи. Растворитель отгоняют при пониженном давлении, а остаток экстрагируют хлороформом (200 мл). Полученный экстракт концентрируют в вакууме, а остаток пе рекристаллизовывают из смеси ацетона и этанола (1:1, объем/объем), в результате чего получают 24-метилен- циклоартаниловый сложный эфир 4-бу- тирилокси-3-метокси-б -этилкоричной кислоты (22,8 г), выход 77„8%, т.пл. 127-128°С.
Удельное вращение tOj, + 33 s 7° (с 1,00, СНС1,).
Вычислено, %: С 78,94; Н 9587. СД7Н70Ог (мол.м. 715,03) Найдено, %: С 78,89; Н 9,88. ИК (КВг) ) , см- : 3400, 2920, 2850, 1760, 1710, 1625, 1510, 1230, 1120.
ПНР (CDCl),Ss 0,36,(1H,1/2AB кв., 4,8 Гц); 0,52-2,22 (29Н, м); 0,61 (1Н, 1/2 АВ кв., 4,8 Гц); 0,92 (6Н, с); 0,97 (6Н, с); 1,03 (ЗН, т, 7,2 Гц); 1,18 (ЗН, т,7,2Гц); 1,60 (9Н, с); 2,22-2,82 (4Н, м); 3,81 (ЗН, с); 4,48-4,90 1Н, м); 6,70-7,18 (ЗН, м); 7,40-7,64 (1Н,м). б) Получение 24-метиленциклоарта- нилового сложного эфира 4-окси-З- метокси- о6 этилкоричной кислоты
24-Метиленциклоартачиловый сложный эфир 4-бутирилокси-3-метокси- - этилкоричной кислоты (21,5 г, 0,0301 моль), полученный на стадии аэ растворяют в диоксане (200 мл) и к полученному раствору добавляют водный аммиак (20 мл) по каплям. Полученную смесь нагревают до 50°С и перемешивают в течение 5 ч. Затем растворитель отгоняют при пониженном давлении, а остаток экстрагируют хлороформом (200 мл), Полученный экстракт концентрируют в вакууме, а остаток перекристалли- зовывают из этанола до получения 24-метиленциклоартанилового сложного эфира 4-окси-2 метокси-тЪ этилко153889240
ричной кислоты (17,3 г), выход 89,1%, т.пл. 137-138°С.
Удельное вращение «Ого + 37,7° 5 (с 1,00, СНС1Э).
Вычислено, %: С 80,07; Н 10,00. (мол.м. 644,94)
Найдено, %: С 80,13; Н 10,12.
ИК (КВг) , 3400, 2930, Ю 1696, 1235, 1130.
ПМР (CDC13),&: 0-,38(1Н,1/2АВкв. 4,8 Гц); 0,52-2,22 (27Н, м)} 0,62 (1Н, 1/2 АВ кв., 4,8 Гц); 0,91 (6Н, с); 0,97 (6Н, с); 1,21 (ЗН, т, 15 7,2 Гц); 1,62 (9Н, с); 2,57 (2Н, ш.с, кв., 7,2 Гц); 3,97 (ЗН, с); 4,48-4,86 (1Н, м); 5,78 (1Н, ш.с); 6,70-7,00 (ЗН, м); 7,53 (1Н, м).
П р им ер 42. Получение цик- 20 лобранилового сложного эфира 4-ок- си-3-пропокси- -этилкоричной кислоты .
Указанное соединение получают по примеру 316, однако, в качестве 25 исходного материала используют
циклобраниловый сложный эфир 4-бу- тирилокси-З-пропокси-о -этилкоричной кислоты (22,1 г, 0,0297 моль) вместо циклоартенилового сложного эфи- 30 ра 4-бутирилокси-3-метокси-оЈ-этил- коричной кислоты, выход 17,8 г (89,1%), т.пл. 140-141аС.
Удельное вращение 3го+ 36,8° (с 1,00 СНС1,).
Вычислено, %: С 80,31; Н 10,18.
35
40
45
50
55
С45Н6804 (мол.м. 672,99) Найдено, %: С 80,36; Н 10,12. П р и м е р 43. Получение 24-метиленциклоартанилового сложного эфира 4-окси-3-пропокси-аЈ-пропилкорич- ной кислоты.
Указанное соединение получают по примеру 316, однако, 24-мети- ленциклоартаниловый сложный эфир 3-проп окси-4-валерилокси- -пропил- коричной кислоты (23,5 г,0,0305моль) используют вместо циклоартенилового сложного эфира 4-бутирилокси-З-ме- токси-оЈ-этилкоричной кислоты.
Выход 17,2 г (82,1%), т.пл.121°С.
Удельное вращение oOiu + 39,1 (с .1S00, CHC13).Ъ
Вычислено, %: С 80,41; Н 10,27.
С4ё Н7о04 (мол.м. 687,02)
Найдено, %: С 80,32; Н 10,34.
Примеры 44-46.
а) Получение циклоартенилового, циклобранилового и 24-метиленциклоВычислено, %: С 80,31; Н 10,18.
5
0
5
0
5
С45Н6804 (мол.м. 672,99) Найдено, %: С 80,36; Н 10,12. П р и м е р 43. Получение 24-метиленциклоартанилового сложного эфира 4-окси-3-пропокси-аЈ-пропилкорич- ной кислоты.
Указанное соединение получают по примеру 316, однако, 24-мети- ленциклоартаниловый сложный эфир 3-проп окси-4-валерилокси- -пропил- коричной кислоты (23,5 г,0,0305моль) используют вместо циклоартенилового сложного эфира 4-бутирилокси-З-ме- токси-оЈ-этилкоричной кислоты.
Выход 17,2 г (82,1%), т.пл.121°С.
Удельное вращение oOiu + 39,1 (с .1S00, CHC13).Ъ
Вычислено, %: С 80,41; Н 10,27.
С4ё Н7о04 (мол.м. 687,02)
Найдено, %: С 80,32; Н 10,34.
Примеры 44-46.
а) Получение циклоартенилового, циклобранилового и 24-метиленцикло4
артанилового сложных эфиров 3-бу- тирилокси-с -этилкоричной кислоты.
Указанные соединения получают по примеру 34а, где в каждом случае используют З-бутирилокси-ji- этилкоричную кислоту (3,50 г, 0,0135 моль) и циклоартенол (2,85 г, 0,0067 моль), циклобранол (2,95 г, 0,0067 моль) и 24-метиленциклоарта- нол (2,95 г, 0,0067 моль) соответственно.
Выход(Температуря плавления и удельное вращение (с 1,00; СНС1Э) каждого из продуктов приведены в табл. 2.
б) Получение циклоартенилового, циклобранилового и 24-метиленцикло- артанилового сложных эфиров 3-окси- ti-a этилкоричной кислоты.
Указанные соединения получают по примеру 346, где используют соединения, полученные на стадии а, (каждого по 0,003 моль).
Выход, температура плавления и удельное вращение (с 1,00,СНС13) каждого продукта приведены в табл.3.
П р и м е р 47. Получение циклоартенилового сложного эфира 4-амино- 3-метоксибензойной кислоты.
4-Ацетамидо-З-метоксибензойную кислоту (6,5 г, 0,031 моль) в диокса не (110 мл) подвергают взаимодействи с тионилхлоридом (21,0 мл), а затем пиридином (0,5 мл) при 20 С. Полученную смесь перемешивают при 50° С в течение 5 мин, затем выпаривают досуха при пониженном давлении, а к остатку добавляют раствор циклоартено- ла (10,0 г, 0,023 моль) в диоксане (50 мл), бензола (50 мл), а затем пиридина (20 мл). Смесь нагревают при 70°С в течение 3 ч, растворитель отгоняют при пониженном давлении. Остаток растворяют в хлороформе (100 мл), и хлороформный раствор промывают насыщенным водным раствором бикарбоната натрия. Водный раствор экстрагируют хлороформом (5x10 мл). Весь хлороформный раствор сушат и концентрируют при пониженном давлении, а остаток очищают на хромато- графической колонке с силикагелем (растворитель - хлороформ этилацетат (1:1, объем/объем), в результате чего получают циклоартениловый сложный эфир 4-ацетамидо-З-метоксибен- зойной кислоты (10,8 г), выход 76,5%, т.пл. 224-225°С.
8892 42
Удельное вращение + 61,5° (с 1,00, СНС1,).
. Циклоартениловый сложный эфир s 4-ацетамидо-З-метоксибензойной кислоты (10,0 г, 0,016 моль) подвергают взаимодействию с 30%-ной НС1 (20 мл) в тетрагидрофуране (200 мл) при кипячении с обратным холодиль- Ю ником в течение 2 ч. Затем растворитель отгоняют при пониженном дав0
5
0
5
0
5
реформе (300 мл), и хлороформный слой промывают последовательно 1н. 5 водным NaOH (200 мл) и насыщенным рассолом. Водные растворы экстрагируют хлороформом трижды. Объединенные хлороформные растворы сушат и концентрируют, а остаток очищают на 0 хроматографической колонке с силикагелем (растворитель- этилацетат гексан 1:4, объем/объем), в результате чего получают циклоартениловый сложный эфир 4-амино-З-метоксибен- 5 зойной кислоты (5,0 г), выход 58,7%, т.пл. 186-187°С.
Удельное вращение eij + 64,4 (с 1,00, СНС1,). Х
Фармакологические действие.
Испытания на острую токсичность проводят с использованием 5 мышей- самцов линии ddy (30+2 г) и 5 крыс- самцов линии Wistar (100+2 г) для каждого соединения при оральном введении.
Испытаниям на острую токсичность подвергают следующие соединения: циклоартениловый эфир 4-окси-З-ме- токсибензойной кислоты (пример 8); циклобраниловый эфир 4-окси-З-меток- сибензойной кислоты (пример 11); 24-метиленциклоартаниловый эфир 4-ок- си-3-метоксибензойной кислоты (пример 22); циклоартениловый эфир 3- этокси-4-оксибензойной кислоты (пример 16); циклобраниловый эфир 3- этокси-4-оксибензойной кислоты (пример 17); циклоартениловый эфир 4-ок- си-3-пропоксикоричной кислоты (пример 19); циклобраниловый эфир 3- этокси-4-оксикоричной кислоты (пример 18); циклоартениловый эфир 3,4- диоксибензойной кислоты(пример 7); циклобраниловый эфир 3,4-диоксибен- зойной кислоты (пример 12); циклоартениловый эфир 3,4-диоксикорич- ной кислоты (пример 1); циклобраниловый эфир 3,4-диоксикоричной кислоты (пример 9); 24-метиленциклоартаниловый эфир 3,4-диоксикорич- ной кислоты (пример 20); циклоарте- ниловый эфир орто-оксибензойной кислоты (пример 3); циклобраниловый эфир орто-оксибензойной кислоты (пример 13); циклоартениловый эфир пара-оксибензойной кислоты (пример 4); циклобраниловый эфир пара- оксибензойной кислоты (пример 15); циклоартениловый эфир мета-оксибен- зойной кислоты (пример 5); циклоартениловый эфир 4-окси-З-метокси- oi-метилкоричной кислоты (пример 28) циклобраниловый эфир 4-окси-З-ме- токси-сЈ- метилкоричной кислоты (пример 29); 24-метиленциклоартани- ловый эфир 4-окси-З-метокси-сс-ме- тилкоричной кислоты (пример 30); циклоартениловый эфир 4-окси-З-ме- токси- -этилкоричной кислоты (пример 31); циклобраниловый эфир 3-эток си-4-окси- л метилкоричной кислоты (пример 35); циклоартениловый эфир 4-окси-0Ј-этилкоричной кислоты (пример 34); циклоартениловый эфир 4 ок- си-3-пропокси-аб-метилкоричуой кислоты (пример 39).
Описанные сложноэфирные соединения и, в качестве контрольных лекарств, циклоартенол, 24-метилен- циклоартанол, циклобрапол и jp -ори- занол, принудительно вводят указанным мышам и крысам с помощью горлового зонда в дозах 0,1-5 г/кг для мыши и 2-6 г/кг для крысы. В ходе испытания температуру вольера с животными поддерживают в интервале 22-23°С. После введения животных наблюдают в течение двух недель. При этих дозах ни одно из животных не умерло. При наблюдении не был обнаружен симптом токсикоза и различий в поведении и в весе тела между животными, подвергшимися испытанию, и нормальными животными, которым не вводили соединения. При проверкеэ осуществленной после двухнедельного наблюдения, не было обнаружено макроскопических повреждений каких- либо частей основных органов. Таким образом, предлагаемые соединения обладают столь низкой токсичностью,чт было невозможно определить значение
ДЦ6ь .
Метод А. Фармакологического испытания на антигиперлипидемическую активность проводят по двум методикам (А и В) .
0
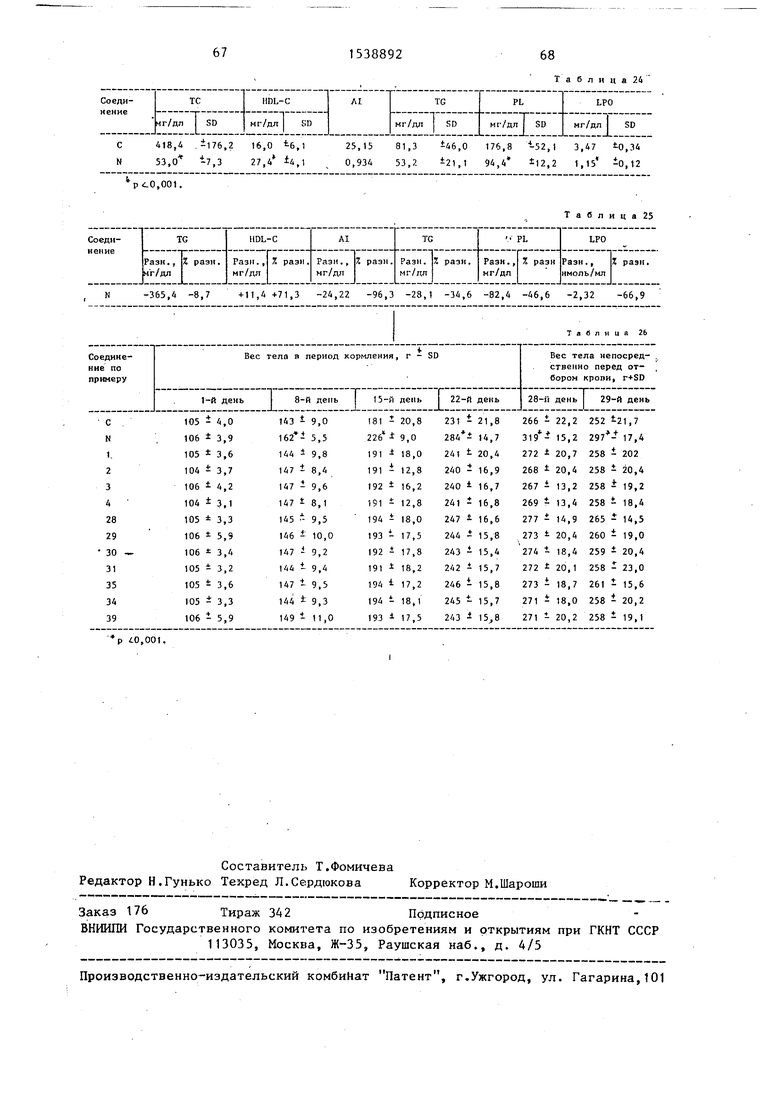
А.В качестве испытуемых животных использзтот крыс-самцов линии Wistar (100+1 г, в каждую группу входит по 10 крыс). Рацион для контрольной группы получают смешением 20% казеина, 62,5% глюкозы, 10% гидрированного кокосового масла, 2% порошкообразного агара, 4% солевой смеси, содержащей витамины, 1% холестерина и 0,5% холевой кислоты (Фукуши- ма и др. Gakugaku Lassi. 1962, 89, № 6, p. 857-862). Рацион для испытуемых групп получают тщательным смешением 1% каждого из следующих соединений: циклоартенол, 24-ме- тиленциклоартанол и циклобранол с рационом контрольных групп. Каждую крысу содержали в вольере при постоянной температуре 23+1°С и постоянной относительной влажности в течение 2 недель, в продолжение которых ей давали 10 г описанного рациона в день. В конце крыс лишали 5 пищи, за исключение воды, на 16 ч (с 16°° 14-го дня для испытания до 8°° 15-го дня испытания) и после анестезии пентабарбиталом натрия (торговое название Нембутал) из каждой крысы отбирали кровь из нисходящей брюшной аорты. После этого в сыворотке определяют ТС, HDL-C, TG, PL и LPO.
В. В качестве испытуемых животных используют крыс-самцов линии Wistar ( г формируют группы по 8 крыс и контрольную группу из 16 крыс, который дают гиперлипидемический рацион) . В качестве обычного рациона используют порошкообразный рацион (СЕ-2, производство Clea Gapan Snc). Гиперлипидемический рацион получают, добавляя в обычный рацион холестерин (1%) и холевую кислоту (0,5%). Каждое испытуемое соединение (1%) для введения смешивается с гиперлипидеми- ческим рационом. В вольере содержат по две крысы, которым дают описанный рацион и воду по потребности. Таким образом, крыс кормят в течение 4 недель при постоянной температуре 23+1°С и постоянной относительной влажности 55+5%. Затем крыс лишают пищи, но не воды, на 16 ч (с 16°° 28-го дня испытания до 8°° 29-го дня испытания), анестезируют пентабарбиталом натрия и из каждой крысы отбирают кровь через нисходящую брюшную аорту. После этого в
0
5
0
5
0
5
451
сыворотке определяют ТС, HDL-C, TG, PL и LPO описанным способом.
Методика определения общей концентрации холестерина (ТС) в сыворотке.
Используют ТС из К-набора (производство Ltd). Принцип определения следующий. Сложный эфир холестерина в сыворотке гидролизуют холестерин- эфирной гидролазой до свободного холестерина и жирных кислот. Весь свободный холестерин окисляют хо- лестериноксидазой с образованием Д4-холестенола и перекиси водорода. Фенол и 4-аминоантипирин окислительно конденсируют друг с другом с помощью образовавшейся перекиси водорода и пероксидазы. Образовавшееся красное хиноновое окрашенное соединение определяют колориметрически по поглощению при 500 нм с использованием спектрофотометрии, определяя таким образом ТС.
Получение образующей окраску жидкости.
Образующий окраску реагент (одна порция) состава 25000 ед. холесте- ринэстеразы, 25 ед. холестеринокси- дазы, 3554 ед. пероксидазы, 20 мг 4-аминоантипирина.
Буферный раствор: 100 мл раствора, содержащего фенол (33,3 мг), дигидрофосфат калия (489,9 мг) и безводный гидрофосфат натрия (908,5 мг) в очищенной воде.
Стандартный раствор: 100 мл раствора, содержащего холестерин (300 мг).
Раствор одной порции образующего окраску реагента в 160 мл буферного раствора называют образующей окраску жидкостью.
Образующую окраску жидкость (3,0 мл) тщательно смешивают с образцом сыворотки (0,02 мл). Смесь один раз нагревают при 37°С в течение 15 мин и с помощью спектрофотометра измеряют поглощение при 500 нм Найденное поглощение обозначают как ЕА. Кроме того, образующую окраску жидкость (3,0 мл) тщательно смешивают со стандартным раствором. Смес обрабатывают и измеряют поглощение при 500 нм так же, как описано выше. Найденное поглощение обозначают как ES. Как ЕА, так и ES определяют с учетом результата пустого/опыта,
10
0
892
46
проводимого с использованием одной образующей окраску жидкости(3,0 мл),
ЕА Значение ТС -- х 300 мг/дл.
Методика определения концентрации липопротеина высокой плотности холестерина (HDL-C) в сыворотке.
Используют HDL-C из N-набора (производство Nippon Shoji kaisha Ltd). Липопротеин ультравысокой плотности (VLDL) и липопротеин низкой плотности (LDL) осаждают из сыворотки действием гепарина. Осадок отделяют цент- 5 рифугированием. Липопротеин высокой
5
0
5
0
5
0
5
плотности (HDL) растворяется в отделенном супернатанте. Сложные эфиры холестерина этой фракции гидролизуют холестерин-эфирной гидролазой до свободного холестерина и жирных кислот. Весь свободный холестерин окисляют холестериноксидазой с образованием д -холестенола и перекиси водорода. Фенол и 4-аминоантипирин окислительно конденсируют друг с другом с помощью образовавшейся перекиси водорода и пероксидазы. Образовавшееся красное хиноновое окрашенное соединение измеряют колориметрически по поглощению при 500 нм с помощью спектрофотометра, определяя таким образом HDL-C.
Методика определения общей концентрации фосфолипидов (PL) в сыворотке.
Для определения используют PL из К-набора (производство Nippon Kais- , ha, Ltd). Лецитин, сфингомиелин и лизолецитин разлагают фосфолипазой до холина и соответственно до фос- фатидной кислоты, N-ацилофингозифос- фата или лизофосфатидной кислоты. Результирующий холин количественно разлагают холиноксидазой до перекиси водорода и бетаина. С помощью этой перекиси водорода и пероксидазы фенол и 4-аминоантипиридин конденсируют с образованием красного хинонового пигмента, после чего на спектрофотометре измеряют поглощение при 500 нм и определяют таким образом PL.
Методика определения общей концентрации триглицеридов (TG) в сыворотке .
Содержание TG в сыворотке определяют с помощью триглицеридчого испытательного набора (производство
47
Wako Pure Chemical Industries, Ltd), в котором в качестве реагента используют ацетилаиетон„ спеду- ющим образом.
Сывороточные белки осаждают смешением иэопропилового спирта и образца сыворотки. При этом липиды и сахариды сыворотки экстрагируются в спой изопропилового спирта о К раствору в изопропиловом спирте добавляют адсорбент для адсорбирования соединений, мешающих окрашиванию. После центрифугирования смеси к су- пернатанту прибавляют гидроокись калия, омыляя триглецирид и освобождая глицерин. После этого рН смеси доводят до 6 добавлением буферного раствора и добавляют раствор метапериодата натрия для окисления глицерина в муравьиную кислоту (1 моль из 1 моль глицерина) и формальдегид (2 моль из 1 моль глицерина) . Образовавшийся в результате альдегид оставляют реагировать с ацетилацетоном и аммиаком в буферном растворе с образованием циклического соединения 3,5-диапетил- 1,4-дегидробутидина. Этот желтый ги мент определяют, измеряя поглощение при 410 нм на спектрофотометре, и определяют таким образом содержание TG.
Методика определения общей кон - центрации липидных перекисей (LPO) в сыворотке.
Для этого определения используют липопероксидныи испытательный набор (производство Wako Pure Cxemi- cal Industrie,Ltd) в соответствии с методикой Яги, основанной на использовании тиобарбитуровой кислоты (K.Jagi. Biochem, Med, 1976., 15, p. 212. Vitamin. 1975, 49, p. 403), К образцу сыворотки (0,05 мл) прибавляют физиологический солегой раствор (1,0 мл) и осторожно перемешивают смесь. После центрифугирования (3000 об/мин, 10 мин) смеси и супернатанту (0,5 мл) прибевляют 12 н.серную кислоту (4,0 мл) и проводят тщательное перемешивание. Прибавляют 10%-ный водный раствор фос- форно-вольфрамовой кислоты (0,5 мл) смесь тщательно перемешивают, оставляют стоять в течение 5 мин, и цент рифугируют при 3000 об/мин в течение 10 мин. Результирующий осадок тщательно суспендируют в смеси
to
г-
, - 55
3889248
1/12н. серной кислоты (2,0 мл) и 10%-ного водного раствора фосфорно вольфрамовой кислоты с помощью сме сителя. Затем суспензию центрифугируют при 3000 об/мин в течение 10 мин, после чего полученный осадок суспендируют в дистиллированной воде (4,0 мл) с помощью мешалки. После этого с суспензией тщательно смешивают ТЕ А-Реагент (1,0 мл, 50%-ный уксуснокислый раствор, содержащий тиобарбитуровую кислоту). Смесь помещают в центрифужную про15 бирку и нагревают на кипящей водяной бане в течение 60 мин со стеклянным ыариком, закрывающим верх пробирки. После охлаждения пробирки в проточной воде в течение 5 мин к
2о смеси прибавляют бутанол (5,0 мл) и, закрепив пробирку, тщательно перемешивают в течение 20 с с помощью смесителя, проводя таким образом экстракцию реакционного продукта в
25 бутанол. Смесь центрифугируют при 3000 об/мин в течение 10 мин. Измеряют флуоресценцию бутального слоя. После определения нулевой точки с помощью пустого опыта измеряют
30 интенсивность флуоресценции (F) 0,1 мл стандартного раствора (1,1,3,3-тетраэтоксипропан,5ммоль/мл я интенсивность флуоресценции образца f при 553 нм и при длине волны возбуждающего излучения 515 нм).
35 Таким образом, в данной методике продукт реакции LPO с тиобарбитуровой кислотой идентичен продукту реакции малондиальдегида с тиобарбитуро- воЈ кислотой, В соответствии с этим коьцентрация LPO определяется как количество малондиальдегида в 1 мл сыворотки. Стандартный раствор представляет собой 5 нмоль/мл водный раствор 1,1,3,3-тетраэтоксипро40
45
шается в малондиальдегид. Так как в данной методике используется 0,1 мл стандартного раствора, то количество 1,1,3,3-тетраэтоксипропана равно 0,5 нмоль. Затем содержание LPO (нмоль/мл сыворотки рассчитывают по следующему уравнению:
л , f 1,0 1,05 f ° 5 Х F X Х F X
Антерогенный показатель (AI) опреде ляется как (ТС- HDL- С) LDL-C
49
Результаты фармакологических испытаний на гиполипидемическую активность.
Гиполипидемическое действие предлагаемых соединений на сывороточные липиды и на гидроперекиси сывороточных липидов. Выбранные для этого соединения являются теми же соединениями, которые были отобраны при описании острой токсичности. Испытания проводили описанным способом,- в которых крыс кормили рационом с высоким содержанием холестерина.
Произведе но тестирование известных соединений- циклоартенола, 24- метиленциклоартанола и циклобранола с целыо оценки противогиперлипиде- мического воздействия указанных средств.
Результаты испытаний на гиполипидемическую активность циклоартенола, циклобранола и 24-метиленциклоартанола, которые использовали в качгестве контрольных лекарств, показаны в таблицах 4 и 5 (в соответствии со способом Айв табл. 18 и 19 ( в соответствии со способом В и сводятся к следующему,Гиполипидемическое воздействие при использовании обоих методов тестирования в основном идентично. Уменьшение общего содержания холестерина (ТС) в сыворотке крови наблюдалось для обеих групп животных, которым давался рацион с повышенным содержанием холестерина, содержащий циклоарте- нол, и которым давался рацион с повышенным содержанием холестерина, содержавши циклобранол, при значимых величинах уменьшения (р 0,05 согласно методу А, и ,01 согласно методу В) по сравнению с контрольной группой животных, которым двался рацион, содержащий только повышенное количество холестерина. Понижение общего содержания холестерина (ТС) в случае использования 24-метиленциклоартанола незначительно и не давало значимых величин согласно методу А, давая при этом значимые величины согласно методу В (,05). Что касается HD L-C, то циклоартенол понижает его содержание на значимую величину (,05 согласно методу А и Р 0,01 Согласно методу В), 24-метиленциклоарта- нол понижает его незначительно, так что в результате использования обо15
10
15
20
25
889250
их методов тестирования получаются незначимые величины. Циклобранол проявляет напротив тенденцию к повышению содержания HDL-C в достаточно значительной мере.
Предлагаемые соединения являются гиполипидемическими средствами, которые могут значительно понижать общее содержание холестерина и повышать содержание HD L-C в сыворотке крови. Любой из тритерпениловых спиртов, например циклоартенол, циклобранол или 24-метиленциклоартанол, при использовании их поодиночке, значительно понижает уровень общего содержания холестерина в сыворотке крови. Однако при проведении их тестирования не наблюдалось повышение содержания HDL-C при достижении гиполипидемического воздействия ни согласно методу А, ни согласно ме- . тоду В.
Циклоартенол и циклобранол обнаруживают тенденцию к уменьшению показателя AI согласно способу А, да как 24-метиленциклоартанол обнаруживает только незначительную тенденцию к увеличению AI. Согласно способу тестирования В все три три- терпеюшовые спирта обнаруживают тенденцию к уменьшению атерогенного показателя AI. Что сасается значений TG, PL и L РО, то яри тестировании по обоим способом все три спирта не дают сколь-нибудь значительного изменения значений этих показателей.
Если сравнивать воздействие указанных трех тритерпениловых спиртов, то следует отметить, что циклобранол имеет тенденцию к понижению ТС, AI, TG, PL и LPO, но повышает при этом HDL-C, и, следовательно, он имеет воздействие, отличное от циклоартенола и 24-метиленцнклоар- танола. При этом можно констатировать, что циклобранол превосходит по гиполипидемическому воздействию циклоартенол и 24-метиленциклоартанол.
Гиполипидемическое действие предлагаемых соединений, испытанных по способу А, представлено в табл. 6-17.
Действие предлагаемых соединений и действие циклоартенола, циклобранола, 24-метиленциклоартанола оризанола, использованных в качест30
35
40
45
50
55
51
ве контрольных лекарств, испытанных по способу В, показано в тэбл„20,21
Табл. 20-23 показывают, что ТС, PL и LPO в группе, питающейся нормальным рационом (обозначается как N), с высокой достоверностью подавляются (р с 0,001), за исключением HDL-C, который с высокой достоверностью повышается (,001), в отличие от контрольной группы, питавшейся гиперлипидемическим рационом (обозначается как С)„ Тенденция TG подавляется в N показана в С, однако эта разница TG в N и С незначительна.
Гиполипидемическое действие улучшенных сывороточных липидных компонентов четко прослеживается в группах, питающихся гиперлипидемическим рационом, содержащим каждое из предлагаемых соединений или каждое из контрольных лекарств, по сравнению с этим действием в группе, питающейся только гиперлипидемическим рационом. В частности, предлагаемые соединения оказывают заметно лучшее действие на два или больше липидных компонента ТС, HDL-C} PL и LPO, чем контрольные соединения. I По способу А содержание ТС изменяется предлагаемыми соединениями следующим образом. Соединения по примерам 11,17,18,7,12,3,13,4,15 и 27 снижают уровень ТС со средней достоверностью. Соединения по примерам 8,22,16,19,9 и 5 снижают концентрацию ТС с низкой достоверностью (рСО,05). Соединения по примерам 1 и 20 существенно не снижают концентрацию ТС, но проявляют
пониженную тенденцию, 1
В способе В уровень снижается контрольными лекарствами, т„е„ тремя тритерпениловыми спиртами и J1- оризанолом, со средней достоверностью (,01) по сравнению с уровнем ТС в контрольной группе, получившей только гиперлипидемический рацион. В противоположность этому, соединения по примерам 28, 29 и 30 подавляют уровень ТС с высокой достоверностью (р -0,001). Соединения по примерам 31,35,34 и 39 снижают уровень ТС со средней достоверностью (р 0,01).
3889252
Содержание HDL-C в способе А изменяется предлагаемыми соединениями следующим образом.
Соединение по примеру 3 повышает содержание HDL-C с высокой достоверностью (р- 0,001), соединения по примерам 11,17 и 12 - со средней достоверностью (,01) и соедиJQ нения по примерам 18,7 и 13 - с низкой достоверностью (,05). Соединения по примерам 22,19, 4 и 5 слабо изменяют или слегка снижают содержание HDL-C, а соединения по
15 другим примерам проявляют тенденцию незначительно повышать это содержание.
В способе В действие испытуемых соединений на HDL-C следующее.
2Q Контрольное лекарство - циклоарте- нол вызывает снижение с высокой достоверностью (,01), в то время как другие контрольные лекарства- циклобранол, 24-метиленциклоартенол
25 и fr-оризаноп проявляют тенденцию незначительно повышать или снижать содержание. В отличие от этого соединения по примерам 28,29,30,35 и 39 с высокой достоверностью
30 ( 0,001) повышают содержание
HDL-C, а соединения по примерам 31 и 34 повышают со средней достоверностью (,01). В частности, соединения по примерам 29,30, и 35 вызывают заметное повышение содержания HDL-C по сравнению с группой, получающей нормальный рацион.
Все соединения без исключения проявляют ясную тенденцию подавлять уровень AI в способах А или В.
В способе А содержание TG не снижается достоверно, а остается неизменным или незначительно снижается всеми испытуемыми соединениями, за исключением того, что соединение по примеру 27 снижает содержание с низкой достоверностью (,05). В способе В предлагаемые соединения, а также контрольные лекарства проявляют тенденцию слегка или в некото- 50 рой степени подавлять TG, но недостоверно,
В способе А соединения по примерам 17,18,7,12,3,13,27 достоверно снижают уровень PL (р Ј0,001), сое- 55 динения по примерам 8,11,16,19 и 15 снижают со средней достоверностью (р.4 0,01), а соединения по примерам 22,9 и 4 - с уровнем достовеп35
40
5315
ности ,05. Соединения по примерам 1,20 и 5 проявляют очевидную тенденцию снижать уровень, но недостоверно.
В спсобе В контрольные лекарства проявляют тенденцию слегка снижать уровень PL, но недостоверно. В отличие от этого, соединения по примерам 28,29,30,35 и 39 снижают содержание PL с уровнем достоверности p-dO,001, соединения по примерам 3t и 39 - с уровнем достоверности ,01.
В способе А соединения по ттриме- рам 4 и 15 снижают уровень LPO с достоверностью ,001, а соединения по примерам 8,11,16,17,18 и 5 - с уровнем достоверности ,05 Другие предлагаемые соединения проявляют явную тенденцию снижать уровень, но незначительно. В способе В контрольное лекарство - -оризанол снижает уровень LPO с достоверно- стью ,01, а контрольные лекарства, представляющие собой тритерпени
ловые спирты, проявляют явную тенденцию к снижению, но незначительному. В отличие от этого соединения по примерам 28,29,30,31,35,32,34 и 39 снижают уровень LPO с достоверностью р 0,001.
Большинство предлагаемых соединений в испытаниях по способу А или В проявляют явную тенденцию повышать содержание HDL-C и снижать уровни ТС, AT, PL и IPO. Сравнение с эффектами, наблюдаемыми при введении только свободных тритерпени- ловых спиртов, показывает, что гипо- липидемические активности предлагаемых соединений представляют собой синергетические эффекты.
Увеличение веса тела крыс, использованных для испытаний на гипо- липидемическую активность в способе В, показано в таблице 7-1. Вес тела крыс, получающих нормальный рацион, достоверно повышается (р 4 0,001) по сравнению с весом тела крыс контрольной группы, получающих гиперли- пидемический рацион. Группы крыс, получающие гиперлипидемический рацион, содержащий каждое из контрольных лекарств, обнаруживают небольшое увеличение веса тела, но недостоверное, по сравнению с контрольной группой крыс, получающих только гиперлипидемический рацион.
54
При определении антигиперлипиде- мической активности по способу А суточная доза каждого из предлагаемых соединений равна 1% в 10 г/день гиперлипидемического рациона, т.е. 100 мг.
В способе В дозу каждого из предлагаемых соединений приблизительно рассчитывали как 210 мг/день для каждой крысы, в основном из количества потребленного рациона, содержащего соединение. Например, цикло- артениловый эфир 4-окси-3-метокси- А- метилкоричной кислоты (пример 28), циклобраниловый эфир З-этокси-4-ок- си- -метилкоричной кислоты (пример 35) содержат соответственно свяг занную 4-окси-3-метокси- -метилко- ричную кислоту (70,8 мг), 3-этокси- 4-окси- -метилкоричнуга кислоту (72,5 мг).
Каждую из этих органических кислот в свободной форме прибавляют к, гиперлипидемйческому рациону и результирующий рацион вводят крысам
0
5
5
0
ределении антигиперлипидемической активности, однако при указанных
0 выше дозах свободных кислот (59,4- 72,5 мг/день) а нтигиперлипидемичес- кое действие не наблюдается. Таким образом, установлена, что в действии предлагаемых соединений не участвуют органические кислоты, освобождаемые в результате гидролиза три- терпенилового эфира органической кислоты.
В табл. 5-26 приняты следующие обозначения.
Соединение С - сыворотка контрольной группы из 10 крыс, получающих гиперлипидемической рацион, в табл. с 5 по 26, соединение 1 - сыворотка группы из 10 крыс, получавших гиперлипидемический рацион, содержащий 1% циклоартенола в качестве контрольного лекарства, в табл. 5 и 6, соединение 2 - сыворотка группы из 10 крыс, получавших гиперли0 пидемический рацион, содержащий 1% циклобранола в качестве контрольного лекарства, в табл. 5 и 6, соединение 3 - сыворотка группы из 10 крыс, получавших гиперлипидеми-
5 ческий рацион, содержащий 1% 24-ме- тиленциклоартанола в качестве контрольного лекарства, в табл. 5 и 6. SD - стандартное отклонение.
5
551
Раэн. означает разницу Q - Qc a разн. обозначает (Q - Qc)x 100/QC, где Q - концентрация липидного компонента в образце сыворотки; Qc - концентрация липидного компонента в сыворотке контрольной группы..
По примерам - сыворотка группы из 10 крыс, получавших гиперлипи- демический рацион, содержащий 1% соединения по каждому из примеров, в табл. 6-26.
Соединение С - сыворотка контрольной группы из 16 крыс, получавших гиперлипидемический рацион, в табл. 18-26, соединение 1 - сыворотка группы из 8 крыс, получавших гиперлипидемический рацион, содержащий 1% циклоартенола в качестве контрольного лекарства, в табл. 18- 21 и 26, соединение 2 - сыворотка группы из 8 крыс, получавших гиперлипидемический рацион, содержащий 1% циклобранола в качестве котроль- ного лекарства, в табл. 18-21 и 26, соединение 3 - сыворотка группы из 8 крыс, получавших гиперлипидемический рацион, содержащий 1 % 24-ме- тиленциклоартанол в качестве контрольного лекарства, в табл. 18-21 и 26.
В табл. 20 соединение N - сыворотка группы из 8 крыс, получавших обычный рацион (это относится и к последующим таблицам), соединение 4 - сыворотка группы из 8 крыс, получавших гиперлипидемический рацион, содержащий 1% -оризанола, по примерам - сыворотка группы из 8 крыс, получавших гиперлипидемический рацион, содержащий 1% соединения по каждому из примеров, в табл. 20-26.
Это относится также к последующи таблицам.
Таким образом, предлагаемый способ позволяет получить новые три- терпениловые эфиры органических кислот, обладающие более высокой проти вогиперлипидимической активностью.
Формула изобретения
Способ получения тритерпениловых эфиров органических кислот общей формулы
56
10
15
|
0
5
0
где R, - группа COO R&,CH CRSCOOR ;
R2 - Н, ОН-группа;
R3 - Н, группы ОН, кокси;
R - Н, группы ОН, амино-;
Rg- - Н, С,-С4-алкил;
R - циклоартенил, циклобранил, 24-метиленциклоартанил, причем замещение в бензольном кольце может быть парой, выбранной из ряда ОН-группа и С,-С.-алкокси- группа, аминогруппа и С1-С -алкоксигруппа, две ОН-группы, за исключением тритерпениловых эфиров феруловой кислоты, или хотя бы один из радикалов R2 и RJ. является ОН-группой или R4 - аминогруппа, отличающийся тем, что сложный эфир тритерпенилового спирта общей формулы
35
где
Rr
имеет указанные значения;
-Н, С -Сй-ацилокси;
-Н, С(-С4-алкокси-, ацилокси-;
Н, Сг-С6 ацилокси-, Сг-С5 ациламидо-, причем замещение в бензольном кольце может быть парой, выбранной из ряда Сг-С6-ацилок- си- и С,-С -алкокси-, С2-С -ациламидо- и С,-С4- алкокси-, две С2-С6 ацилок- сигруппы, и хотя бы один
из радикалов Rr и С -Су-ацилоксигруппа или радикал R -ациламидо - Сг-С -группа, подвергают деацилированию.
57
153889258
Т а б л и ц а 1
Уровень достоверности pi 0,05.
Таблиц
ТаблицаЗ
Таблицаб
Таблица/
Таблицав
Таблица 10
-16,7 -10,0 -0,2 -0,3
С205,1 127,4 81,5 ±10,1
27166,7 ±28,194,1 9,3
,01. .001.
27
-38,4 -18,7 +15,1 +18,5-0,745 -49,1 -12,7 -37,0 -30,6 -17,6 -0,68 -29,8
32-122,1 -34,7 +0,1 +1,2
-38,1
-37,7
-37,8
-3,2 -23,7 -4,3 +1,5 +11,1 -9,8 -0,7 -5,2 -7,0
Таблица 13
-0,276 -14,9 -0,8 -3,2 -8,0 -5,4 -0,31 -13,2
Т а в л к ц а 14
34,,в173,6±11,0
21,,,0
±10,6
2,27 -0,38 1,59 0,33
Таблица 15
Таблица 17
-17,6 -38,9
+1,9 +3,8 -36,7 -24,0
Таблица 19
-2,5 -2,3 -5,5 -3,9 -5,7 -9,2
-1,6 -0,12 -2,7 -0,20 -6,5 -0,09
-4,3 -7,1 -3,2
,05. ,01. ,001.
Таблица 20
Таблица 23
С418,4 ±176,2 16,0 te,
N53,0 -7,327,4 ±4,1
25,15 81,3 46,0 176,8 -52,1 3,47 0,34 0,934 53,2 ±21,1 94,4 ±12,2 1,15 ±0,12
,001.
-365,4 -8,7
+11,4 +71,3 -24,22 -96,3 -28,1 -34,6 -82,4 -46,6 -2,32 -66,9
р iO.001.
Т а б л и ц а 24
Таблица 25
| Gukagaku, 1У69, 18, 63-67. |
Авторы
Даты
1990-01-23—Публикация
1985-06-03—Подача