Изобретение относится к области получения новых производных 3-бром- 2,6-диметоксибензамида общей формулы
ОСН3
ВгfcrpCQ-NH-{ HQ-Q i-CHf
ОСН3
где X - водород, фтор или хлор, в виде кислотно-аддитивных солей, обладающих нейролептическим свойством.
Целью изобретения является разработка на основе известных методов способа получения новых производных бензамида, проявляющих более высокие фармакологические свойства при низкой токсичности.
Пример 1. Фумарат 1Ґ-(8-бензил- 6-окси-З-нортропанил)-2,6-диметокси-З- бром-бенз амида.
К раствору 5,22 г (20 ммоль) 2,6- диметокси-5-бромбензойной кислоты в 60 мл хлористого метилена добавляют каплю диметилформамида, после чего медленно прикапывают 3,5 мл хлор- ангидрида щавелевой кислоты при 20 С. Когда из реакционной смеси выделяется еще лишь немного газа, кипя- ,тят еще в течение 20 мин. Растворитель упаривают, остаток растворяют в 40 мл сухого хлористого метилена и получаемый раствор при комнатной температуре прикапывают к раствору 4,64 г (20 ммоль) З-амино-б-окси-8- бензил-нортропана и 7,2 мл триэтилсд
Ј СО 4
00
со
О4
амина в 60 мл хлористого метилена. Реакционную смесь отстаивают в течение 3 ч и затем перерабатывают. Раствор разбавляют 100 мл хлористого метилена, два раза промывают по 100 мл воды и затем еще раз промывают 10%-ным натровым щелоком. Органическую массу сушат над сульфатом натрия и с.гущают. Остаток растворяют в метаноле, после чего добавляют 2,32 г метанольной фумаровой кислоты.
Получают 8,6 г (72,7% теории) белых кристаллов с т.пл. 144 С.
Найдено,%: С 54,92; Н 5,38; N 4,70.
Си Нм BrNz04 .
Вычислено,%: С 54,83 Н 5,28 N 4,74.
Пример 2. а) З-Ацетамидо-6- окси-8-бензилнортропан.
К раствору 30 г (0,129 моль) 3- амино-6-окси-8-бензилнортропана и 13,1 г (0,129 моль) триэтиламина в
10
15
20
10 мл смеси диметилформамида и тет- рагидрофурана (4:1) кипятят с обратным холодильником в течение 7 ч. После охлаждения растворителя отго- няйт в вакууме. Остаток смешивают с 200 мл воды и три раза экстрагируют по 100 мл хлористого метилена. Объединенные метиленхлоридные фазы сушат над сульфатом натрия и сгущают в вакууме. Получают 8,9 г (96% теории) белых кристаллов с т.пл. 105 С.
г) 3-Ацетамидо-6-окси-8-(4-фтор- бензил)-нортропан.
Повторяют стадию в) с той разни- цей, что используют 5,53 г (0,033 моль) З-ацетамидо-6-окси-нортропана и 6,08 г (0,033 моль) 4-фторбензилбро- мида. При этом получают 5,7 г (65% теории) белых кристаллов с т.пл. 125ЙС.
д) 3-Амино-6-окси-8-(4-фторбен- зил)-нортропан.
8,9 г 3-ацетамидо-6-окси-8-(4-фтор250 мл хлористого метилена прикапыва- 25 бензил)-нортропана в 100 мл 6 н.со- ют 10,1 г (0,129 моль) ацетилхлори- ляной кислоты кипятят с обратным хода при . Затем кипятят с обратным холодильником в течение Зч. После охлаждения раствор один раз промывают 200 мл 10%-ного натрового щелока и три раза промывают по 200 мл воды. После сушки метиленхлоридной фазы над сульфатом натрия отгоняют растворитель. Получают 28,4 г (80,2% теории).белых кристаллов с т.пл. 108 С.
б)З-Ацетамидо-6-оксинортропан. В автоклаве к раствору 28,4 г
(0,104 моль) 3-ацетамидо-6-окси-8- бензилнортропана в 300 мл метанола добавляют 2,8 г палладия на угле (5%) и подвергают гидрированию под давлением водорода, равным 5 бар. После окончания поглощения водорода раствор отделяют от катализатора путем фильтрации и сгущают в вакууме. Маслянистый остаток подвергают кристаллизации в смеси сложного этилового эфира.уксусной кислоты и этанола (9:1). Получают 6,2 г (85% теории) белых кристаллов с т.пл. 173°С.
в)3-Ацетамидо-6-окси-8-(4-хлор- бензил)-нортропан.
К раствору 5,53 г (0,03 моль) 3- ацетамидо-6-оксинортропана в 50 мл смеси диметилформамида и тетрагидро- фурана (4:1) добавляют 5,04 г Ј0,06 моль) бикарбоната натрия. После прикапывания раствора 5,31 г t (0,033 моль) 4 хлорбензилхлорида в
30
лодильником в течение 7ч. После охлаждения сгущают досуха в вакууме. Остаток растворяют в спирте и добавлением сложного этилового эфира уксусной кислоты до соотношения 1: № доводят до кристаллизации. Получают 4,74 г (77,7% теории) белых кристаллов с т.пл. 250 С (в виде дигидрохлорида.
К 4,74 г (14,8 ммоль) дигидрохло- 35 рида, растворенного в метаноле, добавляют 1,6 г (29,6 ммоль) метанолята натрия и смесь перемешивают в течение 10 мин. Образовавшуюся суспензию фильтруют на кизельгуре и фильтрат сгущают досуха в вакууме. Получают 3,7 г белых кристаллов основания с т.пл. 130°С.
е) 3-Амино-6-Окси-8-(4-хлорбензил)- нортропан.
Повторяют стадию д) с той разницей, что используют 8,9 г З-ацетамидо-6- окси-8-(4-хлорбензил)-нортропана. Получают 5,38 г (47,7% теории) белых кристаллов дигидрохлорида с т.пл. 300°С, которьй также переводят в основание. Получают 4,6 г бежевых кристаллов с .т.пл. 145вС.
ПримерЗ. Гидрохлорид N- {B- (4-фторбенэил)-6-окси-3-нортропанил1- 2,6-диметокси-З-бромбензамида.
Повторяют пример 2 с той разницей, что используют 1,93 г 2,6-диметокси- 5-бромбензойной кислоты, 0,94 г хлор40
45
5
0
10 мл смеси диметилформамида и тет- рагидрофурана (4:1) кипятят с обратным холодильником в течение 7 ч. После охлаждения растворителя отго- няйт в вакууме. Остаток смешивают с 200 мл воды и три раза экстрагируют по 100 мл хлористого метилена. Объединенные метиленхлоридные фазы сушат над сульфатом натрия и сгущают в вакууме. Получают 8,9 г (96% теории) белых кристаллов с т.пл. 105 С.
г) 3-Ацетамидо-6-окси-8-(4-фтор- бензил)-нортропан.
Повторяют стадию в) с той разни- цей, что используют 5,53 г (0,033 моль) З-ацетамидо-6-окси-нортропана и 6,08 г (0,033 моль) 4-фторбензилбро- мида. При этом получают 5,7 г (65% теории) белых кристаллов с т.пл. 125ЙС.
0
лодильником в течение 7ч. После охлаждения сгущают досуха в вакууме. Остаток растворяют в спирте и добавлением сложного этилового эфира уксусной кислоты до соотношения 1: № доводят до кристаллизации. Получают 4,74 г (77,7% теории) белых кристаллов с т.пл. 250 С (в виде дигидрохлорида.
К 4,74 г (14,8 ммоль) дигидрохло- 5 рида, растворенного в метаноле, добавляют 1,6 г (29,6 ммоль) метанолята натрия и смесь перемешивают в течение 10 мин. Образовавшуюся суспензию фильтруют на кизельгуре и фильтрат сгущают досуха в вакууме. Получают 3,7 г белых кристаллов основания с т.пл. 130°С.
е) 3-Амино-6-Окси-8-(4-хлорбензил)- нортропан.
Повторяют стадию д) с той разницей, что используют 8,9 г З-ацетамидо-6- окси-8-(4-хлорбензил)-нортропана. Получают 5,38 г (47,7% теории) белых кристаллов дигидрохлорида с т.пл. 300°С, которьй также переводят в основание. Получают 4,6 г бежевых кристаллов с .т.пл. 145вС.
ПримерЗ. Гидрохлорид N- {B- (4-фторбенэил)-6-окси-3-нортропанил1- 2,6-диметокси-З-бромбензамида.
Повторяют пример 2 с той разницей, что используют 1,93 г 2,6-диметокси- 5-бромбензойной кислоты, 0,94 г хлор0
5
ангидрида щавелевой кислоты, 0,75 г триэтиламина и 1,85 г З-амино-6-окси- 8-(4-фторбензил)-нортропана. Получаемое сырое основание переводят в гидрохлорид путем добавления метанольной соляной кислоты. Получают 1,8 г (44% теории) белых кристаллов с т.пл. 140°С.
Найдено,% : С 51,83; Н 5,33, N 4,94.
С„ H26BrFNtO, x HC1 (529,84) Вычислено,%: С 52,14; Н 5,14; N 5,29.
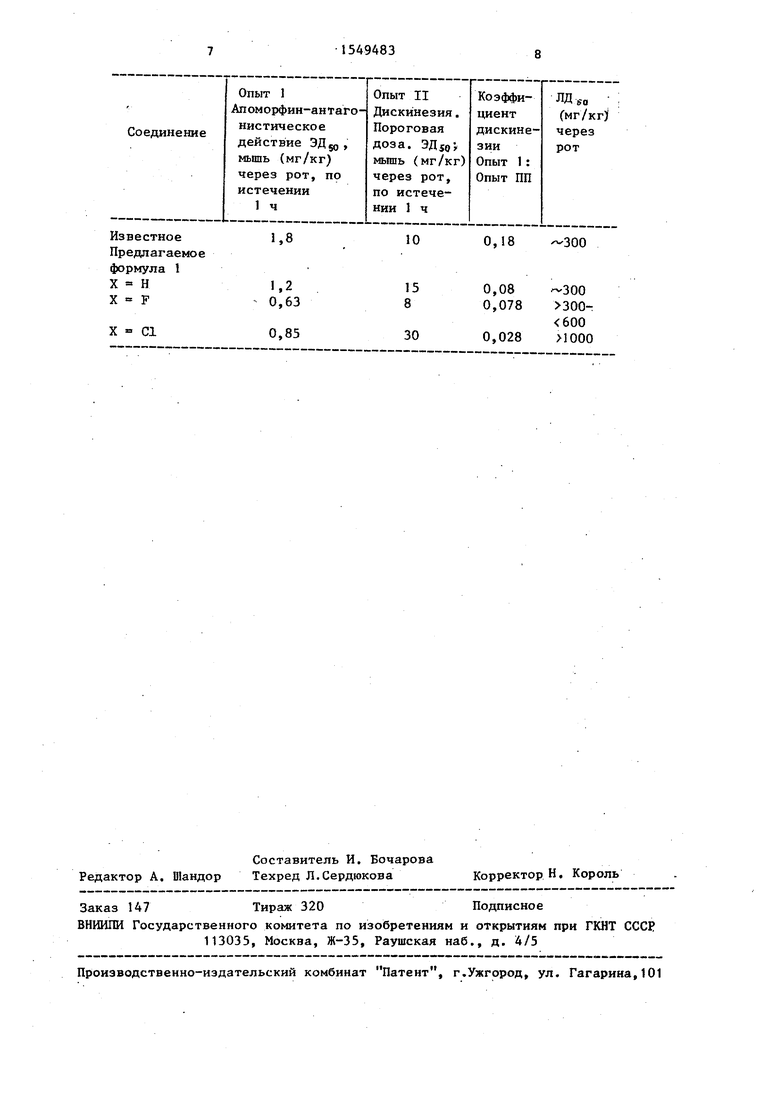
ром уксусной кислоты, сушат над сульфатом натрия и сгущают в вакууме. Получают 4,7 г белых кристаллов. Повтор ное солеобразование с использованием D/-/ миндальной кислоты с последующим переведением в основание приводит к получению 2,06 г чистого (+)-энантио- мера с показателем вращения ei + 11,8 (с 0,01; метанол). Путем обработки метанольной соляной кислотой получают 2,1 г белых кристаллов /+/-гидрохлорида с т.пл. 162-175 С. В таблице приведены сравнительные
10
П р и м е р 4. Гидрохлорид N 8-(4- )$ фармакологические данные для извест- хлорбензил)-6-окси-3-нортропанил - ного и предлагаемого соединений. 2,6-диметокси-З-бромбензамида.Апоморфин-антагонистическое дейПовторяют пример 2, однако исполь- ствие определяетя по известной методике Косталла (Б. Косталл и др. 20
зуют 11,55 г 2,6-диметокси-5-бром- бензойной кислоты, 5,63 г хлоран- гидрида щавелевой кислоты и 4,49 г 3-амино-6-окси-8-(4-хлорбензил) -нор- тропана в 200 мл хлористого метилена. При этом получают 17 г (75% теории ) белых кристаллов основания с т.пл. . Путем добавления метанольной соляной кислоты образуются белые кристаллы гидрохлорида с т.пл. 162-165°С.
Найдено,%: С 49,96; Н 5,49; N 4,74.
C,ziH26BrClNj,04 x HC1 (546,30)
Вычислено,%: С 50,57; Н 4,97; N 5,13.
П р и м е р 5. /+/-N-,8-(4-хлорбензил )-6-окси-3-нортропанил1-2,6- диметокси-3-бромбензамид в виде гид-.
рохлорида.
1
10 г (19,58 ммоль) основания и 2,97 г (19,58 ммоль) D/-/миндальной кислоты растворяют в 15 мл этанола. Затем добавляют простой эфир до образования легкого помутнения (примерEurap l.Pharmacol. 50, с. 39, 1978), а дискинезия - по известной методике И. Либманн и Р. Ниль см. Psychophar- macology 6j8, с. 25-29, 1980).
25 Формула изобретения
Способ получения производных 3- бром-2,6-диметоксибензамида общей формулы
30
35
40
ОСН3
Br- -co-NH-{ но-0нснг-(о)-х рсн3
где X - водород, фтор или хлор, в виде кислотно-аддитивных солей, о т личающий ся тем, что соединение общей формулы
H2N-/HOTN-CH2-XO)-X
где X имеет указанные значения,
но 45 мл). Через ночь при 20°С образу-дс подвергают взаимодействию с соединеются первые кристаллы. Оставляют стоять еще в течение 72 ч, после чего кристаллизация закончена. Прозрачный надосадочньш раствор удаляют декантированием. Кристаллы два раза промывают смесью простого эфира и этанола (4:1), отсасывают и сушат. Получают 6,5 г белых кристаллов соли миндальной кислоты. С целью дальнейшей очистки сырую соль обработкой 10%-ным аммиаком переводят в основание, которое экстрагируют сложным этиловым эфинием сЬормулы
ОСН3
5Cfe
СОС1 ОСНо
55
в присутствии акцептора кислоты триэтиламина в среде инертного растворителя с последующим выделением целевого продукта в виде кислотно-аддитивных солей.
94836
ром уксусной кислоты, сушат над сульфатом натрия и сгущают в вакууме. Получают 4,7 г белых кристаллов. Повторное солеобразование с использованием D/-/ миндальной кислоты с последующим переведением в основание приводит к получению 2,06 г чистого (+)-энантио- мера с показателем вращения ei + 11,8 (с 0,01; метанол). Путем обработки метанольной соляной кислотой получают 2,1 г белых кристаллов /+/-гидрохлорида с т.пл. 162-175 С. В таблице приведены сравнительные
10
ствие определяетя по известной методике Косталла (Б. Косталл и др.
Eurap l.Pharmacol. 50, с. 39, 1978), а дискинезия - по известной методике И. Либманн и Р. Ниль см. Psychophar- macology 6j8, с. 25-29, 1980).
25 Формула изобретения
Способ получения производных 3- бром-2,6-диметоксибензамида общей формулы
ОСН3
Br- -co-NH-{ но-0нснг-(о)-х рсн3
где X - водород, фтор или хлор, в виде кислотно-аддитивных солей, о т-, личающий ся тем, что соединение общей формулы
40
H2N-/HOTN-CH2-XO)-X
где X имеет указанные значения,
подвергают взаимодействию с соед
нием сЬормулы
ОСН3
5Cfe
СОС1 ОСНо
в присутствии акцептора кислоты триэтиламина в среде инертного растворителя с последующим выделением целевого продукта в виде кислотно-аддитивных солей.
ое
1,8
1,2 0,63
0,85
10
0,18
-300
0,08 0,078
0,028
-300 300- 600 Я 000


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пиперазинсодержащих производных мочевины или тиомочевины или их кислотно-аддитивных солей | 1985 |
|
SU1387877A3 |
| Способ получения пиперазинилсодержащих производных мочевины или тиомочевины или их солей с соляной кислотой | 1984 |
|
SU1542415A3 |
| Способ получения производных тетрагидро(фуро- или тиено)-[2,3-с]пиридина или их гидрохлоридов или четвертичных солей с метилйодидом | 1988 |
|
SU1657064A3 |
| Способ получения производных пирролидинона или их кислотно-аддитивных солей | 1984 |
|
SU1373318A3 |
| ПРОИЗВОДНЫЕ КСАНТИНА В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ИНДИВИДУАЛЬНЫХ ИЗОМЕРОВ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ АНТАГОНИСТОВ АДЕНОЗИНА | 1992 |
|
RU2057752C1 |
| ПРОИЗВОДНЫЕ ПИРАЗИНА И ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ | 1992 |
|
RU2124008C1 |
| Способ получения пиперазинсодержащих углеводородов или их кислотно-аддитивных солей | 1986 |
|
SU1574174A3 |
| Способ получения производных 1,2,4-триазолокарбамата или их кислотно-аддитивных солей | 1985 |
|
SU1436873A3 |
| Способ получения 9-амино-5,6,6 @ ,7-тетрагидро-4Н-бензо @ , @ тиазоло @ 4,5- @ хинолинов или их кислотно-аддитивных солей в виде рацемата, энантиомеров или смеси энантиомеров | 1987 |
|
SU1480771A3 |
| Способ получения @ -(2-метоксиэтил)-нороксиморфона или его кислотно-аддитивной соли | 1983 |
|
SU1195909A3 |
Изобретение относится к гетероциклическим соединениям, в частности к получению производных 3-бром-2,6-диметоксибензамида ф-лы @ -CO-NH-HO-N-CH2 @ -X, где X-H, F или CL,в виде кислотно-аддитивных солей, которые обладают фармакологическими свойствами. Цель - разработка способа получения более активных соединений. Получение ведут реакцией N-(8-бензил-6-окси-3-нортропанил)-2,6-диметокси-3-бромбензамида или его N-CL - или и F - бензилпроизводного с 2,6-диметокси-5-бромбензойной кислотой в присутствии акцептора кислоты триэтиламина в среде инертного растворителя с последующим выделением целевого продукта в виде кислотно-аддитивных солей. 1 табл.

| Патент ФРГ № 3340629, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1990-03-07—Публикация
1987-08-28—Подача