С Јъ





Изобретение относится к гетероциклическим соединениям, в частности к получению 1,3,4-тиадиазол 2 циан- амида ф-лы (I); CH-S-C(NR,12.)N, где RJ - Н, R,, CN, или их фармацевтически приемлемых солей, обладающих противовирусной активностью. Цель - разработка способа получения более активных соединений. Получение ведут реакцией соединения N CH-S-C((NlTu)(, где R ( - алкил , с аммиаком. Для получения целевого соединения (I), где R 5 - Н, а Кд. - CN, и соединения (I), где R и R образуют «СОШ), разделяют эти соединения с последующим вьщелением целевого продукта и при необходимости переводом его в фармацевтически приемлемую соль путем обработки соответствующим органическим или неорганическим основанием. Предпочтительно реакции с аммиаком подвергают соединение, где Rf - меI СП тил. 1 а.п. ф-лы, 4 табл.
Изобретение касается способа получения нового производного 2 амино 1,3,4- тиадиазола, а именно 1,3,4- тиадиазол 2-цианамида или его фяг-ма- цевтически приемлемых солей формулы
.S Mi-CN
If П N-N
обладающих противовирусными свойствами.
Цель изобретения - получение HQ- вого производного 2-амино-1,3,4-тиадиазола или его фармацевтически приемлемых солей, обладающего Фармакологическими преимуществами перед 2- амино-1,3,4-тиадиазолоМо
Пример получения. Этиловый сложный эфир (1,3, диазол 2 иламино)тиоксометшт карбаминовой кислоты.
В перемешиваемый раствор 19,2 г
(190 мл) 2-амино-1,3,4-тиадиазола в 200 мл ацетонитрица добавляют одной порцией 25 г (190 мм) этоксикарбонил изотиоцианата Реакционную смесь пе
CD
Ы
ремешивают при 24°С в течение шестнадцати часов. Осадок собирают фильтрацией, промывают три раза этилацета- том и сушат, в результате чего полу- чают 35 г (выход 80%) этилового сложного эфира Х1,3,4-тиадиазол-2-иламино)тиоксометид карбаминовой кислоты
Вычислено; %: С 31,02; Н 3,47; N 24,12.
C6H6N40ZSZ
Найдено, %: С 31,32; Н 3,27; N 24,40.
Пример получения2. 1,3,4 Тиадиазол-2 илтиомочевина.
Раствор 10 г этилового сложного эфира Ј( 1,3,4-тиадиазол-2 иламино) тиоксометил -карбаминовой кислоты (из примера 1) в 150 мл 1 н„ раствора гидрата окиси натрия кипятят с обрат- ным холодильником в течение 90 мин. Раствор охлаждают и концентрируют выпариванием при пониженном давлении. Осажденное твердое вещество собирают фильтрацией и растворяют в 20 мл воды Водный раствор подкисляют добавлением 200 мл 1 н. раствора хлористоводородной кислоты. Продукт собирают фильтрацией и подвергают рекристаллизации из И,М-диметилформамида, в результате чего получают 5 г 1,3,4- тиадиазол-2-илтиомочевины. Температура точки плавления 253 С.
Вычислено, %: С 22,49; Н 2,52; N 34,975 S 40,02.
C3H4N4S2
Найдено, %: С 22,73; Н 2,33; N 34,74; S 40,26.
Пример 1. Метиловый сложный эфир н -1,3,4-тиадиазол-2-илкарбами- мидотионовой кислоты.
Смесь 4,8 г 1,3,4 тиадиазол 2-ил тиомочевины (из примера получения 2) в 45 мл 2 н. раствора гидрата окиси натрия, 15 мл этанола и 4 мл метил иодида нагревают до 40°С и поддерживают при этой температуре в течение десяти минуто Смесь подкисляют добавлением 50 мл 1 н. раствора хлористоводородной кислоты. Реакционную смесь концентрируют выпариванием при пониженном давлении Осажденное твердое вещество собирают фильтрацией и сушат, в результате чего получают 3,02 г метилового сложного эфира N - 1,3,4 тиадиазол 2-илкарбамимидотио новой кислоты. Температура точки плавления 116-117°
0 5 Q
0
с
5
0
Вычислено, %: С 27,57; Н 3,47; N 32,15; S 36,80.
C4H6W4S4
Найдено, %: С 27,78; Н 3,55; N 31,93; S 36,54.
Н-ЯМР (300 МГц) J (D6 Si) U: 2,2; (ЗН S, СН3); 8,90, шир. с. (2Н, NH2); 9,08, с, (1Н, кольцевой Н),
Масс-спектр магнитной индукции (МИ): исходный ион 174.
П р и м е р 2. Сложный этиловый эфир N -1,3,4 тиадиазол 2-илкарбами- мидотионовой кислоты
S N.NH2
fT,c
N-N S-CH2CH3
Раствор 3,2 г (20 мл) 1,3,4-тиади- илтиомочевины в 100 мл N,N- диметилформамида, содержащий 1,6 мл (20 мм) этил иодида и 2,12 г (20 мл) карбонат натрия, перемешивают при 24°С в течение двадцати четырех часов. Реакционную смесь фильтруют и фильтрат концентрируют до масла при помощи выпаривания растворителя при пониженном давлении. Масло подвергают хроматографической обработке на колонне, содержащей композицию Уотер- за, с использованием для элюирования смеси 75% этил ацетата/гексан (объем/объем) . Соответствующие фракции собирают, концентрируют до сухого состояния, в результате чего получают твердое вещество, которое после кристаллизации из диэтилового просто- го эфира и гексана идентифицируют, как 2,08 г N -1,3,4 тиадиазол-2 ил карбамимидотионовой кислоты.
Вычислено, %: С 31,90; Н 4,28; N 29,76; S 34,06.
С N482
Найдено, %: С 32,18; Н 4,18; N 29,59; S 34,08.
ИК (КВг), см : 3259,9; 3089,2; 1624,2; 1510,4; 1416,8; 1377,3; 1347,1; 1247,1; 1209,5; 718,5.
Масс-спектр МИ: 188.
Примеры . Следующие сложные эфиры тиадиазолилкарбамимидоти- оновой кислоты получают в результате взаимодействия 1,3,4-тиадиазол-2- илтиомочевины с алкилгалогенидом в соответствии с методиками, которые использовали в примерах 1 и 2.
Н-бутиловый сложный эфир N -1,3,4- тиадиазол-2-илкарбамидотионовой кислоты, выход 1,68 г, температура точки плавления 40вС.
Масс-спектр МИ: 216.
Хлоргидрат сложного 2-пиридинил- метилового эфира N -1,3,4-тиадиазол 2-илкарбамимидотионовой кислоты, выход 3,72 г„
Н-ЯМР (300 МГц) (Dg ДМСО/Ме4 Si) Ј: 4,64 (с., 2Н, СН2); 7,82 (т., 1Н, Н пиридина), 7,98 (д., 1Н, Н пиридина), 8,40 (т., Н, Н пиридина), 8,79 (д., 1Н, Н пиридина), 9,11 (с., 1Н, кольцевой Н)„
Масс-спектр МИ: 251.
Цианометиловый сложный эфир N - 1,3,4-тиадиазол-2 ил карбамимидоти оновой кислоты, выход 1,04 г„
1Н-ЯМР (300 МГц) (d6 ДМСО/Ме4 Si) Ј: 4,14 (с., 2Н, СН2), 9,09 (ш. с., 24, Н2); 9,15 (с., 1Н, кольцевой Н).
Масс-спектр МИ: 199С
Пример получения Зо Фениловый сложный эфир jjC 1,3,4-тиадиа зол 2-иламино)тиоксометил л-карбами- новой кислоты.
Раствор 3,8 г (50 мл) тиодианата аммония в 100 мл ацетонитрила, содержащий 7,8 г (50 мм) фенил хлорформи- ата, перемешивают при 24°С в течение одного часа. Реакционную смесь фильтруют в суспензию 6,88 т (50 мм) хлор гидрата 2-амино-1,3,4-гиадиазола в 75 мл ацетонитрила и 25 мл окиси про
пилена. Реакционную смесь перемешивают в течение двух часов при 24 С, а затем фильтруют, в результате чего получают твердый осадок, идентифицированный как 6,42 г фенилового сложного эфира Ј(1,3,4-тяадиазол-2 илами но)тиоксаметкп -карбаминовой кислоты
Масс-спектр МИ: 280.
i
Примеры получения 4-6 „ В соответствии с общей методико из примера получения 3 получают следующие продукты:
Н-гексиловый сложный эфир Ј(1,3,4 тиадиазол-2 иламино)-тиоксометил |- карбаминовой кислоты
Вычислено, %: С 41,65; Н 5,59; N 19,43; S 22,24
C40F e T4°2si
Найдено, %: С 41,64; Н 5,31;
N 19,28; S 11,,
Метиловый сложный эфир Г( 1,3,4- тиадиазол 2-иламино)тиоксометил - карбаминовой кислоты.
Масс-спектр МИ: 218.
Виниловый сложный эфир (1,3,4- тиадиазол-4-иламино)тиоксометил)-кар- баминовой кислоты.
Масс-спектр МИ: 230.,
Пример получения 7. Этиловый сложный эфир (метилтио)- (1,3,4 тиадиазол 2-иламино)метил - карбаминовой кислоты:
Смесь 6,96 г (30 мл) этилового сложного эфира Ј( 1,3,4-тиадиазол-1-2- иламино)тиоксометилЛ-карбаминовой ки
примером получения 1, в 45 мл 1 н.
раствора гидрата окиси натрия, содержащую 9,0 г (4 мл) метил иодида и 15 мл метанола, нагревают до 40°С и поддерживают в течение десяти минут. Реакционную смесь охлаждают до 5е С
и фильтруют. Фильтрованную лепешку промывают водой и сушат на воздухе, в результате чего получают 4,72 г этилового сложного эфира Ј(метилтио) (1,3,4-тиадиазол-2-иламино)метшГ|- карбаминовой кислоты„
Вычислено, %: С 34,13; Н 4,09; N 22.75: S 26,04.
Cf HwN4°2sa
Найдено, %t С 34,41; Н 4,84;
N 22,91; S 25,94.
Пример получения 8„ Этиловый сложный эфир (этилтио)-О, 3,4 тиадиаз ол-2 иламино-метил j-карбаминовой кислоты.
Ј(1,3,4 Тиадиазол-2-иламино) тиок- сометил -карбаминовая кислота (6,96 г) взаимодействует с 4 мл этил иодида в соответствии с методикой из примера получения 7, в результате чего получают 1,83 г этилового сложного эфира Ј(этилтио)(1,3,4-тиадиа- зол 2-иламино)метшт -карбаминовой кислоты.
Масс-спектр МИ: 260.
Пример 6. 1,3,4-Тиадиазол 2- цианамид и 1,3,4-тиадиазол-гуанидин.
Смесь 5,0 г метилового эфира N-1, 3,4-тиадиазол-2 илкарбамидотиокислоты (из примера 1) в 50 мл аммиака и 100 мл этанола нагревают в автоклаве при 140°С в течение 14 ч. ТСХ на си- ликагельных пластинках (66% CHJC13, 26% МеОН, 8% НОАс) показала два новых пятна, одно из которых идентично 1 -тиадиазол -цианамид,, Растворитель удаляют выпариванием и неочищенное вещество перемешивают с 200 мл 1 норм. НС1 и фильтруют для
удаления нерастворимого 1,3,4 тиади- азол-2 цианамида.
Выделенное соединение имело следующие характеристики:
FD масс-спектр: 126.
Вычислено, %: С 28,57; Н 1,60; N 44,42; S 2,5,42.
C.
Найдено, %: С 28,95; Н 1,80; N 43,60; S 24,87.
Подкисленный фильтрат выпаривают досуха, остаток очищают с помощью жидкостной хроматографии (HP LC), элюируют 90% МеОН/Н20 и получают 1,5 г 1,3,4 тиадиазол 2-гуанидина„
Это соединение имеет следующие характеристики.
И ЯМР (300 МГц) (D6 ДМСО (Ме Si) Si 8,37 (пир. с. 4Н, NF2), 9,27 (с, 1Н, кольцо);
FD масс-спектр: 144.
Пример. К раствору 1,38 г 1,3,4 тиадиазол 2-цианамида в 10,5 мл 1 норм, едкого натра добав- ляют 100 мл этанола. Смесь фильтруют растворитель удаляют из фильтрата, получая масло„ Масло кристаллизуют из 20 мл метанола и 100 мл изопро- лилового спирта, медленно удаляя ме- танол при помощи выпаривания при П9 ниженном давлении и получают 980 мг натриевой соли 1,3,4 тиадиазол-2 ци анамида.
4НЯМР (300 МГц) (D6 ДМСО ( Si) о: 8,68 (с, 1Н, кольцо Н);
FD масс-спектр: 126
Вычислено, %: С 24,33; Н 0,68; N 37,83; S 21,65.
C3HN4SNa
Найдено, %: С 24,59; Н 0,87; N 38,06; S 21,90.
Как было установлено, тиадиазол или его соли обладают противовирусной активностью в стандартных испы- таниях и, таким образом, могут быть использованы для лечения или профилактики заболеваний, которые вызываются разнообразными вирусами и широко распространены. К общим вирусам, против которых, как было установлено тиадиазолы являются активными, относятся все испытанные штампы А и В гриппа,включая такие штаммы гриппа, как А-Энн-Эрбор, А-Гонг-Конг, В-Ве- ликие Озера, В-Тайвань, В-Сингапур, А-Бразилия, А-Техас, А-Фукушина, В-Мэри-Лэнд и т.п. К другим вирусам, против которых можно использовать
предложенный способ, относятся Пара- Грипп. Респираторные Синциальные Вирусы, различные штаммы Лишая I и И, вирусы ЕСпО и Vaccinia, кори, Seralini Forest, а также те вирусы, которые приводят к синдрому приобретенного иммунного дефицита.
Тиадиазоловые противовирусные агенты проявляли свою активность против упомянутых вирусов как в лабораторных условиях, так и при испытании на живом организме. Особенно детально исследована их активность в живом организме против гриппа А-Энн- Эрбор.
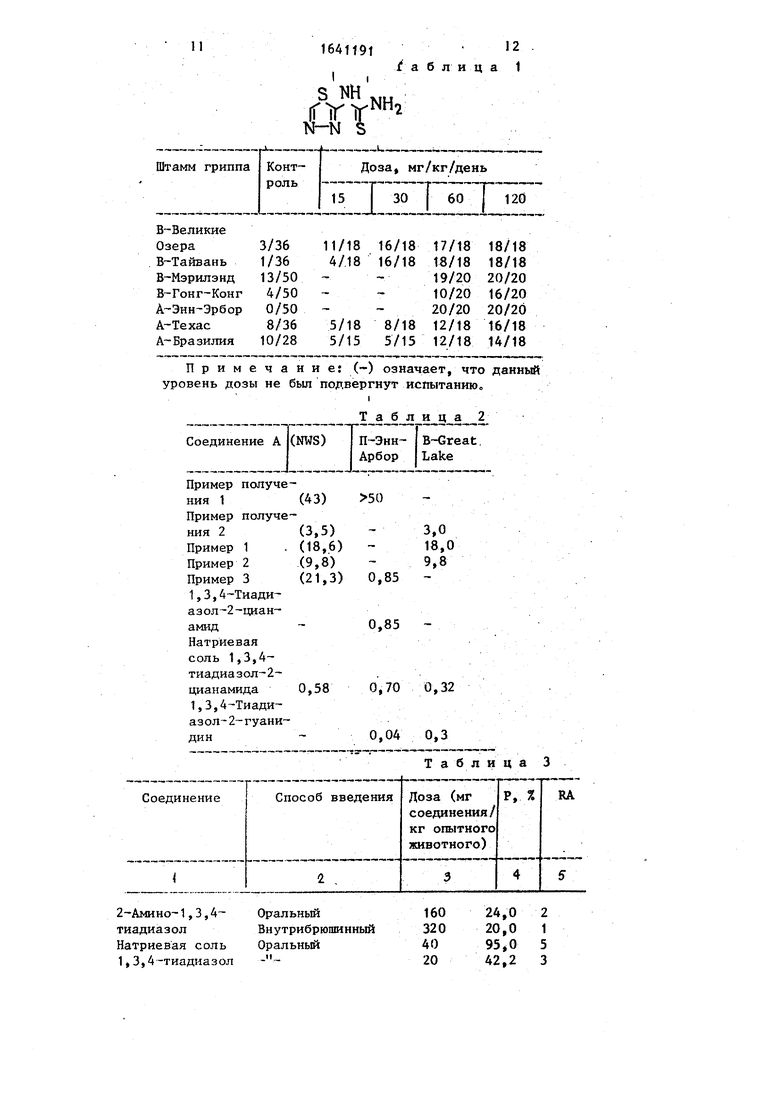
Соединения, являющиеся предметом изобретения, были испытаны на живом организме против самых разнообразных штаммов гриппа, при этом использовали процедуру анализа гриппа у мышей и были получены хорошие результаты. В табл. 1 указана активность соединения из примера получения 2 в широком диапазоне доз при применении его стоматическим способом вместе с кормом к мышам, зараженным различными штаммами гриппа А и В, причем указано количество животных, оставшихся в живых через 10 дн. в каждой испытываемой группе.
Исследование по уменьшению пятен обеспечивает количественную оценку ингибиторов размножения вирусов в культуре клеток ткани в лабораторной системе.
В этом испытании восприимчивые МДСК-клетки выращивали в 25 см2 колбах Фалькон при 37°С в среде 199 вместе с 5% инактивированной сыворотки плода теленка (СПТ) пенициллином (300 ед./мл) и стрептомицином (300 мкг/мл). После образования слившихся монослоев среду для выращивания извлекали и в каждую колбу добавляли 0,3 мл разбавленного соответствующим образом вируса. После адсорбции в течение одного часа при комнатной температуре на поверхности с зараженными клетками наносили равные части 1% Агара и 2% Среда 199, 2,5% СПТ, пенициллин и стрептомицин, варьируя при этом концентрации испытываемого соединения, содержащегося в агаровом накрывающем слое. Эти соединения растворяли в диметил сульфоокиси (ДМСО) в концентрации 10000 мкг/мл, а затем порцию
разбавляли до необходимой концентрации при помощи смеси агаровой сре- ды. Колбы инкубировали до тех пор, пока контрольные колбы не указывали на оптимальный размер пятна (2- 10 мм). Раствор, содержащий 10% формалина и 2% ацетата натрия, добавляли в каждую колбу с тем, чтобы инактивировать вирус и зафиксировать лист с клетками на пластиковой поверхности . Пятна считали после окрашивания окружающих клетки областей кристаллическим фиолетовым красителем. Результаты, полученные для колб дублетов для каждой концентрации, усредняли и сравнивали с контрольными колбами. Ингибирование образования пластинок на 50% (1уо) оценивали при помощи нанесения на график всех результатов с ингибированием в процентах в области от 10 до 90. Результаты, полученные для трех штаммов гриппа (активность ин витро отженные в виде Р и RA (индекс относительной активности: 5 - наиболее ак тивное, 1 - наименее активное).
В табл. 4 описана активность ин виво двух из трех соединений относительно гриппа Гонконг-В. Информация в столбцах таблицы та же, что в табл. 3.
10 Соединения изобретения характеризуются низкой степенью токсичности к живым организмам.
15
20
Формула изобретения
. Способ получения 1,3,4-тиа- диазол-2-цианамида формулы
rrNRlR
N-N
носительно вирусов гриппа представлены в табл. 2.
50
Для использования в лабораторных условиях эти соединения могут быть добавлены в культуру ткани с целью подавления роста вируса в ней.
Данные in vivo, сравнивающие активность ин виво 2 амино-1,3,4-тиа- диазола, 1,3,4-тиадиазол-2-цианамида и натриевой соли 1,3,4-тиадиазол-2- цианамида против вирусов гриппа Энн- Арбора и Гонконг-В, получены и проанализированы с использованием описанной методики.
В табл. 3 описаны активность ин виво указанных трех соединений по отношению к гриппу Энн-Эрбор-А. Стол бец 1 этой таблицы раскрывает проверяемое соединение. Столбцы 2 и 3 описывают способ, используемый для введения проверяемого соединения, и вводимую дозу соответственно. Столбцы 5 и 6 описывают результаты, вырагде. R - Н,
,мкг/мп) - CN
или его фармацевтически приемлемых
солей, отличающийся тем, что соединение формулы
30
(NH2l(SRO
N-N
алкил ,
где R 35 подвергают реакции с аммиаком для получения целевого соединения (I), где R ( - Н, а Кл - CN, и соединения (I), где R 4 и RЈ образуют -C(NH2)2, и разделяют эти соединения с после-
40 дующим выделением целевого продукта или переводом в его в фармацевтически приемлемую соль путем взаимодействия с соответствующим органическим или неорганическим основанием.
45 2. Способ по п. 1, отличающийся тем, что реакции с аммиаком подвергают соединение формулы (II), где R - метил.
4119110
женные в виде Р и RA (индекс относительной активности: 5 - наиболее ак тивное, 1 - наименее активное).
В табл. 4 описана активность ин виво двух из трех соединений относительно гриппа Гонконг-В. Информация в столбцах таблицы та же, что в табл. 3.
10 Соединения изобретения характеризуются низкой степенью токсичности к живым организмам.
15
Формула изобретения
. Способ получения 1,3,4-тиа- диазол-2-цианамида формулы
20
rrNRlR
N-N
30
(NH2l(SRO
N-N
алкил ,
где R подвергают реакции с аммиаком для получения целевого соединения (I), где R ( - Н, а Кл - CN, и соединения (I), где R 4 и RЈ образуют -C(NH2)2, и разделяют эти соединения с после-
дующим выделением целевого продукта или переводом в его в фармацевтически приемлемую соль путем взаимодействия с соответствующим органическим или неорганическим основанием.
Примечание: (-) означает, что уровень дозы не был подвергнут испытанию
i
Соединение A (NWS) I B-Great
Оральный
Внутрибрюшинный
Оральный
Таблица 3
24,02
20,01
95,05
42,23
Таблица 4
| Преобразователь перемещения в код | 1988 |
|
SU1531221A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| I | |||
| Med | |||
| Chem | |||
| Контрольный висячий замок в разъемном футляре | 1922 |
|
SU1972A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ АВТОМАТИЧЕСКОГО ПУСКА В ХОД ТУШАЩИХ ПРИБОРОВ | 1923 |
|
SU1082A1 |
Авторы
Даты
1991-04-07—Публикация
1988-06-29—Подача