Изобретение относится к получению новых 6-(ациламиноарил)-4,5-дигидро- 3(2Н)-пиридазинопроизводных, которые оСпадают подавляющими агрегацию тромбоцитов, гипотензивными, подавляющими наделение желудочного сока или положительно изотропными свойствами.
Цель изобретения - получение новых 6-(ациламиноарил)-4,5-дигидро-3-(2Н)- пиридазинонов, обладающих ценными фармакологическими свойствами при низкой токсичности.
Пример . 5,8г (20 ммоль) 6-Гп-(3-хлорпропиониламино)фенил -4,5- дигидро-3(2Н)-пиридазинона перемешивают в течение 8 ч при 80°С с 3,5 г (25 ммоль) карбоната калия и 2,17 г (25 ммоль) морфолина в 50 мл диметил- формамида. После прибавления 500 г льда (воды) кристаллизат- отсасывают. ,
После перекристаллизации из диметил- формамида воду высушивают в высоком вакууме при 50°С и получают 5,4 г (82%) 6-(п-3-(1-морфолино)-пропионил- аминофенил)-4,5-днгидро-3(2Н)-пирида зинона в виде бесцветных кристаллов. Т 183-185вС.
Аналогично примеру 1 получают соединения примеров 2-102 (см.табл.1). Если соединения выделяются в виде масел, то их можно очищать путем экстракции хлористым метиленом и/или хроматографии на колонне через снлика- гель или окись алюминия смесями хлористого метилена/метанола в качестве г растворителей.
Аналогично примеру 1 получают преобразованием 6-Јм-(3-хлорпропионила-. мино)-фенил -4,5-дигидро-З(2Н)-пириЈ
00
ГС On
и
дазинона соединения примеров 103-105, приведенные в табл.2.
Аналогично примеру I получают из 6-fn- (3-хлорпропиониламино) -фенил - 3(2Н)-пиридазинона и 6-Јп-(3-хлорпро- пиониламино)-фенил }-5-метил 3(2Н)-пи- ридазинона или соответственно (3-хлорпропиониламино) -фенилТ-б-метил 3(2Н)-пиридазинона соединения примеров 106-115 приведенные в табл.3.
Аналогично примеру 1 получают взаимодействием 6-Гп-(хлор- или бромал- каноил(амино)-феншГ -5-метил-3(2Н)- пиридазиноков с 4-фенилпиперидином или фенилпиперазином соединения примеров 116-126, приведенные в табл.4.
Пример
г f
, , 127. 6-{п- з-(2-фенил этиламино)пропиониламино| -фенил (- 4, 5-дигидро-З(2Н)-пиридазинон.
11,18 г (40 ммоль) 6-Гп-(3-хлор- пропиониламино) - фенил1-4,5-дигидро- 3(2Н)-пиридазинона-вводят Б 250 мл этанола. После прибавления по каплям 26,5 г (220 ммоль) 2-фенилэтиламина кипятят в течение 6 ч с обратным холодильником. Нерастворимые части от- фильтровывают и маточный раствор после удаления растворителя кристаллизуют прибавлением ацетона. После двухкратной перекристаллизации из метанола получают 5,3 г 6-Гп-р-(2 фенил этиламино)пропиониламино фенил|-4,5- дигидро-3(2Н)-пиридазинона-НС1. Т 2б9-270°С.
Для перевода в свободное основание полученный гидрохлорид растворяют в метаноле и прибавляют эквимолярное количество метилата натрия. После удаления растворителя и прибавления воды вещество экстрагируют хлористым мети- яеном. После высушивания фазы хлорис того метилена над и удаления растворителя вещество смешивают и отсасывают. Получают 6-|п-13-(2-фенил- этиламино)пропиониламшк -фенил|-4,5 - дигидро-3-(2Н)-пиридазинон. Т
П
13°132°С.
Фармакологические испытания полученных соединений проводили согласно следующим методам.
1, Торможение индуцированной коллагеном агрегации тромбоцитов человека В пробирке.
Богатая тромбоцитами плазма получается центрифугированием веночной
g
5
0
5 Q г
0 5
0
5
цитратной крови (300 г, 10 мин при 4°С). Фотометрическое измерение агрегации тромбоцитов осуществляется при добавлении MgClj (конечная концентрация 10 ммоль/л) и коллагена типа Stago (конечная концентрация 0,02 мг/мл) в агрегометре Ворна МКЗ. Мерой агрегации служит максимальное изменение экстинкции за секунду.
Тормозящая агрегацию активность веществ проверяется через инкубационный период, составляющий 10 мин.
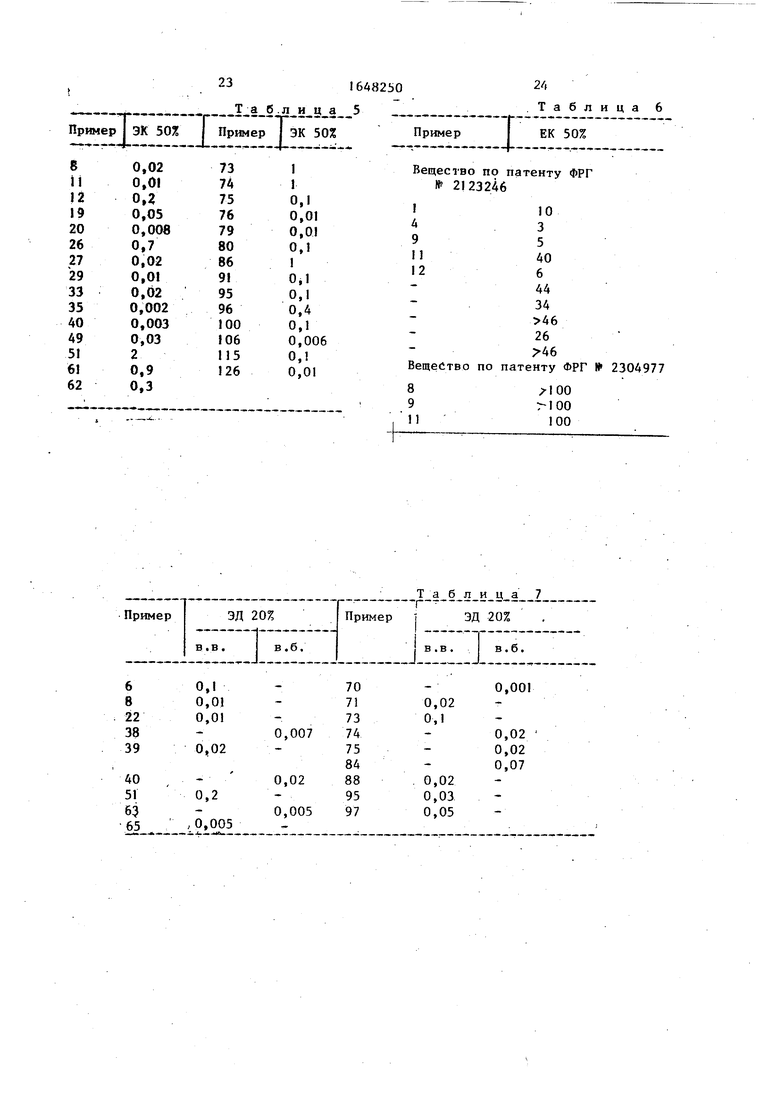
В качестве ЭК 50% определяется концентрация, вызывающая 50%-ное торможение агрегации, приведенная в табл.5.
При опыте I испытанные вещества показывали значения, приведенные в табл.6.
2.Понижающее кровяное давление действие на крысе.находящейся под наркозом.
Для исследования понижающего кровяное давление действия группам по 3-5 крыс-самцов штамма Sprague-Dawley (240-280 г), находящихся под урета- новым наркозом, вводится вещество внутрибрюшинно или внутривенно (1,78 мг/кг внутрибрюшинно).
Измерение кровяного давления в сонной артерии осуществляется с помощью датчика Стэтэма. В качестве ЭД 20% определяется доза, понижающая среднее кровяное давление в сонной артерии на 20%, приведенная в табл.7.
В отношении их токсичности соединения 1 соответствуют или являются менее токсичными, чем известные соединения.
При опыте 2 (снижение кровяного давления) определяли значения, приведенные в табл.8.
3.Торможение секреции кислоты желудочного сока.
Торможение кислот секреции кислоты желудочного сока выражается в повышении значения рН слизистой желудка. Оно исследуется на группах по 4 крыс-самок штамма Sprageu-Dawley (160-180 г). Животные не получали в течение 48 ч никакого корма (воду по желанию). Они получают предварительно (через рот) различные дозы испытуемых веществ. Через 1 ч животные наркотизируются гексаборбарбиталом натрия (46,4 мг/кг внутривенно). Затем вводится в ЖРЛУДОК электрод рН и из о р м у л а изобретения
Способ получения 6-(ацнламино ,арил)-А,5-дигидро-3(2Н)-пиридазино- производных общей формулы
RiRZ
fVRj-CONH
N-NH
де заместители фениленового остатка находятся друг относительно друга в положении мета или пара{ А и В - водород или вместе образуют связь;,5 RJ - водород или С -С -алкил; Rg, - водород или R j и R вместе означают остаток алкилен, при условии, что А и В - водород, 40 R3- Cj-C -алкилен с неразвет- , вленной цепью, незамещенный или замещенный одним- двумя С -Су-алкилами; R,j.-a) имидазол-1 -ил или д5 ) группа общей формулы
/N
(CH2)m
где пунктирная линия означает добавочную связь; R,
и означают водород, ал кильные остатки , незамещенные или замеи R, - одинаковые или различные 6
m 0,1;
или R и Rg
вместе образуют ал- ,киленовую цепь с , или в) группа общей формулы
25
R9-N-CH2-CH2-N- (СН2)РХ
где Rft 9
углеводородный остаток Cj-Cj или С(Ј, незамещенный или замещенный фенилом, незамещенный или замещенный меток- сигруппой, гстероарил с 5-6 членами кольца, который может содержать атом кислорода;
р 2,3, или г) группа общей формулы
- N RIO R«,
где R
(о
и атомы водорода, углеводородные остатки. , незамещенные или замещенные одним или двумя фенилами, или циклоалкильные группы Cj-Cjj, незаме- ., щенные или замещен-, ные фенилом, или адамантильные остатки, или бензоконденсиро- ванные циклоалкильные1 группы Cy-C7t или д), группа формулы
Ь5
(Ш2)2
)
R13 ACH2-N,
де R и R,a водород, атомы галогена, алкильные или алкоксильные ос- татки , или
) группа общей формулы
R|VA
ЈЈ
RB
де G - атом кислорода или серы;
Rj4 и RJC Н или С|-С ралкил при условии, что если R., R, А и В означают
10
15
атомы водорода, то RJ не означает метилен, незамещенный или замещенный алкилом CJ-GJ-, и если R, А и В озна-20 чают атомы водорода, то Rf означает атом водорода или алкил , RJ означает метилен, незамещенный
25
или замещенный алкилом, R не означает группу формулы по п.ц, где и Rj9 водород или Сд-Сц. ал- кил,
или их фармацевтически приемлемых солей, отличающийся тем, что соединение общей формулы
Ri R2
-M-ifi
5
0
N-N н
2 и R3имеют
5
X-R3-CONH
где А и В, RI, R2 и R3имеют указанные значения;
X - атом галогена,
подвергают взаимодействию с соединением общей формулы
R4- H,
где R имеет указанные значения, с последующим выделением целевого про дукта в свободном виде или в виде их фармацевтически приемлемых солей.











| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пиридазинаминов, или их фармацевтически приемлемых солей присоединения кислот, или их стереохимических изомеров, или их таутомеров | 1985 |
|
SU1384198A3 |
| Способ получения производных гетразепина | 1989 |
|
SU1738089A3 |
| ПРИМЕНЕНИЕ ПЕРФТОРАЛКИЛСОДЕРЖАЩИХ КОМПЛЕКСОВ МЕТАЛЛОВ В КАЧЕСТВЕ КОНТРАСТНЫХ ВЕЩЕСТВ ПРИ МАГНИТНО-РЕЗОНАНСНОЙ ТОМОГРАФИИ ДЛЯ ВИЗУАЛИЗАЦИИ ВНУТРИСОСУДИСТЫХ ТРОМБОВ | 2003 |
|
RU2328310C2 |
| 7-АЦИЛАМИНОЦЕФАЛОСПОРИНЫ, ЗАМЕЩЕННЫЕ В ПОЛОЖЕНИИ 3 ЦИКЛИЧЕСКИМИ АМИНОГУАНИДИНОВЫМИ ГРУППАМИ | 1999 |
|
RU2245884C2 |
| Способ получения производных изоксазола | 1986 |
|
SU1493106A3 |
| Способ получения производных 1,4-дигидропиридина | 1988 |
|
SU1650011A3 |
| Производные оксадиазолилалкилпурина, проявляющие противокашлевую активность | 1988 |
|
SU1602862A1 |
| Способ получения 6-метил-3,4-дигидро-1,2,3-оксатиазин-4-он-2,2-диоксида или его калиевой соли и способ получения аммоний ацетоацетамид-N-сульфонатов | 1985 |
|
SU1342418A3 |
| Способ получения производных карбаминовой кислоты | 1985 |
|
SU1402253A3 |
| ПРОИЗВОДНЫЕ ХИНОЛОН- И НАФТИРИДОНКАРБОНОВОЙ КИСЛОТЫ В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫХ ИЗОМЕРОВ, ИХ ГИДРАТЫ И СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2105770C1 |
Изобретение относится к гетероциклическим соединениям, в частности к получению 6-(ациламиноарил)-4,5-ди- гидро-3(2Н)-пиридазинопроизводных или их фармацевтически приемлемых солей. Цель - разработка способа получения указанных соединений. Получают из гало идпроизводного 6-(алканоиламино- арил)-4,5-дигидро-З(2Н)-пиридаэина и имидазола или в случае необходимости соответствующего соединения, 9 табл.
С«Н5 Т ;Ы-СН2СН2- C H5 O N CH2CH2
LiX N-CH2CH7- vx scN-CHjCHj-
@-Ок-снгсн2и @KDN CH2CHV
;м-снгсн 13
-CH2CH2Таблица I
R, R2
- -м-viч.
p-R -Rj-CONHN N
и4о
Hto
CH,
CH.
CH.
87-89 165-: 66 1 19-121 191-192 228-230
i/4
238-240
D нг°
-снг2 44-247
-СН -ГН2240-241
UZZZZZJ
i 4 2 2
,s Оы-снгсн7и
-ClJ2CH7i7 QN-CH2CH218Ј)N-CH CH219CgH5-NXDN CH2CH7
COC2H5
NC.
20
,сн,« c,HH5 -CHlCHr
C HcS°HsK -CH CH - .™г iS O -0 0
©
2 C6H5-C-N-ON CH2CH
0
26
CeHs-C-N-O-CHiCHf 0
CjHa-CN-CHjCHjr
28C$Hs-()N-CHaCH229C1-@H)N-CH7CHZ30F- 0)CN-CH7CHr31HO- I)N-CHZCH2 OE°52S Ј -I552i-i
ZZZZ Z ZIJZZLLZ
-Cllj-CHjj-CHj-CH,- 191-192
CH
НЙ-150
D t°
150-152
I/A Hto3
-CHj154-155
l,25 Нго -CHt-CH2115-117
вго
CH.
H208-210
С1Ц
239-240
Си,о
CH,
HПЭ-П5
Г«Л
H197-199
D «t°J
CH.
H168-169
CH,
H245-247
H261 -263
D «t°3
CH,
H204-J06
H235-236
D H«°J
CH,H200-201
CH,H210-212
i/2 lyfjCH,H187-1W
36
- ((-NQN-CHaCHj- CJ
37
g)-NQN-CH2CH2Cl
38
ОСНз 0)-NQN-CH,CH2
CH2-NQN-CH2CHr H3CO
C6H5-N0N-CH CH2
41C6H5-NQN CH2CH21,2HOCH2CH2-MQN-CH2CH2
A3
HOCH2CH2-NQN-CH2CH2 C6H5CH2-NQN-CH2CH2- 45 C6H5-CH2-NQN-CH2CH2А6 -О снгсн2„ C2M502C-NQN-CH2CH248 (RJ-NQN-CH2CHj1 49 С°Хы)ы-сн,сн7
CH,
H145-147
i/2 Hto
H235-236
207-209
i/2 иго снэи86-89
fl/5 HtoJCH3H261-263
255-257
Г1 z°
CHjH228-230
И200-202
fl,5 H2oJCH,H193-195
l/4
H252-254
I
50 (°Л-О-снг$нг
И J
51 -сн7сн2-1
52 О-снгсн,53СвН5-См-СНгСбН5- -снг54
55 QN-ШГ
5 CsHs-CX сн
s: С6н5 -сн5СН3
58C6H5-ON-CH7CH7CH259с6н5О-сн2снгсн НС1
60CeHs-CN-0 0 0
61CeHs-CN- 0 ™ 0
62QN-CH2CH7CH2CHa63(о О -сн2-снг64CeHs-NQN-СНг-сНгCHjO
45 снэо-)-мО-сн2
СН30
,, снЭ°ТгГТ х1
CHjO- N-CHa-CHj67OKDN CH2CH2
68C6H5 QN-CH2CH2CH/
..5Кв93 5 И«.тавпА 1
L1J..-41$J6
i НгО НН224-225
l Hto CH3H198-200
l/2
H248-251
CM,H
170-171
i r4o
-CHt-199-200
-CH,184-185
l HtOJ
194-IJS
i нго
CH,
112-113
l/2 ,Н
295-297
l/2
129-130
l/2 ,Н
115-117
/2
H190-192
CH,H118-124
-CHt-CHt-255-257
CH,H92-96
3/4
H129-130
H263-265
il207-209
69 C«HS-Oi-CH2CH2- СН3
70 (О)
}N-CHrCHa4Ct
71 CfiHrNQ№-CHjCHj
« СбН.гСН2СН7JHfN-CH2CH273
H
t -N-CH2-CH2CH3 n-CnH9-N-CHy-CHj C$H5 CH3 75 CjHs-CHj-CH-Wz-N-CHj-CHj
U
СИэ-С- -мО-Фг-сНгCH3СНз- -NQN-CHa-CHj§V-NQN-CH2-CHZ
C -NQN-CH2-CH 2 - CF3 C6H5-CH- CH-CH2-NQN-CH2-CH7CH3CSH5-CH-NQN-CH2-CH2C6H5-CH2-CH2-r)N-CH2- CH г83 CH}-XDN-CH2-CH 84
CHj CHjCH3
HO-C-(CH2)(CH2)2-CH-NQbMCH2lrCH3CH3
85
C -OTCH,0
86
N-CH,CH,I
I
Продолжение табл.I
f s б
183-184
CHfH
63-65
-CH2-265-267
H121-123
CH3H
f25
CH,
H60-66
CH,H
50-54
CH,H
201-202
CH,HI25-127(0,5H20)
CH,К185-187
CHj
H85-87
CH,H132-135
СНЭН115-120
CHjH95-102
CH,
Hor
CH,И200-202
CHjH187-J 89
87 -СН2-СН288 SQN-CH2-CH,
Ul2-LHj
п- С,г H j-NH-CHj-CH CHjO,СН5
CHjO X 4H2-CH2-N-CHrCH2СН3
(сн5Г):н-ы-сн2-сн2.ГЦ-МН-СН2-СН293I -Adementyl-NH-CHj-CI j §XD NH CHrcH2CHj
Ч
0(JN-CH2-CH W y
сн,
+QN-CH CH
С6Н5-О СН7 СНГ C6H5-CHj-N -CH2-CH2NH-CH2-CH2(Oj -NH-CHj-CHjCHj(yNH-CHj lHCI
CHJ CH3
102
+Q -NH-CH2-CH2По ТСХ, Ч10г (Mprck), толщина слоя 0,25 мм, AcOH:EtOAc:MeOH 20:5:5, R 0,13
1648250
иг:
„ Продолжение тзРл.1
си.
II85-87
сн.
Н183-185
сн,
Н 123-Ш
сн,
Я58-60
СН,
НU9-I50
СН,
11122-126
CHj, 1175-78
Cll,II 39-142
175-177
Cll.
H13-95 (0.5|140)
СНЭ11170-173
CH3II226-228(,5HzO/
CH,
H270-271
CH,
H164-185
19
1648250 Rl «2
R rR3-CO-NH
H-U-H .
iH
--
V,
. - -rt-f-n-bat-fi
IIEllIl
i CtHs-QN-CHjCHf10 C|Hs-) cHjCH2Ю5O-CHz-CH2Я
R, R,
RrVc-NH- o -4 o
H
Пример
R4-R,10
)м-снгсн2, ,0 -сн2-сн2©- lON-CH2-CH2111 (O-CHfCHtN
112
(OK ;N-cHo-CH,2-v.n2
11 з (5)-NON-CH2-CH2114
@XjN-CH2-CHr
115
1648250 Rl «2
20
H-U-H . Таблица
Т„м С
CH|
H189-190
H182-183
H154-156
R, R,
Таблица 3
Г R Т R4 I Т„Л
H235-237
H249 (l 0,5 )
II300 (X0,5 HZ0)
H250-251 (M HClxl H20)
H260-261 (0,25 Hj.0)
H144-145 (Hi HfO)
CH3H223-226 (0,5 )
CHH124-127 (nHClx H.O)
CH5 239-240 №20)
H209-212 (xO,75-H20)
Таблица 4
23 (патент ФРГ Ю,0 2304977)
| ПОЧВООБРАБАТЫВАЮЩИЙ АГРЕГАТ | 1995 |
|
RU2123246C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Заявка ФРГ В 23049777, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1991-05-07—Публикация
1984-01-20—Подача