Изобретение относится к химии фос- форорганических соединений, а именно к способу получения новых окисей трис-{гид- рохлорид-{3-имино-3-алкокси(алкилтио)про- пил}-фосфинов общей формулы
2 ХО
3
СП
где R - Сч - Се ал кил или изоалкил;
Х-О или S,
которые являются полупродуктами для получения функциональных третичных фосфи- ноксидов.
В настоящее время окиси третичных фосфинов находят широкое применение в
различных областях народного хозяйства и техники в качестве добавок к полимерам, экстрагентов, полупродуктов для синтеза физиологически активных веществ, моющих и косметических препаратов, э также для извлечения редких и драгоценных металлов.
Целью изобретения является разработка доступного способа получения окисей трис-{гидрохлорид- 3-имино-3-алкокси(ал- килтио)-пропил}-фосфинов.
Предлагаемый способ заключается в том, что окись трис- -цианэтил)-фосфина подвергают взаимодействию со спиртом или тиоспиртом и хлористым водородом, взятыми при молярном соотношении 1:(3- 3,3):(7,3-20,8), в среде диоксана при 8-15°С
О 4 Ы Ю
с последующим взкуумированием реакционной смеси и кристаллизацией целевых продуктов из д /юкоановых растворов. Процесс протекает по следующем схеме:
р (си2си 2та Vi-з R хн -знс о
тг (М
- РССИоСИоС
о
3
где R - Ci-Сб-аякил или и.чозлкил;
X - С /ши 3,
Исход; и п 1-с-|/ циэнзтил)-фос- ф-л;;а ipfiM-irc s , j. i; ,-- e ::U M веществом, которое не расыо.оячо к срг; к /г:ескцх растворителях, сил О - 3Я иГ- рГЬ М ДУ10:СОЗН. Б
воде хоро:ио р-:,лi.riptb o, нс осуществить процесс . Г лд1 ряс ссоре невозможно вследств / мизхой гидролитической устойчивое 1. |г-, / : огмых гидрохлорядов, Попытки ооущьствленик процесса в суспензиях приводя к слипанию частиц исходной ОКИСИ ГрИС-(/ ЦИЗНЗТ1/:.н)фОСфКНЗ У
условиях синтеза. Возможность осущестз- лзния указанного процесса достигается в результате 1чспользог. новой среды - диохсанз, насыщен юге хлористым оодоро- дом. Ргсгвор:лмость и одмой окисм фоссЬи- на и полученных п идуюов обсуловленз
ВЫСОКОЙ ПОЛЯрНОС ГЬ О СИСТЯ 1Ь ДИОКСЭНхяорлсгый воАОрод. 1спользоаа;- 8 в н о м п о о ц о с с е з и а ч и е л ь ч о г о и з 5 У г к а хлорис 0го водорода /мйел и другие положительные стороны. Ьагожер, з реакциях синтеза г длохяор.асп имлдатов хлористый водород я пяется гэтолько рэагомтом, но и катализатором. И за УТОК хлористого водорода зи&чительии псзышзет скорость процесса и под сольет достигнуть выхода цо- левых продуктов, гфа О/ чес:;.и близкого к коя 1честве;-;но /|у (98,5-99,7%), что позволяет осуществить выделение полученных целевых вешиств из реекиионкой смеся - простым и эффект мвным способом Вы деление получен к -ix веи .естй достигают удалением части избыточного хлористого водорода (при этом отгоняется из системы i , часть диоксина) путем вэкуумирования с помощью водоструйного насоса при комнатной температуре. Для белее эффективного удаления хлористого водорода через полученную реакционную смесь с помощью ;сг-лилляра пропускают осушенный воздух. В конце процесса закуумирования из реакционной мчссы проходит кристаллизация полученных целевых соединений, которые
далее отделяются фильтрацией, многократно промываются нз фильтре сухим диокса- ном, После удаления следов растворителя вакуумированием с почти количественными
выходами (не ниже 98,5%) получают гидрохлориды формулы (I),
Полученные гидрохлориды представляют собой белого цвета сыпучие кристаллические вещества, гигроскопичные на
воздухе, поэтому длительно хранить их следует в условиях, исключающих попадания влаги.
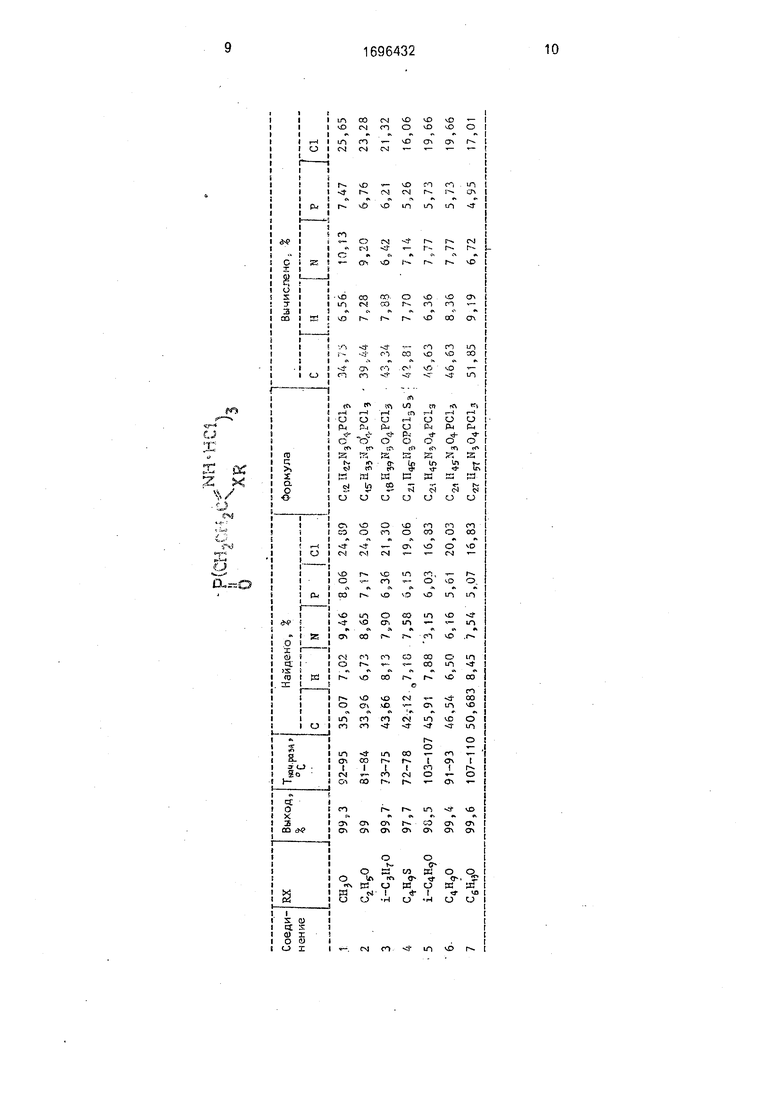
Свойства и данные анализов полученных соединений приведены в таблице 1,
П р л м е р 1, Получение окиси трис- гидрохлорйд-(3-имино-3-бутокси)пропил -фос- фина (соединение 6).
В колбу, снабженную барботером и от- воднсй трубкой, помещают 2,1 г {0,01 моль)
окиси трис- -цизмэт 1л)-фосфина, 2,5 г (0,034 моль) абсолютного спирта, 9 мл абсолютного диоксана. Далее реакционную смесь насыщают сухим хлористым водородом при температуре около 10° С. Отвод
тепла осуществляют с помощью охлаждающей бзни, состоящей из льда и воды. Через 20 мин насыщение хлористым водородом прекращают (при этом окись трис-(/ -цианэ- тил)-Фосф ина и частично образовавшийся
гидрохлорид имидата полностью растворяются). Привес хлористого водороде составляет 4.3 г, т.е. 3,5-кратный по сравнению с теоретемесхим. Реакционную смесь, герметично закрытую, помещают в холодильник
на 15 ч. Затем большую часть избытка хлористого водорода и дмоксанз удаляют вакуу- жированием (температура компактная, Рост 20 ГПа, через смесь пропускают по капилляру осушенный воздух) в течение 3 ч. Выделившийся иг раствора кристаллический продукт отделяют фильтрацией и трижды промывают небольшими проциями (по 4-6 мл) абсолютного диоксана. После промывки усадок помещают в колбу и с целью осушки
вновь вакуумируют на масляном насосе (Рост 3-10 ГПз, температура комнатная, продолжительность 4 ч. Получают 5,4 г окиси трис- гидрохлорид-(3-имино-3-бутокси)про- пил -фосфина. Выход 99,4%. Мол.масса
0 540,95. Полученное соединение хорошо растворяется в воде, одновременно подвергаясь гидролизу, умеренно растворимо в диметилсульфоксиде и не растворимо в хлороформе, бензоле, эфире, а также в дру5 гих органических растворителях. Температура немала разложения 91-93° С.
Найдено, %: С 46,54; Н 8,50; N 8,16: Р 5,61; С 20,03.
C21H45N304PCI3
Вычислено, %: С 46.63; Н 8,33; N7,77; Р 5,73; CI 19,66.
По аналогичной методике получают и остальные вещества, приведенные в таблице./
Пример 2. Получение окиси трис- гид- рохлорид-{3-имино-3-метокси)пропил -фос- фина (соединение 1).
Смесь 2, i г (0,01 моль) окиси трис-(#-ци- анэтил)-фосфика, 0,96 г (0,03 моль) абсолютного метилового спирта и 9 мл абсолютного диоксана насыщают сухим хлористым водородом при температуре около 10° С. Привес НС 2,8 г (0,077 моль). Через 15 ч после вакуумирования, фильтрации, промывки продукта диоксаном и вакуумирования пол- учают 4,13 г окиси трис- гидрохлорид-(3- имино-3-метокси)пропил -фосфина. Виход 99,3%. Температура начала разложения 92- 95° С.
Найдено, %: С 35,07; Н 7,02; N 9,46; Р 8,06; CI 24 89.
С12Н2 №СМРС1з
Вычислено, %: С 34,75; Н 6,56; N 10,13; Р7.47; CI 25,65.
П р и м е р 3. Получение окиси трис- гид- рохлорид-(3-имино-3-этокси)пропил -фос- фина (соединение 2).
Смесь 2,1 г (0,01 моль) окиси трис-{ -ци- анзшл)-фосфина, 1,Ь (0,03 моль) абсолютного спирта и 9 мл абсолютного диоксана насыщают сухим хлористым водородом. Привес HCi составляет 2,7 г(0,073 моль), т.е. 7,3-кратный по отношению к нитрилу. После вакуумироваьля, фильтрации полученного продукта, промывки диоксаном и вакууми- рованмя получаю-; 4,54 г окиси трис-{гидро- хлорид-(3-имино-3-это сси)пропил -фосфингк . Выход 99%. Мол.масса 456,8. Температура начала разложения 81-84° С.
Найдено, %: С 38,96; Н 6,73; N 8,65; Р 7,17; С 24,06.
С15Нзз№СмРС1з
Вычислено, %: С 39,44; Н 7,28; N 9,20; Р 6,78; CI 23,28.
Пример 4. Получение окиси трис- гидрохлорид-(3-имино-3-изопропокси)про пилТ-фосфина (соединение 3).
Смесь 2,65 г (0,012 моль) окиси трис-(Ы- цианэтил)-фосфина 2,4 г (0,04 моль) абсолютного изопропилового спирта и 12,9 мл абсолютного диоксана насыщают сухим хлористым водородом в течение 30 мин при 10-12° С. Привес HCI составляет 9,1 г (0,25 моль). Через 15 ч после вакуумирования. фильтрации полученного продукта, промывки диоксаном и вакуумирования получают 6,3 г окиси трис- гидрохлорид-(3-имино-3- изопропокси)пропил -фосфина. Выход
99,7%. Мол.масса 498,67. Температура начала разложения 73-75° С.
Найдено, %: С 43,66; Н 8,13; N 7,90; Р 6,38; С 21,30, 5С18Нз9№СЦРС з
Вычислено, %: С 43,34; Н 7,88; N 8,42; Р 6,21; С121,3.
П р и м е р 5. Получение окиси трис- гид- рохлорид-{3-имино-3-изобутокси)лропил}- 10 фосфина (соединение 5).
Смесь 2,1 г (0,01 моль) окиси трис- 5-ци- анэтил)-фосфина, 2.5 г (0,03 моль) абсолют- .ного изобутилового спирта и 6 мл диоксана насыщают сухим хлористым водородом при 15 10-14° С. Привес HCI составляет 3.77 г (0,1 моль). Через 15 г после вакуумирования, фильтрации полученного продукта, промывки его диоксаном и вакуумирования получают 5,35 г окиси трис- гидрохлорид-(3-ими- 0 но-3-изобутокси)-пропил -фосфина. Выход 99,7%, Мол.масса 498,67. Температура начала разложения 73-75° С.
Найдено, %; С 43,66; Н 8,13; N 7,90; Р 6,38; CI 21,30. 5Ci8H39N3CMPCl3
Вычислено, %: С 43,34; Н 7,88; N 8,42; Р 6,21; CI 21.3. ,
П р и м е р 5 . Получение окиси трис-{гид- рохлорид-(3-имино-3-изобутокси)-пропил 0 -фосфина (соединение 5).
Смесь 2,1 г (0,01 моль) окиси трис- 3- ианэтил)-фосфина, 2,5 г (0,03 моль) абсолютного изобутилового спирта и 6 мл диоксана насыщают сухим хлористым водородом при 5 10-14° С. Привес HCI составляет 3,77 г (0,1 моль). Через 15 ч после вакуумирования, фильтрации полученного продукта, промывки его диоксаном и вакуумирова- ния оплучают 5,35 г окиси трис- гидрохло- 0 рид-(3-имино-3-изобутокси)-лропил -фосфи- на. Выход 98,5%. Мол.масса 540,95. Температура начала разложения 103-107°С.
Найдено, %: С 45,91; Н 7,88; N 8,15; Р 6,68; CI 18,83. 5C21H45N3CMCI3P
Вычислено, %: С46.63; Н 8,38; N 7,77; Р 5,73; CI 19,66.
Примерб. Получение окиси трис- гид- рохлорид-(3-имино-3-гексилокси(пропил}- 0 фосфина (соединение 7).
Смесь 2,1 г(0,01 моль) окиси трис- 9-ци- анэтил)-фосфина, 3,07 г(0,03 моль) абсолютного гексанола и 9 мл сухого диоксана насыщают сухим хлористым водородом при 5 12-15° С. Привес HCI составляет 3,8 г (0,11 моль). Через 15 ч после вакуумирования, фильтрации полученного продукта, промывки диоксаном и вакуумирования получают 6,25 г окиси трис- гидрохлорид-(3-имино-3гексилокси)пропил -фосфина. Выход.99,6%. Мол.масса 625,1. Температура начала разложения 107-110° С.
Найдено, %: С 51,83; Н 8,45; N 7,54; Р 5,07; CL 16,83.
Cl2H57N304PCl3
Вычислено, %: С 51,88; Н 9,19; N 6.72; Р 4.95; CI 17,01.
Пример 7. Получение окиси трис- гид- рохлорид-(3-имино-3-бутилтио)пропил}-фо- сфина (соединение 4).
В колбу, снабженную барботером и отводной, трубкой, загружают 2,3 г (0,11 моль) окиси трис- -цианэтил)-фосфина, 3.1 г (0,033 моль) свежеперегнанного бутилмер- каптана и 10 мл абсолютного диоксана. Насыщение реакционной массы проводят осушенным хлористым водородом при температуре около 10° С. Отвод тепла реакции осуществляют с помощью охлаждающей бани. Через 20 мин насыщение хлористым водородом прекращают (при этом получают вязкую массу, имеющую желтую окраску). Привес хлористого водорода составляет 6,5 г (0,178 моль). Реакционную смесь, герметично закрытую, оставляют в холодильнике на 15 ч. Избыток хлористого водорода и частично диоксан удаляют вакуумировани- ем, при этом выделившийся из раствора продукт отделяют фильтрацией, многократно промывают абсолютным диоксаном и далее помещают в колбу и вакуумируют на масляном насосе (Рост 8-10 ГПа, температура 20° С, продолжительность 4 ч). Получают 6,32 г окиси трис- гидрохлорид- (3-имино-3-бутилтио)пропил -фосфина. Выход 97,7%. Температура начала разложения 75-78° С.
Найдено, %: С 42,12; Н 7,18; N7 58; Р 6,15; CI 19,06.
С12Н45МзОРС1з5з
Вычислено, %: С 42,81; Н 7,70; N 7,14; Р 5,26; CI 18,06.
Таким образом, способ получения окисей трис- гидрохлорид-(3-имино-3-алкокси- (алкилтио)пропил -фосфинов отличается простотой, технологичностью, высокой эф- фективностью и позволяет получать новый класс фосфорорганических соединений с высокими выходами (97,7-99,7%), которые являются удобными промежуточными продуктами при получении труднодоступных функциональных третичных фосфинокси- дов.
Формула изобретения
Способ получения окисей трис-{гидро- хлорид- 3-имино-3-алкокси(алкилтио)про- пил}-фосфинов общей формулы
Р(сн2сн2с ш НС1}
Ъ 2 2 XR ;3
где R - Ci-Сб-алкил или изоалкил;
X - О или S, заключающийся в том. что окись трис- б-цианэтил)-фосфина подвергают взаимодействию со спиртом или тиоспиртом и хлористым водородом, взятым в молярном соотношении (1:3)-(3,3-7,3) - 20,8, в среде диоксана при температуре 8-15° С с последующим вакуумированием реакционной смеси при комнатной температуре и кристаллизацией целевых продуктов из диокса- новых растворов.
(CH,r;;,e NH KS
2Ъ
XR
со



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения алкил -имино-алккоксиалкилметилфосфонатов | 1975 |
|
SU544659A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АМИДОВа- | 1972 |
|
SU356843A1 |
| Способ получения 9-замещенных 2,3-дигидроимидазо [1,2-а] бензимидазола или их солей | 1981 |
|
SU952848A1 |
| Гидрохлориды производных 7-(2-окси-3-амидинопропил)-теофиллина,обладающие противогистаминной активностью и бронхорасширяющим действием | 1980 |
|
SU1100875A1 |
| Способ получения 1-алкил-3-окси5-хлор-1,2,4-триазолов или их солей | 1975 |
|
SU682128A3 |
| Способ получения производных 3(2Н)пиридазинона или их фармацевтически приемлемых солей | 1986 |
|
SU1468415A3 |
| Способ получения производных 2-(тиенил-2)- или 2-(тиенил-3) этиламина | 1982 |
|
SU1148563A3 |
| 3-Фенил-3-о-оксифенил- (фенилизопропил) пропиламин или его соли, обладающие сосудорасширяющим действием | 1975 |
|
SU696009A1 |
| НОВОЕ ПРОИЗВОДНОЕ 3-АЗАБИЦИКЛО[3.1.0]ГЕКСАНА И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНСКИХ ЦЕЛЯХ | 2014 |
|
RU2701861C1 |
| Способ получения 2-(фурилметил)-6,7бензоморфанов | 1972 |
|
SU479290A3 |
Изобретение касается замещенных фосфинов, с частности получения окисей трис-{гидрохлорид- 3-имино-3-алкокси(эл- килтио)пропил}фосфинов общей ф-лы P(0){CH2-CH2-C(XR)-NH , где R-Ci - Се-алкил или изоалкил; X - кислород или сера, которые как полупродукты могут быть использованы в синтезе третичных фосфинов. Цель - создание нового способа получения указанных веществ. Для этого ведут реакцию трис-(/3-циаэнтил)фосфина со спиртом или тиоспиртом и НС1 молярное соотношение 1:(3-3,3).(7,3-20,8) в среде диоксана при 8-15°С с последующим вэкуумирова- нием реакционной смеси при комйатной температуре и кристаллизацией целевого продукта из диоксанового раствора. Эти условия обеспечивают выход целевых продуктов до 97,7-99,7 %. 1 табл.

| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ р-(ДИАЛКОКСИФОСФОН)- ИМИНОКАРБОНОВЫХ КИСЛОТ | 0 |
|
SU405903A1 |
| Способ получения фосфорилированных имидатов | 1973 |
|
SU507041A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Авторское свидетельство СССР № 695175, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1991-12-07—Публикация
1989-11-29—Подача