тез соответствующего белка, плаэмиды pGCS2-142 для его экспрессии, а также штамм-продуцент E.coli К802 (pGCS2-142) рекомбинантной капсидной структуры, обеспечивающий выход конечного продукта в количестве не менее 13,2% суммарного белка Е.соИ.
Рекомбинантная плазмида pGCS2-142. состоит из следующих элементов: ДНК плазмиды рНВс1315, которая представляет собой вариант плазмиды рНВсЗ, содержащей ген НВсАд с оптимизированным участков инициации трансляции, но с мутантным геном НВсАд, содержащим полилинкерную вставку по 144-й аминокислоте и предназначенным для внедрения чужеродных последовательностей по этому участку, протяженность 6900 п.о.; Фрагмент генома HBV из плазмиды рНВ320 (7), соответствующий последовательности между сайтами рестрикции iV stll1,794 и N al l1626 и кодирующий участок preS2 (1--55) протяженностью 168 п.о. Размер плазмиды 7050 п.о., мол.м. 4,5 МД.
В состав ДНК рекомбинантной плазмиды pG32-142 входят гены: ген НВс Ад Д preS2(1-55). обеспечивающий синтез конечного продукта: ген fia, обеспечивающий устойчивость к ампициллину.
Ген ИВсАд Л - ppeS2 (1-55) находится под контролем тандема промоторов Ptrp.
Плазмида pGCS2-142 амплифицируется при добавлении в среду хлорамфеникола, неконьюгативна.
Сущность способа конструирования плазмиды pGCS2 142 состоит s том. что фрагмент гена preS2, именуемый HBVpre 82 (1-55) протяженностью 168 п.о. внедряют по сайтам рестрикции EcoRV и Clal в векторную плазмидурН В1315 с образованием рекомбинантного гена НВсАд А- рге S2(),
Штамм-продуцент НВсАд Д - рге $2 (1-55) получают трансформацией клеток Е,соИ К802 рекомбинантной плазмидой ДHKpGCS2-И2.
Морфологические признаки: клетки палочковидной формы, грамотрицательные,.
Культуральные признаки: клетки растут на обычно используемых питательных сре дах, образуют колонии средней величины.
Физико-биохимические признаки: оптимальная температура культивиро.вания 37°С, оптимум рН 7,0-7,4. В качестве источника углерода используют углеводы, в качестве источника азота - минеральные соли, а также органические соединения в виде пептона, триптора, аминокислот.
Устойчивость к нтибиотикам: устойчив к ампициллину, что обусловлено наличием
плазмиды. Присутствие в штамме плазмидной ДНК подтверждается путем проверки устойчивости к ампициллину, а также путем выделениями анализа плазмидных ДНК экспресстметрдом.
Штамм депонирован в коллекции Центрального музея промышленных микроорганизмов под номером ВКПМ В-4977.
П р име р 1. Конструирование рекомби0 натной плазмидной ДНК pGC$2-142.
10 мкг плазмиды рНВ1315, выделенной стандартным методом, расщепляют (частично) 3 ед. рестриктазы EcoRV в 25 мкл раствора, содержащего 10 тМ трис-НС1, рН 7,5; 50
5 mMNaCI. 10 mMMgCl2 и 1 тМ дитиотрейтол (ДТТ) в течение 30 мин при 37°С. Рестриктазу анактивируют 15-минутным nporpeeaHi/tем при 65°С. К 20 мкл реакционной смеси добавляют 6 мкл раствора Б, содержащего
0 70 тМ трис-НС1, рН 8,0: 70 тМ MgCl2 и 10 гпМ ДТТ, воду до конечного объема 60 мкл и 15 ед. рестриктазы Ciat, Инкубацию при 47°С проводят в течение 2 ч. После очистки на агарозном геле (на бумаге ДЕ-81) известным методом фрагмент ДНК с мол.м. 4,42 М,Д (размером -6900 п.о.) растворяют в 20 мкл Н20(ДНК 1).
50 мкг плазмиды рНВ 320, полученной очисткой на оксиапатите, расщепляют 25 ед.
0 рестриктазы Нра I и 25 ед. рестриктазы EcoBlll (Mst II) в 250 мкл раствора В, содержащего 10 тМ трис-НС1, рГ 8,5: Ю тМ MgCi2 и 1тМ ДТТ в течение 3 ч при . После очистки на агарозном геле на бумаге
5 ДЕ-81) известным методом фрагмент Hpal816-Mstll1794 с мол.м. 0,62 Мд (размером 978 п,о.) растворяют в 20 мкл НаО (ДНК 2).
2 мкг ДНК 2 расщепляют 4 ед. рестрик0 тазы Hin 111 (Nla 111) в 20 мкл раствора Г, содержащего 10 тМтрис-НС1, рН 8,5; 10 тМ МдС12и50 тММаС втечение2ч при37°С. Фрагмент MsttП794- 4lal l1626 размером 168 ri.o. шзсле очистки на 2%-ном агарозном
5 геле (на бумаге ДЕ-81) растворяют в 10 мкл Н20(ДНКЗ).
Выравнивание липких концов вектора и клонируемого фрагмента проводят совместно, для чего 0.1 мкг ДНК 1 и 0,05 мкг ДНК 3
0 инкубируют с 4 ед. Т4 ДНК-полимеразы в 10 мкл раствора Д, содержащего 20 тМ трисНС1, рН 7,5; 10 mMMgCl2, 1 тМ ДТТ и 33 тМ dATF. dCTP, dTTP, dGTP в течение 30 мин при 37°С. Т4 ДНК-полимеразу инактивиру5 ют 15-минутным прогреванием при 65°С.
После выравнивания липких крнцов зашивку вектора и клонирующего фрагмента проводят в 12 мкл раствора Д с добавлением 10 ед. Т4 ДНК - лигазы и АТР до конечной концентрации 500 гпМ в течение 12 ч при
4°С. К реакционной смеси добавляют 100 мкл клеток E.coli RR1, обработанных 100 тМ CaCl2 (конечная концентрация 5 10 кпеток/мл) для трансформации клеток по известному методу.
Отбор клонов осуществляют путем рестрикцирнного анализа плазмидной ДНК, выделенной экспресс-методом. Плазмида с ожидаемой рестрикционной картой получает наименование pCCS2-142.
Штамм-продуцент Е,со11 К802 (pGCSa142). Выделение и очистка рекомбинантного белка НВсАд А-pre 52(1-55).
Штамм-продуцент получают трансформацией клеток E.coIT К802,рекомбинантной плазмидой pGCS2-142. Клетки выращивают в солевой среде М9 с добавкой, г/л: казаминовые кислоты 10; глюкоза 2, ампициллин 0,02. до оптической плотности ОПб50 4-5. Клетки собирают центрифугированием и лизируют в трехкратном объеме буфера, содержащего 0.06 М трис-НС1, рН 8.0, 0.15 М NaCI. 0.1% тритон Х100. 0,005 МЭДТА, 3 мг/мл лизоцима. После инкубации В:течение 30 мин при 4°С клетки подвергают трехкратному замораживанию - оттаиванию, добавляют дезоксирибонуклеазу и MgCl2 до конечной концентрации 20 мг/мл и 10 гпМ соответственно и инкубируют 30 мин при 4°С. Лизат осветляют центрифугированием (10 000 9, 4°С. центрифуга). НВс Ад Д -pre 82 (1-55)очищают следующим образой. Лизат подвергают фракционированию сульфитом аммония. НВс А А - рге Sz (1-55) собирают в осадке, полученном при 30% насыщения сульфатом аммония. Осадок растворяют в 0,04 М фосфате натрия, рН 8,0, 0,15 М NaCI, 0,1% тритоне XI00до конечной концентрации белка 25-50 мг/мл,.и 6-7 мл этого раствора наносят на колонку с Сефарозой CL4B (2.1 75 см), уравновешенную тем же буфером, но без тритона Х100. Фрак- ции. проявляющие НВсАд-активность. собирают и используют либо непосредственно, либо после концентрирования переосаждением 50%-ным Сульфатом аммония.
Определение НВсАд-активности методом РИД.
Титр определяют с помощью р адиальной иМмуно-диффузии по Ухтерлойи. Для этого готовят двукратные серийные разведения клеточного лизата и титрйрунэт против анти-Н Во антител человека. В качестве стандарта используют очищенйый НВсАд, полученный из рекЬмбинантных бактерий (1 мг/мл). Результаты титровайия НВсАд-активности методом РИД приведены в табл, 1. (синтез НВс Ад А-рге $2 (1-55)
н бактериях E.coli К802, несущих рекомбинантнуюплазмиднуюДНК PGCS2-142).
Определение рге 52-ак.ти8ности методом иммуноблотинга. Мол.м. белка НВсАд 5 А-pre 52(1-55).
Для иммуноблотинга клетки (6 м г) суспендируют в 100 мкл буфера для нанесения образцов на полиакриламидный гель, содержащего 2 %- ныйдодецилсул.ьфат натрия
10 (ДСН) и 2%-ный.у9-меркаптоэтанрл и лизируют 2 мин прогреванием на кипящей водяной бане. Полученные лизаты (2-4 мг/мл белка) наносят на полиакриламидный градиентный гель (12-18%) размером 150х
15 х150 X 0.75 мм. Электрофорез проводят в течение 15 ч при силе тока 7 мА. После электрофореза белки переносят на нитроцеллюлозу. Фильтры инкубируют с моноклональнымианти-рге 52 антителами мыши
0 МАЕ в разведении 1:500 на буфере TBS, содержащем 50 тМ трир-НС, рН 7.8; 150
тМ NaCI 0.1% тритон XIQO, 1 % БСА, в течение 15 ч при 2б°С. После .трехкратной отмывки буфером ТВ5фильтрЬ1 инкубируют 2
5 ч при 20°С с коньюгатрм пероксидазы с антителами против иммуноглобулинов мыши в разведении 1:200. Фильтры отмывают буфером ТВ5 (3-5 раз) и проявляют диаминобензидином. Лизаты клеток, штам0 ма-продуцента обнаруживают при этом появление специфических зон окраски, соответствующих белку С мрл.м. 22,3 МД (или длиной 212 аминокислот), что соответствует схеме коне труирования. Контроль5 -ные лизаты клеток E.coli К802 () таких зон не обнаруживают,
Электронномикроскопическая характеристика рекомбинантных капсидных структур НВс Ад А - рге 52 (1-55).
0Препараты очищенного белка НВсАд
А- рге 5(1-55) готовит методом негативного контрастирования с применением 1 %-ного уданйлацетата и исследуют на электронном микроскопе 1Е1УЙ 100 С при ус5 коряющем напряжении 80 кВ и инструментальном увеличении 100 000 раз. Белок (1-55) образует капсиды диаметром 25 нм. OnpeAeWeHvie рге 52-активйости в составе капсидных структур НВс Ад А -pre 52
0 (1-55) методом энзимоиммунологического анализа на твердой фазе.
В качестве твердой фазы используют полистиррловые 96-луночйые планшеты для иммунологических реакций. Очищенный белок НВс Ад А- рге 52 (1-55) разводят до концентраций 10 мкг/мл в 50 тМ ЫаНСОзNa2C03; рН 9,5 и вносят в лунки планшетов по 100 мкл а каждую. Инкубируют 16 ч при 37°С. после чего раствор удаляют из лунок.
планшеты высушивают. В лунки вносят моноклональные анти-рге $2 антитела мыши МАЕ в разведении 1:5000 на буфере ТВ. После инкубации в течение 2 ч при планшеты отмывают 5-6 раз дистиллиро- 5 ванной водой и вносят по 100 мклконьюгата пероксидазы хрена с белком S.aureu.s в разведении 1:5000 на буфере TBS. После инкубации в течение 1 ч планшеты отмывают и проводят цветную реакцию, в лунки вносят 10 по 100 мкл 0,25%-ного раствора ортофенилендиамина 2HCI в 0,1 М цитрате натрия, рН 5,0, 0,02% Н202, инкубируют 30 мин при 20°С, реакцию останавливают добавлением 100 мкл 0,1 N HCI. Появление 1«)ричневой 15 окраски свидетельствует о наличии рга S2активности. Для количественной оценки активности, измеряют оптическую плотность при 492 нм и определяк5т величину P/N {табл.2)..20
Отсутствие рэакции в отри-цательном контроле (НВсАд) свидетельствует о специфичности связывания анти-рге $2 антител рекомбикантными капсидными структурами НВс Ад А- рге S2 (1-55). Иммунологине- 25 екая активность рекомбинантных антител приведена в табл. 2.
Иммуноэлектронная микроскопия капсидных структур с использованием коллоидного золота.30
Капсиды НВсАд Д - рге 52(1-55) сорбируют на никелевой сеточке, покрытой формваровой пленкой, в течение 15мин. Сеточку промывают 0,5 мл раствора PBS, содержащего 0,05%-ный Твин 20 (PBS - Твин 20) и 35 инкубируют 15 мин вО,03 мл 0,1%-ного раствора БСА в воде, промывают 0,5 мл PBS Твин 20, инкубируют 15 мин в 0,03 мл раствора моноклональныхантирге 52 антител м.ыши МАЕ в разведении 1:10, промывают 40 0,5 мл PBS - Твин 20, инкубируют 20 мин в 0,03 мл антител (крйлика) против иммуноглобулинов (в разведении 1:5); промывают 0,5 мл PBS - Твин 20. Сеточку помещают на 1 ч в 0,03 мл раствора рА-AU, 45 содержащего белок А, который коньюгирован с частицами коллоидного золота диамртром 8-10 нм, промывают 0,5 мл PBS Твин 20 и затем 1 мл Н2О. Капсиды окрашивают методом негативного контрастирова- 50 НИИ 0,15 мл 2%7ного уранилацетата. Всё операции вьтолняются при 20°С, В случае поверхностной локализации соответствующихэпитопов капсиды на электронной микрофотографии окружены венчиком частиц 55 коллоидного золота.
В качестве отрицательного коитроля использованы капсиды НВсАд, не несущие
3питом рге $2 (). Эти капсиды не образуют комплексов с коллоидным золотом.
Иммуногенная активность рекомбинантных капсид НВсАд Д-рге 82 (1-55),
Для определения иммуногенности рекомбинантными капсидами НВсАд А - рге $2 (1-55) иммунизируют кроликов. Для этого смешивают 2 мг антигена, растворенного в 1 мд физиологического раствора PBS, с 1,25 мл полного адъюаанта Фрейнда и получают гомогенную эмульсию. Антиген вводят подкожно. И| ъекции антигена повторяют на 14й и 2Т-Й день и с 28-го дня начинают брать кровь. Специфичность антител определяют методом VlcDA с использованием двух антигенов: НВсАд (для определения антиНВс антител (fr-pre S)i белок-оболочки РНК-фага fr, несущий весь участок рге S - для определения анти-рге $2 антител. Титры антител на 28-й день иммунизации приведены в табл. 3 (иммуногенность химерных капсид НВсАд А -pre 52(1-55).
Ф О р.м у л а из о б р ет е н и я
1.Рекомбинантная плазмидная ДНК pGC52-142, кодирующая кор-антиген вируса гепатита В, лишенный ДНК 39 С-концевых аминокислот с зкспонир ванным на его поверхности эпитопом рге 52 (1-55) размером 7071 п.о. и мол.мае. 4,53 МД, содержащая плазмидную ДНК рНВс 1315 размером 6900 п.о.; Mstlll794 - NIal111626, фрагмент плазмидной ДНК рНВ 320, кодирующий последовательность участка рге 52 вируса гепатита В, размером 17 п.о,: уникальные; сайты рестрикции и их координаты: ВатН1(0), sphi (191), Sal 1(276), Nrul(599). 5naК1871) Af 1(2098), PstJ(3236), 5cal(3471), Xlal(5176); гены, регуляторные участки, генетические маркеры: ген НВсАд А - рге Sa (1-55), обеспечивающий синтез рекомби-: нантныхкапсидных структур: НВсАд А рге 52 (t-55). координаты 5087-5-740,- тандем промоторов Ptrp; ген 51а, обеспечивающий устойчивость к ампициллину (координаты 2918-3778),;
2,Способ конструирования рекомбинантной плазмидной ДНК pGC52-142, заключающийся в том. что NIalM Mst l1794, фрагмент длиной 168 п.о., кодирующий участок рге Sz (1-55), выделяют из плазмйдырНВ 320 П.О., заполняют и удаляют липкие концы с помощью ДНК полимеразы, встраивак т в вектор для экспрессии pHBc13t5 по сайтам EcoRV и Clal в положении 144 аминокислоты гена НВсАд так. что за 144 аминокислотой образуется вставка рге $2 (1-55). что вызывает терминацию трансляции, исключающую 39 С-концевых
аминокислот гена HBcAg. трансформируют рекомбинантными ДНК штаммы бактерий Escherlchia coll, отбирают с помощью контактирования ивыделяют из этих клонов целевую плазмиду,,
3. Штамм бактерий Escherlchia соП ВКПМ В-4977 продуцент кор-антигена, Ьируса гепатита В. лишенного 39С аминокислот с экспонированным на его иоверхности эпитопомргё 52(1-55).



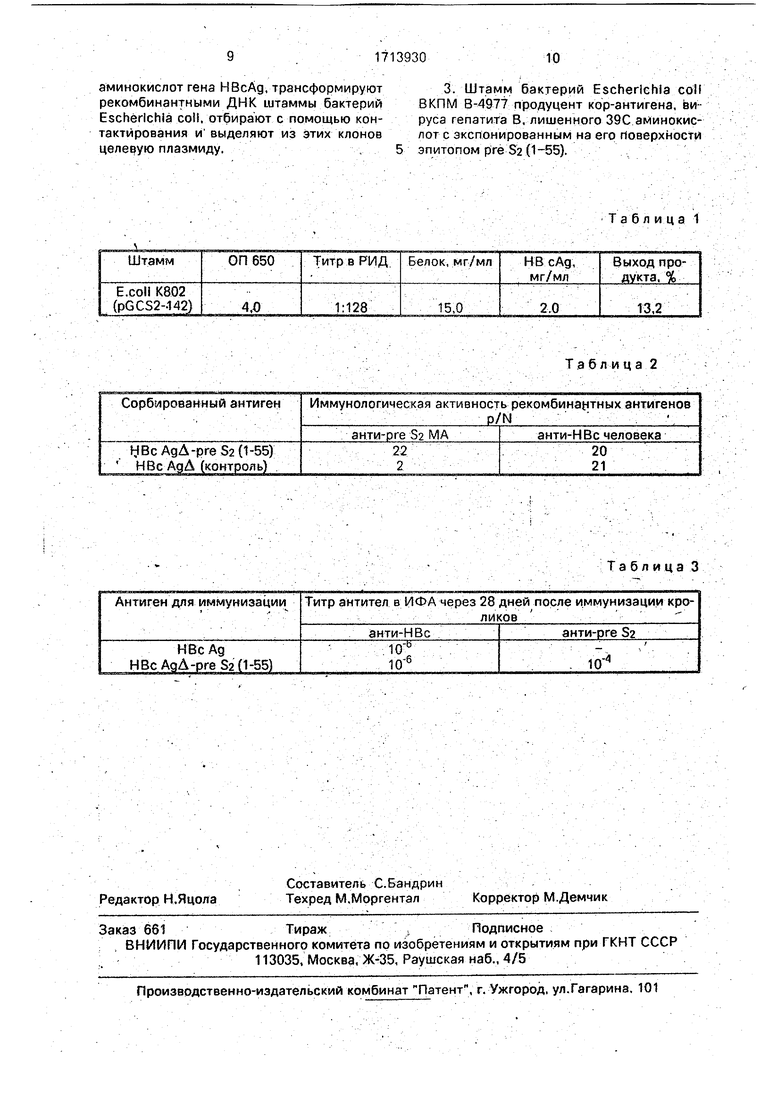

Т а б л и ц а 1
Т а б ли ц а 2
Таблица 3
| Борисова Г | |||
| П | |||
| и др | |||
| ДАН СССР, 1984, т | |||
| АППАРАТ ДЛЯ ОБОГАЩЕНИЯ РУД ПО МЕТОДУ ВСПЛЫВАНИЯ | 1915 |
|
SU279A1 |
| П | |||
| и др | |||
| ДАН СССР, 1988, с, 298 | |||
| с | |||
| Рефлектор для дуговых ламп | 1924 |
|
SU1474A1 |
Авторы
Даты
1992-02-23—Публикация
1989-08-10—Подача