Изобретение относится к химическим методам определения и может быть использовано при определении содержания витамина А и каротиноидов в масляных концентратах, витаминных премиксах, биологическом материале в химических, фармацевтических, сельскохозяйственных и прочих биологических исследованиях, а также при контроле производства витамина А.
Известен способ определения витамина А, включающий омыление материала спиртовым раствором щелочи, экстракцию неомыляемой фракции органическим растворителем и проведения цветной реакции с фосфорно-молибденовой кислотой.
Недостатками данного способа являются низкая точность и высокая погрешность
определений, так как фосфорно-молибдено- вая кислота дает цветную реакцию с большим числом различных соединений, т.е. является неспёцифическим реагентом, что приводит к существенному завышению результатов. Кроме того, серьезные затруднения представляет сама фосфорно-молиб- деновая кислота вследствие ее низкой стабильности.
Наиболее близким к предлагаемому по технической сущности и достигаемому эффекту является способ определения витамина А и каротиноидов, включающий омыление материала спиртовым раствором щелочи в течение 90 мин, экстракцию неомыляемой фракции бензолом, выдерживание экстрагирующей смеси в течение 15 мин для раздеVI
ю
со ел
00
ления водного и бензольного слоев, промывку бензольного слоя водой для удаления щелочи, разделение полученного экстракта витамина А и каротиноидов на две равные части. В первой спектрофотометрически определяют каротиноиды, используя в качестве раствора сравнения чистый бензол (длина волны 460 нм). Во вторую часть экстракта добавляют 5 мл спиртового раствора соляной кислоты, встряхивают и помещают в темное место. Через 15 мин кислоту нейтрализуют эквивалентным количеством щелочи, бензольный слой промывают водой и центрифугируют для осветления. Полученный раствор спектрофотометрируют при 390 нм; в качестве раствора сравнения используют раствор, в котором ранее определяли каротиноиды.
Недостатки прототипа заключаются в следующем.
Используемый экстрагент - бензол дает устойчивые эмульсии с водными растворами щелочей, которые дополнительно стаби- лизируются присутствием этанола и поверхностно-активных веществ, выделившихся в процессе омыления из анализируемых образцов. При отстаивании системы гидролизат - экстрагент даже спустя 30 мин после экстрагирования разделение фаз происходит не полностью. При отделении бензольного слоя от водного часть бензола с растворенными веществами теряется вместе с водой.
Аналогичный процесс, хотя и в меньшей степени, наблюдается при отмывке бензольного экстракта водой для удаления примесей щелочи.
Образование водно-бензольных эмульсий приводит к понижению точности анализа, занижению полученных результатов.
Деление экстракта на две части вносит дополнительную операцию в ход анализа, еще больше понижает точность определений и увеличивает их продолжительность.
Для перевода витамина А в аналитическую форму (дегидровитамин А) часть бензольного экстракта заливают спиртоьым раствором кислоты, спустя 15 мин смесь нейтрализуют и опять промывают. Перевод витамина А в дегидроформу проводится в двухфазной системе бензол-вода что неэффективно (скорость дегидратации в гетерогенной среде ниже). Кроме того, в процессе промывки снова образуется эмульсия, при этом теряется часть дегидроформы витамина А.
После промывки раствор остается мутным. Для его осветления приходится использовать дополнительную операцию - центрифугирование, что удлиняет анализ.
В процессе анализа приходится работать длительное время с бензолом-ядом кумулятивного действия.
Цель изобретения -упрощение и сокращение длительности процесса.
На чертеже представлен график, поясняющий способ.
Согласно предлагаемому способу биологический материал заливают 2 н. водно0 этанольным раствором щелочи, добавляют в качестве антиоксиданта аскорбиновую киоГоту и омыляют в течение 60-90 мин при 60° С; из полученного гидролизата этилаце- тэтом извлекают витамин А и каротиноиды.
5 Экстракт 2-3 раза промывают водой до удаления следов щелочи, переносят в мерную пробирку или колбу, доводят его объем до заданной величины. Аликврту 3 мл спектрофотометрируют на длине волны 450 нм от0 носительно чистого этилацетатз, затем в кювету микропипеткой добавляют 1,0-2,7% (объем) тетрафторборной кислоты, полученную смесь встряхивают и через 2-5 мин снова спектрофотометрируют при 390 нм.
5 По оптической плотности экстракта при 450 нм определяют содержание каротиноидов в биологическом материале, при 390 нм - количество витамина А по приросту оптической плотности.
0 При использовании предлагаемого способа точность определения каротиноидов в 1,4 раза, а витамина А в 2,1 раза выше, чем способа-прототипа. Время, затрачиваемое на анализ согласно предлагаемому способу,
5 меньше в 1,8 раза.
Пример. Определение витамина А и каротиноидов в печени кур.
Навеску гомогенизированной куриной печени (0,5 г) заливают 5 мл 2 н. водно-эта0 нольного раствора гидроокиси натрия, добавляют 0,05 г аскорбиновой кислоты и нагревают при 60°С в течение 90 мин. Затем к гидролизату добавляют 15 мл этилацетата и хорошо встряхивают.
5 Этилацетатный экстракт промывают 2- 3 раза дистиллированной водой, затем в мерную пробирку переносят полученный раствор и доводят этилацетатом объем до 15 мл. Удаление остатков воды проводят встря0 хиванием экстракта с 3-5 г безводного сульфата натрия.
После осушивания 3 мл экстракта фото- метрйруют на длине волны 450 нм для определения концентрации каротиноидов. В
5 качестве раствора сравнения используют чистый этилацетат. Для определения концентрации витамина этот же экстракт фото- метрируют на длине волны 390 нм и, таким образом, получают начальную оптическую плотность экстракта. Затем в обе кюветы
микропипеткой добавляют 0,05 мл тетрафторборной кислоты и отмечают прирост оптической плотности -ДА. Через 2-4 мин, когда оптическая плотность экстракта перестает расти, записывают ее максимальное значение. Измерения проводят также на длине волны 390 нм. По разнице между вторым и первым измерениями рассчитывают прирост оптической плотности.
С помощью пересчетной формулы (или калибровочного графика) по величине А450 находят содержание каротиноидов, по А - количество витамина А в исследуемом образце. Содержание витамина А рассчитывают по формуле
V Кд . , „390
(А
),
где Хд - количество витамина А в пробе, мкг/г;
V - объем этилацетата, мл;
g - навеска образца, г;
Кд - калибровочный коэффициент (тангенс угла наклона калибровочной прямой), равен 6,09;
- оптическая плотность раствора при 390 нм до добавления тетрафторбррной кислоты;
А2 - оптическая плотность раствора после добавления тетрафторборной кислоты при 390 нм.
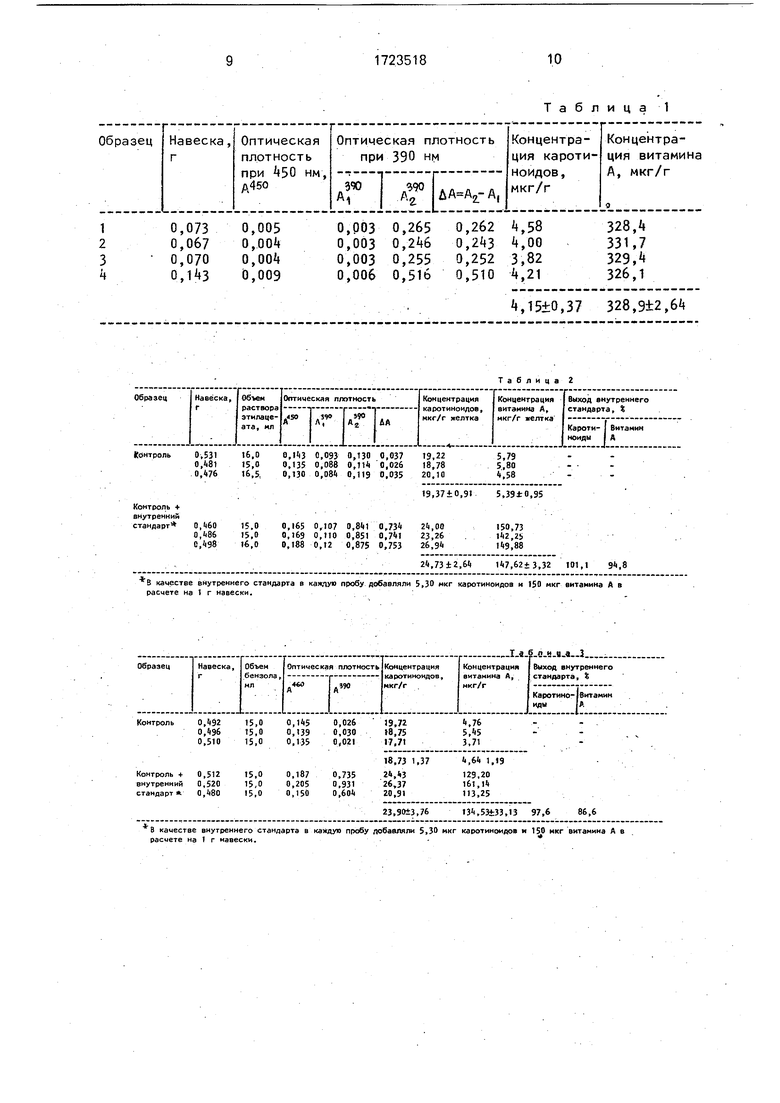
Данные анализа печени кур приведены в табл, 1.
П р и м е р 2. Определение витамина А и каротиноидов в желтке куриных яиц. Сравнительные испытания предлагаемого способа и прототипа.
Навеску 1 г яичного желтка анализируют по способу-прототипу и предлагаемому способу, как описано в примере 1. Результаты испытаний приведены в табл. 2 и 3.
Проведенные испытания показали, что использование предлагаемого способа позволяет повысить точность определения каротиноидов в 1,4 раза, витамина А - в 2,1 раза по сравнению с прототипом. Время, затрачиваемое на анализ согласно предлагаемому способу, меньше в 1,8 раза.
П р и м е р 3. Определение витамина А и каротиноидов в комбикорме.
Навеску комбикорма 2-3 г помещают в круглодонную колбочку, добавляют 5 мл 2 н. водно-этанольного раствора гидроокиси натрия, 0,05 г аскорбиновой кислоты и нагревают при 60°С в течение 90 мин. Дальнейшие операции проводят согласно примеру 1.
П р и м е р 4. Определение витамина А и каротиноидов в премиксе.
Способ осуществляют так же, как в примере 3, лишь уменьшив навеску до 50 - 100мг.
П р и м е р 5. Определение витамина А 5 и каротиноидов в плазме крови.
Плазму крови (5-6 мл) помещают в круглодонную колбу, щелочной гидролиз и все другие операции проводят согласно примеру 1.
0 Определение витамина А. и каротиноидов в любых других субстратах проводят так же, как описано в примере 1.
П р и м е р 6. Определение зависимости скорости дегидрирования витамина А от ко5 личества тетрафторборной кислоты в этила- цетате.
К 3 мл этил ацетатного экстракта витамина А (концентрация витамина А
°66,3 м кг/мл) добавляют 0,03-0,50 мл тет0 рафторборной кислоты. Первое измерение оптической плотности на длине волны 390 нм проводят через 60 с после смешивания растворов, все последующие изменения - с интервалом 30 с. При этом в зависимости от
5 дозы внесенной HBF4 за строго определенное время в каждом случае витамин А полностью переходит в дегидроформу, при этом оптическая плотность достигает максимального значения и в течение длительно0 го времени не изменяется.
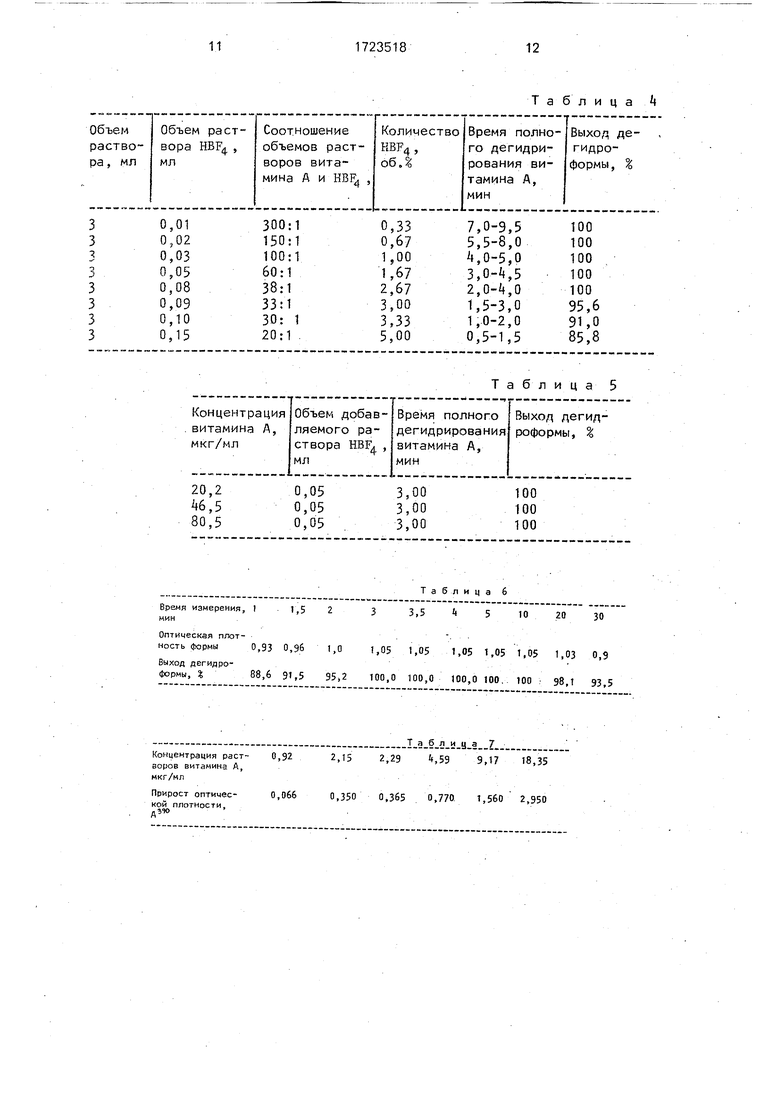
Результаты приведены в табл. 4. Из данных табл. 4 следует, что наиболее быстрая дегидратация со 100%-ным выходом в течение 2-5 мин наблюдается при
5 добавлении к этилацетатному раствору витамина А тетрафторборной кислоты в количестве 1,0-2,7 об. %, т.е. когда соотношение этилацетат; HBF4 лежит в пределах 100:1- 38:1. При добавлении тетрафторборной кис0 лоты в количестве менее 1,0% скорость образования дегидроформы витамина А уменьшается за счет разбавления раствора. Если же количество реагента более 2,7%, в анализируемом растворе создаются усло5 вия протекания побочной реакции. При
этом дегидроформа либо образуется не полностью, либо не образуется вообще.
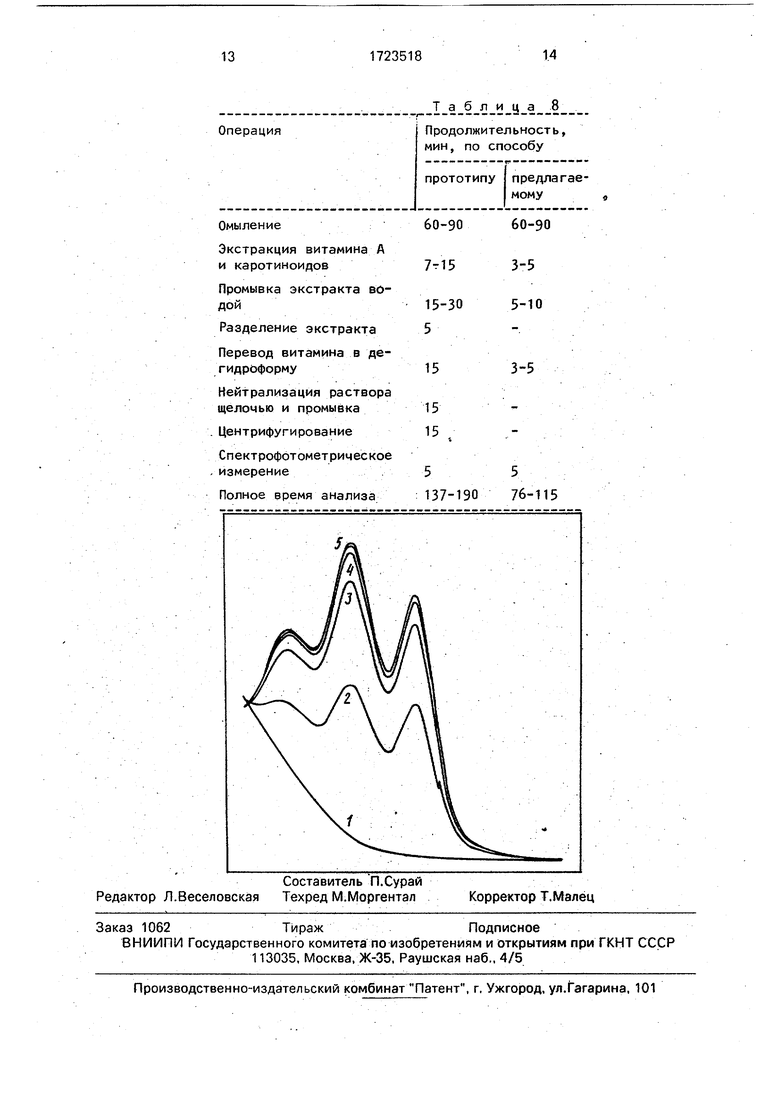
Графически процесс дегидратации витамина А тетрафторборной кислотой пред0 ставлен на чертеже. На нем изображена часть спектра витамина еще до добавления тетрафторборной кислоты, т.е. чистого витамина А (кривая 1) в области 340-450 нм и часть спектра дегидроформы витамина А по5 еле добавления тетрафторборной кислоты через каждые 30 с. измерения (кривые 2-6). Доза HBF4 0,05 мл. Как видно из чертежа, полное дегидрирование витамина А наступает уже через 2 мин, что также подтверждает данные табл. 4.
Пример. Определение зависимости времени полного дегидрирования витамина А от его содержания в растворе.
К одинаковым объемам раствора витамина А (3 мл) с различной его.концентрацией добавляют одно и то же количество тетрафторборной кислоты - 0,05 мл. При этом скорость реакции дегидрирования, время выхода и процент выхода аналитической формы витамина А остаются неизменными.
Результаты измерений приведены в табл. 5.
Из данных табл. 5 следует, что изменение концентрации витамина А не оказывает влияния на скорость и полноту дегидратации, т.е. предлагаемый способ применим для большого интервала концентраций витамина А.
ПримерВ. Определение устойчивости дегидррформы витамина А.
К 3 мл раствора витамина А добавляют 0,05 мл тетрафторборной кислоты. Определение оптической плотности раствора проводят каждые 30-60 с..
Результаты измерений представлены в табл. 6.
Максимальное количество дегидрофор- мы в данном случае образуется через 3 мин. Измерения показывают, что полученная де- гидроформа витамина А устойчива во времени и не разлагается при проведении анализа в течение 10-20 мин. .
Приме р 9. Построение калибровочных графиков для определения витамина А и каротиноидов.
Масляный препарат витамина А разбавляют гексаном в 250, 1000 и 2500 раз. Алик- воты растворов 1-3 мл заливают 5 мл 2 н. водно-этанольного раствора гидроокиси натрия; омыление и все дальнейшие операции проводят, как описано в примере 1.
Результаты испытаний приведены в табл. 7.
Через полученные точки проводят калибровочную прямую. Калибровочный коэффициент (тангенс угла наклона прямой) Кд равен 6,097.
Калибровочный график для определения каротиноидов строят с помощью растворов бихромата калия. Калибровочный коэффициент Кк равен 4,46.
П р и м е р 10. Сравнение продолжительности анализа согласно предлагаемому и
известному способам.
Сравнение предлагаемого способа и прототипа указывает на то, что время, затрачиваемое на анализ образца по способу с тетрафторборной кислотой, значительно
меньше, чем по прототипу; способ упрощается за счет устранения ряда операций в ходе анализа.
Результаты сравнения приведены в табл, 8.
Таким образом, использование в качестве экстрагента этилацетата исключает образование в процессе экстракции эмульсии и способствует более быстрому разделению фаз, что повышает точность определений и
сокращает продолжительность анализа; использование для дегидратации витамина А тетрафторборной кислоты позволяет упростить способ и сократить время его выполнения за счет устранения ряда а.налитических операций; замена бензола нетоксичным этилацетатом улучшает условия работы, расширяет возможности использования способа.
Проведенные испытания показали, что
при использовании предлагаемого способа точность определений каротиноидов повышается в 1,4 раза, витамина А - в 2,1 раза. Время анализа сокращается при этом в 1,8 раза.
Формула изобретения
Способ одновременного количественного определения витамина А и каротиноидов, включающий щелочной гидролиз пробы, экстракцию определяемых веществ.
органическим растворителем, обработку
экстракта минеральной кислотой и спектрофотометрический анализ, отличающий с я тем, что, с целью упрощения и ускорения
процесса, в качестве органического растворителя используют этилэцетат, а из минеральных кислот используют тетрафторбор- ную кислоту в количестве, обеспечивающем ее содержание в смеси с экстрактом 1,0- 2,7%, при этом обработку экстракта проводят в течение 2-5 мин.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения концентрации витамина А | 1988 |
|
SU1670602A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВИТАМИНА C | 2002 |
|
RU2229132C2 |
| Способ количественного определения нитратов в пищевых продуктах | 1988 |
|
SU1649426A1 |
| Способ количественного определения фталевого ангидрида | 1974 |
|
SU551544A1 |
| Способ определения количества каротиноидов в яичном желтке | 1990 |
|
SU1721505A1 |
| Способ определения сантохина | 1978 |
|
SU705334A1 |
| Способ определения удельной активности липаз в реакциях переэтерификации жиров и масел | 1988 |
|
SU1558872A1 |
| Способ определения витамина @ | 1982 |
|
SU1109631A1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ | 1992 |
|
RU2054484C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЕНЗОЛА И ЕГО МЕТИЛЬНЫХ ПРОИЗВОДНЫХ | 1993 |
|
RU2069351C1 |
Изобретение относится к химическим методам определения и может быть исполь- ювано при определении содержания витамина А и каротиноидов в масляных концентратах, витаминных премиксах, биологическом материале, в химических, фармацевтических, сельскохозяйственных и прочих биологических исследованиях, а также при контроле производства витамина А. Целью изобретения является упрощение и сокращение длительности процесса. Способ включает щелочной гидролиз пробы, экстракцию определяемых веществ органическим растворителем, обработку экстракта минеральной кислотой и спектро- фотометрический анализ, при этом в качестве органического растворителя используют этилэцетат, а из минеральных кислот используют тетрафторборную кислоту в количестве, обеспечивающем ее содержание в смеси с экстрактом 1,0-2,7%, при этом обработку экстракта проводят в течение 2-5 мин. 1 ил., 8 табл.
В качестве внутреннего стандарта в каждую пробу добавляли 5,30 нкг каротиноидов и 150 икг витамина А расчете на Т г навески.Оптическая плот- .
ноеть формы0,930,96 1,01,05 1,05 1,05 1,05 1,05 1,03 0,9
Выход дегидроФ°рмы, 88,691,5 95,2 100,0 100,0 100,0 100. 100 98,1 93,5
2,15 2,29 4,59 9,17 18,35
0,92
0,066
0,350 0,365 0,770. 1,560 2,950
Таблица .Ц
Таблица 5
Омыление60-90
Экстракция витамина А
и каротиноидов 7-15
Промывка экстракта водой15-30
Разделение экстракта 5
Перевод витамина в дегидроформу15
Нейтрализация раствора щелочью и промывка 15
Центрифугирование 15
Спектрофотометрическое
измерение5
Полное время анализа137-1
Таблица 8
i-------------------
| Способ определения витамина а в пищевых продуктах | 1976 |
|
SU590664A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J.Vitaminology, 1961, 7 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1992-03-30—Публикация
1989-07-10—Подача