Изобретение относится к органической химии, а именно к новым тиофосфорилированным оксимам лактамов общей формулы I
(C2H5O)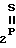 ON= C
ON= C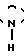 (CH2)n где n=3-5.
(CH2)n где n=3-5.
Предлагаемые соединения обладают инсектоакарицидной активностью и могут найти применение в сельском хозяйстве.
Известны соединения общей формулы II
R3-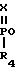 N= C
N= C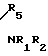 где R1 и R2, одинаковые или разные, - С1-С6-алкил, С1-С6-алкоксил, С3-С6-циклоалкил и т.д.; R3 и R4, одинаковые или разные, - С1-С6-алкил, С1-С6-алкоксил, С6-С10-арилокси и т. д. ; R5-C1-C4-алкил, С1-С4-алкоксил и т.д., R1 и R5 могут образовать кольцо, Х-кислород или эти соединения обладают гербицидной активностью.
где R1 и R2, одинаковые или разные, - С1-С6-алкил, С1-С6-алкоксил, С3-С6-циклоалкил и т.д.; R3 и R4, одинаковые или разные, - С1-С6-алкил, С1-С6-алкоксил, С6-С10-арилокси и т. д. ; R5-C1-C4-алкил, С1-С4-алкоксил и т.д., R1 и R5 могут образовать кольцо, Х-кислород или эти соединения обладают гербицидной активностью.
Наиболее близкими по структуре к соединениям формулы I являются соединения общей формулы III
(RO)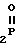 -N
-N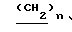 C= NC6H4X где R=C2-C4-алкил; Х - метил, метокси, хлор или нитрогруппа; n= 3-5, которые обладают инсектоакарицидной активностью. Однако их эффективность недостаточно высока.
C= NC6H4X где R=C2-C4-алкил; Х - метил, метокси, хлор или нитрогруппа; n= 3-5, которые обладают инсектоакарицидной активностью. Однако их эффективность недостаточно высока.
Предлагаемые новые соединения общей формулы I получают взаимодействием диэтилхлортиофосфата с соответствующими оксимами лактамов в органических растворителях при нагревании в присутствии триэтиламина.
Строение соединений формулы I доказано данными элементного анализа и ИК-спектроскопии. ИК-спектры соединений формулы I содержат полосы валентных колебаний NH-групп при 3420-3460 см-1.
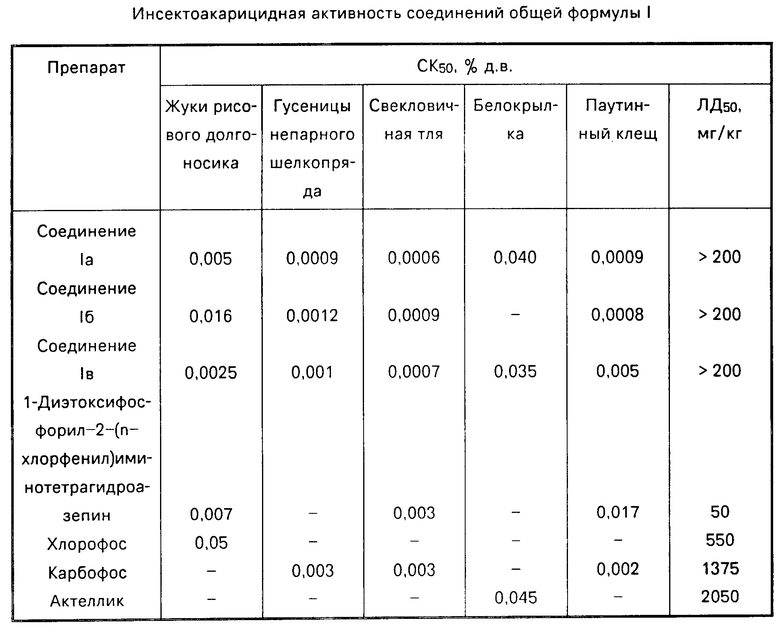
При испытаниях на жуках рисового долгоносика, гусеницах непарного шелкопряда, свекловичной тле, белокрылке, паутинном клеще соединения формулы I показали эффективность, превышающую эффективность соответствующих эталонов.
П р и м е р 1. Получение 0-(диэтокситиофосфорил)пирролидон-2-оксима (соединение Ia, n=3).
Смесь 0,5 г (0,005 моль) пирролидон-2-оксима, 0,94 г (0,005 моль) диэтилхлортиофосфата, 0,7 мл (0,005 моль) триэтиламина в 40 мл хлороформа нагревают в течение 1 ч при 50оС. Хлороформ упаривают в вакууме, остаток обрабатывают бензолом. Осадок гидрохлорида триэтиламина отфильтровывают, фильтрат упаривают в вакууме и получают 1,2 г 0-(диэтокситиофосфорил)пир- ролидон-2-оксима (выход 96% от теоретического), т.пл. 48-49оС (из смеси бензол-гексан).
Найдено, % : С 37,88; 37,66; Н 6,93; 6,79; N 10,95; 10,58; S 12,89; 12,64; Р 12,00; 12,10.
С8Н17N2О3РS
Вычислено, %: С 38,08; Н 6,79; N 11,10; S 12,70; Р 12,27.
ИК-спектр (СНСl3 ,ν, см-1) 3460 (NH), 1660 (С=N).
П р и м е р 2. Получение 0-(диэтокситиофосфорил)пиперидон-2-оксима (соединение 1б, n=4).
Смесь 0,57 г (0,005 моль) пиперидон-2-оксима, 0,94 г (0,005 моль) диэтилхлортиофосфата, 0,7 мл (0,005 моль) триэтиламина в 30 мл хлороформа нагревают в течение 1 ч при 50оС. Хлороформ упаривают в вакууме. Остаток обрабатывают бензолом, осадок гидрохлорида триэтиламина отфильтровывают, фильтрат упаривают в вакууме, остаток экстрагируют горячим гексаном. Выделяют из гексана 1,1 г 0-(диэтокситиофосфорил)пиперидон-2-оксима (выход 80% от теоретического) в виде желтого масла.
Найдено, % : С 40,40; 40,61; Н 6,90; 7,12; N 10,88; 10,86; Р 11,23; 11,36; S 11,76; 11,43.
С9Н19N2O3RS
Вычислено, %: С 40,59; Н 7,19; N 10,52; Р 11,63; S 12,04.
ИК-спектр (СНСl3, ν, см-1): 3420 (NH), 1653 (С=N).
П р и м е р 3. Получение 0-(диэтокситиофосфорил)пергидроазепинон-2-оксима (соединение Iв, n=5).
Смесь 0,6 г (0,0047 моль) пергидроазепинон-2-оксима, 0,9 г (0,0047 моль) диэтилхлортиофосфата, 0,7 мл (0,005 моль) триэтиламина в 30 мл хлороформа нагревают в течение 1 ч при 50оС. Хлороформ упаривают в вакууме. Остаток обрабатывают бензолом, осадок гидрохлорида триэтиламина отфильтровывают, фильтрат упаривают в вакууме. Получают 1,3 г 0-(диэтилтиофосфорил)пергидроазепинон-2-оксима (выход 99% от теоретического), т.пл. 43оС (из гексана).
Найдено, %: С 42,82; 42,39; Н 7,95; 7,64; N 9,53; 9,88; Р 11,20; 11,25; S 11,82; 11,82.
С10Н21N2О3PS
Вычислено, %: С 42,84; Н 7,55; N 9,99; Р 11,04; S 11,43.
ИК-спектр (СНCl3, ν, см-1): 3440 (NH), 1625 (С=Н).
П р и м е р 4. Испытания биологической активности соединений.
Новые соединения в качестве инсектицидов испытывают на жуках рисового долгоносика (С.oryzae), свекловичной тле (A.fabae L.), гусеницах непарного шелкопряда (L.dispar L.), белокрылке (Т.vaporavium Westw.); в качестве акарицидов - на паутинном клеще на фасоли (T.urticae Koch.)
Жуков рисового долгоносика спрыскивают 2,5 мл водно-ацетонового раствора испытуемого вещества в концентрации 0,1% д.в. Учет гибели жуков проводят через 48 ч.
Свекловичную тлю подсаживают в чашки, опрыснутые 2,5 мл водно-ацетонового раствора испытуемого вещества в концентрации 0,01% д.в. Учет гибели тли проводят через 24 ч.
Гусениц непарного шелкопряда опрыскивают 2,5 мл водно-ацетонового раствора испытуемого вещества в концентрации 0,01% д.в. Учет гибели гусениц проводят через 24 ч.
Белокрылку помещают на растения, обработанные водно-ацетоновым раствором испытуемого вещества в концентрации 0,1% д.в. Учет гибели белокрылки проводят через 24 ч.
Стандартные высечки листьев фасоли с подсаженными на них взрослыми клещами опрыскивают 2,5 мл водно-ацетонового раствора испытуемого вещества в концентрации 0,02% д.в. После высыхания капельно-жидкой влаги высечки с обработанными клещами помещают во влажную камеру. Учет гибели клещей проводят через 48 ч.
Для соединений, давших гибель насекомых и клещей 100%, определяют СК50 и сравнивают с СК50 эталона. Результаты испытаний приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| 3- ИЛИ 5-АМИДО-1-[ДИЭТОКСИ(ТИО)ФОСФОРИЛ]ПИРАЗОЛЫ, ОБЛАДАЮЩИЕ ИНСЕКТОАКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1986 |
|
SU1383757A1 |
| ФОСФОРИЛИРОВАННЫЕ N-АЛКИЛБЕНЗАМИДОКСИМЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ И ИНСЕКТОАКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1189067A1 |
| 4,5-ДИГИДРО-4-(О,О-ДИЭТИЛТИОФОСФОРИЛ)-5-МЕТИЛ-1,2,4-ТРИАЗИН-6-ОН, ОБЛАДАЮЩИЙ ИНСЕКТИЦИДНОЙ И АКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1988 |
|
SU1527872A1 |
| Фосфорилированные триметилизомочевины, обладающие инсектоакарицидной активностью | 1978 |
|
SU707233A1 |
| 1-( ДИЭТИЛТИОФОСФОРИЛТИО )МЕТИЛ -5- МЕТИЛ - 4,5 - ДИГИДРО -6- ОКСО - 1,2,4 - ТРИАЗИНЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ И АКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1621453A1 |
| @ -Этинильные эфиры дитиофосфорной кислоты,обладающие инсектоакарицидной активностью | 1980 |
|
SU948107A1 |
| Фосфорилированные триметилизотиомочевины, обладающие инсектоакарицидной активностью | 1978 |
|
SU707232A1 |
| ФОСФОРИЛИРОВАННЫЕ 2-АЛКИЛАМИНОДИГИДРО-1,3-ТИАЗИНЫ, ОБЛАДАЮЩИЕ ИНСЕКТИЦИДНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1157831A1 |
| S-(2,2,5-Триметилоксазолидинил-3-карбонилметил)-0,0-диалкилтио-, или дитиофосфаты, или О-диалкилтиофосфонаты, обладающие афицидной активностью | 1988 |
|
SU1530629A1 |
| N @ -(фосфонато)-диазен-N-оксиды | 1990 |
|
SU1747450A1 |
Сущность изобретения: продукт: 0-(диэтокситиофосфорил)пирролидон-2-оксим, C8H17N2O3PS выход 96%, т.пл. 48 - 49°С; 0-(диэтокситиофосфорил)пиперидин-2-оксим, C9H17N2O3PS выход 80%; 0-(диэтокситиофосфорил)пергидроазепинон-2-оксим, C10H21N2O3PS выход 99%, т.пл. 43°С. Реагент 1: (C2H5O)P(S)Cl реагент 2: 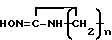 где n = 3 - 5. Условия реакции: в среде органического растворителя в присутствии амина при 50°С. 1 табл.
где n = 3 - 5. Условия реакции: в среде органического растворителя в присутствии амина при 50°С. 1 табл.
Тиофосфорилированные оксимы лактамов общей формулы
где n = 3 - 5,
обладающие инсектоакарицидной активностью.
| Авторское свидетельство СССР N 1034378, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1994-12-30—Публикация
1990-02-01—Подача